荧光检测试纸的制备方法、检测系统及检测方法与流程
1.本发明涉及医疗诊断技术领域,具体地,涉及一种荧光检测试纸的制备方法、检测系统及检测方法。
背景技术:
2.由于儿童的免疫系统尚未发育完善,老年人免疫力衰减,前期因诊疗不及时、不得当,亦会引发并发症,重则并发其他器官系统损伤。此外各病原体的用药不同,细菌性和支原体感染需使用抗生素药物。因此快速和准确的诊断以及适当的治疗,是减少住院和不必要的抗菌药物滥用而造成耐药菌株产生的重要前提。
3.目前,病原体检测一般是需要在医院检验室进行,但去医院就诊就会有一系列问题,具体如:(1)病人多,排队挂号、候诊、检查、取药、治疗等手续多,等待时间长且操作复杂;(2)医院众多患者的接触,也存在患者之间交叉感染的可能;(3)经济负担相对高一点。
4.现有公开号为cn104977409a的中国专利,其公开了一种荧光微球免疫层析试纸条的制备方法及定量检测方法。以无皂乳液聚合法制备的发光纳米粒子为标记,采用免疫层析技术,制备荧光微球免疫层析试纸条,然后制成构成包括样本垫、玻璃纤维膜、硝酸纤维素膜和吸水纸的检测卡,其中硝酸纤维素膜上固定有检测线和质控线。在检测过程中,采用荧光微球最佳激发光源进行激发,发射出的荧光经过滤光片后,用ccd扫描技术或光纤技术,将发射光谱收集、聚集和倍增后,转换成数值信号,再将测定的检测线荧光强度乘以校正系数,把校正后的荧光强度代入预先设置在荧光分析仪中的标准曲线,即可通过荧光分析仪自动计算获得样本中待测物的浓度。
5.发明人认为,针对现有技术中的检测系统,目前市场上急需一种能够实现零加样,零污染,且配合仪器和app,可以进行既往数据回顾的用于检测试纸的检测系统
技术实现要素:
6.针对现有技术中的缺陷,本发明的目的是提供一种荧光检测试纸的制备方法、检测系统及检测方法。
7.根据本发明提供的一种荧光检测试纸的制备方法,包括:包被nc膜、制备荧光垫、制备样品垫以及试纸条组装;包被nc膜包括如下步骤:s1.1、制备包被缓冲液、c线溶液以及t线溶液,备用;s1.2、调试微量蛋白点膜系统各参数、将c管线放入c线溶液中、将t管线放入t线溶液中,并将nc膜粘贴到pvc板上,将c线和t线分别结合到nc膜上;s1.3、将调试好的微量蛋白点膜放入温度在37度-60度的干燥箱干燥,保持12小时以上,备用;制备荧光垫包括如下步骤:s2.1、选择标记物:选择比本底物质荧光寿命高5-6个数量级的稀土离子作为荧光标记物;s2.2、微球活化:将标记物与荧光微球原液混合,再在混合液中加入mes 6.0缓冲液混匀,再加入nhs和edc混匀,然后再离心去上清,之后再加入mes 6.4缓冲液重悬;s2.3、抗体偶联:加入单克隆抗体,超声分散后混匀;s2.4、微球封闭:加入微球封闭液,超声分散后混匀;s2.5、清洗保存:将封闭后的微球溶液离心,去上清,再向去上清后的微球溶液中加
入微球保存液混匀,然后再进行超声分散,并在2-8摄氏度的环境温度下保存;s2.6、紫外分光光度计检测:取标记好的荧光微球加入超纯水混匀,紫外分光光度计检测320nm处吸光度值,并推算出荧光标记物原始od值;s2.7、配制缓冲液:0.05m tris ph 8.5
±
0.1、含不超过3%蔗糖、2%海藻糖;s2.8、稀释荧光标记物:用配制好的缓冲液稀释荧光标记物的浓度至0.2-0.60d/ml,超声铺垫;s2.9、形成荧光垫:用制备好的荧光标记物工作液浸泡玻璃纤维素纸,将浸泡好的玻璃纤维素纸放入真空腔内干燥六小时,真空腔内的真空压在1.0bar以下;制备样品垫包括如下步骤:s3.1、制备样品垫处理液:50mm tris ph8.5、含不超过0.3%酪蛋白钠;s3.2、形成样品垫:用制备好的样品垫处理液浸泡玻璃纤维素纸,将浸泡好的玻璃纤维素纸取出,置于干燥箱干燥十二个小时;试纸条组装包括如下步骤:s4.1、将吸水纸进行切割,再将切割后的吸水纸贴于pvc板上并使其边缘与nc膜覆盖1-2mm;s4.2、将荧光垫进行切割,再将切割后的荧光垫贴于pvc板上并使其边缘与nc膜覆盖1-2mm;s4.3、将样品垫进行切割,再将切割后的样品垫贴于pvc板上并使其边缘与荧光垫覆盖1-2mm;s4.4、将贴好的pvc板进行切割,形成试纸条。
8.优选地,针对步骤s1.2、调试微量蛋白点膜系统各参数包括:调整微量蛋白点膜系统的划膜长度在0-300mm;调整微量蛋白点膜系统的划膜喷量为0.8-1.2μl/cm。
9.优选地,针对步骤s2.6标记好的荧光微球溶液与超纯水的体积比为1比199或1比399。
10.根据本发明提供的一种荧光检测试纸,采用权利要求1所述的检测试纸制备方法,包括样品垫、荧光垫、pvc板以及nc膜以及吸水纸;所述nc膜粘贴在pvc板上,且所述nc膜上结合有c线和t线;所述吸水纸、荧光垫以及样品垫三者依次贴合在pvc板上,且所述吸水纸的边缘覆盖nc膜1-2mm,所述荧光垫的边缘覆盖nc膜1-2mm,所述样品垫的边缘覆盖荧光垫1-2mm。
11.根据本发明提供的一种荧光检测系统,采用权利要求4所述的检测试纸,还包括检测仪器、具有检测app的智能终端以及检测卡壳;所述检测app的智能终端与检测仪器信号连接;所述检测试纸设置在检测卡壳内,且所述检测试纸的一端伸出检测卡壳;所述检测卡壳伸入检测仪器的检测口,且所述检测仪器能够读取到检测试纸的反应区。
12.优选地,还包括预分装试剂承载装置,所述预分装试剂承载装置与检测卡壳具有检测试纸伸出端的一端卡接配合,且所述检测卡壳远离预分装试剂承载装置的一端伸入检测仪器的检测口内。
13.根据本发明提供的一种荧光检测系统的检测方法,采用权利要求5所述的荧光检测试纸的检测系统,检测方法包括如下步骤:s1、所述智能终端上的检测app启动,所述检测app按照预设的步骤引导使用者进行操作,录入相应信息;s2、撕开所述预分装试剂承载装置的封口膜,将采集的样本在所述预分装试剂承载装置中进行洗脱处理得到待测样本;s3、取出具有所述检测试纸的检测卡壳,按照检测app和/或所述检测仪器的提示将具有检测试纸的检测卡壳插入检测仪器的检测口内,待用;s4、将所述检测卡壳位于检测仪器外的一端与具有检测样本的分装试剂承载装置插接,并使所述检测试纸伸出检测卡壳的一端浸润在待测样本中,开始计时;s5、通过所述检测仪器内的pd传感器检测c线的干条背景值,再对c线进行定时检测,之后再对c线的干条背景值和c线的定时检测值进行对比;若c线的定时检测值与c线的干条背景值相同,则检测失败,检测结束;若c线的定时检测值与c线的干条背
景值不相同,且c线的定时检测值与c线的干条背景值的差值不超过阈值,则检测失败,检测结束;若c线的定时检测值与c线的干条背景值不相同,且c线的定时检测值与c线的干条背景值的差值超过阈值,则进入步骤s6;s6、待到达反应时间后,通过所述检测仪器内的pd传感器扫描并判读检测试纸上的反应视窗区域后得到信号值,分析信号值转换成检测结果并在app上呈现检测结果,检测结束。
14.优选地,针对步骤s2,所述预分装试剂承载装置内预设有洗脱液;所述预分装试剂承载装置内经洗脱处理得到的待测样本能够满足:当所述预分装试剂承载装置水平放置时,所述待测样本能够完全浸润与之连接的检测卡壳内的检测试纸的伸出端。
15.优选地,针对步骤s4,所述预分装试剂承载装置与检测卡壳连接并密封,且所述预分装试剂承载装置的液体不会侧漏到检测卡壳内。
16.优选地,针对步骤s5,对c线进行定时检测的时间为开始计时后的三分钟。
17.与现有技术相比,本发明具有如下的有益效果:
18.1、本发明通过将荧光微球和免疫层析技术结合生产制备试纸条,利用荧光微球的特性使得试纸条对产品的检测灵敏度下限更低,相比于传统的胶体金平台,至少有五倍的性能优势,并搭配检测卡壳和预分装试剂承载装置,实现了检测试纸完全封闭式的检测,有助于提高检测的准确性,且有助于减少对环境的生物源性的污染,使用便捷,适用于家庭等特殊环境;
19.2、本发明通过在检测试纸接触待测样本后的三分钟对c线的数值进行检测,结合c线的基础值进行对比,能够提前对检测结果是否有效进行预判,从而有助于减少使用者对无效检测的等待时间;
20.3、本发明通过测量的c线初始值,结合c线的定时检测值,将最终值的读数除以最初值的读数,得到单线在最终读数的值相对于最初本底值的变化情况,有助于消除本底间由于差异导致的读数不精准,进而有助于提高检测的准确度,且能够通过具有检测app的智能终端和检测仪器进行既往数据回顾。
附图说明
21.通过阅读参照以下附图对非限制性实施例所作的详细描述,本发明的其它特征、目的和优点将会变得更明显:
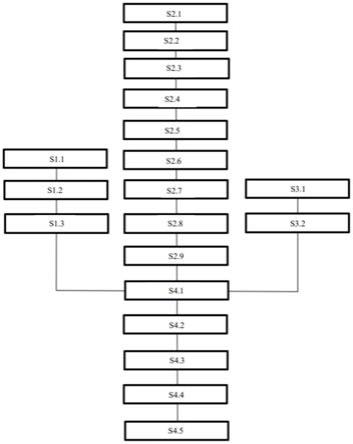
22.图1为本发明主要体现荧光检测试纸制备方法的流程示意图;
23.图2为本发明主要体现荧光检测系统的检测方法的流程示意图。
具体实施方式
24.下面结合具体实施例对本发明进行详细说明。以下实施例将有助于本领域的技术人员进一步理解本发明,但不以任何形式限制本发明。应当指出的是,对本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变化和改进。这些都属于本发明的保护范围。
25.实施例1
26.如图1所示,根据本发明提供的一种荧光检测试纸的制备方法,包括:包被nc膜、制备荧光垫、制备样品垫以及试纸条组装;
27.包被nc膜包括如下步骤:
28.s1.1、制备包被缓冲液、c线溶液以及t线溶液,备用。包被缓冲液:10mm pbs,ph7.2;c线溶液:使用包被缓冲液稀释羊抗鼠至工作浓度;t线溶液:使用包被缓冲液稀释包被抗体至工作浓度。
29.s1.2、调试微量蛋白点膜系统各参数、将c管线放入c线溶液中、将t管线放入t线溶液中,并将nc膜粘贴到pvc板上,将c线和t线分别结合到nc膜上。具体的,调试微量蛋白点膜系统各参数包括:调整微量蛋白点膜系统的划膜长度在0-300mm;调整微量蛋白点膜系统的划膜喷量为0.8-1.2μl/cm。
30.s1.3、将调试好的微量蛋白点膜放入温度在37度-60度的干燥箱干燥,保持12小时以上,备用。本技术优选将调试好的微量蛋白点膜放入温度为45度的干燥箱内干燥。
31.制备荧光垫包括如下步骤:
32.s2.1、选择标记物:选择荧光寿命比本底物质荧光寿命高5-6个数量级的稀土离子作为标记物。稀土离子的荧光半衰期较长,其特性为stoke位移大,且荧光微球表面修饰合适密度的羧基集团,用于与蛋白或抗体的共价偶联,提高了标记物的稳定性。
33.s2.2、微球活化:将标记物与荧光微球原液混合,再在混合液中加入mes 6.0缓冲液混匀,再加入nhs和edc混匀,然后再离心去上清,之后再加入mes 6.4缓冲液重悬。具体的,向一个干净的2ml离心管中加入适量的荧光微球原液和标记物,再加入适量mes6.0缓冲液混匀,之后再加入适量nhs和适量edc混匀30min。16000g离心15min去上清,加入适量mes 6.4缓冲液重悬。
34.s2.3、抗体偶联:加入适量单克隆抗体,超声分散后混匀。超声分散混匀的时间为120min,超声参数:功率20%,超声1s,停止2s。超声时间2min。
35.s2.4、微球封闭:加入适量微球封闭液,超声分散后混匀。超声分散混匀的时间为60min,超声参数:功率20%,超声1s,停止2s。超声时间2min。
36.s2.5、清洗保存:将封闭后的微球溶液离心,去上清,再向去上清后的微球溶液中加入微球保存液混匀,然后再进行超声分散,并在2-8摄氏度的环境温度下保存。具体的,16000g离心15min,去上清,加入适量微球保存液混匀,超声分散,2-8℃保存。超声参数:功率20%,超声1s,停止2s,超声时间2min。
37.s2.6、紫外分光光度计检测:取标记好的荧光微球加入超纯水混匀,紫外分光光度计检测320nm处吸光度值,并推算出荧光标记物原始od值。具体的,荧光微球溶液与超纯水的体积比为1比199或1比399。取标记好的微球10ul加1990ul超纯水中混匀,紫外分光光度计检测320nm处吸光度值,并推算出荧光标记物原始od值。荧光标记物原始od值是通过紫外分光光计测出来的数据乘上相应的稀释倍数得出。
38.s2.7、配制缓冲液:0.05m tris ph 8.5
±
0.1、含不超过3%蔗糖、2%海藻糖。
39.s2.8、稀释荧光标记物:用配制好的缓冲液稀释荧光标记物的浓度至0.2-0.60d/ml,超声铺垫,超声参数:功率25%,超声1s,停止2s,超声时间2min。
40.s2.9、形成荧光垫:用制备好的荧光标记物工作液浸泡玻璃纤维素纸,将浸泡好的玻璃纤维素纸放入真空腔内干燥六小时,真空腔内的真空压在1.0bar以下。每30ml荧光标记物工作液铺制在一张300mm
×
250mm的玻璃纤维素纸上。
41.制备样品垫包括如下步骤:
42.s3.1、制备样品垫处理液:50mm tris ph8.5、含不超过0.3%酪蛋白钠;
43.s3.2、形成样品垫:用制备好的样品垫处理液浸泡玻璃纤维素纸,将浸泡好的玻璃纤维素纸取出,置于干燥箱干燥十二个小时。每40ml样品垫处理液铺制在一张300mm
×
250mm的玻璃纤维素膜上,并使玻璃纤维素纸浸泡均匀。
44.试纸条组装包括如下步骤:
45.s4.1、将吸水纸进行切割,再将切割后的吸水纸贴于pvc板上并使其边缘与nc膜覆盖1-2mm。吸水纸切成300mm
×
20.5mm长条,优选吸水纸边缘与nc膜覆盖1mm。
46.s4.2、将荧光垫进行切割,再将切割后的荧光垫贴于pvc板上并使其边缘与nc膜覆盖1-2mm。荧光垫切成300mm
×
8mm长条,优选荧光垫边缘与nc膜覆盖1mm。
47.s4.3、将样品垫进行切割,再将切割后的样品垫贴于pvc板上并使其边缘与荧光垫覆盖1-2mm。样品垫切成300mm
×
30mm长条,优选样品垫边缘与荧光垫覆盖1mm。
48.s4.4、将贴好的pvc板进行切割,形成试纸条。将贴好的pvc板置于切条机上,按3.85mm/板进行生产。
49.s4.5、将切好试纸条装入特制的塑料卡壳,扣紧卡壳,与干燥剂一起装入铝箔袋内,热封口,即完成试纸条的制备。
50.发明人认为利用荧光微球的特性,使得试纸条检测的灵敏度下限更低,相对于传统的胶体金平台,至少有五倍性能优势。
51.实施例2
52.基于实施例1,采用上述的荧光检测试纸的制备方法,根据本发明提供的一种荧光检测试纸,包括样品垫、荧光垫、pvc板以及nc膜以及吸水纸。nc膜粘贴在pvc板上,且所述nc膜上粘贴有c线和t线。吸水纸、荧光垫以及样品垫三者依次贴合在pvc板上,且吸水纸的边缘覆盖nc膜1-2mm,荧光垫的边缘覆盖吸水纸1-2mm,样品垫的边缘覆盖荧光垫1-2mm。本技术优选1mm。
53.使用检测试纸时,配上特制的检测卡壳和预分装试剂承载装置,预分装试剂承载装置包含预分装的稀释液,用户将采集后的样本直接在预分装试剂承载装置中进行洗脱,后将含有待测样本的预分装试剂承载装置与检测卡壳组装可形成完全密封反应环境,避免了开放式反应造成的生物源性的污染,适用于家庭环境等特殊环境。
54.实施例3
55.基于实施例2,采用上述的荧光检测试纸,根据本发明提供的一种荧光检测系统,还包括检测仪器、具有检测app的智能终端以及检测卡壳,检测app的智能终端与检测仪器信号连接,具体的,具有检测app的智能终端与检测仪器通过蓝牙连接。
56.检测试纸设置在检测卡壳内,且所述检测试纸的一端伸出检测卡壳,检测卡壳伸入检测仪器的检测口,且检测仪器能够读取到检测试纸的反应区。
57.还包括预分装试剂承载装置,预分装试剂承载装置与检测卡壳具有检测试纸伸出端的一端卡接配合,且检测卡壳远离预分装试剂承载装置的一端伸入检测仪器的检测口内。
58.实施例4
59.如图2所示,基于实施例3,采用上述的荧光检测系统,根据本发明提供的一种荧光检测系统的检测方法,检测方法包括如下步骤:
60.s1、智能终端上的检测app启动,检测app按照预设的步骤引导使用者进行操作,录入相应信息;
61.s2、撕开预分装试剂承载装置的封口膜,将采集的样本在所述预分装试剂承载装置中进行洗脱处理得到待测样本。预分装试剂承载装置内预设有洗脱液,预分装试剂承载装置内经洗脱处理得到的待测样本能够满足:当预分装试剂承载装置水平放置时,待测样本能够完全浸润与之连接的检测卡壳内的检测试纸的伸出端。
62.s3、撕开铝箔袋,取出具有检测试纸的检测卡壳,按照检测app和检测仪器的提示将具有检测试纸的检测卡壳插入检测仪器的检测口内,待用。
63.s4、将检测卡壳位于检测仪器外的一端与具有检测样本的分装试剂承载装置插接,并使检测试纸伸出检测卡壳的一端浸润在待测样本中,开始计时。预分装试剂承载装置与检测卡壳连接并密封,且保证预分装试剂承载装置的液体不会侧漏到检测卡壳内。
64.s5、通过检测仪器内的pd传感器检测c线的干条背景值,再对c线进行定时检测,之后再对c线的干条背景值和c线的定时检测值进行对比。对c线进行定时检测的时间为开始计时后的三分钟。
65.若c线的定时检测值与c线的干条背景值相同,则检测失败,检测结束。
66.若c线的定时检测值与c线的干条背景值不相同,且c线的定时检测值与c线的干条背景值的差值不超过阈值,则检测失败,检测结束。
67.若c线的定时检测值与c线的干条背景值不相同,且c线的定时检测值与c线的干条背景值的差值超过阈值,则进入步骤s6。
68.c线的定时检测值与c线的干条背景值的差值不超过阈值的原因可能是待测样本溶液的量过少、检测试纸条自身质量等各种原因,通过对c线的定时检测,可以提前告知用户检测失败的结果,节省了用户的等待时间,缩短了失败的检测带来的时间上的成本。
69.且对于最终检测结果,可以通过最终按仪器内部设置的反应时长,将最终值的读数除以c线的干条背景值的读数,得到单线在最终读数的值相对于最初本底值的变化情况,以此来消除本底间由于差异导致的读数不精准。
70.s6、待到达反应时间后,反应时间一般为10-15分钟,通过检测仪器内的pd传感器扫描并判读检测试纸上的反应视窗区域后得到信号值,分析信号值转换成检测结果并在app上呈现检测结果,检测结束。app上呈现的检测结果包括阳性、阴性、无效等结果,并给出有无病原体感染。
71.使用时,按照产品说明书步骤进行操作,保证试纸条样品端浸润在待测样本中,在开始计时后的3分钟利用仪器做定时检测,监测c线的情况。若在3分钟内没有检测到待测样本层析完成,则仪器发出检测失败的信号,避免用户等待较长的层析全过程下可提前做复测。
72.等待反应结束后,根据使用的仪器、借助仪器算法给出检测结果,并通过app显示出检测结果。整个操作简单、反应时间短,用户可预先居家自测病原体,避免了在医院中造成的交叉感染以及避免了去医院排队挂号带来的人力,物力和财力的浪费。
73.优选例1
74.基于实施例3和实施例4,检测卡壳和预分装试剂承载装置插接配合后具有良好的密封性能,能够防止预分装试剂承载装置内的待测样本漏出。
75.具体的,检测卡壳内固定有检测试纸,检测试纸的样品吸取段自检测卡壳的一端伸出并裸露,检测卡壳上开设有观察窗,检测试纸的结果显示区与观察窗相对应。检测卡壳和预分装试剂承载装置之间连接有连接结构,当检测卡壳与预分装试剂承载装置通过连接结构连接时,预分装试剂承载装置的内腔形成密闭空间,且检测试纸的样品吸取段探入预分装试剂承载装置的内腔。
76.检测卡壳包括相互扣合的上盖和下底,上盖和下底均为长条形结构,上盖和下底之间形成有用于容纳检测试纸的间隙,检测试纸由上盖和下底配合压紧固定。上盖上开设有观察窗,检测试纸的结果显示区与观察窗相对应,检测试纸的样品吸取段从检测卡壳长度的一端探出。
77.上盖和下底上均一体成型有定位扣件和第一定位挡筋。上盖和下底通过两个定位扣件扣合为一体,且两个定位扣件均位于检测卡壳远离检测试纸的样品吸取段探出的一侧。第一定位挡筋在上盖和下底的中部分别间隔一体成型有多个,且任一第一定位挡筋均与检测试纸抵紧配合,借助第一定位挡筋对检测试纸进行卡紧固定,避免其内外滑动,将上盖与下底进行扣合时,通过两个定位扣件进行过盈配合,确保上盖和下底完全密封。
78.连接结构包括连接卡套和尾端卡扣,尾端卡具有弹性,尾端卡在检测卡壳上检测试纸的样品吸取段伸出的一端的的上盖和下底上均一体成型有一个,且两个尾端卡扣远离检测卡壳的一端均形成有倒钩结构。连接卡套呈中空圆桶形,且连接卡套的内径自其一端向另一端逐渐增大,连接卡套内一体成型有内圈,内圈与连接卡套内径最大的一端固定连接,且内圈与连接卡套的内壁呈间隔设置。
79.连接卡套从检测卡壳具有检测试纸样品吸取段的一端套设检测卡壳,直至推不动为止,通过两个尾端卡扣与连接卡套内圈的配合,当连接卡套套至预定工位时,连接卡套的内圈分别与两个尾端卡扣的倒钩结构抵紧,保证上盖和下底的完全密封。
80.预分装试剂承载装置内灌装有检测试剂,并使用封口膜对其进行热封口或是加盖进行密封,确保该装置在使用前无液体渗漏减少。
81.需要进行检测时,首先打开预分装试剂承载装置的封口,垂直将检测卡壳按照检测试纸的样品吸取段向下插入预分装试剂承载装置内,直至推不动为止,通过预分装试剂承载装置内圈由大到小结构与卡套内圈中段由小到大结构进行过盈配合,可以确保预分装试剂承载装置水平放置时,其中的液体不会侧漏。另外检测试纸的样品吸取段可以浸入到预分装试剂承载装置内的液体中,通过两个第一定位挡筋压紧检测试纸,可以牢牢地固定住检测试纸,同时也避免了预分装试剂承载装置内的液体在水平放置的一瞬间内冲至检测试纸上,这样0-5分钟层析反应内,预分装试剂承载装置内的液体可以逐渐从检测试纸的样品吸取端层析到检测试纸的结果显示区以至检测试纸的顶端,直至层析反应结束。最后插入仪器中或借助肉眼透过观察窗进行读值。
82.上盖上还开设有透气窗,0-5分钟反应结束后,仪器通过扫描判读观察窗区域后得到信号值,分析信号值转换成检测结果并给出有无病原体感染或肉眼观察观察窗区域内检测试纸的线条显色强弱,以及结合结果判读标准给出有无病原体感染。
83.发明人认为本技术中预分装试剂承载装置和检测卡壳之间的连接密封还可以采用其它能够达到上述效果的现有技术中的连接结构。
84.发明人认为,预分装试剂承载装置作为一个样本预处理装置或样本处理装置,处
理的样本类型不仅包含拭子样本,也可以是粪便、血液以及尿液等样本。进一步地,本技术中的试纸检测辅助装置能够用于非定量检测也可以用于定量检测。
85.优选例2
86.基于实施例3和实施例4,检测卡壳插入检测仪器的检测口内包括水平插入状态、抬升状态以及到位状态三种状态。
87.其中抬升状态是由设置在检测仪器检测口处的抬升装置实现的,具体的,抬升装置是由现有技术中的弹性件或弹性组件制作而成,抬升装置作用于检测卡壳的底部,从而实现检测卡壳抬升。
88.优选例3
89.基于实施例3和实施例4,检测仪器呈竖直设置,检测仪器包括底座和与底座插接配合的检测仪器本体,检测时将检测卡壳自下向上插入检测仪器的检测口内,并使检测卡壳上的检测试纸的裸露端位于下方;将预分装试剂承载装置稳定放置在底座上,并使检测仪器本体和底座插接配合时,位于检测仪器内的检测卡壳能够插入预分装试剂承载装置内,并使检测试纸的裸露端完全浸没在预分装试剂承载装置内的待测样本内。
90.本领域技术人员知道,除了以纯计算机可读程序代码方式实现本发明提供的系统及其各个装置、模块、单元以外,完全可以通过将方法步骤进行逻辑编程来使得本发明提供的系统及其各个装置、模块、单元以逻辑门、开关、专用集成电路、可编程逻辑控制器以及嵌入式微控制器等的形式来实现相同功能。所以,本发明提供的系统及其各项装置、模块、单元可以被认为是一种硬件部件,而对其内包括的用于实现各种功能的装置、模块、单元也可以视为硬件部件内的结构;也可以将用于实现各种功能的装置、模块、单元视为既可以是实现方法的软件模块又可以是硬件部件内的结构。
91.在本技术的描述中,需要理解的是,术语“上”、“下”、“前”、“后”、“左”、“右”、“竖直”、“水平”、“顶”、“底”、“内”、“外”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本技术和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本技术的限制。
92.以上对本发明的具体实施例进行了描述。需要理解的是,本发明并不局限于上述特定实施方式,本领域技术人员可以在权利要求的范围内做出各种变化或修改,这并不影响本发明的实质内容。在不冲突的情况下,本技术的实施例和实施例中的特征可以任意相互组合。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1