一种检测低聚软骨基质蛋白的试纸条及检测方法与流程
1.本发明涉及免疫层析法定量检测技术领域,具体而言,涉及一种检测低聚软骨基质蛋白的试纸条及检测方法。
背景技术:
2.低聚软骨基质蛋白(cartilage oligomeric matrix protein,comp),又称软骨低聚基质蛋白、软骨低聚物基质蛋白或软骨寡聚基质蛋白。低聚软骨基质蛋白属于一种骨代谢标志物,它是一种由五个独立的次级单位经二硫键相连的五聚蛋白,最早发现于软骨,近年也少量出现于肌腱和滑膜,但在皮肤、肺等结缔组织中却未曾有报道。软骨由于疾病的发生在破碎时会释放蛋白分子进入滑液中,在血液中也可以发现这些蛋白如低聚软骨基质蛋白。
3.低聚软骨基质蛋白的检测对骨关节炎、类风湿关节炎软骨病变等疾病的早期诊断、预后及疗效观察具有重要的临床意义。目前国内外临床上检测低聚软骨基质蛋白的常用方法有酶联免疫吸附法(elisa)。该方法存在耗时长、灵敏度低、背景值高、操作繁琐的问题,且易产生假阳性和假阴性结果,elisa检测需要专业人员进行操作,不适应临床对低聚软骨基质蛋白快速准确定量检测的需要。目前国内检测低聚软骨基质蛋白的产品较少,临床上迫切需要建立一种快速、便捷、准确的检测低聚软骨基质蛋白的产品或方法。
4.鉴于此,特提出本发明。
技术实现要素:
5.本发明的目的在于提供一种检测低聚软骨基质蛋白的试纸条及检测方法以解决上述技术问题。
6.本发明是这样实现的:
7.本发明提供了一种检测低聚软骨基质蛋白的试纸条,其包括基板,基板上依次设置有样品垫、结合垫、硝酸纤维素膜和吸水垫,结合垫上固定有示踪物标记的抗低聚软骨基质蛋白抗体1和示踪物标记的质控线配体1,硝酸纤维素膜上设置有检测线和质控线,检测线上固定有抗低聚软骨基质蛋白的抗体2,质控线上固定有能与质控线配体1特异结合的配体2。
8.上述抗低聚软骨基质蛋白的抗体1和抗低聚软骨基质蛋白的抗体2是针对低聚软骨基质蛋白的两种不同表位的抗体。可以根据需要选择市售的对低聚软骨基质蛋白具有高亲和力的抗体。
9.本发明利用试纸条中具特异性的抗低聚软骨基质蛋白的抗体与待检样本中低聚软骨基质蛋白(抗原)结合的特性,可以实现待测样本中的低聚软骨基质蛋白的快速、准确检出。
10.与现有技术相比,本发明提供的检测试纸条具有如下优势:制作方便,体积小、便于携带且成本较低,克服了酶联免疫吸附法(elisa)制作复杂、体积大、不便于携带等缺点,
可以实现单人份检测。
11.上述试纸条具有检测灵敏度高,可以满足定量检测的需求。通过免疫分析仪对结果进行判读,可实现自动化,减少主观因素的影响,提供便利、快速、可靠、结果可重复的诊断结果。采用上述试纸条适用于各种医疗现场的检测所需。
12.在本发明应用较佳的实施方式中,上述示踪物是一种能发光且能与抗低聚软骨基质蛋白抗体1和质控线配体1结合的物质。
13.在一种可选的实施方式中,示踪物包括不限于胶体金、量子点、荧光微球、上转发光、时间分辨荧光或金磁纳米。示踪物是一种能发光且能与抗低聚软骨基质蛋白抗体1和质控线配体1结合的物质。示踪物发光的强度可利用特定仪器定量判读或检测。而通过将示踪物与抗低聚软骨基质蛋白抗体1以及质控线配体1偶联,从而对形成的偶联复合物进行示踪,在层析作用下,偶联复合物中的抗低聚软骨基质蛋白抗体1先与样本中的低聚软骨基质蛋白结合,再一起与检测线上的抗低聚软骨基质蛋白抗体2结合,而偶联复合物中的质控线配体1直接与硝酸纤维膜上的配体2结合,最终,检测线位置的示踪物含量与待测样本中的低聚软骨基质蛋白的浓度成正相关,而质控线上的示踪物含量在同一批试纸条中基本不变。通过与已知不同浓度的低聚软骨基质蛋白在试纸条上检测所制定的标准曲线进行比较分析,实现对低聚软骨基质蛋白的定量检测。
14.在本发明应用较佳的实施方式中,上述质控线配体1和配体2为一对能发生特异性结合的生物材料。
15.在本发明应用较佳的实施方式中,上述质控线配体1选自如下物质中的任意一种:兔抗牛血清白蛋白与二硝基苯酚偶联物、x igy,其中所述x为兔、羊、牛、马、猪、鼠、狗、猫、兔、骆驼、驴、鹿、貂、鸡、鸭或鹅;配体2选自如下物质中的任意一种:牛血清白蛋白与二硝基苯酚偶联物、z抗x igy;z为兔、羊、牛、马、猪、鼠、狗、猫、兔、骆驼、驴、鹿、貂、鸡、鸭或鹅,且x与z不同;在本发明应用较佳的实施方式中,上述z为羊,x为鸡。
16.在本发明应用较佳的实施方式中,上述检测线上抗低聚软骨基质蛋白的抗体2的包被浓度为1-1.2mg/ml;
17.质控线上配体2的包被浓度为1-1.2mg/ml。
18.在上述包被浓度下可以满足低聚软骨基质蛋白的快速高灵敏度检出。
19.在本发明应用较佳的实施方式中,上述试纸条还包括卡壳,卡壳具有腔体,试纸条固定设置在腔体内,在卡壳上还设有加样孔和观察窗,加样孔对应样品垫设置,观察窗对应硝酸纤维素的检测线和质控线设置。
20.在本发明应用较佳的实施方式中,上述样品垫上还设置有红细胞截留膜;在一种可选的实施方式中,红细胞截留膜为滤血膜。样品垫用于过滤样本中的红细胞或其他杂质。
21.当样本中含有红细胞时,红细胞被滤血膜阻挡,可以减少红细胞对检测结果的影响,提升检测的准确度。因而,本发明提供的试纸条可以满足全血样本的检测。
22.本发明还提供了一种使用上述检测低聚软骨基质蛋白的试纸条进行低聚软骨基质蛋白检测的方法,方法为非疾病的诊断目的,其包括:
23.上样至样品垫上,采用能对示踪物含量进行定量检测的仪器对试纸条的检测线进行检测,根据已知浓度的低聚软骨基质蛋白在试纸条上检测所制定的标准曲线(例如五点取样测得的标曲),获得低聚软骨基质蛋白的定量结果。
24.在本发明应用较佳的实施方式中,上述低聚软骨基质蛋白的含量根据检测线示踪物含量与质控线示踪物含量的比值来计算。
25.本发明具有以下有益效果:
26.本发明利用试纸条中具特异性的抗低聚软骨基质蛋白的抗体与待检样本中低聚软骨基质蛋白(抗原)结合的特性,可以实现待测样本中的低聚软骨基质蛋白的快速、准确检出。
27.与现有技术相比,本发明提供的检测试纸条具有如下优势:制作方便,体积小、便于携带且成本较低,克服了酶联免疫吸附法(elisa)制作复杂、体积大、不便于携带等缺点,可以实现单人份检测。
28.上述试纸条具有检测灵敏度高,可以满足定量检测的需求。通过免疫分析仪对结果进行判读,可实现自动化,减少主观因素的影响,提供便利、快速、可靠、结果可重复的诊断结果。采用上述试纸条适用于各种医疗现场的检测所需。
附图说明
29.为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
30.图1为本发明的试纸条的局部截面结构示意图;
31.图2为本发明的试纸条的整体截面结构示意图;
32.图3为实验例1绘制的标准曲线图。
33.附图标记:1-pvc底板;2-样品垫;3-结合垫;4-硝酸纤维素膜;5-吸水垫;6-卡壳。
具体实施方式
34.为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
35.以下结合实施例对本发明的特征和性能作进一步的详细描述。
36.实施例1
37.本实施提供了一种低聚软骨基质蛋白定量检测试纸条及检测方法。试纸条参照图1所示,其包括pvc底板1(即为基板),pvc底板1上依次设有样品垫2、结合垫3、硝酸纤维素膜4和吸水垫5。具体地,样品垫2搭接在结合垫3上,结合垫3和吸水垫5分别搭设于硝酸纤维素膜4沿层析方向上的两端。
38.本实施例在结合垫3上固定有量子点标记的抗低聚软骨基质蛋白抗体1和量子点标记的鸡igy,鸡igy的包被量为3.0μl/cm。抗低聚软骨基质蛋白抗体1的包被量为3.0μl/cm。量子点标记的方法如下:先用edc
·
hcl活化量子点表面羧基,然后把活化后的量子点与标记抗体混匀后反应2小时再使用封闭剂进行封闭出来,每个步骤后都是通过离心的方式进行上清液去除,最后保存在保存溶液中。
39.抗体1来自hytest,进行脱盐置换缓冲体系等处理后使用。
40.硝酸纤维素膜4上设有检测线与质控线,检测线上固定有抗低聚软骨基质蛋白另一表位的抗体2,抗体2购买自hytest,质控线固定有羊抗鸡igy,原料来源于北京佰桥瑞景生物科技有限公司。
41.检测线上抗低聚软骨基质蛋白的抗体2的包被浓度为1mg/ml;
42.质控线上所述配体2的包被浓度为1mg/ml。
43.nc膜包被前先配制包被缓冲液,分别将抗低聚软骨基质蛋白另一表位的抗体2配制为抗体2包被工作液,用于后续的t线划膜;将羊抗鸡igy配制为质控线(c线)上抗体的包被工作液。
44.将上述包被工作液通过划膜仪以1ul/cm的包被量及50mm/s的包被速度包被到nc的相应位置上(c线距nc膜下缘1.6cm,c、t线间距为0.6cm),送入37℃烘箱烘烤12-24h后装入装有干燥剂的铝箔袋密封,备用。
45.结合垫的制备如下:
46.1)探针制备:配制探针制备试剂。
47.(1)取量子点悬液100μl,分散在200μl反应缓冲液(25mm pb缓冲液(ph6.0
±
0.2))中,混匀。
48.(2)加入偶联剂edc(10mg/ml)12μl,恒温(30度)混匀孵育0.5h。15000rpm离心20min,去上清后,将量子点分散在100μl反应缓冲液中,超声分散均匀。
49.(3)取100μg抗低聚软骨基质蛋白抗体1,分散在200μl反应缓冲液中,将活化后的量子点迅速加入到抗体中,混匀;恒温(30度)混匀孵育1h。
50.(4)12000rpm离心15min,去除游离的抗体。
51.(5)加封闭液200μl,充分超声(功率10-20%)分散,恒温(30度)混匀孵育2h。
52.(6)12000rpm离心15min,去上清后,加入保存液200μl,充分超声(功率10-20%)得到量子点标记的抗低聚软骨基质蛋白抗体1探针溶液。采用同样方法制备量子点标记的鸡igy探针溶液。
53.2)配制探针稀释液:用探针稀释液(0.01m pb缓冲液)分别稀释量子点标记的抗低聚软骨基质蛋白抗体1探针溶液和量子点标记的鸡igy探针溶液,配制成探针工作液(其中抗低聚软骨基质蛋白抗体1探针溶液的稀释度为1:80,鸡igy量子点探针溶液的稀释度为1:200),然后通过喷金仪以3ul/cm的包被量及50mm/s的包被速度均匀喷到处理好的结合垫上,重复喷一次,送入45℃烘箱烘烤12-24h后装入装有干燥剂的铝箔袋密封,备用。
54.参照图2所示,试纸条还包括卡壳6,卡壳6具有腔体,其上设有加样孔和观察窗,pvc底板1、样品垫2、结合垫3、硝酸纤维素膜4和吸水垫5均固定于腔体内。
55.使用上述试纸条进行低聚软骨基质蛋白检测的方法如下:
56.从加样孔加入待测样本,样本中的低聚软骨基质蛋白经过样品垫2后与结合垫3中的量子点标记的抗低聚软骨基质蛋白抗体结合并沿着硝酸纤维素膜4向吸水纸5方向进行侧向流动,流经检测线时被抗低聚软骨基质蛋白另一表位的抗体结合并停留在检测线上。结合垫中的量子点标记的鸡igy在经样本中的液体的带动下,沿着硝酸纤维素膜4向吸水纸5方向进行侧向流动,流经质控线时被质控线上的鸡igy结合并停留在质控线上。
57.采用能对量子点含量进行定量检测的量子点荧光免疫分析仪从观察窗对试纸条
进行检测。检测线位置的量子点荧光强度(t)与待测样本中的低聚软骨基质蛋白的浓度成正相关,而质控线上形成的量子点标记的鸡igy的量子点荧光强度(c)在同一批次的试纸条上为基本一致的恒定值。采用已知不同浓度的低聚软骨基质蛋白在试纸条上检测,计算相应的t/c值并制定校准曲线,检测时利用样本在试纸条上的t/c值并结合校准曲线,实现对低聚软骨基质蛋白的定量检测。
58.实施例2
59.在本实施例中,示踪物采用胶体金。结合垫3上胶体金标记的抗低聚软骨基质蛋白抗体1和胶体金标记的鸡igy,包被量为3.0μl/cm。胶体金标记的方法已非常成熟,在此不再详述。胶体金标记的抗低聚软骨基质蛋白抗体1的标记量同实施例1。
60.与实施例1相比,检测仪器为胶体金免疫分析仪。其余检测方法以及试纸条的制备方法同实施例1。
61.实施例3
62.在本实施例中,示踪物采用荧光微球。结合垫3上荧光微球标记的抗低聚软骨基质蛋白抗体1和荧光微球标记的鸡igy,包被量为3.0μl/cm。荧光微球标记的方法如下:荧光微球以二甲亚砜溶解,待标记抗体脱盐置换缓冲体系并检测蛋白浓度,按比例将荧光微球与待标记抗体混合,避光振荡混匀2小时,加氢氧化钠溶液中止反应,再用透析膜脱盐,计算标记比率待用。荧光微球标记的抗低聚软骨基质蛋白抗体1的标记量同实施例1。
63.与实施例1相比,检测仪器为荧光免疫分析仪。其余检测方法以及试纸条的制备方法同实施例1。
64.实施例4
65.在本实施例中,示踪物采用金磁纳米。结合垫3上金磁纳米标记的抗低聚软骨基质蛋白抗体1和金磁纳米标记的鸡igy,包被量为3.0μl/cm。金磁纳米标记的抗低聚软骨基质蛋白抗体1的标记量同实施例1。
66.与实施例1相比,检测仪器为金磁纳米免疫分析仪。其余检测方法以及试纸条的制备方法同实施例1。
67.实施例5
68.在本实施例中,示踪物采用上转发光。结合垫3上具有上转发光标记的抗低聚软骨基质蛋白抗体1和上转发光标记的鸡igy,包被量为3.0μl/cm。上转发光标记的抗低聚软骨基质蛋白抗体1的标记量同实施例1。
69.与实施例1相比,检测仪器为上转发光免疫分析仪。其余检测方法以及试纸条的制备方法同实施例1。
70.实施例6
71.在本实施例中,示踪物采用时间分辨荧光。结合垫3上时间分辨荧光标记的抗低聚软骨基质蛋白抗体1和时间分辨荧光标记的鸡igy,包被量为3.0μl/cm。时间分辨荧光标记的抗低聚软骨基质蛋白抗体1的标记量同实施例1。
72.与实施例1相比,检测仪器为时间分辨荧光分析仪。其余检测方法以及试纸条的制备方法同实施例1。
73.实施例7
74.在本实施例中,示踪物采用量子点。结合垫3上量子点标记的抗低聚软骨基质蛋白
抗体1和量子点标记的鸡igy,包被量为3.0μl/cm。量子点标记的抗低聚软骨基质蛋白抗体1的标记量同实施例1。
75.本实施例的其余部分与实施例1相同。
76.实施例8
77.与实施例1相比,区别仅在于,在样品垫中采用或加入滤血膜,当样本中含有红细胞时,红细胞被滤血膜阻挡,可以减少红细胞对检测结果的影响。本发明提供的试纸条适用于全血样本的检测。
78.实验例1
79.采用已知不同浓度的低聚软骨基质蛋白在试纸条上检测,计算相应的t/c值并制定校准曲线,检测时利用样本在试纸条上的t/c值并结合校准曲线,实现对低聚软骨基质蛋白的定量检测。实际定标时,在检测线性范围内选择5至11个不同浓度的低聚软骨基质蛋白校准备品采用试纸条进行检测,计算每个浓度校准品的t/c值,以t/c值为横坐标,浓度为纵坐标,对曲线进行二元多项式拟合,计算y=ax2+bx+c的a、b、c的值。检测样本时,将样本检测得到的t/c值代入标准曲线公式,即可得到样本中低聚软骨基质蛋白的浓度。
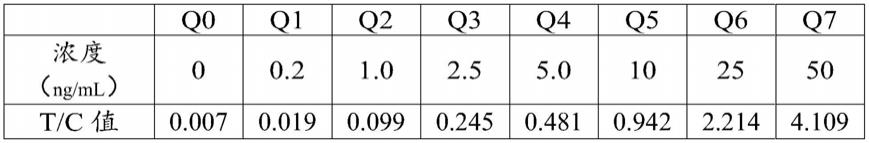
80.使用工作校准品q0-q7进行3次重复检测,记录对应t/c值,计算平均值,以工作校准品浓度为纵坐标,以工作校准品对应的t/c值平均值为横坐标进行曲线拟合。
81.聚集蛋白聚糖定量检测值参照下表所示,由此绘制的标准曲线参照图3所示。
[0082][0083]
本实验例的其余部分与实施例1相同,在本实施例中未解释的特征,均采用实施例1的解释。
[0084]
由上述测试结果可知,分析灵敏度为0.2ng/ml。线性范围:在0.2-50ng/ml浓度范围内,r2=1,本试剂盒检测线性相关系数可以满足r≥0.990的要求。
[0085]
实验例2
[0086]
对每批次试纸条上的质控线上示踪物光学强度的c值进行检测并计算平均值及sd,在检测时对c值设置一范围,高于或低于此范围时,认为试纸条在检测过程中存在问题,仪器予以报警或不报告结果。可以起到质控的效果。
[0087]
本实施例的其余部分与实施例1相同,在本实施例中未解释的特征,均采用实施例1的解释。
[0088]
实验例3
[0089]
本实验例进行稳定性测试。
[0090]
经过对201001、201101、201102三批(实施例1制备的检测聚集蛋白聚糖的试纸条)产品的实时稳定性(2-8℃、8-30℃)实验,至20个月时,产品各项性能指标均符合要求。
[0091]
经过对201001、201101、201102三批(实施例1制备的检测聚集蛋白聚糖的试纸条)产品的开封稳定性试验,结果表明,撕开铝箔袋30分钟内对检测结果无影响。
[0092]
经过对201001、201101、201102三批(实施例1制备的检测聚集蛋白聚糖的试纸条)产品的加速稳定性试验(37℃),其结果表明,本发明生产的聚集蛋白聚糖测定试剂盒(量子
点荧光免疫层析法)的稳定性可以保证有效期为18个月。
[0093]
经过对201001、201101、201102三批(实施例1制备的检测聚集蛋白聚糖的试纸条)产品的运输稳定性实验(模拟高低温运输),其结果表明,上述检测聚集蛋白聚糖的试纸条(量子点荧光免疫层析法)能经受住运输过程中遇到温度过高和过低的极端天气的考验。
[0094]
经过对血清、血浆、全血样本在2-8℃和-20℃保存条件下的稳定性实验,其结果表明,血清、血浆、全血样本可在2-8℃保存5天,血清、血浆样本可在-20℃保存3个月。
[0095]
实验例4
[0096]
本实验例对实施例1提供的试纸条进行分析重复性测试和准确度测试。
[0097]
重复性
[0098]
同一批次的检测试剂对检测范围内某个浓度的样本进行重复检测10次,计算10次测量结果的平均值(m)和标准差(sd),根据公式cv=sd/m
×
100%得出变异系数。
[0099]
批间精密度
[0100]
三个批次的检测试剂对检测范围内某个浓度的样本各重复检测10次,计算30次测量结果的平均值(m)和标准差(sd),根据公式cv=sd/m
×
100%得出变异系数。
[0101]
准确度
[0102]
同一批次的检测试剂对检测范围内某个浓度的样本进行重复检测3次。根据公式(1)计算相对偏差b。
[0103]
b=(m-t)/t
×
100%
ꢀꢀ
(1)
[0104]
式中:b——相对偏差;
[0105]
m——测量浓度均值;
[0106]
t——标定浓度。
[0107]
结果显示,重复性测试变异系数cv值为9.6%;批间精密度cv值为12.1%。准确度测试相对偏差为7.5%。
[0108]
另外,本实验例还检测了钩状效应:发现实施例1提供的试纸条在3000ng/ml浓度范围内不会产生钩状效应。
[0109]
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1