检测新型冠状病毒中和抗体的试剂盒及其制备方法与应用
1.本发明涉及生物医药检测技术领域,尤其涉及一种检测新型冠状病毒中和抗体的试剂盒及其制备方法与应用。
背景技术:
2.新型冠状病毒肺炎(covid-19)暴发流行对全球公众健康构成了严重威胁。covid-19患者与2003年严重急性呼吸综合征和2012年中东呼吸系统综合征患者症状相似,表现出一系列包括干咳、发热、头痛、呼吸困难等症状,病死率达3-5%。截至2021年8月31日,全球超过2.1亿人确诊covid-19,453万人死亡,同时该病给全球带来严重的经济损失。2020年1月20日,卫健委发布2020年1号公告,将新型冠状病毒感染的肺炎纳入乙类传染病,并采取甲类传染病的预防、控制措施。将新型冠状病毒感染的肺炎纳入检疫传染病管理。
3.新型冠状病毒(severeacute respiratory syndrome coronavirus 2,sars-cov-2)中有个重要的棘突s蛋白(spike protein),s蛋白上有一个受体结合结构域,叫做receptorbinding domain(rbd),是与人体细胞上ace2直接结合的位点。研究证实s-rbd是中和抗体主要的抗原表位,针对s-rbd产生的特异性抗体可以阻断新型冠状病毒与ace2结合,从而使病毒不能入侵宿主细胞,起到“中和”病毒的作用,故称为中和抗体。
4.新型冠状病毒已形成全球大流行,对公共健康、社会经济等造成严重负担,迫切需要有效的控制手段。疫苗成为世界各国对抗新型冠状病毒的重要手段。据卫生健康委,截至2021年8月31日,全国累计报告接种新型冠状病毒疫苗206758.9万剂次。新型冠状病毒中和抗体的检测可以反映群体的感染率、个人的康复情况以及疫苗的效果,但传统的病毒中和实验需使用活病毒和细胞,且对实验室安全性及操作人员技能要求较高。这种耗时长、要求高的传统中和检测方法显示不适用于传播速度快、感染覆盖范围广的新型冠状病毒。因此,建立快速检测中和抗体的方法十分有意义。
技术实现要素:
5.为解决上述技术问题,本发明提供了一种检测新型冠状病毒中和抗体的试剂盒及其制备方法与应用。通过s-rbd特异性结合中和抗体的双抗原夹心法,这种方法只采用s-rbd作为抗原来检测总中和抗体,包括针对s-rbd中和表位的igg、igm、iga总抗体,其灵敏度和特异性比单独检测igg或igm更高。
6.本发明的第一个目的是提供一种检测新型冠状病毒中和抗体的试剂盒,包括卡壳、位于所述卡壳内的试纸条;所述试纸条包括pvc底板、吸水垫、反应膜、结合垫和样品垫;所述结合垫上负载有胶体金标记的羊抗鼠igg抗体和检测抗原;所述反应膜上设有检测线t线和质控线c线;所述检测线靠近所述结合垫一侧,所述质控线靠近所述吸水垫一侧;所述检测线上包被有捕获抗原,所述质控线上包被有质控物;编码所述捕获抗原和检测抗原均为s-rbd蛋白;所述s-rbd蛋白的核苷酸序列如seq id no.1所示;所述s-rbd蛋白的氨基酸序列如seq id no.2所示。
7.所述seq id no.1的序列如下:
8.agggtacaaccgacggagtccatcgtacggtttccgaacatcactaacttatgcccattcggagaagttttcaatgcaacgagattcgcatccgtctatgcatggaaccgaaagcgaattagcaattgcgtggccgattatagcgtactatacaattcagctagcttctccacgttcaaatgctatggggtatcgcccaccaagttgaatgacctatgttttactaacgtctatgccgacagttttgtaataagaggagacgaggtacggcaaatcgcaccggggcaaactggaaaaattgcggattataactacaagcttccggacgattttacgggttgtgtgatagcatggaactcgaataacttagacagcaaggtcggtggcaactacaactacctttataggttgtttcggaaatcaaatttaaagccattcgagagagacataagtacggagatataccaagccggtagtacaccctgtaatggtgttgaagggttcaattgctatttcccgttgcagtcgtatggttttcaaccaacaaacggtgttggatatcagccgtaccgggtggttgttctatccttcgagctcctacacgccccagctacggtctgtggtccaaagaagtcgacaaacctagtcaagaataaatgtgttaacttt。
9.所述seq id no.2的序列如下:
10.rvqptesivrfpnitnlcpfgevfnatrfasvyawnrkrisncvadysvlynsasfstfkcygvsptklndlcftnvyadsfvirgdevrqiapgqtgkiadynyklpddftgcviawnsnnldskvggnynylyrlfrksnlkpferdisteiyqagstpcngvegfncyfplqsygfqptngvgyqpyrvvvlsfellhapatvcgpkkstnlvknkcvnf。
11.在本发明的一个实施例中,所述s-rbd将新型冠状病毒s蛋白的rbd序列连接到载体上,5’端加入序列及信号肽序列,3’端加入6个组氨酸(his-tag)的编码序列,构建好的表达载体通过质粒大量提取获得高纯度质粒,形成新型冠状病毒s-rbd蛋白。
12.在本发明的一个实施例中,所述新型冠状病毒s-rbd蛋白的制备方法,具体包括以下步骤,
13.(1)将新型冠状病毒s蛋白的rbd序列连接到载体上,5’端加入序列及信号肽序列,3’端加入6个组氨酸(his-tag)的编码序列和翻译终止密码子;
14.(2)构建好的表达载体通过质粒提取获得高纯度质粒,将质粒瞬时转染悬浮细胞hek293f细胞,于4-6天收集细胞培养液的上清液;将所有的细胞上清液混合后通过滤膜过滤,除去细胞碎片,得到滤过液;
15.(3)使用镍离子亲和层析纯化细胞上清液,以含20mm咪唑的咪唑缓冲液洗涤亲和柱,以除去非特异结合蛋白,然后以含50、250、500mm咪唑的咪唑缓冲液进行梯度洗脱,将含有目的蛋白的洗脱液浓缩,再通过凝胶过滤层析进一步纯化即可。
16.在本发明的一个实施例中,在步骤(1)中,所述信号肽序列如seq id no.3所示。
17.所述seq id no.3的序列如下:
18.mhssallcclvlltgvra。
19.在本发明的一个实施例中,在步骤(2)中,采用0.22μm的滤膜进行过滤。
20.在本发明的一个实施例中,在步骤(3)中,所述咪唑缓冲液中缓冲液的配制方法:7.8gna2hpo4·
2h2o,17.54g nacl,加适量水溶解后定容到1000ml,并调节ph至8.0。
21.在本发明的一个实施例中,在步骤(3)中,选择10kda截留分子量的超滤管将洗脱液浓缩。
22.在本发明的一个实施例中,在步骤(3)中,镍离子金属鳌合亲和层析介质为ni-nta。
23.在本发明的一个实施例中,在步骤(3)中,凝胶过滤层析柱为superdex20010/
300gl。
24.在本发明的一个实施例中,在步骤(3)后,采用sds-page鉴定蛋白纯度。
25.在本发明的一个实施例中,所述反应膜设置于所述pvc底板中部位置,所述吸水垫设置于所述pvc底板一端并叠压搭接在所述反应膜的一端上,所述结合垫设置于所述pvc底板另一端并叠压搭接在所述反应膜的另一端上,所述样品垫挨着结合垫设置于所述pvc底板上并叠压搭接在所述结合垫上。
26.在本发明的一个实施例中,所述捕获抗原的划膜浓度为0.5-1.5mg/ml;所述检测抗原的金标浓度为0.1-0.3mg/ml。
27.在本发明的一个实施例中,所述捕获抗原的划膜浓度为1mg/ml;所述检测抗原的金标浓度为0.2mg/ml。
28.在本发明的一个实施例中,所述质控物为羊抗鼠igg抗体。
29.在本发明的一个实施例中,所述反应膜的制备方法包括以下步骤,将羊抗鼠igg抗体包被在硝酸纤维素膜上形成质控线c线、s-rbd蛋白包被在硝酸纤维素膜上形成检测线t线,所述羊抗鼠igg抗体和所述s-rbd蛋白在硝酸纤维素膜上的划线流量均为0.8-1.0μl/cm,所述质控线c线和检测线t线相互平行且间隔距离为3-5mm。
30.在本发明的一个实施例中,所述反应膜的制备方法包括以下步骤,将羊抗鼠igg抗体包被在硝酸纤维素膜上形成质控线c线、s-rbd蛋白包被在硝酸纤维素膜上形成检测线t线,所述羊抗鼠igg抗体和所述s-rbd蛋白在硝酸纤维素膜上的划线流量均为0.9μl/cm,所述质控线c线和检测线t线相互平行且间隔距离为4mm。
31.在本发明的一个实施例中,所述羊抗鼠igg抗体的浓度为0.8-1.2mg/ml;所述s-rbd蛋白的浓度为1.3-1.7mg/ml。
32.在本发明的一个实施例中,所述羊抗鼠igg抗体的浓度为1mg/ml;所述s-rbd蛋白的浓度为1.5mg/ml。
33.在本发明的一个实施例中,所述羊抗鼠igg抗体和s-rbd蛋白分别用磷酸盐缓冲液稀释。
34.在本发明的一个实施例中,所述磷酸盐缓冲液的规格为0.01m,ph=7.4。
35.在本发明的一个实施例中,所述反应膜的制备过程中,羊抗鼠igg抗体和s-rbd蛋白是通过喷金划膜一体机依次分别划在硝酸纤维膜上。
36.在本发明的一个实施例中,所述结合垫的制备方法包括以下步骤,将胶体金标记的羊抗鼠igg抗体和检测抗原均匀喷涂在玻璃纤维垫上进行烘干。
37.在本发明的一个实施例中,所述羊抗鼠igg抗体和检测抗原的喷涂流量为8-12μl/cm。
38.在本发明的一个实施例中,所述羊抗鼠igg抗体和检测抗原的喷涂流量为10μl/cm。
39.在本发明的一个实施例中,所述结合垫上胶体金标记的羊抗鼠igg抗体和检测抗原的体积比为1:1.2-1.8。
40.在本发明的一个实施例中,所述结合垫上胶体金标记的羊抗鼠igg抗体和检测抗原的体积比为1:1.5。
41.在本发明的一个实施例中,所述烘干的温度为35-40℃;烘干的时间为10-14h。
42.在本发明的一个实施例中,所述烘干的温度为37℃;烘干的时间为12h。
43.本发明的第二个目的是提供一种所述的试剂盒在检测新型冠状病毒中和抗体中的应用,包括以下步骤,取8-12μl待测样本加入到试纸条上反应10-15min。
44.在本发明的一个实施例中,所述样本可以用2-3滴稀释液进行稀释;所述稀释液为含4-6%聚乙烯吡咯烷酮(pvp)的磷酸盐缓冲液。
45.在本发明的一个实施例中,所述的试剂盒在检测新型冠状病毒中和抗体中的应用,包括以下步骤,取10μl待测样本加入到试剂盒的加样孔中,再加入3滴样本稀释液反应15min。
46.在本发明的一个实施例中,所述的样本稀释液为含5%聚乙烯吡咯烷酮(pvp),ph为7.4的磷酸盐缓冲液。
47.检测原理是通过标记物标记的抗原与待检血清中的相应抗体形成免疫复合物,然后再与固定在固相载体上的特异性抗原结合形成标记的抗原-抗体-固相抗原复合物,通过标记物判断抗体含量。其中,捕获抗原即结合到固定载体上,用于捕获抗体的抗原,检测抗原即标记有标记物的抗原。
48.本发明的技术方案相比现有技术具有以下优点:
49.(1)本发明所述的检测新型冠状病毒中和抗体的试剂盒以新型冠状病毒s-rbd蛋白作为捕获抗原和检测抗原,由于该方法基于病毒特异性的抗原检测抗体,从机制上可以有效减少假阳性;且相比于单独或联合检测新冠igg或igm抗体,该双抗原夹心法检测的是包含igm、igg、iga的总抗体,其灵敏度和特异性比单独或联合检测igg或igm更高。
50.(2)本发明所述的检测新型冠状病毒中和抗体的试剂盒具有简便快捷、稳定性好、灵敏度高和特异性好等特点,对新冠病毒疫苗的效用评估、接种人群的筛查和随访康复人群中和抗体水平评估具有重要意义。
51.(3)本发明所述的检测新型冠状病毒中和抗体的试剂盒经过试验证明,其普遍适用于各类型的疫苗接种后,接种人群的中和抗体水平的评估,且操作简单,适合现场快速检测,快速出结果,结果直观,可以准确测定待测物的含量。
附图说明
52.为了使本发明的内容更容易被清楚地理解,下面根据本发明的具体实施例并结合附图,对本发明作进一步详细的说明,其中:
53.图1为本发明经凝胶过滤层析进一步纯化得到的新型冠状病毒s-rbd蛋白的凝胶过滤层析图。
54.图2为本发明采用sds-page鉴定蛋白纯度的电泳图。
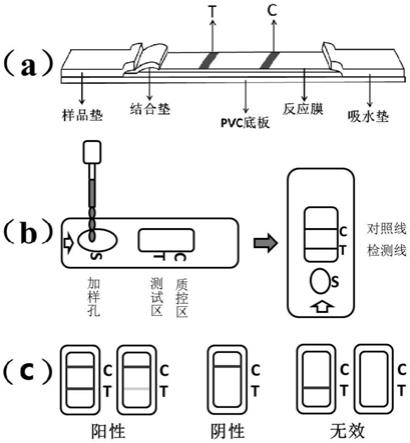
55.图3为本发明用于检测新型冠状病毒中和抗体的试剂盒结构图和判定方法;其中,(a)为试纸条的示意图,(b)为试剂盒的产品示意图,(c)为判定方法。
56.图4为本发明双抗原夹心检测试剂盒对接种过疫苗的血清样本检测显色图。
57.图5为本发明双抗原夹心检测试剂盒对未接种过疫苗的血清样本检测显色图。
58.图6为本发明双抗原夹心检测试剂盒对不同浓度质控中和抗体的检测显色图。
具体实施方式
59.下面结合附图和具体实施例对本发明作进一步说明,以使本领域的技术人员可以更好地理解本发明并能予以实施,但所举实施例不作为对本发明的限定。
60.除非另有定义,本技术所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“及/或”包括一个或多个相关的所列项目的任意的和所有的组合。
61.下述实施例中涉及的试剂如下:
62.重悬缓冲液:由0.1%吐温20、5%蔗糖、0.5%peg 6000、0.02%叠氮化钠、1%聚乙烯吡咯烷酮、1%甘露糖醇、1%山梨糖醇和0.2%牛血清蛋白溶解到磷酸盐缓冲液(0.02m,ph=7.4)配制而成。
63.咪唑缓冲液中的缓冲液:7.8g na2hpo4·
2h2o,17.54g nacl,加适量水溶解后定容到1000ml,并调节ph至8.0。
64.实施例
65.一种检测新型冠状病毒中和抗体的试剂盒及其制备方法与应用,具体包括以下步骤:
66.a、新型冠状病毒s-rbd蛋白的制备,具体包括以下步骤:
67.(1)将新型冠状病毒s蛋白的rbd序列连接到pcmv3-s1sp-rbd载体上,5’端加入序列及信号肽序列,3’端加入6个组氨酸(his-tag)的编码序列;
68.(2)构建好的表达载体通过质粒提取获得高纯度质粒,将质粒瞬时转染悬浮细胞hek293f细胞,于5天收集细胞培养液,将所有培养液离心得到上清液;
69.(3)使用镍离子亲和层析纯化细胞上清液,以含20mm咪唑的咪唑缓冲液洗涤亲和柱,以除去非特异结合蛋白,然后用分别含50、250、500mm咪唑的咪唑缓冲液进行梯度洗脱,收集各阶段洗脱峰,用sds-page检测目的蛋白的分子量大小和纯度。将含有目的蛋白的洗脱液用10kda的超滤管进行浓缩,再通过ge公司akatpurifier蛋白纯化系统以superdex20010/300gl凝胶过滤预装柱进一步纯化,将收集到的蛋白进行制样,结果如附图1所示,采用sds-page鉴定蛋白纯度,结果如附图2所示。
70.从附图1-2可以看出,经过亲和层析和凝胶过滤层析后可获得单一峰型、纯度较高的目的蛋白。
71.b、胶体金纳米粒子的制备,具体包括以下步骤:
72.取22.5ml氯金酸溶液(4g/l)加入到装有277.5ml超纯水的锥形瓶中,上述溶液保持磁力搅拌并加热(300℃),溶液沸腾后,向上述溶液中加入8ml的柠檬酸钠溶液(20mg/ml),并保持加热和搅拌30min,反应完成后自然冷却至室温即得到胶体金纳米粒子溶液。
73.c、胶体金纳米粒子标记的羊抗鼠igg抗体的制备,具体包括以下步骤:
74.取上述胶体金纳米粒子溶液5ml到15ml离心管中,并用0.1m碳酸钾溶液将上述胶体金纳米粒子溶液ph值调节至8.2,然后加入50μg羊抗鼠igg抗体,涡旋混匀后静置45min,然后加入10%(m/v)牛血清蛋白溶液,涡旋混匀后静置2h,反应完成后在9000rpm和4℃条件下离心50min,底部沉淀用0.5ml重悬缓冲液复溶,得到胶体金纳米粒子标记的羊抗鼠igg抗体。
75.d、胶体金纳米粒子标记的检测抗原(s-rbd蛋白)的制备,具体包括以下步骤:
76.取上述胶体金纳米粒子溶液5ml到15ml离心管中,并用0.1m碳酸钾溶液将上述胶体金纳米粒子溶液ph值调节至8.2,然后加入75μg s-rbd蛋白,涡旋混匀后静置45min,再加入10%(m/v)牛血清蛋白溶液,涡旋混匀后静置2h,反应完成后在9000rpm和4℃条件下离心50min,最后底部沉淀物用0.5ml重悬缓冲液复溶,得到胶体金纳米粒子标记的检测抗原(s-rbd蛋白)。
77.e、检测新型冠状病毒中和抗体的试剂盒的制备,具体包括以下步骤:
78.(1)反应膜的制备:硝酸纤维素膜上依次划有相互平行的检测线t线和质控线c线,检测线t线和质控线c线间隔距离为4mm;将羊抗鼠igg抗体和捕获抗原s-rbd蛋白分别用磷酸盐缓冲液(0.01m,ph=7.4)稀释到1mg/ml和1.5mg/ml;将稀释后的羊抗鼠igg抗体和捕获抗原s-rbd蛋白通过喷金划膜一体机依次分别划在硝酸纤维膜上,划线流量均为0.9μl/cm,其中,捕获抗原的划膜浓度为1mg/ml。
79.(2)结合垫的制备:将有胶体金标记的羊抗鼠igg抗体和捕获抗原s-rbd蛋白按照体积比1:1.5的比例混合后用喷金划膜一体机均匀喷涂在1cm宽的玻璃纤维垫上,喷涂流量为10μl/cm,最后37℃下烘12h制备得到结合垫,其中,检测抗原的金标浓度为0.2mg/ml。
80.(3)试剂盒的制备:将反应膜粘贴在在pvc底板中间位置,吸水垫粘贴在pvc底板一端并叠压搭接在反应膜的一端上,结合垫粘贴在pvc底板另一端并叠压搭接在反应膜的另一端上,样品垫挨着结合垫粘贴在pvc底板上并叠压搭接在结合垫上,即得到试纸板,将上述试纸板沿纵向斩切成3mm的试纸条,使得每条均包含pvc底板、吸水垫、反应膜、结合垫和样品垫,最终将上述试纸条封装到卡壳即得到用于新型冠状病毒中和抗体检测的免疫层析试纸卡,其结构如附图3(a-b)所示。试剂盒的判定方法为:t检测线和c质控线都出现清晰可见的红色条带,判为阳性,t线颜色越深,阳性越强;只有c质控线出现清晰可见的红色条带,判为阴性;若c质控线不出现红色条带,判为无效,如附图3(c)所示。
81.应用例
82.取10μl待测血清样本加入到检测卡的加样孔中,再加入3滴样本稀释液,流过结合垫与胶体金标记的检测抗原(s-rbd蛋白)反应,再流过反应膜与固定的捕获抗原和胶体金标记的羊抗鼠igg抗体结合,最后流到吸水垫,室温反应15min后通过裸眼即可观察结果。其中,样本稀释液为含5%聚乙烯吡咯烷酮ph为7.4的磷酸盐缓冲液,3ml/管。
83.将上述检测试纸卡检测所收集的40份接种过两针新冠疫苗的血清样本和20份未接种疫苗的阴性血清样本,结果如附图4-5所示,发现该试纸卡能有效的检测出阳性血清,且未接种疫苗的血清均为阴性,特异性较好。
84.测试例
85.将质控中和抗体用磷酸盐缓冲液稀释至50ng/ml、10ng/ml、2ng/ml,取10μl稀释好的抗体加入到检测卡的加样孔中,再加入3滴样本稀释液,室温反应15min后通过裸眼即可观察结果。结果如附图6所示,对于质控中和抗体,检测限可达到2ng/ml,灵敏度较高。其中,样本稀释液为含5%聚乙烯吡咯烷酮ph为7.4的磷酸盐缓冲液。
86.显然,上述实施例仅仅是为清楚地说明所作的举例,并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引申出的显而易见的变化或变
动仍处于本发明创造的保护范围之中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1