一种基于拉曼光谱的肿瘤早期诊断系统的制作方法
1.本发明涉及医学诊断技术领域,更具体地说,它涉及一种基于拉 曼光谱的肿瘤早期诊断系统。
背景技术:
2.全球每年约有880万人死于癌症,占全球每年死亡总人数的约六 分之一,在死亡的癌症患者中,恶性肿瘤患者据有一席之地。导致癌 症死亡的一大原因是由于治疗不及时,在晚期恶性肿瘤患者进行治疗 时,往往会由于肿瘤的治疗方法复杂以及治疗效果不确定,造成患者 的治疗质量下降。
3.头颈部恶性肿瘤发病率较高,在世界范围内,是第六大最常见的 癌。且其发病较隐匿,早期极易与炎症、溃疡等病变混淆,不易察觉, 目前,确诊绝大多数恶性肿瘤的“金标准”仍然是组织活检,但由于 组织学诊断较为主观,耗时较长,并且会对病人造成一定创伤,所以 仅能用于诊断临床可见的病变。然而有些早期病变通过临床检查难以 发现,甚至未出现组织病理学改变,但其细胞内某些生化物质及细胞 代谢、分泌已发生改变。因此,颌面部恶性肿瘤的早期诊断和有效治 疗是改善患者预后的关键。临床医生需要一种快速无创的确诊恶性肿 瘤的方法。
4.拉曼光谱是以光的非弹性散射为基础的一种振动光谱,其原理是 拉曼效应。当入射光照射某物质时,很少部分光子发生非弹性散射, 处于基态的分子吸收了光子的能量后跃迁至某一虚态,处于虚态的分 子发射光子而回到某一较低能量级,光子的方向和频率都发生改变, 这部分散射称为拉曼散射。拉曼光谱是拉曼散射的强度相对波长的函 数图,不同化学键有特定的拉曼位移谱带,拉曼光谱可提供不同物质 的分子结构信息,因此被称为“分子指纹”。与其他光谱相比,拉曼 光谱不需要对样本进行检测前处理,检测速度较快,对组织无损伤, 并且信号不受样本内水分水份干扰,更适合用于体内检测和体液检 测,可用于检测组织、细胞、血液、唾液等样本。现已有大量研究证 实拉曼光谱可用于诊断恶性肿瘤,如胃癌、肺癌、鼻咽癌等。因此, 拉曼光谱有广泛应用于头颈部恶性肿瘤的早期诊断的潜力。
5.传统拉曼光谱信号极其微弱,且易受荧光背景干扰。1977年van duyne等人发现吸附在粗糙银表面上的分子比普通溶液中的分子拉曼 信号增强了百万倍,这种粗糙贵金属表面增强拉曼信号的现象称为表 面增强现象。常用的表面增强剂有金溶胶和银溶胶。表面增强拉曼光 谱(sers)对组织无损伤,和传统拉曼光谱相比,拉曼信号更强,背 景荧光信号更弱,准确率和灵敏度高,便于实时检测,适合检测血液、 唾液等水分水份含量高、浓度较低的体液样本。血清和唾液中含有能 够检测恶性肿瘤的生物标志物,与活检相比,收集患者的血清、唾液 对患者的创伤更小,检测速度更快。
6.因此,本发明旨在设计一种基于拉曼光谱的肿瘤早期诊断系统, 可用于肿瘤早期诊断,且具有无创、快速、便捷等优点。
技术实现要素:
7.为了克服现有技术中所存在的上述缺陷,本发明提供了一种基于 拉曼光谱的肿瘤早期诊断系统,本发明利用表面增强拉曼光谱对用户 体液样本进行检测,结合样本预处理、拉曼光谱检测和肿瘤诊断于一 体,可完成基于拉曼光谱的肿瘤早期诊断,且无需病理医生观察、诊 断等主观性过程,完全可以形成针对肿瘤的诊断、筛查系统,用户可 通过本系统自行诊断,相比于传统病理组织切片检查,节省时间,提 高准确度,更加有利于患者的准确诊断以及患者的大规模筛查。
8.本发明的上述技术目的是通过以下技术方案得以实现的:一种基 于拉曼光谱的肿瘤早期诊断系统,包括箱体状的诊断设备,诊断设备 内设有竖直设置的隔板,隔板将诊断设备内部分隔为腔室一和腔室 二,腔室一内由上至下依次间隔设有横板一、横板二、横板三、横板 四、横板五和横板六,横板一与横板二之间设有电子抽屉一,横板三 和横板四之间设有电子抽屉二,横板五和横板六之间设有电子抽屉 三;电子抽屉一内设有存放板,存放板的顶面设有若干个穿过存放板 的壁厚的穿孔,每个穿孔内均设有唾液采集管,电子抽屉二内设有离 心机,电子抽屉三内设有拉曼光谱仪;腔室二内设有控制处理器和供 电装置,控制处理器与电子抽屉一、电子抽屉二、电子抽屉三、离心 机和拉曼光谱仪均为电连接;诊断设备的外壁嵌设有与控制处理器连 接的主控面板。
9.通过采用上述技术方案,主控面板与控制处理器电连接,用户可 通过主控面板对电子抽屉一、电子抽屉二、电子抽屉三、离心机和拉 曼光谱仪发出控制指令,从完成样本的预处理、拉曼光谱检测和待测 样本的快速诊断。
10.进一步的,诊断设备的外壁嵌设有无线通讯模块,无线通讯模块 与控制处理器电连接。
11.通过采用上述技术方案,可实现诊断设备与外界的信息交互。
12.进一步的,无线通讯模块远程信号连接于用户终端和数据库。
13.通过采用上述技术方案,诊断设备内的诊断结果可通过无线通讯 模块传输至用户终端,且当诊断结果为阳性时,将用户的样本数据传 输至数据库,扩大数据库。
14.进一步的,诊断设备的外壁嵌设有语音提示模块,语音提示模块 与控制处理器电连接。
15.通过采用上述技术方案,语音提示模块可对用户进行样本预处 理、样本光谱检测或样本的诊断时进行语音提示。
16.进一步的,控制处理器设有处理单元、控制单元和诊断单元,诊 断单元内设有有肿瘤诊断模型;
17.处理单元用于对用户检测样本的数据进行处理并传输;
18.控制单元用于对电子抽屉一、电子抽屉二、电子抽屉三、离心机 和拉曼光谱仪发出控制指令;
19.诊断单元用于诊断用户的体液样本。
20.通过采用上述技术方案,处理单元用于对用户检测样本的数据进 行处理并传输,控制单元用于对电子抽屉一、电子抽屉二、电子抽屉 三、离心机和拉曼光谱仪发出控制指令,诊断单元用于诊断用户的体 液样本。
21.进一步的,肿瘤诊断模型的建立包括以下步骤:
22.s1:划分样本:将样本集以4:1的比例随机分层划分为训练集和 测试集;
23.s2:特征值预处理:采用归一化方法将训练集特征值标准化并导 出标准化模型,利用标准化模型对测试集样本的特征值进行归一化处 理;
24.s3:特征降维:使用主成分分析pca,获取特征主成分信息,对 特征进行降维处理;
25.s4:参数优化:采用支持向量机算法建立模型,利用训练集进行 网格寻参,寻参过程使用五折交叉验证法,评分函数选为auc,选取 最优的参数组合用于最终模型的建立;
26.s5:模型建立:使用网格寻参获得的最优参数,使用整个训练集 训练最终模型;
27.s6:模型判断阈值修正:对建立好的模型的判断阈值进行修正, 以确保模型的稳健性,修正后的阈值依据原数据集中正负样本比例而 定,计算公式如下:
[0028][0029]
其中,thnew为修正后的判断阈值,大于该阈值的预测结果被判 断为正样本,n+,n-分别为正负样本的数目;
[0030]
s7:外部测试:使用最终模型对外部测试集进行预测,并计算评 分函数。
[0031]
通过采用上述技术方案,该肿瘤诊断模型可根据数据库内储存的 阳性病例的样本数据定期更新甚至实时更新,数据库的扩大可有提高 该肿瘤诊断模型的诊断准确率。
[0032]
进一步的,唾液采集管为salivette唾液收集管。
[0033]
综上所述,本发明具有以下有益效果:本发明利用表面增强拉曼 光谱对用户体液样本进行检测,结合样本预处理、拉曼光谱检测和肿 瘤诊断于一体,可完成基于拉曼光谱的肿瘤早期诊断,且无需病理医 生观察、诊断等主观性过程,完全可以形成针对肿瘤的诊断、筛查系 统,用户可通过本系统自行诊断,相比于传统病理组织切片检查,节 省时间,提高准确度,更加有利于患者的准确诊断以及患者的大规模 筛查。
附图说明
[0034]
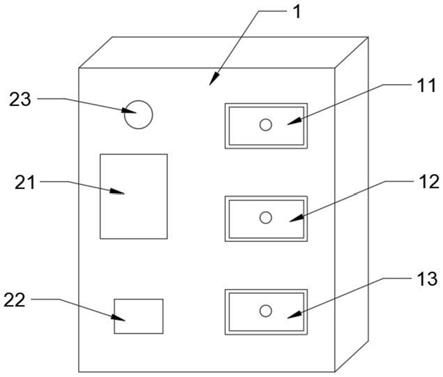
图1是本发明实施例中诊断设备的结构示意图;
[0035]
图2是本发明实施例中诊断设备的内部结构示意图;
[0036]
图3是本发明实施例中存放板的结构图;
[0037]
图4是本发明实施例中诊断设备、用户终端和数据库之间的信号 传递框图;
[0038]
图5是本发明实施例中肿瘤诊断的流程框图;
[0039]
图6是本发明实施例中的受试者信息表;
[0040]
图7是本发明实施例中鳞癌组、腺癌组、正常组的唾液平均sers 光谱图;
[0041]
图8是本发明实施例中鳞癌组、正常组唾液的平均光谱及差异光 谱图;
[0042]
图9是本发明实施例中腺癌组、正常组唾液的平均光谱及差异光 谱图;
[0043]
图10是本发明实施例中鳞癌组、腺癌组唾液的平均光谱及差异 光谱图;
[0044]
图11是本发明实施例中口腔鳞癌组、腺癌组、正常组唾液分类 参数表;
[0045]
图中:1、诊断设备;2、隔板;3、腔室一;4、腔室二;5、横 板一;6、横板二;7、横板三;8、横板四;9、横板五;10、横板六; 11、电子抽屉一;12、电子抽屉二;13、电子抽屉三;14、存
放板; 15、穿孔;16、唾液收集管;17、离心机;18、拉曼光谱仪;19、控 制处理器;20、供电装置;21、主控面板;22、无线通讯模块;23、 语音提示模块。
具体实施方式
[0046]
以下结合附图1-11对本发明作进一步详细说明。
[0047]
实施例:如图1至图3所示,一种基于拉曼光谱的肿瘤早期诊断 系统,包括箱体状的诊断设备1,诊断设备1内固定连接有竖直设置 的隔板2,隔板2将诊断设备1内部分隔为腔室一3和腔室二4,腔 室一3内由上至下依次间隔固定连接有横板一5、横板二6、横板三 7、横板四8、横板五9和横板六10,横板一5与横板二6之间安装 有电子抽屉一11,横板三7和横板四8之间安装有电子抽屉二12, 横板五9和横板六10之间安装有电子抽屉三13,电子抽屉一11、电 子抽屉二12和电子抽屉三13均采用电动滑轨的方式实现智能控制; 电子抽屉一11内安装有存放板14,存放板14的顶面开设有若干个 穿过存放板14的壁厚的穿孔15,每个穿孔15内均放置有唾液采集 管,唾液采集管为salivette唾液收集管,电子抽屉二12内安装有 离心机17,电子抽屉三13内安装有拉曼光谱仪18;腔室二4内安装 有控制处理器19和供电装置20,控制处理器19与电子抽屉一11、 电子抽屉二12、电子抽屉三13、离心机17和拉曼光谱仪18均为电 连接;诊断设备1的外壁嵌设有与控制处理器19连接的主控面板21。
[0048]
诊断设备1的外壁嵌设有无线通讯模块22,无线通讯模块22与 控制处理器19电连接,无线通讯模块22远程信号连接于用户终端和 数据库;诊断设备1的外壁嵌设有语音提示模块23,语音提示模块 23与控制处理器19电连接,控制处理器19设有处理单元、控制单 元和诊断单元,诊断单元内设有有肿瘤诊断模型,处理单元用于对用 户检测样本的数据进行处理并传输,控制单元用于对电子抽屉一11、 电子抽屉二12、电子抽屉三13、离心机17和拉曼光谱仪18发出控 制指令,诊断单元用于诊断用户的体液样本。
[0049]
其中,肿瘤诊断模型的建立包括以下步骤:
[0050]
s1:划分样本:将样本集以(4:1)的比例随机分层划分为训练集和 测试集;
[0051]
s2:特征值预处理:采用归一化方法将训练集特征值标准化并导 出标准化模型,利用标准化模型对测试集样本的特征值进行归一化处 理;
[0052]
s3:特征降维:使用主成分分析pca,获取特征主成分信息,对 特征进行降维处理;
[0053]
s4:参数优化:采用支持向量机算法建立模型,利用训练集进行 网格寻参,寻参过程使用五折交叉验证法,评分函数选为auc,选取 最优的参数组合用于最终模型的建立;
[0054]
s5:模型建立:使用网格寻参获得的最优参数,使用整个训练集 训练最终模型;
[0055]
s6:模型判断阈值修正:考虑到在采样时,临床正负样本的不均 衡性,对建立好的模型的判断阈值进行修正,其中原默认值为0.5, 以确保模型的稳健性,修正后的阈值依据原数据集中正负样本比例而 定,计算公式如下:
[0056][0057]
其中,thnew为修正后的判断阈值,大于该阈值的预测结果被判 断为正样本,在本实施例中,正样本为肿瘤样本,n+,n-分别为正负 样本的数目;
[0058]
s7:外部测试:使用最终模型对外部测试集进行预测,并计算评 分函数auc,acc,bacc等。
[0059]
当用户使用诊断设备1时,可通过主控面板21获取操作提示, 其中语音提示模块23可辅助提示操作步骤以及注意事项:
[0060]
s1:提示用户收集清晨时的唾液样本,且收集前需漱口1min, 此时主控面板21控制电子抽屉一11弹出,用户取出唾液收集管16 后,电子抽屉一11回到原来位置;
[0061]
s2:用户收集样本完成后,通过主控面板21点击下一步操作, 主控面板21打开电子抽屉二12和离心机17,提示用户将收集的唾 液以3000rpm转速离心2min,离心完成后,关闭电子抽屉二12和 离心机17;
[0062]
s3:离心完成后,此时通过主控面板21进入下一步操作,主控 面板21控制打开电子抽屉三13和拉曼光谱检测仪,用拉曼光谱仪 18检测待测样本,值得一提的是,用拉曼光谱仪18检测时,可在唾 液样本内滴入等比例的银溶胶,对样本进行表面增强光谱检测;
[0063]
s4:用户可在主控面板21内输入自身信息,检测完毕后,诊断 设备1可将诊断结果通过无线通讯模块22传输至用户终端。
[0064]
如图4所述,一种基于拉曼光谱的肿瘤早期诊断系统,多个诊断 设备1可设于多个场所,且每个诊断设备1可用于多个用户,当诊断 设备1检测到有用户样本确诊为肿瘤阳性时,可通过无线通讯模块 22将诊断为阳性的用户样本信息传输至数据库,扩充数据库,且数 据库的更新有利于建立新的准确率更高的诊断模型。
[0065]
如图5所示,是基于拉曼光谱的肿瘤早期诊断流程框图,其中, 样本预处理包括:对收集的唾液进行离心操作,具体为以3000rpm 转速离心2min,离心完成后,加入等比银溶胶充分均匀混合,置于 干净的铝片表面,室温下自然风干。
[0066]
银溶胶的制备采用盐酸羟胺还原硝酸银法。将9ml 0.1mol/l氢 氧化钠溶液加入10ml 0.06mol/l盐酸羟胺溶液中混合,然后将此混 合溶液迅速加入180ml 0.0011mol/l硝酸银溶液中,一边加入一边搅 拌均匀,得到乳灰色混合液。最后,将该乳灰色溶液以10000rpm转 速室温下离心10min,去除上清液,下层沉淀即为银溶胶。
[0067]
如图6-图11所示,本发明为验证肿瘤诊断模型的准确性,以口 腔鳞癌患者与唾液腺恶性肿瘤患者和非恶性肿瘤志愿者的唾液样本 光谱检测做比较实验,得出结论。
[0068]
如图6和图7所示,本次实验共获取高质量sers光谱139条, 其中口腔鳞癌患者51条,唾液腺恶性肿瘤患者16条,非恶性肿瘤志 愿者72条。图7显示了三组唾液归一化后的平均光谱。在拉曼位移 447、496、591、636、729、810、880、1002、1049、1133、1205、 1266、1324、1441、1650cm-1处,鳞癌、腺癌患者及非恶性肿瘤患 者唾液的拉曼光谱均发现拉曼峰,三组的光谱位置和形态大致相似, 但谱峰强度存在差异。
[0069]
如图8所示,比较鳞癌组与正常组的拉曼光谱,求得差异光谱, 可见与正常组相比,鳞癌组在拉曼位移496、591、636、1133、1200、 1266、1324、1441、1650cm-1处谱峰强度增加,1324cm-1处谱峰强 度差异有统计学意义(p《0.1),提示与胶原、嘌呤有关;在拉曼位移 447、880、1049cm-1处谱峰强度减弱,其中447、1049cm-1处谱峰 强度差异有统计学意义(p《0.1),提示与苯基、蛋白质有关。
[0070]
如图9所示,比较腺癌组与正常组的拉曼光谱,求得差异光谱, 可见腺癌组在拉曼位移636、810、1049、1133、1205、1324、1650cm-1 处谱峰强度增加,其中拉曼位移1133、
1205、1324cm-1处谱峰强度 差异有统计学意义(p《0.1),提示与胶原、苯丙氨酸、酪氨酸、嘌呤、d-甘露糖有关;在拉曼位移447、496cm-1处谱峰强度减弱,其中 446cm-1处谱峰强度差异有统计学意义(p《0.1),提示与苯基有关。
[0071]
如图10所示,比较鳞癌组与腺癌组的拉曼光谱,求得差异光谱, 可见与腺癌组相比,鳞癌组在拉曼位移447、496、591、729、1441、 1650cm-1处谱峰强度增加,其中拉曼位移496cm-1处谱峰强度差异 有统计学意义(p《0.1),提示与糖原有关;在拉曼位移810、1049、 1133、1205、1324cm-1处谱峰强度减弱,其中1049、1205cm-1处 谱峰强度差异有统计学意义(p《0.1),提示与胶原、苯丙氨酸、酪氨 酸或其他蛋白质有关。
[0072]
运用支持向量机方法,经小波变换去除噪音后,对口腔鳞癌患者、 唾液腺恶性肿瘤患者及非恶性肿瘤患者的血清拉曼光谱信息进行分 析,建立鉴别诊断模型,并验证其有效性。在鳞癌组与正常组的比较 中,选择正则化参数c=7,核函数宽度σ=0.02,69条鳞癌光谱中有 55条被归于鳞癌组,59条正常光谱中有46条被归于正常组。在腺癌 组与正常组的比较中,选择正则化参数c=90,,核函数宽度σ=0.13, 经样本平衡处理,62条腺癌光谱全部被归于腺癌组,66条正常光谱 中有60条被归于正常组。在鳞癌组与腺癌组的比较中,选择正则化 参数c=700,核函数宽度σ=0.27,经样本平衡处理,53条鳞癌组血 清光谱中有45条被归于鳞癌组;46条腺癌光谱全部被归于腺癌组。 计算每个鉴别诊断模型的灵敏度(se)、特异性(sp)、准确度(acc)、 matthew相关系数(mcc),结果如图11所示。鳞癌组与正常组准确 度为78.9%,腺癌组与正常组准确度为95.3%,鳞癌组与腺癌组准确 度为91.9%,表明该诊断模型稳定性较好,可用于鉴别不同疾病患者 的血清样品。
[0073]
工作原理:应用拉曼光谱仪18对肿瘤患者的体液进行检测,获 取不同肿瘤患者体液的特征性拉曼光谱数据,对数据进行减除背景、 降噪、平滑及归一化处理后,应用支持向量机对不同肿瘤患者体液的 特征性拉曼光谱数据进行分析建立的涎腺肿瘤诊断模型对肿瘤患者 体液的拉曼光谱数据进行分析,快速、准确、便捷的给出诊断报告。
[0074]
本具体实施例仅仅是对本发明的解释,其并不是对本发明的限 制,本领域技术人员在阅读完本说明书后可以根据需要对本实施例做 出没有创造性贡献的修改,但只要在本发明的权利要求范围内都受到 专利法的保护。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1