一种不同温度下水产动物中磺胺嘧啶给药方案的确定方法与流程
1.本发明涉及水产药物药效领域,特别是涉及一种不同温度下水产动物中磺胺嘧啶给药方案的确定方法。
背景技术:
2.鱼类是变温动物,其体温随环境温度的变化而变化。温度可以改变鱼类的心率、呼吸次数、心输出量、排泄率、代谢酶的活性等生理参数,从而对渔药的吸收、代谢、分布和排泄产生直接或间接的影响,从而改变渔药的动力学参数,对效果产生作用,因此给药方案需要发生改变。
3.鮰爱德华氏菌属肠杆菌科爱德华氏菌属,是一种革兰氏阴性短杆菌,是斑点叉尾鮰的重要致病原。近年来,斑点叉尾鮰的养殖在我国迅速发展,尤其在湖北、湖南和四川等省份有大量的分布。随着养殖规模的不断扩大,养殖密度的增加,疾病的危害越来越严重。鮰爱德华氏菌是斑点叉尾鮰的重要致病原,发病快、致死率高,导致了大量的经济损失。磺胺嘧啶具有良好的生物膜透过能力,对此细菌仍有良好的治疗效果。
4.为确定不同温度下磺胺嘧啶的给药方案,本发明旨在发明一种不同温度下水产动物中磺胺嘧啶给药方案的确定方法。
技术实现要素:
5.本发明的目的是提供一种不同温度下水产动物中磺胺嘧啶给药方案的确定方法,以解决上述现有技术存在的问题,本发明的不同温度下水产动物中磺胺嘧啶给药方案的确定方法能够提高磺胺嘧啶的治疗效果。
6.为实现上述目的,本发明提供了一种不同温度下水产动物中磺胺嘧啶给药方案的确定方法,包括以下步骤:
7.步骤一:从临床病鱼中分离出鮰爱德华氏菌,采用微量稀释法测定磺胺嘧啶对鮰爱德华氏菌的mic值;
8.步骤二:分别在18℃和24℃环境温度下对斑点叉尾鮰进行单次口灌给药,给药后分别采集组织样品;
9.步骤三:对斑点叉尾鮰进行单次静脉给药,给药后采集组织样品;
10.步骤四:对步骤二和步骤三采集的组织样品分别测定磺胺嘧啶的残留量;
11.步骤五:进行药动学参数计算,包括药时曲线下面积、吸收速率常数、消除速率常数、表观分布容积;
12.步骤六:根据计算公式1确定磺胺嘧啶的给药方案;
13.所述计算公式1为:
[0014][0015]
所述计算公式1中:dose为药物剂量;cmin为磺胺嘧啶在鱼体内稳态浓度,根据mic
确定;vd为表观分布容积;ka为吸收速率常数;k为消除速率常数;f为生物利用度;δ为给药间隔;
[0016]
所述生物利用度的计算公式2为:
[0017][0018]
所述计算公式2中:aucoral为口服给药下药时曲线下面积;auciv为静脉给药下药时曲线下面积;doseiv为静注剂量;doseoral口服剂量。
[0019]
进一步地,在步骤二和步骤三中,采样时间点为给药后的0.083、0.167、0.5、1、2、8、16、24、48和72h。
[0020]
进一步地,在步骤二和步骤三中,所述组织样品为血液、肌肉+皮、肝、肾和鳃。
[0021]
进一步地,在步骤四中,采用高效液相色谱法测定磺胺嘧啶的残留量。
[0022]
本发明公开了以下技术效果:
[0023]
通过本发明方法可以获得磺胺嘧啶在不同温度下的药动学参数,通过对鮰爱德华氏菌的药效学数据,制定不同环境温度下的给药方案,为水产养殖的临床用药提供技术支持,更科学的提高用药效率和药物安全,降低细菌病害对水产养殖造成的巨大经济损失。
具体实施方式
[0024]
现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
[0025]
应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
[0026]
除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。
[0027]
在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见得的。本发明说明书和实施例仅是示例性的。
[0028]
关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
[0029]
实施例1
[0030]
1.实验动物
[0031]
健康斑点叉尾鮰150尾(平均体重420.4
±
37.2g),购自中国水产科学研究院长江水产研究所试验基地。试验用水采用增氧泵连续充氧,保持水中溶氧大于4.8mg/l,ph为7.2~7.8,温度分为两组分别为18
±
0.5℃和24
±
0.5℃。试验前,鱼放置于玻璃水族箱内暂养
一周。
[0032]
2.药品及试剂
[0033]
药品:磺胺嘧啶粉购自湖北艾博科技有限公司,含量大于98%;标准品磺胺嘧啶购自德国dr.ehrenstorfer公司,含量大于99%。
[0034]
试剂:
[0035]
无水硫酸镁和氯化钠磷酸氢二钠购自上海国药集团,分析纯;中性氧化铝粉和c18粉购自天津博纳艾杰尔科技有限公司;乙腈、水和甲酸(纯度88%)均为色谱纯,购自美国j.t.baker公司。
[0036]
3.主要仪器
[0037]
高速冷冻离心机(20pr2520,日本日立);电子天平(mettler-toledoae-240,梅特勒-托利多公司);氮吹仪(kd200,巩义予华有限公司);漩涡混合仪(上海康华生化仪器制造公司);高效液相色谱-串联质谱(thermo tsq quantumacess max,美国thermo公司)。
[0038]
4.试验采样
[0039]
采样时间点为给药后的0.083、0.167、0.5、1、2、8、16、24、48和72h,每个时间点采集5尾鱼,分别采集血液、肌肉+皮,肝、肾和鳃。
[0040]
5.不同温度下水产动物中磺胺嘧啶给药方案的确定
[0041]
步骤一:从临床病鱼中分离出鮰爱德华氏菌,采用微量稀释法测定磺胺嘧啶对鮰爱德华氏菌的mic值。首先将菌种复苏,将磺胺嘧啶标准溶液倍比稀释成各种浓度。将二者按照体积比1:1加入到96孔板中,接入到96孔板中的细菌终浓度为5
×
105cfu/ml,并在15min内完成96微孔板的混菌,并设置阳性和阴性对照组。然后放入恒温培养箱中,于28℃培养24h,最小澄清孔药物浓度即mic值。
[0042]
步骤二:在18℃环境温度下,以50mg/kg bw对斑点叉尾鮰进行单次口灌给药,给药后按照“4.试验采样”进行样品采集。
[0043]
步骤三:在24℃环境温度下,以50mg/kg bw对斑点叉尾鮰进行单次口灌给药,给药后按照“4.试验采样”进行样品采集。
[0044]
步骤四:在18和24℃环境温度下,分别对斑点叉尾鮰进行单次静脉给药,给药剂量为5mg/kg bw,给药后按照“4.试验采样”进行样品采集。
[0045]
步骤五:采集的组织经过样品前处理,之后进行hplc测定,结果见表1-表2。
[0046]
样品前处理:称取水产品样品1ml或1g,再加入无水硫酸钠1.5g和氯化钠0.75g,加入提取剂纯乙腈5ml进行漩涡,4500g离心5min后取上清液。然后按照以上程序再提取一遍,合并上清。在上清液加入分散固相萃取试剂中性氧化铝粉和c18粉(1:1)150mg,漩涡之后4000g离心2min后,上清液移入另一离心管中,45℃水浴中氮气吹干,再加入体积比为15%乙腈和水的混合液进行复溶,经0.22μm的有机滤膜过滤,滤液经高效液相仪进行检测。
[0047]
高效液相检测样品中磺胺嘧啶的残留量:
[0048]
色谱柱为c18柱,100mm
×
2.1mm,粒径1.7μm;流速0.5ml/min,柱温为30℃。流动相为a为乙腈(含15%甲醇),b为水相(含0.1%甲酸)
[0049]
等度洗脱:a:b=20:80
[0050]
紫外检测器检测,检测波长为280nm。
[0051]
步骤六:评估不同温度下的药动学参数。
[0052]
采用软件3p97进行药动学参数计算,包括药时曲线下面积、吸收半衰期、消除半衰期、达峰时间、峰浓度、表观分布容积和清除率。
[0053]
步骤七:根据不同温度下药动学参数的变化,根据公式确定磺胺嘧啶的给药方案。
[0054]
所采用的公式为:
[0055][0056]
dose为药物剂量;cmin为磺胺嘧啶在斑点叉尾鮰。体内稳态浓度,根据mic确定;vd为表观分布容积;ka为吸收速率常数;k为消除速率常数;f为生物利用度;δ为给药间隔。
[0057]
生物利用度的计算公式:
[0058][0059]
aucoral为口服给药下药时曲线下面积;auciv为静脉给药下药时曲线下面积;doseiv为静注剂量;doseoral口服剂量。
[0060]
表1 18℃下磺胺嘧啶在斑点叉尾鮰血浆和组织中的浓度(μg/kg,n=5)
[0061][0062]
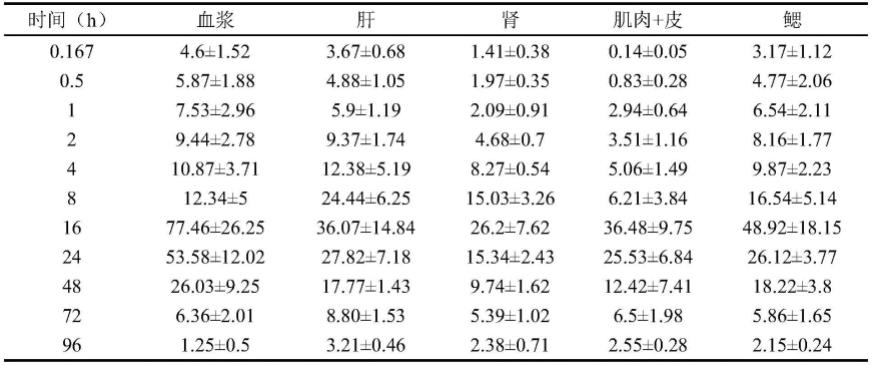
表2 24℃下磺胺嘧啶在斑点叉尾鮰血浆和组织中的浓度(μg/kg,n=5)
[0063][0064][0065]
在本发明中,磺胺嘧啶在血浆、鳃、肌肉+皮、肝和肾中的检测限分别为7.0μg/l(μg/kg)和定量限分别为10μg/l(μg/kg)。为了准确测定样品,考察了本发明方法的准确度和精密度(表3)。磺胺嘧啶在高、中和低浓度的回收率估计分别为83.5%-92.1%。日内和日间
变异系数(cv%)均小于10%。
[0066]
表3磺胺嘧啶及代谢物在斑点叉尾鮰肝、肾和肌肉+皮中准确度和精密度的考察
[0067][0068]
6.药动参数的计算(见表4)
[0069]
采用经典房室进行血浆和组织中药动学参数的拟合。
[0070]
通过赤池信息准则确定房室。
[0071]
计算药动学参数如表4:
[0072]
表4在不同温度下磺胺嘧啶在斑点叉尾鮰血浆、肾、肝、肌肉+皮和血浆中的药动学参数
[0073][0074][0075]
注:auc,药时曲线下面积;ka_hl,吸收半衰期;k_hl,消除半衰期;ka,吸收速率常数;k,消除速率常数;tmax,达峰时间;cmax,峰浓度;vd,表观分布容积;cl,系统清除率;na,无法获得。
[0076]
以上所述的实施例仅是对本发明的优选方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1