一种小柴胡胶囊糖类成分的定量指纹图谱检测方法与流程
1.本发明涉及一种中药的检测方法,具体涉及小柴胡胶囊糖类成分的定量指纹图谱检测方法。
背景技术:
2.小柴胡胶囊是由柴胡、黄芩、甘草、党参、大枣、生姜、姜半夏七味药材通过煎煮、渗漉、浓缩、干燥等工艺制备而成,可用于外感病,邪犯少阳证,症见寒热往来、胸胁苦满、食欲不振、心烦喜呕、口苦咽干等。2020版《中国药典》(一部)采用高效液相色谱法测定小柴胡胶囊中的黄芩苷含量用于其质量控制,同时采用柴胡、甘草、党参对照药材定性鉴别这三味药材。考虑到小柴胡胶囊药味较多,药典中只针对黄芩苷这一种成分进行定量检测的方法无法全面体现出制剂质量,因此需要建立指纹图谱方法进行综合性整体评价。
3.多指标成分同时定量检测在2020版《中国药典》(一部)使用很多,是公认检测中药质量的可行方法。指纹图谱是另一种检测中药质量的有效方法,采用相似度等指标总体体现指纹图谱的光谱或者色谱峰信息,就可以定量地反映中药整体质量情况,所以近年来指纹图谱技术得到了长足发展。
4.但目前文献中对于小柴胡胶囊质控方法报道较少。尤其是未见小柴胡胶囊中糖类成分定量指纹图谱方法的报道。
技术实现要素:
5.本发明的主要目的是提供一种小柴胡胶囊糖类成分的定量指纹图谱,该检测方法可以弥补现有分析方法对于药效成分质量控制的不足,从而更加全面的评价小柴胡胶囊的质量,对于控制小柴胡胶囊的质量和临床疗效有着重要作用。
6.为了实现上述目的,本发明采用以下技术方案:
7.本发明的目的之一:提供一种小柴胡胶囊糖类成分的指纹图谱检测方法,所述的小柴胡胶囊包括以下药材:柴胡、黄芩、甘草、党参、大枣、生姜、姜半夏。所述的指纹图谱检测方法,包括以下步骤:
8.(1)对照品混合溶液以及供试品溶液的制备:
9.对照品混合溶液的制备:精密称定核糖醇、果糖、蔗糖、水苏糖对照品,分别用60%乙腈溶液溶解并定容至10ml,摇匀后得到4种对照品溶液,将4种单标各移取适量于同一50ml容量瓶中,加入60%乙腈溶液精密定容,摇匀后得到混标储备液。将混标储备液稀释5倍,即得含0.6512mg/ml核糖醇、2.189mg/ml果糖、1.636mg/ml蔗糖、0.6767mg/ml水苏糖组成的对照品混合溶液。
10.供试品溶液的制备:取小柴胡胶囊内容物于研钵中,研碎,精密称定,置于25ml容量瓶中,加入60%乙腈溶液,加热超声溶解,放冷至室温后定容,摇匀,离心,取上清液,即得。
11.(2)高效液相色谱测定
12.将步骤(1)中的对照品混合溶液和供试品溶液注入液相色谱分析测定,仪器为:thermo scientific ultimate3000高效液相色谱仪;色谱条件为:色谱柱:nh2p-50 4e色谱柱(4.6
×
250mm,5μm),以水(a)-乙腈(b)作为流动相进行梯度洗脱,洗脱方式:0~10min,78%~74%b;10~28min,74%~50%b;28~33min,50%b,流量:0.6ml/min;柱温:30℃;电喷雾式检测器(cad)的雾化温度35℃,采样频率10hz,滤光片5s,幂函数1.0,进样体积为10μl。
13.(3)建立定量指纹图谱并进行质量评价
14.取10个不同批次小柴胡胶囊按照步骤(1)方法制备得到10个不同批次的供试品溶液,按照步骤(2)进行高效液相色谱分析,记录色谱图;根据10个不同批次的色谱图,以不同批次共有的色谱峰确定共有峰和定量检测指标。同时通过建立的指纹图谱相似度和测定的糖类成分对小柴胡胶囊进行质量评价。
15.优选的,步骤(2)中的雾化温度为35℃,在该雾化温度下,色谱峰分离较好,基线较为平稳,峰面积较大响应较好。
16.优选的,步骤(2)中的进样体积为10μl,在该进样体积下,峰面积较大响应较好。
17.优选的,步骤(3)中的定量检测指标为:核糖醇、果糖、蔗糖、水苏糖。在本发明的检测条件下,上述四种成分可以充分分离。
18.优选的,步骤(3)中的共有峰数量为7。
19.本发明的目的之二:提供一种小柴胡胶囊糖类成分的含量测定的方法。
20.色谱条件如下:仪器:thermo scientific ultimate3000高效液相色谱仪;色谱条件为:色谱柱:nh2p-50 4e色谱柱(4.6
×
250mm,5μm),以水(a)-乙腈(b)作为流动相进行梯度洗脱,洗脱方式:0~10min,78%~74%b;10~28min,74%~50%b;28~33min,50%b,流量:0.6ml/min;柱温:30℃;进样体积为10μl。
21.精密称定核糖醇、果糖、蔗糖、水苏糖对照品适量,分别加60%乙腈稀释成不同浓度的溶液,注入高效液相色谱进行分析,以各个化合物的浓度为横坐标,峰面积为纵坐标,绘制标准曲线,计算回归方程,计算不同批次样品中的指标成分含量。
22.本发明的目的之三:提供一种小柴胡胶囊糖类成分的定量指纹图谱在小柴胡胶囊质量控制中的应用。
23.将10个批次的小柴胡胶囊的供试品溶液的色谱图导入“中药色谱指纹图谱相似度评价系统”(国家药典委员会2012版),生成对照指纹图谱,将不同批次的小柴胡胶囊的供试品溶液导入相似度评价软件,计算相似度,对相似度低于0.9的批次,认为质量差异较大,不建议放行。
24.企业可自行设定糖类成分的含量标准,若未达到企业内控标准,也可以认为质量不合格,不建议放行。
25.本发明的有益效果为:
26.本发明首次建立了小柴胡胶囊中糖类成分的定量指纹图谱,填补了现有方法对糖类成分控制不足的空白,所述的定量指纹图谱可用于全面评价小柴胡胶囊的质量。针对小柴胡胶囊中的7种中药材,本发明筛选出4种糖类成分进行测定。其中,水苏糖是一种功能性低聚四糖,可促进益生菌生长,起到调节肠道菌群的作用,作为药效成分,对其进行检测和质量控制是十分必要的;核糖醇是d-核糖的还原产物,以游离的状态存在于柴胡的根中,是
柴胡的特征性成分,建立其指纹图谱可体现小柴胡胶囊中柴胡的部分质量信息;果糖、蔗糖在小柴胡胶囊中含量较多,因此也有必要对其进行检测。
附图说明
27.构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用来解释本发明,不构成对于本发明的不当限定。
28.图1为小柴胡胶囊样品糖类成分部分化合物的lc/q-tof-ms负离子模式下的总离子流图。
29.图2为混合对照品(a)和样品(b)的色谱。
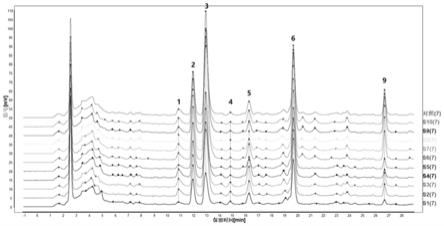
30.图3为10批小柴胡胶囊糖类成分hplc指纹图谱。
具体实施方式
31.应该指出,以下详细说明都是示例性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
32.需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作和/或它们的组合。
33.1.实验仪器与材料
34.1.1仪器
35.thermo scientific ultimate3000高效液相色谱仪,配置thermo scientific dionex corona veo电喷雾式检测器、在线脱气机、四元泵、自动进样器、柱温箱以及thermo scientific dionex chromeleon 7色谱数据系统(7.2sr5版);lc/q-tof-ms分析系统:agilent 6546四极杆-飞行时间质谱仪,带有agilent masshunter workstation data acquisition数据采集软件(version 10.1),agilent masshunter qualitative analysis数据处理软件(version 10.0);色谱柱为nh2p-504e色谱柱(4.6
×
250mm,5μm);电子天平(ab204-n,mettler toledo公司)。小型高速离心机(ab204-n,mettler toledo公司)。指纹图谱相似度评价软件为“中药色谱指纹图谱相似度评价系统”(国家药典委员会2012版)。
36.1.2试剂
37.乙腈(色谱纯,德国merck公司),水为mili-q超纯水。
38.核糖醇对照品(hplc》99%,上海融禾医药科技发展有限公司,批号:210916),果糖对照品(hplc》99%,上海融禾医药科技发展有限公司,批号:210519),蔗糖对照品(hplc》99%,上海融禾医药科技发展有限公司,批号:210620),水苏糖对照品(hplc》99%,上海融禾医药科技发展有限公司,批号:211026)。
39.2.实验条件
40.2.1对照品混合溶液的制备
41.精密称定核糖醇、果糖、蔗糖、水苏糖对照品,分别用60%乙腈溶液溶解并定容至10ml,摇匀后得到4种对照品溶液,将4种单标各移取适量于同一50ml容量瓶中,加入60%乙腈溶液精密定容,摇匀后得到混标储备液。将混标储备液稀释5倍,即得含0.6512mg/ml核糖
醇、2.189mg/ml果糖、1.636mg/ml蔗糖、0.6767mg/ml水苏糖组成的对照品混合溶液。
42.2.2供试品的制备
43.取小柴胡胶囊内容物于研钵中,研碎,精密称定,置于25ml容量瓶中,加入60%乙腈溶液,加热超声溶解,放冷至室温后定容,摇匀,离心,取上清液,即得。
44.2.3色谱条件
45.色谱条件为:色谱柱:asahipak nh2p-50 4e色谱柱(4.6
×
250mm,5μm),以水(a)-乙腈(b)作为流动相进行梯度洗脱,洗脱方式:0~10min,78%~74%b;10~28min,74%~50%b;28~33min,50%b,流量:0.6ml/min;柱温:30℃;进样体积为10μl。
46.2.4液相色谱—三重四级杆—飞行时间质谱(lc/q-tof-ms)条件
47.以上述的液相色谱分析条件作为高分辨质谱分析的色谱条件。
48.质谱条件如下:离子源:电喷雾离子源(esi);采集模式:采用负离子模式;扫描模式:ms;扫描范围:m/z 100-1500;干燥气温度320℃,干燥气流量8l/min;雾化器压力35psi;鞘气温度350℃,鞘气流量11l/min;毛细管电压3500v;喷嘴电压1000v;破碎电压175v;锥孔电压65v;八极杆射频电压峰峰值:750v。确定分析方法后,用高分辨质谱检测样品,得到样品的总离子流图。根据高分辨质谱得到的准确相对分子质量,推测并且用对照品比对确定了其中的7个色谱峰的化学成分,其编号及推断结果见表1。
49.表1小柴胡胶囊样品糖类成分部分化合物的lc/q-tof-ms分析
[0050][0051]
3.方法学验证
[0052]
3.1指纹图谱的方法学验证
[0053]
3.1.1实验方法
[0054]
指纹图谱的方法学验证主要包括进样精密度、重复性和样品稳定性考察。
[0055]
进样精密度实验:取同一份供试品溶液,连续进样6次。选择一个参照峰,分别计算各共有峰与参照峰的保留时间与峰面积的比值,得到各共有峰相对保留时间和相对峰面积的相对标准偏差(rsd)值。
[0056]
方法重复性实验:取六份平行制备的供试品溶液,分别进样分析。选择一个参照峰,分别计算各共有峰与参照峰的保留时间与峰面积的比值,得到各共有峰相对保留时间
和相对峰面积的rsd值。
[0057]
样品稳定性实验:取同一份供试品溶液,于0,4,8,12,16,24h进样分析,选择一个参照峰,分别计算各共有峰与参照峰的保留时间与峰面积的比值,得到各共有峰相对保留时间和相对峰面积的rsd值。
[0058]
3.2.2实验结果
[0059]
测定了编号为s1-s10不同批次的小柴胡胶囊,在该条件下确定了7个共有峰,由于果糖(3号峰)峰面积相对较大,且与相邻色谱峰的分离度较好,将其定为参照峰,分别计算进样精密度、重复性和样品稳定性实验项下各个色谱峰的相对保留时间的平均值和rsd值,结果见表2和3。在进样精密度和重复性条件下,各个色谱峰的相对保留时间和相对保留峰面积的rsd值均小于4%,符合指纹图谱要求。稳定性实验条件下,各个色谱峰的相对保留时间和相对保留峰面积的rsd值均小于4%,说明供试品溶液在24h内稳定。
[0060]
表2进样精密度、重复性和样品稳定性实验各峰相对保留时间结果
[0061][0062]
表3进样精密度、重复性和样品稳定性实验各峰相对峰面积结果
[0063]
[0064]
3.2含量测定方法学验证
[0065]
3.2.1实验方法
[0066]
该分析方法也适用于小柴胡胶囊中糖类成分的含量测定,方法学验证包括各含量测定成分的线性、精密度、稳定性、重复性和加样回收实验的考察。
[0067]
线性考察:取系列不同浓度的对照品混合溶液,分别进样10μl分析。以各成分测定的峰面积为纵坐标,浓度为横坐标制作标准曲线,得到线性回归方程与分析范围,分别计算其方法的检测限(lod)与定量限(loq),lod的计算方式如公式(3.1)所示,loq的计算方式如公式(3.2)所示。
[0068][0069][0070]
其中,σ为响应值的偏差,s为标准曲线的斜率。
[0071]
进样精密度实验:取同一份供试品溶液,连续进样6次,计算得到各成分峰面积以及保留时间的rsd值。
[0072]
重复性实验:取六份平行制备的供试品溶液,分别进样分析,计算得到各成分含量的rsd值。
[0073]
溶液稳定性实验:取同一份供试品溶液,于0,4,8,12,16,24h进样分析,计算得到各个成分含量的rsd值。
[0074]
加样回收实验:分别取已知含量的样品溶液9份,分为3组。设低、中、高三个浓度水平,控制对照品加入量与供试品中待测成分量之比分别在0.8:1.0,1.0:1.0,1.2:1.0左右,每种浓度平行制备3份供试品溶液进行测定。精密加入50mg样品与适量混合对照品贮备液,用60%乙腈超声加热溶解,放至恢复室温后,定容至25ml,摇匀,离心,后取上清液进样分析。
[0075]
3.2.2实验结果
[0076]
结合对照品定位与质谱结果,鉴定了2、3、5、6、7、8、9号峰分别为核糖醇、果糖、葡萄糖、蔗糖、麦芽糖、棉子糖、水苏糖。从中选取峰面积较大、峰形较优的核糖醇、果糖、蔗糖和水苏糖4个成分作为含量测定成分。
[0077]
核糖醇、果糖、蔗糖和水苏糖的回归方程、线性范围以及检测限、定量限结果见表4,4种化合物的线性拟合结果均大于0.999,符合中国药典的要求。进样精密度实验结果见表5和表6,重复性实验结果见表7,溶液稳定性实验结果见表8,其中精密度、重复性、稳定性rsd均小于3%,符合中国药典的要求,说明该方法线性良好,且供试品溶液在24h内稳定。加样回收实验结果见表9,各成分平均回收率均满足要求,且rsd值均小于4%,证明该优化得到的方法准确可靠,可用于小柴胡胶囊中糖类成分的含量测定。
[0078]
表4各成分的回归方程、相关系数和线性分析范围
[0079][0080]
表5进样精密度结果(峰面积)
[0081][0082]
表6进样精密度结果(保留时间)
[0083][0084]
表7重复性实验结果
[0085][0086]
表8溶液稳定性实验结果
[0087][0088]
表9加样回收实验结果
[0089][0090]
3.3样品含量测定结果及质控示例
[0091]
11批供试品溶液的定量成分含量测定结果见表10。各个批次小柴胡胶囊中核糖醇含量在0.8985~2.281%,果糖含量在1.815~9.018%,蔗糖含量在2.735~5.320%,水苏糖含量均低于2.430%,相差较大。其中,果糖和蔗糖含量较高。
[0092]
如果企业内控标准设定核糖醇含量不低于1%,果糖含量不低于2%,蔗糖含量不低于3%,水苏糖含量不低于0.5%,那么认为批次s4和s11不符合内控标准,不建议放行。
[0093]
表10 11批供试品溶液定量成分含量测定结果
[0095][0096]
注:“0”表示该成分含量低于定量限
[0097]
3.4指纹图谱相似度评价及质控实例
[0098]
将10批正常批次(s1-s10)小柴胡胶囊的供试品的原始图谱数据导入中药色谱指纹图谱相似度评价系统软件,并生成对照谱图,如图3所示。将各供试品与对照谱图进行比较,相似度结果见表11。由表可知,各供试品指纹图谱与对照谱图的相似度均在0.90以上,各批次的小柴胡胶囊糖类成分具有较好的质量一致性。
[0099]
表11 10批正常批次小柴胡胶囊供试品溶液指纹图谱的相似度评价结果
[0100]
[0101][0102]
取另一新批次s11的样品与对照指纹图谱比对,计算所得相似度为0.888,相似度低于0.9,认为该批次小柴胡胶囊的质量与正常批次相差较大,建议不予放行。
[0103]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1