基于激光捕获显微切割技术的空间分辨蛋白质组学方法
1.本发明属于蛋白分析技术领域,具体涉及一种基于激光捕获显微切割技术的空间分辨蛋白质组学方法。
背景技术:
2.蛋白质是细胞功能的实际执行者,近年来基于质谱的蛋白质组学技术的进步,促进了对临床组织样本的蛋白质组学研究,从而推动了对疾病的认识和治疗。然而传统的蛋白质组学方法往往将临床组织作为整体进行蛋白质提取、酶解和分析,导致细胞异质性和空间定位信息的丢失。激光捕获显微切割技术(laser capture microdissection,lcm)是一种能从组织中分离出特定细胞群体或组织学区域、同时保留空间定位信息的技术,其发展使特异性地对组织样品中某一个或一类细胞进行空间分辨蛋白质组学研究成为可能。2021年初,nature methods将空间分辨转录组技术(spatially resolved transcriptomics,srt)评为2020年度方法。然而,具有高灵敏度的空间分辨蛋白质组技术(spatially resolved proteomics,srp)的开发与应用是蛋白质组学领域的瓶颈之一。与已经发展到较高分辨率的测序技术相比,匹配空间转录组的空间蛋白质组技术平台还处在发展的伊始。
3.福尔马林固定石蜡包埋(formalin-fixed and parrffin-embedded,ffpe)是临床与科研领域保存组织样品最常用的方法,在室温下储存数十年的ffpe样品中的蛋白质信息依然可以保持稳定。将巨大的ffpe样品库与lcm技术相结合,能为空间分辨蛋白质组学研究提供宝贵的资源。然而,为了提高空间分辨率,一个lcm样品可能只包含几十到几百个细胞,对应的亚微克级别的蛋白质很容易在酶解和脱盐等前处理步骤中损失。同时,极低的样品量对色谱分离方法和质谱检测的灵敏度也提出了新的要求。
4.为了减少亚微克级蛋白质样品在前处理过程中的损失,有课题组开发了一种基于亲水性顺磁珠的one-pot蛋白质前处理方法(single-pot,solid-phase-enhanced sample-preparation,sp3),能够相对快速、高效地除去组织裂解、蛋白质提取和酶解过程中引入的去垢剂和无机盐,并减少转移过程对痕量样品造成的巨大损失。然而该方法仅适用于处理来自细胞或新鲜组织的微量蛋白质样品,在处理ffpe组织时需要5mm
×
5mm
×
5μm的起始样品量。过大的组织取样面积会急剧降低空间分辨率,使组织中来自不同的细胞信息被同质化,难以针对性地分析组织中珍贵的细胞类型。此外,ffpe组织制备中的甲醛固定及石蜡包埋处理会导致组织细胞中的蛋白质发生广泛的分子交联,限制了蛋白质的提取效率,损害了免疫反应活性,还会导致质谱对蛋白质的鉴定能力大幅下降。因此,要想通过lcm技术和质谱技术从痕量ffpe样本中选取高分辨率的空间分辨蛋白质组学信息,就需要针对性地开发适用于痕量ffpe样本的空间分辨蛋白质组学前处理方法和质谱分析方法。
技术实现要素:
5.针对现有技术中的不足,本发明的目的是提供一种适用于lcm产生的痕量组织样
品的蛋白质组学前处理方法:即采用激光捕获显微切割的磁珠法痕量分析(lcm-magnetic trace analysis,lcm-mta)及质谱分析方法,能够显著降低单个样本所需的起始组织面积,提升蛋白质提取效率和质谱鉴定能力。
6.为达到上述目的,本发明的解决方案是:
7.一种基于激光捕获显微切割技术的空间分辨蛋白质组学方法,其包括如下步骤:
8.(1)、将组织切片置于激光捕获显微切割(lcm)仪的载物台上,选取目标组织后,进行切割并收集至显微切割专用管的管盖上;
9.(2)、向步骤(1)的管盖上加入裂解液,并完全覆盖目标组织,在50-70℃水浴下原位孵育裂解1.5-2.5h,之后将含蛋白质的裂解液离心收集至管底;
10.(3)、向步骤(2)裂解得到的蛋白质溶液中加入终浓度为5-20mmol/l的还原剂和终浓度为10-100mmol/l的烷基化试剂进行一步反应或顺次反应,蛋白质的还原烷基化的反应体系中,烷基化试剂终浓度不低于还原剂终浓度的2倍,之后冷却至室温;
11.(4)、向步骤(3)中加入0.5-1.5μl、30-70μg/μl的磁珠,再加入乙醇,之后在室温下震荡混匀,于磁力架上静置后去除上清液,用不同浓度的乙醇冲洗磁珠;
12.(5)、在步骤(4)冲洗后的磁珠中加入缓冲液,在水浴中超声,加入终浓度为1-100ng/μl的蛋白水解酶,在恒温振荡仪上300-1500rpm边震荡边酶解蛋白质溶液;
13.(6)、步骤(5)酶解4-24h的样品于磁力架上静置后,收集上清液并加入甲酸溶液至终浓度0.1-1wt%进行酸化终止酶解反应;
14.(7)、将步骤(6)的肽段溶液进行色谱分离和质谱检测。
15.作为本发明优选地,步骤(1)中,组织切片的厚度为3-20μm。
16.作为本发明优选地,步骤(1)中,组织切片选自福尔马林固定石蜡包埋(ffpe)组织切片、组织芯片或新鲜组织的冰冻切片中的一种以上。
17.作为本发明优选地,步骤(2)中,水浴的温度为60℃,原位孵育裂解的时间为2h。
18.作为本发明优选地,步骤(2)中,裂解液包括十二烷基硫酸钠(sodium dodecyl sulfate,sds)、聚乙二醇辛基苯基醚(triton x-100)、吐温20(tween 20)、乙基苯基聚乙二醇(np-40)、乙二胺四乙酸(edta)、氯化钠(nacl)、4-羟乙基哌嗪乙磺酸(hepes)、甘油(glycerol)、蛋白酶抑制剂(complete protease inhibitor)和二硫苏糖醇(dtt)。
19.作为本发明优选地,步骤(2)中,裂解液需覆盖痕量组织,推荐加入的裂解液需铺满黏附或承装痕量组织的管盖等容器底部,以保障完全裂解。
20.作为本发明优选地,步骤(3)中,还原剂选自二硫苏糖醇(dtt)或三(2-羧乙基)膦(tcep)中的一种以上。
21.作为本发明优选地,步骤(3)中,烷基化试剂选自碘乙酰胺(iaa或iam,iodoacetamide)、氯乙酰氨(caa或clam,chloroacetamide)、碘乙酸或n-乙基马来酰亚胺中的一种以上。
22.作为本发明优选地,步骤(3)中,裂解液体系中,加入终浓度10mmol/l还原剂tcep和终浓度40mmol/l烷基化试剂caa,一步法进行蛋白质的还原烷基化反应。
23.作为本发明优选地,步骤(3)中,反应的温度为80-97℃,反应的时间为1-10min。
24.作为本发明优选地,步骤(3)中,反应的温度为95℃,反应的时间为5min。
25.作为本发明优选地,步骤(4)中,磁珠的工作浓度不低于0.5μg/μl;磁珠和步骤(3)
的蛋白质溶液中蛋白质的质量比不低于10:1。
26.作为本发明优选地,步骤(4)中,不同浓度的乙醇的含量为50-99.99wt%。
27.作为本发明优选地,步骤(5)中,缓冲液可以选择与碳酸氢铵相当缓冲能力的羟乙基哌嗪乙硫磺酸(hepes)或四乙基硼氢化铵(teab)等。
28.作为本发明优选地,步骤(5)中,蛋白水解酶可以为与胰蛋白酶、胞内蛋白酶赖氨酸-c(lys-c蛋白酶),或葡萄球菌v-8蛋白酶(glu-c蛋白酶)、胞内蛋白酶赖氨酸-n(lys-n蛋白酶)、天冬氨酸蛋白酶(asp-n蛋白酶)、胰凝乳蛋白酶等蛋白水解酶。
29.作为本发明优选地,步骤(5)中,蛋白水解酶的终浓度为25ng/μl,单次加入2.5μl、0.1μg/μl的胰蛋白酶。
30.作为本发明优选地,步骤(5)中,蛋白水解酶还可分两次加入,蛋白水解酶于最适温度下在恒温振荡仪上300-1500rpm边震荡边酶解蛋白质溶液,第二次加蛋白质水解酶需间隔2-6h。
31.作为本发明优选地,步骤(7)中,色谱分离的仪器为纳升级液相色谱仪,质谱检测的仪器为捕集离子淌度飞行时间质谱,质谱采集模式选自数据依赖性采集-平行累积串行碎裂或数据非依赖性采集-平行累积串行碎裂中的一种以上。
32.由于采用上述方案,本发明的有益效果是:
33.第一、本发明的空间分辨蛋白质组学方法能将起始组织切片样品量下降至0.005mm2×
8μm(即约70μm
×
70μm
×
8μm,大约15个细胞),能够显著降低单个样本所需的起始组织量,显著提升蛋白质提取效率和质谱鉴定能力,可以与现有主流空间分辨转录组技术的分辨率对接。从而将引领该领域的科学创新,完成“弯道超车”,并将获得巨大的经济效益。
34.第二、本发明的原位水浴蛋白质前处理方案相比现有前处理技术,能显著提高痕量ffpe组织中蛋白质的回收能力。另外,本发明中的前处理流程可以完全通过自动化工作站实现,降低人为操作对痕量样品处理引入的误差,从而减少处理大批量样品时所需的人力和时间成本。
35.第三、与过滤辅助样品制备(filter aided sample preparation,fasp)、细胞外基质(extracellular matrix,ecm)富集等蛋白质组学前处理方法相比,本发明对ecm组分的回收具有优势,可省去繁琐的ecm蛋白或膜蛋白的富集步骤,真实原位地还原包含空间定位信息的全蛋白质组数据。
附图说明
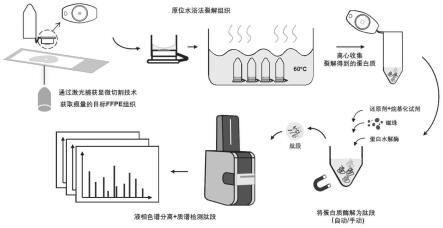
36.图1为本发明的基于激光捕获显微切割技术的空间分辨蛋白质组学方法的流程图。
37.图2为本发明实施例1中通过激光捕获显微切割经苏木精-伊红(h-e)染色后结直肠癌组织ffpe切片示意图。a)切割前的结直肠癌组织;b)切割后的结直肠癌组织;c)切割下来的面积约0.3mm2的结直肠癌肿瘤实质组织。
38.图3为本发明中蛋白质提取条件的过程示意图。a)本发明所用裂解液与常规的4wt%的sds裂解液对蛋白质提取效果的比较;b)不同时间的水浴对ffpe组织裂解效果的影响;c)本发明所用的原位水浴法和常规水浴法对蛋白质提取效果的比较;a)和c)的显著性
检验方法为双尾t-检验,*:p值《0.05;**:p值《0.01;***:p值《0.001。
39.图4为本发明中激光捕获显微切割不同面积的痕量组织示意图及定量蛋白质数目。a)经激光捕获显微切割得到的不同面积的痕量组织在管盖上的实物图;b)激光捕获显微切割得到的痕量组织,通过lcm-mta法制备的肽段样品,取1/2肽段样品,上样至液质联用质谱仪,经质谱仪鉴定得到的含定量信息的蛋白质数目及对应痕量组织面积的示意图。
40.图5为本发明中结直肠癌组织的肿瘤实质组(ct-p)和间质组(ct-s)的定量蛋白质主成分分析图。
41.图6为本发明中结直肠癌组织的肿瘤实质组(ct-p)和间质组(ct-s)的定量蛋白质的功能富集图。
42.图7为本发明中lcm-mta法、fasp法和ecm富集法三种前处理方法对ecm蛋白质的富集能力示意图。a)有定量信息的ecm蛋白质数量占定量总蛋白质的比例;b)三种方法富集到的ecm蛋白质的大类分类结果;c)三种方法富集到的ecm蛋白质的小类分类结果。
43.图8为本发明的实施例4中应用于不同厚度切片、不同染色方式、不同显微切割仪器及不同质谱采集模式的结果图。a)从不同厚度的切片中获得定量蛋白质数目的比较;b)从不同染色方式染色的切片中获得定量蛋白质数目的比较;c)不同染色方式获得定量蛋白质的韦恩图;d)从不同显微切割仪器及不同质谱采集模式中对同一染色方式染色的切片分析获得定量蛋白质数目的比较;显著性检验方法为双尾t-检验,ns:p值≥0.05;*:p值《0.05;**:p值《0.01。
44.图9为本发明的实施例4中应用于用h-e或ihc染色的同一结直肠癌ffpe组织切片的肿瘤实质组(ct-p)、肿瘤间质组(ct-s)和三级淋巴结构(ct-tls)的定量蛋白质主成分分析图。
45.图10为本发明的实施例4中h-e或ihc染色后的lcm-mta处理、fasp处理和ecm富集处理三种方法对ecm蛋白质的富集能力示意图。a)有定量信息的ecm蛋白质数量占定量总蛋白质的比例;b)三种方法富集到的ecm蛋白质的大类分类结果;c)三种方法富集到的ecm蛋白质的小类分类结果。
具体实施方式
46.本发明提供了一种基于激光捕获显微切割技术的空间分辨蛋白质组学方法。具体地,亚微克级别的蛋白质的前处理和液相分离-质谱检测条件都需要针对性地优化。
47.如图1所示,本发明的基于激光捕获显微切割技术的空间分辨蛋白质组学方法包括如下步骤:
48.(1)、通过lcm技术从组织切片上切割分离痕量面积的目标组织或细胞:
49.将组织切片使用h-e染色法进行染色后,置于激光捕获显微切割仪lcm的载物台上,选取目标组织后,进行切割并收集至显微切割专用管的管盖上;
50.(2)、建立了一种原位水浴蛋白质提取方法,针对性地解决lcm切割的痕量组织样品难收集和难裂解:
51.向步骤(1)的管盖上加入裂解液,并完全覆盖目标组织,在50-70℃水浴下原位孵育裂解1.5-2.5h,之后将含蛋白质的裂解液离心收集至管底;
52.(3)、利用亲水性磁珠对提取的蛋白质进行裂解液置换、还原烷基化及酶解:
53.蛋白质的还原烷基化:向步骤(2)裂解得到的蛋白质溶液中加入终浓度为5-20mmol/l的还原剂和终浓度为10-100mmol/l的烷基化试剂进行一步反应或顺次反应,蛋白质的还原烷基化的反应体系中,烷基化试剂终浓度不低于还原剂终浓度的2倍,之后冷却至室温;
54.(4)、蛋白质的溶液置换:向步骤(3)中加入0.5-1.5μl、30-70μg/μl的磁珠,再加入乙醇至终浓度为50wt%,之后在室温下以1,000rpm震荡混匀8min,于磁力架上静置后去除上清液,用不同浓度的乙醇冲洗磁珠;
55.(5)、蛋白质的酶解:在步骤(4)冲洗后的磁珠中加入7.5μl、100mmol/l的缓冲液,在水浴中超声,再加入终浓度为1-100ng/μl的蛋白水解酶,并在37℃下以300-1500rpm的速度边震荡边酶解4-24h;
56.(6)、步骤(5)酶解后的样品于磁力架上静置后,收集上清液并加入1μl、0.1-1wt%甲酸溶液进行酸化;
57.(7)、将酶解后的肽段送入色谱分离和液质联用质谱仪检测并进行数据库检索分析。
58.其中,在步骤(1)中,组织切片的厚度为3-20μm。优选地,使用的组织切片的厚度为5μm和8μm,这种切片厚度既能在显微镜下进行病理结构观察,又能在同样的切割面积中获得更多的组织或细胞,利于后续蛋白质的提取和质谱检测,但这并非对本发明适用组织切片厚度的限制,本发明普适于常规或稍厚的病理切片。激光捕获显微切割仪可以选用mmi cellcut、zeiss palm microbeam、leica lmd6、leica lmd7及其他相似工作原理的激光捕获显微切割仪。
59.尽管本发明针对性地解决了组织样品h-e染色切片的蛋白质组学前处理难题,但本发明的适用范围并不仅限于ffpe组织样品的h-e染色切片,同样适用于组织芯片样本、不经染色的ffpe组织切片、经免疫组织化学(immunohistochemistry,ihc)等其他染色方式染色的ffpe组织切片、以及染色或不染色的新鲜组织制备的冰冻切片等临床病理样本。
60.在步骤(2)中,水浴的温度优选为60℃,原位孵育裂解的时间优选为2h。
61.在步骤(2)中,裂解液包括1wt%的sds、1wt%的triton x-100、1wt%的tween 20、1wt%的np-40、5mmol/l的edta、50mmol/l的nacl、50mmol/l的hepes、1%(vol/vol)的glycerol、1
×
complete protease inhibitor和5mmol/l的dtt。
62.在步骤(3)中,还原剂选自dtt或tcep中的一种以上;烷基化试剂选自iaa、caa、碘乙酸或n-乙基马来酰亚胺中的一种以上。
63.优选在反应体系中一步法进行蛋白质的还原烷基化,反应体系中还原剂终浓度为10mmol/l tcep,烷基化试剂终浓度为40mmol/l caa。
64.在步骤(3)中,反应的温度可以为80-97℃,优选为95℃;反应的时间可以为1-10min,优选为5min。
65.在步骤(4)中,磁珠的工作浓度不低于0.5μg/μl。
66.在步骤(4)中,磁珠和步骤(3)的蛋白质溶液中蛋白质的质量比不低于10:1。
67.在步骤(4)中,不同浓度的乙醇的含量可以为50-99.99wt%。
68.在步骤(5)中,缓冲液可以包括但不限于碳酸氢铵、hepes或teab等。
69.在步骤(5)中,蛋白水解酶可以包括但不限于胰蛋白酶、lys-c蛋白酶、glu-c蛋白
酶、lys-n蛋白酶、asp-n蛋白酶、胰凝乳蛋白酶等其他蛋白水解酶,进行单独或顺序消化蛋白质,从而产出肽段混合物。
70.在步骤(5)中,蛋白水解酶的终浓度优选为25ng/μl,单次加入2.5μl、0.1μg/μl胰蛋白酶。
71.在本发明的一个优选方案中,利用自动化液体工作站,可以全自动地完成蛋白质的裂解液置换、还原烷基化及酶解步骤,并提升前处理通量至一批96个lcm组织样品。自动化程序启动前应准备好足量0.5mol/l的caa、0.5mol/l的tcep、50μg/μl磁珠、100mmol/l的碳酸氢铵、0.1μg/μl的胰蛋白酶和0.1wt%甲酸,自动化液体工作站应配有加热震荡模块和适配96孔板的磁力架。
72.在步骤(7)中,本发明采用纳升级液相色谱仪nanoelute进行色谱分离,采用捕集离子淌度飞行时间质谱timstof进行质谱检测,质谱采集模式为数据依赖性采集-平行累积串行碎裂(data dependent acquisition-parallel accumulation serial fragmentation,dda-pasef),但本发明并不限制于使用该采集模式。作为优选方案,在本发明的实施例4中,采用数据非依赖性采集-平行累积串行碎裂(data independent acquisition-parallel accumulation serial fragmentation,dia-pasef)可以获得更好的数据质量和同等面积的组织下近似乃至更高的定性及定量蛋白质数量。
73.以下将结合实施例对本发明的实施方案进行详细描述。然而,应当理解的是,以下实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中除注明的试剂和仪器,其余所用试剂和仪器的类型、型号、品质、性质或功能相同或相似的材料均可以用于实施本发明。下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
74.以下实施例中所用主要仪器如表1所示:
75.表1
[0076][0077]
实施例1结直肠癌ffpe组织lcm
[0078]
(1)、制片
[0079]
结直肠癌ffpe组织切片与制片按照常规方法进行,切片厚度为5μm,载玻片使用lcm专用覆膜玻片。使用h-e染色法对该切片进行染色。
[0080]
(2)、挑选目标组织与激光捕获显微切割
[0081]
将染色后的结直肠癌ffpe组织切片置于激光捕获显微切割仪的载物台上,于镜下
找到肿瘤实质组织,手动选取面积约0.3mm2的结直肠癌ffpe目标组织后,机器自动切割并收集结直肠癌ffpe目标组织到配套收集管的管盖上。切割前后进行拍照记录,明确切割位置。
[0082]
如图2所示,所用的结直肠癌ffpe组织切片切割前如图2中a)所示,切割后如图2中b)所示,显微切割特异切取的0.3mm2结直肠癌肿瘤实质的痕量组织如图2中c)所示。
[0083]
实施例2痕量ffpe组织的蛋白质提取与酶解
[0084]
(1)、组织裂解和蛋白质提取
[0085]
向0.5ml规格的lcm专用收集管的管盖上加入34μl裂解液,使黏附在管盖上的痕量ffpe组织被完全覆盖。盖紧收集管,将收集管倒置没入60℃水浴中原位孵育裂解2h,裂解完成后待冷却至室温,以5,000
×
g离心30s,将含有组织蛋白质的溶液离心收集到管底。
[0086]
其中,裂解液包括1wt%的sds、1wt%的triton x-100、1wt%的tween 20、1wt%的np-40、5mmol/l的edta、50mmol/l的nacl、50mmol/l的hepes、1%(vol/vol)的glycerol、1
×
complete protease inhibitor和5mmol/l的dtt。
[0087]
(2)、蛋白质的还原烷基化
[0088]
向步骤(1)中裂解得到的蛋白质溶液中加入2.96μl、0.5mol/l的caa和0.75μl、0.5mol/l的tcep,使caa终浓度为40mmol/l,tcep终浓度为10mmol/l。在95℃反应5min,冷却至室温。
[0089]
(3)、蛋白质的溶液置换
[0090]
按照磁珠最小工作浓度为0.5μg/μl,磁珠与蛋白质的质量比不低于10:1的比例,向还原烷基化后的蛋白质样品中加入1μl、50μg/μl的磁珠,再加入无水乙醇至乙醇终浓度为50wt%。将样品在24℃以1,000rpm震荡混匀8min,再转移至磁力架上,静置2min后去除上清液。向磁珠沉淀中加入200μl、80wt%的乙醇冲洗2次,再加入180μl无水乙醇冲洗一次。
[0091]
(4)、蛋白质的酶解
[0092]
向步骤(3)获得的磁珠中加入7.5μl、100mmol/l的碳酸氢铵,在水浴中超声5min,再加入2.5μl、0.1μg/μl的胰蛋白酶,使胰蛋白酶终浓度为25ng/μl。在37℃下以1,000rpm的速度边震荡边酶解4h。
[0093]
(5)、肽段的收集
[0094]
将步骤(4)中完成酶解的样品管放置在磁力架上,静置2min后转移上清液至新的样品管中。向上清液中加入1μl、0.1wt%甲酸溶液对肽段样品进行酸化。
[0095]
实施例3肽段的质谱鉴定及数据处理
[0096]
取4μl实施例2中获得的肽段溶液进行蛋白质组学分析。具体地,采用纳升级液相色谱仪nanoelute进行色谱分离,采用捕集离子淌度飞行时间质谱timstof进行质谱检测。使用自灌注的色谱柱,柱长为25cm,内径为75μm,填料为1.9μm的reprosilpur c18 beads(dr.maisch gmbh,germang)。流动相a为0.1wt%甲酸溶于纯水,流动相b为0.1wt%甲酸溶于纯乙腈。液相色谱分离梯度如表2所示。
[0097]
表2
[0098]
[0099][0100]
使用timstof的dda-pasef模式采集数据时,每个采集循环包括一次ms1扫描和8次pasef ms/ms扫描;离子积累时间为100ms,离子迁移率范围为1/k0=1.35vs
·
cm-2-0.75vs
·
cm-2
;m/z《700的前体离子在ms/ms分析中采取2th的隔离窗口,m/z》700的前体离子采取3th的隔离窗口。随着迁移率的增加,碰撞能量呈线性下降,在1/k0=1.6vs
·
cm-2
时为59ev,在1/k0=0.6vs
·
cm-2
时为20ev。单电荷前体离子通过一个多边形过滤器(polygon filter,otof control,bruker daltonik gmbh)被排除。
[0101]
质谱采集的原始数据及蛋白质定性定量分析采用peaks online进行。所用数据库为swissprot_human database(数据截止至2020年5月25日)。检索条件:胰酶酶切;允许最多3个漏切位点;固定修饰为半胱氨酸的脲基甲基化;可变修饰为蛋氨酸的氧化和肽段n-端的乙酰化;denovo匹配时前体离子的容错度为15ppm,碎片离子的容错度为0.05da;假阳性率(false discovery rate,fdr)小于1%。
[0102]
此外,原位水浴法还进行了组织裂解液、水浴裂解时间和水浴方式的测试:
[0103]
组织裂解液测试:
[0104]
向0.5ml规格的lcm专用收集管的管盖上分别加入34μl本发明使用裂解液或对照的4wt%sds裂解液,使黏附在管盖上的痕量ffpe组织被完全覆盖。室温静置孵育30min后,以5,000
×
g离心30s,将管盖上的组织和裂解液一起收集至管底,在60℃水浴中孵育裂解2h。
[0105]
水浴裂解时间测试:
[0106]
向0.5ml规格的lcm专用收集管的管盖上加入34μl裂解液,使黏附在管盖上的痕量ffpe组织被完全覆盖。室温静置孵育30min后,以5,000
×
g离心30s,将管盖上的组织和裂解液一起收集至管底,在60℃水浴中分别孵育裂解30min、60min、90min和120min。
[0107]
水浴方式测试:
[0108]
向0.5ml规格的lcm专用收集管的管盖上加入34μl裂解液,使黏附在管盖上的痕量ffpe组织被完全覆盖。对照组在室温静置孵育30min后,以5,000
×
g离心30s,将管盖上的组织和裂解液一起收集至管底,在60℃水浴中孵育裂解2h。原位水浴组则直接将收集管倒置没入60℃水浴中原位孵育裂解2h,裂解完成后待冷却至室温,以5,000
×
g离心30s,将含有
组织蛋白质的溶液收集到管底。
[0109]
结果分析:
[0110]
首先,选用厚度为8μm的人胎盘ffpe组织切片进行激光捕获显微切割技术的磁珠法痕量分析的前处理方法,比较了不同前处理方法对体积相同的组织样品最终鉴定到的肽段和蛋白质数量的影响,如图3所示。图3中a)为本发明所用裂解液与常规的4wt%sds裂解液对蛋白质提取效果的比较,测试的组织切片量均为约1mm2×
8μm,左图为色氨酸定量法检测得到的肽段浓度(μg/μl),右图为质谱检测得到的定量蛋白质数量;图3中b)为不同时间的水浴对ffpe组织裂解效果的影响,测试的组织切片量均为约7mm2×
5μm,可以观察到120min时溶液内的组织沉淀显著减少;图3中c)为本发明所用的原位水浴法和常规水浴法对蛋白质提取效果的比较,图为质谱检测得到的定量蛋白质数量,测试的组织切片量均为约0.1mm2×
8μm。不同组的样品均来自同一人类胎盘组织ffpe切片。
[0111]
相比蛋白质组学前处理中常规使用的4wt%sds裂解液,本发明所用裂解液在处理同样体积的组织后能提取到显著增多的蛋白质(图3中a)所示);使用本发明所用裂解液在60℃水浴中裂解同样体积的组织30min、60min、90min、120min后,通过观察浑浊度可以发现,在水浴120min时裂解液中的组织沉淀显著减少,溶液趋于澄清(图3中b)所示);使用同样的裂解液、水浴温度和时间,与在溶液内裂解组织的常规水浴法相比,使用本发明的原位水浴法处理同样体积的组织能提取到显著增多的蛋白质(图3中c)所示)。
[0112]
其次,发明人切割了不同面积的厚度为8μm的人胎盘ffpe组织(图4中a)所示),按照本发明的方法进行样品前处理和液相色谱-质谱检测,获得含有定量信息的蛋白质数量及对应痕量组织面积情况如图4中b)所示。结果显示,该发明获得的定量蛋白质数目与样品面积呈良好的线性相关(r2≈0.95),且在样品面积低至0.005mm2时仍可获得超过500种包含定量信息的蛋白质数据,可以与现有主流空间分辨转录组技术的分辨率对接。
[0113]
为了进一步证明lcm技术应用在疾病相关的蛋白质组学研究中的必要性,选用厚度为5μm的人结直肠癌ffpe组织切片,通过lcm技术分别切割了三组病人面积约为0.3mm2的肿瘤实质组织或肿瘤组织周围的间质,按照本发明的方法进行前处理和质谱检测。比较肿瘤实质组织和间质组织的质谱结果可以发现,来源于同一ffpe组织切片的不同组织类型在蛋白质水平上呈现出显著差异(图5),即来源于同一ffpe组织切片的不同组织类型在主成分1(34.3%)和主成分2(33%)上均能分开,说明了基于lcm技术的痕量组织样品的蛋白质组学检测技术发展的必要性。
[0114]
此外,对上述lcm-结直肠癌ffpe组织切片的蛋白质组学数据进行功能富集分析后,发现细胞外基质这一类回收难度大的蛋白质在结果中存在显著的富集(图6),仅展示显著性最好的前20项。与蛋白质组学前处理中常用的fasp酶解方法相比,lcm-mta处理能回收到比例更高的ecm蛋白质;与alexandra naba等人于2014年发表在bmc cancer上针对ecm蛋白质进行富集后的结果相比,ecm占定量总蛋白的比例相同(图7中a)所示)。对lcm-mta处理富集到的ecm蛋白质进行分类可以看出,与fasp或ecm富集法相比,lcm-mta对ecm蛋白质的富集是广泛、无偏的(图7中b)所示和图7中c)所示)。
[0115]
实施例4
[0116]
(1)、制片
[0117]
结直肠癌ffpe组织切片与制片按照常规方法进行,切片厚度为3μm及4μm两种,载
玻片使用lcm专用覆膜玻片。使用h-e染色法或ihc方法对两种厚度切片分别进行染色。
[0118]
(2)、挑选目标组织与激光捕获显微切割
[0119]
将染色后的结直肠癌ffpe组织切片置于leica lmd7激光捕获显微切割仪的载物台上,于镜下分别找到肿瘤间质组织、实质组织、三级淋巴结构(tertitary lymphoid structures,tls),手动选取面积约0.3mm2的结直肠癌ffpe目标组织后,机器自动切割并通过重力收集结直肠癌ffpe目标组织到商品化的96孔板中。切割前后进行拍照记录,明确切割位置。
[0120]
(3)、组织裂解和蛋白质提取
[0121]
将收集了切割下的目标组织的96孔板以2,000
×
g离心10min,确保目标组织均处于孔板底部。加入20μl裂解液,使96孔板底部的痕量ffpe组织被完全覆盖。用热封膜封板后,将96孔板放入pcr仪中孵育裂解2h,裂解完成后待冷却至室温,以2,000
×
g离心1min,将含有组织蛋白质的溶液离心收集到管底。
[0122]
其中,裂解液包括1wt%的sds、1wt%的triton x-100、1wt%的tween 20、1wt%的np-40、5mmol/l的edta、50mmol/l的nacl、50mmol/l的hepes、1%(vol/vol)的glycerol、1
×
complete protease inhibitor和5mmol/l的dtt。
[0123]
(4)、蛋白质的上机前处理
[0124]
显微切割收集的组织中的蛋白质经裂解后,还原烷基化、溶液置换、酶解、肽段收集过程均与实施例2的步骤(2)至步骤(5)一致。
[0125]
(5)、肽段的质谱鉴定及数据处理
[0126]
取步骤(4)中获得的肽段溶液中一致肽段含量的样品进行蛋白质组学分析。具体地,采用纳升级液相色谱仪nanoelute进行色谱分离,采用捕集离子淌度飞行时间质谱timstof进行质谱检测。色谱柱、流动相及液相分离梯度与实施例3中一致。使用timstof的dia-pasef模式采集数据,每个采集循环包括一次ms1扫描和8次pasef ms/ms扫描;离子积累时间为100ms,离子迁移率范围为1/k0=1.35vs
·
cm-2-0.75vs
·
cm-2
。随着迁移率的增加,碰撞能量呈线性下降,在1/k0=1.6vs
·
cm-2
时为59ev,在1/k0=0.6vs
·
cm-2
时为20ev。单电荷前体离子通过一个多边形过滤器(polygon filter,otof control,bruker daltonik gmbh)被排除。在扫描范围400-1200m/z间一共设定了64个范围为26th的数据非依赖前体离子隔离窗口,相邻隔离窗口间有1th的重叠。
[0127]
质谱采集的原始数据及蛋白质定性定量分析采用spectronaut(v15.0)进行。所用数据库为swissprot_human database(数据截止至2020年5月25日)。检索条件:胰酶酶切;允许最多3个漏切位点;固定修饰为半胱氨酸的脲基甲基化;可变修饰为蛋氨酸的氧化和肽段n-端的乙酰化;denovo匹配时前体离子的容错度为15ppm,碎片离子的容错度为0.05da;fdr小于1%。
[0128]
结果分析:
[0129]
本实施例使用了与前述实施例不同品牌、不同收集原理的激光捕获显微切割仪,对不同厚度、不同染色方式的结直肠癌ffpe组织切片进行了显微切割、蛋白质组学前处理,并在lc-ms/ms采集中使用了与前述实施例不同的数据采集模式,对结果进行了分析。在上样肽段量相同的前提下,ffpe的组织切片厚度对鉴定到含有定量信息的蛋白质数目没有显著影响(图8中a)所示),但不同的染色方式会导致鉴定结果出现显著差异,其中ihc染色相
比h-e染色能够鉴定到更多含有定量信息的蛋白质(图8中b)所示),但不同染色方式对鉴定到的蛋白质类别基本不产生影响(图8中c)所示),说明不同厚度、不同染色方式的组织切片均适用于本发明。对比上述本发明中的实施例结果发现,在上样肽段量相同的前提下,来自同一类型组织、使用同一切片染色方式的ffpe组织样品,即便使用不同的激光捕获显微切割仪器切割、使用不同的lc-ms/ms数据采集模式进行检测,鉴定到含有定量信息的蛋白质数目也没有显著差异(图8中d)所示),说明了前述发明应用的普适性。进一步对不同染色方式的蛋白质组学结果进行分析,可见来自两种染色方式染色的同一ffpe组织切片的不同组织类型在蛋白质鉴定及定量水平上均呈现出显著差异(图9),说明了基于本发明技术对不同组织细胞类型的精准切割,从而对所获痕量组织样品进行空间分辨蛋白质组检测的必要性,且本实施例所用的拓展方法不影响前述发明的效果。针对细胞外基质这一类回收难度大的蛋白质,对上述两种染色方式染色的切片的蛋白质组学数据进行分析(图10),发现与蛋白质组学前处理中常用的fasp酶解方法相比,lcm-mta处理能回收到比例更高的ecm蛋白质;与alexandra naba等人于2014年发表在bmc cancer上针对ecm蛋白质进行富集后的结果相比,ecm占定量总蛋白的比例相似(图10中a)所示)。对lcm-mta处理富集到的ecm蛋白质进行分类可以看出,与fasp或ecm富集法相比,lcm-mta对ecm蛋白质的富集是广泛、无偏的,且不同的组织切片染色方法不会影响这一富集效果(图10中b)所示和图10中c)所示),进一步证明了前述发明可以对细胞外基质这一类回收难度大的蛋白质进行富集鉴定,且本实施例所用的拓展方法不影响前述发明的效果。
[0130]
上述对实施例的描述是为了便于该技术领域的普通技术人员能理解和使用本发明。熟悉本领域技术人员显然可以容易的对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中,而不必经过创造性的劳动。因此,本发明不限于上述实施例。本领域技术人员根据本发明的原理,不脱离本发明的范畴所做出的改进和修改都应该在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1