使用医疗设备的组织接触感测的制作方法
相关申请的交叉引用
本申请要求于2015年2月20日递交的临时专利号62/118,897的优先权,通过引用的方式将其整体并入本文。
本公开涉及医疗设备以及制造医疗设备的方法。更具体地,本公开涉及组织诊断和/或消融。
背景技术:
以开发了多种体内医疗设备用于医疗用途例如血管内用途。这些设备中的一些包括导线、导管等等。这些设备由多种不同的制造方法中的任意一种制造并且可以根据多种方法中的任意一种来使用。在已知的医疗设备和方法中,每种都具有特定的优点和缺点。日益需要提供一种可替换的医疗设备以及可替换的医疗设备制造和使用方法。
技术实现要素:
本公开提供了医疗设备的设计、材料、制造方法和使用替换。公开了一种示例性电生理医疗设备。该医疗设备包括:
包括远端部的导管轴,其中,远端部包括具有多个标测电极的感测组件;
其中,多个标测电极包括至少一个电流承载电极、第一感测电极和第二感测电极;
其中,第一感测电极与电流承载电极隔开第一距离;
其中,第二感测电极与电流承载电极隔开第二距离;
其中,第一距离与第二距离不同;以及
耦接到多个标测电极的控制器;
其中,控制器能够至少部分地基于第一距离和第二距离来计算参数。
可替换地或另外,参数指示医疗设备与组织的接近度。
可替换地或另外,计算参数包括感测在第一电极与一个或多个回路电极之间的第一电压电位,以及感测在第二电极与一个或多个回路电极之间的第二电压电位。
可替换地或另外,计算参数包括求解至少一个线性方程,以及其中,至少一个线性方程包括第一距离、第二距离、第一电压和第二电压。
可替换地或另外,感测组件包括多个齿条,以及其中,多个电极设置在多个齿条上。
可替换地或另外,感测组件包括多个齿条,以及其中,多个齿条包括面朝外的表面,以及其中,多个电极设置在面朝外的表面上。
可替换地或另外,感测组件包括多个齿条,以及其中,多个电极设置在篮形物中。
可替换地或另外,多个电极中的每个被设计为在感测配置和电流承载配置中顺序地和/或同时地操作。
可替换地或另外,进一步包括在显示器上显示参数。
可替换地或另外,显示参数包括显示与参数相对应的置信值。
可替换地或另外,在显示器上显示参数进一步包括显示解剖外壳和/或电解剖图,其指示一个或多个电极与组织的接近度。
另一种用于感测组织接近度的示例性系统包括:
包括远端部的导管轴,其中,远端部包括具有多个电极的感测组件;
其中,多个电极包括电流承载电极、第一感测电极和第二感测电极;
其中,第一感测电极定位为与电流承载电极相距第一距离;
其中,第二感测电极定位为与电流承载电极相距第二距离;
其中,第一距离与第二距离不同;
处理器,其中,处理器被设计为:
同时地:
(a)至少部分地基于第一距离和第二距离检测第一参数,以及
(b)检测在多个电极中的至少一个上的阻抗增加。
可替换地或另外,其中,通过阻抗的至少100%的改变来定义阻抗增加。
可替换地或另外,其中,同时地检测阻抗增加指示多个电极中的至少一个嵌入到组织中。
可替换地或另外,其中,至少部分地基于第一距离和第二距离同时地检测第一参数包括感测第一电极与一个或多个回路电极之间的第一电压电位以及感测第二电极与一个或多个回路电极之间的第二电压电位。
可替换地或另外,同时地检测第一参数包括求解至少一个线性方程,以及其中,至少一个线性方程包括第一距离、第二距离、第一电压和第二电压。
可替换地或另外,同时地检测阻抗增加包括测量电流承载电极与一个或多个回路电极之间的阻抗。
另一种示例性电生理医疗设备包括:
包括远端部的导管轴;
具有多个电极的感测组件,其中,多个电极包括四个或更多个端子;
其中,四个或更多个端子包括一个或多个电流承载电极和一个或多个感测电极;
其中,一个或多个电流承载电极、一个或多个感测电极或这两者包括标测电极;
其中,四个或更多个端子被设计为测量电特性;以及
耦接到感测组件的处理器。
可替换地或另外,其中,电特性是电压、阻抗或这两者。
可替换地或另外,其中,电特性指示医疗设备与组织的接近度。
另一种用于感测与组织的接触的医疗设备包括:
导管轴,其中,轴包括远端部;
耦接到导管轴的远端部的感测组件,其中,感测组件包括多个电极;以及
其中,多个电极至少包括第一标测电极,以及其中,第一标测电极被设计为检测阻抗增加,以及其中,通过阻抗的100%或更多的增加来定义阻抗增加。
一些实施例的以上摘要不是意图描述每个所公开的实施例或者本公开的每个实现。下文的附图、和详细描述更具体地例示了这些实施例。
虽然公开了多个实施例,但是通过显示并且描述了本发明的说明性实施例的以下详细描述,本发明的其他实施例将对于本领域熟练技术人员显而易见。因此,附图和详细描述被视为是说明性而不是限制性的。
附图说明
结合附图考虑以下详细描述可以更完整地理解本公开,其中:
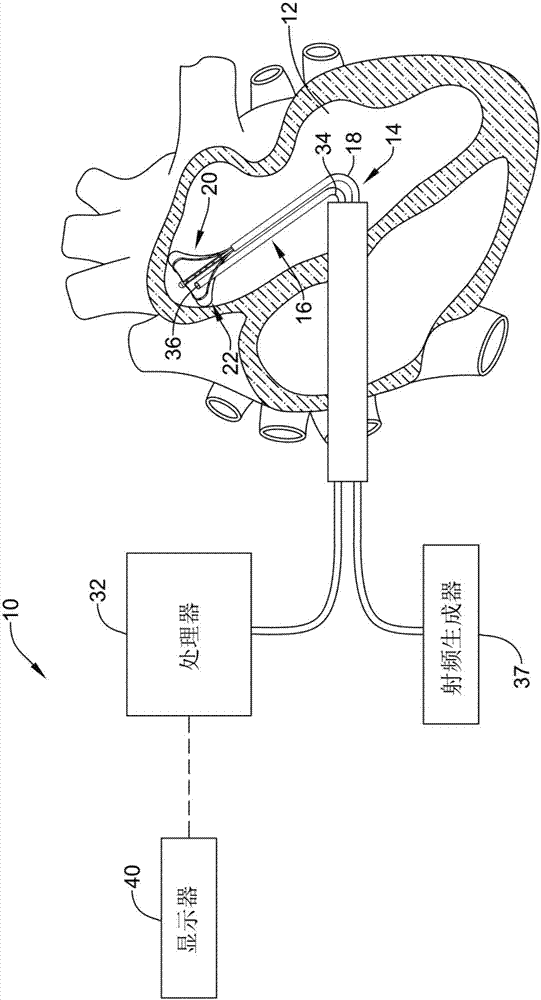
图1是示例性组织诊断和/或消融系统的平面图;
图2示出了包括电极结构、导管轴和把手的示例性医疗设备;
图3示出了包括感测电极的示例性篮状物电极结构(basketelectrodestructure);
图4示出了具有多层的示例性电极;
图5示出了具有多层的示例性电极;
图6至图8示出了在血液和组织之间移动与图1的系统一起使用的示例性电极结构;
图9示出了具有与尖端电极相隔不同距离的多个感测电极的示例性电极结构。
虽然本公开可修改成多种修改和替换形式,但是其细节已在附图中以实例形式显示以及将会详细描述。但是要理解,不意图将本发明限于所述具体实施例。相反,意图覆盖落入本公开的精神和范围中的全部修改、等效物和替换物。
具体实施方式
对于下文限定的术语,应该应用这些定义,除非在权利要求或者本说明书的其他地方给出了不同的定义。
本文假设所有数值通过术语“大约”来修饰,不管有没有明确指示。术语“大约”通常涉及本领域熟练技术人员会视为与所引用的值等效的数字范围(例如具有相同的功能或结果)。在许多实例中,术语“大约”可以包括进位到最接近的重要数的数字。
通过端点记载的数值范围包括在该范围内的全部数字(例如1到5包括1、1.5、2、2.75、3、3.80、4和5)。
如说明书和所附权利要求中所使用的,单数形式“一”、“一个”和“该”包括复数个指代物,除非其内容明确指示不是这样。如说明书和所附权利要求中所使用的,术语“或”通常用于意味着包括“和/或”,除非其内容明确指示不是这样。
注意到在说明书中指代的“一个实施例”、“一些实施例”、“其他实施例”等等指示所述实施例可以包括一个或多个具体特征、结构和/或特性。然而,该记载无须意味着全部实施例包括该具体特征、结构和/或特性。另外,当结合一个实施例来描述具体特征、结构和/或特性时,应该理解可以结合无论是否明确描述的其他实施例来使用该具体特征、结构和/或特性,除非明确相反地说明。
应该参考附图来阅读下文的详细描述,其中在不同的附图中类似的元件被相同标号。无需按比例描绘的附图描述了说明性的实施例并且不是意图限制本发明的范围。
有助于异常心脏功能的心律不齐和/或心脏病理可能源自心脏细胞组织。一种可用于治疗心律不齐和/或心脏病理的技术可以包括有助于心律不齐和/或心脏病理的组织基层的消融。通过热量、化学或用于在组织基层中造成损害的其他方式的消融可以将病变组织与正常心脏循环隔离。在一些情况中,电生理疗法可以涉及使用标测和/或诊断导管来定位有助于心律不齐和/或心脏病理的组织,以及随后使用消融电极来破坏和/或隔离病变组织。
在执行消融程序之前,内科医生和/或临床医生可以使用专用标测和/或诊断导管来精确定位有助于和/或导致心律不齐或其他心脏病理的组织。通常希望在执行消融程序之前精确地定位靶向的组织以便有效地减轻和/或消除心律不齐和/或心脏病理。另外,组织的精确靶向可以防止或降低(接近靶向组织定位的)健康组织被损坏的可能性。
可以应用多种方法来精确定位可以执行消融或其他疗法程序的靶向组织。一种示例性方法可以包括利用消融、标测和/或诊断导管来确定导管有多接近靶向组织。另外,消融、标测和/或诊断导管可以包括位于导管的远端部上的一个或多个感测电极。电极可以感测、测量和/或向处理器提供与心脏组织和周围媒介的电特性有关的信息。通过使用感测到的和/或测量到的信息,处理器可能能够将导管的远端部的空间位置与心脏组织关联。例如,电极可以感测心脏组织和/或周围媒介的阻抗、电阻、电压电位等等以及确定诊断和/或消融导管的远端部距离心脏组织多远。
通常,诊断(例如标测)导管上的电极的尺寸、形状和空间可以助于可以被诊断导管感测和/或测量到电特性的准确性。例如,本文公开的一些方法和/或技术可以从第一电极发射电流,以及使用其他电极测量局部组织的电压、阻抗或其他电特性。此外,在一些实例中,电极的尺寸可以直接影响处理器的测量响应的量级。例如,如在后文详细讨论的,通过使用与其他感测电极配置相比更小而平的电极,可以增大与组织接触相对应的阻抗测量。小而平的电极可以增加给定电极可变得完全嵌入和/或环绕心脏组织的可能性。将感测电极完全嵌入心脏组织中可以直接对应于确定电极是否与心脏组织接触。
另外,更大的电极可能(与更小的电极相比)更易检测到远场电活动。远场电活动的检测可能不利地影响局部(例如靶向的)电活动的检测。
因此,在一些实例中,可能希望在标测和/或诊断导管的远端部中利用和包括小而平的电极。例如,本文公开的一些医疗设备和方法可以包括结合其他感测方法、电极、消融电极、诊断导管和/或其他医疗设备来使用一个或多个相对小而平的电极感测和测量电活动。此外,本文公开的一些医疗设备和方法可以利用从小而平的电极采集的电特性来估计组织接近度和/或接触。还公开了其他方法和医疗设备。
图1是用于接入患者身体中的靶向组织区域以用于诊断和治疗目的的系统10的示意图。图1整体显示了布置在心脏的区域中的系统10。例如,系统10可以布置在心脏的任意腔室中如左心房、左心室、右心房或右心室、心血管系统的另一个区域或者其它解剖区域。虽然所示实施例显示系统10用于感测与心肌组织的接触和/或接近,但是系统10(以及本文所述的方法)可以可替换地配置为用于其他组织应用如用于感测前列腺、大脑、胆囊、子宫、神经、血管和身体的其他区域(包括通常未由导管接近的区域)中的组织的程序。
系统10包括标测导管10或探针14。在一些实例中,系统10还可以包括消融导管或探针16。可以使用合适的皮下接入技术将每个探针14/16经过静脉或动脉(例如股骨静脉或动脉)独立引入选定的心脏区域12。可替换地,标测探针14和消融探针16可以组装成集成的结构以同时引入和布置在心脏区域12中。
标测探针14可以包括柔性导管主体18。导管主体18的远端承载三维多电极结构20。在所述实施例中,结构20采取限定开口的内部空间22的篮状物的形式(见图2),但是可以使用其他多电极结构。结构20承载多个标测电极24(图1上没有明确显示但是在图2上显示了),每个标测电极24具有在结构20上的电极位置以及导电组件。每个电极24可以被配置为感测邻近解剖区域中的电特性(例如电压和/或阻抗)。
电极24可以电耦接到处理系统32。信号线(未显示)可以电耦接到结构20上的每个电极24。信号线可以延伸经过探针14的主体18并且将每个电极24电耦接到处理器系统32的输入。电极24可以感测与它们在心脏中的物理位置邻近的解剖区域有关的电特性。感测到的心脏电特性(例电压、阻抗等等)可以被处理系统32处理以通过生成已处理输出——来辅助用户例如医生,以识别心脏中适合于诊断和/或治疗程序例如消融程序的一个或多个场点。
处理系统32可以包括专用电路(例如离散逻辑元件以及一个或多个微控制器;专用集成电路(asic)、或特别配置的可编程设备如可编程逻辑器件(pld)或者现场可编程门阵列(fpga)),用于接收和/或处理获得的生理活动。在一些实例中,处理系统32包括通用微处理器和/或专用微处理器(例如数字信号处理器或dsp,其可以被优化以处理激活信号),其执行指令以接收、分析和显示与接收到的生理活动有关的信息。在该实例中,处理系统32可以包括当被执行时执行一部份信号处理的程序指令。程序指令可以例如包括由微处理器或微控制器执行的固件、微代码或者应用代码。上述实现仅仅是示例性的,并且读者将认识到处理系统32可以采取任意合适的形式接收电信号以及处理接收到的电信号。
消融探针16包括承载一个或多个消融电极36的柔性导管主体34。一个或多个消融电极36可以电连接到配置为传递消融能量到一个或多个消融电极36的射频(rf)生成器37。消融探针16可以关于待治疗的解剖特征以及结构20是可移动的。消融探针16可以定位为邻近或者在结构20的电极24之间,以及消融探针16关于待治疗的组织定位。
处理系统32可以输出数据到合适的设备例如显示设备40,其可以为用户显示相关的信息。在一些实例中,设备40是显示器(例如crt、led)或其它类型显示器或打印机。设备40以对于用户有用的形式给出相关的特征。另外,处理系统32可以生成位置识别输出以显示在设备40上辅助用户引导消融电极与被识别为要消融的场点处的组织接触。
图2示出了标测导管14以及显示了在远端处适用于图1中所示的系统10的标测电极24。标测导管14可以包括柔性导管主体18、其远端可以承载具有标测电极或传感器24的三维多电极结构20。标测电极24可以感测心肌组织中的电特性(例如电压、阻抗)。感测到的心脏电活动可以由处理系统32处理以辅助用户经由生成的和显示的相关特性识别具有心律不齐或其他心肌病理的场点。该信息然后可用于确定应用合适的疗法如消融到所识别的场点的合适的位置以及导航一个或多个消融电极36到所识别的场点。
所示的三维多电极结构20可以包括基底组件41和远端尖端42,柔性齿条44以圆周间隔的关系整体在它们之间延伸。如本文所讨论的,结构20可以采取限定开口内部空间22的篮状物的形式。结构20可以在末梢从收缩配置张开成更开口的配置。在一些实例中,齿条44由弹性惰性材料如镍钛诺、其他金属、硅胶、合适的聚合体等等制造并且连接在基底组件41和远端尖端42之间。在一些实例中,齿条44可以由聚对二甲苯制造成。如图2中所示,齿条44可以包括实质上平坦的面向外的表面21以及可以类似于这样一种条带即该条带具有实质上减小的厚度以及从远端尖端42延伸到导管主体18。在一些实例中,齿条44可以具有矩形和/或卵形横截面。这些仅仅是实例,设想了其他横截面形状。设想其他形状、配置和设置包括在美国专利8103327中公开的设置,通过引用的方式将其完整的公开并入本文。
在本文所述的一些实施例中,远端尖端42可以包括消融电极。此外,在一些实例中,远端尖端42可以包括耦接到rf生成器37的消融电极。远端尖端42可以发射消融能量和/或电流。
在一些实例中,齿条44定位在弹性预拉伸状态下,以弯曲和贴合它们接触的组织表面。在图2中所示的实例中,8个齿条44形成三维多电极结构20。在其他实例中,可以使用更多或更少的齿条44。如所示,每个齿条44承载8个标测电极24。在三维多电极结构20的其他实例中,在每个齿条44上可以布置更多或更少的标测电极24。可滑动鞘50可以沿导管主体18的主轴可移动。相对于导管主体18远离地移动鞘50可以导致鞘50在结构20上移动,从而将结构20折叠成适合于引入和/或移出解剖结构如心脏的内部空间的紧凑低轮廓状况(profilecondition)。相反,相对于导管主体18靠近地移动鞘50可以暴露结构20,允许结构20弹性扩张并且呈现图2中所示的预拉伸位置。
在其他实例中,可滑动鞘50(或其他布置轴)可以连接到远端尖端42。此外,结构20的布置可以包括操作耦接到远端尖端42的可滑动鞘50(或其他布置轴)。例如,可以通过在近端方向中推动可滑动鞘50(或其他布置轴)来完成结构20的布置。可滑动鞘50(或其他布置轴)的近端移动可以导致远端尖端42在近端方向中移动。随着远端尖端42向近端移动,其可以迫使齿条44张开以及采取例如图2中所示的结构20的形状。
信号线(未显示)可以电耦接到每个标测电极24。信号线可以延伸经过标测导管20的主体18(或者否则经过和/或沿着主体18)进入把手54,它们在把手54中耦接到可以是多管脚连接器的外部连接器56。连接器56可以将标测电极24电耦接到处理系统32。应该理解,这些描述仅仅是实例。在美国专利号6,070,094、6,233,491和6,735,465中可以找到关于这些以及其他标测系统和用于处理由标测导管生成的信号的方法的附加细节,通过引用的方式将这些公开明确并入本文。
为了说明系统10的操作,图3是包括多个标测电极24的示例性篮状物结构20的示意性侧视图。在所示实例中,篮状物结构包括64个标测电极24。标测电极24设置成8个齿条(标记为a、b、c、d、e、f、g和h)中的每一个上的8个电极的组(标记为1、2、3、4、5、6、7和8)。虽然64个电极的设置被显示为布置在篮状物结构20上,但是标测电极24可以可替换地设置成不同数量(更多或更少齿条和/或电极),在不同结构上和/或在不同位置中。另外,多个篮状物结构可以布置在相同的或不同的解剖结构中以同时获得来自不同的解剖结构的信号。
图4显示了沿齿条44设置的示例性电极60。电极60可以是多个标测电极24中的任意一个。在一些实例中,如在图4所示的实例中,电极60可以沿齿条44的表面粘附。然而,设想电极60可以使用多种方法耦接到齿条44。如本文所讨论的,电极60可以描述为“粘附”、“位于”和/或嵌入和/或装入在本文设想的任意结构上。这不是意图限制。沿齿条44定位/放置电极60可以包括嵌入、部分地嵌入、装入、部分地装入、孤立、附接、粘附、固定、结合到外表面,嵌入在壁中等等。另外,如关于图1-3所显示和描述的,设想多个电极60可以粘附到齿条44。
在一些实例中,电极60可以包括基层62和顶层64。顶层64可以是应用在基层62上的材料层。例如,在一些实例中,基层62可以由黄金制造成,而顶层64可以由氧化铱制造成。聚对二甲苯的遮蔽层可以应用到基层62上使得仅仅暴露顶层64。在一些应用中,基层62可以用作电镀层。例如,电极结构20可以由这样一种制造方法构造成即该制造方法可以与在半导体制造中利用的类似的过程有些相似。换句话说,制造过程可以包括沿底层62、在底层62上、在底层62中,与底层62嵌入地“印刷”或“分层”顶层64。此外,示例性制造方法可以包括形成这样一种材料(例如黄金)的底层62即在该材料上可以“印刷”、“分层”、“电镀”、“喷溅”等顶层64(例如氧化铱)。制造方法还可以包括在顶层64和/或底层62上和/或中分层一个或多个附加层。附加的材料层可以包括轨迹、电路组件等等。在一些实例中,层的一部分可以去除以暴露下面的层。这些仅仅是实例,设想了其他材料和制造技术。此外,虽然下文的讨论涉及前文描述的电极结构,但是设想包括没有多个层的多种电极设计可以与本文公开的任意医疗设备、系统或方法一起使用。
图5显示了包括齿条44、底层62、顶层64的电极60的平面视图。图5显示底层62在顶层64下方并且具有实质上与齿条44的长度对齐的长度。顶层64的长度由字母“x”描述。此外,图5显示了顶层64具有与齿条44的纵轴垂直并且由字母“y”描述的宽度。在一些实例中,顶层64可以具有.25-1.5mm、.5-1.25mm、.75-1.0mm等等的暴露长度。在一些实例中,顶层64的长度可以是.95mm。
如图4和5中所示,电极60可以具有实质上小的轮廓。该降低的轮廓可以允许电极60嵌入到齿条44中、设置为与齿条44的外表面21“齐平”、在齿条44的顶表面上略微“出位”地搁置或者比齿条44显著出位地搁置。在电极60嵌入在齿条44中的情况中,电极60的表面而不是顶层64的表面可以不暴露于与齿条44的最外表面接触的表面。换句话说,在一些情况中,电极60的唯一暴露的表面包括顶层64。
图4和图5将电极60(包括底层62和顶层64)描述为具有大体矩形。这仅仅是一个实例。设想电极60(及其任意部分)可以是圆形、梯形、正方形、卵形、三角形等等。
如上所述,篮状物结构20可以伸进解剖结构中并且邻近要治疗的解剖结构(例如心脏的左心房、左心室、右心房或右心室)定位。另外,处理系统32可以被配置为记录来自每个标测电极24的选定电特性(例如电压、阻抗等等)。在一些实例中,这些电特性可以提供与篮状物结构20和解剖结构之间的关系相对应的诊断信息。
一种用于估计组织接触的示例性方法可以包括确定模型的参数以及随着导管14的远端在不同的媒介之间(例如在血液与组织之间)移动观察参数的变化。可以理解,随着在心脏腔室内操作导管14,导管14可以在血液和组织之间移动。
比例因子可以是用于该目的的模型中的参数。模型可以涉及一个或多个感测电极与参考电极之间的一个或多个电位差。参考电极可以是相距电位测量电极一个距离放置的电极。例如,参考电极可以放置在患者背部。感测电极可以是篮状物结构20上的电极24的多种组合中的一个。
另外或可替换地,模型还可以涉及电流承载电极与一个或多个感测电极之间的空间中的距离。电流承载电极可以具有多种形式。例如,电流承载电极可以是篮状物结构20上的标测电极和/或定位在远端尖端42上的远端消融尖端电极中的任意一个。
在一些配置中,感测电极与参考电极之间的电位测量可以建模为与电流承载电极和感测电极之间的距离成反比。例如,该关系可以建模为:
在该实例中,参数k可以用于估计组织接触。以上方程式仅仅是一个实例。设想了其他模型和参数。在一些实例中,参数k可以称为“k因子”。
如上所述,该模型可以涉及一个或多个感测电极之间的电位差以及电流承载电极与感测电极之间的距离。例如,图9示出了包括电流承载电极70和四个感测电极63、65、67和68的示例性远端尖端42。图9仅仅是个实例。要理解,篮状物结构20上的任意标测电极24的组合和配置可用于本文所述任意实施例。例如,任意一个标测电极24可以被配置为感测和/或电流承载电极。
在一些实例中,以上电极与电位值之间的关系可以由以下方程式表示:
可以理解,变量
可以使用多个已知的用于优化或线性递归的技术来估计以上线性方程组中的参数k和c。例如,可以使用最小二乘法来估计k和c。设想了其他方法。此外,可以理解,以上线性方程组可以以其它方式设置。例如,线性方程可以组合使得参数c消失并且仅剩k要估计。
比例因子k可以与给定媒介的传导率成反比。换句话说,比例因子k可以对于具有不同传导率的两个媒介不同。例如,血液的传导率大于心脏组织的传导率,并且因此,与心脏组织相比,对于血液来说,比例因子k将是更低的。
通过知道电位差以及绝对距离值,可能能够求解比例因子k的(以上)线性方程组。应该注意到,为了求解所公开的线性方程组,感测电极必须定位在相距电流注入电极的不同距离处。如果例如距离全部相同,则方程式的右手边的矩阵会是奇异矩阵并且导致无限数量个等效解。参考图9,可以看出,感测电极63、65、67、68定位在距电流注入电极70不同的距离处。
图9示出了沿齿条44纵向定位的感测63、65、67、68。然而,设想感测电极63、65、67、68可以定位为除了沿纵轴之外的配置并且仍然保持感测电极与电流承载电极70之间的可变距离。另外,在一些实例中,可以将感测电极的数量降低到两个或三个以及求解比例因子k的对应的线性方程组。在其他实例中,可能希望增加感测电极的数量;使用公知的技术如最小二乘法也可以估计参数k。
从以上讨论可以理解,可以利用已知变量求解比例因子k的所公开的线性方程组。因此,随着导管14的远端部在不同媒介(例如血液、组织)之间移动,系统10可以确定和比较不同的比例因子值。比例因子的差可以用作组织接触的诊断指示器。
此外,因为每个单独的标测电极24可以配置为感测和/或电流承载电极,所以通过使用复用的测量,多个电极可以用于指示组织接触。复用可以包括任意数量个已知的技术如时分、频分或者码分复用。例如,在一个频或时“隙”中,电极63可以是电流承载电极,而电极65、67和68可以是感测电极。在第二频或时隙中,电极65可以是电流承载电极,而电极63、67和68可以是感测电极。要理解,结构20上的任意电极组合可以是电流承载电极和/或感测电极。此外,因为电流承载电极看到的大部分阻抗是由于最靠近电极的传导媒介,所以任意给定电极可以指示电极结构20的不同部分与组织的接触。因此多个电极可以组合以提供两个或更多个空间不同的接触指示器。
从以上讨论可以理解,与其他电极结构相比,本文公开的标测电极24的尺寸和设置可能更适合用于检测局部化的比例因子k。小而平的电极几何形状可以使得施加的电流分布与利用更大的不平的电极将要实现的电流分布相比对于附近的组织更加局部化。标测电极的靠近的间隔可以导致比例因子与利用更大电极间隔将要实现的比例因子相比的更加局部化的估计。
使用比例因子k来估计组织接触可能相当可靠。然而,在一些实例中,系统10的定位和/或配置可以改变比例k因子结果。在这些实例中,可能希望利用用于估计组织接触的补充方法。设想了各种用于估计组织接触的补充方法。例如,用于估计组织接触的补充方法可以包括将测量的心脏激活的幅度或者其空间或时间衍生值与门限值比较。另一种示例性的用于估计组织接触的补充方法可以包括确定肯定地识别组织接触的门限阻抗值。更具体地,在一些实例中,系统10可以能够感测和/或测量阻抗增加并且将阻抗增加与组织接触的可视、可听等等指示相关联。
例如,系统10可能能够利用门限阻抗测量来感测标测电极24与相邻组织之间的接触。通常,可以通过应用已知电压或电流到给定媒介以及测量结果电压或电流来测量给定媒介的阻抗。换句话说,可以通过在两个电极之间注入电路以及测量被电流注入经过的电极之间的结果电压来获得给定介质的阻抗测量。电压电位的比率提供了电流传播经过的媒介的阻抗的指示。
例如,在一些实例中,可以在电极24与一个或多个回路电极(returnelectrode)(例如贴片电极、迷你电极、测量电极、感测电极等等)之间注入电流。可以根据上文公开的方法测量与电流承载电极24相邻的媒介(例如组织、血液)的阻抗。例如,如果电极24邻近或嵌入心脏组织,则通过测量电极24与一个或多个回路电极之间的电压电位的比率可以确定心脏组织的阻抗。虽然上文的讨论整体描述了以单极性模式利用电流承载电极和回路电极,但是设想电极24可能能够操作在或者配置为操作在双极性感测模式中。
电极的尺寸和形状可能影响电极24测量细胞组织和/或周围媒介(例如血液)的电特性的能力(或无能)。在一些实例中,电极24维持与心脏组织的接触的程度可能影响感测到的电响应的量级。例如,当电极24完全覆盖和/或嵌入在组织中时,可以感测到加大的阻抗值。在一些实例中,加大的阻抗值可以描述为“阻抗增加”。因此该阻抗增加可以直接对应于组织接触。可以理解,图4中所示的电极60的实质上平坦的减小的轮廓以及相对较小的形状可以增加随着电极60相邻组织定位时其完全被组织覆盖从而触发阻抗增加的可能性。此外,可以由处理系统32感测阻抗增加,以及在一些实例中,输出信号到显示器40指示电极60已经与组织接触。阻抗增加可以是测量到的基准阻抗值的量级的100%、150%、200%、250%、300%、350%、400%、450%、500%、600%、700%、800%、900%、1000%、2000%、50000%或更多。
图6至图8是示出了在示例性心脏腔室中正在操作的电极结构20的一系列图。更具体地,图6至图8描述了电极结构20向前经过血液朝向心脏组织。例如,图6显示了电极结构20,其包括完全被血液包围的标测电极24。图7显示了定位在血液/组织界面的标测电极24,而图8显示了嵌入在组织中的电极结构20。在这些实例中,随着在心脏腔室中操作电极结构20,多个标测电极24中的一个或多个可以连续感测与它们各自的外表面邻近的阻抗值。另外,处理系统32可以连续地操作以“感测”来自电极24中的任意一个的阻抗增加。例如,随着标测电极24从图6中示出的位置移动到图8中示出的嵌入位置,处理系统32可以感测到阻抗增加以及输出组织接触的对应指示到显示器40。
从以上讨论可以理解,本文公开的电极的尺寸和形状与相对更大的非平坦电极相比可能更适合于检测阻抗增加。换句话说,本文公开的电极尺寸和形状可以更容易地覆盖和/或嵌入在邻近组织中,从而导致更大数量的感测到的阻抗增加以及因此组织接触的肯定指示。
除了本文公开的任意实施例之外,另外或可替换地,在一些实例中,可能希望通过同时使用两个或更多个本文讨论的方法来感测组织接触。如上所述,在一些实例中,当操作在解剖结构(例如心脏腔室)中时,处理系统32可能难以感测或比较k因子值的变化。因此,可能希望处理系统32在监视和确定k因子的变化的同时感测阻抗增加。然而,在一些实例中,处理系统32可以不管尚未利用k因子方法检测到组织接触,就检测与肯定组织接触有关的阻抗增加。(在没有经由k因子方法的肯定的组织接触的情况下)检测到阻抗增加,系统10可以设计为的组织接触的肯定指示输出端显示器和/或医生。类似地,不管尚未检测到阻抗增加,处理系统10就可以时不时感测与肯定组织接触相对应的k因子变化。此外,设想在一些实例中,系统10可以同时感测k因子改变和阻抗增加,这两者提供组织接触的肯定指示。
除了本文公开的任意实施例之外,另外或可替换地,通过在电极结构20上的任意标测电极24之中利用四端子感测配置(其中任意数量可以操作为感测和/或电流承载电极),可以实现本文公开的任意电特性的测量的改善。通常,四端子感测配置通过一对“电流承载”电极来驱动电流以及测量不同的一对“感测”电极上的电压。
四端子感测配置的一个优点在于测量到的阻抗可能对于电极自身的阻抗不敏感。在两端子感测配置中,测量到的阻抗包括周围媒介和两个电极。相反,四端子感测配置测量这样一种电极上的电压即经过该电极的电流是可忽略的。结果,测量到的阻抗是周围媒介的阻抗并且大体取决于电极以及其与周围媒介的界面的阻抗。
另外,在一些实例中,通过在电极结构20上的任意标测电极24之中利用三端子感测配置(其中任意数量可以操作为感测和/或电流承载电极),可以实现本文公开的任意电特性(例如阻抗)的测量的改善。三端子感测的一些实例可以在美国专利申请8,449,535中找到,通过引用的方式将其整体并入本文。此外,在至少一些实例中,在可应用的程度上,三端子感测可用于代替本文描述的四端子感测配置。
可以理解,电极结构20上的标测电极24的任意组合可以包括和/或利用四端子感测。另外,设想电极结构20上的任意单独的标测电极24可以操作为感测电极或电流承载电极。另外,如上所述,系统10可以复用感测配置使得标测电极24是感测和电流承载电极。
此外,设想利用k因子方法、阻抗方法或者两者的组合来感测组织接触可以根据希望进一步包括四端子感测。例如,可以使用四端子感测来获得k因子方法的电压值。类似地,可以使用四端子感测来获得阻抗增加方法的阻抗增加值。另外,任意方法可以利用四端子感测与任意其他方法相结合。例如,“k因子四端子”方法可以与阻抗增加方法同时利用,因而该阻抗增加方法可以包括或不包括四端子感测。另外,“阻抗增加四端子”方法可以与k因子方法同时利用,因此,该k因子方法可以包括或不包括四端子感测。
在一些实例中,标测电极24可以可操作地耦接到处理器32。此外,从标测电极24生成的输出可以被发送到系统10的处理器32以便以本文讨论的一种或多种方式来处理和/或以其他方式处理。如本文所述的,来自电极对的电特性(例如阻抗)和/或输出信号可以至少部分地形成接触估计的基础。
此外,系统10可能能够处理或者可以配置为处理来自标测电极24的电信号。至少部分地基于来自标测电极24的处理输出,处理器32可以生成输出到显示器(未显示)以便被医生或其他用户使用。在向显示器生成输出的实例和/或其他实例中,处理器32可以可操作地耦接到显示器或者否则与显示器通信。通过示例的方式,显示器可以包括与系统10的使用有关的各种静态和/或动态信息。在一个实例中,显示器可以包括目标区域的图像、解剖外壳、传递在解剖外壳上的位置处实现的组织接近度的图、包括组织接近度信息的电解剖图、结构20的图像和/或用于传递与组织接近度有关的信息的指示器中的一个或多个,其可以被用户和/或被系统10的处理器分析以确定心脏中的心律不齐基层的出现和/或位置,以确定心脏中的导管18的位置和/或以做出与导管18和/或其他细长组件的使用有关的其他确定。
系统10可以包括与处理器32通信的指示器。指示器可能能够提供与从结构20的一个或多个电极接收到的输出信号的特征有关的指示。在一个实例中,可以在显示器上向临床医生提供与结构20和/或交互的和/或正在被标测的心肌组织的特性有关的指示。在一些情况中,指示器可以提供可视的和/或可听的指示以提供与结构20和/或交互的和/或正在被标测的心肌组织的特性有关的信息。例如,系统10可以确定测定的阻抗对应于心脏组织的阻抗值并且因此可以输出彩色指示器(例如绿色)到显示器。彩色显示器可以允许内科医生更容易地确定是否应用消融疗法到给定心脏位置。这仅仅是一个实例。设想系统10可以利用多种指示器。
在一些实施例中,处理器32可以按照对于临床医生不直接可见的方式来使用来自标测电极24的已处理输出。例如,用于接触估计的已处理信息可以包括在用于导管局部化、解剖外壳和电解剖图生成或者图像注册的算法中。
在一些实施例中,显示器可以包括合并了组件接近度信息的解剖外壳或者电解剖图。例如,心脏组织的阻抗值被测量的解剖外壳区域可能比血液的阻抗值被测量的区域更不透明。在其他实例中,用于显示特征如电压、激活时间、主频率等等的电解剖图可以在血液的阻抗值被测量的区域中显示指示器(例如、彩色、纹理、样式等等)。在两个情况中,已经发生(或者发生可能性高于给定概率或者可接收门限的)组织接触的区域的指示可以指导内科医生移动导管和采集测量。解剖外壳和电解剖图的实例可以在美国专利申请公开号20120184863、美国专利申请公开号20120184864、美国专利申请公开号20120184865中找到,通过引用的方式将其整体并入本文。
在一些实例中,可以根据本文公开的任意过程和/或方法对于结构20上的一个或多个标测电极24采集组织接近度数据。另外,采集到的参数和/或组织接近度值可以显示在如上面讨论的解剖外壳和/或电解剖图上。
在其他实例中,组织接触信息可用于遮蔽解剖外壳和/或电解剖图的一部分。此外,该外壳或图的被显示(或遮蔽)的部分可以对应于组织接触的门限置信等级。例如,遮蔽的部分可以对应于低于门限置信值的参数值。
如上文所讨论的,临床医生可以操作用于显示(或遮蔽)组织接触位置的解剖外壳和/或电解剖图,以便生成解剖区域(例如心脏腔室)的更准确的诊断表示。
通过引用的方式将以下文献并入本文:美国专利申请公开号us2008/0243214、美国专利申请公开号us2014/0058375、美国专利申请公开号us2013/0190747、美国专利申请公开号us2013/0060245和美国专利申请公开号us2009/0171345。
在不脱离本发明的范围的前提下可以对于示例性实施例做出各种修改和增加。例如,虽然上文公开的实施例涉及特定特征,但是本发明的范围还包括具有特征的组合的实施例以及不包括上文公开的全部特征的实施例。因此,本发明的范围意图包括落入权利要求及其等效物的范围中的全部该替换、修改和变形。
- 还没有人留言评论。精彩留言会获得点赞!