白头翁皂苷B4在制备治疗疼痛的药物中的应用的制作方法
本发明属于药物用途技术,具体涉及白头翁皂苷b4在制备治疗疼痛的药物中的应用。
背景技术:
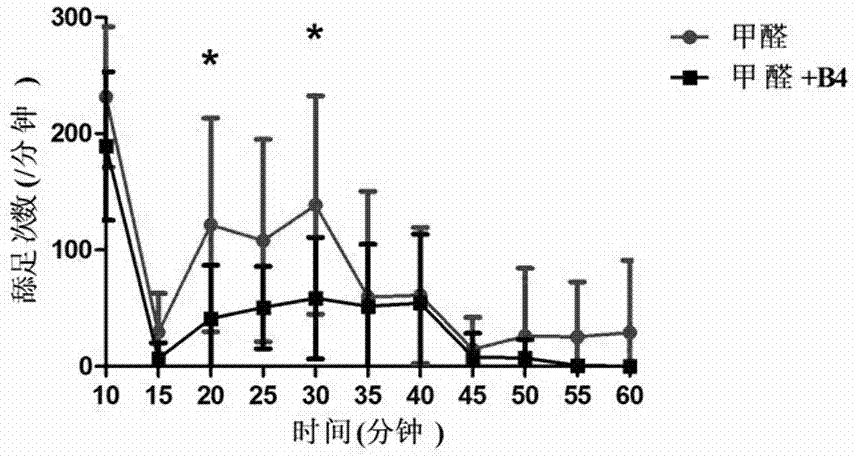
:疼痛是一种不愉快的感觉,是伴有实际或潜在组织损伤的情绪体验,是临床上最常见的症状,会给患者造成多方面的损害,严重影响人们的生活质量,目前疼痛仍是困扰病人的一个常见问题。疼痛可分为多种。按疼痛的部位,可分为浅表痛、深部痛和牵涉痛,例如由机械性、化学性、物理性的不良刺激引起皮肤和黏膜部位的疼痛。深部痛是指内脏、胸膜、关节、腹膜等部位受刺激而产生的疼痛。常表现为灼痛,不呈局限性。牵涉痛是指深部痛表现为远离病灶的浅表痛,如胆囊炎表现为右肩痛。此外,按疼痛起因分为炎症性痛、神经病理性痛、癌痛、创伤性疼痛等,按疼痛程度可分为轻度痛、中度痛、重度痛、极度痛等。持续的疼痛严重影响人们的生活质量,给患者带来痛苦,可导致患者的抑郁、情绪低落。据统计,全世界人口1/3以上遭受着持续或反复发作的疼痛折磨。导致疼痛的原因很多,目前疼痛机制研究比较多,但是疼痛的机制还不是很清楚。疼痛根据其神经生理学机制可分为感受性疼痛和神经病理性疼痛两类,前者直接由伤害性刺激引起,与组织损伤有关;后者由躯体感觉神经系统的损伤或疾病直接造成的慢性疼痛。目前,大家比较关心的还有癌性疼痛,有75%~95%的晚期癌和转移癌患者都有癌症疼痛。癌症诱导的骨疼痛(简称骨癌痛)是癌症疼痛的典型代表,是一种独特的疼痛状态,严重影响癌症患者的生活质量,目前尚缺乏有效的治疗手段。肿瘤组织压迫并侵蚀邻近的感觉神经,肿瘤细胞及相关免疫细胞释放一系列因子致敏外周伤害性感受器,肿瘤导致的骨质破坏和局部缺血、缺氧的微环境是骨癌痛形成的起始因素,在这些因素的持续刺激下中枢神经系统也被致敏,并对骨癌痛的维持起重要作用。临床上癌症疼痛主要表现为:持续的进行性的背景痛(ongoingpain)、突破痛(beakthroughpain)和痛觉异常。骨癌痛的治疗药物包括非类固醇类药、阿片类药物、二膦酸盐类药物和其他尚在开发中的药物等。此外,在各种类型的病理性疼痛中,神经性疼痛(neuropathiepain)被视为最难攻克的难题。神经性疼痛是指由神经系统受损或功能失调引起的病理性疼痛。主要表现为:1)自发性疼痛,如外伤、肿瘤、烧伤、病毒感染、糖尿病和化疗药物等多种原因引起神经损伤,从而引起的疼痛;2)痛敏,就是痛反应增强;3)痛超敏,指痛阈显著下降。外周和中枢机制共同参与神经病理痛的发生。外周神经损伤后,早期的异位放电不仅是早期急性痛的重要原因。并且这些异位放电不断轰击脊髓背角等中枢部位.诱发产生脊髓背角长时程增强等中枢敏化现象,中枢敏化和下行易化系统的激活等中枢机制在神经病理痛后期维持中起到重要作用。关节疼痛是一种常见的疼痛疾病,其基本病理改变为多种致病因素引起的进行性关节软骨变性、破坏及丧失,关节软骨及软骨下骨边缘骨赘形成,由此引起关节疼痛、僵硬、肿大、畸形及功能障碍,其中关节疼痛为最突出的症状。随着病情的进展,疼痛呈轻度至中度间歇性疼痛,最后发展成为持续性疼痛。关节疼痛的机制是复杂的,包括支配关节的a8和c纤维具有小的感受野,可以被关节的伤害性刺激所激活,这些感受器能够感受关节的机械刺激,也能感受关节的化学刺激。此外,关节内还有一些其他的神经纤维,不能够被正常的伤害性刺激所激活,称之为静止感受器,只有在关节内损伤已经形成,才能被激活并应答、敏化,从而形成痛敏。此外,伴随外周损伤,导致神经中枢敏化包括活化、调控以及修饰,因此关节疼痛是一个复杂的过程。目前治疗疼痛的药物有两大类,包括以阿片类药物(麻醉性缓解疼痛药)和非甾体类药为主。阿片类药物作用于中枢神经系统,有强大的缓解疼痛作用,临床上主要用于癌性疼痛和其他各种锐痛的治疗。然而,因其成瘾性而在临床应用受到很大的限制。非甾体类缓解疼痛药是具有解热、缓解疼痛,但是长期大量使用会产生严重的不良反应,包括胃肠道反应、肝肾毒性、引发心血管系统疾病和出血倾向。因此,选择性高、安全性好、副作用小的新型缓解疼痛药物的研究和开发日益成为医药界研究的热点。目前,上市用于临床治疗和临床实验中的缓解疼痛药物还包括(1)激肽受体抑制剂类,包括缓激肽和胰激肽受体抑制剂以及速激肽受体拮抗剂,这类药物具有高效、长效缓解疼痛作用,并且在镇咳、止吐等方面也有良好的开发前景;(2)选择性环氧化酶抑制剂。代表药物有替尼达普,一种脂氧合酶-环氧合酶双效抑制剂;(3)no合酶抑制剂,如7-硝基吲唑,此药对血压、血管平滑肌无影响;(4)辣椒素衍生物。目前,临床已局部应用辣椒素缓解疼痛,如乳房切除后疼痛等,但因其烧灼感而限制了应用。白头翁为毛莨科植物白头翁(pulsatillachinensis(bunge)regel)的干燥根,始载于《神农本草经》。是中医治疗热毒血痢的临床常用药,尤善清大肠湿热及血分热毒。目前对白头翁化学成分、药理作用、含量测定等已有较为广泛的研究。现代药理研究发现白头翁具有增强免疫功能、抗肿瘤、抗病原微生物、抗寄生虫、保肝、毒性及治疗内毒素血症等作用。白头翁的化学成分研究始于60年代初,共分得了约19种成分,主要为皂苷和内酯等成分,目前认为白头翁的有效化学成分主要为三萜皂苷。最近的研究表明白头翁皂苷元(23-羟基白桦酸)具有最有效的抗黑色素瘤作用,低糖基白头翁皂苷能促进皮肤胶元蛋白合成及抗自由基氧化,故可将其应用于皮肤抗老化化妆品行业及保健食品行业。白头翁主要有效成分为皂苷类成分,其中白头翁皂苷b4为其主要代表。近年来对于b4的化学结构及含量测定的研究居多,对于其药理活性却知之甚少。近年也已有关于白头翁皂苷b4抗肝癌的研究,但对白头翁皂苷b4的疼痛作用尚未有文献报道。技术实现要素:本发明公开了白头翁皂苷b4在治疗疼痛中的应用。为达到上述发明目的,本发明采用如下技术方案:白头翁皂苷b4在制备治疗疼痛的药物中的应用。本发明还公开了一种治疗疼痛的药物,其活性成份为白头翁皂苷b4。上述技术方案中,所述治疗疼痛的药物还包括药物辅料。本发明还公开了一种治疗疼痛的药物的制备方法,将白头翁皂苷b4与药物辅料混合,制备治疗疼痛的药物。白头翁皂苷b4在制备治疗足肿胀的药物中的应用。白头翁皂苷b4在制备提高痛阈值的药物中的应用。白头翁皂苷b4在制备减轻踝关节变形和滑膜组织异常增生的药物中的应用。本发明还公开了一种治疗疼痛的试剂,包括白头翁皂苷b4、药物辅料以及包装瓶。本发明的药物为片剂、丸剂、滴丸剂、胶囊剂、颗粒剂、散剂、涂剂、巴布剂、喷雾剂或注射剂。本发明药物的剂量为0~60mg/kg,且不含0,优选5~60mg/kg。本发明采用小鼠醋酸扭体法,观察给药后不同剂量组的小鼠扭体次数,采用福尔马林诱导的小鼠疼痛模型,观察舔足时间和次数,采用大鼠完全弗氏佐剂诱导模型,通过热板实验,足趾容积,机械性痛阈测定,病理学检查等测定进行观察。结果表明在小鼠醋酸扭体实验中,与造模组比较,白头翁皂苷b4各剂量组的小鼠扭体次数明显减少,b4低剂量组(12.5mg/kg)的数据具有统计学意(p<0.05),b4中剂量组(25mg/kg)的扭体次数减少有显著性差异(p<0.01),b4高剂量(50mg/kg)的扭体次数减少具有非常显著性差异(p<0.001),并且与阳性对照组(aspirin)相比,扭体次数也明显减少,具有显著性差异(p<0.01);在福尔马林诱导的疼痛模型中,白头翁皂苷b4(50mg/kg)减少小鼠的舔足时间和次数(p<0.05);白头翁皂苷b4(6.25mg/kg)抑制大鼠的关节肿胀,降低足体积肿胀度(p<0.05)和痛阈值(p<0.05),病理切片显示白头翁皂苷b4减轻踝关节的变形和滑膜组织的异常增生,并减少细胞浸润。在小鼠热板实验中,b白头翁皂苷4(12.5mg/kg)能提高小鼠的痛阈。总之,白头翁皂苷b4对醋酸所致小鼠扭体模型,热辐射痛模型,福尔马林诱导的小鼠疼痛模型和大鼠疼痛模型具有良好的缓解疼痛作用。附图说明图1白头翁皂苷b4对醋酸所致小鼠扭体反应的影响;图2为小鼠甲醛模型的舔足次数的变化图;图3为小鼠甲醛模型的两相中舔足次数的变化图;图4为小鼠甲醛模型的两相中舔足时间的变化图;图5为15d各组大鼠足肿胀情况比较图;图6为白头翁皂苷b4对弗氏佐剂模型大鼠足体积的影响图;图7为白头翁皂苷b4对热板实验的小鼠痛阈提高率的影响图;图8为各组大鼠机械痛阈的变化图;图9为大鼠踝关节与膝关节滑膜组织病理切片情况图;图10为小鼠热辐射甩尾实验痛阈提高百分率图。具体实施方式白头翁皂苷b4(纯度为99.8%),由苏州大学天然药物化学课题组分离纯化而得;完全弗氏佐剂cfa(其含有在液体石蜡中的10mg/ml热灭活的结核分枝杆菌),每支10ml,sigma公司产品;冰乙酸:纯度99.5%,江苏强盛功能化学股份有限公司,批号20160601;甲醛:国药集团化学试剂有限公司,含量37-40%,批号20161011。el204电子天平,梅特勒-托利多仪器(上海)有限公司生产;pv-200足趾容积测量仪,成都泰盟科技有限公司生产;rb-200智能热板仪,成都泰盟科技有限公司生产;vonfreyfilaments纤毛机械刺激丝。观察指标足体积测量造模成功后,每天腹腔注射b4给药,在第6h,1天,2天,3天,11天,13天,15天,17天和19天给药后1h测量大鼠足肿胀,根据容积排水法原理在足容积测量仪上测定足体积,求出肿胀度(δml=肿胀后关节体积-肿胀前关节体积)。热板实验(20±2)℃室温条件下,置大鼠于(55±0.5)℃的热板测痛仪上,以大鼠舔后足作为痛反应的指标,大鼠接触热板至舔后足所经历的时间为痛阈值;造模前两天每天测量痛阈值,取平均值作为给药前(基础)痛阈值。在第6h,1天,2天,3天,11天,13天,15天,17天和19天测量给药后1h各大鼠的痛阈值,并计算各大鼠给药前后痛阈值的差值(基础痛阈值-给药后痛阈值),痛阈提高率=[(基础痛阈值-给药后痛阈值)/基础痛阈值]×%。机械性痛阈测定纤毛机械刺激丝法检测痛阈是较常用的慢性疼痛模型检测方法。检测时,将大鼠置于塑料板隔开的单独空间内,底部是铁制网格结构。在安静环境下,将大鼠置于疼痛检测架上,用透明鼠笼约束大鼠,适应10min后,使用vonfreyfilaments纤毛机械刺激丝,刺激大鼠的后足,每次测评均从轻到重(1.2,1.4,2.0,4.0,6.0,8.0,10,12,15,26和50g)触压后足的足底表面,当vonfreyfilaments纤毛机械刺激丝弯曲90°,大鼠仍然不抬足,视为无反应,以刺激开始6s内出现躲避或抬足记为阳性反应。每次刺激持续3s,间隔15s,连续5次。若3次不抬足,换用更高克数的纤毛;若5次中有3次抬足,则返回下一克数的纤毛,直到每5次测试中有3次抬足。能够引起3/5次抬足的最低vonfrey纤毛克数被定义为机械痛阈值(mwt)。先提前1天测量基础值,然后在第6,24,48,72h,11天,13天,15天,17天和19天测量机械痛阈值(mwt),并计算痛阈差值。组织病理检查第21天脱颈处死大鼠,解剖对照组、弗氏佐剂诱导模型组、b4给药组大鼠,取右后足的膝关节滑膜组织和踝关节,并保持关节完整。置于多聚甲醛固定液中固定至少24h,然后脱钙2-3天。脱钙完全后,将整个踝关节纵向切为4μm切片,膝关节滑膜横切。石蜡包埋切片,he染色,在光镜下观察细胞浸润,滑膜增生及关节破坏情况。热辐射甩尾实验(20±2)℃室温条件下,轻轻将小鼠置于热辐射甩尾仪上,以小鼠甩尾作为痛反应的指标,小鼠接触热辐射甩尾仪的辐射热刺激至甩尾所经历的时间为痛阈值;计算各大鼠给药前后痛阈值的差值(基础痛阈值-给药后痛阈值),痛阈提高率=[(基础痛阈值-给药后痛阈值)/基础痛阈值]×%。统计学处理所有数据表示为平均值±标准差,统计分析使用spss13.0统计软件分析结果。单因素方差分析用于确定各实验组值之间的统计学显着性差异。p<0.05为有统计学意义。实施例一18-22g的icr小鼠50只,合格证号:scyk(苏)2013-0003,随机分为4组,即醋酸扭体模型组,b4低剂量组(12.5mg/kg),中剂量组(25mg/kg)和高剂量组(50mg/kg),阳性对照组。给药组的给药剂量分别为12.5mg/kg,25mg/kg,50mg/kg。阳性对照药物为阿司匹林。小鼠提前适应实验室环境1天,给药组小鼠提前1h腹腔注射白头翁皂苷b4,造模组给予等量生理盐水,腹腔注射0.6%-1%醋酸溶液,观察并记录各鼠在20min内扭体次数。小鼠扭体表现为伸展后肢、腹部内凹和臀部抬高。图1白头翁皂苷b4对醋酸所致小鼠扭体反应的影响(***与造模组相比,p<0.001;**与造模组相比,p<0.01;*与造模组相比,p<0.05),与造模组相比,白头翁皂苷b4各剂量组的小鼠扭体次数明显减少,尤其是本发明的技术方案与现有成熟临床药物阳性对照组(aspirin)的扭体次数相当甚至减少;结果显示白头翁皂苷b4有较强的缓解疼痛作用。实施例二19-21g清洁级的icr雄性小鼠32只,合格证号:scyk(苏)2013-0003,随机分为甲醛造模组和b4给药组(50mg/kg)。所有实验动物均由昭衍(苏州)新药研究中心有限公司提供。19-21g的icr雄性小鼠适应实验室环境3天。分为造模组和b4给药组(50mg/kg),实验前把小鼠放入观察笼(10×20×15cm)内适应环境1h,从观察笼内取出。用25μl微量注射器在小鼠右后足趾皮下注射20μl的2%甲醛溶液,立即放入观察笼内观察舔足时间和次数。产生一种明显的自发性痛行为反应,即右后足表现出缩腿、舔爪及颤抖等反应,观察1h,分为12个时间段,每5min为一个时间段,记录小鼠舔足时间,作为疼痛指标。把观察得到的小鼠实验数据分为2个时间段处理:0-10min时间段为第一相,这个时间段实验小鼠感受急性疼痛的时间段,15-55min时间段为第二相。在小鼠右后足趾皮下注射20μl的2%甲醛溶液后,小鼠产生舔足反应在第1相(0-10min)中立即发生双相伤害感染行为,结果见图2-4,图2为小鼠甲醛模型的舔足次数的变化,图3为小鼠甲醛模型的两相中舔足次数的变化,图4为小鼠甲醛模型的两相中舔足时间的变化。与造模组比较,b4给药组(50mg/kg)舔足次数和时间逐渐减少;在第2相(15-55min)中b4给药组(50mg/kg)的舔足次数明显减少(p<0.05)(见图3),舔足时间有一定程度减少(见图4)。实施例三年龄4-6周的清洁级雌性sd大鼠20只,合格证号:scyk(苏)2013-0003,体重180-210g,随机分为3组,即空白对照组8只,完全弗氏佐剂诱导的模型组,白头翁皂苷b4给药组(6.25mg/kg),每组6只。给药组提前2天腹腔注射白头翁皂苷b4,每天1次。第0天给药后1h开始造模,除对照组足趾皮下注射0.1ml生理盐水外,其他组通过在右后足跖皮下单次注射0.1mlcfa(其含有在液体石蜡中的10mg/ml热灭活的结核分枝杆菌);足爪肿胀,表现为对侧后肢和双前肢足爪肿胀,进行性加重,耳和尾部出现结节和红斑,提示弗氏佐剂诱导模型诱导成功。对照组和弗氏佐剂诱导模型组给生理盐水,给药组大鼠腹腔注射白头翁皂苷b4,均每天1次,连续腹腔注射21天。白头翁皂苷b4给药组的剂量为6.25mg/kg。在第6h,1天,2天,3天,11天,13天,15天,17天和19天给药后1h观察足肿胀,热板实验和机械丝痛阈三项指标。完全弗氏佐剂模型大鼠的足肿胀一般变化情况为:足肿胀程度在第3天时达到峰值,属于急性期;之后开始消退,而后在第14天足肿胀度又开始增大达到另一个峰值,然后慢慢消肿。除正常对照组外,其余2组大鼠在第0天注射0.1mlcfa之后,在第1天时右后足明显肿胀,造模后的足体积测量实验显示造模成功;第3天后可见b4给药组(6.25mg/kg)中大鼠足肿胀逐渐消退,该组大鼠在第15天后足肿胀更是明显消肿,具有缓解疼痛的效果。第15天各组大鼠足肿胀情况见图5,a:正常组;b:造模组;c:b4给药组(6.25mg/kg)。在第6h,1天,2天,3天,11天,13天,15天,17天和19天,正常对照组、完全弗氏佐剂诱导模型组、白头翁皂苷b4给药组(6.25mg/kg)的大鼠足体积的比较见图6;b4给药组(6.25mg/kg)的大鼠足体积与模型组相比明显减小,说明b4给药组(6.25mg/kg)抑制大鼠足肿胀。从第11天开始到19天b4给药组(6.25mg/kg)大鼠右后足体积与造模组相比有显著性差异(p<0.01),而且在第11天的数据有非常显著性差异(p<0.001)。从表1中可看出,第19天造模组大鼠的足体积大于正常大鼠,说明完全弗氏佐剂诱导模型在实验期间造模成功,且从造模第2天起发现白头翁皂苷b4给药组(6.25mg/kg)抑制足肿胀,肿胀度减小。表1造模后19d各组大鼠右后足关节肿胀度的变化(`x±s)组别剂量(mg/kg)足肿胀体积(△ml)正常-0.18±0.19弗氏佐剂诱导模型-0.92±0.19###b46.250.43±0.18**注:###与正常对照组相比,p<0.001,**与造模组相比,p<0.01。第6h,1天,2天,3天,11天,13天,15天,17天和19天的热板实验结果见表2和图7。与造模组比较,白头翁皂苷b4给药组(6.25mg/kg)大鼠给药后从第13天开始明显抑制热板所致大鼠疼痛反应,延长动物痛阈值。痛阈提高率变化情况见图7,b4给药组(6.25mg/kg)的大鼠在第15、17天的痛阈提高率相对完全弗氏佐剂诱导模型组具有统计学意义(p<0.05),而第13、19天的痛阈提高率有显著性差异(p<0.01)。表2造模后19d白头翁皂苷b4对热板刺激的影响(`x±s)组别剂量(mg/kg)痛阈差值(s)痛阈提高率(%)正常_0.05±2.700.05±0.30弗氏佐剂诱导模型_-4.87±3.73#-0.44±0.14#b46.25-1.13±4.000.08±0.19*注:#与正常对照组相比,p<0.05;*与造模组相比,p<0.05。第6h,1天,2天,3天,11天,13天,15天,17天和19天的机械丝痛阈值结果见图8。由图8可知,弗氏佐剂诱导模型组大鼠机械痛阈值逐渐降低,与对照组相比差异有统计学意义(p<0.05);在第2、11、19天b4给药组(6.25mg/kg)与模型组比较,明显延长痛阈值,其差异有统计学意义(p<0.05)。结果表明白头翁皂苷b4给药组(6.25mg/kg)具有缓解疼痛作用。各组动物的踝关节病理学检查结果显示,正常对照组中滑膜衬里层是由1~2层滑膜细胞及滑膜下层组成,无明显细胞浸润;弗氏佐剂诱导模型组踝关节病理切片可见关节软骨变薄不明显;但是白头翁皂苷b4给药组(6.25mg/kg)的踝关节结构保持完整,无明显软骨破坏,滑膜无明显增生。弗氏佐剂诱导模型组膝关节的滑膜组织细胞明显浸润,滑膜异常增生,血管扩张;白头翁皂苷b4给药组(6.25mg/kg)滑膜病理改变较模型组明显减轻,滑膜细胞层增生程度减弱,细胞浸润明显减少。说明白头翁皂苷b4减轻踝关节的变形和滑膜组织的异常增生,并减少细胞的浸润(见图9,踝关节比较:①正常对照组;②弗氏佐剂诱导模型组;③b4给药组(6.25mg/kg)。滑膜组织比较:④正常对照组;⑤弗氏佐剂诱导模型组;⑥b4给药组(6.25mg/kg)。图10所示为小鼠热辐射甩尾实验结果,生理盐水对照组给生理盐水后,痛阈没有改变。b4给药组(6.25mg/kg)腹腔注射2小时后,与生理盐水组相比,痛阈明显提高,阳性对照抗炎药地塞米松不能提高小鼠的痛阈,无法起到镇痛作用。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1