一种用于图像引导的肿瘤精准穿刺活检的方法与流程
本发明属计算机图形学及外科医学领域,具体涉及基于图像引导的肿瘤精准穿刺活检的方法。
背景技术:
肿瘤个体化诊疗研究进入瓶颈阶段,需要结合新的研究思路和方向。目前,分子医学及个体化治疗方案主要是通过基因组学(genomics)和蛋白组学(proteomics)来检测肿瘤个体化特性。这类方法的最大局限性是:需要通过穿刺活检方式抽取部分肿瘤组织作为病理检测标本,由于肿瘤生长过程中内部的空间和时间的异质性,随机抽的小部分组织不能代表完整肿瘤组织的特性。因此,迫切需要发掘肿瘤术前精准穿刺活检手术的新方法,为肿瘤术前规划及手术方案定制等提供了一体化的辅助方案。
常规的肿瘤穿刺活检手术,是根据不同的肿瘤病变情况,通过内窥镜钳取、手术切除或穿刺针吸取的方法从患者的病变部位取出一小块组织,做一定的病理学切片处理后,通过显微镜观察病灶细胞和组织的形态结构变化,做出病理诊断。在这过程中,医生需要通过一些图像辅助操作确定出肿瘤的位置,如ct引导穿刺、超声引导穿刺、mri引导穿刺等,这些辅助操作用来帮助医生来判断肿瘤的空间位置、穿刺活检的部位、穿刺的方向和深度,从而规划出穿刺的路径,引导穿刺针进行穿刺,抽取病灶的小部分组织进行活检。但现有的引导及导航设备,都只是针对肿瘤整体进行穿刺,穿刺引导图像也只限于二维的灰度图像引导,无法呈现肿瘤内部特征及三维影像学特征。
技术实现要素:
本发明公开了一种用于图像引导肿瘤精准穿刺活检方法,用以提高肿瘤外科穿刺活检手术的成功率及肿瘤病理结果精准术前判断。
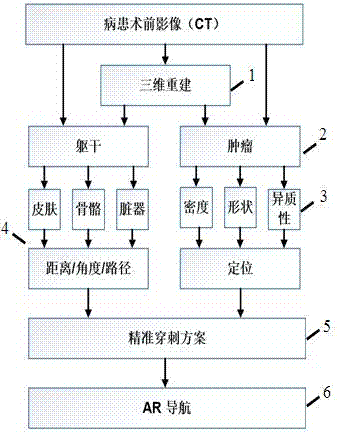
具体步骤包括,患者术前影像重建(1),目标肿瘤图像分割(2),肿瘤内部异质性四维热图重建(3),穿刺路径规划(4),三维图像配准(5),术中ar导航(6);本发明针对肿瘤生长过程中内部的空间和时间的异质性特点,针对现有的肿瘤穿刺活检手术中随机抽小部分病变组织,不能代表完整肿瘤表型这一问题,通过定量影像学分析,发掘了肿瘤术前精准穿刺活检手术的新方法,为肿瘤术前规划及手术方案定制等提供了一体化的辅助方案。
作为优选,所述的患者术前影像重建模块包括面绘制和体绘制两种方案;所述的影像包括ct/petct/mri等模式医学图像;面绘制过程包括区域生长、阈值设定、手动设定、marchingcube重建、拉普拉斯平滑处理,体绘制包括rayingcasting重建、手动划分、alpha设定、纹理映射。
作为进一步优选,所述的重建后人体模型主要保留皮肤轮廓、穿刺手术部位毗邻骨骼、上下腔主动脉、肿瘤脏器、肿瘤脏器内部动、静脉血管。
作为优选,所述的目标肿瘤图像分割采用手动加阈值分割方法。通过观察图像的灰度值及各器官组织的区域分布,使用手动分割的方法,先粗略的提取出完整的肿瘤区域,从而减少处理的数据量,再通过阈值分割更进一步的对手动分割提取的区域细化处理,去除多余的邻近组织和血管,得到更精确的肿瘤区域。
作为优选,所述的肿瘤整体的异质性分布,细化为肿瘤表面和肿瘤内部异质性。
作为进一步优选,通过分析重建后三维肿瘤表面的法线特征获取肿瘤纹理特征,获得其表面平滑程度和与周围组织的粘连范围,从而表征肿瘤外表面异质性,为引导穿刺活检提供肿瘤表面的最优穿刺平面。
作为进一步优选,通过定量分析分割后肿瘤图像灰度值梯度变化规律,获得肿瘤内部异质性特征,并提取肿瘤内部异质性最强点,绘制肿瘤异质性分布四维可视化热图,作为活检穿刺手术的目标靶点。
作为优选,所述的穿刺路径为穿刺点到肿瘤内部异质性最强靶点最优距离;所述的最优距离是避开患者重要脏器、骨骼、神经、血管,肿瘤脏器内部血管等重要功能性部位的最短距离。
作为进一步优选,所述的穿刺路径规划是指,根据病人个体解剖学结构、肿瘤病灶大小、位置及与其周围血管脏器的定量关系,结合穿刺手术需要制定穿刺深度、穿刺角度、穿刺点规划,血管避让等方案;其中穿刺深度为从穿刺点皮肤到肿瘤穿刺靶点的最优距离,穿刺角度为穿刺针与穿刺皮肤平面夹角,穿刺点为活检手术开始穿刺起始点,血管避让为穿刺过程中尽量并避免出血情况发生。
作为优选,所述的三维图像融合包括基于图像的融合及基于红外传感器的融合配准。
作为进一步优选,所述的基于图像的融合方案通过二维码及图像标定,将重建的肿瘤及躯干与真实患者躯干融合;所述的基于红外传感器的融合配准通过将标定的红外传感器作为配准的参照。
作为优选,所述的术中ar导航是指通过增强现实技术,通过头盔、虚拟眼镜、投影等增强现实观看设备,将融合后的图像呈现在手术医生眼前,从而指导进行肿瘤精准穿刺活检手术。
附图说明
图1.为本发明方法的步骤示意图;
图2.为非小细胞肺癌(nsclc)术前ct图(0.51*0.51*0.5mm);
图3.为nsclc患者三维立体重建图(面重建);
图4.为肿瘤ct图像帧定量分析;
图5.为肿瘤内部异质性四维热图定量重建;
图6.为ar导航模式下肿瘤穿刺活检界面。
具体实施方式:
下面结合附图对本发明作详细说明。如图1本发明结构示意图所示,下面以肺部肿瘤中的非小细胞肺癌(nsclc)穿刺活检手术,作为具体实施方案进行进一步描述,但不作为本发明的限定:
图1.为本发明方法的步骤示意图,具体包括:患者术前ct重建(1),目标肿瘤图像分割(2),肿瘤内部异质性四维热图重建(3),穿刺路径规划(4),三维图像配准(5),术中ar导航(6),其中:
(1)患者术前ct重建
如图2为非小细胞肺癌(nsclc)穿刺活检手术ct图像,通过调用vtk可视化sdk中marchingcube算法,将患者影像进行三维重建;再通过专业胸外科专业医生通过区域划分、阈值限定、以及手动划分对生成的数据重复评估矫正;呼吸系统空间位置不变情况下,进行平滑处理及纹理渲染,包括:细分网格,拉普拉斯平滑处理,光照、透明度调节,着色(shader)以及不同结构的分层渲染等,最终所的模型如图3所示,包括外层皮肤(半透明)、骨骼(黄色)、肺(粉红色)、主动脉、静脉(深红色)以及非小细胞肺部肿瘤(黑色)。
(2)目标肿瘤图像分割
通过观察图像的灰度值及各器官组织的区域分布,将含有肺部肿瘤细节特征的ct图像帧进行特殊处理;首先使用手动分割的方法,先粗略的提取出完整的肿瘤区域,从而减少处理的数据量;再通过阈值分割更进一步的对手动分割提取的区域细化处理,去除多余的邻近组织和血管,得到更精确的肺部肿瘤区域。如图4为分割后用于下一步定量分析肺部肿瘤内部异质性的ct图像。
(3)肿瘤内部异质性四维热图重建
肺部肿瘤的四维数据是指肿瘤“空间三维细节+异质性”,这里包括非小细胞肿瘤的表面特性、空间体积、最大直径和肿瘤内部异质性。我们通过重建后三维肿瘤表面的法向量特征获取肿瘤纹理特征,获得其表面平滑程度和与周围组织的粘连范围,从而表征肿瘤表面异质性,为引导穿刺活检提供肿瘤表面的最优穿刺平面;通过定量分析分割后肿瘤图像灰度值梯度变化规律,获得肿瘤内部异质性特征,并提取肿瘤内部异质性最强点,绘制肿瘤异质性分布四维可视化热图,作为活检穿刺手术的目标靶点。如图5为非小细胞肺癌患者重建后的肿瘤四维热图。其中p’和q’即为通过定量影响分析后的肿瘤内部异质性最强的穿刺靶点。
(4)穿刺路径规划
医师通过病人个体解剖学结构、肿瘤病灶大小、位置及与其周围肺动脉、肺静脉、气管的定量关系,结合穿刺手术制定穿刺深度、穿刺角度、穿刺点规划,血管避让方案;其中穿刺深度规划,这里肺部肿瘤两名患者的规划路径分别是在7、8肋骨之间和4、5肋骨之间,在避开肺动脉、静脉前提下,从穿刺点皮肤到肿瘤穿刺靶点的最小距离分别为11.3cm和12.1cm,预测激发活检深度为1.5cm-2.2cm;进针角度为斜进针67度和垂直进针,穿刺角度活检针型号为18g巴德活检针。
(5)三维图像配准
肺部肿瘤三位配准通过在患者身上安放红外传感器进行融合标定,我们设置了19个红外传感器,其中在肺部穿刺过程中16个被系统识别并标定,融合精度为6.7mm,从而将重建的肿瘤及躯干与真实患者躯干融合。
(6)术中ar导航
连接外部增强现实设备(htcvive),将手术图像实时传送至具有立体显示功能的头盔或大屏幕投影显示,用以沉浸感操作及手术教学;如图6所示为通过增强显示头盔呈现在医生眼前的融合景象。手术规划路径、肿瘤特征等都可以实时呈现在医生眼前。
以上仅为本发明的一种实施方案,应当指出,对于技术领域的普通技术人员来说,在不脱离本发明原理前提下的改进和润色,都视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!