具有缓解老年皮肤干裂瘙痒功效的外用植物提取物、化妆品及其制备方法与流程
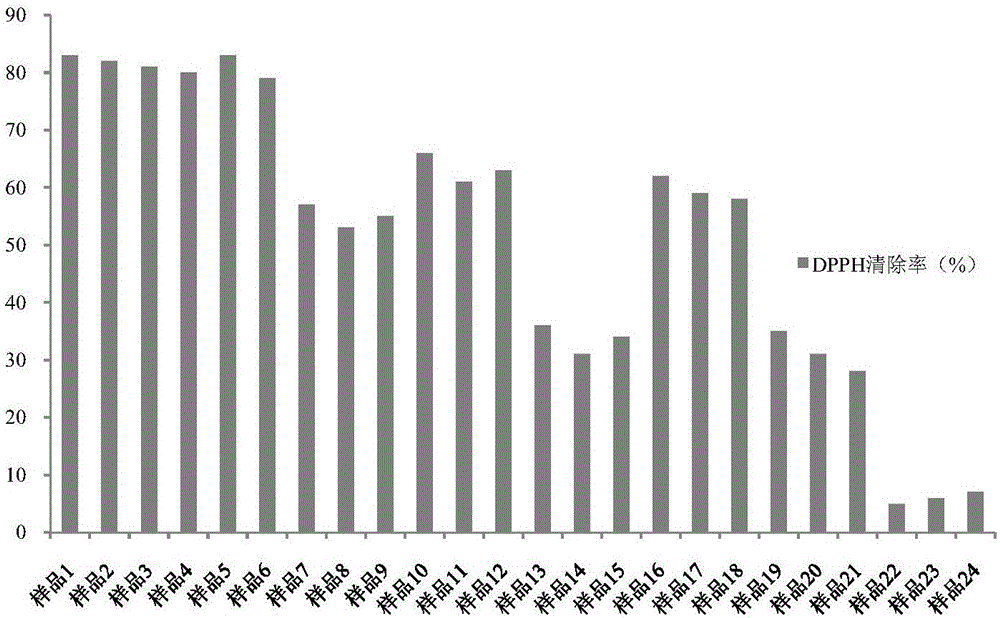
本发明涉及一种外用植物提取物及其制备方法,具体地说是一种具有缓解老年皮肤干裂瘙痒功效的外用植物提取物及由该植物提取物制备得到的化妆品。
背景技术:
:老年皮肤由于皮脂腺萎缩,皮脂分泌减少,皮肤表面ph升高,皮肤屏障受损,导致老年皮肤出现干燥、瘙痒、龟裂等症状。中医认为老年皮肤干燥瘙痒属血虚风燥,用药宜养血润燥,祛风止痒。目前现有市售相关产品均以保湿为主,无法从根本缓解和治疗老年皮肤瘙痒。如何获得一种对老年皮肤干裂瘙痒具有优异缓解功效及天然无刺激的植物提取物为本领域技术人员研究的热点。植物提取物作为化妆品添加剂有诸多优势,如植物提取物成分天然、刺激性低和功效卓越等,因此,植物提取物作为功效添加剂在化妆品中的应用日益增多。植物原料中的功效成分有脂肪酸、甾醇、木脂素、酯类、多烯类、吡咯衍生物、酮类、醌类等油溶性成分,除此之外还会含有一些像糖类、氨基酸、蛋白质等非油溶性物质。目前植物提取物在化妆品领域应用受困的主要原因有(1)提取效率过低,由于植物原料的特性,提取效果过低造成提取成本的增加,因此很多企业优先选择低成本的合成化学原料来代替天然植物原料,以增加经济效益。(2)植物原料提取物的稳定性不佳。植物原料在添加进化妆品各剂型中,往往稳定性不好,在储存和运输过程中易出现变质、析出或沉淀的现象,不仅使产品腐坏率增加造成成本增加,还会直接影响功效,造成消费者使用感受下降。尤其是对于油剂型化妆品来说,油剂型化妆品对澄清度有极高的要求,一旦出现轻微析出和沉淀即会影响产品质量及性能。因此目前化妆品企业急需一种适用于工业生产的,提取率高、提取物稳定性好的植物提取物制备工艺。对现有植物原料功效成分的提取方法介绍如下,目前现有制备工艺有以下几种:1.浸泡提取花草浸泡油具有悠久的应用历史,古埃及人和古希腊人已经学会用油脂吸收花瓣和药草的气味,作为药物或化妆品使用。浸泡油常用植物油做为溶剂,原料与油脂的比例约为1:3(v/v),常温浸泡,需要反复投料2~3次,浸泡时间需要1~3个月。浸泡油在化妆品油剂型中使用时有较好的兼容性,但是此种方法提取效率低,提取时间较长不利于工业生产。2.油脂直接高温提取普济方、太平圣惠方等古籍中,记载了诸多油膏,以中药并油、脂煎焦去滓,用于治疗皮肤疾病或美容。至今民间仍保留了许多经方、验方,将麻油烧热煎煮中药得到药油,用于缓解皮肤的各种不适症状。所以使用油脂直接高温煎煮也是传统提取方法之一,但是此种方法比较原始、提取效率低、不能有效提取植物中的活性成分,耗时长,物料浪费严重,提取效率低等严重制约了工业化生产。3.水蒸气蒸馏法水蒸气蒸法是植物精油提取常用的方法,但是此种方法只适用于提取植物中芳香类的易挥发性成分,而不挥发性成分则无法提取利用。4.溶剂法提取溶剂提取是生产植物提取物的常用方法,一般以乙醇、丙酮、氯仿等作为溶剂,具有设备简单,提取率高等特点。但此方法制备的提取物,对化妆品剂型要求较高,不适合添加入所有剂型,尤其是在油剂型化妆品中的溶解性较差,使得植物提取物加入纯油剂化妆品中后会有沉淀析出,严重影响产品质量,制约了其在纯油剂型化妆品中的应用。5.超临界提取超临界提取是近年兴起的新技术,提取溶剂时超临界流体,一般为超临界co2,具有无毒无害,提取率高,提取物纯度高等优点。但设备复杂、投入成本高,提取成本高,使得工业化大批量生产受限。且超临界提取得到的提取物一般与油脂的兼容性差,影响其在油剂型化妆品中的应用。上述现有方法存在诸多缺陷,受提取效率的限制,制备成本过高,有机溶剂排放造成环境污染等问题也日渐凸显。因此,本领域急需解决上述用于化妆品和护理产品添加的植物提取物制备中存在的问题。技术实现要素:本发明的首要目的在于提出一种具有缓解老年皮肤干裂瘙痒功效的植物提取物。本发明的第二目的在于提出一种提取效率高,提取物性质稳定的植物提取物的制备方法。本发明的第三目的在于提出由上述植物提取物制备得到的化妆品。本发明的发明思路为:本发明选择的组合物利用“君、臣、佐、使”的组方原则,将五种植物进行配伍,各组分协同起效,通过清热消炎、祛风止痒、固护屏障、养阴生津,达到滋润肌肤,缓解干燥、瘙痒、龟裂的目的,结合对制备方法的改进,显著增加了活性成分的提取效率,从而得到一种高效的植物提取物。为实现本发明的目的,本发明采用如下技术方案:一种具有缓解老年皮肤干裂瘙痒功效的外用植物提取物,其中,所述外用植物提取物由下述重量份配比的原料经下述方法制备而成:(1)按照下述重量份配比称取各原料,混匀;牛蒡子1~10、野菊花1~10、地肤子1~10、五味子1~10、绿豆1~10;(2)第一次提取:按照料液比为1:10~100m/m混合原料和溶剂一,40~90℃条件下提取0.5~2h;本发明所用溶剂一为乙醇、氯仿和丙酮中的一种或多种的混合。料液比与提取温度对提取效率及提取成本有至关重要的影响,针对提取溶剂一的理化性质选择与其更匹配的料液比和提取参数不仅可以提高提取效率,还可以增强与下步溶剂二提取的协同性。本发明料液比范围内植物原料与溶剂一接触更充分,植物原料中的活性成分更易被提取,提取效率更高的同时不会造成溶剂及植物原料的浪费,提取成本更经济。优选的第一次提取料液比范围值为1:10~50m/m,此范围内提取效果更好,且与溶剂二协同性更强。本发明提取温度和时间优选40~90℃条件下提取0.5~2h。提取温度和时间直接影响提取物性质,不恰当的提取温度和时间可能造成提取过程中植物原料的氧化变性、挥发性成分的损失及热敏性成分性质改变等,此范围内提取物功效成分在溶剂内的溶解性及物质交换速率均最佳,提取物功效优异且稳定。上述步骤(2)的条件参数更适合于下述步骤(3)配合,可与步骤(3)产生协同增效的功效。(3)第二次提取:按照料液比为1:10~100m/m加入溶剂二,40~90℃条件下提取0.5~2h;本发明所用溶剂二为下述原料中的一种或多种的混合,分别是:白油,运动粘度(40℃)≤30cst,推荐采用白油3#、5#、7#、10#、15#、26#;氢化聚异丁烯,运动粘度(40℃)≤30cst,推荐采用氢化聚异丁烯parleam6、parleamex;氢化聚癸烯,运动粘度(40℃)≤30cst,推荐采用氢化聚癸烯pao2、pao4、pao6;辛酸/癸酸甘油三酯、异硬脂酸异硬脂醇酯和植物油。植物油推荐采用大豆油、向日葵籽油、芝麻油、澳洲坚果油、甜杏仁油、橄榄油、葡萄籽油、燕麦油、茶油中的一种或多种的混合。溶剂二和溶剂一的配合对本发明技术效果尤为重要,发明人经实验验证,两溶剂之间不能完全互溶,完全互溶虽然可以保证较好的提取效率,但添加进化妆品中稳定性不好,易出现析出沉淀等不良情况。两溶剂也不能完全不互溶,两溶剂不互溶则不能起到协同增效的作用,提取效率非常低且提取物稳定性差。因此溶剂一和溶剂二部分互溶技术效果最佳,为了使两溶剂配合提取效率更高提取成本更经济,发明人将第二次提取的温度和时间控制在上述条件参数范围内,不仅可以同时提高溶剂一和溶剂二部分互溶共同提取的提取效果,还可以有效避免提取效率趋于缓慢增加提取成本等问题。根据溶剂二特性,提取温度不宜过高,控制在90℃以下最佳,温度也不宜过低,低于40℃会影响功效成分在溶剂二内的溶解性以及溶剂一与溶剂二的相溶性,进而影响提取效率。根据上述方法的描述,溶剂一和溶剂二的选择尤为重要,二者配合需要协同增效提高植物原料的提取效率,并且为了适应工业生产,提取过程需短,提取物品质需高即添加稳定性好,提取成本也需较低。因此,本发明发明人经实验验证发现,如果本发明溶剂二极性大于溶剂一,提取效率及提取物稳定性均较差。发明人惊喜的发现如果溶剂一比溶剂二极性更强,溶剂一和溶剂二在一定条件下可部分互溶,此特点可增强活性成分在溶剂二中的溶解性,使得某些原本不溶于油脂,或者在油脂中溶解性差的物质能够很好的溶解在溶剂二中。二者配合提取,即可满足上述化妆品植物原料提取所需的所有条件,极大的提高了植物活性成分的提取效率,得到的提取物性质稳定,与化妆品其他原料兼容性极佳。本发明可以选择上述记载的诸多溶剂中的一种进行单一溶剂提取,也可以根据实际提取的植物原料特性进行多溶剂的复配提取,溶剂之间复配比例可以根据本领域技术人员经验或者实际需要任意比例复配,无具体限定。因为溶剂二的特性,水对溶剂二的稳定性影响巨大,所以溶剂一优选无水体系,以乙醇为例,优选无水乙醇。本发明溶剂二选择极性较溶剂一弱的提取溶剂,温和无刺激,与植物原料中的功效成分相容性好。溶剂二可以选择上述记载的诸多溶剂中的一种进行单一溶剂提取,也可以根据实际提取的植物原料特性进行多溶剂的复配提取,溶剂之间复配比例可以根据本领域技术人员经验或者实际需要任意比例复配,无具体限定。上述步骤(3)中第二次提取料液比较佳范围值为1:10~50m/m。(4)去除溶剂一;本领域技术人员公知的可去除溶剂的方法均可应用在此,本发明推荐的较佳方法是:在40~80℃减压浓缩至溶剂一完全去除,减压范围一般控制在0.01mpa至负0.15mpa。溶剂一可能对皮肤有一定刺激性,去除溶剂一可以使产品性能更加温和,安全无毒副作用。溶剂一还可以采用膜浓缩、超滤、反渗透、渗透气化等方式脱除。(5)精滤至澄清;此步骤的目的是使最终提取物更加稳定澄清,精滤过程使用的是0.2~10μm孔径的滤板进行过滤。为了更有利于上述减压浓缩和精滤步骤的进行,并且更好的保护减压浓缩及精滤设备,在步骤(3)和步骤(4)之间还可以增加粗滤步骤,粗滤的条件是60~100目粗滤,滤去原料渣。为了保持过滤料液的稳定,粗滤之前还可以增加冷却步骤,将料液冷却至40℃或40℃以下再进行粗滤最佳。植物原料在第一次提取之前还可以进行预处理,预处理的目的是为了使提取溶剂更容易渗透细胞壁,进一步提高提取效率。预处理的步骤不是必须的,本发明提取率高主要取决于溶剂一和溶剂二的配合以及针对溶剂一二所使用的工艺步骤及参数,预处理可以在本发明所达到的提取率的基础上进一步缩短提取时间,但对于不便于预处理的植物原料也可以不使用预处理步骤。发明人推荐的预处理的步骤如下述,其他本领域技术人员公知的可实现预处理目的的步骤也可应用于此。(1)粗粉碎:将原料粉碎至20~60目;粉碎步骤可利用本领域公知的粉碎设备进行,如切割机、破壁机、粉碎机等,粉碎步骤可以一次性完成,也可以分步骤由粗至细逐步完成。(2)高温高压处理,此处所述的高温一般为至少等于或高于100℃的温度,本发明控制在100~130℃为宜。高压指0.1mpa以上,控制在0.1~0.2mpa范围内效果最佳。处理时间不宜过长,控制在30min以内为佳。植物细胞壁的主要成分是纤维素和果胶,本发明采用高温高压预处理原料,是利用水蒸气破坏多糖分子间的氢键,使细胞壁结构松散,更有利于后续提取过程中溶剂透过细胞壁进入,使提取效率更佳。(3)干燥,干燥的目的是去除高温高压后多余的水汽,更利于后期提取过程的进行和提取物的稳定,在本发明中50~80℃干燥1~2h为佳。其他本领域技术人员公知的干燥手段也可以应用于此。上述植物提取物在制备具有缓解老年皮肤干裂瘙痒功效的化妆品中的应用。一种具有缓解老年皮肤干裂瘙痒功效的化妆品,其中,所述化妆品由上述的植物提取物及化妆品领域常用辅料制成。一种具有缓解老年皮肤干裂瘙痒功效的化妆品,其中,所述化妆品由下述重量份配比的原料制成:向日葵籽油1~10、植物甾醇酯1~10、红没药醇0.1~0.5、权利要求1至6中任意一项所述外用植物提取物75~95、丁羟基甲苯0.1~0.3。一种上述化妆品的制备方法,其中,所述制备方法的步骤如下:(1)按上述配比称取各原料;(2)将植物甾醇酯和丁羟基甲苯加入所述外用植物提取物中,50~60℃下加热搅拌溶解20~40min;(3)降温至30~40℃后加入向日葵籽油和红没药醇,搅拌均匀,即得。上述方法制备得到的是油剂型化妆品,利用本发明植物提取物及护肤品领域常规方法及辅料也可以制备得到其他剂型,如乳液、膏霜、爽肤水、面膜或洗面奶等。本发明制剂推荐使用方法为:以涂抹方法施于人体皮肤表面,轻轻按摩直至吸收。本发明的有益结果:本发明利用牛蒡子、野菊花、地肤子、五味子和绿豆配合且给出了最佳的配伍用量,各组分之间协同起效,结合本发明提出的新的不同极性双溶剂对化妆品植物原料有效提取的方法可以使治疗老年皮肤瘙痒干裂的效果得到极大提升。本发明的发明点之一在于根据对提取溶剂的优化及具体溶剂的选择配合,对提取步骤及提取条件参数的优化,起到了协同起效的功效,进而使提取效率大幅增加。植物提取效率的评测主要通过植物原料的抗氧化和抗炎功效来评价,通过本发明方法提取得到的提取物通过功效实验可以看出在上述两功效方面远远优于现有技术提取得到的提取物。本发明提取方法有效的缩短了提取时间,提取效率大幅高,所用设备常规且低廉,均有效的降低了植物提取物制备成本,本发明非常适合大规模工业化生产。更重要的是,本发明提取得到的植物提取物成分更加稳定,与化妆品各种剂型的辅料兼容性更好,尤其是添加进油剂型化妆品中,有效的改进了现有技术提取物析出及出现沉淀等影响产品质量和功效的缺陷,使得化妆品更易储存运输,产品品质更佳,且使用时效果更佳。附图说明图1为样品1~24提取效果通过dpph清除率评价图;图2为样品25~30提取效果通过dpph清除率评价图;图3为样品31~36提取效果通过dpph清除率评价图;图4为组方筛选实验dpph清除率评价图;图5为组方筛选磷酸组胺致痒阈实验评价图;图6为本发明的止痒功效评价图。具体实施方式为了使本领域技术人员更加详细的了解本发明所述提取方法,发明人提供如下具体实施例,所涉及到的试剂均为本领域内公知且可市售购买获得的,所述涉及到的仪器设备也是本领域的技术人员公知且能够掌握和运用的设备。以下实施例不得理解为任何意义上的对本发明权利要求的限制。本发明具体实施方式中使用的原料和设备购买厂家见表1和表2。表1本发明所用原料表2设备来源实施例1(1)按照下述重量份配比称取各原料,混匀;牛蒡子1g、野菊花3g、地肤子6g、五味子10g、绿豆9g;(2)第一次提取:按照料液比为1:10m/m加入乙醇,混合,60℃条件下提取1h;(3)第二次提取:按照料液比为1:10m/m加入向日葵籽油,60℃条件下搅拌提取1h;(4)40℃减压浓缩至乙醇完全去除;(5)滤板孔径10μm,精滤至滤液澄清,即得。实施例2(1)按照下述重量份配比称取各原料,混匀;牛蒡子10g、野菊花2g、地肤子1g、五味子4g、绿豆6g;(2)第一次提取:按照料液比为1:30m/m加入乙醇,混合,40℃条件下提取2h;(3)第二次提取:按照料液比为1:30m/m加入氢化聚异丁烯(20cst),40℃条件下搅拌提取2h;(4)50℃减压浓缩至乙醇完全去除;(5)滤板孔径1μm,精滤至滤液澄清,即得。实施例3(1)按照下述重量份配比称取各原料,混匀;牛蒡子4g、野菊花1g、地肤子10g、五味子7g、绿豆2g;(2)第一次提取:按照料液比为1:40m/m加入无水乙醇,混合,90℃条件下提取0.5h;(3)第二次提取:按照料液比为1:40m/m加入辛酸/癸酸甘油三酯,90℃条件下搅拌提取0.5h;(4)80℃减压浓缩至乙醇完全去除;(5)滤板孔径0.2μm,精滤至滤液澄清,即得。实施例4(1)按照下述重量份配比称取各原料;牛蒡子8g、野菊花10g、地肤子1g、五味子1g、绿豆9g;(2)粗粉碎:将各原料药粉碎至20目混匀;(3)高温高压处理:0.1mpa,100℃,处理5min;(4)干燥:50℃干燥1h;(5)第一次提取:按照料液比为1:50m/m加入氯仿,混合,55℃条件下提取1.5h;(6)第二次提取:按照料液比为1:50m/m加入白油(7cst),55℃条件下搅拌提取1.5h;(7)40℃减压浓缩至氯仿完全去除;(8)滤板孔径0.2μm,精滤至滤液澄清,即得。实施例5(1)按照下述重量份配比称取各原料;牛蒡子2g、野菊花5g、地肤子2g、五味子4g、绿豆10g;(2)粗粉碎:将各原料药粉碎至40目混匀;(3)高温高压处理:0.2mpa,130℃,处理20min;(4)干燥:60℃干燥2h;(5)第一次提取:按照料液比为1:60m/m加入氯仿,混合,80℃条件下提取1h;(6)第二次提取:按照料液比为1:60m/m加入辛酸/癸酸甘油三酯,80℃条件下搅拌提取1h;(7)60℃减压浓缩至氯仿完全去除;(8)滤板孔径10μm,精滤至滤液澄清,即得。实施例6(1)按照下述重量份配比称取各原料;牛蒡子8g、野菊花3g、地肤子2g、五味子5g、绿豆1g;(2)粗粉碎:将各原料药粉碎至60目混匀;(3)高温高压处理:0.1mpa,100℃,处理30min;(4)干燥:75℃干燥1h;(5)第一次提取:按照料液比为1:70m/m加入氯仿,混合,75℃条件下提取2h;(6)第二次提取:按照料液比为1:70m/m加入氢化聚癸烯(30cst),75℃条件下搅拌提取2h;(7)75℃减压浓缩至氯仿完全去除;(8)滤板孔径6μm,精滤至滤液澄清,即得。实施例7(1)按照下述重量份配比称取各原料;牛蒡子2g、野菊花7g、地肤子9g、五味子3g、绿豆4g;(2)粗粉碎:将各原料药粉碎至30目混匀;(3)高温高压处理:0.2mpa,130℃,处理15min;(4)干燥:70℃干燥1h;(5)第一次提取:按照料液比为1:80m/m加入丙酮,混合,65℃条件下提取1h;(6)第二次提取:按照料液比为1:80m/m加入异硬脂酸异硬脂醇酯,65℃条件下搅拌提取1h;(7)45℃减压浓缩至丙酮完全去除;(8)滤板孔径2μm,精滤至滤液澄清,即得。实施例8(1)按照下述重量份配比称取各原料;牛蒡子4g、野菊花6g、地肤子2g、五味子7g、绿豆1g;(2)粗粉碎:将各原料药粉碎至50目混匀;(3)高温高压处理:0.1mpa,120℃,处理25min;(4)干燥:60℃干燥1h;(5)第一次提取:按照料液比为1:90m/m加入丙酮,混合,65℃条件下提取1.5h;(6)第二次提取:按照料液比为1:90m/m加入大豆油,65℃条件下搅拌提取1.5h;(7)50℃减压浓缩至丙酮完全去除;(8)滤板孔径4μm,精滤至滤液澄清,即得。实施例9(1)按照下述重量份配比称取各原料,混匀;牛蒡子1g、野菊花4g、地肤子7g、五味子3g、绿豆2g;(2)粗粉碎:将各原料药粉碎至50目混匀;(3)高温高压处理:0.2mpa,125℃,处理20min;(4)干燥:65℃干燥2h;(5)第一次提取:称取粗粉碎后的样品,按照料液比为1:100m/m加入氯仿乙醇混合液(氯仿乙醇按照质量比1:1复配),混合,80℃条件下提取2h;(6)第二次提取:按照料液比为1:100m/m加入芝麻油,80℃条件下搅拌提取2h;(7)55℃减压浓缩至溶剂一完全去除;(8)滤板孔径8μm,精滤至滤液澄清,即得。实施例10(1)按照下述重量份配比称取各原料,混匀;牛蒡子10g、野菊花9g、地肤子10g、五味子9g、绿豆5g;(2)粗粉碎:将各原料碎至40目,混匀;(3)高温高压处理:0.2mpa,110℃,处理30min;(4)干燥:60℃干燥1.5h;(5)第一次提取:按照料液比为1:30m/m加入乙醇,混合,80℃条件下提取1h;(6)第二次提取:按照料液比为1:20m/m加入辛酸/癸酸甘油三酯,70℃条件下搅拌提取2h;(7)冷却至40℃以下,60目粗滤;(8)60℃减压浓缩至溶剂一完全去除;(9)冷却至40℃以下,滤板孔径1μm,精滤至滤液澄清,即得。实施例11(1)按照下述重量份配比称取各原料,混匀;牛蒡子10g、野菊花2g、地肤子5g、五味子2g、绿豆10g;(2)粗粉碎:将各原料粉碎至50目混匀;(3)高温高压处理:0.1mpa,120℃,处理15min;(4)干燥:75℃干燥1h;(5)第一次提取:按照料液比为1:45m/m加入氯仿和丙酮混合溶剂(二者之间按照质量比1:1复配),混合,90℃条件下提取1h;(6)第二次提取:按照料液比为1:35m/m加入辛酸/癸酸甘油三酯和氢化聚癸烯(17cst)复配物(二者按照质量比1:1复配),70℃条件下搅拌提取1h;(7)冷却至40℃以下,80目粗滤;(8)70℃减压浓缩至溶剂一完全去除;(9)冷却至40℃以下,滤板孔径1μm,精滤至滤液澄清,即得。实施例12(1)按照下述重量份配比称取各原料,混匀;牛蒡子3g、野菊花6g、地肤子2g、五味子1g、绿豆7g;(2)粗粉碎:将各原料粉碎至60目;(3)高温高压处理:0.1mpa,130℃,处理10min;(4)干燥:80℃干燥1.5h;(5)第一次提取:按照料液比为1:55m/m加入乙醇和丙酮混合溶剂(二者之间按照1:1复配),混合,80℃条件下提取1h;(6)第二次提取:按照料液比为1:65m/m加入橄榄油和澳洲坚果油复配物(二者按照质量比1:1复配),60℃条件下搅拌提取1h;(7)冷却至40℃以下,100目粗滤;(8)80℃减压浓缩至溶剂一完全去除;(9)冷却至40℃以下,滤板孔径6μm,精滤至滤液澄清,即得。实施例13(1)按照下述重量份配比称取各原料,混匀;牛蒡子5g、野菊花2g、地肤子1g、五味子10g、绿豆3g;(2)粗粉碎:将各原料粉碎至30目;(3)高温高压处理:0.1mpa,100℃,处理30min;(4)干燥:60℃干燥1h;(5)第一次提取:按照料液比为1:20m/m加入氯仿和乙醇混合溶剂(二者之间按照质量比1:1复配),混合,70℃条件下提取1h;(6)第二次提取:按照料液比为1:10m/m加入白油(16cst)和氢化聚异丁烯(11cst)混合溶剂(二者按照质量比1:1复配),70℃条件下搅拌提取1h;(7)冷却至40℃以下,90目粗滤;(8)80℃减压浓缩至溶剂一完全去除;(9)冷却至40℃以下,滤板孔径5μm,精滤至滤液澄清,即得。实施例14(1)按照下述重量份配比称取各原料,混匀;牛蒡子2g、野菊花1g、地肤子7g、五味子5g、绿豆9g;(2)粗粉碎:将各原料粉碎至40目;(3)高温高压处理:0.2mpa,120℃,处理10min;(4)干燥:70℃干燥1h;(5)第一次提取:按照料液比为1:60m/m加入乙醇,混合,90℃条件下提取1h;(6)第二次提取:按照料液比为1:50m/m加入葡萄籽油和燕麦油混合溶剂(二者按照质量比1:1复配),50℃条件下搅拌提取1.5h;(7)冷却至40℃以下,90目粗滤;(8)80℃减压浓缩至溶剂一完全去除;(9)冷却至40℃以下,滤板孔径5μm,精滤至滤液澄清,即得。实施例15(1)按照下述重量份配比称取各原料,混匀;牛蒡子9g、野菊花3g、地肤子1g、五味子2g、绿豆5g;(2)粗粉碎:将各原料粉碎至40目;(3)高温高压处理:0.2mpa,130℃,处理10min;(4)干燥:70℃干燥1h;(5)第一次提取:按照料液比为1:30m/m加入氯仿,混合,60℃条件下提取1h;(6)第二次提取:按照料液比为1:90m/m加入甜杏仁油,80℃条件下搅拌提取1h;(7)冷却至40℃以下,90目粗滤;(8)80℃减压浓缩至溶剂一完全去除;(9)冷却至40℃以下,滤板孔径0.5μm,精滤至滤液澄清,即得。实施例16具有缓解老年皮肤干裂瘙痒功效的油剂型化妆品(1)按照下述配比称取各原料;向日葵籽油1g、植物甾醇酯10g、红没药醇0.3g、实施例1制备植物提取物95g、丁羟基甲苯0.2g(2)将植物甾醇酯和丁羟基甲苯加入所述外用植物提取物中,50℃下加热搅拌溶解40min;(3)降温至30℃后加入向日葵籽油和红没药醇,搅拌均匀,即得。实施例17具有缓解老年皮肤干裂瘙痒功效的油剂型化妆品(1)按照下述配比称取各原料;向日葵籽油9g、植物甾醇酯1g、红没药醇0.5g、实施例10制备植物提取物75g、丁羟基甲苯0.1g(2)将植物甾醇酯和丁羟基甲苯加入所述外用植物提取物中,60℃下加热搅拌溶解30min;(3)降温至35℃后加入向日葵籽油和红没药醇,搅拌均匀,即得。实施例18具有缓解老年皮肤干裂瘙痒功效的油剂型化妆品(1)按照下述配比称取各原料;向日葵籽油10g、植物甾醇酯6g、红没药醇0.1g、实施例15制备植物提取物80g、丁羟基甲苯0.3g(2)将植物甾醇酯和丁羟基甲苯加入所述外用植物提取物中,55℃下加热搅拌溶解20min;(3)降温至40℃后加入向日葵籽油和红没药醇,搅拌均匀,即得。本发明功效实验本发明溶剂一和溶剂二的配合,结合本发明优化的提取工艺及提取参数,可起到协同增效的功效,使得提取率更高,提取物性质更优异更稳定,提取成本更低,适合工业化应用。虽然本发明的溶剂一和溶剂二均属于本领域公知提取溶剂,但本发明所用溶剂一和溶剂二配合提取在现有技术中无记载,原因是两溶剂配合提取存在诸多问题,如极性选择错误,互溶度不佳或工艺步骤条件参数选择错误将直接影响提取产品的稳定性及提取效率等,因此本发明并非现有技术的简单结合。下面利用功效实验对本发明做进一步详细说明。一、本发明溶剂一和溶剂二的选择1、溶剂一选择植物提取常用的,与各类活性成分兼容性好,提取率高,具有代表性的溶剂;考虑到实验证实的溶剂一极性应大于溶剂二提取效果最好,故最终确定为乙醇、丙酮和氯仿。发明人认为上述技术效果已经达到本发明要求故不必再进行进一步溶剂一的筛选,这样也是为了减少溶剂二选择时的工作量。2、溶剂二的选择过程简述:溶剂二选择极性小于溶剂一的溶剂,以油脂类为佳。(1)植物油:各植物油性质相似,故仅选一种为代表,分别与溶剂一的三种溶剂复配提取,均有较好的效果;(2)白油:选择限定粘度范围内和范围外的两种白油(一般为临界值附近的数值,如26和32),分别与溶剂一的三种溶剂复配提取,粘度范围内的白油效果好,范围外的效果不好;(3)氢化聚异丁烯、氢化聚癸烯:这两种都是烯烃聚合物,仅选择一种为代表,重复白油筛选的工作,即选择限定粘度范围内和范围外的,(一般为临界值附近的数值,如26和32)分别实验,得到不同的提取效果;(4)辛酸/癸酸甘油三酯:与溶剂一的三种溶剂复配提取,均有较好的效果;(5)异硬脂酸异硬脂醇酯:与溶剂一的三种溶剂复配提取,均有较好的效果;(6)聚二甲基硅氧烷(硅油):硅油是硅链,对碳链的活性成分溶解效果差,分别与溶剂一复配,提取效果均不好。以上是溶剂筛选部分的实验思路,即溶剂选择部分的样品1~24。样品1~24的原料及制备方法相同,只是提取溶剂不同。具体制备方法如下:(1)按照下述重量份配比称取各原料,混匀;牛蒡子10g、野菊花9g、地肤子10g、五味子9g、绿豆5g;(2)粗粉碎:将各原料粉碎至40目,混匀;(3)高温高压处理:0.20mpa,110℃处理30min;(4)干燥:60℃干燥1.5h;(5)第一次提取:按照料液比为1:30m/m加入溶剂一,混合,80℃条件下提取1h;(6)第二次提取:按照料液比为1:20m/m加入溶剂二,70℃条件下搅拌提取2h;(7)冷却至40℃以下,60目粗滤得滤液;(8)60℃减压浓缩至溶剂一完全去除;(9)冷却至40℃以下,精滤至滤液澄清,即得。样品1~24所用溶剂见表3表3样品溶剂表3.测试结果:本部分内容是对溶剂二的筛选,溶剂一固定为乙醇、氯仿、丙酮。(1)dpph清除自由基实验:植物提取物的成分复杂,对于提取物有效成分的分析及定量比较困难,因此本领域技术人员通过对抗氧化活性检测来评定有效成分提取的效率,往往提取效率好的工艺制备得到的提取物会有更优异的抗氧化活性功效。抗氧化活性一般采用dpph自由基清除实验评价。dpph(2,2-联苯基-1-苦基肼基)是一种稳定存在的有机氮自由基,广泛应用于体外抗氧化剂能力研究。基于dpph在515nm左右有特征吸收峰,抗氧化剂提供氢原子将dpph上的单电子还原使其颜色减弱,据其吸光值的减少量来评价自由基的清除程度。样品1~24抗氧化活性实验结果见图1。(2)稳定性实验,见表4。表4不同溶剂提取样品的稳定性比较实验结果:1.样品1~3为植物油(植物油性质相似,仅以向日葵籽油为例)分别与溶剂一复配提取,植物油与乙醇、丙酮、氯仿复配,均有良好的提取效果。2.样品4~6为辛酸/癸酸甘油三酯分别与乙醇、丙酮、氯仿复配提取,均有良好的提取效果。3.样品7~9为异硬脂酸异硬脂醇酯分别与乙醇、丙酮、氯仿复配提取,均有较好的提取效果。4.样品10~12是白油(26cst,符合本发明限定的运动粘度≤30cst的要求)分别与乙醇、丙酮、氯仿复配提取,均有较好的提取效果。5.样品13~15是白油(32cst,不符合本发明限定的运动粘度≤30cst的要求)分别与乙醇、丙酮、氯仿复配提取,提取效果都较差。6.样品10~15是将运动粘度≤30cst的白油,与运动粘度>30cst的白油作对比,通过提取效果的差异,说明选择运动粘度≤30cst白油的原因。7.样品16~18是氢化聚癸烯(30cst,符合本发明限定的运动粘度≤30cst的要求)分别与乙醇、丙酮、氯仿复配提取,均有较好的提取效果。8.样品19~21是氢化聚癸烯(46cst,不符合本发明限定的运动粘度≤30cst的要求)分别与乙醇、丙酮、氯仿复配提取,提取效果都较差。9.样品16~21与白油类似,是将运动粘度≤30cst的氢化聚癸烯,与运动粘度>30cst的作对比,通过提取效果的差异,说明选择运动粘度≤30cst氢化聚癸烯的原因。另外,氢化聚癸烯和氢化聚异丁烯都是聚合物,因此仅以氢化聚癸烯为例进行说明。10.样品22~24是聚二甲基硅氧烷(硅油,pmx200,6cst)分别与乙醇、丙酮、氯仿复配提取,由于硅油是硅链结构,对碳链的活性成分溶解效果差,因此提取效果均很差,表现为dpph清除率极低;由于兼容性差,导致其稳定性也不好,表现为样品混浊或活性成分析出(沉淀)。通过上述实验,本发明优选出的溶剂二包括植物油(样品1~3),辛酸/癸酸甘油三酯(样品4~6),异硬脂酸异硬脂醇酯(样品7~9),运动粘度(40℃)≤30cst的白油(样品10~12),运动粘度(40℃)≤30cst的氢化聚异丁烯(与氢化聚癸烯同为烯烃聚合物,仅以氢化聚癸烯为例进行实验),运动粘度(40℃)≤30cst的氢化聚癸烯(样品16~18)。本发明作为对比反例的溶剂二包括运动粘度(40℃)>30cst的白油(样品13-15),运动粘度(40℃)>30cst的氢化聚癸烯(样品19-21),6cst聚二甲基硅氧烷pmx200(样品21-24)。根据上文中的对比实验可知,通过分别和溶剂一(乙醇、丙酮、氯仿)进行复配提取,植物油,辛酸/癸酸甘油三酯,异硬脂酸异硬脂醇酯,运动粘度(40℃)≤30cst的白油、氢化聚异丁烯和氢化聚癸烯,均具有较好的提取效果,且提取后的产品稳定性好,适合作为本发明的溶剂二,与溶剂一配合,实现本发明中的提取工艺。而运动粘度(40℃)>30cst的白油、氢化聚异丁烯和氢化聚癸烯,由于粘度增大,不利于提取过程中的物质传递,导致提取效果不理想,不适合作为本发明的溶剂二。硅油(聚二甲基硅氧烷)由于结构差异,与植物中的碳链活性成分相容性不好,进而导致提取效率低,且提取后的产品稳定性差,也不适合作为本发明的溶剂二使用。二、本发明提取参数的确定1.第二次提取温度选择实验:第二步是溶剂一溶剂二协同提取,因此此步骤提取至关重要,第二步提取温度直接影响到两溶剂的互溶程度及提取效率。在本实验中溶剂一以乙醇为例,溶剂二以辛酸癸酸甘油三酯为例。具体制备工艺如实验一,具体步骤如下:(1)按照下述重量份配比称取各原料,混匀;牛蒡子10g、野菊花9g、地肤子10g、五味子9g、绿豆5g;(2)粗粉碎:将各原料粉碎至40目;(3)高温高压处理:0.20mpa,110℃处理30min;(4)干燥:60℃干燥1.5h;(5)第一次提取:按照料液比为1:30m/m加入乙醇,混合,80℃条件下提取1h;(6)第二次提取:按照料液比为1:20m/m加入辛酸癸酸甘油三酯,提取温度具体见表5,搅拌提取2h;(7)冷却至40℃以下,90目粗滤得滤液;(8)60℃减压浓缩至溶剂一完全去除;(9)冷却至40℃以下,精滤至滤液澄清,即得。表5样品序号步骤(5)提取温度2530℃2640℃2755℃2870℃2990℃3095℃样品25~30提取效果通过dpph清除率评价,实验方法见dpph自由基清除实验。结果见图2。可见,在提取物温度在40~90度之间提取效率最高,低于40℃或高于90℃的情况下提取效率过低,如果采用不良温度只能通过延长提取时间来提高提取率,那么会影响提取工艺在工业应用上的经济效益。样品25~30的稳定性实验方法见稳定性比较,结果见表6所示。表6不同温度提取样品的稳定性比较本部分内容是对第二步提取的工艺参数筛选,以温度为例,比较了30℃、40℃、55℃、70℃、90℃和95℃六个温度条件下,产品的dpph和稳定性,40~90℃提取效果(dpph)和稳定性都较好,30℃提取效果差,95℃提取效果较差,由于温度过高,产品的稳定性也较差,出现变色和异味,因此最终的提取温度推荐采用40℃~90℃范围,最佳提取温度是70℃。2.第二次提取料液比实验:第二步是溶剂一溶剂二协同提取,此步骤提取至关重要,第二步提取料液比直接影响溶剂一和溶剂二的互溶度,配合提取的提取效率在本实验中溶剂一以乙醇为例,溶剂二以辛酸癸酸甘油三酯为例。具体制备工艺如实验一,具体步骤如下:(1)按照下述重量份配比称取各原料,混匀;牛蒡子10g、野菊花9g、地肤子10g、五味子9g、绿豆5g;(2)粗粉碎:将各原料粉碎至40目;(3)高温高压处理:0.2mpa,110℃处理30min;(4)干燥:60℃干燥1.5h;(5)第一次提取:按照料液比为1:30m/m加入乙醇,混合,80℃条件下提取1h;(6)第二次提取:按照表7料液比加入辛酸癸酸甘油三酯,70℃条件下搅拌提取2h;(7)冷却至40℃以下,90目粗滤得滤液;(8)60℃减压浓缩至溶剂一完全去除;(9)冷却至40℃以下,精滤至滤液澄清,即得。表7样品序号步骤(5)料液比311:2321:10331:20341:50351:100361:150样品31~36提取效果通过dpph清除率评价,实验方法见dpph自由基清除实验。结果见图3。可见,在料液比为1:10~100提取效率高,且在1:10~50提取效率高。三、本发明组合物的各原料药及配伍选择优化本发明原料药的选择思路:本发明选择的组合物按照“君、臣、佐、使”的组方原则,通过君药、臣药清热、疏风、止痒,佐药收敛固涩、养阴生津,使药清热消炎,加强君、臣药物功效,达到滋润肌肤,顾护屏障,缓解干燥、瘙痒的效果。本实验各样品的制备方法相同,原料药总质量是10g,各样品组方的组分及配伍关系不同,详见表8。具体制备方法步骤如下:(1)按照表8重量份配比称取各原料,混匀;(2)粗粉碎:将各原料粉碎至40目;(3)高温高压处理:0.10mpa,100℃处理30min;(4)干燥:60℃干燥2h;(5)第一次提取:按照料液比为1:30m/m加入乙醇,混合,80℃条件下提取1h;(6)第二次提取:按照料液比为1:20m/m加入辛酸癸酸甘油三酯,70℃条件下提取2h;(7)冷却至40℃以下,60目粗滤得滤液;(8)60℃减压浓缩至溶剂一完全去除;(9)冷却至40℃以下,精滤至滤液澄清,即得。表8样品1~10组方效果通过dpph清除率和磷酸组胺致痒阈值实验评价,实验方法见dpph自由基清除实验和磷酸组胺致痒阈值实验。结果见图4、图5。结果表明,样品7(本发明组方)的组方及用量效果最好,样品1~6、8~12组方效果不佳。四、本发明方法与现有技术方法提取效率比较植物提取物的成分复杂,对于提取物有效成分的分析及定量比较困难,因此本领域技术人员通过对抗氧化活性和抗炎活性的检测来评定有效成分提取的效率,往往提取效率好的工艺制备得到的提取物会有更优异的功效。抗氧化活性一般采用dpph自由基清除实验评价。抗炎活性一般采用抑制透明质酸酶实验评价。透明质酸酶是过敏反应的参与者,有研究表明透明质酸酶与炎症、过敏有强相关性,透明质酸酶体外抑制试验常作为测定抗过敏活性的方法。抗过敏活性以透明质酸酶抑制率为指标,透明质酸酶抑制率越大则抗过敏活性越强。本发明功效实验的样品制备如下述样品1(现有技术油脂两次提取):称取牛蒡子10g、野菊花9g、地肤子10g、五味子9g、绿豆5g,粉碎至40目,0.2mpa,110℃处理30min,60℃干燥1.5h;料液比1:30(m/m),加入辛酸/癸酸甘油三酯,80℃搅拌提取1h;料液比1:20(m/m),再次加入辛酸/癸酸甘油三酯,70℃搅拌提取2h;冷却至40℃以下,滤板孔径1μm,精滤至澄清,即得。样品2(现有技术乙醇两次提取):称取牛蒡子10g、野菊花9g、地肤子10g、五味子9g、绿豆5g,粉碎至40目,0.2mpa,110℃处理30min,60℃干燥1.5h;料液比1:30(m/m),加入乙醇,80℃搅拌提取1h;料液比1:20(m/m),再次加入乙醇,70℃搅拌提取2h;冷却至40℃以下,过滤,得到滤液;60℃减压浓缩;滤板孔径1μm,精滤至澄清,即得。样品3(溶剂一极性小于溶剂二的情况下两次提取):牛蒡子10g、野菊花9g、地肤子10g、五味子9g、绿豆5g,粉碎至40目,0.2mpa,110℃处理30min,60℃干燥1.5h;料液比1:30(m/m),加入环己烷,80℃搅拌提取1h;料液比1:20(m/m),加入丁二醇,70℃搅拌提取2h;冷却至40℃以下,过滤,得到滤液;60℃减压浓缩,除去环己烷;滤板孔径1μm,精滤至澄清,得到提取物。样品4:实施例10。1.dpph自由基清除实验(1)实验方法:取dpph溶液1ml和样品液1ml,充分振荡混合均匀,静置30min,用酶标仪在517nm波长下测定其吸光度。dpph自由基清除率计算公式:dpph自由基清除率%=[(b+c)-a]/b*100式中:a为试样溶液与dpph溶液混合后的od值,b为无水乙醇与dpph溶液混合后的od值,c为无水乙醇与试样溶液混合后的od值。(2)实验结论:如表9所示。表9不同工艺制备样品dpph清除率对比样品名称受试浓度%清除率%样品1525样品2553样品3536样品4583样品1采用油脂直接提取,由于油脂分子量较大,不易通过细胞壁和细胞膜,提取胞内活性成分,且粘度较高,不利于提取过程中的物质传递,故dpph清除率低。样品2采用乙醇提取,乙醇是优良的溶剂,提取出油溶活性成分的同时,大量的水溶性多糖也随之溶出;浓缩时,多糖等粘性物质裹挟部分油溶活性成分析出,形成沉淀,造成了活性成分的损失,故dpph清除率较低。样品3采用两步法双溶剂提取,但溶剂1(与溶剂2比)极性较弱,溶剂2(与溶剂1比)极性较强,溶剂1与细胞膜相互作用弱,不利于两种溶剂进入细胞提取活性成分,破坏两溶剂间的协同增效作用,导致提取率降低,故dpph清除率较低。样品4为本发明的实施例10制备提取物,样品4提取物时间料液比等参数与样品1、2和3相同,但dpph清除率显著高于样品1、2和3,且远远优于样品1和2的效果之和。发明人用其它实施例做了同样的对比,得到相同的结论。2.抑制透明质酸酶实验(1)实验方法:取0.1ml0.25mmol/l的氯化钙溶液和0.5ml透明质酸酶液37℃保温培养20min;加入样品液0.5ml,继续37℃保温培养20min;加入0.5ml透明质酸纳液37℃保温30min,常温放置5min;加入0.1ml0.4mol/l氢氧化钠溶液和0.5ml乙酰丙酮溶液,置沸水浴中加热15min后立即用冰水冷却5min;加入埃尔利希试剂1.0ml并用3.0ml无水乙醇进行稀释,放置20min显色,用酶标仪在555nm波长下测定其吸光度。透明质酸酶抑制率计算公式:透明质酸酶抑制率%=[(a-b)-(c-d)]/(a-d)*100式中:a为对照溶液吸光度(用醋酸缓冲液代替样品溶液),b为对照空白溶液吸光度(用醋酸缓冲液代替样品溶液及酶液),c为试样溶液吸光度值,d为试样空白溶液吸光度(用醋酸缓冲溶液代替酶液)。(2)实验结论:如表10所示。表10不同工艺制备样品透明质酸酶抑制率对比样品名称受试浓度%抑制率%样品1514样品2551样品3519样品4569样品1采用油脂直接提取,由于油脂分子量较大,不易通过细胞壁和细胞膜,提取胞内活性成分,且粘度较高,不利于提取过程中的物质传递,故透明质酸酶抑制率低。样品2采用乙醇提取,乙醇是优良的溶剂,提取出油溶活性成分的同时,大量的水溶性多糖也随之溶出;浓缩时,多糖等粘性物质裹挟部分油溶活性成分析出,形成沉淀,造成了活性成分的损失,故透明质酸酶抑制率较低。样品3采用两步法双溶剂提取,但溶剂1(与溶剂2比)极性较弱,溶剂2(与溶剂1比)极性较强,溶剂1与细胞膜相互作用弱,不利于两种溶剂进入细胞提取活性成分,破坏两溶剂间的协同增效作用,导致提取率降低,故透明质酸酶抑制率低。样品4为本发明的实施例10制备提取物,样品4原料、提取物时间和料液比等参数与样品1、2和3相同,但透明质酸酶抑制率明显高于样品1、2和3,且远远优于样品1和2的效果之和。发明人利用本发明其他实施例得到的提取物重复上述实验,结果与上述相同,在此不赘述。五、本发明与现有技术相比得到的提取物在油剂型化妆品中稳定性比较1.用于油剂型化妆品中澄清度比较(1)实验方法:取样品液3.0g和油剂型化妆品常用辅料油脂27.0g,加热至50℃左右,搅拌溶解20min,静置冷却1h后,观察样品在油脂中的溶解情况。样品与油脂相容性好,则溶解后的样品澄清透明;样品和油脂相容性差,则溶解后的样品变浑浊。因此,样品在油脂中的溶解性可以用其溶解后的浑浊程度(浊度)来表征。浊度属于一种光学特性,是由于液体中的微小颗粒引起的光的散射,浊度越高则散射光量越大。本实验采用hi93414高精度数据型浊度测量仪检测样品浊度。所测数值越低证明浊度越低澄清度越好,证明产品稳定性佳。(2)样品制备工艺:与dpph自由基清除实验样品相同。表11不同工艺样品浊度对比(3)实验结论:如上表所示。样品1本身为油脂提取,因此在油剂型化妆品辅料中浊度比较优异;样品2为醇溶性提取物,与油脂的相容性较差,故浊度高。样品3的提取溶剂,颠倒了本发明的溶剂极性,使得终产品的溶剂极性较强,与油脂相容性差,故浊度高。样品4采用溶剂一和溶剂二配合提取,并优化了提取工艺,使得活性成分与化妆品常用辅料油脂的相容性好,故浊度较低,甚至可以等同于油脂提取得到的提取物。发明人用其它实施例做了同样的对比,得到相同的结论。2.稳定性实验(1)实验方法:取样品液10g和辛酸/癸酸甘油三酯190g,加热至50℃左右,搅拌溶解20min,将配置好的样品平均分成五份,分别放置于避光(室温暗盒中)、冷藏(4℃冰箱)、光照(28℃光照培养箱)、热(45℃烘箱)、冷冻(-15℃冰箱)五个条件下,并分别在第7天、14天、30天观察稳定性。(2)样品信息:上述样品1、2、3、4。表12不同工艺样品稳定性对比(3)实验结论:如上表所示。样品130天稳定性实验可见其有少量沉淀,并且具有轻微异味,说明样品变质。样品230天稳定性实验可见其有大量沉淀,说明样品稳定性变差。样品330天稳定性实验可见,其外观具有大量沉淀,说明样品稳定性变差。样品430天稳定性实验可见,外观澄清透明,气味正常,说明本发明制备提取物稳定性优于样品1、2和3。发明人用其它实施例做了与现有技术同等条件的对比,得到相同的结论。六、本发明方法与现有方法技术成本比较根据dpph自由基清除实验结果可知,提取条件相同时(料液比、提取温度、提取时间),本发明(样品4)的提取效率远高于油脂直接提取(样品1)及乙醇提取(样品2)。表13本发明与现有技术工业化应用的成本比较通过上述表格可知,本发明提取效率远远优于样品1和样品2。如果想达到与本发明相同提取效率,原料需要增加至现有两倍用量。原料增加的同时,提取溶剂也需要成倍增加,现有技术乙醇提取已经比本发明有机溶剂用量多了至少一倍,如果增加原料至两倍量,有机溶剂至少比本发明多三倍。因此本发明与现有提取工艺相比成本低廉,原料、提取溶剂用量更少,在制备、储存和运输上的成本更低。并且由于本发明大幅度减少了有机溶剂的用量,有效的避免了有机溶剂回收及排放的成本,更重要的是极大的降低了对环境污染的风险。综上,本发明与现有技术相比具有节约成本、减少物料、减少能量消耗、环保的优点,非常适用于目前节能减排的工业化大生产。七.动物及人体功效实验功效测试样品配方表如下表所示。表14本发明护肤组合物制剂配方原料名称添加量(%)辛酸/癸酸甘油三酯55氢化聚异丁烯25白油-1615样品5添加样品分别为实施例10、16、17、18,空白组添加样品为辛酸/癸酸甘油三酯。实施例16、17和18为油剂型产品,可以单独使用,也可以与本实验一样作为添加剂使用,具体使用方法不对最终效果产生影响。1.磷酸组胺致痒阈值实验机体产生炎症时,肥大细胞中作为化学传递物质的组胺起着重要作用。皮肤干燥,导致屏障受损,进而引发炎症反应。痒是皮肤干燥引起的一种症状,也与局部肥大细胞释放组胺有关。采用磷酸组胺致豚鼠皮肤瘙痒模型,评价本发明提取物及油剂型化妆品的止痒效果。实验方法:实验分空白组、样品组(实施例10、16、17、18)。在豚鼠受损皮肤处涂抹受试样品,空白组涂抹等量基质(配方见表14),随后滴加相应浓度的磷酸组胺,留置3min,无反应时每隔3min递增浓度,直至出现瘙痒反应为止,计算每组动物的平均致痒阈值。致痒阈值越大,说明止痒效果越明显。结果见图6。结果表明,添加本发明的护肤组合物制剂,可显著提高豚鼠耐受磷酸组胺的致痒阈值,从而缓解瘙痒。发明人用其它实施例做了同样的对比,得到相同的结论。2.人群试用在试用周期内(6周),共筛选30位老年人纳入适用范围,组间脱落1人,受试人群中未出现不良反应或3级以上的皮肤刺激,故本次测试的有效志愿者人数为29人。志愿者筛选标准:50~65周岁,有皮肤干燥、瘙痒等问题的的老年人。人体测试样品配方见表14。试用方法:取2~3滴本发明护肤组合物制剂,涂抹于受试者的曲臂内侧,轻轻按摩。测试结束后(第6周),请受试者填写调查问卷,从吸收效果、滋润效果、保湿效果、缓解瘙痒等方面,对样品进行评分。表15样品使用前后主观评价结果样品吸收效果滋润效果保湿效果缓解瘙痒缓解干裂空白3.53.23.51.32.0实施例103.94.34.54.64.5实施例164.14.64.94.84.8实施例174.44.74.94.84.8实施例184.24.54.94.74.8注:1.评分标准以吸收效果为例,非常不易吸收为1分,不易吸收为2分,一般为3分,易吸收为4分,非常易吸收为5分;其它项目评分标准以此类推。2.表中数据为所有受试者有效评分结果的平均值。对受试者填写的调查问卷进行统计分析(如表15所示)可知,添加本发明的护肤组合物制剂,吸收效果、滋润效果、保湿效果、缓解瘙痒及干裂的平均值高于空白组,说明采用本发明的提取方法所得的样品具有保湿、滋润、缓解瘙痒及干裂等功效。发明人用其它实施例做了与现有技术同等条件的对比,得到相同的结论。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1