抗PD-1抗体及其用途的制作方法
本申请要求美国专利申请62/278,669的优先权,该申请的申请日为2016年1月14日,其全文以引用的方式并入本文中。
电子提交序列表的引用
ascii格式序列表文件“bps_pct_seq_id”创建于2017年1月13日,大小为14kb,其作为序列表正式文本通过efs-web电子提交。包含在该ascii格式文件中的序列表成为说明书的一部分并通过引用整体并入本文。
背景技术
淋巴细胞存在于静息状态,需要抗原刺激进行增殖并增加有效免疫响应。对于t细胞,该信号通过主要组织相容性复合物(mhc)结合的抗原通过t细胞受体(tcr)发送信号进行传递。完全激活t细胞除了需要tcr激活外,还需要引入各种共刺激和共抑制通路(croft,m.(2003)nat.rev.immunol.3:609)。
程序性死亡1,也称为pd-1和cd279,是55kda的细胞表面,是主要由淋巴细胞,尤其是t细胞表达的共抑制受体(blank,c.(2005)cancerimmunol.immunother.54:307)。pd-1配体包括pd-l1和pd-l2,pd-l1又称b7-h1和cd274,pd-l2又称b7-dc和cd273。pd-1:pd-l1或pd-1:pd-l2相互作用抑制t细胞活性,导致增殖减少、促炎性细胞因子分泌减少和t细胞效应子功能的减少,例如t细胞溶解(freeman,g.(2000)j.exp.med.192:1027;latchman,y.(2001)nat.immunol.2:261;rodig,n.(2003)eur.j.immunol.33:3117)。
在健康个体内,通过激活t细胞诱导pd-1表达,在免疫反应成功消除病原体后pd-1表达减弱(vibhakar,r.(1997)exp.cellres.232:25;zajac,a.(1998)j.exp.med.188:2205)。在某些免疫响应未成功的情形下,延长抗原刺激导致pd-1表达提高并“耗尽”t细胞表型(zajac,a.(1998)j.exp.med.188:2205)。在小鼠中敲除pd-1是非致命的,且在非肥胖小鼠糖尿病模型中,敲除pd-1配体,pd-l1,导致免疫调节疾病发展加速(wang,j.(2005)proc.natl.acad.sciusa102:1823)。因此,其主要作用被认为是控制免疫响应,从而通过下调t细胞活性阻止自免疫疾病的发展。
已显示,pd-1负调控淋巴细胞所需的许多肿瘤的配体(pd-l1和pd-l2)表达水平提高。这对于pd-l1尤其如此。鳞状细胞癌、结肠癌和乳腺癌已显示pd-1水平提升(brown,j.(2003)j.immunol.170:1257)。而且,在小鼠肿瘤上的pd-1转基因表达导致肿瘤发生和入侵增加(iwai,y.(2002)proc.natl.acad.sci.usa99:12293)并且通过敲除pd-1,小鼠黑色素瘤模型中的肿瘤生长停止了。
这些临床前的研究证明了使用抗pd-1抗体增强t细胞功能是免疫功能障碍疾病例如癌症的有希望的疗法。临床研究也支持了这种假说。免疫检查点抑制剂的封闭,例如使用抗pd-1抗体,已表明在几种实体瘤中具有临床活性(brahmer,j.(2010)j.clin.oncol.28:3167;brahmerj.(2012)n.engl.j.med.366:2455;hamid,o.(2013)n.engl.j.med.369:134;topalian,s.(2014)j.clin.oncol.32:1020;wolchok,j.(2013)n.engl.j.med.369:122)。第一免疫检查点抑制剂,全人免疫球蛋白(ig)g1单克隆抗体阻断细胞毒素t淋巴细胞抗原4(ctla4),2011年被美国食药监(fda)批准用于治疗转移性黑素瘤。三年后,美国fda批准第一抗pd-1抗体用于治疗晚期黑色素瘤并第一次公布了2015年美国的pd-1阻断第三期试验(robert,c.(2015)n.engl.j.med.372:320)。
尽管pd-1似乎是治疗中的有希望的靶标,还需要开发能够阻断pd-1和其配体pd-l1和pd-l2相互反应的改进的组合物。
技术实现要素:
本发明提供特异性结合人pd-1并阻碍人pd-1结合pd-l1和pd-l2的人源化抗体。特别的,本发明的一个方面提供结合人pd-1的抗体或抗体片段,该抗体或抗体片段具有包括seqidnos.1-3所述的cdr序列的重链可变区;以及包括seqidnos.4-6所述的cdr序列的轻链可变区。
抗体或抗体片段抑制或减少pd-1结合至pd-l1、pd-l2,或pd-l1及pd-l2。抗体优选是嵌合形式,并最优选是人源化形式,用于药物组合物中的活性组分或药剂。优选的,当人pd-1具有一个或多个选自l128a、p130a、i134a、e136a和k78a的突变时,该抗体或抗体片段结合人pd-1。
在一些实施方式中,重链可变区具有seqidnos.7-9中任意一种接触序列或者其中多达三种接触序列。
在一些实施方式中,重链可变区氨基酸序列与seqidno.13具有至少85%的序列一致性,或者与seqidno.13具有至少90%的序列一致性。在进一步的实施方式中,重链可变区氨基酸序列与seqidno.13具有至少95%的序列一致性,或者与seqidno.13具有至少99%的序列一致性。在进一步的实施方式中,重链可变区具有seqidno.13所述的氨基酸序列。
轻链可变区也可具有seqidnos.10-12中任意一种接触序列或者其中多达三种接触序列。
在一些实施方式中,轻链可变区氨基酸序列与seqidno.14具有至少85%的序列一致性,或者与seqidno.14具有至少90%的序列一致性。在进一步的实施方式中,轻链可变区氨基酸序列与seqidno.14具有至少95%的序列一致性,或者与seqidno.14具有至少99%的序列一致性。在进一步的实施方式中,轻链可变区具有seqidno.14所述的氨基酸序列。
在相关的实施方式中,重链可变区具有seqidnos.7-9所述的接触序列,轻链可变区具有seqidnos.10-12所述的接触序列。
在相关方面,提供能够结合人pd-1的抗体或抗体片段,其包括:与seqidno:13所述氨基酸序列至少85%序列一致性的重链可变区,该重链可变区还具有seqidnos.1-3所述的三个cdr序列和seqidnos.7-9所述的三个接触序列;与seqidno:14所述的氨基酸序列至少85%序列一致性的轻链可变区,该轻链可变区还具有seqidnos.4-6所述的三个cdr序列和seqidnos.10-12所述的三个接触序列。
在一些实施方式中,重链可变区与seqidno.13的氨基酸序列具有至少90%的序列一致性,且轻链可变区与seqidno.14的氨基酸序列具有至少90%的序列一致性。在进一步的实施方式中,重链可变区与seqidno.13的氨基酸序列具有至少95%的序列一致性,且轻链可变区与seqidno.14的氨基酸序列具有至少95%的序列一致性。在进一步的实施方式中,重链可变区与seqidno.13的氨基酸序列具有至少99%的序列一致性,且轻链可变区与seqidno.14的氨基酸序列具有至少99%的序列一致性。在进一步的实施方式中,重链可变区具有seqidno.13所述的氨基酸序列,轻链可变区具有seqidno.14所述的氨基酸序列。
可提供各方面的分离形式的每种抗体。当适配于治疗用途时,可将每种抗体与药学可接受载体一起提供。
在本发明其他相关方面,可提供编码任一种抗pd-1抗体或抗体片段的核酸序列。
在另一相关方面,提供干扰pd-l1和人pd-1相互作用的方法,其包括提供包含人pd-1的样品;将pd-1与一种抗pd1抗体或抗体片段接触;并将pd-1暴露于pd-l1。
在另一相关方面,提供干扰pd-l2和人pd-1相互作用的方法,其包括提供人pd-1样品;将pd-1与抗pd1抗体或抗体片段中的一种接触;并将pd-1暴露于pd-l2。
在另一相关方面,提供干扰pd-l1和pd-l2和人pd-1相互作用的方法,其包括提供人pd-1样品;将pd-1与抗pd1抗体或抗体片段中的一种接触;并将pd-1暴露于pd-l1和pd-l2。
在另一相关方面,提供减少细胞中pd-1信号发射的方法,其包括提供表达人pd-1的细胞;将细胞与一种抗pd1抗体或抗体片段接触;并将细胞暴露于pd-l1。
在另一相关方面,提供减少细胞中pd-1信号发射的方法,其包括提供表达人pd-1的细胞;将细胞与一种抗pd1抗体或抗体片段接触;并将细胞暴露于pd-l2。
在另一相关方面,提供减少细胞中pd-1信号发射的方法,其包括提供表达人pd-1的细胞;将细胞与一种抗pd1抗体或抗体片段接触;并将细胞暴露于pd-1和pd-l2。
附图说明
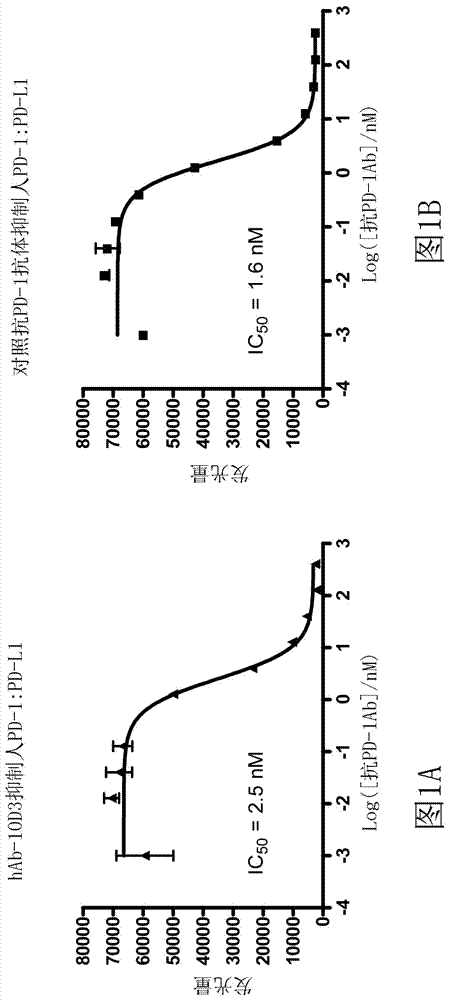
图1a和图1b是描述用一系列不同浓度的bpshab-10d3(fig.1a)与阳性对照相比,抑制人pd-1:pd-l1相互作用的一系列图。
图2描述了用一系列不同浓度的hab-10d3抑制人pd-1:pd-l2相互作用。
图3a和图3b系列图描述了用一系列不同浓度的hab-10d3与阳性对照相比,抑制食蟹猴(m.fascicularis)pd-1:pd-l1相互作用。
图4a和图4b系列图描述了用一系列不同浓度的hab-10d3与对照相比,中和人pd-1信号发射。
图5描述了测试与抗pd-1抗体结合的人pd-1融合蛋白。
图6系列图比较了人pd-1各种突变时,市售merck抗pd-1抗体(cat#71120)与bpshab-10d3的结合,其确认了人pd-1上的不同氨基酸基团涉及结合反应。
具体实施方式
本发明提供抗人pd-1抗体和抗体片段,统一简称为抗pd-1抗体。这些抗体抑制或妨碍人pd-1和pd-l1,人pd-1和pd-l2,或者pd-1同时和pd-l1及和pd-l2的相互作用。在一些实施方式中,抗pd-1抗体作为pd-1活性的拮抗剂,因而减弱或阻断负调控t细胞活性的pd-1抑制性信号。抗pd-1抗体以及阻断pd-1抑制性信号的能力在临床应用中具有多种用途,包括,例如在治疗持续感染、消除肿瘤免疫逃避增强宿主抗癌免疫性,以及提供结合疫苗引入细胞免疫响应的佐剂类性能时增强宿主抗微生物免疫性。
a.定义
除非另有说明,本文使用的所有技术和科学术语具有本领域技术人员通常所理解的声明主题物质所属的一般含义。若本文中术语具有多种定义,以本部分的定义为准。本文提及的所有专利、专利申请、公开文献、公开核苷酸和氨基酸序列(例如在genbank和其他数据库中的序列)通过引用并入本文。当引用是url或其他标识或地址,应理解的是这些标识可改变,网络上的特定信息来来去去,但是通过网络可搜索到对等的信息。引用证明这些信息的可获得性和公开传播。
应理解的是,前述一般描述和后续具体描述仅仅是示例性的和说明性的,并非限制声明的任何主题物质。在本申请中,使用的单数包括复数形式,除非另有说明。应该指出的是,除非上下文明确指明,否则,正如本专利说明书和权利要求书中所使用的那样,单数形式“一”和“这个(该)”包括复数意义。在本申请中,“或”的使用是指“和/或”,除非另有说明。而且,术语“包括”及其他形式,是非限制性的。
本文使用的段落标题仅用于组织目的,并不解释为显示描述的主体物质。
标准的化学术语的定义可在工具书中找到,包括但不限于carey和sundberg“高等有机化学,第4版”第a卷(2000)和b卷(2001)纽约plenum出版社,(careyandsundberg"advancedorganicchemistry4thed."vols.a(2000)andb(2001),plenumpress,newyork)。除非另有指明,质谱、nmr、hplc、蛋白化学、生物化学、重组dna技术和药物学传统方法。
除非提供特殊定义,本文采用的分析化学、合成有机化学和医学和药物化学的术语及实验程序和技术是本领域公认的。标准技术可用于化学合成、化学分析、药物制备、制剂、和递送,和治疗病人。标准技术可用于重组dna、寡核苷酸合成,和组织培养和转化(例如电穿孔、脂质转染)。可采用反应和纯化技术,例如使用制造商说明或本领域常用的或本文描述的试剂盒。上述技术和程序可通常作为传统方法采用,描述为整个申请引用和讨论的各种通用或更具体的参考。
应理解的是,本文描述的方法和组合物并不限于特定方法、方案、细胞系结构体和试剂,其可变化。也应该理解的是,本文所用的名词术语仅用于描述特定的实施方式,并非用于限制本文的方法、化合物和组合物的范围。
此处使用的用抗pd-1抗体“治疗(treat)”、“治疗(treating)”和“治疗(treatment)”包括缓解、缓和或减轻疾病、紊乱或病症,预防其他的症状,减轻或预防潜在的代谢症状病因,抑制疾病、紊乱或病症,例如,阻止疾病、紊乱或病症的发展,舒缓疾病、紊乱或病症,使疾病、紊乱或病症消退,舒缓由疾病、紊乱和病症引起的症状,或阻止疾病、紊乱或病症的症状。术语“治疗”包括但不限于预防和/或治疗处理。
术语“可接受的”或“药学上可接受的”,与抗pd-1抗体剂型有关,是指对治疗主体的总体健康不具有持久有害作用,或不消除一种或多种本文所述抗pd-1抗体的生物活性或性能的组分,且是相对无毒的。
施与抗pd-1抗体或药物组合物“改善”特定疾病、紊乱或病症的症状,术语“改善”是指任何严重程度的减轻,发作延迟、病情减慢、或持续期缩短,不管永久的或临时的,持续的或短暂的,只要归因于使用抗pd-1抗体或包括抗pd-1抗体的药物组合物或与其有关。
本文使用的术语“药物组合”是指混合或组合一种以上活性组分(例如抗pd-1抗体)并包括该活性组分的固定和非固定组合。术语“固定组合”是指一种将一种活性组分(例如抗pd-1抗体)和辅助剂以单一整体或剂量的形式同时给药给病人。术语“非固定组合”是指将活性组分(例如抗pd-1抗体)和辅助剂以独立单位同时、并发或有序的施药给病人,没有特定的中间时间限制,其中这种给药为病人身体提供有效水平的两种药剂。后者还适用于鸡尾酒疗法,例如给予三种或更多种活性组分。
术语“药物组合物”指的是一种或多种抗pd-1抗体和一种或多种其他化学成分,如载体、稳定剂、稀释剂、分散剂、悬浮剂、增稠剂和/或赋形剂的混合物。所述药物组合物使得抗pd-1抗体容易给药到有机体。本领域中存在多种抗pd-1抗体的给药技术,包括但不限于:局部、眼部、眼内、眼周、静脉内、口服、气溶胶、肠胃外给药。
本文使用的术语“载体”是指相对无毒的化学化合物或试剂,其有助于目标试剂(如抗pd-1抗体)结合至细胞或组织内。
术语“稀释剂”是指在递送前稀释目标试剂(如抗pd-1抗体)的化学化合物。稀释剂还可用于稳定试剂,因为其能提供更稳定的环境。溶于缓冲溶液的盐类(其还提供ph控制或维持)用作本领域的稀释剂,包括但不限于磷酸盐缓冲生理盐水。
术语“共给药”等,是指包含给予多种选择试剂(例如抗pd-1抗体或其组合物和助剂)至单一病人,并指包含相同或不同给药途径在相同或不同时间给药的治疗方案。
术语“有效量”或“治疗有效量”指能在某种程度上减轻正在治疗的疾病、紊乱或病症的一种或多种症状的pd-1抗体、试剂、组合物或药物组合物的量。该结果可以是减少和/或减轻生物系统的迹象、症状或病因,或任何其他所需改变。例如,治疗用途的“有效量”是提供疾病症状所需的药效、治疗改善或临床显著下降而没有不适当的副反应。任何个例中合适的“有效量”可使用技术例如剂量递增研究来确定。术语“治疗有效量”包括例如预防有效量。可以理解的是由于抗pd-1抗体、遗传、组合、或药物组合物、年龄、体重、主体的一般情况、治疗的症状、治疗症状的严重性以及处方医师的判断的不同而产生主体间“有效量”的差异。仅举例而言,治疗有效量可通过途径试验,包括但不限于剂量递增临床试验确定。
术语“预防有效量”指应用至病人能在某种程度上减轻正在治疗的疾病、病症或紊乱的一种或多种症状的pd-1抗体、试剂、组合物或药物组合物的量。在这类预防应用中,这种量可依据病人的健康状态、体重等。本领域技术人员能够考虑到通过途径试验,包括但不限于剂量递增临床试验来决定该预防有效量。
本文使用的术语“主体”或“病人”是指动物,其为治疗、观察或试验的主体。仅举例说明,主体可以是但不限于哺乳动物,包括但不限于人。
术语“增强”指增加或延长所需效果的效力或持续时间。仅举例说明,仅“增强”治疗剂效果或其组合指增加或延长效力、持续时间和/或量级,治疗疾病、紊乱或病症的的试剂的效果的能力。当用于病人时,该用途的有效量将取决于疾病、紊乱或病症的严重性,前序治疗,病人健康状况和对药物的响应,以及治疗医师的判断。
术语“调节”指与目标(例如pd-1)直接或间接作用以改变目标活性,例如,增强目标活性,抑制或反抗目标活性,限制目标活性,或延伸目标活性。在某些实施方式中,本文描述的pd-1抗体和药物组合物能够调节一种或多种各自目标(例如一种或多种抗pd-1抗体)的活性。在某些实施方式中,本文描述的抗pd-1抗体调节(例如降低)细胞(例如t细胞)上的pd-1活性,造成例如t细胞激活或增加t细胞效应子功能。
如本文所述,术语“目标”指能够被本文所述选择性结合剂(例如抗pd-1抗体)或药物组合物结合的生物分子(例如目标蛋白或蛋白复合物),例如pd-1,或生物分子的一部分。如本文所述,术语“非目标”指不被本文所述选择性结合剂或药物组合物选择性结合的生物分子或生物分子的一部分。
术语“目标活性”或“细胞响应”指能够被抗pd-1抗体或抗pd-1抗体结合至pd-1受体造成的任何细胞响应。某些示例性目标活性和细胞响应包括但不限于结合亲和性、信号传导、基因表达、细胞迁移、细胞增殖、细胞分化、细胞调节的细胞毒性、以及与癌症相关的一种或多种症状的改善。
术语“氨基酸”指由末端氨基和羧基官能团构成的分析,其末端氨基和羧基官能团之间的碳原子有时包含结合至该碳原子的侧链官能团(例如甲基官能团,其形成氨基酸丝氨酸)。典型氨基酸可分为天然和非天然氨基酸。天然氨基酸例如包括甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、络氨酸、色氨酸、丝氨酸、苏氨酸、半胱氨酸、甲硫氨酸、天冬酰胺、谷氨酰胺、赖氨酸、精氨酸、组氨酸、天冬氨酸和谷氨酸等。非天然氨基酸例如包括l-3,4-二羟基苯丙氨酸、2-氨基丁酸、脱氢丙氨酸、g-羧基谷氨酸、肉毒碱、γ氨基丁酸、羟基脯氨酸、硒代甲硫氨酸等。该本说明书文本中,应理解的是,氨基酸可以是左旋光学异构体或右旋光学异构体。
b.抗pd-1抗体
本发明提供抗体,其也指结合人pd-1的抗体片段。bps抗体10d3(人源化形式也表示为hab-10d3)描述了对于pd-1的高特异性和有效抑制或降低pd-1信号的能力。如图图1-4所示,克隆hab10d3同时干扰pd-1:pd-l1的结合以及pd-1:pd-l2的结合。而且,pd-1的突变分析表明了克隆h-ab10d3与默克公司的抗pd1(型号#71120)相比识别了不同的抗原表位(图6)。克隆huab-10d3的主要区域的序列数据如表1所示:
表1:hab-10d3的序列数据
相应的,本发明提供结合人pd-1的抗体。特别是该抗体具有包含seqidnos.1-3所述cdr序列的重链可变区;以及包含seqidnos.4-6所述cdr序列的轻链可变区。在进一步的实施方式中,重链可变区具有seqidnos.7-9中任意一种接触序列,优选的具有所有三种接触序列。
在一些实施方式中,重链可变区具有与seqidnos.13至少85%序列一致性,优选至少90%序列一致性的氨基酸序列。在进一步的实施方式中,重链可变区具有与seqidno.13至少95%序列一致性,优选至少99%序列一致性的氨基酸序列。人源化抗pd-1抗体hab-10d3具有含seqidno.13所述氨基酸序列的重链可变区。
在一些实施方式中,抗pd-1抗体具有含seqidnos.10-12任一接触序列的轻链可变区,优选含seqidnos.10-12三种接触序列。优选的,轻链可变区氨基酸序列与seqidno.14具有至少85%的序列一致性,优选与seqidno.14具有至少90%的序列一致性。在进一步的实施方式中,轻链可变区氨基酸序列与seqidno.14具有至少95%的序列一致性,优选与seqidno.14具有至少99%的序列一致性。人源化克隆hab-10d3具有包括seqidno.14所述氨基酸序列的轻链可变区。
尽管重链可变区和轻链可变区可分别与其他轻链可变区和其他重链可变区结合,只要能够维持pd-1结合,在一些实施方式中,抗人pd-1抗体包括:与seqidno:13所述氨基酸序列至少85%序列一致性的重链可变区,该重链可变区还具有seqidnos.1-3所述的三个cdr序列和seqidnos.7-9所述的三个接触序列;与seqidno:14所述的氨基酸序列至少85%序列一致性的轻链可变区,该轻链可变区还具有seqidnos.4-6所述的三个cdr序列和seqidnos.10-12所述的三个接触序列。
在进一步的实施方式中,重链可变区与seqidno.13的氨基酸序列具有至少90%的序列一致性,且轻链可变区与seqidno.14的氨基酸序列具有至少90%的序列一致性。在进一步的实施方式中,重链可变区与seqidno.13的氨基酸序列具有至少95%的序列一致性,且轻链可变区与seqidno.14的氨基酸序列具有至少95%的序列一致性。在进一步的实施方式中,重链可变区与seqidno.13的氨基酸序列具有至少99%的序列一致性,且轻链可变区与seqidno.14的氨基酸序列具有至少99%的序列一致性。在人源化克隆hab-10d3中,重链可变区具有seqidno.13所述的氨基酸序列,轻链可变区具有seqidno.14所述的氨基酸序列。
如上所述,本发明包含cdr周边的序列在某一百分率序列一致性之内的变化。关于两个氨基酸或多聚核苷酸序列的术语“百分率序列一致性”是指当进行序列最优比对时两个序列中的相同残基的百分率。因此,80%氨基酸序列一致性是指在两个最优比对的多肽序列中80%的氨基酸是相同的。同样的,85%的氨基酸序列一致性是指在两种最优比对的多肽序列中85%的氨基酸是相同的;90%、95%和99%氨基酸序列一致性是指在两个最优比对的多肽序列中90%、95%和99%的氨基酸是分别相同的。
一致性百分率可通过例如通过对齐氨基酸直接比较两个分子之间的序列信息,计算两个对齐序列之间的精确的匹配数量,除以更短序列的长度,并将结果乘以100。已有计算机程序可用于辅助分析,例如align,dayhoff,m.o.("atlasofproteinsequenceandstructure"),m.o.dayhoffet.,suppl.3:353-358,nationalbiomedicalresearchfoundation,washington,d.c.,其改编了smith和waterman(1981)的用于多肽分析的局部同源性算法advances(appl.math.2:482-489)。确定核苷酸序列一致性的程序可见wisconsinsequenceanalysispackage,第8版(可从geneticscomputergroup,madison,wis.获取),例如bestfit、fasta和gap程序,其依赖于smith和waterman算法。这些程序可容易的利用制造商推荐的自定义参数5并描述于上述的wisconsinsequenceanalysispackage。适合确定序列相似性的算法的一个示例是blast算法,其描述于altschul,etal.,j.mol.biol.215:403-410(1990)。用于执行blast分析的软件通过国家生物技术信息中心可公开获取。同样的,测定百分率同源性的计算机程序也容易获取。
序列一致性的变化允许在cdr之外,因为不是重链和轻链可变区的所有氨基酸序列都需要结合pd-1。尤其是cdr外或cdr和接触位点外的区域,例如骨架区,可以突变成不失去pd-1结合能力。更进一步的,骨架区可进一步突变并因此序列不同,以适应cdr用于不同物种的治疗。可使用下述术语描述突变或变化:位置(#);被取代氨基酸残基。根据该术语,例如甘氨酸残基取代位置上的丙氨酸残基可表示为a#g,其中#表示位置。当氨基酸残基在给定位置被两个或多个可替换氨基酸残基取代,这些残基可通过逗号或斜线分开。例如,用甘氨酸或谷氨酸取代丙氨酸可表示为#g/e,或#g,#e。在相同位置删除丙氨酸可表示为ala#*或a#*,或*#ala或*#a,其中#表示氨基酸位置。多种突变通过+或斜线分开。例如,某位置上的甘氨酸和丝氨酸分别取代丙氨酸和谷氨酸的两种突变(每种表示为“#”),表示为a#g+e#s或a#g/e#s。但氨基酸残基在给定位置#被两个或多个可替换氨基酸残基取代,这些残基可通过逗号或斜线分开。例如,在位置#用甘氨酸或谷氨酸取代丙氨酸表示为a#g,e或a#g/e,或a#g,a#e。当确定位置#适合修饰而没有任何建议的特定修饰,应理解的是,任何氨基酸可取代该位置上的氨基酸残基。因此,当位置#的丙氨酸的修饰被提及但未标明,应理解的是,丙氨酸可以被删除或用任意其他氨基酸残基(例如r,n,d,c,q,e,g,h,i,l,k,m,f,p,s,t,w,y和v中的任意一种)取代。
cdr或cdr和接触区之外的取代可以为保守突变或保守取代。术语“保守突变”或“保守取代”,分别是指本领域技术人员认为是对于第一突变保守的氨基酸突变。在该环境下“保守”是指依据氨基酸特性的相似氨基酸。例如,如果特定位置的突变导致用脂肪族氨基酸残基(例如亮氨酸)取代非脂肪族氨基酸残基(例如丝氨酸),然后在相同位置用不同的脂肪族氨基酸进行取代(例如ile或val)被称为保守突变。氨基酸的其他特性包括氨基大小、疏水性、极性、电荷、pk值以及本领域已知的其他氨基酸特性。相应的,保守取代包括碱性取代碱性,酸性取代酸性,极性取代极性等。由此衍生的氨基酸集合可能因为结构原因而成为保守的。这些集合可以维恩图解形式描述(livingstonec.d.andbartong.j.(1993)"proteinsequencealignments:astrategyforthehierarchicalanalysisofresidueconservation"comput.applbiosci.9:745-756;taylorw.r.(1986)"theclassificationofaminoacidconservation"j.theor.biol.119;205-218)。保守取代可例如通过下表形成,其描述了通常接受的氨基酸维恩图解分类。
表2:氨基酸维恩图解分类
关于表2维恩图解,与seqidnos.13-16(seqidnos.1-6之外,可选的7-12之外)序列一致性的变化可通过以下方式:用另一种疏水氨基酸取代疏水氨基酸;用另一种芳香脂肪族氨基酸取代芳香脂肪族氨基酸;用另一种极性氨基酸取代极性氨基酸;用另一种带正电荷氨基酸取代带正电氨基酸;用另一种带负电氨基酸取代带负电氨基酸;用另一种小氨基酸取代小氨基酸;用另一种微小氨基酸取代微小氨基酸。
pd-1的突变分析显示了取代pd-1的氨基酸l128a,p130a,i134a和k78a不会显著影响hab-10d3结合至pd-1。e136a突变显示了更低的亲和性但是抗pd-1仍能结合。i126a对于抗体结合是需要的。当用merck抗体(cat#71120)在抗pd-1抗体上进行相同的研究,用丙氨酸取代1126,p130,i134,e136和k178中的每一种都显著降低结合至merck抗体。用丙氨酸替代l128完全消除了pd-1结合至merck抗体的能力,其确认了认pd-1的不同氨基酸在pd-1结合中是需要的。图6总结了研究结果。而且,该研究表明抗pd-1抗体上的对应位置可被突变而不失去结合能力。
优选的,当人pd-1具有一个或多个选自l128a、p130a、i134a、e136a和k78a的突变时,该抗体或抗体片段结合人pd-1。
参考seqidnos.1-6,本发明可定义为具有抗pd-1结合活性的一系列cdr区域;然而,在优选实施方式中,多个cdr肽(每种对应单个cdr)结合以形成具有特异性结合至pd-1表位的可变区的抗pd-1抗体。而且,抗体可变区可存在于完整抗体、抗体片段(例如f(ab),f(ab’)2,scfv,迷你抗体、四链抗体及其他)或者抗体或抗体片段的重组衍生物。
术语“抗体”描述了分离的免疫球蛋白,不管是天然的或部分或全部是合成的。因此,本发明的抗pd-1抗体,在一些实施方式中,包括任何具有结合域的多肽或蛋白,该结合域与在本文描述的抗体可变区内的cdr集合相同或大体相同,该抗体可变区特异性结合pd-1表位(例如,至少约80%相同,至少约85%相同,至少约90%相同,至少约95%相同,或至少99%相同)。
在一些实施方式中,不同抗体区域通过参考igg进行描述,其包含4个氨基酸链-两个较长重链和两个较短轻链,其通过二硫键内部相连。重链和轻链每种包含恒定区和可变区。重链由重链可变区和重链恒定区组成。轻链由轻链可变区和轻链恒定区组成。在一些实施方式中,在可变区内具有三种高变区域负责抗原特异性。在一些实施方式中,高变区称为互补决定区(cdr)且插入更保守的侧翼区之间,该侧翼区被称为骨架区(fw)。在各种实施方式中,重链和轻链可变区包含与抗原相互作用的结合域。
在一些方面,抗体可变区存在于重组衍生物。重组衍生物的实例包括单链抗体、二抗、三抗、四抗以及迷你抗体。在一些实施方式中,抗pd-1抗体还包含一种或多种识别相同或不同表位的可变区。
如已介绍的,hab-10d3克隆的cdr源自小鼠;但是hab-10d3是人源化抗体。因此,抗pd-1抗体可以是嵌合抗体或人源化抗体。嵌合抗体是单克隆抗体,由衍生自不同生物的可变区和恒定区构建。例如,嵌合抗体可包含来源鼠的可变区和衍生自目标宿主(例如人)的恒定区。鉴于此,抗pd-1嵌合抗体可通过插入啮齿动物(如小鼠)抗体的可变轻和重基因形成,其结合seqidnos.1-6至哺乳动物表达载体,该表达载体包含分别合适的人轻链和重链恒定域编码区。这些重链和轻链“嵌合”表达载体然后共转染至受体细胞系并经过已知的细胞培养技术,从而同时生产嵌合抗体的轻链和重链。已知这些嵌合抗体具有结合至源啮齿单克隆的能力并在宿主给药时显著降低免疫原性。
人源化抗体在本领域已知是一种来源于非人的抗体,该抗体蛋白序列经过修饰增加与人体天然产生的抗体变体的相似性。尤其是人源化过程通常应用于产生单克隆抗体用于人的给药(例如,抗体开发成抗癌药)。当开发特异性抗体的过程涉及在非人免疫系统生产(例如大鼠/小鼠中),人源化是必须的。用这种方法产生的抗体的蛋白序列部分不同于人体自然产生的同源抗体,并因此在给药给病人时是可能产生免疫性的。为了全面说明,人源化抗体不同于嵌合抗体。后者也具有与人抗体更相似的蛋白序列,但携带更大段非人蛋白。因此,尽管cdr1-6可存在于鼠类或其他哺乳动物,治疗用途通过人源化进行了改良。鉴于此,seqidnos.1-6的cdr已被人源化用于药物剂型。人源化技术在本发明所属领域是已知的。而且,本文提供的一种或多种多肽的人源化可通过“重塑”、“超嵌合化”、“cdr移植”、“镶合”、和“sdr移植”。
抗pd-1抗体可包含额外的组件,包括但不限于除了可变区的组件或者提供或辅助提供有用的和/或附加活性的其他可变区。有用的活性包括例如抗体效应子功能例如依赖抗体的细胞毒性、吞噬作用、补体依赖细胞毒性、和半周期/清理速度。在一些实施方式中,抗体效应子功能通过不同宿主组件调节,例如fcγ受体,新生fc受体(fcrn),和c1q。在各种实施方式中,不同类型的抗体组件或变形用于增强效应子功能。有用的组件或修饰的实例包括使用非岩藻糖基化寡糖,经过修饰的氨基酸以增加稳定性(例如igg4s228p突变),具有增强结合至fcrn的氨基酸,具有增强结合至fcγ受体的氨基酸修饰,以及降低与fcγ受体结合的氨基酸修饰(例如igg1d265a突变)。
抗pd-1抗体能包含fc恒定域,该恒定域经修饰最大程度降低抗体依赖的细胞调节毒性,fcγ受体结合,和/或补体调节细胞毒性。在一些实施方式中,抗pd-1抗体靶向pd-l1封闭区、pd-l2封闭区、pd-l1-非封闭区,或pd-l2-非封闭靶向区,如本文所述,包含在双特异性抗体中。在各种实施方式中,双特异性抗体包含fc或经修饰的fc域,其能够调节抗体效应子功能。在一些实施方式中,双特异性抗体是二价的、三价的、或四价的。
抗pd-1抗体能够包含另外的组件以改变蛋白的物化性能,提供药理学优势。例如,将聚乙二醇(“peg”)结合至分子,在一些实施方式中,但用于治疗时通过降低毒性并提高分子效力来提高安全性。物化改变包括但不限于构型改变、静电结合、和疏水性,其可共同延长治疗剂的系统保留时间。另外,通过结合peg基团增加抗pd-1抗体的分子重量,药理学优势可包括延长循环周期、提升稳定性、和提升保护对抗宿主蛋白酶。peg结合还可影响治疗基团与细胞受体的结合亲和性。peg是非离子型聚合物,由重复单元(—o—ch2—ch2—)构成,以形成从400至大于15000的一系列分子重量的聚合物(例如,市售的具有高达400000分子量的peg聚合物)。
c.核酸
提供包括seqidnos.1-16中任一种的编码抗pd-1多肽序列的核酸序列。编码抗pd-1抗体的重组核酸对于在宿主细胞中表达也是尤其有用的,该宿主实际上作为抗pd-1抗体的工厂。在各种实施方式中,从其他细胞组件或其他污染物(例如存在于细胞的其他核酸或蛋白)纯化时,通过标准技术分离核酸,包括碱/sds处理、cscl结合、柱层析、琼脂糖凝胶电泳和其他本领域已知技术。见例如f.ausubel,etal.,ed.(1987)currentprotocolsinmolecularbiology,greenepublishingandwileyinterscience,newyork。在各种实施方式中,核酸是例如dna或rna,且可包含或不包含内含序列。在优选实施方式中,核酸序列是cdna分子。在各种实施方式中,重组核酸提供编码抗pd-1抗体的重组基因,其独立于宿主基因组存在或作为宿主基因组的一部分。
在一些实施方式中,重组基因包含编码蛋白及蛋白表达调节元件的核酸。通常而言,存在于重组基因的调节元件包括转录启动子、核糖体结合位点、终止子以及可选的存在的操作子。启动子定义为引导rna聚合酶结合至dna并启动rna合成的dna序列。强启动子高频率启动mrna。优选的真核细胞处理元件是聚腺苷酸化信号。也可存在抗体相关内含子。遗传密码的退化是指除了两种氨基酸,多于一种单密码子编码特定氨基酸。这允许构建编码蛋白的合成dna,其中合成dna的核苷酸序列与本文公开的核苷酸序列显著不同,但也编码该蛋白。该合成dna也在本发明保护范围之内。
如果想在特定宿主细胞或生物体中表达dna,该dna的密码子用途可调整以最大化表达该蛋白。一种途径是选择反应特定宿主的密码子用途的密码子。编码相同氨基酸的可替换密码子显示于表3,其通过用t-胸苷替换u-尿嘧啶可自然转换成cdna分子。
表3:编码氨基酸的密码子
可通过表达载体促进重组基因在细胞中的表达。表达载体在此定义为在合适宿主中克隆dna的转录及其mrna翻译所需的dna序列。在各种实施方式中,这类载体用于在各种宿主例如细菌、蓝绿藻、植物细胞、昆虫细胞和动物细胞中表达真核dna。特殊设计的载体允许dna在两宿主之间例如细菌-酵母或细菌-动物细胞穿梭。优选的,除了重组基因,表达载体也包含在宿主细胞中自主复制的复制起点、选择性标记、有限数量的有用的限制酶位点、以及高复制数量的潜能。
在一些实施方式中,表达载体包括但不限于克隆载体、经修饰的克隆载体、特殊设计的质粒或病毒。这类表达载体是可从市场购买,包括哺乳动物、细胞、真菌(如毕赤酵母)以及昆虫细胞表达载体。在一些实施方式中,编码抗体的核酸可通过本领域已知技术整合至宿主染色体。
具有编码抗pd-1抗体可变重链区和可变轻链区中的一种或两种的一种或多种重组基因的核酸可用于产生结合至确定靶向区域或结合蛋白组件的完整结合蛋白。在一些实施方式中,提供完整的结合蛋白,其使用单基因编码包括重链可变区和轻链可变区,例如scfv的单链蛋白,或使用多组分重组区域产生重链可变区和轻链可变区。在一些实施方式中,通过生成包括重链可变区和轻链可变区的多肽产生结合蛋白区域。核酸序列的非限制性实例包括seqidno.18(反翻译重链f(ab))和seq.idno.19(反翻译f(ab))。
e.药物配方
抗pd-1抗体可单独提供或作为药物组合物或药剂提供,优选用于人体。鉴于此,可根据预防或治疗用途将化合物制备成各种药物剂量形式。药物剂量形式的实例是口服制剂、注射剂、栓剂、药膏、膏药等。这些制剂可通过已知的或本发明所属领域技术人员的传统方式制备。
结合至每种剂量形式单位的抗pd-1抗体的量可根据病人医疗条件或制剂类型而不同。每剂量单位的优选量是口服制剂约1-1000mg,注射剂约0.1-500mg,或者栓剂约5-1000mg。每天的剂量可根据病人症状、体重、年龄、性别和其他因素而不同,但成年人每天的通常范围是约0.1-5000mg,优选是约1-1000mg。制剂优选单剂给药或分两剂或四剂给药。
对于口服给药的固体制剂配方,将赋形剂、若有需要还将结合剂、分解剂、润滑剂、着色剂、矫味剂、香料等加入抗pd-1配方,然后通过传统方法制备成片状、包衣片、颗粒、粉末、胶囊或其他。这类辅助剂是本领域已知的,有用的实例是赋形剂例如乳糖、蔗糖、氯化钠、葡萄糖、淀粉、碳酸钙、高岭土、微晶纤维素和硅酸;结合剂如水、乙醇、丙醇、单糖浆、葡萄糖溶液、淀粉溶液明胶溶液、羟甲基纤维素、羟丙基纤维素、羟丙基淀粉、甲基纤维素、乙基纤维素、虫胶、磷酸钙和聚乙烯吡咯烷酮;分解剂例如干淀粉、海藻酸钠、琼脂粉末、碳酸氢钠、碳酸钙、十二醇硫酸钠、单甘油硬脂酸和乳糖;润滑剂如纯化的滑石粉、硬脂酸盐、硼砂和聚乙二醇;矫味剂如蔗糖、苦橙皮、柠檬酸和酒石酸等。
作为非限制性实施方式,片状可以下述组分及比例用传统方式制备。
作为非限制性实施方式,颗粒可以下述组分及比例用传统方式制备。
作为非限制性实施方式,胶囊可以下述组分及比例用传统方式制备。
制备用于口服的液体制剂,可添加矫味剂、缓冲液、稳定剂、香料等至化合物,用传统方法将混合物制备成口服液体制剂、糖浆、炼金药等。有用的矫味剂的实例如上所述。缓冲液的实例包括柠檬酸钠等。稳定剂的实例是胶黄芪、阿拉伯树胶、明胶等。作为非限制性实施方式,糖浆剂可用下述组分和比例用传统方式制备。
注射剂可通过添加ph调节剂、缓冲液、稳定剂、等渗剂、局部麻醉剂等至抗pd-1抗体用传统方式制备为皮下、肌肉或静脉注射剂。ph调节剂和缓冲液的实例是柠檬酸钠、乙酸钠、磷酸钠等。稳定剂的实例是焦亚硫酸钠、edta、巯基乙酸、硫代乳酸等。局部麻醉剂的实例是盐酸普鲁卡因、盐酸利多卡因等。等渗剂的实例是氯化钠、葡萄糖等。作为非限制性实施方式,注射剂可以下述组分及比例用传统方式制备。
栓剂可用常用方式通过在抗pd-1抗体中添加本领域已知的药学可接受的载体制备,例如聚乙二醇、羊毛脂、可可脂和油,脂肪酸甘油三酸脂和表面活性剂(若需要)如吐温。作为非限制性实施方式,栓剂可以下述组分及比例用传统方式制备。
为了制备药膏,可添加本领域所需的常用的碱、稳定剂、湿润剂、防腐剂等。通过传统方法将辅助剂和抗pd-1抗体制成药膏。碱的有用实例包括例如液状石蜡、白凡士林、白蜂蜡、辛基十二烷基醇、石蜡等。防腐剂可为所述的甲基对羟苯甲酸、乙基对羟苯甲酸、对羟苯甲酸丙酯等。
为了制备膏药、药膏、霜、凝胶或糊剂,用传统方式将化合物应用至常用的基底。基底的合适实例是纺织或无纺棉织物、人造纤维、化学纤维等以及软氯乙烯、聚乙烯、聚氨酯的膜或发泡片等。
f.用抗pd-1抗体处理
抗pd-1抗体,即hab-10d3及其变形,可用于治疗性的干扰pd-1和pd-l1和/或pd-1和pd-l2之间的相互作用。抗pd-1抗体单独或结合辅助物给药会以包含药学可接受载体的组合物形式。在一些实施方式中,本文描述的抗pd-1抗体在增强或提高免疫响应尤其是增强t细胞响应的情形下需要通过减弱由pd-1调节的抑制性信号。治疗微生物感染(例如细菌、真菌、病毒)和癌症尤其需要下调pd-1活性。在一些实施方式中,使用抗pd-1抗体阻断pd-1/pd-l1或pd-1/pd-l2相互作用导致增强t细胞响应,与pd-1途径中的下调作用一致。因此,在主体优选是人体中提供增强细胞免疫响应的方法,其包括给与抗pd-1抗体或其药物组合物。增强细胞免疫性是给与抗pd-1抗体治疗和/或预防性治疗的结果。
在一些实施方式中,抗pd-1抗体用于预防性治疗方法的一部分。在一些实施方式中,抗pd-1抗体用作疫苗的佐药以免疫主体,优选人体,对抗特定疾病,包括但不限于微生物感染或癌症。疫苗可用于一般人群或一般人群的子集。一般人群的子集是指有较大风险形成微生物感染或癌症的人。
在一些实施方式中,包括疫苗(预防性或治疗性疫苗)和抗pd-1抗体的组合物进行单次给药或在基础/加强疫苗范围内给药。优选的,疫苗基础和加强给药是不同的,以躲避针对第一递送疫苗的任何宿主免疫性,尤其是疫苗作为“非自身”重组载体的部分进行递送,例如重组非病毒(例如质粒)或病毒(例如腺病毒aav等)载体。因此,提供本文描述的具有一种或多种pd-1抗体结合一种或多种用于主体预防性免疫和/或治疗性治疗的疫苗的组合物以及将该疫苗组合物给药给主体。或者,抗pd-1抗体和疫苗可单独制备且在不同时间点共给药或给药。在一些实施方式中,疫苗包括基于细胞的疫苗。在各种实施方式中,具有抗pd-1抗体的基因细胞的疫苗在细胞治疗前在宿主外给药作为“引发”方法。在各种实施方式中,包含抗pd-1抗体的基因细胞的疫苗在细胞治疗前在宿主外给药作为“引发”方法。
抗pd-1抗体可用于治疗剂以增强病人的细胞免疫响应。在一些实施方式中,抗pd-1抗体单独给药或结合另外治疗剂给药。因此,本发明进一步吸收具有本文描述的具有一种或多种抗pd-1抗体和另外的治疗剂(例如治疗疫苗、抗微生物剂、化学治疗物、对抗其他治疗目标的抗体)的组合物。当与另外的治疗剂组合给药时,每种组分(即抗pd-1抗体和另外的治疗剂)在一些实施方式中,存在于单组分和单剂量给药中。或者,在一些实施方式中,每种组分单独制备且同时或在不同时间点给药给主体。
抗pd-1抗体还可用于治疗微生物感染的病人的治疗方法中,包括将本文所述的有效量抗pd-1抗体或其药物组合物给药给病人的步骤。在一些实施方式中,抗pd-1抗体单独给药或与其他抗微生物物质结合给药。在各种实施方式中,本文所述的抗pd-1抗体给药是治疗已被微生物病原体感染的病人的治疗方案的一部分(治疗性治疗)。或者,抗pd-1抗体在一些实时方式中,用作辅助包括个体对抗感染的预防性方法的一部分(即基于疫苗的方法)。例如,抗pd-1抗体用作辅助剂。
在一些实施方式中,微生物感染能够通过本文所述的抗pd-1抗体给药治疗。在一些实施方式中,微生物感染是持续感染。急性感染通常较快的通过免疫系统恢复身体,而持续感染可持续数月、数年或甚至一生。因此,持续感染是感染性微生物剂(例如病毒、细菌、寄生虫、支原体、真菌)在诱导免疫响应后仍未从宿主清除或消除的结果。持续感染可为慢性感染和/或潜在感染。这些感染可复发,涉及沉默阶段和未杀伤细胞的生产性感染或者甚至产生对宿主细胞的过度伤害。
本文描述的结合pd-1的抗pd-1抗体可作为治疗方案的一部分以治疗患癌主体(优选人体),或者作为预防性方案的一部分给药给易患癌症的个体。这些方法包括给予病人或个体有效量抗pd-1抗体或其组合物。在一些实施方式中,抗pd-1抗体作为单一疗法单独给药或与其他抗癌物质结合给药。作为非限制性实施例,本文描述的抗pd-1抗体结合抗癌疫苗作为预防性或治疗性方案中的辅助剂,其使用上述微生物感染部分相似的方法。因此,在一种实施方式中,本发明提供抑制主体(优选为人体)内肿瘤细胞生长的方法,包含将本文所述的治疗有效量的抗pd-1抗体给予主体。
癌症治疗和/或预防方法包括治疗和/或预防一种或多种常见类型的高频率确诊的癌症(例如血癌、乳腺癌、前列腺癌、结直肠癌、肺癌、前列腺癌、脑癌和皮肤癌),尤其是那些通常响应于免疫治疗的癌症。因此,通过给予本文的抗pd-1抗体阻断来自pd-1的抑制性信号用于治疗本发明的一种或多种癌症(例如卵巢癌、非淋巴实质器官癌(包括心脏、胚胎、骨骼肌和肺);乳腺癌;包括各种淋巴的头和颈癌,例如套细胞淋巴癌、非霍奇金b细胞淋巴癌,ptcl,腺瘤、鳞状细胞癌、喉癌、涎腺癌、胸腺瘤和胸腺癌;白血病;视网膜癌;食管癌;多发性骨髓瘤;黑素瘤;结肠直肠癌;肺癌;宫颈癌;子宫内膜癌;胆癌;肝癌;甲状腺滤泡状癌;胃癌;非小细胞肺癌;胶质瘤;尿道癌(urotheialcancer);膀胱癌;前列腺癌;肾细胞癌;浸润性管癌;以及胶质母细胞瘤)。
本发明的抗pd-1抗体可结合免疫原试剂,例如生癌细胞,纯化的肿瘤抗原(包括重组蛋白、肽和碳水化合物分子),经修饰的免疫细胞,例如嵌合抗原受体(car)t细胞,以及用编码免疫刺激细胞因子的基因转染的细胞。
本发明的抗pd-1抗体可结合标准的癌症治疗剂。例如,在一些实施方式中,抗pd-1抗体给药结合化学疗法。在这些情形下,在一些实施方式中,有可能降低化学疗法试剂的给药剂量。结合抗pd-1抗体和化学疗法的科学原理是由大多数化学疗法化合物的细胞毒性导致的细胞死亡可造成抗原呈递途径中的肿瘤抗原水平提升。结合pd-l1抑制性信号的其他有效组合疗法是辐射、手术、激素消除,以及靶向其他免疫检查点途径的抗体(例如抗ctla4抗体)。每种方案都在宿主内制造肿瘤抗原源。血管生成抑制剂可结合pd-l1阻断。血管生成抑制导致肿瘤细胞死亡,其可将肿瘤抗原流入宿主抗原呈递途径。
具有“抗癌”活性或“抗癌物质”的物质表明该物质抑制生癌细胞增殖,包括抑制肿瘤生长的物质。展示抗癌活性的物质包括但不限于具有细胞毒性化学疗法效果和抗癌疫苗的物质。
抗pd-1抗体及其组合物,可使用一种或多种下述途径给药给宿主:静脉注射(iv),肌肉注射(im),以及皮下注射(sc),静脉注射在治疗性抗体给药领域是标准。在一些实施方式中,使用这些组合物的方案可包括单价或多价组合物及各种组合形态应用。因此,这些制剂,在一些实施方式中,作为单独的或多剂量给药(即通过保持制剂的无菌条件,通过治疗方案在交错时间给予抗pd-1抗体)。
使用本发明抗pd-1抗体的剂量方案可根据多种因素选择,包括类型、物种、年龄、体重、性别和病人医疗条件;资料病症的严重性;给药途径;病人的肾脏、肝脏和心血管功能;以及使用的特定抗pd-1抗体。在一些实施方式中,根据化合物的有效性和稳定性剂量频率不同。剂量频率的实例包括每天、双周、每周、每月和双月。普通药师或兽医可容易的确定抗pd-1抗体的有效治疗和/或预防量并开具处方。在产生效力而不产生毒性的范围内达到抗pd-1抗体浓度的最佳精确度需要基于蛋白可获得性与目标区域的动力学方案。这涉及考虑分布、平衡以及清除药物。可预测的有效剂量范围可以是约0.1mg/kg-20mg/kg,或者0.5mg/kg-5mg/kg。
本文描述的抗pd-1抗体可在合适剂量单独使用。在一些实施方式中,需要与其他试剂共给药或序贯给药。在一些实施方式中,组合治疗方案中的个体组分在治疗过程中的不同时间分别给药或在分开的或单一组合形式中同时给药。应理解的是,本发明包括所有同时或交替治疗方案,术语“给药”应做相应理解。应理解的是,本发明抗pd-1抗体与其他试剂的组合的范围包括基本上任何用于治疗特定疾病的任何药学组合物的任何组合,包括但不限于微生物感染和癌症。当本文描述的抗pd-1抗体结合其他治疗剂使用,每种组分的剂量可与其单独使用时相同或不同。
实施例
下述实例进一步阐明本发明的不同特征。这些实例还描述了实践本发明的有用方法。这些实施例不限制本发明声明的范围。
实例1
生产抗pd-1抗体
用置于完全弗氏佐剂(cfa)的50μg纯化重组人pd-1肽皮下免疫5只balb/c小鼠,然后用置于非完全费氏佐剂(ifa)中的25μg先后免疫4次。预取血(pre-bleed),测试取血样本通过尾静脉收集至微型离心管,允许其凝固,并离心以收集血清。离心后,运行elisa对抗抗原,血清在-20℃存储于微型离心管中。为了开展elisa,简而言之,微量滴定板用来自转染hek293细胞的浓度为1-2μg/mlpbs的纯化重组pd-1融合蛋白覆盖,100μl/孔,在4℃培养过夜,然后每孔用3%bsa的pbs溶液250μl阻断。来自pd-1免疫小鼠的血清稀释液添加至每个孔并在室温下培养1-2小时。用pbs/吐温(0.05%)洗涤板,然后用山羊-抗鼠igg多克隆抗体共轭辣根过氧化物酶(hrp)室温培养1小时。洗涤后,板用tmb底物处理(kpl产品#52-00-01)并用分光光度计在od650处分析。产生抗pd-1抗体最高滴度的小鼠用于融合。按下述进行融合并且杂交瘤细胞上清液通过elisa测试抗pd-1活性。
为了形成杂交瘤,在第127天麻醉后从5只小鼠收集脾脏,在第0天试用peg基于标准方案,将该细胞和永生细胞系融合。这些细胞培养约10天并进行选择。
收集克隆培养上清液并通过上述elisa命中筛出纯化人pd-1肽。elisa命中进行扩展并在生化基屏幕上用纯化的重组肽筛查其抑制人pd-1:pd-l1(pd-l2)的能力。为了进行生化筛选,简言之,将100ngpd-l1(pd-l2)涂覆至pd-1分析缓冲液的96孔板中,然后添加10ng的人pd-1生物素和杂交瘤培养上清液。洗涤步骤后,使用strep-hrp和hrp化学发光底物定量结合的pd-1-生物素的量。选择并多克隆具有最大的抑制效果的克隆10d3并再次通过上述elisa和生化pd-1:pd-l1(pd-l2)反应分析筛出纯化的人pd-1。阳性多克隆进行扩展,制备杂交瘤的总rna,将抗体cdna进行pcr并使用标准测序技术测序。
克隆10d3的嵌合抗体通过融合克隆10d3的可变区形成,该克隆具有取代小鼠恒定区的人igg1恒定区,使用标准克隆技术将融合产物克隆进哺乳动物表达物。用聚乙烯亚胺(pei)转染,使克隆的融合产物在hek293细胞中短暂表达。简言之,悬浮hek293细胞在1x106细胞/ml密度播种,抗pd-1表达的dna与pei在opti-mem中结合并在室温培养15分钟。在培养后,将2μg/mldna和4μg/mlpei的dna-pei混合物加入细胞悬浮液。培养物生长4天。使用蛋白a亲和层析将嵌合抗体从hek293细胞纯化,抗体通过上述elisa和pd-1:pd-l1(pd-l2)结合分析表征。
使用公开可获取的toolforantibodyhuminzation(tabhu)服务器(circe.med.uniroma1.it/tabhu)将嵌合抗pd-1抗体人源化。嵌合抗pd-1抗体的重链和轻链序列上传至服务器。用具有超过2500抗体序列的数据库将这些序列进行blast比对,计算典型结构和生殖系基因。对于重链和轻链序列,标为aab24405的克隆显示了与嵌合抗pd-1抗体最高的同源性。与克隆aab24405非同源的嵌合抗pd-1抗体的fab区域中的选择骨架残基被选择用于通过合成基因合成技术回复突变至相应的人氨基酸。通过与人igg4(s228p突变体)恒定区融合形成该人源化抗pd-1抗体表达构建体,用上述方法表达和纯化,并制备用于进一步表征。
实例2
人pd-1:pd-l1相互作用的抑制
100ng人pd-l1涂覆于96孔板上的pd-1分析缓冲液中,然后添加10ng人pd-1生物素和不同量的hab-10d3抗pd-1中和抗体。洗涤步骤后,使用strep-hrp和hrp化学发光底物定量结合的pd-1-生物素的量。结果显示于图1a,其描述了通过hab-10d3以剂量依赖方式有效抑制pd-1:pd-l1结合。图1b使用嵌合抗pd-1抗体比较的阳性对照。
实例3
人pd-1:pd-l2相互作用的抑制
100ng人pd-l2涂覆于96孔板上的pd-1分析缓冲液中,然后添加6ng人pd-1生物素和不同量的hab-10d3抗pd-1中和抗体。洗涤步骤后,使用strep-hrp和hrp化学发光底物定量结合的pd-1-生物素的量。结果见图2,其描述了通过hab-10d3以剂量依赖方式有效抑制pd-1:pd-l2结合。
实例4
m.fascicularispd-1:pd-l1相互作用的抑制
100ngm.fascicularispd-1涂覆于96孔板上的pd-1分析缓冲液中,然后添加40ngm.fascicularispd-1生物素和不同量的hab-10d3抗pd-1中和抗体。洗涤步骤后,使用strep-hrp和hrp化学发光底物定量结合的pd-1-生物素的量。结果见图3-面板a,其描述了通过hab-10d3以剂量依赖方式有效抑制pd-1:pd-l2结合。图3b使用嵌合抗pd-1抗体比较的阳性对照。
实例5
使用人源化抗人pd-1中和抗体增强t细胞活化。
hek293细胞表达的pd-l1用表达nfat荧光素酶报告子和pd-1的jurkatt细胞培养。在各种量的抗pd-1抗体存在下,通过cd3交联激活t细胞。通过测量荧光素酶活性间接测量激活水平。在该试验中,bps,hab-10d3抗pd-1中和抗体(图4a)与已知可抑制pd-1活性的对照嵌合抗pd-1抗体比较(图4b)。总之,hab-10d3抑制的pd-1信号的ec50为0.38μg/ml(fig.4a),阳性对照嵌合抗体抑制pd-1信号ec50为0.29μg/ml。
实例6
人pd-1,默克抗pd-1ab,和bpshab-10d3之间的生物素标记pd-1突变结合比较
孔用100ngpd-l1,默克抗pa-1抗体(cat#71120)或bpshab-10d3(cat#h10d3)涂覆并在psb缓冲液中过夜。在随后的洗涤和阻断步骤之后,1ng生物素化的pd-1或突变体(置于50μl分析缓冲液中)添加至涂覆孔。seqidno.17提供了产生突变的碱基序列。图5描述了显示人pd-1氨基酸25-167的seqidno.17,结合至连接序列(加粗),结合至人igg1的fc(氨基酸100-330)(下划线),结合至亲和素标记(斜线)。以放大字体显示k78a,i126a,l128a,p130a,i134a,e136a的突变点。在添加strep-hrp之前在室温下培养反应2小时,然后加化学发光底物。在化学发光板读取器上读取发光量。
图6提供结果。默克抗pd-1抗体和bpshab-10d3显示了与人pd-1突变体不同的结合配置,表明在抗体结构和结合位点的差异。
序列表
<110>bps生物科学有限公司
<120>抗pd-1抗体及其用途
<130>10152-201285
<160>19
<170>siposequencelisting1.0
<210>1
<211>6
<212>prt
<213>小鼠(musmusculus)
<400>1
thrserglytyrphetrp
15
<210>2
<211>11
<212>prt
<213>小鼠(musmusculus)
<400>2
tyrilesertyraspglyserlysasntyrasn
1510
<210>3
<211>8
<212>prt
<213>小鼠(musmusculus)
<400>3
glyglyleuprovalmetasptyr
15
<210>4
<211>17
<212>prt
<213>小鼠(musmusculus)
<400>4
lysserserglnserleuleuaspaspasnasnglnlysasntyrleu
151015
ala
<210>5
<211>7
<212>prt
<213>小鼠(musmusculus)
<400>5
phealaserthrarggluser
15
<210>6
<211>9
<212>prt
<213>小鼠(musmusculus)
<400>6
glnglnhistyrthrthrprotyrthr
15
<210>7
<211>9
<212>prt
<213>小鼠(musmusculus)
<400>7
glnglnhistyrthrthrprotyrthr
15
<210>8
<211>11
<212>prt
<213>小鼠(musmusculus)
<400>8
trpileglytyrilesertyraspglyserlys
1510
<210>9
<211>5
<212>prt
<213>小鼠(musmusculus)
<400>9
leuprovalmetasp
15
<210>10
<211>7
<212>prt
<213>小鼠(musmusculus)
<400>10
lysasntyrleualatrptyr
15
<210>11
<211>10
<212>prt
<213>小鼠(musmusculus)
<400>11
leuleuilephephealaserthrargglu
1510
<210>12
<211>8
<212>prt
<213>小鼠(musmusculus)
<400>12
glnglnhistyrthrthrprotyr
15
<210>13
<211>117
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>unsure
<222>(1)..(117)
<223>合成构建体
<400>13
glnvalglnleuglngluserglyproglyleuvallysprosergln
151015
thrleuserleuthrcysservalserglytyrserilethrsergly
202530
tyrphetrpasntrpileargglnpheproglyasnlysleuglutrp
354045
ileglytyrilesertyraspglyserlysasntyrasnproserleu
505560
lysasnargvalthrileileargaspthrserlysasnglnpheser
65707580
leulysleuasnservalthralagluaspthralathrtyrtyrcys
859095
valargglyglyleuprovalmetasptyrtrpglyglnglythrser
100105110
valthrvalserser
115
<210>14
<211>113
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>unsure
<222>(1)..(113)
<223>合成构建体
<400>14
aspilevalmetthrglnserproserserleualaleuservalgly
151015
glulysalathrileglncyslysserserglnserleuleuaspasp
202530
asnasnglnlysasntyrleualatrptyrglnglnlysproglygln
354045
proprolysleuleuilephephealaserthrarggluserglyval
505560
proaspargpheileglyserglyserglythraspphethrleuthr
65707580
ileserserleuglnalagluaspleualaasptyrtyrcysglngln
859095
histyrthrthrprotyrthrpheglyglyglythrasnvalgluile
100105110
lys
<210>15
<211>233
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>unsure
<222>(1)..(233)
<223>合成构建体
<400>15
glnvalglnleuglngluserglyproglyleuvallysprosergln
151015
thrleuserleuthrcysservalserglytyrserilethrsergly
202530
tyrphetrpasntrpileargglnpheproglyasnlysleuglutrp
354045
ileglytyrilesertyraspglyserlysasntyrasnproserleu
505560
lysasnargvalthrileileargaspthrserlysasnglnpheser
65707580
leulysleuasnservalthralagluaspthralathrtyrtyrcys
859095
valargglyglyleuprovalmetasptyrtrpglyglnglythrser
100105110
valthrvalserseralaserthrlysglyproservalpheproleu
115120125
alaprocysserargserthrsergluserthralaalaleuglycys
130135140
leuvallysasptyrpheprogluprovalthrvalsertrpasnser
145150155160
glyalaleuthrserglyvalhisthrpheproalavalleuglnser
165170175
serglyleutyrserleuserservalvalthrvalproserserser
180185190
leuglythrlysthrtyrthrcysasnvalasphislysproserasn
195200205
thrlysvalasplysargvalgluserlystyrglyproprocyspro
210215220
procysproalaproglupheleugly
225230
<210>16
<211>220
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>unsure
<222>(1)..(220)
<223>合成构建体
<400>16
aspilevalmetthrglnserproserserleualaleuservalgly
151015
glulysalathrileglncyslysserserglnserleuleuaspasp
202530
asnasnglnlysasntyrleualatrptyrglnglnlysproglygln
354045
proprolysleuleuilephephealaserthrarggluserglyval
505560
proaspargpheileglyserglyserglythraspphethrleuthr
65707580
ileserserleuglnalagluaspleualaasptyrtyrcysglngln
859095
histyrthrthrprotyrthrpheglyglyglythrasnvalgluile
100105110
lysargthrvalalaalaproservalpheilepheproproserasp
115120125
gluglnleulysserglythralaservalvalcysleuleuasnasn
130135140
phetyrproargglualalysvalglntrplysvalaspasnalaleu
145150155160
glnserglyasnserglngluservalthrgluglnaspserlysasp
165170175
serthrtyrserleuserserthrleuthrleuserlysalaasptyr
180185190
glulyshislysvaltyralacysgluvalthrhisglnglyleuser
195200205
serprovalthrlysserpheasnargglyglucys
210215220
<210>17
<211>397
<212>prt
<213>人工序列(artificialsequence)
<220>
<221>unsure
<222>(1)..(397)
<223>合成构建体
<400>17
leuaspserproaspargprotrpasnproprothrpheserproala
151015
leuleuvalvalthrgluglyaspasnalathrphethrcysserphe
202530
serasnthrsergluserphevalleuasntrptyrargmetserpro
354045
serasnglnthrasplysleualaalapheprogluaspargsergln
505560
proglyglnaspcysargpheargvalthrglnleuproasnglyarg
65707580
aspphehismetservalvalargalaargargasnaspserglythr
859095
tyrleucysglyalaileserleualaprolysalaglnilelysglu
100105110
serleuargalagluleuargvalthrgluargargalagluvalpro
115120125
thralahisproserproserproargproalaglyglnpheglnile
130135140
gluglyargmetaspprolyssercysasplysthrhisthrcyspro
145150155160
procysproalaprogluleuleuglyglyproservalpheleuphe
165170175
proprolysprolysaspthrleumetileserargthrprogluval
180185190
thrcysvalvalvalaspvalserhisgluaspprogluvallysphe
195200205
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
210215220
argglugluglntyrasnserthrtyrargvalvalservalleuthr
225230235240
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
245250255
serasnlysalaleuproalaproileglulysthrileserlysala
260265270
lysglyglnproarggluproglnvaltyrthrleuproproserarg
275280285
gluglumetthrlysasnglnvalserleuthrcysleuvallysgly
290295300
phetyrproseraspilealavalglutrpgluserasnglyglnpro
305310315320
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
325330335
phepheleutyrserlysleuthrvalasplysserargtrpglngln
340345350
glyasnvalphesercysservalmethisglualaleuhisasnhis
355360365
tyrthrglnlysserleuserleuserproglylysglyglyglyleu
370375380
asnaspilepheglualaglnlysileglutrphisglu
385390395
<210>18
<211>699
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>misc_feature
<222>(1)..(699)
<223>合成构建体
<400>18
caggtgcagctgcaggaaagcggcccgggcctggtgaaaccgagccagaccctgagcctg60
acctgcagcgtgagcggctatagcattaccagcggctatttttggaactggattcgccag120
tttccgggcaacaaactggaatggattggctatattagctatgatggcagcaaaaactat180
aacccgagcctgaaaaaccgcgtgaccattattcgcgataccagcaaaaaccagtttagc240
ctgaaactgaacagcgtgaccgcggaagataccgcgacctattattgcgtgcgcggcggc300
ctgccggtgatggattattggggccagggcaccagcgtgaccgtgagcagcgcgagcacc360
aaaggcccgagcgtgtttccgctggcgccgtgcagccgcagcaccagcgaaagcaccgcg420
gcgctgggctgcctggtgaaagattattttccggaaccggtgaccgtgagctggaacagc480
ggcgcgctgaccagcggcgtgcatacctttccggcggtgctgcagagcagcggcctgtat540
agcctgagcagcgtggtgaccgtgccgagcagcagcctgggcaccaaaacctatacctgc600
aacgtggatcataaaccgagcaacaccaaagtggataaacgcgtggaaagcaaatatggc660
ccgccgtgcccgccgtgcccggcgccggaatttctgggc699
<210>19
<211>660
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>misc_feature
<222>(1)..(660)
<223>合成构建体
<400>19
gatattgtgatgacccagagcccgagcagcctggcgctgagcgtgggcgaaaaagcgacc60
attcagtgcaaaagcagccagagcctgctggatgataacaaccagaaaaactatctggcg120
tggtatcagcagaaaccgggccagccgccgaaactgctgattttttttgcgagcacccgc180
gaaagcggcgtgccggatcgctttattggcagcggcagcggcaccgattttaccctgacc240
attagcagcctgcaggcggaagatctggcggattattattgccagcagcattataccacc300
ccgtatacctttggcggcggcaccaacgtggaaattaaacgcaccgtggcggcgccgagc360
gtgtttatttttccgccgagcgatgaacagctgaaaagcggcaccgcgagcgtggtgtgc420
ctgctgaacaacttttatccgcgcgaagcgaaagtgcagtggaaagtggataacgcgctg480
cagagcggcaacagccaggaaagcgtgaccgaacaggatagcaaagatagcacctatagc540
ctgagcagcaccctgaccctgagcaaagcggattatgaaaaacataaagtgtatgcgtgc600
gaagtgacccatcagggcctgagcagcccggtgaccaaaagctttaaccgcggcgaatgc660
- 还没有人留言评论。精彩留言会获得点赞!