多源信息引导激光消融的诊疗方法及系统与流程
本发明涉及医学影像引导激光消融治疗技术领域,特别涉及一种多源信息引导激光消融的诊疗方法及系统。
背景技术
随着生物医学影像及智能化治疗技术的不断提高,现代肿瘤或病变的治疗已经需要将手术逐步转变为微创的智能化治疗方式实施,要求在精确定位手术靶点部位的同时,尽最大可能的降低对病人的正常组织及生理功能的创伤,从而规避了开放式手术遗留的手术创伤大、恢复期长等问题,将对生物组织及生理功能伤害降到最低,并且降低创伤恢复周期时间。肿瘤已成为威胁人类健康的一大杀手,因其引起的高致死率备受人们关注。
手术是目前肿瘤及病变治疗的首选方法。但是,目前手术中最难以解决的问题是肿瘤边界的精确判定及术中精准治疗问题。因此,开发具有多模态跨尺度的结构和功能影像将会为手术提供精准的图像引导具有重要的意义。精准的多模态影像引导的智能化激光消融治疗可以精确靶向定位手术区域、可在手术过程中实现监测和术中引导等特点,同时,在结构影像的基础上提出功能影像的架构,以保证手术过程中能够将功能区域完整保存。这样的诊疗装备具备诊疗一体化、创伤小、创伤恢复快、智能化程度高、疗效好等优点。
目前,多模态影像引导的手术治疗已经给肿瘤或病变治疗带来了很大的进步,使得极大地提高了手术的成功率并降低了术后的复发率。结合术中的功能信息的诊断也增加了手术成功率及降低了生理功能的创伤,但是手术治疗方式中严重依赖于医生经验,对临床手术经验少的医生,实现高精准的手术治疗将会具有重大的挑战。因此,开发智能化的诊疗装备对手术医生和外科医生来说具有重要的意义,同时在实现智能化的数字诊疗装备能够为将来的远程手术带来巨大的福音。
技术实现要素:
本发明旨在至少在一定程度上解决相关技术中的技术问题之一。
为此,本发明的一个目的在于提出一种多源信息引导激光消融的诊疗方法,该方法有效提高了诊疗的实时性、准确性和适用性,简单易实现。
本发明的另一个目的在于提出一种多源信息引导激光消融的诊疗系统。
为达到上述目的,本发明一方面实施例提出了一种多源信息引导激光消融的诊疗方法,包括以下步骤:获取医学多源信息或多模态信息,并量化生物组织及病变组织,并且获取所述病变组织的立体边界结构与术中当前病变组织的结构功能信息;通过激光消融病变组织消融治疗得到激光消融输出参数,并且结合生物病变组织的量化分析调整所述激光消融输出参数;根据所述多源信息引导所述激光消融输出参数,以进行激光消融治疗。
本发明实施例的多源信息引导激光消融的诊疗方法,通过使用多维度多源信息判断病变的过程中耦合匹配激光消融输出参数,实现实时的激光消融治疗,并达到精准的微创高效高精准病变治疗,不仅可以实现肿瘤或病变的高效智能化精准诊断,而且可以实现病变的实时治疗达到高效高精准的智能化治疗,并且能采集术中的实时成像,从而有效提高了诊疗的实时性、准确性和适用性,简单易实现。
另外,根据本发明上述实施例的多源信息引导激光消融的诊疗方法还可以具有以下附加的技术特征:
进一步地,在本发明的一个实施例中,所述多源信息包括术前医学影像、术中医学影像及术中信息,且所述激光消融输出参数包括激光辐射功率、激光输出持续时间、激光探头与生物组织的高度和激光探头旋转角度中的一种或多种。
进一步地,在本发明的一个实施例中,还包括:绘制病变边界及量化病变信息的功能效果;检测术中的血流功能、术中病变边界、术中神经功能信息。
进一步地,在本发明的一个实施例中,所述结合生物病变组织的量化分析调整所述激光消融输出参数,进一步包括:分析并构建病变区域的大小与病变组织量化,其中,在术前结构影像的诊断基础上完成术中小尺度的立体病变区域与边界构建,并且在术中建立功能信息与生物组织结构的对应。
进一步地,在本发明的一个实施例中,还包括:在得到术前与术中影像与信息的量化及分析和激光消融输出参数组后,构建基于影像信息与激光消融参数组的映射关系,并构建激光消融的耦联消融路径,以根据所述映射关系引导所述耦连消融路径在肿瘤或病变部位实施激光输出治疗。
为达到上述目的,本发明另一方面实施例提出了一种多源信息引导激光消融的诊疗系统,包括:信息获取模块,用于获取医学多源信息或多模态信息,并量化生物组织及病变组织,并且获取所述病变组织的立体边界结构与术中当前病变组织的结构功能信息;激光消融参数模块,用于通过激光消融病变组织消融治疗得到激光消融输出参数,并且结合生物病变组织的量化分析调整所述激光消融输出参数;引导模块,用于根据所述多源信息引导所述激光消融输出参数,以进行激光消融治疗。
本发明实施例的多源信息引导激光消融的诊疗系统,通过使用多维度多源信息判断病变的过程中耦合匹配激光消融输出参数,实现实时的激光消融治疗,并达到精准的微创高效高精准病变治疗,不仅可以实现肿瘤或病变的高效智能化精准诊断,而且可以实现病变的实时治疗达到高效高精准的智能化治疗,并且能采集术中的实时成像,从而有效提高了诊疗的实时性、准确性和适用性,简单易实现。
另外,根据本发明上述实施例的多源信息引导激光消融的诊疗系统还可以具有以下附加的技术特征:
进一步地,在本发明的一个实施例中,所述多源信息包括术前医学影像、术中医学影像及术中信息,且所述激光消融输出参数包括激光辐射功率、激光输出持续时间、激光探头与生物组织的高度和激光探头旋转角度中的一种或多种。
进一步地,在本发明的一个实施例中,还包括:绘制模块,用于绘制病变边界及量化病变信息的功能效果;检测模块,用于检测术中的血流功能、术中病变边界、术中神经功能信息。
进一步地,在本发明的一个实施例中,所述消融模块进一步用于分析并构建病变区域的大小与病变组织量化,其中,在术前结构影像的诊断基础上完成术中小尺度的立体病变区域与边界构建,并且在术中建立功能信息与生物组织结构的对应。
进一步地,在本发明的一个实施例中,还包括:构建模块,用于在得到术前与术中影像与信息的量化及分析和激光消融输出参数组后,构建基于影像信息与激光消融参数组的映射关系,并构建激光消融的耦联消融路径,以根据所述映射关系引导所述耦连消融路径在肿瘤或病变部位实施激光输出治疗。
本发明附加的方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
本发明上述的和/或附加的方面和优点从下面结合附图对实施例的描述中将变得明显和容易理解,其中:
图1为根据本发明一个实施例的多源信息引导激光消融的诊疗方法的流程图;
图2为根据本发明一个具体实施例的多源信息引导激光消融的诊疗方法的流程图;
图3为根据本发明一个实施例的多模信息与激光输出参数的关系构建示意图;
图4为根据本发明一个实施例的多源信息引导激光消融治疗的针对生物组织的路径规划示意图;
图5为根据本发明一个实施例的多源信息引导激光消融治疗带有横向参数针对生物组织的激光消融路径规划示意图;
图6为根据本发明一个实施例的多源信息引导激光消融的诊疗系统的结构示意图。
具体实施方式
下面详细描述本发明的实施例,所述实施例的示例在附图中示出,其中自始至终相同或类似的标号表示相同或类似的元件或具有相同或类似功能的元件。下面通过参考附图描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
下面参照附图描述根据本发明实施例提出的多源信息引导激光消融的诊疗方法及系统,首先将参照附图描述根据本发明实施例提出的多源信息引导激光消融的诊疗方法。
图1是本发明一个实施例的多源信息引导激光消融的诊疗方法的流程图。
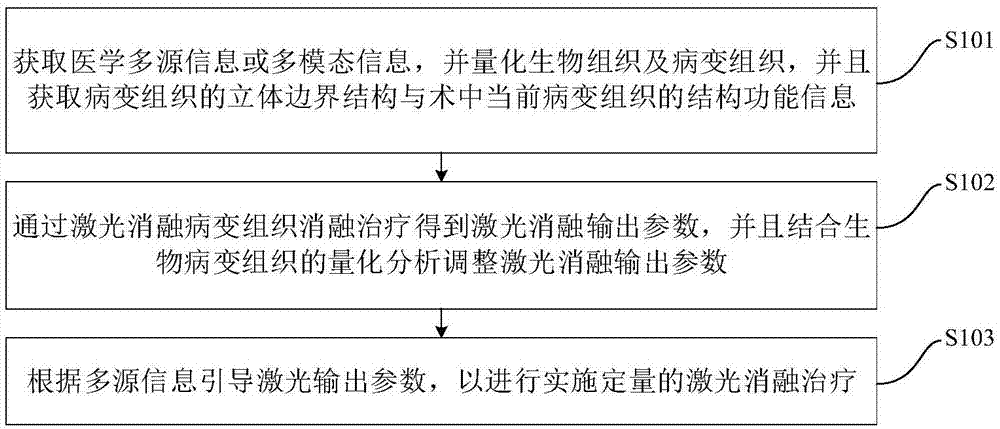
如图1所示,该多源信息引导激光消融的诊疗方法包括以下步骤:
在步骤s101中,获取医学多源信息或多模态信息,并量化生物组织及病变组织,并且获取病变组织的立体边界结构与术中当前病变组织的结构功能信息。
可以理解的是,术前术中多维度光学影像及信息诊断,获取病变识别的多源信息,在术前实现病变的识别与边界划分,并对手术过程中实现实时的诊断与病变组织的识别与诊断。也就说,医学多源信息或多模态信息的获取诊断,量化生物组织及病变组织,同时给出病变组织的立体边界结构及术中实时给出病变组织的结构功能信息。
如图2所示,术前术中多模态影像(ct(computedtomography,计算机体层摄影)/mri(magneticresonanceimaging,磁共振成像)/超声等术前影像)、手术路径规划及手术导航(在术前影像的引导下对手术路径实现规划,找到合适的手术入路)、在精准手术路径引导下术中影像(术中光学影像及功能信息采集及基于多源信息的术中病变诊断)。在诊疗过程中,基于mri、ct、pet(positronemissioncomputedtomography,正电子发射型计算机断层显像)和超声等的术前影像对生物组织实现大尺度、多模态影像采集与获取,将病变的影像精准识别并分析达到结构功能影像信息的精准融合,并具有微米级的空间分辨率,成像速度快,成像深度达到毫米级;同时还具有无创无辐射、能检测组织的深度形成透视效果的立体结构图像等特点。
进一步地,在本发明的一个实施例中,多源信息包括术前医学影像、术中医学影像及术中信息。
可以理解的是,术中多源信息具有生物组织小尺度结构影像与功能信息的诊断与识别,给出了病变区域的量化分析。多源信息包含了术前医学影像,该影像实现宽场大尺度生物组织成像,多源信息还包含了术中医学影像及术中信息,该影像及信息具有术中快速诊断效果。
也就是说,多源信息的诊断中具有术前宽场大尺度、多模态等医学影像效果,并在术前的影像中实现多模态影像分割、融合配准等操作,完成术前的大尺度诊断。术中多源信息包含了精准的快速成像、术中信息获取,其中的术中信息包含了生物组织病变结构功能信息,并通过合理的术中分析算法实现术中精准诊断与病变识别。
具体而言,如图3所示,多源信息的诊断中具有术前宽场大尺度、多模态等医学影像效果,并在术前的影像中实现多模态影像分割、融合配准等操作,完成术前的大尺度诊断。术中多源信息包含了精准的快速成像、术中信息获取,其中的术中信息包含了生物组织病变结构功能信息,该类术中信息的提取可使用oct(opticalcoherencetomography,光相干断层成像系统)、pat(photoacoustictomography,光声断层成像)、荧光成像、荧光光谱、拉曼光谱、电生理监测等医学术中信息采集实现,并通过合理的术中分析算法实现术中精准诊断与病变识别,的术前术中信息能够在常规的医学检查中得到,针对具体的病变实现初步筛查和分析,进一步地实现深入的检查。
术前影像能够在显示中实现激光消融手术治疗的导航与规划,结合手术规划实现病变部位的靶向定位,在治疗的同时实现微创的开放式精准治疗,在术前的影像诊断中,基于人工智能的精准诊断能够提高或改变目前的诊断方式,尤其是基于深度学习的诊断算法将综合多位专家医生的经验实现高效率高精准的病变诊断与精准识别,达到甚至超出专家医生的诊断结果。
进一步地,在本发明的一个实施例中,还包括:绘制病变边界及量化病变信息的功能效果;检测术中的血流功能、术中病变边界、术中神经功能信息。
可以理解的是,使用基于人工智能方法实现术前诊断,绘制病变边界及量化病变信息的功能效果;还包括术中的血流功能、术中病变边界定位、术中神经功能信息提取等功能信息判断。其中,术前影像的诊断具有基于深度学习的深度方向和表面方向的边界方向诊断及病变部位整体结构影像及病变边界区域的绘制。
具体而言,术中成像与信息获取后,将基于图像结构纹理特征、光谱特性、光学衰减等的术中肿瘤病变特征的识别与提取,智能化的识别肿瘤或病变信息。术中成像与信息获取将能够提供术中肿瘤或病变的边界实时诊断与识别,同时,定位生物组织的功能信息与肢体端的映射关系,辅助后续激光治疗过程中保存好生理功能;结合生理功能分析达到精准的血流量采集或血流速度的采集与获取,进一步地,获取生物组织的代谢情况,分析病变组织的病变程度。
综上,基于术前的大尺度宽场影像实现精准的肿瘤或病变边界的绘制及病变信息的量化,同时给出术中的生理功能定位信息,该信息如血管分布状态、血流量、神经功能信息等,得到生物组织的结构功能影像,并根据生物组织的结构功能影像确定治疗区域,并在治疗区域内进行扫描以获取准实时图像。
在步骤s102中,通过激光消融病变组织消融治疗得到激光消融输出参数,并且结合生物病变组织的量化分析调整激光消融输出参数。
可以理解的是,合理选择合适的激光消融参数组,基于激光消融病变组织消融治疗给出激光治疗消融输出参数,同时结合生物病变组织的量化分析控制合适的激光消融输出参数。
具体而言,如图2所示,激光消融输出参数的控制(在术前/术中诊断引导下对激光输出参数控制达到精准的消融治疗)、术中成像与信息采集实时监测激光消融效果(观察激光消融治疗后生物组织的结构影像及功能信息)。基于激光消融输出参数实时控制激光消融治疗,该治疗主要根据实际的消融区域实现特定的组织消融治疗,针对特定的生物组织调节激光消融输出参数,根据输出参数在术中实时调节并进一步分析。激光消融治疗的激光输出参数组能够给生物组织的激光消融治疗提供进一步精准的激光消融治疗效果。
术中成像与信息获取后,将基于图像结构纹理特征、光谱特性、光学衰减等的术中肿瘤病变特征的识别与提取,智能化的识别肿瘤或病变信息。术中成像与信息获取将能够提供术中肿瘤或病变的边界实时诊断与识别,同时,定位生物组织的功能信息与肢体端的映射关系,辅助后续激光治疗过程中保存好生理功能;结合生理功能分析达到精准的血流量采集或血流速度的采集与获取,并获取生物组织的代谢情况,分析病变组织的病变程度。
进一步地,在本发明的一个实施例中,结合生物病变组织的量化分析调整激光消融输出参数,进一步包括:分析并构建病变区域的大小与病变组织量化,其中,在术前结构影像的诊断基础上完成术中小尺度的立体病变区域与边界构建,并且在术中建立功能信息与生物组织结构的对应。
可以理解的是,术前影像与术中信息的病变量化分析,具体包括:病变区域的大小与病变组织量化分析构建,在术前结构影像的诊断基础上完成术中小尺度的立体病变区域与边界构建,同时在术中建立功能信息与生物组织结构的对应。
进一步地,在本发明的一个实施例中,激光消融输出参数包括激光辐射功率、激光输出持续时间、激光探头与生物组织的高度和激光探头旋转角度中的一种或多种。
可以理解的是,激光消融输出参数调节实现精准治疗,具体包括:激光辐射功率、激光输出持续时间、激光探头与生物组织的高度、激光探头旋转角度等因素。其中,激光辐射功率与持续时间是激光固有可调节参数,功率和持续时间的调节可使用激光设备直接调节或者使用计算机控制输出调节;激光探头与生物组织的高度、激光探头旋转角度都是外部前端设备所需要给出的调节参数,高度与角度的调节过程中需要辅助特定的前端设备装置。
具体而言,激光消融治疗需要使用合适的消融输出参数实现精准的激光参数控制,以至于在消融过程中达到高效高精准的治疗肿瘤或病变区域。激光输出参数主要包含了激光输出辐射功率、激光输出持续时间、激光探头与生物组织的高度、激光探头旋转角度等因素。
其中,术中的病变诊断与识别将能够提供实时的丰富的影像引导信息或者功能结构引导信息实现激光消融参数的控制与耦合,具体包括:激光辐射功率与持续时间是激光固有可调节参数,功率和持续时间的调节可使用激光设备直接调节或者使用计算机控制输出调节;激光探头与生物组织的高度、激光探头旋转角度都是外部前端设备所需要给出的调节参数,高度与角度的调节过程中需要辅助特定的前端设备装置。
在步骤s103中,根据多源信息引导激光消融输出参数,以进行激光消融治疗。
可以理解的是,本发明实施例结合多源信息引导激光消融的激光输出参数控制的诊疗方法,开发结构简单及易于操作的前端结构并实现多源信息引导激光消融治疗,从而实现对病变精准消融治疗。如图2所示,在术中影像的引导观察病变位置直至病变组织治疗完成(结束激光输出,完成消融治疗)。
进一步地,在本发明的一个实施例中,还包括:在得到术前与术中影像与信息的量化及分析和激光消融输出参数组后,构建基于影像信息与激光消融参数组的映射关系,并构建激光消融的耦联消融路径,以根据映射关系引导耦连消融路径在肿瘤或病变部位实施激光输出治疗。
可以理解的是,映射关系主要是基于多源信息的肿瘤或病变边界量化与激光消融输出参数组织的结构化耦合与对应,并对在耦合过程中设计相应的前端机构实现影像/信息引导激光消融参数的合适输出,同时在激光耦联路径下达到精准的消融治疗。
具体而言,如图4所示,采用客观计算方法来对诊疗系统的基本架构进行集成,其中,在术前与术中影像与信息的量化及分析和激光消融输出参数组的计算后,构建基于影像信息与激光消融参数组的映射关系,并构建激光消融的耦联消融路径。在生物组织上的激光消融路径具有立体效果,尤其是针对立体结构的肿瘤或病变部位位置,激光消融同样具有重要的耦联路径,该路径与激光输出参数之间的关系如下式所示:
rtpath={pi(ai,bi,ci),li}={pi(ai,bi,ci),(ti,pi,θi,hi},i=1,...,n其中,rtpath是激光消融的规划路径,a、b、c分别是激光消融模型的横向和纵向消融参数;t、p、θ、h是激光辐射参数,它们分别是激光辐射功率、辐射持续时间、探头相对旋转角度和激光探头与生物组织表面的高度。pi是激光消融过程中每一个消融参数点的中心位置。
构建的多源信息与激光消融参数之间的映射关系引导激光消融耦连消融路径在肿瘤或病变部位实施激光输出治疗,建立在肿瘤区域的外部消融路径、中间消融路径、内部消融路径。设置合适的激光消融参数组并设置起始点p1,激光探头将会按照设计的探头路径进行,最后达到终点pk。
进一步地,通过控制激光消融输出参数实现激光探头的内部路径、中间路径、外部路径的激光参数结构量化及诊疗控制输出;内部路径种的激光输出参数中功率、持续时间、探头高度和旋转角度相对最大,中间路径适当降低输出参数,外部路径中将输出参数设置最小。
如图5所示,经过多源信息引导激光消融的光学诊疗系统治疗之后的生物组织中,冠状面的结构能够清晰分析激光消融耦联路径与激光消融边界和生物病变组织边界的匹配程度。在冠状面上能够进一步看出激光消融后带有横向参数的耦联激光消融路径规划。该路径在生物组织层面上能够更具体体现冠状面的多源信息引导激光消融的智能化治疗过程。
需要说明的是,基于fd-oct和荧光成像及高光谱成像能提供微米级分辨率的图像信息引导手术,克服了现有超声、生物活检的手术中引导和分析,同时还能降低ct的放射性,克服了术中mri、ct的分辨率缺陷;提供了方便的扫描方式、简单装置结构和光路结构、高度降低制造成本,使用二维振镜提高了成像速度以至于在手术过程中能够实时引导手术实施。
本发明实施例的应用场景主要是肿瘤、病变的切除,尤其是肿瘤边界和残余肿瘤的辨识,例如神经外科的手术中的肿瘤(胶质瘤、室管膜瘤、黑色素瘤等)。探头具有结构简单、成本低廉、病变治疗使用简单、操作简单、成像速度快、图像空间分辨率高、体积小、质量轻、图像效果明显等优点。
综上,本发明实施例的方法既可以对软组织尤其是脑组织及脑干组织的立体结构功能成像,又可以分辨采集oct和荧光高光谱图像,并且能采集术中的实时成像,具有结构简单医学影像及信息丰富、智能化程度高、成本低廉、操作简单、术前术中病变信息量化成像速度快、诊疗一体化程度高图像空间分辨率高、体积小、基于图像诊断精度高、质量轻治疗效果明显、图像效果明显术中对生理功能损伤小等的优点。
根据本发明实施例提出的多源信息引导激光消融的诊疗方法,通过使用多维度多源信息判断病变的过程中耦合匹配激光消融输出参数,实现实时的激光消融治疗,并达到精准的微创高效高精准病变治疗,不仅可以实现肿瘤或病变的高效智能化精准诊断,而且可以实现病变的实时治疗达到高效高精准的智能化治疗,并且能采集术中的实时成像,从而有效提高了诊疗的实时性、准确性和适用性,简单易实现。
其次参照附图描述根据本发明实施例提出的多源信息引导激光消融的诊疗系统。
图6是本发明一个实施例的多源信息引导激光消融的诊疗系统的结构示意图。
如图6所示,该多源信息引导激光消融的诊疗系统10包括:信息获取模块100、激光消融参数模块200和引导模块300。
其中,信息获取模块100用于获取医学多源信息或多模态信息,并量化生物组织及病变组织,并且获取病变组织的立体边界结构与术中当前病变组织的结构功能信息。激光消融参数模块200用于通过激光消融病变组织消融治疗得到激光消融输出参数,并且结合生物病变组织的量化分析调整激光消融输出参数。引导模块300用于根据多源信息引导激光消融输出参数,以进行激光消融治疗。本发明实施例的系统10通过使用多维度多源信息判断病变的过程中耦合匹配激光消融输出参数,实现实时的激光消融治疗,从而有效提高了诊疗的实时性、准确性和适用性,简单易实现。
进一步地,在本发明的一个实施例中,多源信息包括术前医学影像、术中医学影像及术中信息,且激光消融输出参数包括激光辐射功率、激光输出持续时间、激光探头与生物组织的高度和激光探头旋转角度中的一种或多种。
进一步地,在本发明的一个实施例中,本发明实施例的系统10还包括:绘制模块和检测模块。
其中,绘制模块用于绘制病变边界及量化病变信息的功能效果;检测模块,用于检测术中的血流功能、术中病变边界、术中神经功能信息。
进一步地,在本发明的一个实施例中,消融模块300进一步用于分析并构建病变区域的大小与病变组织量化,其中,在术前结构影像的诊断基础上完成术中小尺度的立体病变区域与边界构建,并且在术中建立功能信息与生物组织结构的对应。
进一步地,在本发明的一个实施例中,本发明实施例的系统10还包括:构建模块。其中,构建模块,用于在得到术前与术中影像与信息的量化及分析和激光消融输出参数组后,构建基于影像信息与激光消融参数组的映射关系,并构建激光消融的耦联消融路径,以根据映射关系引导耦连消融路径在肿瘤或病变部位实施激光输出治疗。
需要说明的是,前述对多源信息引导激光消融的诊疗方法实施例的解释说明也适用于该实施例的多源信息引导激光消融的诊疗系统,此处不再赘述。
根据本发明实施例提出的多源信息引导激光消融的诊疗系统,通过使用多维度多源信息判断病变的过程中耦合匹配激光消融输出参数,实现实时的激光消融治疗,并达到精准的微创高效高精准病变治疗,不仅可以实现肿瘤或病变的高效智能化精准诊断,而且可以实现病变的实时治疗达到高效高精准的智能化治疗,并且能采集术中的实时成像,从而有效提高了诊疗的实时性、准确性和适用性,简单易实现。
此外,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括至少一个该特征。在本发明的描述中,“多个”的含义是至少两个,例如两个,三个等,除非另有明确具体的限定。
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
- 还没有人留言评论。精彩留言会获得点赞!