雷帕霉素缓释剂型及制备方法、雷帕霉素缓释注射剂及应用与流程
本发明涉及医药
技术领域:
,尤其是涉及一种雷帕霉素缓释剂型及制备方法、雷帕霉素缓释注射剂及应用。
背景技术:
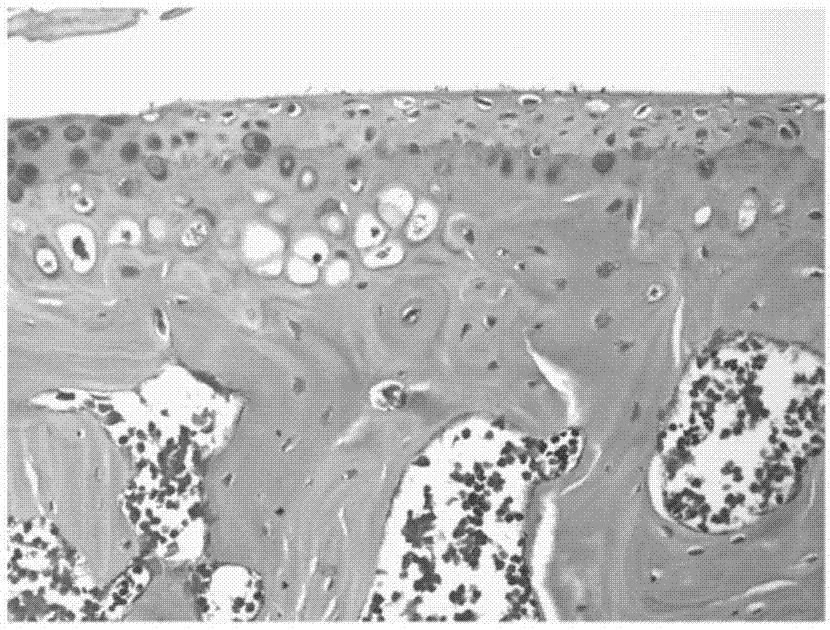
骨关节炎(oa)也称为退行性关节炎,是在老年人和肥胖者中最普遍的疾病。oa是关节的疾病,但是不同于类风湿性关节炎(ra),这种疾病不是系统性的,通常只影响一个或数个关节。这种疾病导致关节软骨的总的破坏,下方骨头的硬化和骨赘形成,造成运动能力丧失和疼痛。最终的结果往往是需要全关节置换。世界卫生组织调查发现,全世界有10%的男性和18%的女性患有不同程度的oa,在亚洲地区,每6个人中就有1人患有oa,而目前我国oa患者已超过1亿,并随着我国人口老龄化的加剧,这一数据呈逐年上升的趋势。oa造成的疼痛和不便不仅影响患者的日常生活质量,其高达53%的致残率更使其成为人类致残的头号杀手。在西方发达国家,膝骨关节炎诊治的相关费用逐年上升,约占国民生产总值的1-2.5%,给患者和社会带来了沉重的经济负担。oa的发生与多种因素有关,包括年龄、性别、遗传、肥胖和创伤等。目前临床上的oa药物,治疗oa的症状而不是疾病本身。缓解oa症状的常用药物包括非甾体抗炎药物(nsaid)、非麻醉镇痛剂、麻醉镇痛剂和糖皮质激素等。因此,对于治疗oa存在高度未满足的医疗需求。而对于治疗oa的药物,如雷帕霉素,其为疏水性药物,不能直接注射,需要采用有机溶剂如dmso溶解才可以注射,但有机溶剂具有毒性,会给患者带来不可避免的毒副作用。此外,还存在药物保留时间短,需要多次重复注射的问题。有鉴于此,特提出本发明。技术实现要素:本发明的第一个目的在于提供一种雷帕霉素缓释剂型,以缓解现有技术中存在的雷帕霉素保留时间短,需要多次重复注射的技术问题。本发明的第二个目的在于提供上述雷帕霉素缓释剂型的制备方法,该方法操作简单,方便快捷,制备得到的雷帕霉素缓释剂型稳定性良好,利于工业化生产。本发明的第三个目的在于提供一种雷帕霉素缓释注射剂,缓解了现有技术中雷帕霉素需要采用有机溶剂如dmso溶解才可以注射,会给患者带来不可避免的毒副作用,且保留时间短,需要多次重复注射的技术问题。本发明的第四个目的在于提供上述雷帕霉素缓释剂型或雷帕霉素缓释注射剂在抑制mtorc1中的应用。本发明的第五个目的在于提供上述雷帕霉素缓释剂型或雷帕霉素缓释注射剂在制备治疗骨关节炎的药物中的应用。本发明提供了一种雷帕霉素缓释剂型,所述雷帕霉素缓释剂型包括:雷帕霉素和缓释材料;其中,所述雷帕霉素与所述缓释材料的质量比为1:10-50。进一步地,所述雷帕霉素还包括雷帕霉素衍生物和雷帕霉素类似物。进一步地,所述缓释材料包括高分子缓释材料和小分子缓释材料;优选地,所述高分子缓释材料选自海藻酸钠、壳聚糖、聚乳酸-羟基乙酸共聚物、聚己内酯、聚乳酸、聚三亚甲基碳酸酯、聚羟基乙酸、聚羟基丁酸酯、聚羟基丁酸羟基戊酸共聚物、聚原酸酯和聚酸酐中的一种或多种;优选地,所述小分子缓释材料包括脂类化合物,优选为类脂,更优选为磷脂和/或类固醇。优选地,所述高分子缓释材料的重均分子量为10000-100000道尔顿,优选为10000-80000道尔顿,更优选为10000-50000道尔顿。进一步地,还包括乳化剂,优选为亲水性乳化剂;优选地,所述乳化剂选自聚乙烯醇、吐温80、peg-100硬脂酸酯、甘油硬脂酸酯、花生醇、脂肪醇聚氧乙烯醚、山嵛酸甘油酯或鲸蜡硬脂基葡糖苷中的一种或多种。本发明还提供了上述的雷帕霉素缓释剂型的制备方法,所述制备方法包括:提供配方量的雷帕霉素和缓释材料的有机溶液,与乳化剂混合均匀,去除有机溶剂后,得到所述雷帕霉素缓释剂型。进一步地,所述有机溶剂的沸点不高于50℃;优选地,所述有机溶剂选自丙酮、氯仿、甲胺、二甲胺、乙醚、戊烷、二氯甲烷或二硫化碳中的一种或多种。进一步地,所述有机溶液为每10-30mg缓释材料和0.1-2mg雷帕霉素在0.1-2ml有机溶剂中溶解得到;优选地,每0.1-2ml有机溶剂与1-10ml乳化剂混合;优选地,所述缓释材料为聚乳酸-羟基乙酸,所述有机溶剂为二氯甲烷,所述乳化剂为1%(w/v)聚乙烯醇。本发明还提供了一种雷帕霉素缓释注射剂,包括上述的雷帕霉素缓释剂型或应用上述的制备方法制备得到的雷帕霉素缓释剂型和溶剂。本发明还提供了上述的雷帕霉素缓释剂型或应用上述的制备方法制备得到的雷帕霉素缓释剂型或上述的雷帕霉素缓释注射剂在抑制mtorc1中的应用。另外,本发明还提供了上述的雷帕霉素缓释剂型或应用上述的制备方法制备得到的雷帕霉素缓释剂型或上述的雷帕霉素缓释注射剂在制备治疗骨关节炎的药物中的应用。本发明提供的雷帕霉素缓释剂型,包括质量比为1:10-50的雷帕霉素和缓释材料。该雷帕霉素缓释剂型药物含量高,使用体积小,能够起到药物缓释、控释的作用。同时,该雷帕霉素缓释剂型作用靶点清楚,通过抑制mtorc1,能够有效的缓解和治疗骨关节炎。并且,通过缓释材料的包封,能够使得雷帕霉素给药一次便维持较长期的治疗效果,减少多次给药的成本,降低了患者的疼痛感和刺激性,减少了由于有机溶剂带来的不良反应和安全事故。本发明提供的上述雷帕霉素缓释剂型的制备方法,提供配方量的雷帕霉素和缓释材料的有机溶液,与乳化剂混合均匀,去除有机溶剂后,制得雷帕霉素缓释剂型。该方法操作简单,方便快捷,制备得到的雷帕霉素缓释剂型稳定性良好,体内滞留时间长、释药性好、生物利用度高,利于工业化生产的推广应用。本发明提供的雷帕霉素缓释注射剂,包括上述雷帕霉素缓释剂型和溶剂,其能够不借助于有机溶剂直接注射,减少由于有机溶剂带来的不良反应和安全事故,并且在体内保留时间长,无需多次重复注射,减少多次给药的成本,降低了患者的疼痛感和刺激性。附图说明为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。图1a为本发明实验例1提供的dmm模型小鼠术后4周oa的染色结果图;图1b为本发明实验例1提供的雷帕霉素缓释剂型通过mtroc1靶点治疗dmm模型小鼠术后4周oa的染色结果图;图1c为本发明实验例1提供的dmm模型小鼠术后8周oa的染色结果图;图1d为本发明实验例1提供的雷帕霉素缓释剂型通过mtroc1靶点治疗dmm模型小鼠术后8周oa的染色结果图;图2a为本发明实验例1提供的术后4周根据番红o-快速绿染色的oarsi评分;图2b为本发明实验例1提供的术后8周根据番红o-快速绿染色的oarsi评分;图3a为本发明实验例2提供的aclt模型小鼠术后4周oa的染色结果图;图3b为本发明实验例2提供的雷帕霉素缓释剂型通过mtroc1靶点治疗aclt模型小鼠术后4周oa的染色结果图;图3c为本发明实验例2提供的aclt模型小鼠术后8周oa的染色结果图;图3d为本发明实验例2提供的雷帕霉素缓释剂型通过mtroc1靶点治疗aclt模型小鼠术后8周oa的染色结果图;图3e为本发明实验例2提供的aclt模型小鼠术后12周oa的染色结果图;图3f为本发明实验例2提供的雷帕霉素缓释剂型通过mtroc1靶点治疗aclt模型小鼠术后12周oa的染色结果图;图4a为本发明实验例2提供的术后4周根据番红o-快速绿染色的oarsi评分;图4b为本发明实验例2提供的术后8周根据番红o-快速绿染色的oarsi评分;图4c为本发明实验例2提供的术后12周根据番红o-快速绿染色的oarsi评分。具体实施方式除非本文另有定义,连同本发明使用的科学和技术术语应具有本领域普通技术人员通常理解的含义。术语的含义和范围应当清晰,然而,在任何潜在不明确性的情况下,本文提供的定义优先于任何字典或外来定义。在本申请中,除非另有说明,“或”的使用意味着“和/或”。此外,术语“包括”及其他形式的使用是非限制性的。除非另有说明,本发明的方法和技术一般根据本领域众所周知,且如各种一般和更具体的参考文献中所述的常规方法来进行,所述参考文献在本说明书自始至终引用和讨论。连同本文描述的医学和药物化学使用的命名法、以及其实验室程序和技术是本领域众所周知和通常使用的那些。本发明提供了一种雷帕霉素缓释剂型,包括:雷帕霉素和缓释材料。雷帕霉素(rapa)分子式为c51h79no13,为白色固体结晶,熔点为183-185℃,亲脂性,溶解于甲醇、乙醇、丙酮、氯仿等有机溶剂,极微溶于水,几乎不溶于乙醚。其化学结构式如式(ⅰ)所示:缓释材料是指能够通过延缓药物从该剂型中的释药速率,降低药物进入机体的吸收速率,从而起到更佳的治疗效果的材料。在本发明中,雷帕霉素通过缓释材料的包封,能够延缓雷帕霉素的释药速率,给药一次便维持较长期的治疗效果,减少多次给药的成本,降低了患者的疼痛感和刺激性。其中,雷帕霉素与缓释材料的质量比为1:10-50,例如可以为,但不限于1:10、1:20、1:30、1:40或1:50。当雷帕霉素与缓释材料的质量比在1:10-50范围内时,得到的雷帕霉素缓释剂型稳定性良好,体内滞留时间长、释药性好、生物利用度高。优选地,雷帕霉素与缓释材料的质量比为1:10-30,更优选为1:20。当雷帕霉素与缓释材料的质量比为1:20时,得到的雷帕霉素缓释剂型稳定性更好,体内滞留时间更长、释药性更好、生物利用度更高。本发明提供的雷帕霉素缓释剂型,药物含量高,使用体积小,能够起到药物缓释、控释的作用。同时,该雷帕霉素缓释剂型作用靶点清楚,通过抑制mtorc1,能够有效的缓解和治疗骨关节炎。并且,通过缓释材料的包封,能够使得雷帕霉素给药一次便维持较长期的治疗效果,减少多次给药的成本,降低了患者的疼痛感和刺激性,减少了由于有机溶剂带来的不良反应和安全事故。在一些优选的实施方式中,雷帕霉素还包括雷帕霉素衍生物和雷帕霉素类似物。在一些优选的实施方式中,缓释材料包括高分子缓释材料和小分子缓释材料。优选地,高分子缓释材料选自海藻酸钠、壳聚糖、聚乳酸-羟基乙酸共聚物、聚己内酯、聚乳酸、聚三亚甲基碳酸酯、聚羟基乙酸、聚羟基丁酸酯、聚羟基丁酸羟基戊酸共聚物、聚原酸酯和聚酸酐中的一种或多种;优选地,小分子缓释材料包括脂类化合物,优选为类脂,更优选为磷脂和/或类固醇。其中,磷脂例如可以为,但不限于卵磷脂、鞘磷脂、脑磷脂、磷脂酰丝氨酸、磷脂酰甘油、二磷脂酰甘油或磷脂酰肌醇中的一种或多种;类固醇例如可以为,但不限于胆固醇、谷甾醇、豆固醇、麦角固醇或其衍生物中的一种或多种。更优选地,缓释材料为聚乳酸-羟基乙酸共聚物。聚乳酸-羟基乙酸共聚物(poly(lactic-co-glycolicacid),plga)由两种单体——乳酸和羟基乙酸随机聚合而成,是一种可降解的功能高分子有机化合物,具有良好的生物相容性、无毒、良好的成囊和成膜的性能。当缓释材料选择为聚乳酸-羟基乙酸共聚物时,得到的雷帕霉素缓释剂型具有更优异的稳定性及释药性。在一些优选的实施方式中,高分子缓释材料的重均分子量为10000-100000道尔顿,例如可以为,但不限于10000道尔顿、20000道尔顿、30000道尔顿、40000道尔顿、50000道尔顿、60000道尔顿、70000道尔顿、80000道尔顿、90000道尔顿或100000道尔顿,优选为10000-80000道尔顿,更优选为10000-50000道尔顿。。缓释材料的分子量可以根据是缓解性处理还是治疗性处理而不同。在缓解性应用中,以相对低频率的间隔长期给予相对低的剂量,即需要雷帕霉素的缓释周期更长,此时,可以选择分子量较大的缓释材料。在治疗性应用中,有时需要以相对短的间隔给予相对高的剂量,直至疾病的进展被延缓或停止,即需要雷帕霉素的缓释周期相对较短,此时,可以选择分子量较小的缓释材料。在一些优选的实施方式中,还包括乳化剂,优选为亲水性乳化剂。乳化剂是能够改善乳浊液中各种构成相之间的表面张力,使之形成均匀稳定的分散体系或乳浊液的物质。在本发明中,应用乳化剂对雷帕霉素和缓释材料进行乳化,使得雷帕霉素达到能够直接注射的目的,减少了由于有机溶剂带来的不良反应和安全事故。优选地,乳化剂选自聚乙烯醇、吐温80、peg-100硬脂酸酯、甘油硬脂酸酯、花生醇、脂肪醇聚氧乙烯醚、山嵛酸甘油酯或鲸蜡硬脂基葡糖苷中的一种或多种,更优选地,乳化剂为聚乙烯醇。应用聚乙烯醇对雷帕霉素和缓释材料进行乳化,使得雷帕霉素达到能够直接注射的目的,减少了由于有机溶剂带来的不良反应和安全事故。本发明还提供了上述的雷帕霉素缓释剂型的制备方法,包括:提供配方量的雷帕霉素和缓释材料的有机溶液,与乳化剂混合均匀,去除有机溶剂后,得到雷帕霉素缓释剂型。本发明提供的上述雷帕霉素缓释剂型的制备方法,操作简单,方便快捷,制备得到的雷帕霉素缓释剂型稳定性良好,体内滞留时间长、释药性好、生物利用度高,利于工业化生产的推广应用。在一些优选的实施方式中,有机溶剂的沸点不高于50℃。有机溶剂的沸点不高于50℃,能够保证在后续去除的过程中,通过常温或微热即可蒸发,避免蒸馏、萃取等提纯除杂操作,在保证效果的基础上,使制备工艺更简便。优选地,有机溶剂选自丙酮、氯仿、甲胺、二甲胺、乙醚、戊烷、二氯甲烷或二硫化碳中的一种或多种,更优选地,有机溶剂选自二氯甲烷。二氯甲烷挥发性好,且毒性低。选择二氯甲烷作为有机溶剂,能够最大程度减小毒副作用。在一些优选的实施方式中,有机溶液为每10-30mg缓释材料和0.1-2mg雷帕霉素在0.1-2ml有机溶剂中溶解得到。其中,缓释材料例如可以为,但不限于10mg、15mg、20mg、25mg或30mg,雷帕霉素例如可以为,但不限于0.1mg、0.5mg、1mg、1.5mg或2mg,有机溶剂例如可以为,但不限于0.1ml、0.5ml、1ml、1.5ml或2ml。优选地,每0.1-2ml有机溶剂与1-10ml乳化剂混合。其中,乳化剂例如可以为,但不限于1ml、2ml、3ml、4ml、5ml、6ml、7ml、8ml、9ml或10ml。优选地,缓释材料为聚乳酸-羟基乙酸,有机溶剂为二氯甲烷,乳化剂为1%(w/v)聚乙烯醇。在一些优选的实施方式中,通过搅拌或超声的方法混合均匀,优选为雷帕霉素和缓释材料的有机溶液利用磁力搅拌,与乳化剂混合利用超声。在一些优选的实施方式中,利用自然蒸发的方法去除有机溶剂。在一些优选的实施方式中,去除有机溶剂后,离心并收集雷帕霉素及缓释材料的共聚物,该共聚物可以为微球,也可以为纳米颗粒。本发明还提供了一种雷帕霉素缓释注射剂,包括上述的雷帕霉素缓释剂型或应用上述的制备方法制备得到的雷帕霉素缓释剂型和溶剂。其中,注射剂可包括载体,其是溶剂或分散介质。合适的载体包括水、生理盐水、抑菌水、磷酸盐缓冲盐水、乙醇、多元醇及其混合物,以及高分子胶束。这些组合物必须是无菌的并且是可注射的液体。优选地,所述雷帕霉素缓释注射剂中,雷帕霉素含量为400-500μg/ml,例如可以为,但不限于400μg/ml、420μg/ml、450μg/ml、480μg/ml或500μg/ml。本发明提供的雷帕霉素缓释注射剂,其能够不借助于有机溶剂直接注射,减少由于有机溶剂带来的不良反应和安全事故,并且在体内保留时间长,无需多次重复注射,减少多次给药的成本,降低了患者的疼痛感和刺激性。本发明还提供了上述的雷帕霉素缓释剂型或应用上述的制备方法制备得到的雷帕霉素缓释剂型或上述的雷帕霉素缓释注射剂在抑制mtorc1中的应用。mtor(mammaliantargetofrapamycin)是一种丝氨酸/苏氨酸激酶。营养、生长因子、应激等信号可激活mtorc1(mtorcomplex1),调节蛋白质翻译、核糖体生物合成、细胞生长增殖、代谢与衰老等多种生物学功能。mtorc1是确定的oa治疗靶点,mtorc1活化在骨关节炎的各种病理变化,包括关节软骨衰老退变与破坏、软骨下骨增生与骨赘形成、血管形成、滑膜炎症等过程中起重要作用,抑制mtorc1活化或敲除mtorc1可有效缓解上述症状与延缓骨关节炎进展。本发明提供的雷帕霉素缓释剂型或雷帕霉素缓释注射剂,作用靶点清楚,通过抑制mtorc1,能够有效的治疗和缓解骨关节炎。另外,本发明还提供了上述的雷帕霉素缓释剂型或应用上述的制备方法制备得到的雷帕霉素缓释剂型或上述的雷帕霉素缓释注射剂在制备治疗骨关节炎的药物中的应用。此外,根据本发明的方法递送的组合物可包括额外的或第二药剂,例如有机二磷酸盐、化疗药剂、放射性药剂、tnf-拮抗剂、非类固醇抗炎药剂、类固醇、抗氧化剂、血管生成抑制剂、基质金属蛋白酶抑制剂、维生素、选择性雌激素受体调节剂、雌激素-孕酮、雄激素、降血钙素、抗生素、组织蛋白酶k抑制剂、抑制素、整合素受体拮抗剂、造骨细胞合成代谢剂或选择性血清素再吸收抑制剂、葡糖胺、透明质酸或其混合物。需要说明的是,根据公开的方法治疗的患病的“受治者”、“患者”或“动物”可以是人类或非人类哺乳动物,因此,所述患病的“受治者”、“患者”或“动物”可以是人类和狗、猫、小鼠、大鼠、牛、绵羊、猪、山羊、或灵长类动物,并且可包括实验室动物、牲畜和家畜。为了有助于更清楚的理解本发明的内容,现结合具体的实施例详细介绍如下。如无特别说明,本发明实施例中使用的雷帕霉素,纯度99%以上,购于medchemexpress公司。plga50/50,分子量30000,纯度99%以上,购于济南岱罡公司。1,2-distearoyl-sn-glycero-3-phosphocholine(dspc),dspe-mpeg2000购于avantipolarlipids,胆固醇(chol)购于sigma公司,纯度均为99%以上。聚己内酯(pcl)分子量10000,纯度99%以上购于sigma公司。实施例1本实施例提供了一种雷帕霉素缓释剂型,包括质量比为1:20的雷帕霉素和聚乳酸-羟基乙酸共聚物(plga50/50)。其通过如下方法制备得到微球:(1)将20mgplga和1mg雷帕霉素溶解于1ml二氯甲烷(dcm)中;(2)准备6ml1%聚乙烯醇(pva)溶液,超纯水溶解;(3)将(1)倒入(2)中,磁力搅拌30min;(4)将(3)超声4min;(5)在磁力搅拌下,自然蒸发(4)中的有机溶剂;(6)将(5)在室温下离心20min,12000g;(7)收集微球,用超纯水润洗两次,冻干保存;(8)制备10mg/ml可注射plga包裹雷帕霉素剂型,其中雷帕霉素含量为450μg/ml。实施例2本实施例提供了一种雷帕霉素缓释剂型,包括质量比为1:10的雷帕霉素和聚乳酸-羟基乙酸共聚物(plga50/50)。其通过如下方法制备得到微球:(1)将10mgplga和1mg雷帕霉素溶解于1ml二氯甲烷(dcm)中;(2)准备6ml1%聚乙烯醇(pva)溶液,超纯水溶解;(3)将(1)倒入(2)中,磁力搅拌30min;(4)将(3)超声4min;(5)在磁力搅拌下,自然蒸发(4)中的有机溶剂;(6)将(5)在室温下离心20min,12000g;(7)收集微球,用超纯水润洗两次,冻干保存;(8)制备10mg/ml可注射plga包裹雷帕霉素剂型,其中雷帕霉素含量为600μg/ml。实施例3本实施例提供了一种雷帕霉素缓释剂型,包括质量比为1:50的雷帕霉素和聚乳酸-羟基乙酸共聚物(plga50/50)。其通过如下方法制备得到微球:(1)将50mgplga和1mg雷帕霉素溶解于1ml二氯甲烷(dcm)中;(2)准备6ml1%聚乙烯醇(pva)溶液,超纯水溶解;(3)将(1)倒入(2)中,磁力搅拌30min;(4)将(3)超声4min;(5)在磁力搅拌下,自然蒸发(4)中的有机溶剂;(6)将(5)在室温下离心20min,12000g;(7)收集微球,用超纯水润洗两次,冻干保存;(8)制备10mg/ml可注射plga包裹雷帕霉素剂型,其中雷帕霉素含量为180μg/ml。实施例4本实施例提供了一种雷帕霉素缓释剂型,包括质量比为1:20的雷帕霉素和聚乳酸-羟基乙酸共聚物(plga50/50)。其通过如下方法制备得到纳米粒:(1)将20mgplga和1mg雷帕霉素溶解于1ml丙酮中;(2)准备6ml1%聚乙烯醇(pva)溶液,超纯水溶解;(3)在磁力搅拌下,将(1)倒入(2)中;(4)自然蒸发(3)中的有机溶剂;(5)将(4)在室温下离心20min,12000g;(6)收集纳米粒,用超纯水润洗两次,冻干保存;(7)制备10mg/ml可注射plga包裹雷帕霉素剂型,其中雷帕霉素含量为450μg/ml。实施例5本实施例提供了一种雷帕霉素缓释剂型,包括质量比为1:10的雷帕霉素和dspc/chol/dspe-peg。其通过标准薄膜水化和重复过膜挤出方法制备得到脂质体:(1)在圆底烧瓶中,将10mgdspc/chol/dspe-peg2000(6:4:1的摩尔比)与1mg雷帕霉素溶解于5ml氯仿中;(2)50℃下,减压旋转蒸发1h除去氯仿成膜;(3)加入适量pbs,60℃水化薄膜,制备10mg/ml雷帕霉素脂质体分散液;(4)利用手持式脂质体挤出器(lf-1,avestin公司)制备粒径为100nm左右的脂质体囊泡;(5)可注射脂质体包裹雷帕霉素剂型,其中雷帕霉素含量为700μg/ml。实施例6本实施例提供了一种雷帕霉素缓释剂型,包括质量比为1:50的雷帕霉素和聚己内酯(pcl)。其通过如下方法制备得到微球:(1)将75mgpcl和1mg雷帕霉素溶解于5mldcm中;(2)准备30ml1%聚乙烯醇(pva)溶液,超纯水溶解;(3)将(1)倒入(2)中;(4)在磁力搅拌下,自然蒸发(3)中的有机溶剂;(5)将(4)在室温下离心20min,12000g;(6)收集微球,用超纯水润洗两次,冻干保存;(7)制备33.8mg/ml可注射plga包裹雷帕霉素剂型,其中雷帕霉素含量为450μg/ml。对比例1将雷帕霉素溶解在二甲基亚砜(dmso)中,制备50mg/ml储液。用pbs将储液稀释为10μm雷帕霉素注射液(dmso为0.02%)。实验例1c57小鼠dmm模型实验本实验例通过对照组1、模型组2、实施例1-5组及对比例组组进行动物实验,每组10只,具体操作如下:使用10%水合氯醛腹腔注射对8-10周龄大的c57小鼠进行麻醉处理,进行固定并消毒。实验侧使用显微刀片切开髌骨韧带内侧,钝性分离肌肉及脂肪垫等,暴露出关节腔及内侧半月板胫骨韧带。使用显微刀片或显微剪将内侧半月板韧带切断,并且切除部分内侧半月板,随后止血并用生理盐水冲洗伤口,逐层缝合组织与皮肤,构建小鼠内侧半月板失稳(dmm)模型。对照侧打开皮肤暴露内侧半月板后不做进一步处理直接缝合。术中应注意避免损伤关节软骨,术后每日检查伤口,定时给予青霉素肌注防止感染,膝关节不进行固定,保持在正常的饲养环境下,动物可自行活动,自由进食饮水。除对照组1和模型组2外,分别对实验各组小鼠注射相应的雷帕霉素制剂。其中,实施例1-6提供的雷帕霉素缓释剂型每次10μl,每4周注射一次;对比例1提供的注射剂每次10μl,每周注射两次。术后4周,对各组小鼠的oa进展进行分析,评分标准为:软骨结构状况评分/分正常软骨0软骨正常,但软骨染色减弱0.5关节表面平整,有少量纤维覆盖1关节软骨浅层纤维组织覆盖,并且可见薄层软骨剥脱2软骨层轻度磨损(<20%全层软骨)3软骨层中度磨损(20%-80%全层软骨)5软骨层重度磨损(>80%全层软骨)6对各组小鼠进行评分,结果如下表1所示:表1内侧半月板失稳模型小鼠治疗效果从上述结果可以看出,本发明实施例1-6提供的雷帕霉素缓释剂型,通过缓释材料对雷帕霉素进行缓释、控释,能够在每4周注射一次的基础上,维持有效的缓解和治疗骨关节炎的作用。不仅疗效优于对比例1提供的现有技术,且给药一次便维持较长期的治疗效果,相比于现有技术的每周给药两次,能够减少多次给药的成本,降低了患者的疼痛感和刺激性,减少了由于有机溶剂带来的不良反应和安全事故。图1a-1d及图2a和图2b显示了注射10μl本发明实施例1提供的雷帕霉素缓释剂型到小鼠膝关节,分别在术后4周、8周对oa进展进行分析。oarsi评分具有显著差异(p=0.002,p=0.007)。通过番红o-快速绿染色,染成蓝色的是细胞核,染成红色的是生长板软骨和关节软骨,染成绿色的是骨、软骨下骨以及其他组织。从图中可以看出,施用本发明实施例1提供的雷帕霉素缓释剂型的治疗组可以有效的缓解oa的进程,达到治疗oa的目的。实验例2c57小鼠aclt模型实验实验分组同实验例1,具体操作如下:使用10%水合氯醛腹腔注射对8-10周龄大的c57小鼠进行麻醉处理,消毒膝关节附近皮肤,实验侧膝关节沿髌骨外侧切开,逐层分离肌肉及皮下组织,显露前交叉韧带近胫骨点。随后将膝关节屈曲90度,将前交叉韧带钩住后在中端切开,避免伤及半月板及后交叉韧带,进行抽屉实验证实前交叉韧带断裂,随后止血并用生理盐水冲洗伤口,逐层缝合关节囊及皮肤,构建小鼠前交叉热带切断(aclt)模型。对照侧使用同样方法显露前交叉韧带但不切断,术后每日检查伤口,定时给予青霉素肌注防止感染,膝关节不进行固定,保持在正常的饲养环境下,动物可自行活动,自由进食饮水。除对照组1和模型组2外,分别对实验各组小鼠注射相应的雷帕霉素制剂。其中,实施例1-6提供的雷帕霉素缓释剂型每次10μl,每4周注射一次;对比例1提供的注射剂每次10μl,每周注射两次。术后4周,对各组小鼠的oa进展进行分析,评分标准同实验例1。对各组小鼠进行评分,结果如下表2所示:表2前交叉热带切断模型小鼠治疗效果组别4w评分/分8w评分/分12w评分/分对照组1000模型组22.83.25.1实施例11.21.92.2实施例21.12.02.2实施例31.32.12.3实施例41.32.22.4实施例51.12.12.4实施例61.32.22.5对比例11.52.43.0从上述结果可以看出,本发明实施例1-6提供的雷帕霉素缓释剂型,通过缓释材料对雷帕霉素进行缓释、控释,能够在每4周注射一次的基础上,维持有效的缓解和治疗骨关节炎的作用。不仅疗效优于对比例1提供的现有技术,且给药一次便维持较长期的治疗效果,相比于现有技术的每周给药两次,能够减少多次给药的成本,降低了患者的疼痛感和刺激性,减少了由于有机溶剂带来的不良反应和安全事故。图3a-3f及图4a-4c中显示了注射10μl本发明实施例1提供的雷帕霉素缓释剂型到小鼠膝关节,分别在术后4周、8周和12周对oa进展进行分析。oarsi评分具有显著差异(p=0.001,p=0.001和p=0.0023)。通过番红o-快速绿染色,染成蓝色的是细胞核,染成红色的是生长板软骨和关节软骨,染成绿色的是骨、软骨下骨以及其他组织。施用本发明实施例1提供的雷帕霉素缓释剂型的治疗组可以有效的缓解oa的进程,达到治疗oa的目的。最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1