一种组合物及其制备方法与在防治乳腺疾病中的应用与流程
本发明涉及中医药技术领域,尤其涉及一种组合物及其制备方法与在防治乳腺疾病中的应用。
背景技术:
乳腺增生是女性最常见的乳房疾病,在青春期或青年女性中,经前有乳房胀痛、有时疼痛会波及肩背部,经后乳房疼痛逐渐自行缓解,仅能触到乳腺有些增厚,无明显结节,这些属于生理性的增生。而乳腺增生症是乳腺间质的良性增生,是正常乳腺小叶生理性增生与复旧不全,乳腺正常结构出现紊乱,属于病理性增生,它是既非炎症又非肿瘤的一类病。病理性的乳腺增生,以小叶腺泡、末梢导管和结缔组织均发生不同程度的增生为特征(分小叶增生型,纤维腺病型,纤维化型)以及小叶末梢导管和腺泡高度扩张成囊为特征(乳房囊性增生病)。极少部分的乳腺小叶增生会伴随导管上皮增生,且呈现重度异形,成为癌前期病变,需积极治疗定期检查,防患于未然。
西医认为,乳腺在内分泌激素,特别是雌/孕激素的作用下,随着月经周期的变化,会有增生和复旧的改变。由于焦虑、压力、不运动等无可避免的外界因素引起内分泌激素代谢失衡,雌激素水平增高,可以出现乳腺组织增生过度和复旧不全,经过一段时间以后,增生的乳腺组织不能完全消退,就形成乳腺增生症。
中医认为,乳房的结构为中空管腔,亦不与水谷直接接触,但又以通疏泄为要,乃奇恒之腑,通过经络与肝、胃、脾相连接。乳络是宗经之所,为多条经脉交汇之所,其中,肝经,上贯膈,布胸肋,绕乳头;胃经,贯乳中;脾经,经乳外侧;这些正经与各自的别络、浮络等在乳房迂曲环绕,同行气血、濡养乳房。乳腺增生病属于中医“乳癖”范围,《疡科心德集》中是这样描述的:“有乳中结核,形如丸卵,不疼痛,不发寒热,皮色不变,其核随喜怒而消长,此名乳癖……”。《外科正宗》曰:“忧虑伤肝,思虑伤脾,积想在心,所愿不得志者,致经脉痞涩,积聚成核,初如豆大,渐如棋子”。
目前,针对乳腺增生的治疗方案包括:心理治疗、中医中药治疗、西药治疗、手术治疗。其中药物治疗方案居多,但是西药治疗多以激素类药物为主,长期口服会引起多种不良反应和副作用,对身体造成伤害。而中药药品主要有乳块消、乳癖消、天冬素片、平消片、散结灵。但目前的中药药品治疗效果有限,且味数多、动物性药材多,如某些组合物含蜈蚣、僵蚕等动物性药材,不宜长期服用。因此,开发安全、无副作用、便于长期服用,并标本兼顾、有效缓解乳房症状的内服保健品具有现实意义。
技术实现要素:
有鉴于此,本发明要解决的技术问题在于提供一种组合物及其制备方法与在防治乳腺疾病中的应用。提供的组合物能够多靶点的有效治疗乳腺增生。
本发明提供的组合物由如下质量份的组分组成:
本发明一些实施例中,所述组合物由如下质量份的组分组成:
一些具体实施例中,所述组合物由如下质量份的组分组成:
一些具体实施例中,所述组合物由如下质量份的组分组成:
一些具体实施例中,所述组合物由如下质量份的组分组成:
一些具体实施例中,所述组合物由如下质量份的组分组成:
一些具体实施例中,所述组合物由如下质量份的组分组成:
中医认为乳腺增生症始于肝郁,而后血淤痰凝成块,治宜疏肝理气解郁。本配方化裁自1000年文化传承双古方,人参养荣汤和柴胡疏肝散,精选疏肝解郁之品,醋炙醋香附、白芍,令乳络通达,理气散结;独有的复合多糖专利技术,巧用熟地黄、枸杞、黄精、党参多糖的精妙搭配,令肝肾脾同补,在乳络通达的同时,让乳络气血充盈满溢,荣养乳房,缓解乳房胀痛,消减乳房肿块;配合抗氧化活性因子-葡萄籽提取物,保护乳房悬韧带,全面维护和保养乳房健康。各组分相互配合,相互促进,起到良好的增效协同作用。
本发明还提供了一种提取物,其由本发明所述的组合物制得。
本发明所述提取物的制备方法,包括
醋香附、白芍经水提、浓缩喷粉,制得组分a;
熟地黄、黄精、枸杞子、党参,经水提、醇沉,取沉淀物,干燥制得组分b;
葡萄籽经醇提、柱层析、浓缩、干燥,制得葡萄籽提取物;
将组分a、组分b和葡萄籽提取物混合,制得所述提取物。
本发明所述水提中,水的质量为药材总质量的5~20倍,提取温度为80~100℃,时间为0.5~4h,提取次数为2次。
具体实施例中,水的质量为药材总质量的8倍,提取温度为100℃,时间为1h,提取次数为2次。
本发明中,所述浓缩采用真空浓缩,也可以是常温加热浓缩、冷冻浓缩、结晶浓缩等方式。
本发明所述醇沉采用体积分数为80%~95%的乙醇水溶液,最终至乙醇体积分数为75%以上。
具体实施例中,所述醇沉采用体积分数为95%的乙醇水溶液,最终至乙醇体积分数为75%。
葡萄籽的提取中,醇提采用体积分数为65%~85%的乙醇水溶液;乙醇水溶液的质量为葡萄籽质量的5~20倍。时间为0.5~4h,提取三次。
具体的,葡萄籽提取物的制备方法为:将葡萄籽洗净,加65%~85%乙醇,提取时乙醇的用量优选为葡萄籽总重量的5~20倍,提取优选三次,每次提取时间0.5~4h,过滤,将提取液浓缩,柱层析分离出有效成分(原花青素),经乙醇梯度洗脱,收集洗脱液,经浓缩、喷干、粉碎,制得葡萄籽提取物。
经鉴定,白芍、醋香附的水提物主要成分为芍药苷和醋香附酮、醋香附烯、醋香附子醇、异醋香附醇等醋香附挥发油。熟地黄、黄精、枸杞子、党参经水提醇沉,所得提取物的主要成分为多糖,可提升机体免疫力,预防乳房问题的发生。本发明所述葡萄籽提取物的主要成分为原花青素,其可自行制备,也可于市场购得,制备方法采用醇提法。
本发明所述组合物、提取物或所述制备方法制得的提取物在制备调节内分泌水平的产品中的应用。
本发明中,所述内分泌激素为雌二醇、孕酮、促黄体生成素、卵泡刺激素和/或催乳素。
本发明所述调节内分泌是指对内分泌激素的双向调节,在内分泌激素在非正常的升高或降低的情况下,既可使过量的内分泌激素向正常转化,也可使过低的内分泌激素向正常状态转化,最终使内分泌激素水平达到平衡状态。
雌二醇(e2)、孕酮(p)、催乳素(prl)、促黄体生成激素(lh)、卵泡刺激素(fsh)与乳腺的发育和健康状态密切相关。本发明研究表明,相对于健康状态的大鼠,乳腺增生大鼠的e2、p、prl、lh、fsh水平皆显著增高,乳房组织表现为乳头竖起,较坚实,充血,增高(2~3mm)。而给予本发明提供的组合物后,e2、p、prl、lh、fsh水平皆降低,趋近于正常值,乳头充血明显减少。
具体的,本发明所述组合物、提取物或所述制备方法制得的提取物在制备抑制乳腺增生患者e2、p、prl、lh、fsh水平的产品中的应用。
本发明所述组合物、提取物或所述制备方法制得的提取物在制备调节雌激素受体和/或孕激素受体表达水平的产品中的应用。
本发明所述组合物、提取物或所述制备方法制得的提取物在制备改善乳腺增生的产品中的应用。
本发明中,所述改善乳腺增生包括:改善乳腺弥漫性增生、改善乳房疼痛和/或改善乳房触痛。
本发明对乳腺增生模型大鼠第二对乳头直径、乳头高度进行测量,结果表明与模型对照组相比,给予本发明组合物的大鼠第二对乳头直径、乳头高度均明显缩小(p<0.01)。经过组织切片检测,模型组大鼠乳腺小叶数量明显增多,腺泡数明显增多,有的腺泡腔扩大,内有分泌物;有的乳腺导管上皮细胞明显增生,局部呈乳头状或复层增生,管腔扩张,内有脱落上皮细胞及分泌物,伴间质纤维组织增生。而给予本发明组合物的大鼠乳腺小叶数量明显减少,腺泡数明显减少,乳腺导管上皮细胞增生明显减少。另外,临床调查结果显示:以轻度乳腺疼痛和中度乳腺疼痛者为合格样本,剔除已形成病变样本。服用本发明提供的组合物三个月后,受试者的乳房疼痛程度、乳房触痛程度、肿块大小、肿块质地和肿块分布范围均比基线时期有明显改善(p<0.05),尤其是乳房疼痛程度(51.6%)、乳房触痛程度(51.6%)改善最明显。相对于各对照组,本发明提供组合物的效果最优,该效果存在统计学差异,说明本发明提供的组合物中各组分设置合理,能够起到良好的增效协同作用。
本发明所述组合物、提取物或所述制备方法制得的提取物在制备抗氧化的产品中的应用。
本发明中,所述抗氧化包括:降低血清lpo和/或mda水平、提高总抗氧化能力、提高gsh-px酶活力、提高sod酶活力。
本发明以d-半乳糖造大鼠的氧化损伤模型,与正常对照组相比,模型对照组大鼠t-aoc明显减小(p<0.01),gsh-px活力明显降低(p<0.01)。与模型对照组相比,给予本发明组合物的大鼠t-aoc显著提高(p<0.05),gsh-px活力明显上升(p<0.01)。与正常对照组相比,模型对照组大鼠sod活性明显降低(p<0.05),lpo、mda含量显著升高(p<0.01)。与模型对照组相比,给予本发明组合物的大鼠sod活性明显升高(p<0.01),lpo、mda含量显著降低((p<0.01)。相对于各对照组,本发明提供组合物的效果最优,该效果存在统计学差异,说明本发明提供的组合物中各组分设置合理,能够起到良好的增效协同作用。
本发明还提供了一种改善乳腺增生和/或抗氧化的产品,其包括:本发明所述组合物、提取物或所述制备方法制得的提取物。
本发明所述的改善乳腺增生和/或抗氧化的产品为药物、保健品或食品。
具体的,本发明提供了治疗乳腺增生的药物。还提供了抗氧化的保健品或食品。
本发明提供的产品还包括辅料。
所述辅料为药学上可接受的辅料、食品中可接受的配料和/或保健品中可接受的辅料。
本发明所述产品的剂型为注射剂或口服制剂。
所述口服制剂为散剂、片剂、颗粒剂、胶囊剂、溶液剂、乳剂、混悬剂、丸剂或糖浆剂。
本发明还提供了一种改善乳腺增生的方法,其为给予本发明提供的产品。
所述给予的方式为口服,给予的剂量为2.1g/d。
本发明提供了由熟地黄,枸杞子,黄精,党参,白芍,醋香附,葡萄籽组成的组合物,该组合物能够具有种改善乳腺增生和/或抗氧化的作用,相对于各对照组,本发明提供组合物的效果最优,该效果存在统计学差异,说明本发明提供的组合物中各组分设置合理,能够起到良好的增效协同作用。服用本发明提供的组合物后受试者的乳房疼痛程度、乳房触痛程度、肿块大小、肿块质地和肿块分布范围均比基线时期有明显改善。且该制剂安全无副作用。
附图说明
图1服用组合物对乳房疼痛总体评价(t2b);“*”代表该组别基线值,与一月、二月、三月相比,差异具有显著性(p<0.05),改善明显(top2)=改善很明显(5-6分)+改善明显(3-4分);
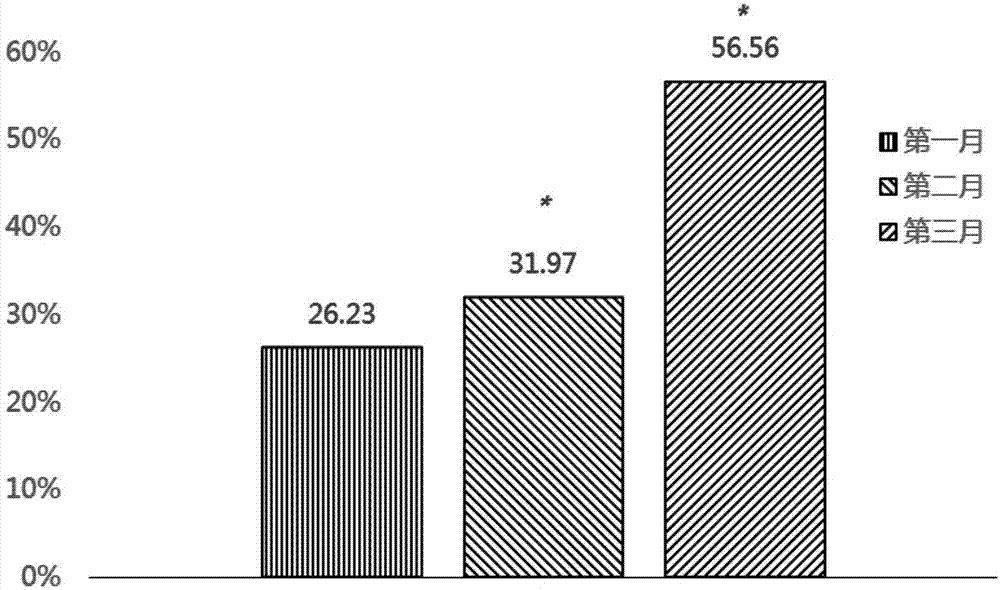
图2服用组合物对乳房疼痛改善总体评价(n=122,%),改善很明显=5-6分;改善明显=3-4分;有点明显=1-2分;无改善=0;
图3服用组合物期间乳房疼痛天数均值(n=122,mean),“*”代表该组别基线值,与一月、二月、三月相比,差异具有显著性(p<0.05);
图4服用组合物前后乳房疼痛天数改善情况(图中数值为与0周的差值);
图5服用组合物前后症状体征评估均值,“*”代表该组别与初始值相比,差异具有显著性(p<0.05);
图6症状体征改善情况(n=122,%);
图7症状体征改善人数占比(n=122,%);
图8示各组乳腺组织光镜观察,100×;其中,图8-a示正常对照组乳腺组织光镜观察,100×;图8-b示模型对照组乳腺组织光镜观察,100×;图8-c示组合物1组乳腺组织光镜观察,100×;图8-d示组合物2组乳腺组织光镜观察,100×;图8-e示组合物3组乳腺组织光镜观察,100×;图8-f示组合物4组乳腺组织光镜观察,100×;图8-g示组合物5组乳腺组织光镜观察,100×;图8-h示对照品1组乳腺组织光镜观察,100×;图8-i示对照品2组乳腺组织光镜观察,100×;图8-j示乳癖消组乳腺组织光镜观察,100×。
具体实施方式
本发明提供了一种组合物及其制备方法与在防治乳腺疾病中的应用,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
本发明采用的试材皆为普通市售品,皆可于市场购得。
下面结合实施例,进一步阐述本发明:
实施例
各组组合物配方如表1:
表1组合物配方(质量份)
制备工艺:
将醋香附、白芍混合,加入总投料量的8倍饮用水,加热100℃提取2.0h;第二次提取加入总投料量的7倍饮用水,加热100℃提取1.0h,过滤,将两次提取液合并浓缩,温度为65~85℃,真空度为-0.04~-0.07mpa,浓缩至固形物含量为20±5%时趁热出料,备用;将熟地黄、黄精、枸杞子、党参混合,加入总投料量的10倍饮用水,加热100℃提取2h,第二次提取加入总投料量的8倍饮用水,加热100℃提取1.0h,过滤,将两次提取液合并浓缩,温度为65~85℃,真空度为-0.04~-0.07mpa,浓缩至固形物含量为20±5%时趁热出料,加入85%以上的乙醇,需先加浓缩液再边搅拌边缓慢加入乙醇,调至乙醇浓度为75%,静置过夜(12h以上)。
功效学研究
1、对乳腺增生的抑制作用
1.1实验单位:
广东省中医院工程技术研究院
1.2实验目的:
观察评价中草药组方对大鼠乳腺增生抑制作用。
1.3实验材料:
1.3.1药材
本中草药组方由无限极(中国)有限公司提供。空白对照品:蒸馏水。阳性对照品:乳癖消片,辽宁好护士药业(集团)有限责任公司。苯甲酸雌二醇注射液,
1.3.2试剂
苯甲酸雌二醇注射液,上海通用药业股份有限公司,批号1207241。
黄体酮注射液,上海通用药业股份有限公司,批号13003146。
大鼠雌二醇酶联免疫检测试剂盒(elisakitforrate2),上海西唐生物科技有限公司,batchno:1307251。
大鼠催乳素酶联免疫检测试剂盒(elisakitforratprl),上海西唐生物科技有限公司,batchno:1308083。
大鼠孕酮酶联免疫检测试剂盒(elisakitforratp),上海西唐生物科技有限公司,batchno:1307251。
大鼠卵泡刺激素酶联免疫检测试剂盒(elisakitforratfsh),上海西唐生物科技有限公司,batchno:1306251。
大鼠促黄体生成激素酶联免疫检测试剂盒(elisakitforratlh),上海西唐生物科技有限公司,batchno:1306252。
0.9%氯化钠注射液,四川科伦药业股份有限公司,批号m12071027。
1.3.3剂量设置:
空白对照组、中草药组方1组(752.32mg·kg-1)、中草药组方2组(752.32mg·kg-1)、中草药组方3组(752.32mg·kg-1)、中草药组方4组(752.32mg·kg-1)、中草药组方5组(752.32mg·kg-1)、对照组1(752.32mg·kg-1)、对照组2(752.32mg·kg-1)。
1.4实验方法与检测指标:
造模方法:除正常对照组外其余各组大鼠肌肉注射苯甲酸雌二醇0.5mg·kg-1,1次/d,连续25d。随后改用肌肉注射黄体酮4mg·kg-1,1次/d,连续5d,正常对照组不注射激素仅给予大鼠肌肉注射生理盐水0.2ml/只,连续30d。各给药组按剂量灌胃给药,正常对照组、模型对照组灌胃给予等体积蒸馏水,每组大鼠10只,每天1次,连续30d。末次给药后1h,用游标卡尺测量第2对乳头的直径及高度,并观察其外观。动物眼眶静脉丛取血,分离血清,测定动物血清中雌二醇e2、孕酮p、催乳素prl、促黄体生成激素、卵泡刺激素fsh含量。以8%硫化钠局部脱毛处理,动物处死后完整剥离并取下大鼠胸部第2对乳房。10%甲醛溶液固定,石蜡包埋切片,第2对乳腺组织苏木素-伊红(he)染色光镜观察(图8)。
1.5联合用药的q值计算(金正均法):
根据文献的方法用改进的公式计算联合用药的q值:q=ea+b/(ea+eb-ea×eb)。ea+b表示合用的数据,ea表示单用a的数据,eb表示单用b的数据,用抑制率或提高率数据进行计算。q值小于0.85表明两药合用后产生拮抗作用;q值大于0.85,小于1.15表明两药合用后产生效应相加作用;q值大于1.15表明两药合用后产生协同促进效应作用。
1.6实验结果:
1.6.1对乳腺增生大鼠第2对乳头直径及高度的影响
末次给药后1h,用游标卡尺测量第2对乳头的直径及高度,并观察其外观。
表2对乳腺增生大鼠第2对乳头直径及高度的影响(
注:与正常对照组比较*p<0.05,**p<0.01;
与模型对照组比较#p<0.05,##p<0.01。
与组合物1组比较△p<0.05,△△p<0.01。
与组合物2组比较☆p<0.05,☆☆p<0.01。
与组合物3组比较◇p<0.05,◇◇p<0.01。
与组合物4组比较
与组合物5组比较
结果:人类乳腺增生的程度参差不齐,常为局限性包块;而大鼠的乳腺增生多为弥漫性,表现为乳房整体增大、乳头增高、乳头直径增大。本实验结果中,与正常对照组相比,模型对照组大鼠第二对乳头直径、乳头高度均显著增大(p<0.01)。与模型对照组相比,组方1、2、3、4、5组和乳癖消片组大鼠第二对乳头直径、乳头高度均明显缩小(p<0.01)。组方2、3、4、5组第二对乳头直径、乳头高度均较组方1组大(p<0.01或p<0.05)。对照品1组第二对乳头直径、乳头高度均较组方1、2、3、4、5组大(p<0.01)。对照品2组第二对乳头直径、乳头高度均较组方1、2、3、4、5组大(p<0.01)。对照品3组第二对乳头直径、乳头高度均较组方1、2、3、4、5组大(p<0.01或p<0.05)。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1*e对照品3)=0.160/(0.052+0.055-0.052*0.055)=1.536,1.536>1.15,表明对照品1与对照品3合用具有协同降低乳头直径的作用。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1*e对照品3)=0.201/(0.050+0.015-0.050*0.015)=3.152,3.152>1.15,表明对照品1与对照品3合用具有协同降低乳头高度的作用。
1.6.2对乳腺增生大鼠血清雌二醇e2、孕酮p含量的影响
动物眼眶静脉丛取血,分离血清,测定动物血清中雌二醇e2、孕酮p。
表3对乳腺增生大鼠血清雌二醇e2、孕酮p含量的影响(
注:与正常对照组比较*p<0.05,**p<0.01;
与模型对照组比较#p<0.05,##p<0.01。
与组合物1组比较△p<0.05,△△p<0.01。
与组合物2组比较☆p<0.05,☆☆p<0.01。
与组合物3组比较◇p<0.05,◇◇p<0.01。
与组合物4组比较
与组合物5组比较
结果:与正常对照组相比,模型对照组大鼠雌二醇e2、孕酮p含量均显著升高(p<0.01)。与模型对照组相比,组合物1、2、3、4、5组和乳癖消片组大鼠雌二醇e2、孕酮p含量明显降低(p<0.01)。组合物2、4、5组e2含量较组合物1组高(p<0.01或p<0.05)。对照品1、2和3组雌二醇e2含量和孕酮p含量较组合物1、2、3、4、5组高(p<0.01或p<0.05)。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1×e对照品3)=0.357/(0.087+0.043-0.087×0.043)=2.846,2.846>1.15,表明对照品1与对照品3合用具有协同降低e2的作用。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1×e对照品3)=0.271/(0.107+0.088-0.107×0.088)=1.454,1.454>1.15,表明对照品1与对照品3合用具有协同降低p的作用。
1.6.3对乳腺增生大鼠血清催乳素prl、促黄体生成素lh、卵泡刺激素fsh含量的影响
实验结束时动物眼眶静脉丛取血,分离血清,测定动物血清中催乳素prl、促黄体生成激素lh、卵泡刺激素fsh含量。
表4对乳腺增生大鼠血清prl、lh、fsh含量的影响(
注:与正常对照组比较*p<0.05,**p<0.01;
与模型对照组比较#p<0.05,##p<0.01。
与组合物1组比较△p<0.05,△△p<0.01。
与组合物2组比较☆p<0.05,☆☆p<0.01。
与组合物3组比较◇p<0.05,◇◇p<0.01。
与组合物4组比较
与组合物5组比较
结果:与正常对照组相比,模型对照组大鼠催乳素prl、促黄体生成激素lh、促卵巢激素fsh均显著升高(p<0.01)。与模型对照组相比,组合物1、2、3、4、5组和乳癖消片组大鼠催乳素prl、促黄体生成激素lh、卵泡刺激素fsh含量明显降低(p<0.01)。组合物2组prl含量较组合物1组高(p<0.05)。组合物2、4、5组lh含量较组合物1组升高(p<0.01或p<0.05)。对照品1、2和3组催乳素prl、促黄体生成激素lh、促卵巢激素fsh含量较组合物1、2、3、4、5组高(p<0.01或p<0.05)。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1×e对照品3)=0.518/(0.068+0.028-0.068×0.028)=5.460,5.460>1.15,表明对照品1与对照品3合用具有协同降低prl的作用。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1×e对照品3)=0.312/(0.037+0.052-0.037×0.052)=3.595,3.595>1.15,表明对照品1与对照品3合用具有协同降低lh的作用。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1×e对照品3)=0.293/(0.066+0.076-0.066×0.076)=2.139,2.139>1.15,表明对照品1与对照品3合用具有协同降低fsh的作用。
1.6.4对乳腺增生大鼠第2对乳头病理形态观察
实验结束后,取下大鼠胸部第2对乳房。10%甲醛溶液固定,石蜡包埋切片,第2对乳腺组织苏木素-伊红(he)染色光镜观察。结果如附图8。
结果:大体观察时,正常对照组的乳头形态与试验开始时一样,隔毛看不见乳头位置,将毛分开后,仅见乳头呈小米样,紧贴在皮肤上,苍白、柔软、个别稍隆起(1mm左右)。乳腺增生病大鼠模型组形态学改变特征为乳头竖起,较坚实,充血,增高(2~3mm)。中草药组方各剂量组大鼠乳头形态表现为乳头竖起、充血明显减少。镜下观察时,正常对照组乳腺小叶及腺泡均未见明显增生,腺泡数4~5个,腺泡腔不扩大。模型对照组乳腺小叶数量明显增多,腺泡数明显增多,有的腺泡腔扩大,内有分泌物;有的乳腺导管上皮细胞明显增生,局部呈乳头状或复层增生,管腔扩张,内有脱落上皮细胞及分泌物,伴间质纤维组织增生。中草药组方各剂量组大鼠乳腺小叶数量明显减少,腺泡数明显减少,乳腺导管上皮细胞增生明显减少。照品1、2、3组乳腺小叶数量明显增多,腺泡数明显增多,乳腺导管上皮细胞增生明显增多。
1.7实验结论
本发明组方各剂量组和乳癖消片对大鼠乳腺增生均有明显的抑制作用,整体效果联方高剂量组最好。
2抗氧化作用研究
2.1实验目的
观察评价中草药组方的抗氧化作用
2.2实验材料:
2.2.1药材
本中草药组方由无限极(中国)有限公司提供。空白对照品:蒸馏水。阳性对照品:平消胶囊,国药准字z61021330,西安正大制药有限公司。
2.2.2试剂
d-(+)-galactose,国药集团化学试剂有限公司,批号20130917。
总抗氧化能力(t-aoc)试剂盒,南京建成生物工程研究所,批号20131211。
谷胱甘肽-过氧化物酶(gsh-px)测试盒,南京建成生物工程研究所,批号20140220。
超氧化物歧化酶(sod)wst-1法测定试剂盒,南京建成生物工程研究所,批号20140416。
脂质过氧化物(lpo)测试盒,南京建成生物工程研究所,批号20140228。
丙二醛(mda)测试盒,南京建成生物工程研究所,批号20140225。
2.2.3剂量设置:
空白对照组、中草药组方1组(752.32mg·kg-1)、中草药组方2组(752.32mg·kg-1)、中草药组方3组(752.32mg·kg-1)、中草药组方4组(752.32mg·kg-1)、中草药组方5组(752.32mg·kg-1)、对照组1(752.32mg·kg-1)、对照组2(752.32mg·kg-1)。
2.3实验方法与检测指标:
取spf级sd雌性大鼠80只,随机留取10只大鼠作为正常对照组外,其余70只大鼠作为造模组。造模组大鼠用d-半乳糖125mg/kgbw腹腔注射造模,注射量为0.2ml/100g,每日1次,连续造模6周,正常对照组大鼠10只同法腹腔注射等体积生理盐水。造模6周后取血测mda,按mda水平分组,分别为模型对照组、中草药组方组、对照品组、平消胶囊组,每组10只。
各给药组灌胃给予不同浓度受试样品,正常对照组、模型对照组同法灌胃给予同体积蒸馏水,每天1次,连续30天。在给受试样品的同时,模型对照组和各给药组继续腹腔注射给予相同剂量d-半乳糖。实验结束后处死动物,取血测定血清总抗氧化能力(t-aoc)、谷胱甘肽-过氧化物酶(gsh-px)、脂质过氧化物(lpo)、丙二醛(mda)含量、超氧化物歧化酶(sod)。
2.4联合用药的q值计算(金正均法):
根据文献的方法用改进的公式计算联合用药的q值:q=ea+b/(ea+eb-ea×eb)。ea+b表示合用的数据,ea表示单用a的数据,eb表示单用b的数据,用抑制率或提高率数据进行计算。q值小于0.85表明两药合用后产生拮抗作用;q值大于0.85,小于1.15表明两药合用后产生效应相加作用;q值大于1.15表明两药合用后产生协同促进效应作用。
2.5实验结果:
2.5.1对d—半乳糖致衰老大鼠t-aoc、gsh-px的影响
实验结束后处死动物,取血测定血清总抗氧化能力(t-aoc)、谷胱甘肽-过氧化物酶(gsh-px)。
表5对d-半乳糖致衰老大鼠t-aoc、gsh-px的影响(
注:与正常对照组比较*p<0.05,**p<0.01;
与模型对照组比较#p<0.05,##p<0.01。
与组合物1组比较△p<0.05,△△p<0.01。
与组合物2组比较☆p<0.05,☆☆p<0.01。
与组合物3组比较◇p<0.05,◇◇p<0.01。
与组合物4组比较
与组合物5组比较
结果:与正常对照组相比,模型对照组大鼠t-aoc明显减小(p<0.01),gsh-px活力明显降低(p<0.05)。与模型对照组相比,组合物1、2、3、4、5组t-aoc明显升高,gsh-px活力明显升高,呈显著性差异(p<0.01或p<0.05)。对照品1、2和3组中t-aoc含量对比组合物1、2、3、4、5组显著降低,gsh-px活力对比组合物1、2、3、4、5组显著降低(p<0.01或p<0.05)。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1×e对照品3)=1.613/(0.333+0.354-0.333×0.354)=2.006,2.006>1.15,表明对照品1与对照品3合用具有协同升高t-aoc的作用。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1×e对照品3)=0.467/(0.264+0.196-0.264×0.196)=0.912,0.85<0.912<1.15,表明对照品1与对照品3合用产生效应相加作用,共同升高gsh水平。
2.5.2对d-半乳糖致衰老大鼠sod、lpo、mda含量的影响
实验结束时,取血测定血清脂质过氧化物(lpo)、丙二醛(mda)含量、超氧化物歧化酶(sod)。
表6对d-半乳糖致衰老大鼠sod、lpo、mda的影响(
注:与正常对照组比较*p<0.05,**p<0.01;
与模型对照组比较#p<0.05,##p<0.01。
与组合物1组比较△p<0.05,△△p<0.01。
与组合物2组比较☆p<0.05,☆☆p<0.01。
与组合物3组比较◇p<0.05,◇◇p<0.01。
与组合物4组比较
与组合物5组比较
结果:与正常对照组相比,模型对照组大鼠sod活性明显降低(p<0.05),lpo、mda含量显著升高(p<0.01)。与模型对照组相比,组合物1、2、3、4、5组大鼠sod活性明显升高(p<0.01),lpo、mda含量显著降低(p<0.01)。组合物4、5组大鼠lpo、mda含量较组合物1组降低(p<0.01或p<0.05)。对照品1、2和3组中sod活性对比组合物1、2、3、4、5组显著降低(p<0.01或p<0.05),lpo、mda含量对比组合物1、2、3、4、5组显著升高(p<0.01)。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1×e对照品3)=0.470/(0.205+0.197-0.205×0.197)=1.061,0.85<1.06<1.15,表明对照品1与对照品3合用产生效应相加作用,共同升高sod水平。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1×e对照品3)=0.463/(0.094+0.130-0.094×0.130)=2.179,2.179>1.15,表明对照品1与对照品3合用具有协同降低lpo的作用。e组合物1q值=e组合物1/(e对照品1+e对照品3-e对照品1×e对照品3)=0.566/(0.220+0.233-0.220×0.233)=1.408,1.408>1.15,表明对照品1与对照品3合用具有协同降低mda的作用。
3临床应用统计
以组合物1样品作为受试样品。
3.1甄选条件:轻度乳腺疼痛和中度乳腺疼痛者为合格样本,剔除已形成病变样本。实际纳入样本122人。
3.2参照全国中医学会中医外科分会乳腺病专业委员会2002年第8次会议通过的标准制定。症状体征评估利用大夫手诊,按照乳房疼痛程度、乳房触痛程度、肿块大小、肿块质地、肿块分布范围进行评估。
3.3参照视觉模拟评分法(visualanaloguescale,vas)用于疼痛的评估。该法在临床使用较为广泛,临床治疗前后使用同样的方法即可较为客观的做出评分,并对疼痛治疗的效果进行较为客观的评价。vas按照国际上认可自我疼痛评估对照0-10分从无痛至重度疼痛的“标尺“上分级程度的数字给出自己的乳房疼痛分值,结果如图1~2。
3.4根据受试者自我感知的疼痛分值看,服用产品三个月后,56.56%的受试者疼痛改善明显,38.52%的受试者感知有点改善,仅有4.92%的受试者疼痛分值无改善,充分说明该中草药组合物对乳房疼痛的改善效果显著。
3.5根据图3~4所示,服用产品一个月后,与基线时期相比服用该中草药组合物受试者自觉乳房疼痛天数均有明显减少(p<0.05)。随着服用时间的增长,受试者的乳房疼痛天数越短。服用该中草药组合物三个月后,受试者乳房疼痛时长缩短了1.65天。
3.6参照全国中医学会中医外科分会乳腺病专业委员会2002年第8次会议通过的标准制定。计算治疗前后各分改善率:改善率=(治疗前总积分-治疗后总积分)/治疗前总积分×100%,痊愈:改善率>90%,显效:改善率70%-89%,有效:改善率30%-69%;无效:改善率<30%
总有效=痊愈+显效+有效
结果如图5~6所示,受试者服用该中草药组合物的改善情况,从专家手诊症状体征情况看,服用该组合物三个月后,受试者乳房症状体征均值由(6.69分)降至(3.12分),从改善的总有效率来看,三个月后总有效率达到64.75%,有统计学差异(p<0.05)。
备注:“*”代表该组别与初始值相比,差异具有显著性(p<0.05)。
3.7如图7所示,服用产品一个月后,受试者乳房触痛程度改善较明显(40.2%)、其它指标也有一定改善。随着服用时间的增长,受试者的各项症状体征均逐渐改善。服用该中药组合物三个月后,受试者的乳房疼痛程度、乳房触痛程度、肿块大小、肿块质地和肿块分布范围均比基线时期有明显改善(p<0.05),尤其是乳房疼痛程度(51.6%)、乳房触痛程度(51.6%)改善最明显。
以上仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!