具有抗皮肤衰老功能的二醇型人参皂苷纳米乳及其制备方法与流程
本发明涉及一种纳米乳剂及其制备方法和用途,具体涉及具有抗皮肤衰老功能的二醇型人参皂苷纳米乳及其制备方法。
背景技术:
人参是五加科多年生草本植物(panaxginseng,c.a.mey.),含有氨基酸、维生素、多糖、人参挥发油、无机元素、生物碱、肽类物质、脂肪类、皂苷、有机酸、黄酮类、甾醇、木质素、酶类等多种化学成份,其中人参皂苷是人参主要的活性成分。按照人参皂苷元的差别,将人参皂苷分成齐墩果酸类皂苷、原人参三醇类皂苷和原人参二醇类皂苷。二醇型人参皂苷在抗癌、抗衰老、补元气、增强机体抵抗力、改善记忆力等方面具有非常显著的疗效。近年来,由于二醇型人参皂苷在抗衰老方面的功效显著,将其应用于药品和化妆品领域以达到抗皮肤衰老的研究成为一项热门研究。但二醇型人参皂苷极性大,脂溶性差,不易透过皮肤,所以给皮肤用药带来一个很大难题。
技术实现要素:
鉴于上述所述的人参二醇型人参皂苷提取物作为产品的不足,本发明的目的在于提供一种以二醇型人参皂苷为原料的、具有抗皮肤衰老功能的二醇型人参皂苷纳米乳及其制备方法。
一种二醇型人参皂苷纳米乳,由如下组分组成:由二醇型人参皂苷提取物和水组成的水相、油相和混合乳化剂;其中,所述水相和油相的质量比为5~8:45,所述油相和混合乳化剂的质量比为7.5~8:2~2.5,所述二醇型人参皂苷提取物在水相中的质量浓度为15~25%,所述二醇型人参皂苷提取物含有的二醇型人参皂苷rb1、rb2、rc和rd的含量之和不低于38%。
在上述技术方案中,所述油相为棕榈酸异丙酯或肉豆蔻酸异丙酯,所述的混合乳化剂由司盘80和1,2-丙二醇按质量比3:1~3配置得到。
在上述技术方案中,所述二醇型人参皂苷提取物的制备方法包括如下步骤:
(1)将人参粗粉与ph为11~13的ca(oh)2水溶液按料液比g:ml=1:10~15的比例混合,在提取温度为20℃~35℃,超声功率120w~160w的条件下进行提取,提取液过滤,得人参皂苷提取液;
(2)将步骤(1)得到的人参皂苷提取液通过大孔吸附树脂柱,先用水洗脱,然后用体积百分浓度为35%~85%的乙醇梯度洗脱,收集洗脱液,浓缩、冷冻干燥,得二醇型人参皂苷提取物。
在上述技术方案中,所述二醇型人参皂苷提取物的制备方法包括如下步骤:
(1)将人参粗粉与ph为13的ca(oh)2水溶液按料液比g:ml=1:10的比例混合,在提取温度为20℃,超声提取功率160w的条件下进行提取,提取液过滤,得人参皂苷提取液;
(2)将步骤(1)得到的人参皂苷提取液通过大孔吸附树脂柱,用3~6倍柱体积的水洗脱,然后依次用3~6倍柱体积的35%乙醇、3~6倍柱体积的85%乙醇洗脱,收集85%乙醇洗脱液,浓缩、冷冻干燥,得二醇型人参皂苷提取物。
在上述技术方案中,在步骤(2)中,先用3~6倍柱体积的水洗脱,然后依次用3~6倍柱体积的35%乙醇、3~6倍柱体积的60%乙醇、3~6倍柱体积的85%乙醇洗脱,收集85%乙醇洗脱液,经浓缩、冷冻干燥得二醇型人参皂苷提取物的干燥品。
本发明中,将步骤(1)得到的人参皂苷提取液通过大孔吸附树脂柱吸附,静置2h以上,使人参皂苷等非极性以及弱极性成分充分吸附于大孔吸附树脂,之后,先用水洗脱,以除去未吸附的大部分极性杂质;然后用35%乙醇洗脱,以除去三醇型人参皂苷和少部分杂质;之后再用60%乙醇洗脱,进一步除去其它型人参皂苷和杂质,以提高提取物中的二醇型人参皂苷的纯度,本发明中该步骤可省略;最后用85%乙醇洗脱,以收集二醇型人参皂苷,主要含有rb1、rb2、rc和rd四种,其含量之和不低于总提取物量的38%。
在上述技术方案中,在步骤(1)中,所述的提取步骤中,提取次数为1~3次,每次提取时间为20~60min,优选为20min。
在上述技术方案中,在步骤(2)中,将所述的人参皂苷提取液,过滤,滤液浓缩至浸膏,加入80%乙醇溶解,经过滤得人参皂苷滤液;人参皂苷滤液浓缩除去乙醇,加入蒸馏水溶解,得人参皂苷水溶液,水溶液以流速0.2~0.3ml/s的速率通过预先用水洗至无乙醇味的大孔吸附树脂柱,上柱结束后可放置2h或以上,以使滤液中的人参皂苷等成分充分吸附于大孔吸附树脂上。所述大孔吸附树脂优选采用大孔吸附树脂d101。
本发明还提供上述的二醇型人参皂苷纳米乳的制备方法,包括如下步骤:
(a)按照配比将由司盘80和1,2-丙二醇组成的混合乳化剂加入到油相中,在40℃的加热条件下以650~1300r/min的转速搅拌混合,得澄清透明状态的混合溶液;
(b)将二醇型人参参皂苷提取物溶于水得水相,将水相逐滴加入到步骤(a)得到的混合溶液中,搅拌均匀。
在上述技术方案中,在步骤(b)中,在40℃、650~1300r/min的转速搅拌下将水相逐滴加入到步骤(a)得到的混合溶液中。
本发明还提供一种用于抗皮肤衰老的化妆品组合物,该组合物包含有上述的二醇型人参皂苷纳米乳。该组合物还可以包括化妆品可接受的辅料,对于所述辅料的种类以及使用量不进行特别限定,根据需要可以采用本领域常规的辅料以及使用量,并可制备得到含有上述二醇型人参皂苷纳米乳的具有抗皮肤衰老的化妆品组合物。所述化妆品组合物可以为液体型、乳液型、膏霜型化妆品及面膜类美容保养护肤品。
本发明的有益效果:
本发明将二醇型人参皂苷制成w/o型纳米乳,易溶于水的二醇型人参皂苷被包裹于内水相,表面为油相,这大大增加了乳剂与皮肤的亲和性,又由于乳剂粒径在纳米级别,使其透过皮肤的性能显著增加,而且对二醇型人参皂苷具有一定的保护作用和缓释作用,显著提高了其抗皮肤衰老功能。采用碱水超声提取法提取得到作为活性成分的二醇型人参皂苷提取物,其中二醇型人参皂苷rb1,rb2,rc,rd的含量之和不低于38%。本发明采用恒温低能乳化法制备纳米乳,制备工艺简便,质量易于控制。
附图说明
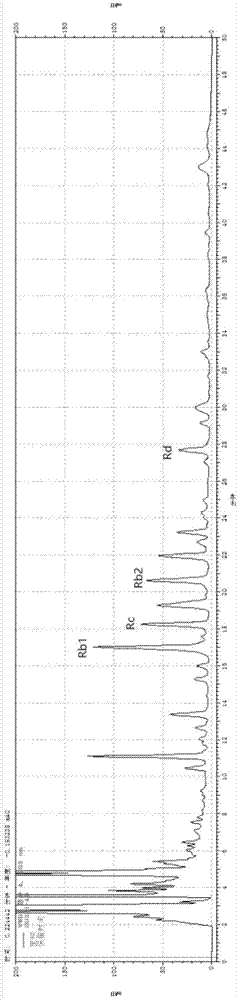
图1为二醇型人参皂苷提取物干燥品hplc色谱图。
图2为二醇型人参皂苷纳米乳的粒径测量结果。
图3为二醇型人参皂苷纳米乳的皮肤累计透过量结果。
图4为二醇型人参皂苷纳米乳的皮肤滞留量结果。
图5为二醇型人参皂苷纳米乳各组的羟脯氨酸含量测定结果。
图6为二醇型人参皂苷纳米乳各组的i型胶原含量测定结果。
图7为二醇型人参皂苷纳米乳各组的iii型胶原含量测定结果。
图8为二醇型人参皂苷纳米乳各组的timp-1含量测定结果。
图9为二醇型人参皂苷纳米乳各组的timp-2含量测定结果。
图10为二醇型人参皂苷纳米乳各组的mmp-1含量测定结果。
具体实施方式
下面结合附图和具体实施方式对本发明作进一步的详细说明,但本发明并不局限于这些实施方式。下述实施例中,如无特殊说明,所使用的实验方法均为常规方法,所用材料、试剂等均可从生物或化学公司购买。
人参粗粉:五年生干燥人参,粉碎,粉末过四号筛,得粒径约250μm的粗粉,用于提取。
实施例1
二醇型人参皂苷提取物,按照如下方法制备得到:
(1)将人参粗粉与ph=13的ca(oh)2水溶液按料液比=1:10(g:ml)的比例混合,在提取温度为20℃,超声提取功率为160w,提取时间20min的条件下进行提取,提取完成后将药物残渣过滤,得人参皂苷提取液;提取液过滤,滤液浓缩至浸膏,加入80%乙醇溶解,过滤得人参皂苷滤液,人参皂苷滤液浓缩除去乙醇,加入蒸馏水溶解,得人参皂苷水溶液;
(2)大孔吸附树脂(d101,国药集团化学试剂有限公司)装入分离柱中,用水洗柱子至大孔吸附树脂无醇味,人参皂苷水溶液湿法上柱,流速为每秒0.2ml,静置2小时后用4倍柱体积水洗柱,以除去大部分杂质,然后用3倍柱体积35%乙醇洗脱,除去三醇型人参皂苷和少部分杂质,再用3倍柱体积85%乙醇洗脱,收集85%乙醇洗脱液;
(3)将85%乙醇洗脱液,回收乙醇,浓缩液在-20℃下冷冻干燥72h,制得二醇型人参皂苷提取物干燥品。
取干燥品500mg,加入50ml甲醇,超声溶解,得10mg/ml溶液。用hplc法检测,检测方法:色谱柱hypersilgoldc18(250mm×4.6μm,5μm),检测波长为203nm,进样量为10μl,柱温为40℃,流速为1.000ml/min,梯度洗脱如下表1:
表1梯度洗脱表
检测结果如图1,通过峰值的计算,可得干燥品中含有二醇型人参皂苷rb1,rb2,rc,rd,其含量之和约为42%。
实施例2
以实施例1制备得到的二醇型人参皂苷提取物的原料,制备二醇型人参皂苷纳米乳,制备方法如下:
(1)司盘80与1,2-丙二醇按质量比2:1的混合得混合乳化剂,将棕榈酸异丙酯(即油相)与混合乳化剂按照质量比7.5:2.5混合,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率来搅拌混合,搅拌至混合溶液呈澄清透明状态,得混合溶液;
(2)二醇型人参皂苷提取物溶于水得水相,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率搅拌的条件下,将水相逐滴加入到油相与混合乳化剂的混合溶液中,混合体系由澄清变浑浊的临界点,停止滴加,得二醇型人参皂苷纳米乳。
其中,二醇型人参皂苷提取物在水相中的质量浓度为200mg/ml;所述水相和油相的质量比为8:45。
实施例3
以实施例1制备得到的二醇型人参皂苷提取物的原料,制备二醇型人参皂苷纳米乳,制备方法如下:
(1)司盘80与1,2-丙二醇按质量比2:1的混合得混合乳化剂,将肉豆蔻酸异丙酯(即油相)与混合乳化剂按照质量比7.5:2.5混合,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率来搅拌混合,搅拌至混合溶液呈澄清透明状态,得混合溶液;
(2)二醇型人参皂苷提取物溶于水得水相,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率搅拌的条件下,将水相逐滴加入到油相与混合乳化剂的混合溶液中,混合体系由澄清变浑浊的临界点,停止滴加,得二醇型人参皂苷纳米乳。
其中,二醇型人参皂苷提取物在水相中的质量浓度为200mg/ml;所述水相和油相的质量比为8:45。
实施例4
以实施例1制备得到的二醇型人参皂苷提取物的原料,制备二醇型人参皂苷纳米乳,制备方法如下:
(1)司盘80与peg400按质量比2:1的混合得混合乳化剂,将棕榈酸异丙酯(即油相)与混合乳化剂按照质量比7.5:2.5混合,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率来搅拌混合,搅拌至混合溶液呈澄清透明状态,得混合溶液;
(2)二醇型人参皂苷提取物溶于水得水相,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率搅拌的条件下,将水相逐滴加入到油相与混合乳化剂的混合溶液中,混合体系由澄清变浑浊的临界点,停止滴加,得二醇型人参皂苷纳米乳。
其中,二醇型人参皂苷提取物在水相中的质量浓度为200mg/ml;所述水相和油相的质量比为8:45。
实施例5
以实施例1制备得到的二醇型人参皂苷提取物的原料,制备二醇型人参皂苷纳米乳,制备方法如下:
(1)司盘80与1,2-丙二醇按质量比3:1的混合得混合乳化剂,将棕榈酸异丙酯(即油相)与混合乳化剂按照质量比7.5:2.5混合,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率来搅拌混合,搅拌至混合溶液呈澄清透明状态,得混合溶液;
(2)二醇型人参皂苷提取物溶于水得水相,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率搅拌的条件下,将水相逐滴加入到油相与混合乳化剂的混合溶液中,混合体系由澄清变浑浊的临界点,停止滴加,得二醇型人参皂苷纳米乳。
其中,二醇型人参皂苷提取物在水相中的质量浓度为200mg/ml;所述水相和油相的质量比为8:45。
实施例6
以实施例1制备得到的二醇型人参皂苷提取物的原料,制备二醇型人参皂苷纳米乳,制备方法如下:
(1)司盘80与1,2-丙二醇按质量比1:1的混合得混合乳化剂,将棕榈酸异丙酯(即油相)与混合乳化剂按照质量比7.5:2.5混合,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率来搅拌混合,搅拌至混合溶液呈澄清透明状态,得混合溶液;
(2)二醇型人参皂苷提取物溶于水得水相,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率搅拌的条件下,将水相逐滴加入到油相与混合乳化剂的混合溶液中,混合体系由澄清变浑浊的临界点,停止滴加,得二醇型人参皂苷纳米乳。
其中,二醇型人参皂苷提取物在水相中的质量浓度为200mg/ml;所述水相和油相的质量比为8:45。
实施例7
以实施例1制备得到的二醇型人参皂苷提取物的原料,制备二醇型人参皂苷纳米乳,制备方法如下:
(1)司盘80与1,2-丙二醇按质量比2:1混合得混合乳化剂,将棕榈酸异丙酯(即油相)与混合乳化剂按照质量比8:2混合,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率来搅拌混合,搅拌至混合溶液呈澄清透明状态,得混合溶液;
(2)二醇型人参皂苷提取物溶于水得水相,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率搅拌的条件下,将水相逐滴加入到油相与混合乳化剂的混合溶液中,混合体系由澄清变浑浊的临界点,停止滴加,得二醇型人参皂苷纳米乳。
其中,二醇型人参皂苷提取物在水相中的质量浓度为200mg/ml;所述水相和油相的质量比为1:6。
实施例8
以实施例1制备得到的二醇型人参皂苷提取物的原料,制备二醇型人参皂苷纳米乳,制备方法如下:
(1)司盘80与1,2-丙二醇按质量比2:1混合得混合乳化剂,将棕榈酸异丙酯(即油相)与混合乳化剂按照质量比7.5:2.5混合,在30℃的加热条件下,用磁力搅拌器以转速650r/min的速率来搅拌混合,搅拌至混合溶液呈澄清透明状态,得混合溶液;
(2)二醇型人参皂苷提取物溶于水得水相,在30℃的加热条件下,用磁力搅拌器以转速650r/min的速率搅拌的条件下,将水相逐滴加入到油相与混合乳化剂的混合溶液中,混合体系由澄清变浑浊的临界点,停止滴加,得二醇型人参皂苷纳米乳。
其中,二醇型人参皂苷提取物在水相中的质量浓度为200mg/ml;所述水相和油相的质量比为8:45。
实施例9
以实施例1制备得到的二醇型人参皂苷提取物的原料,制备二醇型人参皂苷纳米乳,制备方法如下:
(1)司盘80与1,2-丙二醇按质量比2:1混合得混合乳化剂,将棕榈酸异丙酯(即油相)与混合乳化剂按照质量比7.5:2.5混合,在40℃的加热条件下,用磁力搅拌器以转速1300r/min的速率来搅拌混合,搅拌至混合溶液呈澄清透明状态,得混合溶液;
(2)二醇型人参皂苷提取物溶于水得水相,在40℃的加热条件下,用磁力搅拌器以转速1300r/min的速率搅拌的条件下,将水相逐滴加入到油相与混合乳化剂的混合溶液中,混合体系由澄清变浑浊的临界点,停止滴加,得二醇型人参皂苷纳米乳。
其中,二醇型人参皂苷提取物在水相中的质量浓度为200mg/ml;所述水相和油相的质量比为8:45。
实施例10
以实施例1制备得到的二醇型人参皂苷提取物的原料,制备二醇型人参皂苷纳米乳,制备方法如下:
(1)司盘80与1,2-丙二醇按质量比2:1混合得混合乳化剂,将棕榈酸异丙酯(即油相)与混合乳化剂按照质量比7.5:2.5混合,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率来搅拌混合,搅拌至混合溶液呈澄清透明状态,得混合溶液;
(2)二醇型人参皂苷提取物溶于水得水相,在40℃的加热条件下,用磁力搅拌器以转速650r/min的速率搅拌的条件下,将水相逐滴加入到油相与混合乳化剂的混合溶液中,混合体系由澄清变浑浊的临界点,停止滴加,得二醇型人参皂苷纳米乳。
其中,二醇型人参皂苷提取物在水相中的质量浓度为250mg/ml;所述水相和油相的质量比为8:45。
实施例11二醇型人参皂苷纳米乳粒径测定
取适量实施例2制备得到的二醇型人参皂苷纳米乳置于粒度测试皿中,使用zeta电位粒度测试仪(manobrook90pluszeta,brookhaven)对其进行粒径测定,测定3次。测定结果如图2,图2可见,二醇型人参皂苷纳米乳平均粒径为17.4nm,符合纳米乳粒度要求。
实施例12二醇型人参皂苷纳米乳体外累计透过量测定
取六只成年雄性小鼠,随机分成两组,每组三只,分别为二醇型人参皂苷纳米乳(实施例2制备得到)组和二醇型人参皂苷水溶液组。取小鼠腹部皮肤,固定于透皮扩散池,两组分别给药3ml浓度为4.2mg/ml人参皂苷纳米乳和4.2mg/ml人参皂苷水溶液。接收液为pbs磷酸盐缓冲液,于0.5h、1h、2h、3h、4h、6h、8h、12h抽样,抽样量2ml,每次抽样后补充2mlpbs磷酸盐缓冲液,每次抽样接收液进行高效液相色谱测定,计算两组二醇型人参皂苷单位皮肤面积累计透过量。
分别对纳米乳组和水溶液组单位皮肤累计透过量作图,结果如图3,可见,纳米乳组二醇型人参皂苷透过量明显高于水溶液组,表明二醇型人参皂苷纳米乳能有效的透过皮肤,具有良好的透皮性能。
实施例13二醇型人参皂苷纳米乳皮肤滞留量测定
在实施例11中,取每组给药12h后小鼠皮肤,空白接收液漂洗皮肤表面残留药物,固定剪取给药部位皮肤,剪碎,用组织匀浆器匀浆,加2mlpbs磷酸缓冲液超声提取20min,8000r/min离心15min取上清液,进行高效液相测定,计算皮肤内滞留二醇型人参皂苷含量。
结果如图4,可见,纳米乳组的二醇型人参皂苷皮肤滞留量显著高于水溶液组,这意味着纳米乳皮肤给药后二醇型人参皂苷能在皮肤部位进行滞留,有一定缓释作用,延长药物作用时间,提高生物利用度。
实施例14二醇型人参皂苷纳米乳抗皮肤衰老动物实验
研究二醇型人参皂苷纳米乳(实施例2制备)对皮肤内胶原蛋白含量的影响:取成年雄性小鼠30只,背部脱毛,平均分成六组,分为人参皂苷纳米乳高剂量组(1.54mg/ml)、人参皂苷纳米乳中剂量组(0.77mg/ml)、人参皂苷纳米乳低剂量组(0.38mg/ml)、人参皂苷水溶液组(0.77mg/ml)、空白纳米乳组、阳性对照组(美肤宝五珍保湿紧致霜)。
每组小鼠每天涂抹给药一次,每只每次给药0.2ml,连续给药4周,每周记录各组小鼠体重变化,第4周处死小鼠,取背部给药部位皮肤,-40℃冻存。
各称取每组每只小鼠皮肤0.5g,剪碎,加入匀浆管中,再加入9倍量0.01mmolpbs缓冲液,用内切式组织匀浆器匀浆,制成10%匀浆液,每管匀浆液用细胞粉碎仪粉碎1min,再于8000r/min离心机中离心10min,取上清液,冻存。
按elisa试剂盒说明书分别检测上清液中羟脯氨酸、i型胶原、iii型胶原、基质金属蛋白酶-1(mmp-1)、基质金属蛋白酶抑制因子-1(timp-1)、基质金属蛋白酶抑制因子-2(timp-2)含量。
结果如图5~10,人参皂苷纳米乳组与其他组相比能显著增加羟脯氨酸、i型胶原、iii型胶原含量,抑制胶原分解的基质金属蛋白酶抑制因子-1(timp-1)和基质金属蛋白酶抑制因子-2(timp-2)显著升高,促进胶原分解的基质金属蛋白酶-1(mmp-1)降低。以上指标并显现出剂量依赖性。由此可见,二醇型人参皂苷纳米乳可通过激活胶原蛋白调控因子,促进皮肤胶原蛋白合成,抑制胶原蛋白酶活性来达到抗皮肤衰老的目的。
以上已对本发明创造的较佳实施例进行了具体说明,但本发明创造并不限于所述实施例,熟悉本领域的技术人员在不违背本发明创造精神的前提下还可作出种种的等同的变型或替换,这些等同的变型或替换均包含在本申请权利要求所限定的范围内。
- 还没有人留言评论。精彩留言会获得点赞!