一种通过太赫兹偏振参数成像方法检测生物体浅层组织的装置及方法与流程
本发明涉及生物体浅层组织的检测装置领域,尤其涉及一种通过太赫兹偏振参数成像方法检测生物体浅层组织的装置及方法。
背景技术:
生物医学研究中光学的显微成像是很有必要的手段。显微成像不仅能提供很多重要的微观结构,而且在病理诊断中,对固定、染色后的组织生物切片进行显微观察更是对多种疾病确诊的"金标准"。现有的光学显微成像方法大多需对样品进行染色、同位素标记等处理,这无疑会对细胞的正常生理过程产生或多或少的影响。oldenbourg等提出将光的偏振与光学显微镜结合,通过测量双折射的改变即可获得细胞的多种结构信息,并设计出了基于液晶可调波片的新型偏振光显微镜lc-polscope。偏振光显微的最大优势在于不需要对样品进行染色、标记等操作,是完完全全无损的细胞成像方法。此后oldenbourg等对偏振显微镜进行了发展完善,提出了优化成像参数,并且最终推出了商用的仪器abrio成像系统。偏振显微的方法作为一种非标记的细胞级成像方法具有广阔的应用前景,abrio成像系统具有参数特异性较高的特点,通过测量样品的双折射分布可获取结构信息,适合研究海洋微生物、细胞等散射效应不明显的样品。然而对于生物组织切片等散射退偏效应无法忽略的样品,利用现有偏振显微参数成像方法将产生较大的误差。因此对于生物组织医学诊断而言,需要对已有偏振显微成像参数进行更多的优化,或者寻找更加具特异性的显微成像指标。
光波位相等矢量参数调制实现非直观成像的新方法利用被测物质结构各向异性所针对性选择的光波矢量参数进行模式化调制,通过近场耦合和远场光场传输变换,通过拟合、过滤、反演来获得成像结果。这种方法不依赖传统的光强差和色调等光学成像参数,通过获得较大量的附加调制光波信息,以绕开衍射极限,实现超分辨,同时它能克服点扫描方式效率低、适应性差的缺点。该方法可以广泛应用于新材料、生物医学、极大规模集成电路等检测的国际前沿纳米工程应用领域。
太赫兹波(terahertzwave,terahertz,t-rays,thz波,t射线),通常是指频率范围在0.1thz—10thz(1thz=1012hz),波长在0.03—3mm之间的电磁波。从频率上看,该波段位于毫米波和红外线之间,属于远红外波段;从能量上看,在电子和光子之间。在电磁频谱上,太赫兹波段基本上还是一个“空白”,因为在这个频段上,光学理论和微波理论研究都不完全适用,从而形成了科学家们通常所说的“太赫兹空隙”(thzgap)。美国《科技评论》将thz技术列为改变未来世界的十大关键技术之一,并称“21世纪为太赫兹时代”。太赫兹波具有瞬态性、低能性、吸水性以及针对生物分子低频振动模式所呈现出的指纹性等特点,决定了其在生物医学等领域的广阔前景。在组织检测方面,太赫兹光谱技术不需要进行复杂的切片染色等样本处理过程,不受病理医生主观因素的影响,有望作为一种无损伤检测手段对内镜检测进行有效辅助,提高组织诊断效率和准确性;在生物分子检测方面,太赫兹光谱技术具有快速、无标记的优势,有望对病变相关生物分子的检测手段形成可靠补充。此外,基于太赫兹光谱技术的生物分子检测研究有望深化对病变组织太赫兹响应机理的认识。
由于新鲜组织样本中水分对太赫兹辐射的强吸收,早期thz射线在医学上的应用主要停留在表皮附近的组织。但成人癌症的85%,包括皮肤癌、乳腺癌、食管癌、结肠癌、膀胱癌及前列腺癌等,都发生在上皮组织(鳞上皮、腺上皮、移行上皮、被覆上皮等),因此研究人员认为使用thz射线有可能检测到这些癌症。以皮肤组织为例,研究发现炎症组织(包括癌症组织和烧伤组织等)与正常组织对太赫兹辐射的吸收特性明显不同,并且根据数据可以进一步推算肿瘤组织的深度和烧伤程度。此外,通过分析折射率的改变还可以分辨皮肤各层之间的分界及厚度,观察角质层的水合作用,监测和评价伤口愈合过程及烧伤组织的程度和范围等。fitzgerld等使用太赫兹脉冲成像技术对乳腺癌患者进行了初步研究,结果发现thz射线能够区分癌组织与健康组织,并且与组织学结果一致。globus等研究发现,通过比较前列腺和膀胱细胞的透射光谱特性,可将2种癌细胞区分开来。
技术实现要素:
本发明提供了一种通过太赫兹偏振参数成像方法检测生物体浅层组织的装置及方法,本发明通过对各光学元器件的不同摆放实现对太赫兹波的控制和探测,采用偏振参数模式化成像方法绕开衍射极限,实现超分辨,同时克服点扫描方式效率低、适应性差的缺点,测量灵敏度高,装置整体布局合理,结构紧凑,操作简单;本发明实现了对生物体浅层组织的成像,可以准确的反映各个组织部位状态,详见下文描述。
一种通过太赫兹偏振参数成像方法检测生物体浅层组织的装置及方法,包括:太赫兹源,所述太赫兹源发射的太赫兹波入射到太赫兹起偏器上,偏振的太赫兹波入射到成一定角度的太赫兹分光镜后,一部分反射到与计算机控制系统输入端相连接的第一太赫兹探测器,一部分透射的太赫兹波作为生物体浅层组织样品检测时的入射光,依次经过第一太赫兹非球面透镜、放置生物体浅层组织样品的全反射棱镜、1/4波片、检偏器、第二太赫兹非球面透镜,最终入射到与计算机控制系统输入端相连接的第二太赫兹探测器。
全反射棱镜固定于二维移动平台上,计算机控制系统接收第一太赫兹探测器与第二太赫兹探测器所接收到的数据及二维移动扫描平台的移动信息。
其中,所述太赫兹源发射的太赫兹波的频率范围为0.3thz—3thz。
其中,所述太赫兹源发射的太赫兹波经太赫兹起偏器进行偏振态的调制,该起偏模块由计算机控制的中空电机带动起偏器转动来实现。
其中,所述二维移动平台由计算机控制系统控制,通过带动全反射棱镜沿y和z方向二维扫描,实现生物体浅层组织样品表面成像。
进一步地,所述全发射棱镜的上表面中心处于太赫兹波经第一太赫兹透镜聚焦的焦点处。
其中,所述生物体浅层组织样品紧贴全反射棱镜。
进一步地,所述太赫兹分光镜反射的太赫兹波作为检测的参考光以降低噪声,其被第一太赫兹探测器接收;透射的太赫兹波作为检测时的入射光,经全反射棱镜、1/4波片、检偏器后被第二太赫兹探测器接收。
其中,所述波片起到相位延迟的作用,波片的材料采用晶体,即双折射材料。
其中,所述计算机控制系统将第二太赫兹探测器的信号除以第一太赫兹探测器的信号作为含有样品信息的太赫兹信号;若太赫兹波的功率相对稳定,第二太赫兹探测器可以省略,直接将第一太赫兹探测器的信号作为含有样品信息的太赫兹信号。
其中,所述计算机控制系统将第二太赫兹探测器的信号除以第一太赫兹探测器的信号作为含有背景信息的太赫兹信号;若太赫兹波的功率相对稳定,第二太赫兹探测器可以省略,直接将第一太赫兹探测器的信号作为含有背景信息的太赫兹信号。
其中,所述计算机控制系统将含有样品信息的太赫兹信号除以含有背景信息的太赫兹信号,获取不同位置处生物体浅层组织样本对太赫兹波的反射与衰减程度。
本发明与现有的技术相比,其显著优点在于:
1.本发明利用太赫兹波对于组织水浓度与细胞密度具有高敏感性的特性,利用太赫兹波对生物分子的灵敏度和特异性以及生物体浅层组织各个部分水浓度不同的特点,实现了组织部位不同区域的检测,其安全性与准确性较高;
2.本发明采用太赫兹atr成像技术,克服了生物样品制备复杂的缺点,避免了对样品的破坏性分析,节省了时间成本和制作成本;
3.本发明采用太赫兹偏振参数成像技术,具有完全无损细胞成像的特点,能够获取生物组织中的光学特性和微观结构信息,为生物组织的检测提供了新的检测技术手段。
附图说明
图1是本发明提供的通过太赫兹偏振参数成像方法检测生物体浅层组织的装置的结构示意图;
各部件代表元件如下:1.太赫兹源;2.太赫兹起偏器;3.太赫兹分光镜;4.第一太赫兹非球面透镜;5.样品;6.全反射棱镜;7.太赫兹1/4波片;8.检偏器;9.第二太赫兹非球面透镜;10.第二太赫兹探测器;11.第一太赫兹探测器;12.二维移动平台;13.计算机控制系统。
图2是太赫兹起偏器。
图3是太赫兹分光镜。
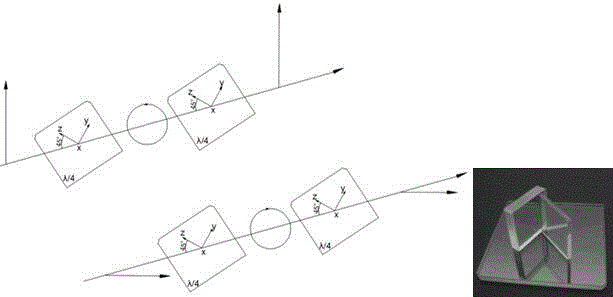
图4是太赫兹1/4波片。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
太赫兹偏振参数成像技术具有完全无损细胞成像的特点,能够获取生物组织中的光学特性和微观结构信息,为生物组织的检测提供了新的检测技术手段。
实施例:一种通过太赫兹偏振参数成像方法检测生物体浅层组织的装置及方法,参见图1,该检测装置包括:1太赫兹源、2太赫兹起偏器、3太赫兹分光镜、4第一太赫兹非球面透镜、5样品、6全反射棱镜、7太赫兹1/4波片、8检偏器、9第二太赫兹非球面透镜、10第二太赫兹探测器、11第一太赫兹探测器、12二维移动平台、13计算机控制系统。
太赫兹源1发射频率范围为0.3thz—3thz的太赫兹波,太赫兹源发射的太赫兹波入射到由计算机13控制的中空电机带动的太赫兹起偏器2上,偏振的太赫兹波入射到太赫兹分光镜3,调整太赫兹分光镜3使其与入射的太赫兹波成一定角度(10—80°),这样放置将入射的太赫兹波分成一定光强的透射太赫兹波和反射太赫兹波,经太赫兹分光镜3反射后的太赫兹波作为生物体组织样品检测时的参考光以降低噪声被第一太赫兹探测器11接收。经太赫兹分光镜3透射的太赫兹波作为生物体组织样品检测时的入射光,依次经过第一太赫兹非球面透镜4、放置生物体浅层组织样品5的全反射棱镜6、1/4波片7、检偏器8、第二太赫兹非球面透镜9,最终被第二太赫兹探测器10接收。
其中,第一太赫兹非球面透镜4与第二太赫兹非球面透镜9焦距相等,且等距离放置于全反射棱镜6的两侧,第一太赫兹非球面透镜4对太赫兹波进行会聚,在焦点处光斑最小,全反射棱镜6固定于二维移动扫描平台12上,调整二维移动扫描平台12的位置,使得全反射棱镜6的上表面中心处于太赫兹波会聚的焦点处,待测生物样品5的待测面与全反射棱镜6的上表面紧密接触,经过全反射棱镜6后的太赫兹波再经过第二太赫兹非球面透镜9会聚入射到第二太赫兹探测器10。
计算机控制系统13控制中空电机带动起偏器2转动来进行偏振态的调制,同时采集两个太赫兹探测器10与11探测到的信号,并控制二维移动扫描平台12沿y和z方向二维扫描,得到生物体组织样品不同位置处的太赫兹波反射与衰减程度。
进一步地,全反射棱镜6为道威棱镜结构设计的硅或锗棱镜,thz波入射方向与棱镜底面平行,棱镜三面抛光,底角和顶角使得太赫兹波折射进入到全反射棱镜6的顶面满足全反射条件。
具体实现时,优选待测生物样品5与全反射棱镜6的上表面紧密接触。
具体实现时,该检测装置的操作如下:
(1)太赫兹源1发射太赫兹波,入射到太赫兹起偏器2上,偏振的太赫兹波入射到太赫兹分光镜3上,太赫兹分光镜3反射的太赫兹波作为生物体样品检测时的参考光以降低噪声,其被第一太赫兹探测器11接收;透射的太赫兹波作为生物体样品检测时的入射光,经衰减全反射棱镜6、1/4波片7、检偏器8后被第二太赫兹探测器10接收;
(2)全反射棱镜6固定于二维移动平台12上,调整二维移动平台12的位置,使得全反射棱镜6的上表面中心处于太赫兹波经第一太赫兹非球面透镜4聚焦的焦点处;
(3)将待测生物样品5放置于全反射棱镜6上,并紧贴全反射棱镜6,计算机控制系统13控制中空电机带动起偏器2转动来进行偏振态的调制,并控制二维移动平台12带动全反射棱镜6沿y和z方向二维扫描,使得上述入射光依次经第一太赫兹非球面透镜4、全反射棱镜6、1/4波片7、检偏器8和第二太赫兹非球面透镜9后被第二太赫兹探测器10接收;计算机控制系统13同时采集第一太赫兹探测器11、第二太赫兹探测器10探测到的信号及样品位置信息;将第二太赫兹探测器10的信号除以第一太赫兹探测器11的信号作为含有样品信息的太赫兹信号;若太赫兹波的功率相对稳定,第二太赫兹探测器10可以省略,直接将第一太赫兹探测器11的信号作为含有样品信息的太赫兹信号;
(4)移除生物体样本,保持全反射棱镜6上表面清洁,计算机控制系统13控制二维移动平台12带动全反射棱镜6沿y和z方向重复扫描步骤(3)的二维区域,使得上述入射光依次经第一太赫兹非球面透镜4、全反射棱镜6、1/4波片7、检偏器8和第二太赫兹非球面透镜9后被第二太赫兹探测器10接收;计算机控制系统13同时采集第一太赫兹探测器11、第二太赫兹探测器10探测到的信号及位置信息;将第二太赫兹探测器10的信号除以第一太赫兹探测器11的信号作为含有背景信息的太赫兹信号;若太赫兹波的功率相对稳定,第二太赫兹探测器10可以省略,直接将第一太赫兹探测器11的信号作为含有背景信息的太赫兹信号;
(5)将步骤(3)所得的含有样品信息的太赫兹信号除以步骤(4)所得的含有背景信息的太赫兹信号,可以获得不同位置处生物体样本对太赫兹波的反射与衰减程度,从而以不同位置处的太赫兹反射或衰减程度得到生物体组织样品的形态情况。
其中,本发明实施例对步骤(3)和步骤(4)的前后执行顺序不做限制。
综上所述,本发明实施例通过对各光学元器件的不同摆放实现对太赫兹波的控制和探测,采用偏振参数模式化成像方法绕开衍射极限,实现超分辨,同时克服点扫描方式效率低、适应性差的缺点,测量灵敏度高,装置整体布局合理,结构紧凑,操作简单;本发明实现了对生物体浅层组织的成像,可以准确的反映各个组织部位状态。
- 还没有人留言评论。精彩留言会获得点赞!