一种蛋白质及其在调控巨噬细胞免疫功能方面的应用的制作方法
本发明涉及一种蛋白质及其在调控巨噬细胞免疫功能方面的应用,属于生物
技术领域:
。
背景技术:
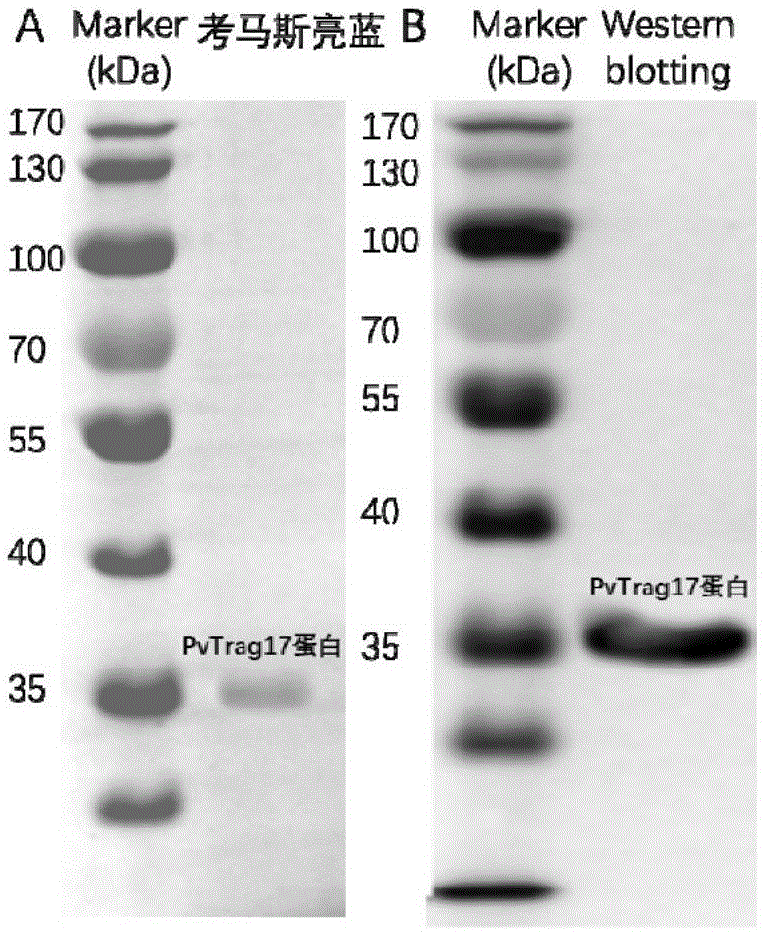
:免疫是人体的一种生理功能,人体依靠这种功能识别“自己”和“非己”成分,从而破坏和排斥进入人体的抗原物质(如病菌等),或人体本身所产生的损伤细胞和肿瘤细胞等,以维持人体的健康。抵抗或防止微生物或寄生物的感染或其它所不希望的生物侵入的状态。因此,免疫力被定义为人体识别和排除异己成分的生理反应,人体内执行这一功能是免疫系统。在当代社会,随着社会的进步发展,生活压力也进一步增加,很大一部分人群处于高幅度压力之下,长期会导致机体免疫功能下降,即免疫力降低。在此不健康状态下,机免疫系统不能正常发挥保护作用,极易招致细菌、病毒、真菌等感染,极易生病;机体的消耗加大,体质虚弱、营养不良、精神萎靡、疲乏无力、食欲降低、睡眠障碍等表现,长此以往会导致身体和智力发育不良,还易诱发重大疾病。因此增强机体免疫功能是当今社会必须重视的一个现状问题。巨噬细胞属免疫细胞,是一种极具异质性的细胞群体,广泛分布在机体组织器官中,在炎症反应、病原体防御和损伤修复中有均发挥重要作用,并能够作为抗原递呈细胞提呈抗原激活免疫应答。巨噬细胞存在一系列连续的功能状态,而m1和m2型巨噬细胞是这已连续状态的两个极端。其中m1型巨噬细胞通过分泌促炎症细胞因子,并专职提呈抗原,参与正向免疫应答,例如m1型巨噬细胞能够分泌no、tnfα、il-6、il-12等促炎因子,参与病原微生物的清除;而m2型通过分泌抑制性细胞因子il-10和/或tgf-b等下调免疫应答,在免疫调节中发挥重要作用,例如,则大量分泌il-10和tgf-β等抗炎因子,参与炎症的消解、组织重塑、血管生成。因此探索调控巨噬细胞定向极化靶点在临床治疗中有非常重要的意义。疟疾是伴随人类出现最早的疾病,至今仍是全球范围内最重要的感染性疾病之一。目前关于疟疾的研究大多数集中在不同种属疟原虫入侵机制和疟疾疫苗的研发,而对疟原虫的药用价值或潜在的临床应用价值研究较少。疟原虫主要通过虫体表面或内部携带的蛋白与肝细胞或红细胞表面受体结合后侵入到机体内。本课题组在对间日疟原虫蛋白进行分析筛选发现pvtrag28是一个的输出蛋白,目前pvtrag17对巨噬细胞的作用尚未见相关研究。技术实现要素:本发明的第一个目的是提供重组pvtrag17蛋白在制备调控巨噬细胞的产品方面的应用。在本发明的一种实施方式中,所述应用包括制备调控巨噬细胞的药物。在本发明的一种实施方式中,所述应用包括促进未活化巨噬细胞向m1型方向极化。在本发明的一种实施方式中,所述药物包括但不限于免疫调节剂。在本发明的一种实施方式中,所述巨噬细胞为未活化的巨噬细胞,包括但不限于raw264.7细胞。本发明的第二个目的是提供制备pvtrag17重组蛋白的方法,所述方法是将来源于疟原虫的pvtrag17蛋白在体外表达。在本发明的一种实施方式中,所述方法包括如下步骤:(1)设计引物,扩增编码所述pvtrag17蛋白的基因,将该基因片段连接到载体上,获得重组质粒;(2)将重组质粒转化到相应的表达细胞中,诱导目的蛋白表达。在本发明的一种实施方式中,所述方法具体包括如下步骤:(1)设计引物,用如seqidno:3和seqidno:4所示引物扩增编码所述pvtrag17蛋白的基因片段,将扩增的基因片段连接到载体上,得到的重组质粒转化到克隆细胞中,提取重组质粒并测序;(2)将测序正确含有目的基因的重组质粒转化到相应的表达细胞中,用iptg诱导目的蛋白表达。在本发明的一种实施方式中,所述表达载体可以为原核细胞表达载体、真核细胞表达载体或昆虫细胞表达载体。在本发明的一种实施方式中,所述的表达细胞可以为原核表达细胞、真核表达细胞或昆虫细胞。在本发明的一种实施方式中,所述表达载体为pet28a(+),所述表达细胞为e.colibl21(de3)。本发明的第三个目的是提供一种抗肿瘤的药物,其含有seqidno.1所示pvtrag17蛋白,及药学上可接受的载体。本发明还要求保护所述pvtrag17蛋白在制备非医药用途的产品方面的应用。有益效果:本发明首次筛选并验证了pvtrag17蛋白在调节巨噬细胞免疫方面的应用,westernblot结果显示pvtrag17蛋白可显著的促进未活化的raw264.7巨噬细胞向m1型巨噬细胞方向极化。将pvtrag17蛋白作用于未活化的raw264.7巨噬细胞,可显著增强raw264.7巨噬细胞分泌no、il-2、il-6、tnf-α的能力,使il-6、tnfα、il-2和inos的mrna水平分别上调6.9倍、7.32倍、11.89倍和11.32倍。附图说明图1为pvtrag17蛋白考马斯亮蓝染色示意图(a)和westernblotting检测图(b),图2为westernblotting法检测pvtrag17对raw264.7细胞极化的影响;图3为elisa法检测pvtrag17对raw264.7细胞分泌il-2、il-6、tnf-α的影响;图4为griess法检测pvtrag17对raw264.7细胞分泌no的影响;图5为rt-pcr法检测pvtrag17对raw264.7细胞inos、il-2、il-6、tnf-α基因表达量的影响具体实施方式实施例1pvtrag17重组质粒的构建原核表达质粒pet28a(+)、宿主菌bl21(de3)及诱导用的iptg均购自北京全式金生物科技有限公司;限制性内切酶、t4dna连接酶、pfudna聚合酶、dntp均购自takara公司。引物的合成和核苷酸序列测序均由苏州金唯智生物科技有限公司完成。琼脂糖亲和介质镍柱(ni)购自qiagen公司。;his-taq标签抗体购自cellsignalingtechnology公司。设计引物通过pcr获取间日疟原虫pvtrag17蛋白的基因序列,引物如下:seqidno.2:ggatccatggaactaaaagccaatatg;seqidno.3:ctcgagtgagtcattatctgtgctcac,其中ggatcc为seqidno.2的酶切位点bamhⅰ;ctcgag为seqidno.3的酶切位点xhoⅰ。以卵形疟原虫基因组为模板,通过pcr扩增获得小鼠pvtrag17基因序列,扩增程序:94℃预变性3min,94℃变性10s、50℃退火30s、72℃延伸90s,循环35次,最后72℃延伸10min。pcr产物进行琼脂糖凝胶电泳检测目的基因扩增条带,然后经过胶回收后,用bamhⅰ及xhoⅰ限制性内切酶对pcr产物及pet28a(+)37℃酶切2h,通过t4连接酶将目的基因过夜连接到原核表达载体pet28a(+)。从-80℃取出e.colidh5α细胞。立即放置于冰上,取连接的产物4μl加入到50μl感受态细胞中,混匀冰浴30min,42℃热激90后取出置于冰浴中2min。在管中加入无抗性的lb培养基1ml,放入37℃摇床中250rpm振荡培养1h。离心后取100μl培养基将菌体重悬,涂匀在含卡那霉素(50μg/ml)的lb平板上置于37℃孵箱中倒置培养过夜后观察菌落生长情况。挑取单克隆,提取质粒后进行测序。测序结果显示,目的基因序列正确。实施例2重组蛋白pvtrag17的表达将测序正确的阳性单克隆接种5ml含卡那霉素的lb培养基,37℃培养过夜,将菌液接种于新鲜500ml含卡那霉素的lb培养基中,当od600为0.6-0.8时,加入1mmol/liptg,诱导8h。取诱导的pvtrag17进行超声破碎裂解,经10%sds-page电泳分析表明pvtrag17蛋白主要定位于包涵体中,分子量大小与预期相符。通过8m尿素溶解包涵体释放pvtrag17蛋白,该蛋白在碳末端带有his-tag标签,因此采用ge公司的his-tag镍柱,按试剂盒说明书进行ni2+亲和色谱纯化。用不同浓度的咪唑将蛋白提纯,咪唑的浓度分别为20mm、50mm、100mm、150mm和250mm,150mm咪唑洗下的蛋白经12%sds-page电泳,考马斯亮蓝染色验证分析。并进一步用westernblot分析目的蛋白纯度。考马斯亮蓝染色结果显示所得纯化产物为目的蛋白,分子量大小与预期相符。westernblot结果显示所表达蛋白的纯度较高、特异性强,见附图1。实施例3pvtrag17蛋白促进巨噬细胞raw264.7极化取对数期raw264.7细胞用含有10%fbs的dmem培养基调整细胞浓度为5×105/ml,以每孔1ml接种于6孔板,置5%co2,37℃培养箱中培养6h,待细胞贴壁后弃上清,pbs缓冲液清洗除去未贴壁细胞。样品组分别加入1ml20μg/ml的pvtrag17,空白组加入等体积培养基。继续培养24h后,裂解细胞后离心取上清用westernblot检测cd80和pd-l1的表达量。westernblot结果显示cd80和pd-l1蛋白印记加深(见附图2),即蛋白表达上调,说明pvtrag17蛋白可显著的促进未活化的raw264.7巨噬细胞向m1型巨噬细胞方向极化。实施例4pvtrag17蛋白促进raw264.7细胞分泌no、il-2、il-6、tnf-α取对数期raw264.7细胞,用含有10%fbs的dmem培养基调整细胞浓度为5×105个/ml,以每孔100μl接种于96孔板,置5%co2,37℃培养箱中培养6h,待细胞贴壁后弃上清,pbs缓冲液清洗除去未贴壁细胞。样品组分别加入100μl不同浓度(5、10、20μg/ml)的pvtrag17,空白组加入等体积培养基。继续培养24h后,收集上清液,用相应elisa试剂盒检测no、il-2、il-6、tnf-α分泌量。在样品浓度范围内,与空白对照组相比较,实验组tnfα、il-6、il-2分泌量显著上调。实验组中tnfα和il-6两种细胞因子的最大分泌量相比较空白组分泌提高了2.91倍和2.71倍;另外相比较空白组无分泌的情况,实验组中il-2分泌量最高达到了2.79pg/ml(附图3);实验组no分泌量提高了3.61倍(附图4)。实施例5pvtrag17蛋白促进raw264.7细胞inos、il-2、il-6、tnf-α基因的表达(1)取对数期raw264.7细胞,用含有10%fbs的dmem培养基调整细胞浓度为1×106个/ml,以每孔1ml接种于6孔板,置5%co2,37℃培养箱中培养6h,待细胞贴壁后弃上清,pbs缓冲液清洗除去未贴壁细胞。样品组分别加入1ml20μg/ml的pvtrag17,空白组加入等体积培养基。继续培养24h后,采用rna提取试剂盒收集各组细胞rna。进一步按照cdna逆转录试剂盒说明书将rna反转录合成dna。(2)合成如下引物(3)rt-pcr反应体系如下所示sybrgreen10μlrox0.4μlcdna1μl上游引物0.5μl下游引物0.5μlddh2o补足20μlpcr反应条件(两步法):95℃预变性30s;95℃变性5s,60℃退火及延伸30s,40个循环;溶解曲线10℃hold;反应结束后,计算基因的相对表达量。结果如附图5。通过对实验结果分析,可知pvtrag17蛋白可使il-6、tnfα、il-2和inos的mrna水平分别上调6.9倍、7.32倍、11.89倍和11.32倍。虽然本发明已以较佳实施例公开如上,但其并非用以限定本发明,任何熟悉此技术的人,在不脱离本发明的精神和范围内,都可做各种的改动与修饰,因此本发明的保护范围应该以权利要求书所界定的为准。sequencelisting<110>江南大学<120>一种蛋白质及其在调控巨噬细胞免疫功能方面的应用<160>4<170>patentinversion3.3<210>1<211>315<212>prt<213>人工序列<400>1metgluleulysalaasnmetlysglyproalaproglnglnlysphe151015serproalalyslysthrglnasnargasnprolysleuserlysmet202530thralailephethrvalserproleuglnileileleuphealaleu354045pheservalpheileleuasnproserhisalaalaserthrgluarg505560glyserilelyscystyrleuproasnasnleumetgluphetrplys65707580aspaspvalaspglnsergluglnleulyslyscysalatrpasnasn859095trpmetmetargleugluserglutrpgluasnpheasnthrsermet100105110lysserlyslysasnvaltrpleuglngluthrgluglnglutrpthr115120125glutrpilelysglnmetgluasnlystrpmetasncysasngluasn130135140ileasnaspglutyrlysasptyrleuileserlysseralathrtrp145150155160thraspgluglutrplysglutrpilelysthrgluglylysasnphe165170175metlysthraspleuglulystrpilelysalalysgluthrserleu180185190aspleuleuleuleuthrglutrpvalglntrplysasnglulysile195200205metalatrpleuleuserglutrplysthrglugluaspthrtyrtrp210215220serglntrpgluhisserthrtrpleulystrpleuasnleuthrgln225230235240lyslyshistrpleulystrplysgluargasnhisarggluglyglu245250255glntrpserthrtrpleuhisvallysgluasnvaltyrilepheser260265270glutrpasnasntrpseriletrplysasnglulysglugluphephe275280285tyrlystrpmetgluaspthrileasnglutrpileasnglulysarg290295300trpasnthrleuvalserthraspasnaspser305310315<210>2<211>948<212>dna<213>人工序列<400>2atggaactaaaagccaatatgaagggtccagcaccccagcaaaagttctcccctgctaag60aaaacacaaaatagaaatcccaagttatccaaaatgacggcaattttcacagtttctcct120ttacagattatcttatttgctctattttcagttttcatcttaaatccctcccatgctgca180agcaccgaaaggggaagtatcaagtgttatcttccaaacaatttaatggaattttggaaa240gatgacgtagatcaatcagaacaattaaaaaaatgtgcgtggaataactggatgatgagg300ttggaatcagaatgggaaaacttcaacacatccatgaagagcaaaaagaacgtatggctc360caagaaacagaacaagaatggaccgaatggattaaacaaatggaaaataaatggatgaat420tgtaatgagaatattaatgatgaatataaggattatcttatatcaaaatctgctacatgg480actgatgaagaatggaaagaatggataaaaacagaagggaaaaactttatgaaaacagat540ttagaaaaatggattaaagcaaaagaaacatcattggatttgttactattaacagaatgg600gtccagtggaaaaatgaaaagatcatggcatggctattgagcgaatggaaaactgaagaa660gacacctactggtcacaatgggaacactcaacatggcttaagtggctcaacttgacccag720aaaaaacattggctcaaatggaaagaaagaaatcatagggaaggtgaacaatggtctact780tggttgcacgttaaagaaaatgtttatatatttagcgagtggaataattggtcaatatgg840aaaaatgaaaaagaagaattcttctacaaatggatggaagatacaattaacgagtggata900aatgagaagaggtggaacaccttggtgagcacagataatgactcataa948<210>3<211>27<212>dna<213>人工序列<400>3ggatccatggaactaaaagccaatatg27<210>4<211>27<212>dna<213>人工序列<400>4ctcgagtgagtcattatctgtgctcac27当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1