一种登革疫苗的免疫效果评价方法与流程
本发明涉及免疫学领域,具体涉及一种登革疫苗的免疫效果评价方法。
背景技术:
登革病毒属于黄病毒科黄病毒属中的一个血清型亚群,依抗原性不同分为1、2、3、4四个血清型,感染后会出现登革热、登革出血热和登革休克综合征。这些疾病广泛流行于热带和亚热带地区,是一种分布广、发病多、危害较大的人类传染病。目前全球范围内有128个国家和地区约39亿人口受到登革病毒的威胁。
现在针对登革病毒已开展了许多研究,但由于目前人是自然界中唯一感染登革病毒并产生症状的宿主,从而使登革病毒动物模型的建立更具挑战性。动物模型是进行病毒致病机制研究和疫苗评价的一种有效工具,登革病毒动物模型主要有两种,非人灵长类动物模型和小鼠模型。其中非人灵长类动物由于成本高且仅能够使登革病毒在其体内细胞中进行复制增殖,引起机体的免疫应答,而不会产生明显的临床症状,被广泛用于研究登革热感染和候选疫苗研发但并不适合早期临床前研究。另一方面,小鼠模型则可以更加经济地用于登革热疫苗临床前研发。目前用以评价登革疫苗免疫效果的小鼠模型主要有野生型乳鼠模型和免疫功能缺陷小鼠模型两种,其中,野生型新生乳鼠常被用以颅内攻毒小鼠免疫血清体外中和病毒后的混合液,根据乳鼠死亡情况来评价疫苗免疫效果。而利用免疫功能缺陷小鼠进行疫苗免疫效果评价时,则是对成年小鼠进行疫苗免疫后,进行登革病毒攻毒并观察小鼠死亡情况。使用这两种模型进行登革疫苗免疫效果评价时,都具有一定的缺点,前者不能准确模拟疫苗在实际使用对象体内的免疫效果,而后者免疫效果虽然直观,但成本高,饲养条件要求严格,体质弱,易死亡。因此构建一个既能准确评价疫苗体内免疫效果,又经济实惠、简单易行,便于获得大量临床前研究论证数据的动物模型显得尤为重要。
乳鼠的自然被动免疫是指母体的特异性抗体通过胎盘或初乳进入胎鼠体内或新生乳鼠体内,使胎鼠或新生乳鼠被动的获得母体抗体的方式。根据抗体生理变化特点可知,新生乳鼠血igg浓度与母体血igg浓度相等。
技术实现要素:
有鉴于此,本发明的目的在于提供一种登革疫苗的免疫效果评价方法,克服现有动物模型的不足,该方法不仅能准确的评价疫苗的免疫效果,相较于现有动物模型还更为经济、易行。
为达到上述目的,本发明提供如下技术方案:
1、一种登革疫苗的免疫效果评价方法,包括如下步骤:
1)准备已测定滴度的登革病毒;
2)利用步骤1)中不同滴度的登革病毒对新生空白子代乳鼠进行颅内攻毒,测得50%乳鼠死亡时的病毒滴度;
3)同时取雌性balb/c小鼠和雄性balb/c小鼠,分别用待检测的登革疫苗对雌性balb/c小鼠和雄性balb/c小鼠进行免疫,免疫结束后,进行合笼直至获得新生免疫子代乳鼠;
4)对新生免疫子代乳鼠颅内注射步骤2)中测得50%乳鼠死亡时的病毒滴度进行攻毒;
5)攻毒后持续观察所有免疫子代乳鼠发病与死亡情况,若免疫子代乳鼠未发病、无死亡情况,则该登革疫苗免疫效果合格;免疫子代乳鼠有死亡情况,则该登革疫苗免疫效果不合格。
优选的,步骤1)中,测定登革病毒的滴度是利用单层vero细胞培养登革病毒,收毒后获得的病毒液通过空斑实验测定滴度。
优选的,步骤2)中,测定50%乳鼠死亡时的病毒滴度具体为:对空白新生乳鼠颅内分别攻毒病毒液原液、病毒液10倍稀释液、病毒液50倍稀释液,病毒液100倍稀释液,注射剂量均为20μl每只,统计乳鼠死亡率,50%乳鼠死亡的浓度即为50%乳鼠死亡的病毒滴度。
优选的,步骤3)中,所述雌性balb/c小鼠和雄性balb/c小鼠的比例为2:1。
优选的,所述雌性balb/c小鼠和雄性balb/c小鼠为6周龄。
优选的,用待检测的登革疫苗免疫次数为4次,每次间隔15天。
优选的,步骤5)中,于攻毒后21天内持续观察所有免疫子代乳鼠发病与死亡情况。
本发明的有益效果在于:本发明公开了一种登革疫苗的免疫效果评价方法,用免疫后成年balb/c小鼠的新生子代乳鼠,以颅内注射的方式进行登革病毒攻毒,通过观察记录攻毒后21天内乳鼠死亡情况以评价疫苗免疫效果。相较于现有的利用野生型乳鼠模型或免疫功能缺陷小鼠模型评价登革疫苗免疫效果的方法,本发明避开不能准确模拟疫苗在实际使用对象中的免疫效果,以及成本高,饲养条件要求严格,体质弱,易死亡的缺点,构建了一个既能准确评价疫苗在实际使用对象体内的免疫效果,且更经济实惠、简单易行的登革疫苗免疫效果评价方法。
附图说明
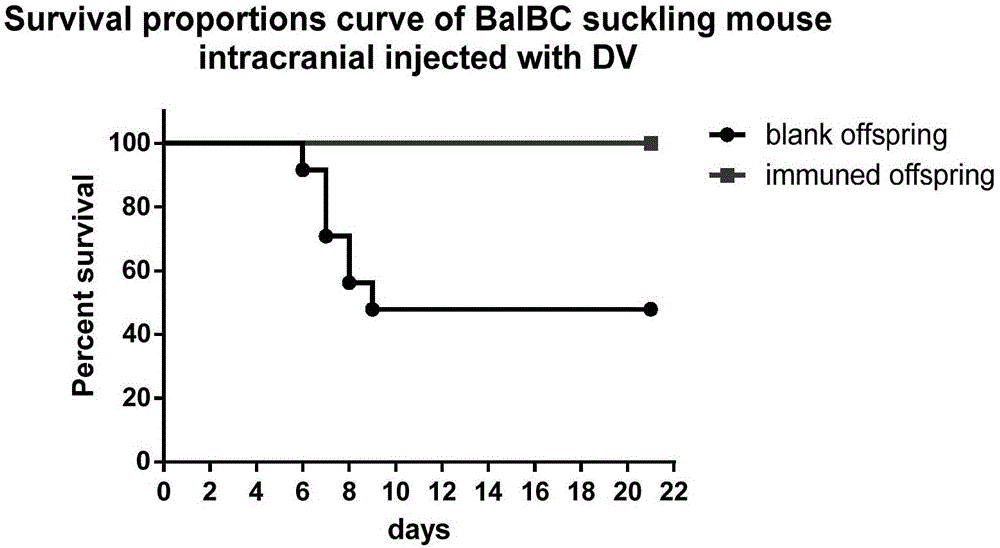
图1为子代乳鼠颅内攻毒(1.25×104)后存活曲线。
图2为子代乳鼠颅内攻毒(1.25×104)后存活曲线。
图3为子代乳鼠颅内攻毒(1.25×104)后存活曲线。
图4为各待测疫苗免疫效果。
具体实施方式
下面结合附图和具体实施例对本发明作进一步说明,以使本领域的技术人员可以更好的理解本发明并能予以实施,但所举实施例不作为对本发明的限定。
一种登革疫苗的免疫效果评价方法,其包括以下步骤:
1)准备已测定滴度的登革病毒,分装后于-80℃冻存备用;避免反复冻融,确保全程使用的登革病毒滴度稳定;
2)准备若干只孕balb/c小鼠,利用步骤1)中病毒对新生空白子代乳鼠进行颅内攻毒;为测得50%乳鼠死亡时的病毒滴度,需对空白新生乳鼠颅内攻毒不同滴度组别的登革病毒,每组注射剂量均为20μl每只;
3)另取10只6周龄雌性balb/c小鼠和5只6周龄雄性balb/c小鼠,用待检测的登革疫苗对以上小鼠进行免疫,免疫结束后,按雌雄比例2:1的比例进行合笼;
4)对新生免疫子代乳鼠颅内注射2)中测得的致50%空白乳鼠死亡的登革病毒进行攻毒,注射剂量为20μl每只,乳鼠总数不小于70只;
5)攻毒后21天内持续观察所有免疫子代乳鼠发病与死亡情况,评价效果表见表1;
免疫子代乳鼠未发病、无死亡情况,则该登革疫苗免疫效果合格。
免疫子代乳鼠有死亡情况,则该登革疫苗免疫效果不合格。
其中发病是指乳鼠出现弓背、消瘦、颤栗等症状;死亡是指特异性死亡,一般死亡时间出现在颅内攻毒6-7天后,攻毒48小时内出现的非特异性死亡情况不计算在内。
进一步,免疫子代乳鼠颅内攻毒致50%空白乳鼠死亡的登革病毒20μl后,观察每只乳鼠体型及精神状态。
如果攻毒21天内免疫子代乳鼠无死亡情况,并且与相近日龄乳鼠的体型和精神状态一致,则该登革疫苗免疫效果合格并且具有优良的免疫效果。
如果攻毒21天内免疫子代乳鼠无死亡情况,但与相近日龄乳鼠相比,体型明显偏小,精神状态不佳,则该登革疫苗免疫效果合格,但抗体水平还未达到使免疫子代乳鼠不产生反应的抗体水平。
表1、疫苗免疫效果评价表
备注:n代表颅内攻毒免疫子代乳鼠总数,起码不小于70只。x为大于0小于n的任一整数。本表以免疫子代乳鼠观察结果为评价疫苗免疫效果的主要指标,体型和精神状态为附带观察。
实施例1
一种登革疫苗的免疫效果评价方法,其包括以下步骤:
1)首先利用单层vero细胞培养登革病毒,收毒后获得的病毒液通过空斑实验测定滴度,结果为(6.25x105);随后将登革病毒液分装成200μl/管、20μl/管、4μl/管和2μl/管,各50管,于-80℃冻存备用;
2)准备若干只孕balb/c小鼠,利用步骤1)中病毒对新生空白子代乳鼠进行颅内攻毒;为测得50%乳鼠死亡时的病毒滴度,需对空白新生乳鼠颅内攻毒不同滴度组别的登革病毒,即培养原液组、10倍稀释组、50倍稀释组和100倍稀释组,其中10倍稀释组、50倍稀释组和100倍稀释组分别在使用前加入180μl、196μl和198μl无菌pbs溶液;每组颅内注射剂量均为20μl每只,致50%乳鼠死亡的病毒滴度组别重复5次,测得50%乳鼠死亡时的病毒滴度为(1.25x104);
3)另取10只6周龄雌性balb/c小鼠和5只6周龄雄性balb/c小鼠,用待检测的登革疫苗对以上小鼠免疫4次,每次间隔15天,最后一次免疫结束后,按雌雄比例2:1的比例进行合笼,获得新生免疫子代乳鼠;
4)对新生免疫子代乳鼠颅内注射步骤2)中测得的致50%空白乳鼠死亡的登革病毒进行攻毒(1.25x104),注射剂量为20μl每只,乳鼠累计总数为82只;
5)攻毒后21天内持续观察所有免疫子代乳鼠发病与死亡情况(图1和表2);
免疫子代乳鼠未发病、无死亡情况,则该登革疫苗免疫效果合格。
免疫子代乳鼠有死亡情况,则该登革疫苗免疫效果不合格。
其中发病是指乳鼠出现弓背、消瘦、颤栗等症状;死亡是指特异性死亡,一般死亡时间出现在颅内攻毒6-7天后,攻毒48小时内出现的非特异性死亡情况不计算在内。
具体的,免疫子代乳鼠颅内攻毒致50%空白乳鼠死亡的登革病毒20μl后,观察每只乳鼠体型及精神状态,并与2)中乳鼠结果对比(图1)。
如果攻毒21天内免疫子代乳鼠无死亡情况,并且与相近日龄乳鼠的体型和精神状态一致,则该登革疫苗免疫效果合格并且具有优良的免疫效果。
如果攻毒21天内免疫子代乳鼠无死亡情况,但与相近日龄乳鼠相比,体型明显偏小,精神状态不佳,则该登革疫苗免疫效果合格,但抗体水平还未达到使免疫子代乳鼠不产生反应的抗体水平。
表2、疫苗免疫效果评价结果:
本实施例,颅内攻毒致50%空白乳鼠死亡的登革病毒20μl后,82只免疫子代乳鼠均未死亡,所有乳鼠体型和精神状态均正常,说明该疫苗免疫效果合格。
实施例2
一种登革疫苗的免疫效果评价方法,其包括以下步骤:
1)首先利用单层vero细胞培养登革病毒,收毒后获得的病毒液通过空斑实验测定滴度(6.25×105),随后将登革病毒液分装成200μl/管、20μl/管、4μl/管和2μl/管,各50管,于-80℃冻存备用;
2)准备若干只孕balb/c小鼠,利用1)中病毒对新生空白子代乳鼠进行颅内攻毒,为测得50%乳鼠死亡时的病毒滴度,需对空白新生乳鼠颅内攻毒不同滴度组别的登革病毒,即培养原液组、10倍稀释组和100倍稀释组,其中10倍稀释组和100倍稀释组分别在使用前加入180μl、196μl和198μl无菌pbs溶液,每组颅内注射剂量均为20μl每只,致50%乳鼠死亡的病毒滴度组别重复5次,测得50%乳鼠死亡时的病毒滴度为(1.25×104);
3)另取10只6周龄雌性balb/c小鼠和5只6周龄雄性balb/c小鼠,用待检测的登革疫苗对以上小鼠免疫4次,每次间隔15天,最后一次免疫结束后,按雌雄比例2:1的比例进行合笼;
4)对新生免疫子代乳鼠颅内注射2)中测得的致50%空白乳鼠死亡的登革病毒进行攻毒(1.25x104),注射剂量为20μl每只,乳鼠累计总数为95只;
5)攻毒后21天内持续观察所有免疫子代乳鼠发病与死亡情况(图2和表3);免疫子代乳鼠未发病、无死亡情况,则该登革疫苗免疫效果合格。
免疫子代乳鼠有死亡情况,则该登革疫苗免疫效果不合格。
所述发病是指乳鼠出现弓背、消瘦、颤栗等症状;死亡是指特异性死亡,一般死亡时间出现在颅内攻毒6-7天后,攻毒48小时内出现的非特异性死亡情况不计算在内。
进一步,免疫子代乳鼠颅内攻毒致50%空白乳鼠死亡的登革病毒20μl后,观察每只乳鼠体型及精神状态,并与2)中乳鼠结果对比(图2)。
如果攻毒21天内免疫子代乳鼠无死亡情况,并且与相近日龄乳鼠的体型和精神状态一致,则该登革疫苗免疫效果合格并且具有优良的免疫效果。
如果攻毒21天内免疫子代乳鼠无死亡情况,但与相近日龄乳鼠相比,体型明显偏小,精神状态不佳,则该登革疫苗免疫效果合格,但抗体水平还未达到使免疫子代乳鼠不产生反应的抗体水平。
表3、疫苗免疫效果评价结果:
本实施例,颅内攻毒致50%空白乳鼠死亡的登革病毒20μl后,95只免疫子代乳鼠均未死亡,64/95乳鼠体型和精神状态正常,31/95乳鼠体型偏小,精神状态不佳,说明该疫苗抗体水平还未达到使免疫子代乳鼠不产生副作用的抗体水平,对部分乳鼠有轻微的影响。
实施例3
一种登革疫苗的免疫效果评价方法,其包括以下步骤:
1)首先利用单层vero细胞培养登革病毒,收毒后获得的病毒液通过空斑实验测定滴度(6.25x105),随后将登革病毒液分装成200μl/管、20μl/管、4μl/管和2μl/管,各50管,于-80℃冻存备用。
2)准备若干只孕balb/c小鼠,利用1)中病毒对新生空白子代乳鼠进行颅内攻毒。为测得50%乳鼠死亡时的病毒滴度,需对空白新生乳鼠颅内攻毒不同滴度组别的登革病毒,即培养原液组、10倍稀释组和100倍稀释组,其中10倍稀释组和100倍稀释组分别在使用前加入180μl和198μl无菌pbs溶液。每组颅内注射剂量均为20μl每只。致50%乳鼠死亡的病毒滴度组别重复5次,测得50%乳鼠死亡时的病毒滴度为(1.25x104)。
3)另取10只6周龄雌性balb/c小鼠和5只6周龄雄性balb/c小鼠,用待检测的登革疫苗对以上小鼠免疫4次,7天后,按雌雄比例2:1的比例进行合笼;
4)对新生免疫子代乳鼠颅内注射2)中测得的致50%空白乳鼠死亡的登革病毒进行攻毒(1.25x104),注射剂量为20μl每只,乳鼠累计总数为79只;
5)攻毒后21天内持续观察所有免疫子代乳鼠发病与死亡情况(图3和表4);
免疫子代乳鼠未发病、无死亡情况,则该登革疫苗免疫效果合格。
免疫子代乳鼠有死亡情况,则该登革疫苗免疫效果不合格。
所述发病是指乳鼠出现弓背、消瘦、颤栗等症状;死亡是指特异性死亡,一般死亡时间出现在颅内攻毒6-7天后,攻毒48小时内出现的非特异性死亡情况不计算在内。
进一步,免疫子代乳鼠颅内攻毒致50%空白乳鼠死亡的登革病毒20μl后,观察每只乳鼠体型及精神状态,并与2)中乳鼠结果对比(图3)。
如果攻毒21天内免疫子代乳鼠无死亡情况,并且与相近日龄乳鼠的体型和精神状态一致,则该登革疫苗免疫效果合格并且具有优良的免疫效果。
如果攻毒21天内免疫子代乳鼠无死亡情况,但与相近日龄乳鼠相比,体型明显偏小,精神状态不佳,则该登革疫苗免疫效果合格,但抗体水平还未达到使免疫子代乳鼠不产生反应的抗体水平。
表4、疫苗免疫效果评价结果:
本实施例,颅内攻毒致50%空白乳鼠死亡的登革病毒20μl后,79只免疫子代乳鼠均未死亡,所有乳鼠体型和精神状态均正常,说明该疫苗免疫效果合格。
实施例4
将免疫效果合格的疫苗免疫小鼠,然后检测小鼠血清抗体效价。小鼠血清用pbs稀释后(1:20000)利用酶联免疫吸附试验进行抗体效价检测。在450nm波长下,使用酶标仪测得吸光度结果如图4所示。结果显示,实施例1中使用疫苗免疫小鼠后,小鼠血清抗体效价为:3.07±0.11;实施例2中使用疫苗免疫小鼠后,小鼠血清抗体效价为:1.99±0.10;实施例3中使用疫苗免疫小鼠后,小鼠血清抗体效价为:2.80±0.04;空白对照组:0.054±0.01;阴性对照组:0.12±0.01。
因此,使用本发明筛选的疫苗能够有效刺激小鼠产生免疫反应,并产生抗体,表明本发明的免疫效果评价方法有效。
以上所述实施例仅是为充分说明本发明而所举的较佳的实施例,本发明的保护范围不限于此。本技术领域的技术人员在本发明基础上所作的等同替代或变换,均在本发明的保护范围之内。本发明的保护范围以权利要求书为准。
- 还没有人留言评论。精彩留言会获得点赞!