灭菌方法与流程
相关申请的交叉引用
本申请要求2017年3月27日提交的美国申请号62/477,030以及2017年10月6日提交的美国申请号62/568,850的优先权,所述申请均以引用的方式整体并入本文。
发明领域
本公开的各种实施方案涉及用于医疗产品灭菌的系统和方法。更确切地说,本公开的具体实施方案涉及用于医疗产品的湿化学灭菌的系统和方法,所述医疗产品的湿化学灭菌包括使用汽化的化学品,诸如汽化的过氧化氢来对预填充注射器(或其他预填充药物递送装置)进行最终灭菌。
附图说明
并入本说明书且构成其一部分的附图示出了各种示例性实施方案,并且连同所述描述一起用于解释所公开的实施方案的原理。附图示出了本公开的不同方面,并且在适当时,说明不同图中的相似结构、部件、材料和/或元件的附图标记被相似地标记。应理解,除了具体示出的那些之外的结构、部件和/或元件的各种组合是预期的并且处在本公开的范围内。
本文描述和示出了许多发明。所描述的发明既不限于其任何单个方面也不限于实施方案,也不限于这类方面和/或实施方案的任何组合和/或变换。此外,所描述的发明的方面和/或其实施方案中的每一个可以单独地或与所描述的发明的其他方面和/或其实施方案中的一个或多个组合地采用。为了简洁起见,本文未单独地论述和/或说明某些变换和组合。值得注意的是,本文中被描述为“示例性”的实施方案或实现方式不应被解释为优于或胜于例如其他实施方案或实现方式;而是,意图反映或指出一个或多个实施方案是一个或多个“示例”实施方案。
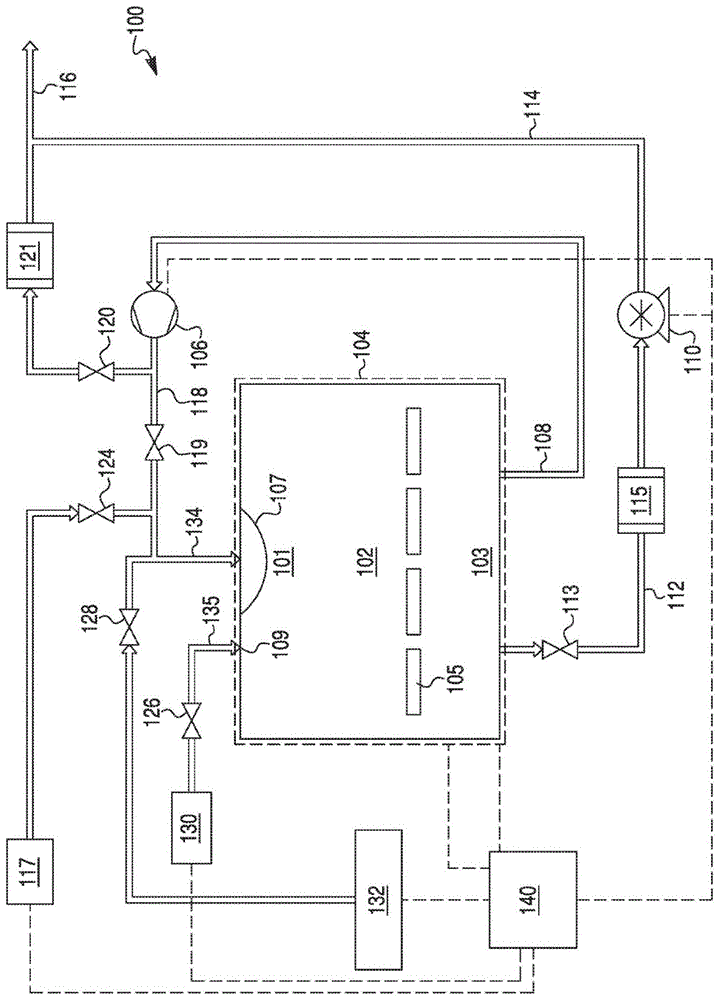
图1是可以用于医疗产品灭菌的示例性灭菌系统的示意图。
图2是使用汽化的化学品对医疗产品进行灭菌的示例性方法中的步骤的流程图。
图3a至图3c是使用汽化的化学品对医疗产品进行灭菌的示例性方法中的步骤的附加流程图。
图4a至图4c是处于使用汽化的化学品对医疗产品进行灭菌的示例性方法中的各个阶段的示例性灭菌系统的示意图。
具体实施方式
如本文所使用,术语“包含(comprises)”、“包含(comprising)”、“包括”、“具有(have)”、“具有(with)”或其任何其他变型意图覆盖非排他性的包含,使得包括一系列元件的过程、方法、物品或设备并不仅仅需要包括这些元件,还可以包括未明确列出或这类过程、方法、物品或设备所固有的其他元件。术语“示例性”是在“示例”而非“理想”的意义上使用。本文中被描述为示例性的任何实现方式不应被解释为优于或胜于其他实现方式。另外,本文中的术语“第一”、“第二”等等并不表示任何次序、数量或重要性,而是用于区分各个元件。类似地,相对于所描述的图提及了相对方位的术语,诸如“前侧”、“顶侧”、“后侧”、“底侧”、“上部”、“下部”等。
如本文所使用,术语“约”和“大约”意味着考虑到所述数值的±10%的可能变动。除非另外明确说明,否则无论是否明确使用这些术语,本文中报导的所有测量值都应被理解为由术语“约”、或术语“大约”修饰。如本文所使用,除非上下文另外明确指明,否则单数形式“一个”、“一种”和“所述”包括复数个提及物。此外,在权利要求中,值、限值和/或范围意指所述值、限值和/或范围加上/减去10%。
如本公开中所使用,术语“灭菌”指代实现对于配制的药物物质或药物产品而言适当的无菌水平以供商业流通和使用。这种无菌水平可以在例如监管指导原则或条例,诸如由美国食品药品监督管理局(u.s.foodanddrugadministration)发布的指导原则中限定。在一些实施方案中,这种无菌水平可以包括例如被置于药物产品的外表面或内表面(例如,注射器的外表面或泡罩包装的内表面)上的生物指示物的微生物群体的6-log减少。在其他实施方案中,这种无菌水平可以包括例如生物指示物的微生物群体的9-log或12-log减少。灭菌指代实现这种适当的无菌水平,同时还实现足够低的残留灭菌化学品含量(例如,汽化的过氧化氢、环氧乙烷等)以供商业流通和使用。这种低残留灭菌化学品含量也可以在监管指导原则或条例中限定。
如本公开中所使用,术语“最终灭菌”指代对在适合于商业流通和使用的容器或包装中,诸如在初级包装部件中或在初级包装部件和次级包装部件两者中的药物产品进行灭菌。
如本公开中所使用,术语“医疗产品”指代在医学上用于活体动物的产品。术语“医疗产品”包括例如药物产品、配制的药物物质、医学植入体、医疗器械或其组合。例如,术语“医疗产品”可以指代包含配制的药物物质的注射器,诸如肠胃外注射器或眼科注射器。其他示例性医疗产品包括例如栓剂施加器和药物治疗、透皮药物递送装置、医学植入体、针、插管、医疗器械和在预期医学使用之前需要灭菌的任何其他产品。
如本公开中所使用,术语“配制的药物物质”指代准备用于医药流通和使用的包含至少一种活性成分(例如,小分子、蛋白质、核酸、或基因治疗药剂)和赋形剂的组合物。配制的药物物质可以包括填充剂、着色剂和其他活性或非活性成分。
如本公开中所使用,术语“药物产品”指代包含配制的药物物质的剂型,诸如用于活性成分的最终剂型。药物产品可以包括用于商业流通或使用的包装,诸如瓶、小瓶或注射器。
如本公开中所使用,术语“汽化的化学品”指代已转化成可以扩散或悬浮在空气中的物质的化学品。在一些情况下,汽化的化学品可以是先与水组合,然后转化成可以扩散或悬浮在空气中的物质的化学品。
如本公开中所使用,术语“流体”指代液体、半液体、蒸汽、或包括氧气、氢气、氮气或其组合的气体。
本公开的实施方案涉及用于将汽化的化学品应用于医疗产品的灭菌中的系统和方法。例如,本公开的实施方案可以涉及用于使用汽化的过氧化氢(vhp)对医疗产品进行最终灭菌的系统和方法。更具体地,本公开的实施方案可以涉及例如用于诸如预填充注射器(pfs)的医疗产品的最终灭菌的系统和方法。
通常期望在灭菌循环中的暴露对正被灭菌的产品不会具有不利的影响并且具有最低限度的损坏或改变风险。经受最终灭菌的医疗产品,诸如pfs因此可能需要灭菌设备、机械设备、控制装置、循环和方法来符合某些限制和要求,以便实现适当的灭菌和/或避免对医疗产品和/或装置、配制的药物物质、药物产品或其他产品的损坏。这类限制和要求可以包括例如:
●医疗产品和/或周围包装在灭菌循环期间可能对深真空压力敏感。例如,pfs可以包括在暴露于深真空环境时易于脱出的预装柱塞。另外,医疗产品可以包括可能受深真空环境影响的易碎材料,诸如玻璃。
●医疗产品、包含于医疗产品中的组合物和/或周围环境在灭菌循环期间可能会受到极端温度的不利影响。例如,包含液体制剂的产品(例如,pfs中的液体药剂)在加热到所述产品在典型的灭菌循环期间可能会暴露于其中的较高温度时可能会不稳定。例如,在这类液体制剂中的药剂在暴露于高温和/或加热到高温时可能会变性、失活、或以其他方式改变。
●医疗产品可能被密集地包装;例如,成批包装的医疗产品可以包含大量完全组装、包装和标记的医疗产品。在最终灭菌的情况下,灭菌剂可能需要横越若干层包装材料、容器材料和/或标记。
●在诸如最终灭菌的一些类型灭菌的情况下,灭菌剂可能需要通过热量或通过质量横越半透膜,以对每个医疗产品的外部以及包装元件的内部进行灭菌。
●用于医疗产品的包装可能会抵抗灭菌材料的渗透,和/或可能对由灭菌引起的温度和压力变化敏感。例如,注射器可以包装在被配置成容纳注射器并限制其移动的塑料‘泡罩’中。这种泡罩可能只是稍微能够透过灭菌材料,和/或可能对压力变化敏感。
●医疗产品可以使用温度或压力敏感元件来密封。例如,pfs可以使用半透气膜‘封盖’来密封。
包括湿化学灭菌的化学灭菌可以提供处理上述医疗产品灭菌的特征中的一些的优点。例如,使用vhp和汽化的水的组合进行的灭菌可以有利地在相对低的温度下执行,从而消除了对将医疗产品暴露于破坏性高温的需求。然而,由于例如灭菌循环实现不完全灭菌,灭菌循环不能在医疗产品的允许温度和/或压力范围内操作,难以从已灭菌的物品中去除有毒的残留vhp和/或灭菌时间长,表明vhp灭菌技术在最终灭菌(例如,pfs的最终灭菌)中的成功应用的证据非常有限。环氧乙烷(“eto”)是vhp的可行的替代品,并且已知是用于对高温和高压敏感的物品进行灭菌的有效试剂。然而,eto对人类的毒性比vhp更大,并且因此在其用于灭菌系统期间和之后呈现出了健康和安全问题。
出于至少以上原因,可能期望将vhp更成功地应用于医疗产品的最终灭菌中。尽管实现相对灭菌“循环效率”(例如,(1)总体灭菌循环时间的减少,和/或(2)灭菌循环操作所在温度的极值的减小),也可能期望如此行为。存在与vhp在(例如,pfs的)最终灭菌中的成功应用相关联的潜在重大价值,并且在将vhp应用于pfs的最终灭菌中时存在提高的循环效率。可以通过最小化对产品的风险,并在商业上通过每单位时间允许更大的医疗产品(例如,pfs)总吞吐量来获得潜在价值。
vhp灭菌的若干方面可能会(积极地或负面地)影响用于医疗产品的灭菌过程的安全性、效果、效率和其他方面。例如:
●诸如vhp的汽化的灭菌化学品可以储存为含水液体混合物,可以在存在水的情况下汽化,和/或可以另外存在于具有水蒸汽的环境中。在一些灭菌条件下,汽化的灭菌化学品可能不像干气体和/或理想气体那样表现。例如,vhp在灭菌室中可能不会完全从水蒸汽解离;vhp反而可能会像vhp和水蒸汽的二元混合物那样表现。
●在一些或整个灭菌循环期间,灭菌室中的化学灭菌剂蒸汽和水蒸汽可以吸附到和/或凝结在具有比灭菌室中的环境温度更低的温度的表面上。例如,在pfs负载的蒸汽灭菌期间,由每个pfs中的含水的高热容液体产品产生的“冷点”可以用于引起蒸汽吸附并促进表面凝结。一旦接近于表面,化学灭菌剂蒸汽和水蒸汽就可以吸附到所述表面,这归因于蒸汽自身的化学性质、在灭菌期间所述腔室内部的操作条件以及pfs负载的表面上相较于腔室环境的其余部分更低的温度。
●在一些或整个灭菌循环期间,与水蒸汽相比较,由于过氧化氢具有比水更大的密度和更低的挥发性的事实,vhp可以优先吸附到表面上。在一些情况下,vhp和水蒸汽可以同时吸附和凝结在表面上,其中与水蒸汽相比较,vhp吸附和凝结的量和百分率更大,并且比水蒸汽更接近于灭菌负载的表面。
●在一些或整个灭菌循环期间,多个吸附层可以形成在pfs负载的表面上。在一些情况下,更为远离所述表面的每个吸附和/或凝结层可能包含更少的vhp和更多的水蒸汽,使得表面上形成vhp对水的梯度。由于vhp和水蒸汽接近于或处于饱和(蒸汽/液体平衡)的二元混合物的热力学行为,vhp可以优先吸附到负载的表面并且凝结在更接近于所述表面之处。蒸汽/液体平衡可以类似于灭菌应用中的vhp和水蒸汽的二元混合物的气体/吸附物平衡。
●在vhp灭菌循环期间或之后,凝结/吸附的过氧化氢可能很难从所述过氧化氢已对其灭菌的表面去除,这部分归因于水蒸汽在凝结的过氧化氢上的凝结、以及水在所述凝结的过氧化氢周围的吸附,这可能会将过氧化氢捕获在已灭菌的表面上的合适位置处。
本文公开的系统和方法可以有利地用于对医疗产品进行成功的灭菌,同时降低灭菌过程对经受灭菌的产品的影响和/或风险。例如,本文公开的系统和方法可以提供来使用vhp对医疗产品进行全面(例如,100%)灭菌,之后从已灭菌的产品完全(例如,100%)去除vhp。本文公开的系统和方法可以例如提高灭菌的效率、安全性和效果,和/或减少灭菌循环时间。另外,虽然可能相对于vhp在pfs的最终灭菌中的使用描述了本公开的各方面,但是对其他医疗产品的灭菌同样是本公开预期的。
本公开还预期“湿化学灭菌”的执行,可以在存在水蒸汽的情况下通过所述湿化学灭菌来实现化学灭菌。“湿化学灭菌”与“化学灭菌”的比较在一些情况下可以类似于“湿热灭菌”与“热灭菌”的比较。在一些情况下,湿化学灭菌可以是比当前存在的化学灭菌技术更有效和高效的实现灭菌的手段,正如“湿热灭菌”在一些情况下被认为比仅仅“热灭菌”更有效和高效一样。
“湿化学灭菌”可以在相对高化学品浓度、高水蒸汽浓度和高压(例如,高于400毫巴)的环境条件协同作用来迫使化学品和水蒸汽像二元混合物一样表现时发生。为了实现期望的相对高的化学品浓度、高水蒸汽浓度和高压,灭菌室(例如,灭菌室102)可以用水蒸汽和灭菌化学品(例如,vhp)的组合饱和,从而使蒸汽凝结在“负载”或有待灭菌的一个或多个物品(例如,产品105)的表面上。大多数可商购获得的过氧化氢可作为处于不同浓度(例如,3%、15%、35%、59%)的含水液体混合物获得和出售,并且因此汽化的过氧化氢通常同时会包括汽化的水。当使用vhp时,由于vhp具有高于水蒸汽的密度,因此vhp可以优先于水蒸汽凝结在有待灭菌的一个或多个物品的表面上。
在本文中应认识到,灭菌负载的具有比周围灭菌环境(例如,灭菌室102的环境温度)更低的温度的一部分可以充当吸引蒸汽凝结在负载的表面区域上的“冷点”。如果负载内的特定“冷点”位于需要蒸汽行进穿过半透膜的包装内部,则这些“冷点”可以有利地吸引汽化的vhp凝结到包围“冷点”的表面区域,从而产生负载的较高密度的凝结的vhp区域,并且促进灭菌化学品扩散穿过其所接触的半透膜。另一方面,应认识到,如果“冷点”过冷,也就是说,在负载或负载的部分与周围灭菌环境(例如,灭菌室102的环境)之间存在过大的温差(δ),则“冷点”的存在可以防止vhp分布和渗透到整个负载上。因此,应认识到,在灭菌环境(例如,灭菌室102)的温度与有待灭菌的物品(例如,产品105)上的“冷点”的温度之间需要平衡的温差,使得vhp被抽吸来凝结在“冷点”处,而不会不利于在负载上的短时间扩散。
现参考附图,图1以图解形式示出了示例性灭菌系统100。灭菌系统100包括灭菌室102,所述灭菌室102由温度控制护套104包围。灭菌室102具有内部空腔,所述内部空腔包括上部内部101和下部内部103。灭菌室102被配置成容纳一个或多个产品105以进行灭菌。流体地连接到灭菌室102的入口导管134被配置成允许各种流体经由灭菌室102中的分配歧管107进入灭菌室102。第二入口导管135也流体地连接到灭菌室102,也允许流体经由入口109进入灭菌室102。鼓风机106经由鼓风机出口导管108流体地连接到灭菌室102。鼓风机循环导管118流体地连接鼓风机106以使流体从鼓风机出口导管108朝向排放管116移动,或经由入口导管134往回朝向灭菌室102移动。排放阀120位于鼓风机循环导管118与排放管116之间,并且选择性地关闭或打开在鼓风机循环导管118与排放管116之间的连接。再循环阀119位于鼓风机循环导管与入口导管134之间,并且选择性地关闭或打开在鼓风机循环导管118与入口导管134之间的连接。真空泵110也经由真空导管112和催化剂转化器115流体地连接到灭菌室102。真空阀113位于真空导管112上,并且选择性地允许、部分地允许或阻止流从灭菌室102流过催化剂转化器115和真空泵110。真空排放导管114将真空泵110流体地连接到排放管116。
若干流体供应也经由入口导管134或入口导管135流体地连接到灭菌室102。空气供应117被配置成经由入口导管134将空气供应到灭菌室102。空气阀124耦合到在空气供应117与入口导管134之间的流体连接,并且选择性地允许、部分地允许或阻止空气从空气供应117经由入口导管134流动到灭菌室102。另外,流体地连接到入口导管134的vhp注射器132被配置成经由入口导管134将vhp注射到灭菌室102。vhp注射器阀128耦合到在vhp注射器132与入口导管134之间的流体连接,并且选择性地允许、部分地允许或阻止vhp从vhp注射器132经由入口导管134流动到灭菌室102。另外,流体地连接到入口导管135的干空气供应130被配置成经由入口导管135将干空气供应到灭菌室102。干空气供应阀126耦合到在干空气供应130与入口导管135之间的流体连接,并且被配置成选择性地允许、部分地允许或阻止干空气从干空气供应130经由入口导管134流动到灭菌室102。控制器140连接到灭菌系统100的一个或多个其他部件,诸如灭菌室102、温度控制护套104、鼓风机106、vhp注射器132、空气供应117、干空气供应130和/或灭菌系统100的任何其他部件。
灭菌系统100可以被配置成在灭菌室102内在各种温度和压力下,并在各种持续时间和/或时间间隔内运行灭菌循环。在一些实施方案中,可以选择性地并单独地修改和定制灭菌系统100可以运行灭菌循环所在的温度、压力和时间间隔。灭菌系统100可以被配置成控制灭菌室102的内部中的环境,所述环境包括温度、压力、湿度、气氛、经由例如入口导管134实现的流体的引入量、经由温度或压力控制装置中的一个或多个,和/或经由例如鼓风机出口导管108和/或真空导管112实现的流体的流出量。另外,灭菌系统100可以包括任何合适数量和位置的传感器,所述传感器被配置成感测例如在整个灭菌系统100中,包括在灭菌室102、温度控制护套104、鼓风机106、真空泵110和/或导管108、112、114、118和134中任一者中的温度、压力、流量、化学浓度或其他参数。这类传感器可以被配置成将感测到的数据传输到例如控制器140和/或人机界面。
灭菌室102可以是限定包括上部内部101和下部内部103的内部的可密封腔室。灭菌室102可以通向开放构型,使得例如产品105的一个或多个物品可以作为负载的一部分放置在内部以进行灭菌,并且可以在灭菌之后移除。在一些实施方案中,灭菌室102可以例如具有操作方位,使得上部内部101位于下部内部103上方,并且使得物质可以从上部内部101附近朝向下部内部103降落(例如,在重力的作用下)。灭菌室102可以具有一个或多个输送设备,入口导管134和入口导管135中的一者或多者可以连接到所述一个或多个输送设备。如图1所示,例如,分配歧管107是一个这样的输送设备。分配歧管107可以被配置成以给定配置,诸如跨越灭菌室102的上部内部101的流或均匀的喷雾将气体、蒸汽或液体分散到灭菌室102中。入口109是另一个这样的输送设备。入口109也可以被配置成以给定配置,诸如跨越上部内部101的流或均匀的喷雾将气体、蒸汽或液体分散到灭菌室102中。在一些实施方案中,分配歧管107可以被配置成以一种配置,诸如均匀的喷雾将气体、蒸汽、或液体分散到灭菌室102中,并且入口109可以被配置成以不同的配置,诸如以流配置将气体或蒸汽分散到灭菌室102中。在一些实施方案中,可能不存在入口109,并且入口导管134和135两者都可以连接到分配歧管107。
温度控制护套104可以是包围灭菌室102的被配置或有效用于提供对灭菌室102内部的环境的温度控制的任何材料。在一些实施方案中,例如,温度控制护套104可以是包围灭菌室102的水护套。在这类实施方案中,通过温度控制护套104的水或其他液体的温度和/或流量可以由例如控制器140控制。
产品105可以是适合于使用灭菌系统100灭菌的任一个或多个物品。在一些实施方案中,产品105可以是处于初级包装、次级包装或两者的医疗产品。在一些实施方案中,产品105可能是具有另外对深真空环境,诸如对压力小于约100毫巴的环境敏感的一个或多个活动部分的医疗产品。产品105因此可以是例如填充有一定体积的配制的药物物质的容器,例如像小瓶或pfs。在另外的实施方案中,产品105可以是或包括对例如高于30℃的高温敏感的医疗产品。这种医疗产品可以包括例如配制的药物物质或可能对高温敏感的其他组成,诸如蛋白质(例如,抗体或酶)、核酸、血液、血液组分、疫苗、过敏原制剂、基因治疗药剂、组织、其他生物物质等。例如,产品105可以是包含包括抗体的配制的药物物质的包装好的pfs。
鼓风机106可以是例如具有以下能力的鼓风机:强制地从灭菌室102的下部内部103抽吸蒸汽和气体使其穿过鼓风机出口导管108,并且经由入口导管134将所述蒸汽和气体往回再引入到灭菌室102的上部内部101(或可选地,将这种蒸汽和气体穿过排放阀120和催化剂转化器121抽吸到排放管116)。鼓风机106可以是被配置或有效用于执行这种功能的任何装置或机构。例如,鼓风机106可以具有叶轮和旋转叶片,或旋转轮叶,它们被配置成将来自下部内部103的蒸汽和气体从鼓风机出口导管108抽吸出来,使其穿过鼓风机循环导管118并且经由入口导管134将所述蒸汽和气体往回抽吸到灭菌室102的上部内部101。在一些实施方案中,如图1所示,鼓风机106可以处于灭菌室102的外部。在其他实施方案中,鼓风机106可以设置在灭菌室102内。在一些实施方案中,鼓风机106可以被配置成以足以产生从灭菌室102的上部内部101到下部内部103的蒸汽和气体流的力从灭菌室102的下部内部103抽吸蒸汽和气体,并且将所述蒸汽和气体往回再引入到上部内部101。这个流可以被称为“湍流”。在一些实施方案中,鼓风机106可以凭借来操作的力可能是可调整的(经由例如控制器140),使得在灭菌室102内可以产生较多湍流(例如,更强烈)或较少湍流的蒸汽和气体流。在一些实施方案中,鼓风机106可以被配置成产生比例如真空泵110更强大的力来抽吸蒸汽和气体。
真空泵110可以是具有以下能力的真空泵:从灭菌室102的内部(例如,下部内部103)抽吸气体,使其经过真空导管112和催化剂转化器115并朝向排放管116抽吸所述气体,从而在灭菌室102和/或包含灭菌室102和例如鼓风机106的封闭系统内产生真空。在一些实施方案中,真空泵110可以具有泵轮、旋转叶片或轮叶,它们被配置成朝向排放管116抽吸蒸汽和气体。真空泵110可以经由例如真空排放导管114流体地连接到排放管116。在一些实施方案中,可以将来自真空泵110和鼓风机106的排放物分离,而不是组合成一体。
在一些实施方案中,真空类型功能也可以或可选地由例如鼓风机106执行,所述鼓风机106可以选择性地使蒸汽和气体循环出入灭菌室102,或者使所述蒸汽和气体离开灭菌室102,穿过排放阀120并流向排放管116。排放阀120可以选择性地打开或关闭,以便准许或阻止气体或蒸汽从鼓风机循环导管118朝向排放管116流动,或朝向入口导管134流动以再引入到灭菌室102中。排放阀120可以手动地控制,或者可以由例如控制器140控制。
灭菌系统100可以包括流体可以经由入口导管134或入口导管135由其引入到灭菌室102中的若干空气和/或蒸汽供应。例如,空气供应117可以是任何空气供应(例如,室内空气、或压缩的干空气)或在外部来自灭菌系统100的其余部分的其他流体。在一些实施方案中,空气供应117可以是包围灭菌系统100的“室内空气”供应,所述室内空气可能已通过室内过滤系统。在一些实施方案中,空气供应117可以包括比“室内空气”更多的水蒸汽。在一些实施方案中,空气供应117可以是经过过滤的室外空气供应。耦合到在空气供应117与入口导管134之间的流体连接的空气阀124可以被配置成选择性地允许、部分地允许或阻止空气从空气供应117经由入口导管134流动到灭菌室102,从而控制到灭菌系统100的封闭部分中的空气引入量。空气阀124可以是手动可控制的和/或可由例如控制器140控制。
干空气供应130可以是具有相对低湿度的空气供应,使得其可以用于对例如灭菌室102和/或导管108、112、114、118和134中的一者或多者的内部进行干燥。在一些实施方案中,例如,干空气供应130中的空气可以包括例如-10℃或更低、-40℃或更低、或在-10℃与-40℃之间的任何温度的露点。在一些实施方案中,干空气供应130可以是清洁的干空气供应,诸如已被灭菌或另外被过滤到至少0.2微米的空气。在一些实施方案中,干空气供应130可以是密封的空气供应。在一些实施方案中,干空气供应130可以是压缩空气供应。耦合到在干空气供应130与入口导管135之间的流体连接的干空气供应阀126可以被配置成选择性地允许、部分地允许或阻止干空气从干空气供应130经由入口导管135流动到灭菌室102。干空气供应阀126可以是手动可控制的和/或可以由例如控制器140控制。在一些实施方案中,代替入口导管135,干空气供应130可以连接到入口导管134。在另外的实施方案中,空气供应117可以供应干空气供应130包括的任何类型空气。
vhp注射器132可以包括vhp、或vhp和汽化的水的供应,并且可以被配置成经由例如入口导管134将vhp或vhp和汽化的水的组合注射到灭菌室102中。vhp注射器132可以被配置成以可调整的浓度将蒸汽注射到灭菌室102中。vhp注射器阀128可以耦合到在vhp注射器132与入口导管134之间的流体连接,并且可以被配置成选择性地允许或阻止vhp从vhp注射器132经由入口导管134流动到灭菌室102。vhp注射器阀128可以是手动可控制的和/或可以由例如控制器140控制。干空气供应阀126和vhp注射器阀128还可以协同使用来允许干空气和汽化的vhp/水的期望的组合经由入口导管134进入灭菌室102。
催化剂转化器115和催化剂转化器121可以是例如本领域中已知适合于将例如在灭菌循环期间在灭菌系统100内循环的有毒的气态或汽化的流体转化为低毒性的气体或蒸汽的任何催化剂转化器。例如,催化剂转化器115、121可以被配置成将通过vhp注射器132注射到灭菌系统100中的vhp转化成水蒸汽、氧气、或其他无毒流体。
灭菌系统100的一些或所有方面可以由例如控制器140控制。控制器140可以是例如模拟或数字控制器,所述模拟或数字控制器被配置成改变灭菌室102的各方面环境,诸如灭菌室102的内部温度或压力,和/或鼓风机106、真空泵110、空气供应117、干空气供应130、vhp注射器132、排放管116中的一者或多者,阀113、119、120、124、126和128中的一者或多者,催化剂转化器115、121中的一者或多者,导管108、112、114、116、118和134中的一者或多者以及灭菌系统100的任何和/或其他方面。在一些实施方案中,灭菌系统100可以由多个控制器140控制。在其他实施方案中,灭菌系统可以仅具有一个控制器140。在一些实施方案中,控制器140可以是数字控制器,诸如可编程逻辑控制器。
在一些实施方案中,控制器140可以被预先编程以使用灭菌系统100执行一个或多个灭菌循环。在一些实施方案中,灭菌系统100可以由具有一个或多个人机界面(“hmi”)元件的控制器控制,所述一个或多个hmi元件可以被配置成允许用户输入或改变灭菌循环的期望的参数,所述灭菌循环可以由灭菌系统100上或可操作地耦合到所述灭菌系统的控制器执行。因此,在一些实施方案中,hmi元件可以用于编程定制的灭菌循环以供灭菌系统100执行。例如,在一些实施方案中,灭菌系统100可以由连接到例如计算机、平板计算机或具有显示器的手持装置的控制器控制。这种显示器可以包括例如用于针对灭菌循环的一个或多个步骤选择或改变期望的温度、压力、时间、vhp引入量等的选项。
图2和图3a至图3c示出了根据本公开的灭菌方法中的阶段和步骤的流程图。如本领域的普通技术人员将认识,可以在与本公开保持一致的同时省略、组合和/或不按顺序执行图2和图3a至图3c中的一些阶段和/或步骤。在一些实施方案中,可以使用例如灭菌系统100或灭菌系统100的变型来执行图2和图3a至图3c中的阶段和步骤。将认识到,为了执行图2和图3a至图3c所示的阶段和步骤,可以使用灭菌系统100的可定制且可控制的方面。例如,在一些实施方案中,可以采用控制器140来指导、调整、或修改可由灭菌系统100执行的一系列灭菌步骤、设定点和阶段。另外,尽管相对于灭菌系统100叙述了图2和图3a至图3c中描述的阶段和步骤,但是本领域的普通技术人员将理解,这些阶段和步骤可以由另一个灭菌系统、或有能力执行所述步骤的另一个系统执行。
图2示出了在诸如灭菌系统100的灭菌系统中的根据本公开的灭菌方法200中的一系列步骤的流程图。根据步骤202,可以对灭菌系统100执行泄漏测试。根据步骤204,可以预调节灭菌系统100。根据步骤206,可以执行灭菌阶段。根据步骤208,可以执行第一通风阶段。根据步骤208,可以执行第二通风阶段。
在执行方法200的步骤之前,可以将诸如产品105的灭菌负载放置在诸如灭菌系统100的灭菌系统的诸如灭菌室102的灭菌室内。然后可以密封封闭系统灭菌环境,所述封闭系统灭菌环境包括灭菌室102、鼓风机出口导管108、鼓风机106、鼓风机循环导管118、入口导管134和连接这些部件的任何元件。
根据步骤202,可以对封闭系统灭菌环境执行泄漏测试。泄漏测试可以包括例如在整个封闭系统中产生真空。可以通过例如使用真空泵110将气体和蒸汽从封闭系统排出来产生真空。在泄漏测试期间,鼓风机106可以处于操作中,以便使任何剩余空气循环穿过封闭系统并且产生均质环境。为了验证在封闭系统内可以保持合适的真空,在某种程度上可以此方式执行泄漏测试。另外,在泄漏测试中在整个封闭系统中包括空气并使空气循环穿过整个封闭系统可以有助于增大在封闭系统内的环境与有待灭菌的负载之间的热传递系数,这可以有助于在灭菌之前平衡在封闭系统内的环境与有待灭菌的负载之间的温度。
根据步骤204,可以预调节灭菌系统(例如,灭菌系统100)。预调节可以包括例如将封闭系统的温度增加到在灭菌阶段期间意图维持的温度(例如,在约25℃与约50℃之间)。在一些实施方案中,可以在比标准化学灭菌程序中执行的时间更长的时间内执行预调节,这可以允许有更多时间来减小在封闭系统中的环境(包括例如灭菌室102的环境)与有待灭菌的负载之间的任何温差。在一些实施方案中,预调节可以执行约15分钟到约两小时,诸如约20分钟到约1.5小时、约25分钟到约1小时、约30分钟到约1小时、约30分钟到约45分钟、约45分钟到约1小时,诸如约30分钟、约40分钟、约45分钟或约1小时。根据步骤204的预调节还可以包括在处于或接近大气压,例如在约400毫巴与约700毫巴之间、在约500毫巴与约700毫巴之间、在约500毫巴与约600毫巴之间、在约800毫巴与约1000毫巴之间或在约900毫巴与约1100毫巴之间的压力下操作。预调节步骤在或接近大气压下的操作可以促进从腔室环境到负载的对流热传递,从而有助于最小化在腔室环境与负载之间的温差。另外,鼓风机106可以在根据步骤204的预调节期间操作,这可以促成更高的热传递系数,以及因此在包括灭菌室102的环境的封闭系统与有待灭菌的负载之间的潜在更快的温度平衡。在封闭系统与有待灭菌的负载之间的温度平衡可以允许“冷点”、或负载之上或之中具有比大部分负载和/或周围环境更冷的温度的位置的升温。例如,pfs的液体内容物可以比其非液体包装更缓慢地吸收热量,从而充当包含pfs的负载内的“冷点”。通过平衡在封闭系统和有待灭菌的负载中的温度减少这类冷点可以有利地允许汽化的灭菌化学品(例如,vhp)均匀地扩散在整个灭菌室102中、越过有待灭菌的负载、和/或扩散穿过有待灭菌的负载中的渗透膜和屏障。然而,在封闭系统与“冷点”之间维持一定温差可能是期望的,以促进vhp和水蒸气到有待灭菌的负载上的优先表面吸附和凝结。
如本文其他位置所论述,还可以预期的是,在一些实施方案中,经由在有待灭菌的负载与周围封闭系统之间保持温差来维持“冷点”还可以具有优点;例如,汽化的灭菌化学品(例如,vhp)在有待灭菌的负载的“冷点”上的受控凝结可以将灭菌化学品集中在所述负载上并且使化学品更有效扩散到负载中,从而减少灭菌室102中实现有效灭菌所需的灭菌化学品的总量。在这类实施方案中,根据步骤204的预调节可以执行更短的时间量和/或在由例如真空泵110产生的浅真空中执行,以便在有待灭菌的负载内允许或维持“冷点”。
根据步骤206,可以执行灭菌阶段。灭菌阶段可以包括例如开始流体通过灭菌系统的循环、实现真空度、将汽化的化学品注射到灭菌室中、维持注射后保持、将气体注射到灭菌室中以转变为更浅的真空以及维持转变后保持。可以多次重复根据步骤206的灭菌阶段。图3a中更详细地示出了根据步骤206的灭菌阶段。
根据步骤208,可以执行第一通风阶段。第一通风阶段可以包括例如实现真空度、保持真空度、破坏真空度以及对所述系统通风和排气。可以多次执行第一通风阶段。图3b中更详细地示出了根据步骤208的第一通风阶段。
根据步骤210,可以执行第二通风阶段。第二通风阶段可以包括例如实现真空度、保持真空度和破坏真空度。可以多次执行第二通风阶段。图3c中更详细地示出了根据步骤210的第二通风阶段。
可以多次执行步骤208和210两者。另外,虽然在一些实施方案中,可以在步骤210之前执行步骤208,但是在替代实施方案中,可以在步骤208之前执行步骤210。
图3a是可以作为灭菌方法200的步骤206执行的灭菌阶段300的流程图。在灭菌阶段300之前,可以将灭菌负载(例如,产品105)引入到灭菌室102中。根据步骤302,可以实现真空度。根据步骤304,可以将汽化的化学品注射到灭菌室中。根据步骤306,可以维持注射后保持。根据步骤308,可以将气体注射到灭菌室中以转变为更浅的真空。根据步骤310,可以维持注射后保持。
作为灭菌阶段300的一部分,可以在灭菌系统100中启动并维持湍流。
根据步骤302,可以在灭菌系统100的灭菌室102内实现真空度。真空度可以是例如在约400毫巴与约700毫巴之间,诸如在约450毫巴与约650毫巴之间或在约450毫巴与约550毫巴之间。例如,真空可以为约450毫巴、约500毫巴、约550毫巴或约600毫巴。这种真空可以促进灭菌化学品在灭菌负载上的高度集中,延长封闭系统保持处于较深真空所在的时间量增加了灭菌负载在灭菌化学品中的暴露。
根据步骤304,可以将汽化的化学品注射到灭菌室中。在一些实施方案中,汽化的化学品可以包括vhp。在一些实施方案中,汽化的灭菌化学品可以是具有例如在约5重量%与约75重量%之间的过氧化氢的浓度的汽化的过氧化氢水溶液。在一些实施方案中,汽化的化学品可以是具有以下浓度的汽化的过氧化氢水溶液:例如在约10重量%与约65重量%之间的过氧化氢、在约15重量%与约60重量%之间的过氧化氢、在约30重量%与约60重量%之间的过氧化氢、在约30重量%与约60重量%之间的过氧化氢、或在约45重量%与约60重量%之间的过氧化氢。在一些实施方案中,汽化的化学品可以是具有约35重量%的过氧化氢(和65重量%的水)的汽化的含水过氧化氢。在另外的实施方案中,汽化的化学品可以是具有约59重量%的过氧化氢(和41重量%的水)的汽化的含水过氧化氢。
在一些实施方案中,注射的vhp供应可以是例如约50g到约700g的含水vhp。例如,注射的vhp供应可以是约50g到约600g、约100g到约600g、约300g到约550g、或约450g到约550g。例如,注射的vhp供应可以为约100g、约200g、约300g、约400g、约450g、约475g、约500g、约525g、约550g、约600g或约650g。在一些实施方案中,注射的vhp供应可以基于在灭菌室102内部灭菌的负载的体积或量而定量。例如,如果诸如预填充注射器的许多药物产品将要在灭菌室102中灭菌,则注射的vhp供应可以是灭菌室102内部的每单位药物产品约0.01到约0.15克vhp,诸如约0.01到约0.10克vhp,诸如每单位药物产品为约0.015克、0.02克、0.025克、0.03克、0.04克、0.05克、0.06克、0.07克、0.08克、0.09克、0.1克或0.11克。在其他实施方案中,注射的vhp供应可以基于灭菌环境的体积,诸如灭菌室102的内部而定量。例如,注射的vhp供应可以是灭菌室中的每立方英尺体积约0.2到3.0克。例如,注射的vhp供应可以是每立方英尺约0.2到约2.0克,诸如每立方英尺约0.25克、约0.50克、约0.75克、约1.0克、约1.2克、约1.4克、约1.5克、约1.6克、约1.8克、或约2.0克。
在一些实施方案中,步骤210还可以包括将干空气从例如干空气供应130注射到灭菌系统中,以便在腔室内部在不同压力下在汽化的化学品与水蒸汽的浓度之间产生期望的平衡。
根据步骤306,可以维持注射后保持。在注射后保持期间,将湍流维持通过包括灭菌室102和鼓风机106的封闭系统。不对其中维持湍流的封闭系统添加或去除流体。可以对维持注射后保持的时间(或“注射后保持时间”)进行选择,以便允许汽化的灭菌化学品有足够的时间接触有待灭菌的负载。在一些实施方案中,注射后保持时间可以为约2分钟到约20分钟。在一些实施方案中,注射后保持时间可以为至少约5分钟、至少约10分钟、或至少约15分钟。在一些实施方案中,注射后保持时间可以为约5分钟到约20分钟、约8分钟到约20分钟、约10分钟到约20分钟、或约10分钟到约15分钟。以此方式,可以避免对将过量vhp添加到系统中以确保其与灭菌负载接触的需求。
根据步骤308,可以将气体注射到灭菌室中以在灭菌室中转变为更浅的真空(即,更高压力)。气体可以是能够破坏或减少灭菌室102中的真空的任何合适的气体。在一些实施方案中,气体可以是干气体,诸如包含氮气的气体(例如,可商购获得的仅为氮气或主要为氮气的供应),或具有例如-10℃或更低的露点的空气。在一些实施方案中,可以从干空气供应130注射气体。可以按体积注射气体,以实现在约500毫巴与约1100毫巴之间,诸如在约550毫巴与约1000毫巴之间、在约600毫巴与约1000毫巴之间、在约700毫巴和约700毫巴与约900毫巴之间或在约750毫巴与约850毫巴之间的压力。例如,第二注射后压力可以为约700毫巴、约750毫巴、约800毫巴、约850毫巴、或约900毫巴。
根据步骤310,可以维持转变后保持。在转变后保持期间,在步骤308期间实现的压力可以维持例如至少约5分钟、至少约10分钟、或至少约15分钟。在一些实施方案中,第二注射后压力可以维持约5分钟到约20分钟、约8分钟到约20分钟、约10分钟到约20分钟、或约10分钟到约15分钟。
可以将灭菌阶段300的步骤重复例如1到10次,诸如2、3、4、5、6、7、8、9或10次。这可以有助于确保对灭菌室102内的灭菌负载的完全灭菌。在一些实施方案中,可以重复灭菌阶段300的次数可以与在每次重复中维持注射后保持的时间成反比。例如,如果维持注射后保持的时间较短(例如,10分钟),则可以将步骤210至216重复更多次。在一些实施方案中,将注射后保持维持更长的时间段(例如,15-20分钟),以增加灭菌负载在灭菌阶段300的每次重复中暴露于灭菌化学品的时间。在另外的实施方案中,可以重复灭菌阶段300的次数可以取决于灭菌过程的期望的vhp总量。在一些实施方案中,例如,至少200g的vhp总量的注射可能是期望的。例如,在一些实施方案中,至少250g的总量注射可能是期望的。在一些实施方案中,在约200g与约700g之间的vhp总量的注射可能是期望的。
图3b是可以在执行根据步骤206的灭菌阶段的一次或多次重复之后作为灭菌方法200的步骤208执行的第一通风阶段320的流程图。根据步骤322,可以实现真空度。根据步骤324,可以保持真空度。根据步骤326,可以破坏真空度。根据步骤328,可以对灭菌系统(例如,灭菌系统100)通风和排气。
根据步骤322,可以在灭菌室102中实现真空度,同时还在灭菌室102的上部内部101附近,诸如经由分配歧管107或入口109将干气体注射到灭菌室102中。干气体可以包括例如氧气和/或氮气。干气体可以具有例如-10℃或更低的露点。可以从例如干空气供应130注射干气体。在将干气体注射到灭菌室102中的同时,可以通过例如真空泵110经由真空导管112、催化剂转化器115和真空排放导管114抽真空。可以比干气体的注射速率更大的速率抽真空,使得能够逐渐地实现真空度。真空度可以是例如在约500毫巴与约850毫巴之间,诸如在约500毫巴与约800毫巴之间、在约550毫巴与约750毫巴之间或在约600毫巴与约700毫巴之间。例如,真空度可以为500毫巴、550毫巴、600毫巴、650毫巴、或700毫巴。在实现期望的真空度的同时将干气体注射在灭菌室102的上部内部101附近减少了vhp和水蒸汽在腔室的上部内部101处的集中,并且促进了灭菌室中的较密集的分子朝向灭菌室102的下部内部(例如,下部内部103),以及在某种程度上通过真空排放导管114离开灭菌系统100的移动。
根据步骤324,可以停止干气体的注射,并且可以将真空度保持例如约1分钟到约20分钟,诸如约2分钟到约20分钟、约5分钟到约20分钟、约5分钟到约15分钟、或约5分钟到约10分钟。例如,可以将真空度维持约2、5、8、10或15分钟。保持真空度可以继续促进较密集的分子(例如,灭菌化学分子)向下朝向灭菌室102的下部内部103,以及远离灭菌负载的沉降。
根据步骤326,可以通过经由例如分配歧管107或入口109将更多干气体添加在灭菌室102的上部内部101附近来破坏真空度。可以添加足以实现更高压力的体积的干气体。更高压力可以是例如比在步骤322中实现的真空度高50到200毫巴。真空度可以是例如在约550毫巴与约1000毫巴之间,诸如在约550毫巴与约850毫巴之间、在约600毫巴与约700毫巴之间或在约650毫巴与约750毫巴之间。例如,真空度可以为约550毫巴、600毫巴、650毫巴、700毫巴、750毫巴、或800毫巴。添加更多干气体可以继续迫使灭菌化学品沉降到灭菌室102的下部内部101,从而使所述灭菌化学品移动离开灭菌负载并将其定位成经由真空导管112或鼓风机出口导管108去除。
根据步骤328,可以对灭菌系统(例如,灭菌系统100)通风和排气。在这个步骤期间,可以在关闭再循环阀119并打开排放阀120的同时打开鼓风机106,使得鼓风机106从灭菌室102内部抽吸流体并且经由催化剂转化器121通过排放管116将所述流体排出。由于鼓风机出口导管108在灭菌室102的下部内部103处连接到灭菌室102,可以通过这个步骤来去除已沉降到下部内部103的较稠密的流体(诸如灭菌化学品)。可以同时允许将空气(例如,来自空气供应117)排入灭菌室102,使得灭菌室102中的压力返回到大气压或在其附近。
可以将第一通风阶段320重复例如1到35次,诸如2、5、10、15、17、19、22、25、27、29、30、32或35次。第一通风阶段320的重复可以确保能将大部分灭菌化学品(例如,vhp)从灭菌系统100去除。
图3c是可以作为灭菌方法200的步骤210执行的第二通风阶段340的流程图。根据步骤342,可以实现真空度。根据步骤344,可以保持真空度。根据步骤346,可以破坏真空度。
根据步骤342,可以在灭菌室102中实现真空度。与第一通风阶段类似,在这个阶段中实现的真空度可以是例如在约500毫巴与约850毫巴之间,诸如在约500毫巴与约800毫巴之间、在约550毫巴与约750毫巴之间或在约600毫巴与约700毫巴之间。例如,真空度可以为500毫巴、550毫巴、600毫巴、650毫巴、或700毫巴。实现真空度可以促进灭菌室102以及因此灭菌负载中水分的去除。因此,可以对灭菌负载进行干燥。
根据步骤344,可以将真空度保持例如约1分钟到约20分钟,诸如约2分钟到约20分钟、约5分钟到约20分钟、约5分钟到约15分钟、或约5分钟到约10分钟。例如,可以将真空度维持约2、5、8、10或15分钟。保持真空度可以继续促进灭菌室102以及因此灭菌负载中水分的去除。因此,可以进一步对灭菌负载进行干燥。在一些实施方案中,可以省略步骤344。
根据步骤346,可以通过从例如干空气供应130添加干气体来破坏灭菌室102中的真空度或将其升高到更高压力。
可以将第二通风阶段340重复例如1到50次,诸如2、5、10、15、20、25、30、35、38、40、42、45、47、49或50次。第二通风阶段340的重复可以确保对灭菌室102和灭菌负载的干燥。
如先前已描述,可以在第一通风阶段320之前或之后执行第二通风阶段340。第一通风阶段320可以确保例如灭菌室102中的灭菌化学品(例如,vhp)的浓度是相对低的,并且第二通风阶段340可以确保灭菌负载是干燥的,并且还可以在第一通风阶段320之后去除灭菌室102中剩余的残留灭菌化学品。在第二通风阶段340在第一通风阶段320之后执行的情况下,第一通风阶段可以确保灭菌室102中的灭菌化学品(例如,vhp)的浓度是相对低的,使得当在第二通风阶段340中干燥灭菌室102和灭菌负载时,剩余的对从灭菌系统100去除残留灭菌化学品的需求很小。
图4a至图4c以图解形式示出了灭菌系统100,并且具体示出了灭菌系统100的哪些部件在阶段300、320和340期间可以激活、打开、或接通(与停用、关闭或断开相反)。为了清楚起见,没有示出控制器140和热护套104。
图4a以图解形式示出了在灭菌阶段300期间处于激活或停用的不同阶段的灭菌系统100的各种部件。如所示,在灭菌阶段300期间,鼓风机出口导管108、鼓风机循环导管118、鼓风机106和再循环阀119在整个灭菌阶段300期间保持打开、接通或激活。空气供应117、空气供应阀124、排放阀120和催化剂转化器121在整个灭菌阶段300中保持关闭、断开或停用。其余部件在灭菌阶段300期间有时打开、接通或激活。下表指出了这些部件何时打开、接通或激活:
表1
图4b以图解形式示出了在第一通风阶段320期间的灭菌系统100的各种部件。如图所示,在第一通风阶段320期间,vhp注射器132、vhp注射器阀128和再循环阀119保持断开或关闭。其余部件如下表中所指示在第一通风阶段320期间有时打开、接通或激活:
表2
图4c以图解形式示出了在第二通风阶段340期间的灭菌系统100的各种部件。如所示,在第二通风阶段340期间,空气供应117、空气供应阀124、vhp注射器、vhp注射器阀128、排放阀120和催化剂转化器121保持关闭。鼓风机出口导管108、鼓风机108、鼓风机循环导管118、再循环阀119、入口134和分配歧管107在通风阶段340期间保持打开。其余部件在通风阶段340期间有时打开、接通或激活。下表指出了这些部件何时打开、接通或激活:
表3
在一些实施方案中,任何或所有上述步骤和阶段可以由灭菌系统100按例如控制器140的指导来自动地执行,所述控制器140可以被编程或提前由例如用户以其他方式进行配置。本文公开的灭菌方法可以被定性为“有限的过度杀灭”灭菌方法,因为所述灭菌方法可以在最小化灭菌方法对产品的影响的同时确保对例如pfs的负载的灭菌。
以上描述是说明性的,并且不意图是限制性的。在不脱离本发明的一般范围的情况下,本领域的普通技术人员可以进行众多修改和/或改变。例如,且如已描述的,上述实施方案(和/或其方面)可以彼此组合使用。另外,在不脱离本发明的范围的情况下,可以去除上述实施方案的部分。此外,在不脱离其范围的情况下,可以进行修改以使特定情况或材料适于各种实施方案的教义。在阅览以上说明书之后,许多其他实施方案对于本领域的普通技术人员而言也将是显而易见的。
- 还没有人留言评论。精彩留言会获得点赞!