紫外线敏感性的判定方法与流程
本发明涉及判定人皮肤的紫外线敏感性的紫外线敏感性的判定方法以及紫外线敏感性降低剂的评价或选择方法。
背景技术:
皮肤因暴露在阳光下会受到各种损害。特别而言,已知:由于紫外线区域(290~400nm)的光而在皮肤内产生的活性氧种(ros)和通过与ros的反应生成的生物体氧化物,作为氧化应激对皮肤产生有害作用,与短期暴露引起的红斑和色素沉积形成以及长期暴露引起的光老化和致癌等密切相关(非专利文献1、2)。
作为保护皮肤免受紫外线伤害的技术,有以下方法:在皮肤上涂敷防晒剂、抗氧化剂等,抑制紫外线照射产生的ros和生物体氧化物的产生,从而预防氧化应激。
另一方面,生物体对于紫外线照射等外部刺激引起的氧化应激具有活性氧种的消除系统和生物体内抗氧化物质等对抗手段。但是,这些对抗手段根据年龄、遗传因素、生活习惯、饮食习惯等有个体差异,每个人对紫外线的预防护理的必要性不同。因此,为了对紫外线进行有效的预防护理,有必要正确地评价紫外线照射等对皮肤产生的氧化应激和皮肤内的抗氧化能力。
作为评价人皮肤的氧化应激的方法,虽然存在使用皮肤活检的方法,但由于是有创的,因此尚未得到广泛使用。虽然利用角质层带剥离对氧化蛋白进行评价是低创的,但是其仅停留在角质层的评价,很难说反映了皮肤内部的状态(非专利文献3)。作为无创的评价方法,虽然存在用拉曼光谱法测定皮肤中类胡萝卜素的报告,但这是单一的抗氧化物的评价,这也很难说反映了整个皮肤的应答(非专利文献4)。
此外,作为直接评价由于紫外线照射引起的氧化应激的敏感性的方法,测定在紫外线照射24小时后引起红斑形成的最少的紫外线量(med;最小红斑量),可以作为由紫外线引起的红斑的容易度的指标,但是由于需要在紫外线照射24小时后判定红斑形成,所以不能说是简便的方法。
在这种情况下,作为能够无创地评价生物体的氧化状态的技术,生物体微弱发光(生物光子:biophoton)的检测技术备受关注。生物光子是生物体随着生命活动而放射出的极其微弱的自发的发光。作为其由来,可以推测出单线态氧和激发羰基化合物类,可以认为由生物体的氧化反应引起的发光。
报道有:生物光子在植物、微生物、动物等各种生物中被观测到,在人皮肤中,尤其是照射紫外线a波(uva)后的生物光子被计测到,根据肤色的不同发光强度也不同(非专利文献5),通过涂敷抗氧化乳霜,发光减少(非专利文献6)。
但是,这些报道以uva刚照射后几分钟的积算值进行评价,没有对时刻变化的氧化应激应答的详细情况进行经时地评价,也没有关于生物光子显示怎样的行为的明确报道。
现有技术文献:
非专利文献1:photodermatol.photoimmunol.photomed.18,75-81(2002)
非专利文献2:toxicology189,21-39(2003)
非专利文献3:skinres.technol.13,84-90(2007)
非专利文献4:j.invest.dermatol.115,441-48(2000)
非专利文献5:photodermatol.photoimmunol.photomed.25,65-70(2009)
非专利文献6:skinpharmacol.physiol.24,300-4(2011)
技术实现要素:
本发明涉及以下的1)和2)。
1)一种紫外线敏感性的判定方法,其包括:向被检验者的皮肤照射紫外线,利用在照射后的规定期间内检测出的生物光子的量来判定紫外线敏感性的工序,该规定期间是其50%以上与照射后第1~3分钟的期间重叠的期间。
2)一种紫外线敏感性降低剂的评价或探索方法,其包括:将试验物质投予被检对象或使试验物质与被检对象接触的工序;和向被检对象的皮肤或皮肤细胞照射紫外线,利用在该照射后的规定期间内检测出的生物光子的量来评价试验物质的工序,该规定期间是其50%以上与照射后第1~3分钟的期间重叠的期间。
附图说明
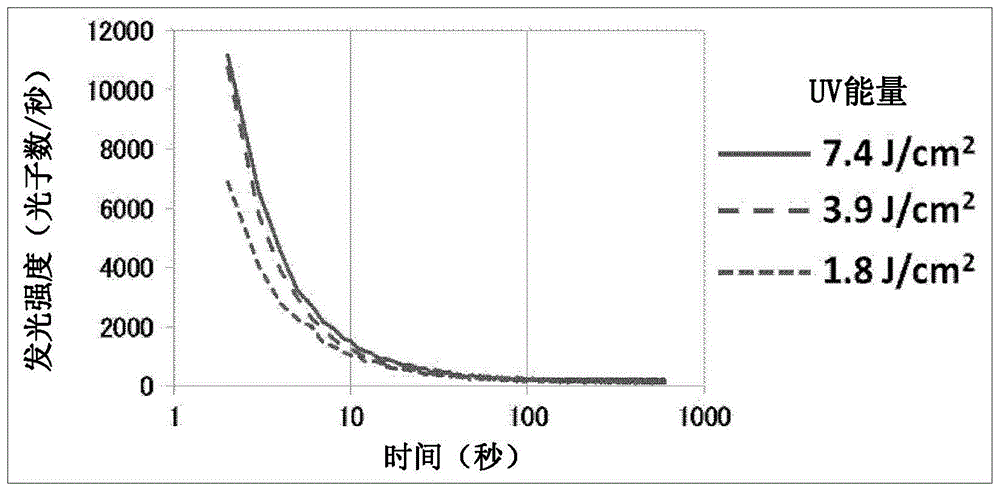
图1是表示紫外线照射后的生物光子量的推移的图。
图2是表示连续涂敷迷迭香水溶液后的应答生物光子量的图。
具体实施方式
本发明涉及提供无创性地快速判定对紫外线的敏感性的方法以及评价和探索紫外线敏感性降低剂的方法的发明。
本发明的发明人研究了可以在早期评价由紫外线引起的皮肤损害的方法,结果发现向人皮肤照射紫外线之后在规定时间内检测出的生物光子与第二天发病的红斑形成密切相关,以该生物光子的量作为指标,能够评价对紫外线的敏感性,并且能够评价和探索降低紫外线敏感性的材料。
根据本发明,能够对以下的措施有所帮助,该措施为:用于能够无创性地快速判定对紫外线的敏感性、防止由于紫外线引起的红斑形成于未然的措施、具体而言、紫外线的物理防御和防晒霜(sunscreen)等的紫外线防御用皮肤外用剂的涂敷等的措施。此外,根据本发明,能够容易且高效地评价或探索紫外线敏感性降低剂。
在本发明的紫外线敏感性的判定方法中,向被检验者的皮肤照射紫外线,在该照射后的规定期间内检测出的生物光子的量被用作指标。
此外,在本发明的紫外线敏感性降低剂的评价或探索方法中,将试验物质投予被检对象的皮肤或皮肤细胞或使试验物质与被检对象的皮肤或皮肤细胞接触,向被检对象的皮肤或皮肤细胞照射紫外线的情况下,在该照射后的规定期间内检测出的生物光子的量被用作指标。
在本发明的方法中,作为照射的紫外线,只要是在紫外区域具有波长的光线,就没有特别限制,具体而言,可以举出波长为285~320nm的uv-b波、或320~400nm的uv-a波。在本发明中,优选a波和b波的混合紫外线,光的强度的比率(a波/b波)优选为6~20、更优选为7~15、进一步优选为8~12。
照射的紫外线的强度没有特别限定,例如,优选为10mw/cm2以上,更优选为20mw/cm2以上,更优选为30mw/cm2以上,且优选为200mw/cm2以下,更优选为170mw/cm2以下,更优选为150mw/cm2以下。此外,优选为10~200mw/cm2,更优选为20~170mw/cm2,更优选为30~150mw/cm2。另外,在本发明中,紫外线的强度是指将uv-b波和uv-a波合并的波长区域(285~400nm)的紫外线的强度。
紫外线的强度可以使用市售的计测器进行计测,可以举出solarmetermodel5.0(uva+b)(solartechinc.)、多功能分光放射计msr-7000n(optoresearch公司)等。
此外,照射时间根据照射的紫外线的强度而不同,例如可以举出5~300秒,优选为5~240秒,更优选为5~200秒。
作为由紫外线的照射强度和照射时间决定的紫外线照射量(照射能量),优选为300~8000mj/cm2,更优选为500~7000mj/cm2,进一步优选为600~6000mj/cm2。
用于照射紫外线的紫外线照射装置只要具有能够发出上述波长范围的光的光源,就没有特别限制,作为光源,例如可以举出低压水银灯、高压水银灯、超高压水银灯、氙灯、金属卤化物灯、木质灯、荧光检查灯等,优选为氙灯。
对于这样的光源,根据需要,通过组合能够选择紫外线区域的波长的光的滤光器,能够调节照射波长。
作为进行紫外线照射的被检验者的皮肤部位,只要是可以进行紫外线照射和生物光子测定的部位,就没有特别限定,被生活紫外线晒到的可能性高的部位,由于每天的紫外线照射的影响,紫外线敏感性发生变动,有可能成为本发明的方法中的测定值的偏差的原因,因此,优选为不容易受到生活紫外线照射的部位。具体而言,可以举出前臂内侧部、上臂内侧部、背部、臀部、腹部等的皮肤,优选前臂内侧部、上臂内侧部、背部、臀部,更优选前臂内侧部或腹部。
此外,作为本发明的紫外线敏感性的评价或选择方法中的被检对象,除了人(被检验者)以外,还可以包括培养表皮细胞或3d皮肤模型或培养皮肤组织等,紫外线照射针对与上述同样的被检验者的皮肤部位、或者培养表皮细胞或皮肤培养组织中的该细胞或组织(皮肤)进行。作为培养表皮细胞,优选为表皮角化细胞(角质细胞:keratinocyte),作为三维培养皮肤细胞,可以使用epidermtm(mattekcorporation公司制造)、episkin(skinethic公司制造)、rhe(skinethic公司制造)、labcyteepi模型(j-tec公司制造)等市售产品。
如后述试验例1所示,向皮肤照射紫外线时产生的生物光子在紫外线刚照射后显示出最大的发光强度,之后发光经时地衰减。而且根据本发明,发现照射后主要在第1~3分钟的期间内的发光强度与紫外线照射24小时后所观察到的红斑形成相关(试验例2和3)。
因此,在本发明的紫外线敏感性的判定方法、或紫外线敏感性降低剂的评价或探索方法中,将紫外线照射后第1~3分钟的期间和其50%以上与该期间重叠的期间设为规定期间,该规定期间的生物光子量被用于判定或评价。
规定期间被设定为其50%以上与上述照射后第1~3分钟的期间重叠的期间,优选设定为70%以上、更优选设定为80%以上、更优选设定为90%以上与照射后第1~3分钟的期间重叠,更加优选其100%重叠的照射后第1~3分钟内的期间。
在此,规定期间与照射后第1~3分钟的期间重叠是指两个期间存在共同的期间,其50%以上重叠是指规定期间的50%以上与照射后第1~3分钟的期间重叠。
此外,紫外线刚照射后的初期期间的生物光子量很多,对本发明的判定或评价的影响较大,因此,本发明的规定期间优选设定为不与紫外线刚照射后的初始期间重叠。具体而言,设定为不与从照射结束后到15秒为止、优选为到30秒为止、更优选为到45秒为止的初始期间重叠。
从测定有效量的生物光子的观点出发,规定期间的长度优选为30秒~3分钟、更优选为40秒~2分钟、进一步优选为50秒~1分钟30秒、更优选为1分钟。
作为更优选的规定期间,例如可以举出照射后第1~2分钟的1分钟、照射后第2~3分钟的1分钟、照射后第1~3分钟的2分钟。
生物光子的检测利用光学检测装置进行,该光学检测装置具备具有能够检测出极微弱的生物光子的高灵敏度且低噪声的ccd等检测部。作为光学检测装置,例如可以使用微弱发光强度检测装置(cla-idfsk、东北电子产业公司制造)。所检测出的放射光的波长根据检测装置的光电子倍增管而不同,上述装置检能够检测出300~850nm的生物光子。此外,为了最大限度地抑制来自测定环境的光的影响,优选在尽可能遮光的空间实施生物光子的测定,例如在暗室中实施。
即,优选在暗室中,使用上述紫外线照射装置向测定部位照射紫外线,然后利用微弱发光强度检测装置测定从紫外线照射部位发出的生物光子。此外,紫外线照射装置中的紫外线放射部和微弱发光强度检测装置中的检测部可以分开,从不用更换装置就能进行紫外线照射和生物光子检测的观点来看,优选将紫外线放射部(具体而言,从紫外线照射装置延伸出的光照射用光纤)和检测部作为一体,通过光路的切换来更换所使用的装置的结构。
关于由紫外线照射产生的生物光子,预先测定紫外线照射前的安静时的发光强度(也称为“稳态生物光子”),接着测定紫外线照射后的规定期间内的发光强度(也称为“照射后生物光子”),将从该值减去安静时的发光强度而得到的值作为发光增量(也称为“应答生物光子”)而算出。
如上所述,紫外线照射后24小时后观察到的红斑的程度与紫外线照射后第1~3分钟的期间检测出的生物光子量呈正相关关系。因此,该生物光子量可以用作用于判定对紫外线的敏感性或者用于评价或探索紫外线敏感性降低剂的指标。在此,“对紫外线的敏感性”是指由紫外线引起的红斑等的炎症反应的强弱或持续时间所表示的炎症反应的程度,其炎症反应的程度是指该对紫外线的敏感性。此外,“紫外线敏感性的降低”是指缓和或抑制对紫外线的敏感性,抑制由紫外线引起的红斑等的炎症反应的发病。
在本发明的紫外线敏感性的判定方法中,例如,按照每个年龄或年龄段、或者每种性别,预先测定在本发明的紫外线照射后的一定期间内检测出的生物光子的量,作为基础数据而获得,根据由其算出的平均值和标准偏差,可以计算出被检验者的年龄(年龄段)、性别上的偏差值,作为判定对紫外线的敏感性的指标。
此外,关于敏感性高(容易发红)、敏感性稍高(容易稍微发红)、标准、敏感性稍低(不易稍微发红)、敏感性低(不易发红)等的对紫外线的敏感性的判定指标,制定将它们与偏差值范围相关联的适当的评价标准,并以此为基础,根据被检验者的偏差值来判定被检验者对紫外线的敏感性。
关于上述的紫外线敏感性的判定方法,与以往的med测定相比较,可以在非常短的时间进行判定,对被检验者的负担也较小。根据本发明的判定方法得到的紫外线敏感性相关的信息,对于对紫外线的物理防御措施或通过涂敷防晒霜(sunscreen)等紫外线防御用皮肤外用剂的紫外线措施,可以作为在购买紫外线防御用皮肤外用剂时产品选择和紫外线防御用皮肤外用剂推荐销售中的产品推荐的指标而发挥作用。
本发明的紫外线敏感性的判定方法相当于用于计测所谓人体的各个器官的结构或功能等而从人体收集各种资料的方法,被用于上述目的。即,不是以医疗为目的来判断人的病情或健康状态等的身体状态或精神状态。在这种意义上,本发明的紫外线敏感性的判定方法也可以被表记为紫外线敏感性的测定方法或紫外线敏感性的检查方法。
本发明的紫外线敏感性降低剂的评价或探索包括:将试验物质投予被检对象或使试验物质与被检对象接触的工序,向被检对象的皮肤或皮肤细胞照射紫外线,利用该照射后的规定期间内检测出的生物光子的量来评价试验物质。
这里,作为被投予的试验物质,没有特别限制,可以是天然存在的物质,也可以是通过化学或生物学的方法等人工合成的物质,另外可以是化合物,也可以是组合物或混合物。其中,优选为确保了安全性的已知的物质、例如医药品、化妆品以及用作它们的原料的物质或组合物。另外,当试验物质是医药品或化妆品等的组合物时,如果该组合物包含紫外线吸收剂或紫外线散射剂等紫外线防御材料,则在本评价或探索方法的紫外线照射中,向被检对象的皮肤或皮肤细胞照射的紫外线被物理地防御,因此有可能影响检测出的生物光子量。因此,在本评价或探索方法中,当试验物质为组合物时,优选该组合物为不包含紫外线吸收剂、紫外线散射剂等紫外线防御材料的组合物。此外,在本评价或探索方法中,在作为试验物质对包含紫外线防御材料的组合物进行评价时,优选在生物光子测定前或紫外线照射前进行将该组合物从被检对象的皮肤或皮肤细胞中除去的处理。
试验物质的投予方式可以是口服或非口服中的任意种,优选非口服的方式。具体而言,优选以软膏、乳膏、乳液、洗剂、凝胶、气溶胶、贴片、胶带、喷雾等各种方式涂敷在皮肤上的方式。
此外,将试验物质投予被检对象或使试验物质与被检对象接触的次数没有特别限制。此外,可以是在紫外线照射的同时或刚刚之前的单次投予或接触,优选在紫外线照射前设置规定的投予或接触期间,在该期间内以规定的投予或接触频率进行一次或多次的投予或接触。当被检对象是人时,投予期间优选为1天以上、更优选为1周以上、进一步优选为4周以上。此外,优选为6个月以下、更优选为3个月以下、进一步优选为2个月以下。投予频率优选每天1次以上、更优选为1次~5次、进一步优选为1次~3次、进一步优选为2次。
当使用培养表皮细胞、3d皮肤模型、培养皮肤组织等作为被检对象时,接触期间优选为1小时以上、更优选为6小时以上、进一步优选为24小时以上。此外优选为72小时以下、更优选为36小时以下、进一步优选为48小时以下。接触频率在上述接触期间中优选为1次以上、更优选为1~4次、进一步优选为1或2次。
然后,测定在紫外线照射后的规定期间内检测出的生物光子,将减少生物光子量的试验物质评价为紫外线敏感性降低剂。
关于减少生物光子量的试验物质的鉴定,例如可以通过比较投予了不同浓度的试验物质时测定的生物光子量来进行。作为更具体的例子,在较高浓度的试验物质投予组与较低浓度的试验物质投予组之间;在试验物质投予组与安慰剂投予组之间;在试验物质投予组与非投予组之间;或者在投予试验物质之前和之后,比较生物光子量。由于试验物质的投予、或者由于较高浓度的试验物质的投予而降低生物光子量的情况下,可以将该试验物质鉴定为生物光子量降低物质。
例如,当试验物质投予组中的生物光子量与对照组(安慰剂投予组或非投予组)相比被认为有降低倾向时,优选被认为在统计学上是显著地降低时,可以将该试验物质鉴定为生物光子量降低物质。
而且,所鉴定的使生物光子量降低的试验物质可以评价为紫外线敏感性降低剂。
以这种方式选择的紫外线敏感性降低剂例如可以作为用于降低紫外线敏感性的皮肤外用剂而使用,或者可以作为用于降低紫外线敏感性的材料或制剂而配合在皮肤外用剂中使用。
关于上述实施方式,本发明进一步公开了以下的方式。
<1>一种紫外线敏感性的判定方法,其包括:向被检验者的皮肤照射紫外线,利用在该照射后的规定期间内检测出的生物光子的量来判定紫外线敏感性的工序,该规定期间是其50%以上与照射后第1~3分钟的期间重叠的期间。
<2>如<1>的方法,其中,规定期间的长度优选为30秒~3分钟、更优选为40秒~2分钟、更优选为50秒~1分钟30秒、更优选为1分钟。
<3>如<1>或<2>的方法,其中,规定期间为紫外线照射后第1~2分钟的1分钟、紫外线照射后第2~3分钟的1分钟或紫外线照射后第1~3分钟的2分钟。
<4>如<1>~<3>中任一项的方法,其中,紫外线照射为a波和b波的混合紫外线的照射。
<5>如<1>~<4>中任一项的方法,其中,紫外线照射为300~8000mj/cm2、更优选为500~7000mj/cm2、进一步优选为600~6000mj/cm2的紫外线照射量。
<6>如<1>~<5>中任一项的方法,其中,根据生物光子的发光强度计算出生物光子的量。
<7>如<1>~<6>中任一项的方法,其中,紫外线敏感性是由紫外线引起的红斑形成。
<8>一种紫外线敏感性降低剂的评价或探索方法,其包括:将试验物质投予被检对象或使试验物质与被检对象接触的工序;和向被检对象的皮肤或皮肤细胞照射紫外线,利用在该照射后的规定期间内检测出的生物光子的量来评价试验物质的工序,该规定期间是其50%以上与照射后第1~3分钟的期间重叠的期间。
<9>如<8>的方法,其中,被检对象是人、培养表皮细胞、3d皮肤模型或培养皮肤组织。
<10>如<8>或<9>的方法,其中,关于试验物质向被检对象的投予或接触,在紫外线照射前设定规定的投予或接触期间,在该期间内以规定的投予或接触频率进行一次或多次投予或接触。
<11>如<10>的方法,其中,关于试验物质向被检验者的投予,作为投予期间,优选为1天以上、更优选为1周以上、更优选为4周以上,并且优选为6个月以下、更优选为3个月以下、更优选为2个月以下,作为投予频率,优选为1天1次以上、更优选为1次~5次、更优选为1次~3次、更优选为2次。
<12>如<10>的方法,其中,关于试验物质向培养表皮细胞、3d皮肤模型或培养皮肤组织的接触,作为接触期间,优选为1小时以上、更优选为6小时以上、更优选为24小时以上,并且优选为72小时以下、更优选为36小时以下、更优选为48小时以下,作为接触频率,在所述接触期间中优选为1次以上、更优选为1~4次、更优选为1次或2次。
实施例
紫外线照射装置
将wg-320滤光片(厚度1mm、涩谷光学公司制造)安装到具有氙灯作为光源的300w型的氙气光源(max-301、朝日分光公司制造)上而使用(紫外线a波(uva):紫外线b波(uvb)=10.8:1)。
试验例1对人的紫外线照射产生的微弱发光
被检验者是一名30多岁的健康男性,在暗室中适应10分钟后进行测定。使用微弱发光强度检测装置(cla-idfsk、东北电子产业公司制造)进行测定,在安静座位使装置的检测部配件与前臂内侧紧贴。另外,该检测部配件与来自紫外线照射装置的光照射用光纤连接而成为一体,成为通过切换光路来切换紫外线照射和微弱发光强度检测的结构。改变部位进行紫外线照射(紫外线强度为15.4、32.5或61.6mw/cm2,照射时间为120秒,紫外线照射量分别为1.8、3.9或7.4j/cm2),分别对从照射结束2秒后开始的发光强度进行了10分钟的计测。
将计测结果表示图1中。可以确认:紫外线照射导致的来自皮肤的生物光子量在紫外线刚照射后达到最大值,之后迅速减少,在减少一定程度后,随着时间经过缓慢地衰减。
试验例2:对人的微弱发光计测和红斑评价(1)
使用与试验例1相同的装置,按照相同的步骤进行紫外线照射和微弱发光强度检测。被检验者是20多岁~30多岁的3名健康男性,在安静座位上使装置的检测部配件与前臂内侧紧贴。在紫外线照射前,对安静时的发射强度进行了3分钟的计测。接着,进行紫外线照射,对从照射结束2秒后开始的发光强度进行了10分钟的计测。将从各时间段的发光的平均值减去安静时发光而得到的值作为紫外线照射引起的发光增量而计算出。紫外线照射和其后的微弱发光计测通过改变照射部位而在多个紫外线照射条件下进行。表1示出了具体的照射条件和计测结果。
此外,关于紫外线照射部位的红斑形成,在照射24小时后,使用高速分光光度计(cms-35fs、村上色彩技术研究所制造)测定皮肤颜色,以照射部位与照射部位附近的非照射部位之间的红度的差值(δa*)进行评价,将其结果示于表1。
根据表1的结果,计算出δa*与紫外线照射引起的发光增量之间的相关系数(r)(表2)。
[表1]
[表2]
*:p<0.05、**:p<0.01
试验例3:对人的微弱发光计测和红斑评价(2)
使用与试验例1相同的装置,按照相同的步骤进行紫外线照射和微弱发光强度检测。被检验者是20多岁~30多岁的10名健康男性,在安静座位上使装置的检测部配件与前臂内侧紧贴。在紫外线照射前,对安静时的发光强度进行了3分钟的计测。接着,进行紫外线照射,对从照射结束2秒后开始的发光强度进行了5分钟的计测。将从各时间段的发光的平均值减去安静时发光而得到的值作为紫外线照射引起的发光增量而计算出。紫外线照射和其后的微弱发光测定通过改变照射部位而在多个紫外线照射条件下进行。表3示出了具体的照射条件和计测结果。
此外,关于紫外线照射部位的红斑形成,与试验例2同样,作为红度的差值(δa*)进行评价,将其结果示于表3。
根据表3的结果,计算出δa*与紫外线照射引起的发光增量之间的相关系数(r)(表4)。
[表3]
[表4]
**:p<0.01
如表2和表4所示,在紫外线照射后第1~2分钟和第2~3分钟的期间检测出的生物光子(应答生物光子)的量与紫外线照射后的红斑形成程度具有显著的正相关关系。
因此,以紫外线照射后主要为第1~3分钟的期间检测出的生物光子的量作为指标,可以判定由紫外线引起的红斑形成所代表的炎症反应所涉及的敏感性。
试验例4:紫外线敏感性降低剂的评价
1)被检验者:10名健康的成年日本男性
2)试验品:3.0%(v/v)*pharcolexrosemarye水溶液
1.0%(v/v)*pharcolexrosemarye水溶液
安慰剂水溶液
*作为试验品的水溶液中的pharcolexrosemarye(一丸自然美健有限公司制造)的浓度
3)应答生物光子测定和解析:
关于应答生物光子,测定以下所示的稳态生物光子和照射后生物光子,从光照射结束后第1~3分钟的期间的照射后生物光子测定值减去稳态生物光子测定值,由此计算出应答生物光子。关于统计解析,通过单因素方差分析和bonferroni的多重比较,进行显著性差异检验。
<稳态生物光子>
使用微弱发光强度检测装置(cla-idfsk、东北电子产业公司制造),对紫外线照射前的各被检验部位的微弱发光进行了1分钟的计测。
<照射后生物光子>
使用与试验例1相同的紫外线照射装置,向被检验部位照射1430mj/cm2的紫外光(与太阳光相同的波长域),使用微弱发光强度检测装置,对从紫外线刚照射后到第3分钟为止的各被检验部位的微弱发光进行计测。
4)试验步骤:
用湿纸巾擦拭腹部,将3个位置标记为被检验部位。被检验部位为5cm见方(5×5cm)。在暗室中适应10分钟后,进行生物光子计测。从测定日的晚上开始,将2mg/cm2的上述试验品1天2次(早、晚)分别涂敷在3个位置的被检验部位,持续4周。连续使用后,以与连续使用之前相同的步骤进行生物光子计测。
5)结果
将连续使用后的应答生物光子值示于图2。与安慰剂进行比较,结果,利用迷迭香(rosemary)3.0%水溶液时明显降低。另外,利用迷迭香的提取物的事先涂敷,抑制由紫外线照射引起的红斑形成是公知的(日本特开2002-87975号公报)。
试验例5:紫外线敏感性降低剂的评价(使用培养细胞的评价)
1)细胞:来自正常人新生儿包皮的表皮角化细胞(冷冻hekn、lifetechnologies)
(培养条件)
按照常规方法,在含有增殖添加剂(humedia-kg、kurabo)的表皮角化细胞用增殖培养基(epilife、lifetechnologies)中,在37℃、5%co2的条件下进行培养。在微弱发光测定中,利用汉克平衡盐溶液(hank’sbalancedsaltsolutions)(hbss、invitrogen)洗净后回收细胞,之后以4×106cells/ml悬浮于hbss,提供细胞悬浮液。
2)试验品:trolox(6-羟基-2,5,7,8-四甲基苯并二氢吡喃-2-羧酸:6-hydroxy-2,5,7,8-tetramethylchroman-2-carboxylicacid)(aldrich)
3)应答生物光子的测定:
关于应答生物光子,测定以下所示的稳态生物光子和照射后生物光子,从光照结束后第2~3分钟的期间的照射后生物光子测定值减去稳态生物光子测定值,由此计算出应答生物光子。另外,关于生物光子测定和紫外线照射,在取下培养皿的盖的条件下进行。
<稳态生物光子>
将1.0ml细胞悬浮液置于35mm的培养皿中,使用微弱发光强度检测装置(cla-idfsk、东北电子产业公司制造),在暗室中对紫外线照射前的发光强度进行了3分钟的测定。
<照射后生物光子>
使用与试验例1相同的紫外线照射装置,照射太阳紫外光模拟器光(125mw/cm2)40秒,对照射后的发光强度进行了5分钟的计测。
4)试验方法
将trolox(最终浓度100μm)或对照溶剂(70%乙醇)添加到70~80%汇合状态的正常人表皮角化细胞中。在24小时后回收细胞,根据上述方法进行了应答生物光子的测定。将对照溶剂组的值设为1,相对地评价测定数据。
5)结果
如表5所示,与对照溶剂组相比,在作为维生素e的水溶性类似物且作为抗氧化剂已知的trolox添加组中,确认了应答生物光子强度的抑制倾向(p<0.1:没有对应的t检验、两侧)。
[表5]
(
试验例6紫外线敏感性降低剂的评价(使用组织培养皮肤的评价)
1)皮肤组织:从美国皮肤库nationaldiseaseresearchinterchange(ndri)购买了来自外科手术的正常人皮肤组织。另外,在组织提供机构中,书面同意将皮肤组织用于研究用途。
(培养条件)
关于人皮肤组织,对皮下脂肪进行修剪后,用刀切成约1cm×1cm的大小的小片,使用6孔板在37℃、5%co2的条件下进行培养。在培养中使用包含10%(v/v)胎牛血清(fetalbovineserum)(fbs)的advanceddulbecco'smodifiedeaglemedium(均为lifetechnologies)。
对培养1天后的皮肤进行生物光子测定。
2)试验品:trolox(6-羟基-2,5,7,8-四甲基苯并二氢吡喃-2-羧酸:6-hydroxy-2,5,7,8-tetramethylchroman-2-carboxylicacid)
3)应答生物光子的测定:
关于应答生物光子,测定以下所示的稳态生物光子和照射后生物光子,从光照射结束后第1~3分钟的期间的照射后生物光子测定值减去稳态生物光子测定值,由此计算出应答生物光子。另外,生物光子测定以及紫外线照射在从培养液中提取出皮肤组织的条件下进行。
<稳态生物光子>
使用微弱发光强度检测装置(cla-idfsk、东北电子产业公司制造),在暗室中对太阳紫外光模拟器光照射前的发光强度进行了3分钟的计测。
<照射后生物光子>
使用与试验例1相同的紫外线照射装置,照射太阳紫外光模拟器光(30mw/cm2)3分钟20秒,对照射后的发光强度进行了5分钟的计测。
4)试验方法
对于培养1天后的培养人皮肤组织,将trolox(最终浓度100μm)或对照溶剂(70%乙醇)添加到培养基中,在24小时后用pbs清洗皮肤组织后,根据上述方法进行了应答生物光子的计测。将对照溶剂组的值设为1,相对地评价测定数据。
5)结果
如表6所示,与对照溶剂组相比,在trolox添加组中,确认了应答生物光子强度的显著抑制(p<0.05:没有对应的t检验、两侧)。
[表6]
(*:p<0.05)
- 还没有人留言评论。精彩留言会获得点赞!