充分多样的双亲性MHCII结合多肽、免疫载体微球及其制备方法和应用与流程
本发明涉及免疫载体微球领域,具体涉及充分多样的双亲性mhcii结合多肽、免疫载体微球及其制备方法和应用。[
背景技术:
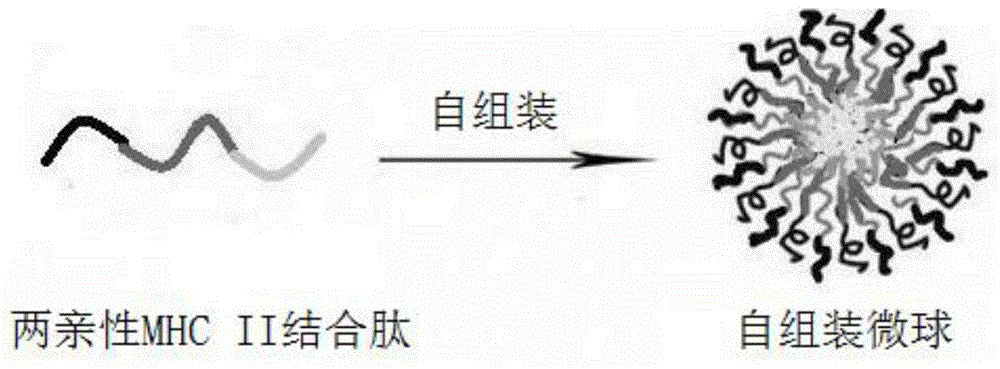
:]一、治疗性疫苗接种疫苗是人类抵御和控制传染性疾病的有效手段之一。传统意义上的疫苗主要是预防性疫苗,其应用对象是健康群体的易感动物及人群,其疫苗成分一般为微生物保护性抗原,可在健康肌体中激活特异性免疫应答,产生特异性抗体和细胞毒t淋巴细胞(ctl),从而获得对该病原体的免疫预防能力。治疗性疫苗(therapeuticvaccine)是近年建立和发展起来的免疫治疗新概念,是指能够打破慢性感染者体内免疫耐受,重建或增强免疫应答的疫苗。治疗性疫苗能在已患病个体诱导特异性免疫应答,消除病原体或异常细胞,使疾病得以治疗,是抗病毒、抗肿瘤的新治疗手段。根据作用机制不同治疗性疫苗可分为两类,一类是通过产生效应细胞起作用,如产生特异性杀伤性t细胞,用于肿瘤治疗或是清除病毒(hbv、hcv、hiv、hpv等)感染细胞;另一类是通过诱导体内产生抗体起作用,抗体可以结合活性分子进而封闭活性分子的功能,抗体还可以通过补体及adcc效应杀伤肿瘤细胞。本发明是以产生抗体为主的治疗性疫苗。二、抗体用于疾病治疗抗体治疗疾病是单克隆抗体技术特别是人源化单克隆抗体技术发展的成果,目前上市临床应用的单克隆抗体超过30种,临床试验中的超过00种,在研的治疗用单克隆抗体超过500种,2013年单克隆抗体销售额超过500亿美元。单克隆抗体研发周期长、生产成本高、治疗费用昂贵。治疗性抗体型疫苗的研究目标是,通过抗原免疫产生内源性抗体来取代外源性单克隆抗体以实现治疗作用。三、抗体产生的免疫学过程b细胞分泌抗体有二种主要机理:t细胞依赖途径(td)和t细胞非依赖途径(ti)。大多数蛋白质产生抗体是td型途径。b细胞td型表达抗体需要双信号活化:抗原表位(b表位)与b细胞受体结合,这是第一信号。抗原通过与b细胞受体结合途径进入b细胞,在细胞的溶酶体(lysosome)、核内体(endosome)内水解成多肽片断并与mhcⅱ结合后,转到细胞膜上展示于b细胞表面,提呈mhcⅱ结合多肽表位(也称th表位或t表位))给cd4+th细胞受体。th细胞识别载体蛋白表位,活化th细胞释放细胞因子,作为b细胞活化分泌抗体的第二信号激活b细胞进入增殖程序,亲和力成熟过程(体细胞突变机利)获得分泌高亲和力、高滴度水平抗体的能力。休止状态的th细胞还不能满足b细胞活化要求,需要dc细胞吞噬抗原,将th表位通过mhcⅱ提呈给th细胞激活th细胞。由此说明,b细胞分泌抗体,实际上涉及上述三个基本过程。dc细胞倾向吞噬颗粒抗原,因此可溶性蛋白一般难以产生高滴度抗体。传统方法是将可溶性蛋白制成乳剂颗粒或吸附于称之谓免疫佐剂凝肽颗粒,才能获得更高滴度抗体。颗粒抗原可以无须免疫佐剂获得高滴度抗体。颗粒化抗原易产生高滴度抗体是免疫实验中普遍现象。一般外源性蛋白均含有b及th表位,在佐剂条件下免疫动物和人可以产生抗体。内源性蛋白不含th表位。二、目前治疗性抗体型疫苗还存在的技术问题1、内源性蛋白作为抗原面临低滴度的问题多肽和内源性蛋白作为抗原免疫不会产生抗体。短肽只有b表位而没有t表位,所以短肽免疫不能产生抗体,称之谓半抗原;内蛋白免疫动物或人一般情况下不能产生抗体,由于b细胞抗体基因不断突变可以产生针对内源性蛋白受体,但与内源性蛋白有高亲和力受体的b细胞则诱导凋亡,仅留下低亲和力受体的b细胞。另一方面,针对内源性蛋白的t细胞在发育过程中被清除而不能再生。内源性蛋白不能诱导动物或人产生高滴度抗体,称之谓b细胞免疫耐受。治疗性疫苗所采用的抗原通常选用人体或者动物的自身蛋白,或称内源性蛋白。为使多肽或内源性蛋白要产生抗体,现有的技术是与外源性强抗原蛋白,免疫学上称之谓免疫载体(immunocarrier)的蛋白化学偶联,引入外源性蛋白用于活化th细胞。免疫载体蛋白常用的有:bsa、ova、klh、破伤风外毒素(tt)、乙肝、戊肝hiv病毒壳蛋白。除了将内源性蛋白与免疫载体(immonocarrier)蛋白化学交联方法,用基因工程技术构建含有免疫载体的融合蛋白作为异源分子提供th表位。也有用异种动物来源的同种蛋白提供th表位。由此带来了新的问题:由于针对内源蛋白高亲和力的b细胞克隆清除,与外源载体蛋白表位高亲和结合的b细胞的丰度比与内源性蛋白表位结合的b细胞的丰度高几个数量级,从而存在交联蛋白(或融合蛋白)分子内蛋白表位免疫竞争的问题。当疫苗进入人体或动物体内,外源载体蛋白表位具有竞争优势,b细胞受体有更高机率结合外源载体蛋白表位并吞噬,产生针对外源载体蛋白的高滴度抗体。而内源性蛋白的相应抗体受抑制,只能产生低滴度抗体,很难实现临床治疗价值。2、特异性问题:只有产生高滴度抗体才能起到治作用。如果以外源性蛋白提供th表位,除了引入上述竞争性抑外,更高滴度外源蛋白抗体因抗体会产生交叉反应可以产生无法预测副反应。3、人类hla多样性动物试验中多数用纯种动物。在常用实验动物中小以鼠为例,表达mhcⅱ的基因h2就是h2-iab。h2-iadh2-ieah2-ieb几种。人类hla复合体是迄今已知的人体最复杂的基因体系。分为hla-ⅰ和hla-ⅱ。前者与细胞免疫相关,后者与抗体免疫相关联。hla-ⅱ类基因区十分复杂,主要包括hla-dp、dq、dr三个亚区和新近确定的dn、do、dm等3个亚区。该区的基因是以它们所编码的肽链(α、β)直接命名,如dra、drb1、drb2等。2014年公布的hla-ⅱ类等位基因型表达的蛋白多达1915种,而且每年有新发现。mhcⅱ由α链和、β链组成,有不同等位基因的αβ链组合,多样要性以万计数。几乎没有一种天然蛋白可以提供如此多的样的mhcⅱ结合多肽满足广泛人群疫苗制备。专利申请文献cn102008619a公开了一种克服b细胞免疫耐受的免疫微球及其应用。该对比文件主要针对的是现有技术中心化学交联蛋白或融合蛋白分子内表位的免疫竞争问题。其采用了免疫微球来解决上述问题,在微球介质的外部包覆疫苗抗原,内部包裹有用于活化t细胞的免疫载体蛋白。进一步的,疫苗抗原的b细胞表位位于免疫微球的表面,免疫载体蛋白的t细胞表位位于所述免疫微球的内部。该方法通过将抗原蛋白及免疫载体蛋白分置于微球表面及内部,避免了抗原蛋白表位与th细胞活化表位同b细胞受体的竞争。该技术存在的问题是:微球内的蛋白容易从微球中漏出来,产生针对载体蛋白高滴度抗体。另一方面,该申请仅仅产生抗体免疫效应。[技术实现要素:]本发明的目的在于解决现有技术中的上述问题。为了实现上述目的,提供一种充分多样的双亲性mhcii结合多肽,其特征在于序列结构为:脂肪酰-β折叠肽-c-mhcⅱ结合多肽-亲水型β折叠肽-马来酰亚胺,序列结构中所述的脂肪酰与c之间的β折叠肽是由5-8个疏水氨基酸构成的序列,所述的亲水型β折叠肽由酸性氨基酸与碱性氨基酸交错组成长度3-5的序列,所述的mhcii的结合多肽的序列是与mhcii具有亲和力的多肽序列或mhcii的随机取代序列,随机取代序列中用于随机取代的氨基酸是与取代位置亲水性相近的氨基酸,构成mhcii结合多肽的充分多样性。所述的偶联基团用于与抗原偶联。c为半胱氨酸,使多肽间形成二硫键。本发明还涉及一种免疫载体微球的制备方法,上述的双亲性mhcii结合多肽通过自组装形成免疫载体微球,mhcii结合多肽在微球中,偶联基团位于微球表面。使疫苗的抗原呈于微球表面,mhcii结合多肽在里面,避免与b细胞受体产生结合竞争。进一步的,所述的组装通过以下方法中的一种实现:a.在有机溶剂/水混合溶剂中自组装,或b.通过模板自组装。所述的在有机溶剂/水混合溶剂优选为乙腈/水混合溶剂,双亲性mhcii结合多肽加入到该混合溶剂中后通过搅拌形成乳液,双亲性mhcii结合多肽通疏水端结合形成微球,挥发其中的乙腈,离心沉淀以分离得到微球。所述的模板为固体脂质,固体脂质溶解于挥发性疏水溶剂中后与水搅拌形成乳液,双亲性mhcii结合多肽通疏水端浸入固体脂质后形成微球,挥发所述的挥发性疏水溶剂,离心沉淀以分离得到微球。本发明还涉及一种免疫载体微球,由上述的制备方法制得。免疫载体微球可以用于制备良性疾病治疗的抗体疫苗。进一步的良性疾病治疗的抗体疫苗包括:ige疫苗、tnf-α疫苗、vegf疫苗、cetp疫苗、dpp4多肽疫苗、阿尔茨海默病疫苗。免疫载体微球可以用于制备肿瘤治疗的抗体疫苗。所述的肿瘤治疗的抗体疫苗包括:egf疫苗、egfr疫苗、pdl-1疫苗、tcr疫苗、bcr疫苗、cd19疫苗、cd20疫苗、vegf疫苗、her2疫苗、mage疫苗、mucin疫苗、pdl疫苗、βhcg疫苗。抗原偶联在免疫载体微球的偶联基团上形成抗原疫苗。本发明还涉及一种联合应用,包括:a.上述抗原疫苗,b.fcr-cart细胞或nk细胞。本发明相对于现有技术而言具有以下优点:1、多肽自组装文献多有报道,但多种不同多肽,多肽长度在20个氨基酸以上,现有的方法不能自组装成规正的微球,尤其充分多样性的mhcⅱ结合多肽或抗原多肽自组装未有报道。2、mhcⅱ结合多肽自组装成微球,代替外源性蛋白,为内源性蛋白提供的mhcⅱ结合多肽。内源的抗原与mhcⅱ结合多肽内外分置,可以避免二者与b细胞受体竞争抑制,免疫可以获得比外源蛋白作为载体更高滴度抗体。3、微球体内裂解后,微球裂解产物是mhcⅱ结合可溶性多肽,尽管外源多肽可以是b细胞表位,但由于不含有th表位,漏出来也不会产生针对载体成份的抗体。特异性好。特别适合于利制备用于良性疾病的治疗性疫苗。4、充分多样的mhcⅱ结合多肽的充分多样性满足不同个体mhcⅱ的多样性要求。是任何天然蛋白载体不可能达到的。5、颗粒有利于被dc或巨噬的细胞吞噬,进而活化静止th细胞起辅助功能。6、该免疫载体微球具有通用性,可通过改变微球表面的官能基团使其具备连接各种抗原的能力,抗原可以是多肽、蛋白、多糖抗原或其他小分子化合物。7、载体的构成成分为多肽或固体脂质、生物相容多糖,无其他化合物成分,制备疫苗有更高的安全性。8、体内产生针对肿瘤细胞的抗体,主要通过adcc途径实现。效应细胞主要是有fc受体的nk细胞。与体外扩增培养的nk细胞合用更有效杀伤肿瘤细胞创造条件。9、肿瘤免疫治疗,以细胞免疫杀伤为主。tc细胞是针对有变异的肿瘤细胞,但某些肿瘤细胞mhcⅰ低表达或不表达,使tc细胞失去免疫杀伤作用。表达fc受体的t细胞比例极少。用本发明的免疫载体微球构建的疫苗产生高滴度抗体与体外基因工程改造表达fc受体并在体外培养扩增t细胞合用,可望获得更好的疗效。除上述应用外,还有更多的应用前景:诸如预防性疫苗、戒毒疫苗、避孕疫苗、实验研究。[附图说明]图1是双亲性mhcii结合多肽自组装成免疫载体微球的示意图。图2是微球的电子显微镜图。图3是四质粒共转染72h后293t细胞的gfp%,其中(r2)=98.3%。图4是不同梯度病毒对293t细胞的感染率图。图5是t细胞上car基因的转染率图。上图为d7天测定结果,下图为d14天测定结果。[具体实施方式]以下,结合实施例和附图对于本发明做进一步说明,实施例和附图仅用于解释说明,而不用于限定本发明的保护范围。实施例1用于小鼠动物试验用的mhcii结合多肽自组装双亲性多肽设计及制备1、用于balb/c小鼠的mhcii结合多肽,依据文献选择破伤风外毒素片断:tt830-844qyikanskfigiteld2、用于c57/bl6小鼠的mhcii结合多肽,依据文献选择鸡蛋卵清蛋白片段:ova324-338isqavhaahaeinea3、用于构建免疫载体微球,含有上述二种mhcii结合多肽的二亲性多肽设计及合成,合成可以采用常规方法:⑴、pal-aaaaggg-c-qyikanskfigiteld-rdkqkk-mal(pal:棕榈酰,mal:马来酰亚胺)。⑵、pal-aaaagggg-c-isqavhaahaeinea-qkdrdk-mal实施例2有机溶剂/水溶剂混合溶剂中的微球制备1、多肽自组装成球原理:如图1所示,二亲性多肽属于高分子表面活性剂,在水/油二相界面,疏水端浸入油相,亲水端游离于水相。若油相呈微球状,双亲性多肽就可以油相微球为模,跨微球界面β平行聚合分布。由于存在二种β折叠肽,当在搅拌条件下油相溶剂蒸发,双亲性多肽又不溶于水,在水相中成为稳定的自组装微球。2、制备操作⑴、合成的双亲性mhcii结合多肽10mg用30-60%乙腈/水溶解。双亲性mhcii结合多肽的浓度为0.1-1mg/ml。⑵、采用与乙腈不互溶的有机溶剂石油醚或环已烷。加含有0.1-1%吐温-80的水,搅拌乳化成微球。⑶、(1)和(2)混合,在通风橱中搅10-30分钟,再置于旋转蒸发器中,30-50℃将有机溶剂除去即可得悬浮于水中的自组装微球。3、结果分析:用粒径分析仪测定大小及电位分析仪定ζ电位。微球为100—500纳米球形颗粒。ζ电位与微球末端基团及溶液离子强度相关。4、离心沉微球,沉淀后用0.05m,ph7.5磷酸缓冲液5ml悬浮,离心沉淀反复2次。5、离心后冰冻干燥低温,微球如图2所示。实施例3固体脂质为模板多肽自组装微球制备1、成球原理:先将棕榈酸溶解在有机溶剂中,乳化成微球作为模板。二亲性多肽溶液倒入与其混合,搅拌条件下,二亲性多肽的疏水端埋入含有棕榈酸的有机相被锚定,亲水端在水相。待有机溶剂挥发形成固体质颗粒,形成分散稳定的微球。颗粒大小可以用超声波或均质机实现控制。条件是溶解二亲性多肽的溶剂与溶解棕榈酸有机相不互溶。本发明用乙腈/水溶解二亲性多肽,棕榈酸用石油醚或环已烷溶解。二种溶剂不互溶。多肽由疏水作用力和正负离子作用力起稳定作用。2、制备操作⑴、用于自组装的二亲性多肽与实例一相同。10mg用30-60%乙腈/水溶解,离心去除不溶解的多肽。浓度为0.5-1mg/ml。⑵、棕榈酸100mg,卵磷脂50mg克溶解于3ml二氯甲烷/石油醚(2:3)中,加到30ml含有1.0%吐温-80乙腈/水溶液中,磁力搅拌后超声乳化。乳化颗0.3-1微米。⑶、将多肽-乙腈/水溶液倒入乳化的中棕榈酸-卵磷脂乳剂中,磁力搅拌,使有机溶剂逐渐挥发。⑷离心沉微球,沉淀后用0.05m,ph7.5磷酸缓冲液5ml悬浮,离心沉淀反复2次。3、结果分析:用粒径分析仪测定大小及电位分析仪定ζ电位。微球为100—500纳米球形颗粒。ζ电位与微球末端基团及溶液离子强度相关。4、离心后冰冻干燥低温保存。实施例4生物凝胶微球包裹的多肽自组装免疫载体微球制备1、原理:用生物凝胶微球包裹药物、蛋白、核酸研究文献很多。包裹多肽只因渗漏严重效果不佳。但双亲性多肽自组装后,成为聚合体则可以克服渗漏问题。该方法可以同时加入细胞因子、免疫促进功能的cpg核酸。2、操作:⑴、实例1制备的自组装微球,在有机溶剂挥发过程中,使之形成小于1000nm的微球,与1%的海藻酸溶液混合。用海藻酸钙微球制备的常规方法,通过均质机形成1-3微米的海藻酸钙微球。按文献方法包复壳聚糖,制成含有自组装多肽,壳聚糖包复的海藻酸钙微球。⑵、微球先用n羟马来酰亚胺丙酸酯修饰用于偶联,然后用戊二醛或环氧氯丙烷固定。3、用光学显微镜检测微球大小,分散性4、pbs洗涤冰冻干燥低温保存。实施例5临床用含有充分多样性mhcii结合多肽选择与设计在线netmhciipan3.0server提供hla-dr、hla-dp、hla-dq结合序列预测。输入来源于风疹病毒壳蛋白序列、来源于破伤风毒素蛋白序列、甲型肝炎病毒的蛋白序列,对hla-dr、hla-dp、hla-dq结合序列预测,得到高亲和力的mhcⅱ结合15肽。dr、dp、dq均取其一个亚类等位基因产物,共取10个,见下表。hla15肽核心序列亲和力(nm)hla-drb1*01:01itdymyltnapsytnymyltnaps4.43hla-drb3*01:01dlvkfisdkikflnpfisdkikfl83.99hla-drb4*01:01llaiagirlhraaiyiagirlhra46.26hla-drb5*01:01niyyrrlynglkfiiyrrlynglk4.13hla-dpa1*01:03-dpb1*01:01fnnftvsfwlrvpkvftvsfwlrv3.02hla-dpa1*02:01-dpb1*09:01klytsylsitflrdfsylsitflr9.99hla-dqa1*01:01-dqb1*02:01ktqlvddfldldmailvddfldld269.66hla-dqa1*04:01-dqb1*03:01yingvlmgsaeitglvlmgsaeit108.65hla-dqa1*05:06-dqb1*03:04slnflggapvcpgqnflggapvcp20.62hla-dqa1*06:01-dqb1*03:05dydqycadvaaeelmycadvaaee84.34每个亚类合成五条多肽:⑴、没有修改的原序列多肽,⑵、4、6、8、10位三个氨基酸随机取代序列,⑶、3、5、7、9、11位三个氨基酸随机取代序列,⑷、2、4、6、8、10、12位三个氨基酸随机取代序列,⑸、3、5、7、9、11、13位三个氨基酸随机取代序列。随机取代氨基酸原则是亲水性相近的氨基酸。亲水性指数表见下:具体操作如下:⑴、15肽第5、7、9、11位四个氨基酸随机取代以hla-drb1*01:01为例,预测结合肽为itdymyltnapsytn亲和力为4.43nm多肽合成时,第5步合成加入m、a、w三种氨基酸原料。第7步合成加入p、t、y三种氨基酸原料。第9步合成加入n、q、e,第11步加入p、t、y三种氨基酸原料。多样性理论计算为81种⑵、15肽第4、6、8、10、12位随机修hla-dpa1*01:03-dpb1*01:01预测结合多肽为fnnftvsfwlrvpkv亲和力为3.02nm多肽合成时,第4步合成加入f、v、i三种氨基酸原料。第6步合成加入v、l、f三种氨基酸原料。第8步合成加入f、v、i,第10步加入l、w、v三种氨基酸原料。第12步加入v、l、f三种氨基酸原料。多样性理论计算为243种。⑶、15肽第3、5、7、9、11、13位随机修改以hla-dqa1*01:01-dqb1*02:01为例,预测结合序列为ktqlvddfldldmai亲和力为269.66nm多肽合成时,第三步合成加入q、d、n,第5步合成加入v、l、f三种氨基酸原料。第7步合成加入d、k、q三种氨基酸原料。第9步合成加入l、w、v,第11步加入l、w、v三种氨基酸原料。第13步加入m、a、w多样性理论计算为729种⑷、15肽第2、4、6、8、10、12、14位随机修改以hla-dqa1*06:01-dqb1*03:05为例,预测结合多肽dydqycadvaaeelm亲和力为84.34nm多肽合成时,第二步合成加入y、p、c,第4步合成加入q、d、n三种氨基酸原料。第6步合成加入c、y、g三种氨基酸原料。第8步合成加入d、k、q第10步加入agm三种氨基酸原料。第12步加入e、n、h三种氨基酸原料。第14步l、w、v。多样性理论计算为种2187。上述操作既利用了计算机预测成果,又产生足够多样性。多肽混合以后的多样性是(1+81+243+729+2187)x10=32410实施例6、临床用充分多样性mhcii结合多肽自组装微球临床用含有充分多样性mhcii结合多肽组装免疫载体微球制备方法与小鼠用的相同,见实施例2、3、4。实施例7抗原与微球偶联制备疫苗多肽抗原可以合成时在末端加半胱氨酸引入巯基,蛋白质分子的氨基上可用spdp试剂引入巯基。微球表面带有马来酰亚胺基,马来酰亚胺可在ph6.5-7.5的条件下与巯基发生特异性反应形成稳定的巯醚键。中性ph值条件下,马来酰亚胺与巯基反应的速率快于氨基1000倍。抗原与微球在ph中性的pbs中反应连接,可以成为疫苗。具体操作参考sima-aldrich:spdpcrosslinkersthermo-fisherscientific:sulfhydryl-reactivecrosslinkerchemistry以下,对于免疫载体微球的具体应用作进一步说明。实施例8、哮喘疫苗ige介导性疾病是一类由ige引发的变态反应性疾病的统称,因其易感者在接触环境中变应原时往往产生过多的ige抗体,通常伴有一种以上的变态反应性疾病而得名。当变应原初次进入机体后,选择性诱导特异性b细胞产生ige抗体应答,而血清中游离的ige可在不结合抗原的情况下通过其fc片段与肥大细胞和嗜碱性粒细胞表面受体结合使机体处于致敏状态。机体再次接触变应原后,多价变应原与致敏细胞表面两个或者两个以上相邻的ige抗体结合,使细胞膜表面受体发生交联,触发致敏细胞脱颗粒,合成及释放生物活性介质,从而引起局部或者全身过敏反应。ige介导性疾病通常包括特应性皮炎atopicdermatitis,ad、变应性鼻炎allergicrhinitis,ar、支气管哮喘asthma,as等,症状重者可导致过敏性休克,危及生命。变态反应性疾病已严重干扰了患者的工作和生活,由此带来的社会负担也是相当可观的。由于ige在变态反应性疾病的发生发展环节中的重要作用,目前已经成为抗变态反应性疾病治疗的一个新的靶点和研究热点。ige的分子结构已清楚,在人ige抗体中与髙亲和力受体和低亲和力受体结合的位点重点位于cε3结构域,奥马佐单抗(omalizumab)是一种能特异性识别ige重链的che3区域,并选择性的与ige结合,抑制ige与高亲和力的ige受体(fceeri)在肥大细胞和嗜碱性粒细胞表面的结合,从而减少过敏性介质的释放,不仅如此,在部分特异反应性患者中还能减少ige受体的数量。il-5单克隆抗体也用于治疗哮喘,第一个是gsk的nucala(mepolizumab),mepolizumab是一种白细胞介素5(il-5)抑制剂,能特异性结合il-5,并阻止其激活il-5受体。该药是首个上市的作用于il-5细胞因子并抑制嗜酸性细胞活性的单抗,用于12岁及以上哮喘患者。第二个是梯瓦的cinqair(reslizumab),于2016年3月23日获得fda批准,2016年8月18日获得ema批准上市。reslizumab是一种白细胞介素-5(il-5)拮抗剂,可结合il-5并阻止其与il-5受体的结合,从而减缓嗜酸性粒细胞相关炎症反应。该药用于治疗18岁及以上患者的重度哮喘。cinqair是第二个获批,进入重度哮喘市场的il-5单抗。il-5也可以制备相应疫苗用于哮喘治疗。本发明构建能够诱导出针对ige受体结合位点(cε3结构域)特异性中和抗体的治疗性疫苗,通过抗原抗体结合,产生的封闭igefc片段上与igefc受体结合的部位,进而阻断由ige介导的变态反应性疾病效应途径,为ige介导性疾病的治疗提供新的途径。本研究用igecε3片断多肽为抗原,构建微球疫苗,并与klh交联物比较。⑴、抗原:igecε3片断多肽序列:gygyqcivdhpdfpkpivrsitktpgqr用化学合成方法合成了小鼠igefc的cε3结构域特异的多肽。该多肽相应单克隆抗体被证实能阻断ige与肥大细胞受体结合并对过敏性疾病治疗有效⑵、mhc2结合序列:麻疹病毒来源isiseikgvivhk及卵清蛋白来源isqavhaahaeinea⑶、自组装多肽序列设计为:pal-aaaaggg-c-isiseikgvivhk-dkqk-malpal-aaaagggc-isqavhaahaeinea-kqrk-mal⑷、自组装将自组装多肽溶于水跟乙腈(体积比1:1)的混合溶剂中,浓度1mg/ml,旋蒸除去乙腈,在乙腈挥发过程中自组装肽逐渐自聚成球,最终得到含有自组装多肽微球的水溶液,冻干得到自组装多肽微球,微球粒径约为2.8微米。(见附图)⑸、微球疫苗制备:抗原多肽第六个氨基酸是半胱氨酸,利用巯基与微球上的马来酰亚氨基连接。反应条件是实施例7中方法。⑹、ige多肽-klh结合物由吉尔生物技术公司合成动物及免疫balb/c小鼠来源于上海实验动物中心。50微克皮下注射免疫,每周一次。最后一次免疫后一周取血用于抗体滴度测定。由吉尔生物技术公司实施。⑺、elisa测定方法文献常规方法。由吉尔生物技术公司实施。⑻、elisa测定结果由公司测定提供。第一组:ige多肽片段偶联自组装多肽载体微球免疫6周elsa测试结果血清稀释倍数第二组:ige多肽片段偶联klh免疫6周elisa测试结果血清稀释倍数⑻、结果分析(a)多肽是半抗原,需要与免疫载体蛋白连接(如bsa、ova、tt、klh)才能诱导抗体产生。klh是经典免疫载体蛋白,与之连接后能高滴度抗体。但产生klh高滴度抗体并远高于抗原的滴度水平。(b)、上述结果显示,本发明的异源mhcⅱ结合多肽自组装微球可以代替传统的异源蛋白作为免疫载体,结果优于klh效果。载体成份抗体滴度很低。il-5单克隆抗体也用于治疗哮喘,第一个是gsk的nucala(mepolizumab),mepolizumab是一种白细胞介素5(il-5)抑制剂,能特异性结合il-5,并阻止其激活il-5受体。该药是首个上市的作用于il-5细胞因子并抑制嗜酸性细胞活性的单抗,用于12岁及以上哮喘患者。于2015年11月4日获得美国fda批准,2015年12月2日获得ema批准,2016年3月28日获得日本pmda批准上市第二个是梯瓦的cinqair(reslizumab),于2016年3月23日获得fda批准,2016年8月18日获得ema批准上市。reslizumab是一种白细胞介素-5(il-5)拮抗剂,可结合il-5并阻止其与il-5受体的结合,从而减缓嗜酸性粒细胞相关炎症反应。该药用于治疗18岁及以上患者的重度哮喘。cinqair是第二个获批,参考文献:vaccine21(2003)1580–1590syntheticigepeptidevaccineforimmunotherapyofallergychangyiwanga,*,alanm.walfielda,xindefanga,brucehammerbergb,johnye。实施例9、ⅱ型糖尿病疫苗ddp-4多肽疫苗dpp-4抑制剂可选择性抑制dpp-4的酶活性,阻止glp-1裂解失活,提高活性glpl的血浆水平,增强其生理作用,降低2型糖尿病患者的hba、空腹血糖和餐后血糖水平。dpp-4抑制剂作为一类新型口服降糖药物。在2型糖尿病治疗中对血糖控制的有效性、良好的安全性和耐受性已经在大量的临床试验和实际应用中得到了证实。实施例10、心血管疾病cetp多肽疫苗制备疫苗用的mhcii结合多肽序列为:fgfpehllvdflqsls胆固醇大部分由肝脏制造。人体内胆固醇的总量为100到200克。其中三分之二在体内自行合成,三分之一来自食物。胆固醇必须和脂蛋白结合才能运送到体内各部分。脂蛋白又分低密度脂蛋白和高密度脂蛋白。胆固醇酯转运蛋白(cholesterylestertransferprotein,cetp)是血浆一种糖蛋白,它能够把胆固醇酯从hdl转移到低密度脂蛋白(ldl)、中间密度脂蛋白(idl)和极低密度脂蛋白(vldl),并交换甘油三酯,从而在调节血浆hdl水平和重塑hdl颗粒组成方面发挥重要作用,高活性的cetp可以降低hdl水平。因此,cetp抑制剂被认为作为冠状动脉粥样硬化最有治疗潜力的药物之一。而且临床iii期的结果令人欣喜。cqyikanskfigitegfpehllvdflqsls是胆固醇酯转运蛋白多肽片断,以此为抗原制备疫苗,产生抗体能抑制cetp运送胆固醇活性,提高hdl/ldl比值。降低外周血液中胆固醇的浓度,预防动脉硬化及相应心脑血管疾病。测试结果如下:血清稀释倍数参考文献:thrombvascbiol.2000;20:2106-2112.vaccine-inducedantibodiesinhibitcetpactivityinvivoandreduceaorticlesionsinarabbitmodelofatherosclerosischarlesw.rittershaus,davidp.miller,lawrencej.thomas,micheled.picard,christopherm.honan,constanced.emmett,carolynl.pettey,hedyadari,russella.hammond,davidt.beattie,alland.callow,henryc.marsh,unas.ryan。实施例11egf蛋白抗肿瘤疫苗egf最早是古巴开发,国内由百泰生物药业有限公司与古巴共同研发的一种化学偶联的多肽类疫苗。egf疫苗系由重组人egf与重组奈瑟氏流脑外膜p64k载体蛋白经化学交联形成的偶联物,与油性佐剂montanideisa51乳化而成。该疫苗免疫人体后,能打破机体对自身抗原(egf)的免疫耐受,诱导高水平抗egf的抗体。该抗体与人体内egf特异性结合,降低血清egf的含量,通过下调egf/egfr信号通道活性,从而抑制肿瘤细胞增殖,实现上皮源性肿瘤的治疗。该疫苗是全球第一个成功通过主动免疫实现肿瘤治疗的疫苗。动物试验及临床研究表明,该疫苗对表皮生长因子受体(egfr)过度表达的恶性肿瘤包括肺癌、头颈癌、卵巢癌等具有较好的疗效,尤其是对非小细胞肺癌疗效显著。目前已在古巴、秘鲁、巴拉圭获批上市用于治疗晚期非小细胞肺癌。中国晚期非小细胞肺癌患者ⅰ期临床研究也已经结束,正在计划开展ⅱ/ⅲ期临床研临床试验结果显示,血清egf含量高的肺癌患者有效。上述egf疫苗是与脑炎球菌外膜蛋白偶联,本发明用新型免疫载体微球,预期优于市售疫苗制剂1、抗原:小鼠egf(megf)是51个氨基酸的基因工程表达蛋白。购于peprotech公司。2、混合小鼠mhcⅱ结合多肽微球构建与实施例4相同3、egf引入巯基参照文献实施。(谈立松等:胃癌单抗-rta结合物的制备及其细胞毒特性研究现代免疫学1988,1988(05)330-333)。4、5mg巯基化的溶于5mlph7.5pbs;压积为2ml,带有mal的mhcⅱ的混合多肽微球悬于5mlph7.5pbs中;二者混合置于磁力搅拌器上4℃冰箱中反应过夜。第二天取出离心弃上清液。pbs洗涤一次,悬于3mlpbs中供免疫用。5、免疫:balb/c小鼠,皮下多点注射共300微升,每二周一次。第四次免疫一周后放血常规方法测定抗体滴度。6、elisa结果实验一、以megf包被酶标板测定抗体滴度血清稀释倍数od4501000200040008000160003200064000blanknegative12.351.551.050.7870.8100.5500.4890.0600.10921.971.590.980.6600.5450.4220.3850.0770.11932.351.881.220.8630.6930.5200.4550.0810.09342.231.811.070.930.6880.5800.4800.8100.10052.591.261.020.8650.7250.6320.5800.0870.095实验二、以空白微球ph9.0碳酸缓冲液中能溶解)包被酶标板测定抗体滴度od4501000200040008000160003200064000blanknegative10.590.3500.0950.1070.2100.1500.1090.0900.12920.850.3900.2800.0600.2040.1220.1150.0770.11030.750.2800.1200.1630.1330.1200.1550.0910.12240.530.110.0720.1930.1080.2000.1150.1000.11050.890.560.1500.0600.1250.1250.1800.0870.091参考文献:therapeuticvaccineagainstdpp4improvesglucosemetabolisminmicepnas|publishedonlinemarch17,2014|e1257实施例12、表皮生长因子受体ⅲ型突变体(egfrvⅲ)微球疫苗的制备及免疫实验egfrvⅲ是表皮生长因子受体膜外部分基因缺失。大约30%-50%的肿瘤中(非小细胞肺癌细胞、乳腺癌和神经胶质瘤)会出现一种称为上皮生长因子突变体iii(egfrviii)的蛋白,而正常细胞中没有这种蛋白。研究人员认为egfrviii可以驱动神经胶质细胞异常增殖和扩散,是导致这种肿瘤高度恶性的原因之一。egfrviii为抗原制备疫疫苗可以诱导机体对含有egfrviii的细胞产生抗体免疫反应,也可以诱生细胞免疫反应。这种新型疫苗包含有合成的egfrviii片段和可以刺激树突细胞的佐剂。(1)抗原序列:固相多肽合成方法合成egfrvⅲ表位多肽,方法同实施例1,序列为:leekkanyvvtdhc(2)egfrvⅲ表位多肽与自组装多肽载体微球偶联,偶联方法同实施例1。(3)免疫策略同实施例2。(4)检测:免结束一周后眼眶放血,收集血清,elisa检测抗体滴度,冻干血清。结果如下,血清稀释倍数参考文献:文献:bmcbiotechnology2010,10:72developmentofanegfrviiispecificrecombinantantibodypujagupta1,shuang-yinhan1,2,marinaholgado-madruga1,siddharthasmitra1,gordonli1,ryantnitta1,albertjwongmolecularcancertherapeutics》,2015,14(5):1141characterizationofabt-806,ahumanizedtumor-specificanti-egfrmonoclonalantibodymolecularcancertherapeuticsclinicaloncology,2017,44(18):931-934.胶质瘤免疫治疗新进展liyi,zhennantao,xuejunyang.advancesintheimmunotherapyofglioma[j].chinesejournalof中国肿瘤013年第卷第8期chinacancer,2013,vol.22,no.8近5年全球抗肿瘤药物研发现状(382–410)andher-1(418–435)sequenceswerethebestcandidatesfortheproductionofavaccineandatherapeuticpeptidemimic实施例13、egfr多肽疫苗(egfr418-435、egfr382-410egfr347-374、)表皮生长因子受体(egfr)是原癌基因c-erb-b1的表达产物。其过表达和突变体均与肿瘤发生发展有密切关系,其在大多数肿瘤中(如膀胱癌、非小细胞肺癌、卵巢癌,头颈部鳞癌、乳腺癌、胶质细胞瘤、胰腺癌、胃癌、前列腺癌、食管癌等)过表达和(或)突变,借助于信号转导使细胞生长失控和恶性化[3]。在各种肿瘤组织中表达率不同,且与肿瘤的分化程度、恶性程度及侵润程度密切相关。以egfr1膜外部分为抗原,产生的单克隆抗体,90%是促进肿瘤细胞生长。膜外部分的多肽构建抗体型疫苗,己经确认有效的是egfr418-435、egfr382-410egfr347-374多肽。本实施例用egfr418-435多肽:slnitslglrslkeisdg用实施例1的微球偶联,免疫balb/c小鼠,8次免疫8周的抗体测定结果如下:参考文献:jimmunolpublishedonline22may2013peptidevaccinesandpeptidomimeticsofegfr(her-1)ligandbindingdomaininhibitcancercellgrowthinvitroandinvivoakevinchufoy,ruthiem.wygle,meganj.miller,jayp.实施例14、her2(人类表皮生长因子受体2)多肽免疫载体微球疫苗构建及免疫实验her2是一种原癌基因,每个人体内的正常细胞膜表面都有少量her2蛋白,her2蛋白可进行信号传导,调控细胞的生长和分裂。当癌细胞内的her2基因高度表达时,细胞膜上会产生过多的her2蛋白,刺激癌细胞的疯狂增长,导致癌细胞不受控制地分裂、生长,增加癌细胞的侵袭性;在her2阳性的乳腺癌中,her2基因大量扩增,导致her2蛋白10-100倍的过表达,从而引起细胞分裂失控,肿瘤侵润性生长。据统计,大约20%-30%的乳腺癌属于her2阳性。her2阳性乳腺癌患者的预后可能会比较差,较易出现复发转移。曲妥珠单抗是抗her2的单克隆抗体,它通过将自己附着在her2上来阻止人体表皮生长因子在her2上的附着,从而阻断癌细胞的生长,曲妥珠单抗(赫赛汀)还可以刺激身体自身的免疫细胞去摧毁癌细胞。与传统化疗药物相比,曲妥珠单抗(赫赛汀)具有更精确的靶向性和低毒性。不良反应相对轻微,耐受性好。2、多肽抗原:her2多肽抗原文献报导很多,在her2二聚体区域的氨基酸序列中,his245、val286、ser288、leu295、his296和lys311形成的空间结构对pertuzumab与her2的结合至关重要。allen等[8]设计了该区域266~296位氨基酸的模拟多肽,经实验证实,与pertuzumab的作用相当。本研究选择her266-296。序列为:gckkifgslaflpesfdgpasntaplqpe4、抗体检测结果:七免结束一周后眼眶放血,收集血清,elisa检测抗体滴度,冻干血清。结果如下,参考文献:vaccines2015,3,519-543;anti-tumoreffectsofpeptidetherapeuticandpeptidevaccineantibodyco-targetingher-1andher-2inesophagealcancer(ec)andher-1andigf-1rintriple-negativebreastcancer(tnbc)jayoverholser1,kristenhenkinsambegaokar1,siobhanm.eze2,eduardosanabria-figueroa3,ritanahta2,3,taniosbekaii-saab4andpravint.p.kaumaya实施例15mucin多肽疫苗1、研究背景:muc1是mucin粘蛋白家族成员,存在于正常腺管上皮细胞及其来源的肿瘤细胞表面,muc1在肿瘤细胞高表达,较正常细胞可达100倍之差。涉及癌种有卵巢癌、肺癌、胃癌乳腺癌,胰腺癌,卵巢癌和多发性骨髓瘤,以muc1为抗原fda的疫苗,批准的是首个进入临床试验的治疗性疫苗。muc1-c包含一个58个氨基酸组成的细胞外结构域(muc1-c/ed)、一个28个氨基酸组成的跨膜结构域和一个72个氨基酸组成的细胞内结构域(muc1-cd),胞外由多肽核心和侧枝糖链构成。其核心肽胞外段含有许多20个氨基的重复串联序列。串联重复被广泛地糖基化,肿瘤细胞表面的糖基化较低。胞外多肽重复序列可以作为疫苗抗原:csapdtrtpapgstappahgvt、即与进入临床试验的blp-25相同,江只是在n端加入半胱氨酸用于偶联微球。2、疫苗制备:微球制备采用实施例4方案3、免疫:balb/c小鼠用于免疫4、抗体测定结果参考文献:pnas|january3,2012|vol.109|no.1|261–266immunerecognitionoftumor-associatedmucinmuc1isachievedbyafullysyntheticaberrantlyglycosylatedmuc1tripartitevaccinevanilakshminarayanana,1,pamelathompsonb,1,margreeta.wolfertb,theresebuskasb,judym.bradleyc,lathab.pathangeyc,cathys.madsena,petera.cohenc,sandraj.gendlera,2,andgeert-janboonsb,2实施例16肿瘤细胞表面抗原egfr制备的微球疫苗与nk细胞联合应用1、研究背景⑴、肿瘤疫苗免疫产生针对肿瘤细胞抗体,体液系统是通过补体杀伤肿瘤细胞。更重要的adcc效应。igg抗体可介导这些细胞发挥adcc作用,其中nk细胞是能发挥adcc作用的主要细胞。在抗体介导的adcc作用的发生过程中,抗体只能与靶细胞上的相应抗原表位特异性结合,而nk细胞等效应细胞可杀伤任何已与抗体结合的靶细胞,故抗体与靶细胞上的抗原结合是特异性的,nk细胞等对靶细胞的杀伤作用是非特异性的是通过抗体fc受体介导的免疫细胞杀伤肿瘤细胞。nk细胞表面有抗体fc受体⑵、nk细胞可释放可溶性nk细胞毒因子(nk,cytotoxicfactor,nkcf),靶细胞表面有nkcf受体,nkcf与靶细胞结合后可选择性杀伤和裂解靶细胞。nk细胞还可释放tnf-α和tnf-β,tnf通过改变靶细胞溶酶体的稳定性,导致多种水解酶渗漏;影响细胞膜磷脂代谢;改变靶细胞糖代谢时ph降低;活化靶细胞核酸内切酶降解dna,从而引起程序性细胞死亡。⑶、肿瘤疫苗产生抗体,通过fc受体召集到肿瘤细胞部位,还可以发挥nk细胞非抗体依赖的自然杀伤功能,对没有抗体结合的肿瘤细胞有旁观者杀伤效果。cancercell27,489–5012015synergisticinnateandadaptiveimmuneresponsetocombinationimmunotherapywithanti-tumorantigenantibodiesandextendedserumhalf-lifeil-2ericf.zhu,1,5,12shuninga.gai,1,5,12caryf.opel,1,5,12byronh.kwan,2,5rishisurana,6martinc.mihm,⑷、nk细胞可以在体外扩增培养,回输改善adcc杀伤肿瘤效果2、肿瘤疫苗egfr多肽疫苗,见实施例133、动物肿瘤模型----小鼠lewislungcancer细胞高表达egfrnk细胞与肿瘤抗体合用的结果nk细胞表面具有fc受体,主要结合人igg1和igg3的fc段(cy2、cy3功能区)。源性抗原,在人体内产生高滴度(高效价)抗体。其中抗体的fc段与nk细胞fc受体结合(adcc效应)直接杀伤靶细胞.,nk细胞组与抗微球egfr抗体+nk组体外杀伤实验的比较1,上述实例:微球egfr经四次免疫最后一周取血于elisa抗体滴度测定,选择nk细胞加抗血清1:10000稀释于96孔板,靶细胞为a549,酶标仪450nm测试(cck8kit),读取各效靶比光密度值/孔.2,nk细胞杀伤靶细胞a549,96孔板效靶比光密度值/孔实验结果显示:nk细胞组与抗微球egfr抗体+nk组体外杀伤实验,靶细胞a549,效靶比为5:1时,抗微球egfr抗体+nk组与nk组比较杀伤效率提高60%左右,优化组合后会产生更好的杀伤效应结果。实施例17、egfr多肽-微球疫苗免疫产生的内源性抗体与体外扩增fcr-car-t细胞合用的试验egfr多肽-微球疫苗免疫产生的抗体见实例13.fcr-car基因的构建和合成,小鼠fcr-car的基因序列如seqidno.23所示,人源fcr-car的基因如seqidn0.24所示。fcr-car的慢病毒包装以nhe1(gctagc)andnot1(gcggccgc)为酶切位点,fcr-car基因连接到病毒载体pcdh。在293t细胞培养收集铺板中计数293t细胞近90*106,转染前24h铺细胞于10cm培养皿约21个,设定共转染组pcdh-gfp&pli1*plp2*p-vsvg(以下简称gfp组)10板,共转染组pcdh-pour&pli1*plp2*p-vsvg(以下简称gfp组)10板,空白对照1板。共收获两种病毒上清液各100ml,经peg8000浓缩后得到病毒浓缩液各300ul,一部分用于感染cd8t细胞,一部分分装后并标注冻存于-80℃。浓缩前后的病毒滴度由感染293t细胞测定。此部分数据包括四质粒共转染293t细胞的感染率、病毒滴度测定。检测得到携带目的基因的穿梭载体对293t细胞的转染率每板均能达到90%以上,四质粒转染293t细胞基本符合病毒包装前提,如图3所示。对病毒浓缩前后的滴度测定得到,病毒原液的滴度大概在2*106t,浓缩后病毒的滴度约为500*106t。病毒滴度提高了250倍,病毒损失率达到25%。不同梯度病毒对293t细胞的感染率如图4所示。图4为梯度稀释病毒浓缩液后对293t细胞的感染。图中以未感染病毒组293t细胞为对照,各稀释倍数下感染后96h的gfp的荧光检测结果。6.fcr-car-t细胞的制备1)抗体包被:将24孔板用1ug/mlanticd3和5ug/mlanticd28包被待用(macs细胞激活试剂与cd8细胞液体积比1:17.5混合均匀)。2)将分离得到的cd8细胞在预包被的细胞板中培养,过程中添加30u/ml的il-2,每孔中0.5×106细胞/0.5mlprmi+10%fbs培养基。3)移入5%c02,37度培养箱中培养,激活24h左右,观察细胞激活状态,当发现细胞呈聚团状态明显时添加病毒液。4)病毒在冰上复苏,按moi=20在t细胞培养液中滴加病毒浓缩液,添加后勿吹打。5)24-48左右感染后,更换细胞完全培养基,il-2为60u/ml,il-7为30u/ml。6)观察细胞培养状态,添加或更换细胞完全培养基,感染t细胞5天左右后,可利用流式细胞仪检测t细胞表面car的表达。设置阴性对照和同型对照。7)继续培养cart细胞,观察细胞培养状态。在细胞培养第14天左右时收集细胞,对细胞进行转染率检测。gfp单染t细胞,gfp的表达相当于car分子的转染率。7.fcr-car-t细胞与肿瘤抗体合用的结果:上述实例9.微球egfr经四次免疫最后一周取血于elisa抗体滴度测定。(1)car-t细胞以1:2比例稀释于96孔板,加入靶细胞a549使效靶比为2.5:1,5.0:1,10.0:1,20.0:1;(2)car-t细胞以1:2比例稀释于96孔板,先加入1:10000稀释的egfr抗血清,室温培育60分钟,然后加入靶细胞a549使效靶比为2.5:1,5.0:1,10.0:1,20.0:1;酶标仪450nm测试(cck8kit),读取各效靶比光密度值/孔。fcr-car-t细胞杀伤靶细胞a549fcr-car-t细胞与肿瘤抗体合用杀伤靶细胞a549序列表<110>上海微球生物科技有限公司<120>充分多样的双亲性mhcii结合多肽、免疫载体微球及其制备方法和应用<130>aj191961<150>2018101514763<151>2018-02-14<160>24<170>siposequencelisting1.0<210>1<211>16<212>prt<213>人工序列(artificialsequence)<400>1glntyrilelysalaasnserlyspheileglyilethrgluleuasp151015<210>2<211>15<212>prt<213>人工序列(artificialsequence)<400>2ileserglnalavalhisalaalahisalagluileasngluala151015<210>3<211>29<212>prt<213>人工序列(artificialsequence)<400>3alaalaalaalaglyglycysglntyrilelysalaasnserlysphe151015ileglyilethrgluleuaspargasplysglnlyslys2025<210>4<211>30<212>prt<213>人工序列(artificialsequence)<400>4alaalaalaalaglyglyglyglycysileserglnalavalhisala151015alahisalagluileasnglualaglnlysaspargasplys202530<210>5<211>15<212>prt<213>人工序列(artificialsequence)<400>5ilethrasptyrmettyrleuthrasnalaprosertyrthrasn151015<210>6<211>15<212>prt<213>人工序列(artificialsequence)<400>6aspleuvallyspheileserasplysilelyspheleuasnpro151015<210>7<211>15<212>prt<213>人工序列(artificialsequence)<400>7leuleualailealaglyileargleuhisargalaalailetyr151015<210>8<211>15<212>prt<213>人工序列(artificialsequence)<400>8asniletyrtyrargargleutyrasnglyleulyspheileile151015<210>9<211>15<212>prt<213>人工序列(artificialsequence)<400>9pheasnasnphethrvalserphetrpleuargvalprolysval151015<210>10<211>15<212>prt<213>人工序列(artificialsequence)<400>10lysleutyrthrsertyrleuserilethrpheleuargaspphe151015<210>11<211>15<212>prt<213>人工序列(artificialsequence)<400>11lysthrglnleuvalaspasppheleuaspleuaspmetalaile151015<210>12<211>15<212>prt<213>人工序列(artificialsequence)<400>12tyrileasnglyvalleumetglyseralagluilethrglyleu151015<210>13<211>15<212>prt<213>人工序列(artificialsequence)<400>13serleuasnpheleuglyglyalaprovalcysproglyglnasn151015<210>14<211>15<212>prt<213>人工序列(artificialsequence)<400>14asptyraspglntyrcysalaaspvalalaalaglugluleumet151015<210>15<211>28<212>prt<213>人工序列(artificialsequence)<400>15glytyrglytyrglncysilevalasphisproasppheprolyspro151015ilevalargserilethrlysthrproglyglnarg2025<210>16<211>13<212>prt<213>人工序列(artificialsequence)<400>16ileserilesergluilelysglyvalilevalhislys1510<210>17<211>15<212>prt<213>人工序列(artificialsequence)<400>17ileserglnalavalhisalaalahisalagluileasngluala151015<210>18<211>25<212>prt<213>人工序列(artificialsequence)<400>18alaalaalaalaglyglyglycysileserilesergluilelysgly151015valilevalhislysasplysglnlys2025<210>19<211>27<212>prt<213>人工序列(artificialsequence)<400>19alaalaalaalaglyglyglycysileserglnalavalhisalaala151015hisalagluileasnglualalysglnarglys2025<210>20<211>16<212>prt<213>人工序列(artificialsequence)<400>20pheglypheprogluhisleuleuvalasppheleuglnserleuser151015<210>21<211>14<212>prt<213>人工序列(artificialsequence)<400>21leugluglulyslysalaasntyrvalvalthrasphiscys1510<210>22<211>22<212>prt<213>人工序列(artificialsequence)<400>22cysseralaproaspthrargthrproalaproglyserthralapro151015proalahisglyvalthr20<210>23<211>1337<212>dna<213>人工序列(artificialsequence)<400>23gctagcgccaccatgtggcagctgctgctgcccaccgccctggtgctgaccgccttcagc60ggcatccaggccggcctgcagaaggccgtggtgaacctggaccccaagtgggtgagagtg120ctggaggaggacagcgtgaccctgagatgccagggcaccttcagccccgaggacaacagc180atcaagtggttccacaacgagagcctgatcccccaccaggacgccaactacgtgatccag240agcgccagagtgaaggacagcggcatgtacagatgccagaccgccctgagcaccatcagc300gaccccgtgcagctggaggtgcacatgggctggctgctgctgcagaccaccaagtggctg360ttccaggagggcgaccccatccacctgagatgccacagctggcagaacagacccgtgaga420aaggtgacctacctgcagaacggcaagggcaagaagtacttccacgagaacagcgagctg480cccatccccaaggccacccacaacgacagcggcagctacttctgcagaggcctgatcggc540cacaacaacaagagcagcgccagcttcagaatcagcctgggcgaccccggcagccccagc600atgttccccccctggcacagccccaagctgttctgggccctggtggtggtggccggcgtg660ctgttctgctacggcctgctggtgaccgtggccctgtgcgtgatctggaccaacagcaga720agaaacagactgctgcagagcgactacatgaacatgacccccagaagacccggcctgacc780agaaagccctaccagccctacgcccccgccagagacttcgccgcctacagacccggcggc840ggcaagtggatcagaaagaagttcccccacatcttcaagcagcccttcaagaagaccacc900ggcgccgcccaggaggaggacgcctgcagctgcagatgcccccaggaggaggagggcggc960ggcggcggctacgagctgggcggcggcagagccaagttcagcagaagcgccgagaccgcc1020gccaacctgcaggaccccaaccagctgtacaacgagctgaacctgggcagaagagaggag1080tacgacgtgctggagaagaagagagccagagaccccgagatgggcggcaagcagcagaga1140agaagaaacccccaggagggcgtgtacaacgccctgcagaaggacaagatggccgaggcc1200tacagcgagatcggcaccaagggcgagagaagaagaggcaagggccacgacggcctgtac1260cagggcctgagcaccgccaccaaggacacctacgacgccctgcacatgcagaccctggcc1320cccagatgagcggccgc1337<210>24<211>1340<212>dna<213>人工序列(artificialsequence)<400>24gctagcgccaccatgtggcagctgctgctgcccaccgccctgctgctgctggtgagcgcc60ggcatgagaaccgaggacctgcccaaggccgtggtgttcctggagccccagtggtacagc120gtgctggagaaggacagcgtgaccctgaagtgccagggcgcctacagccccgaggacaac180agcacccagtggttccacaacgagagcctgatcagcagccaggccagcagctacttcatc240gacgccgccaccgtgaacgacagcggcgagtacagatgccagaccaacctgagcaccctg300agcgaccccgtgcagctggaggtgcacatcggctggctgctgctgcaggcccccagatgg360gtgttcaaggaggaggaccccatccacctgagatgccacagctggaagaacaccgccctg420cacaaggtgacctacctgcagaacggcaaggacagaaagtacttccaccacaacagcgac480ttccacatccccaaggccaccctgaaggacagcggcagctacttctgcagaggcctggtg540ggcagcaagaacgtgagcagcgagaccgtgaacatcaccatcacccagggcctggccgtg600agcaccatcagcagcttcagcccccccggcagcagaaagcccttctgggtgctggtggtg660gtgggcggcgtgctggcctgctacagcctgctggtgaccgtggccttcatcatcttctgg720gtgagaagcaagagaagcagactgctgcacagcgactacatgaacatgacccccagaaga780cccggccccaccagaaagcactaccagccctacgccccccccagagacttcgccgcctac840agaagcggcggcggcaagagaggcagaaagaagctgctgtacatcttcaagcagcccttc900atgagacccgtgcagaccacccaggaggaggacggctgcagctgcagattccccgaggag960gaggagggcggctgcgagctgggcggcggcagagtgaagttcagcagaagcgccgacgcc1020cccgcctaccagcagggccagaaccagctgtacaacgagctgaacctgggcagaagagag1080gagtacgacgtgctggacaagagaagaggcagagaccccgagatgggcggcaagccccag1140agaagaaagaacccccaggagggcctgtacaacgagctgcagaaggacaagatggccgag1200gcctacagcgagatcggcatgaagggcgagagaagaagaggcaagggccacgacggcctg1260taccagggcctgagcaccgccaccaaggacacctacgacgccctgcacatgcaggccctg1320ccccccagatgagcggccgc1340当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1