用于肿瘤早期诊断及治疗的复合纳米材料及制备方法与流程
本发明属于生物医药领域,具体是指一种用于肿瘤早期诊断及治疗的复合纳米材料及制备方法。
背景技术:
目前,降低癌症死亡率最有效的方法是早期筛查和诊断。常规的早期诊断方法包括ct检查、x光检查等,但此类方法大多存在特异性和灵敏度低等缺点。近些年来,基于荧光纳米材料的早期诊断受到人们的广泛关注,如:量子点(qd)、有机染料、金纳米簇(auncs)。其中,量子点具有生物毒性,且制备过程复杂;有机染料的荧光产率低(0.5%~1.0%),且容易发生光漂白产生荧光淬灭现象。相较于量子点和有机染料,金纳米簇不仅合成方法简单、粒径小、生物相容性好,而且具有尺寸依赖且可调的荧光、更高的量子产率(10%-70%)、较强的抗漂白能力,可作为荧光成像材料指导早期诊断。此外,由于单一成像模式不能为早期诊断提供全面的信息,将多种成像技术结合在一起的多模式成像可以有效地弥补单一成像在早期诊断中存在的弊端。因此,多模式成像已经引起了临床医学和生物医学的广泛关注。
近几年,光热治疗已发展成为治疗多种类型实体肿瘤的新方法。光热治疗的主要优点有:1)微创;2)近红外发射光产生的较深组织穿透力;3)肿瘤特异性;4)减小的组织毒性;5)光照可通过在病灶部位的聚集辐射进行时空控制。具有近红外(nir)光吸收的不同纳米粒子,如贵金属纳米材料、半导体、碳复合物以及有机纳米粒子都可用于光热治疗(ptt)。其中,bi2s3nps具有价廉、窄带隙(≈1.3ev)、x衰减系数大、低毒等优点,不仅展现出很强的nir吸收能力和光热转换能力,而且被开发作为一种新型的ct造影剂,可用于ct成像指导的早期诊断。
技术实现要素:
针对现有技术的不足,本发明的目的在于提供一种用于肿瘤早期诊断及治疗的复合纳米材料及制备方法。
为实现上述目的,本发明提供的用于肿瘤早期诊断及光热治疗的纳米复合材料,其特征在于:该纳米复合材料包括硫化铋纳米粒子(bi2s3nps)及金纳米簇(auncs)两种纳米材料,该纳米复合材料通过以下方法制得而成:以bsa作为稳定剂,首先合成bi2s3nps,之后经过透析去除溶液中多余的反应物,再加入氯金酸,得到最终产物。
本发明另一方面还提供了一种用于肿瘤早期诊断及光热治疗的纳米复合材料的制备方法,主要内容如下:
(1)bi2s3nps的制备:取250mgbsa加入至8.0ml纯水中,超声使其完全溶解;将1.0mgbi(no3)3·5h2o溶于1.0ml2mhno3中;将配制的硝酸-硝酸铋溶液加入至bsa溶液中,在25℃下搅拌30min;使用2mnaoh调溶液ph至12,在25℃下反应12h;反应完成后,使用截留分子量为8000-14000的透析袋对bsa@bi2s3nps进行透析,透析外液为超纯水,每2h换一次超纯水,总透析时间为12h,得到bi2s3nps纳米粒子。
(2)bi2s3-auncs纳米复合材料的制备:
首先,计算haucl4的加入体积。设透析后bsa@bi2s3nps中bsa的浓度为c1,氯金酸的加入体积为v2,在制备bsa@auncs时,bsa的浓度为25mg/ml,加入的10mmhaucl4体积为5ml,若加入的haucl4浓度为50mm,折算体积为1ml;使用下列公式计算v2:
其中,
然后,在37℃快速搅拌条件下,加入一定体积(根据上述公式计算)的50mmhaucl4,2min后,使用2m氢氧化钠溶液调ph至12;37℃的条件下搅拌12h;所得样品在10000r/min离心速度下离心3次,每次20min,即制得最终产物bi2s3-auncs纳米复合材料。
本发明即一种基于硫化铋-金纳米簇的可用于肿瘤早期诊断及治疗的纳米复合材料及制备方法,是基于bi2s3nps与auncs的各自优势,使用bsa作为稳定剂和还原剂,制备得到硫化铋-金纳米簇(bi2s3-auncs)纳米复合材料。但由于bi2s3nps对auncs的荧光具有淬灭效应,如何优化硫化铋与金纳米簇之间的配比以实现该纳米复合材料的荧光/ct成像指导下的光热治疗,是我们需要解决的重要难题。针对该问题,我们建设性地提出在bi2s3nps透析完成后,计算所需haucl4的体积。
该材料制备原理如下:bsa含有的丰富氨基酸,bi离子和au离子都可以与bsa中的氨基酸功能基团,如:-sh,-nh3,-cooh等相结合,在酸性条件下分别形成bsa-bi3+,bsa-au3+复合物;由于bsa具有很强的还原能力,因此通过将ph调节至碱性(≈12),可以将bi离子和au离子原位还原为bi原子和au原子,从而形成bi2s3nps以及auncs相结合的复合纳米材料。
在性能考察方面,首先,bi2s3nps不仅具有较好的光热转换能力,还具有ct成像的能力;其次,金纳米簇发出的红色荧光可用于荧光成像指导的早期诊断。bi2s3与auncs结合不仅可以实现荧光-ct双模式成像指导的光热治疗,而且,auncs与bi2s3可以达到协同增强光热治疗的作用。
综上所述,本发明具有如下优点和有益效果:
(1)硫化铋不仅具有较好的光热转换能力,能够通过光引发产生热量,从而杀死癌细胞,而且具有ct成像能力;
(2)金纳米簇作为一种能够发出强烈红色荧光的贵金属纳米材料,具有很好的荧光成像能力,可用于肿瘤的早期诊断。
(3)该复合纳米材料既具有硫化铋的光热性质和ct成像能力,还具有金纳米簇的荧光成像能力,可实现荧光-ct双模式成像指导的光热治疗,以及协同光热治疗效果。
本发明所制备的bi2s3-auncs纳米复合材料具有以下优点:1)制备过程简单,合成时间短;2)使用bsa作为稳定剂,材料的生物相容性好;3)反应在水相中进行,材料稳定性强;4)该纳米复合材料荧光较强无漂白现象;5)低毒性。
本发明中制备的新型复合纳米材料,即bi2s3-auncs,首次将双模式成像指导的早期诊断与光热治疗相结合,既可以实现荧光与ct的双模式成像,又能在短时间内对病灶部位进行高效的光热治疗,大大提高病人的治愈率。相较于大部分的多功能治疗型纳米材料,该纳米复合物集多种成像指导的早期检测与治疗于一体,为今后开辟纳米材料的生物应用领域提供了新的思路。
附图说明
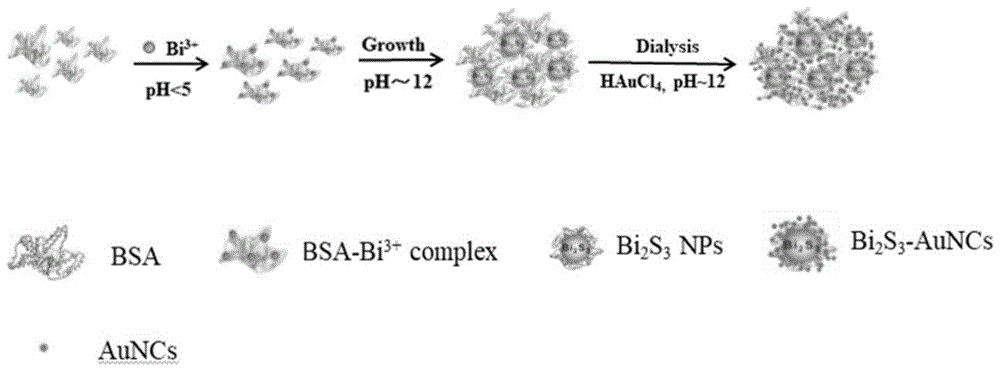
图1是本发明bi2s3-auncs复合物纳米粒子合成示意图;
图2是本发明bi2s3-auncs溶液的荧光发射图谱;
图3是本发明bi2s3-auncs溶液的紫外吸收图谱;
图4是本发明bi2s3-auncs溶液的粒径分布图;
图5是本发明bbi2s3-auncs溶液的电位图;
图6是本发明bi2s3-auncs溶液的光热升温曲线(808nm,1.5w/cm2)。
具体实施方式
以下结合附图和具体实施例对本发明进行进一步详细说明。
本发明的bi2s3-auncs纳米复合材料,包括bi2s3nps与auncs两种材料,。利用bsa中含有的大量氨基酸,bi3+和au3+均可以与氨基酸功能基团,如:-sh,-nh3,-cooh等,相结合,。形成bsa-bi3+,bsa-au3+;通过将ph调节至碱性(~12),bsa表现出很强的还原能力,可以将bi3+和au3+原位还原为bi原子和au原子,从而形成bi2s3nps以及auncs。合成的复合纳米材料不仅可以实现荧光-ct双模式成像指导的光热治疗,bi2s3与auncs还可达到协同光热治疗的作用。
本发明制备方法的具体过程如下:
利用牛血清白蛋白(bsa)作为原料,制备bi2s3nps;透析除去多余的小分子物质;之后加入haucl4,制备bi2s3-auncs;再次透析除去多余的离子等物质;最后离心取沉淀。所述的bi2s3-auncs复合物制备方法的具体步骤如下:
1、bi2s3nps的制备
取240mgbsa加入至8.0ml纯水中,超声使其完全溶解。将1.0mgbi(no3)3·5h2o溶于1.0mlhno3(2m)中。将配制的硝酸-硝酸铋溶液加入至bsa溶液中,在25℃下搅拌混合30min。使用2m的naoh溶液(1ml)调ph至12,最后溶液需在25℃下反应12h。
2、bi2s3nps的制备
取250mgbsa溶于8.0ml纯水中,超声溶解。将1.5mgbi(no3)3·5h2o溶于1.0mlhno3(2m)中。将配制的硝酸-硝酸铋溶液加入至bsa溶液中,在室温下搅拌。30min后,使用2m的naoh溶液调ph至12,最后溶液需在25℃下反应12h。
3、取250mgbsa溶于8.0ml纯水中,超声溶解。将2.0mgbi(no3)3·5h2o溶于1.0mlhno3(2m)中。将配制的硝酸-硝酸铋溶液加入至bsa溶液中,在室温下搅拌。30min后,使用2m的naoh溶液调ph至12,最后溶液需在25℃下反应12h。
4、后处理(离心)
反应完成的溶液进行离心处理。3次离心均为10000r/min,25min,每次离心后分离沉淀与上清,第1次和第2次离心后的上清各进入下一步离心;沉淀使用400μl纯水稀释,检测荧光光谱与粒径。最后离心的上清保留下来。
5、bi2s3nps和bi2s3-auncs的光热效应
取浓度分别为0.175mg/ml,体积为1ml的bi2s3nps或bi2s3-auncs水溶液,使用功率为1.5w/cm2的808nm激光照射10min,每30s记录一次温度(10min内)。绘制bi2s3nps或bi2s3-auncs温度-时间的升温曲线。
- 还没有人留言评论。精彩留言会获得点赞!