一种小分子化合物在抗非洲猪瘟病毒感染中的新应用的制作方法
本发明涉及一种小分子化合物在抗非洲猪瘟病毒感染中的新应用,属于医药技术领域。
背景技术:
非洲猪瘟(africanswinefever,asf)是一种由非洲猪瘟病毒(africanswinefevervirus,asfv)感染引发的猪的广泛出血性、接触性传染病。该病毒以野猪、家猪和部分软蜱为宿主和传播媒介,并主要感染家猪及野猪,引发的病死率可高达100%。自1921年首次暴发于肯尼亚以来,非洲猪瘟疫情持续传播,并于20世纪中叶侵入西非、西欧、加勒比、巴西、外高加索、东欧等地。2018年8月,非洲猪瘟疫情在我国辽宁省沈阳市首次发生,并逐步蔓延至31个省份,造成直接经济损失达数百亿元,对我国养猪业带来了空前的危机。如疫情不能得到及时有效的控制,将极大地影响我国的肉类产量、影响人们的生活。然而,目前尚无商品化疫苗、药物及可靠的治疗方法。
asfv属于非洲猪瘟相关病毒科(asfarviridae)非洲猪瘟病毒属(asfivirus),是一种有囊膜的双链dna病毒。asfv的基因组长度约为170-193kbp,共编码约150-167种病毒蛋白。在asfv编码的众多病毒蛋白中,我们关注一个组蛋白样蛋白——pa104r。pa104r由104个氨基酸组成,具有核酸结合能力。研究表明,pa104r与asfv编码的ii型拓扑异构酶pp1192r同时作用,能够介导asfv的核酸形成超螺旋结构。这种超螺旋结构缩小了病毒核酸的体积,有助于病毒核酸被包装进入新生成的子代病毒中,因而在病毒的复制过程中至关重要。已有研究表明,在细胞水平降低pa104r的表达量,能够有效地抑制asfv的复制,并降低病毒滴度。因此该蛋白可以作为抗病毒药物的靶点,用于抗asfv药物的研发中。本发明的目的是以pa104r为靶点,筛选具有抗asfv作用的小分子化合物,并提供一种有效地治疗和预防非洲猪瘟的药物。
技术实现要素:
本发明的第一个目的是提供化合物或其盐在制备预防或治疗非洲猪瘟的药物中的应用;所述化合物的结构式为
所述疏水基团包括下述任一种:(c1-c6)烷基、(c3-c6)环烷基、苯基、萘基,或在环上经r5取代的(c5-c6)环烷基,或邻位、间位或对位经r5取代的苯基
所述供电子基团是提供π电子的基团,包括但不限于羟基(“-oh”)、(c1-c6)烷氧基(“-or”)、羰基(“c(o)-”)、羧基、羰(c1-c6)烷氧基(“-co2r”)、碳酸酯基(“-oco2r”)、氨基(“-nh2”)、(c1-c6)烷基氨基(“-nhr”)、二(c1-c6)烷基氨基(“-nr2”)、(c2-c6)烯基氨基、二(c2-c6)烯基氨基、(c2-c6)炔基氨基、硫醚(“-sr”)、磺酸基、膦基(“ph2”)、(c1-c6)烷基膦基(“-phr”)、磷酸基、乙烯基(“c=c”)、乙炔基(“c≡c”)、吡啶基、苯基、氨基苯基、羟苯基、(c1-c6)烷基苯基、二(c1-c6)烷基苯基、(c1-c6)烷基苯酚、联苯基和联吡啶基。
在一种实施方式中,供电子基团选自羧基、磷酸基或磺酸基。
在一种实施方式中,所述化合物的结构式为
在一种实施方式中,所述非洲猪瘟包括但不限于由asfvchina/2018/anhuixcgq病毒株,或同源性与其≥85%且具备病毒活性的非洲猪瘟病毒引起的疾病。
本发明的第二个目的是提供一种药物组合物,含有结构式如
在一种实施方式中,所述药物组合物还含有药学上可接受的载体。
在一种实施方式中,所述药物组合物的剂型为片剂、胶囊、颗粒剂、散剂、糖浆剂、口服液或注射剂。
在一种实施方式中,所述药学上可以接受的载体包括一种或多种固体、半固体或液体辅料。
本发明的第三个目的是提供一种猪瘟病毒抑制剂,含有≥3μm的化合物
本发明的优点和效果:
本发明发现了两种抗asfv感染的小分子化合物
附图说明
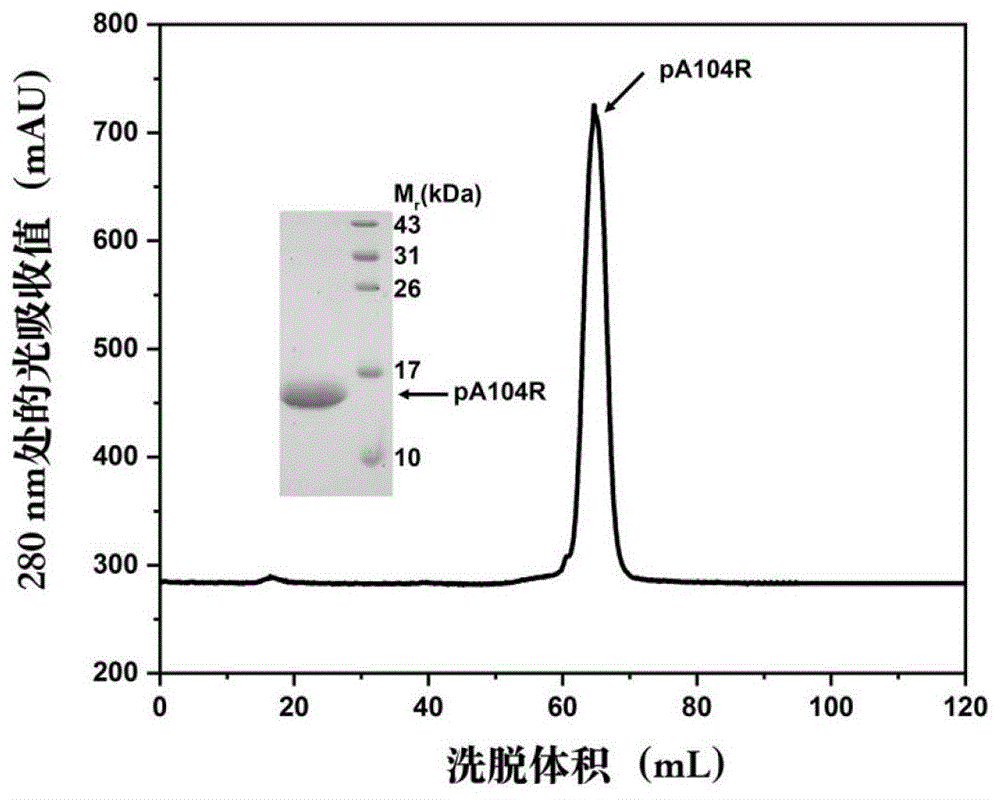
图1为asfv-pa104r蛋白纯化分子筛与sds-page结果;
图2为化合物hw2019001(a)和化合物hw2019002(b)的结构式;
图3为化合物hw2019001(a)和化合物hw2019002(b)阻断asfv-pa104r与dna结合的模式图;
图4为emsa法验证hw2019001和hw2019002阻断asfv-pa104r与dna的结合;
图5为hw2019001和hw2019002对pam细胞的毒性实验结果;
图6为hw2019001(a)和hw2019002(b)对asfv在pam细胞中复制的抑制效果。
具体实施方式
实施例1:asfv-pa104r蛋白的表达和纯化
asfvchina/2018/anhuixcgq病毒株pa104r蛋白的全长dna序列(genbank:ayw34006.1)通过限制性酶切位点ndei和xhoi连接到pet21a载体上。其中asfv-pa104r蛋白编码区的5’端加入了6个组氨酸标签(his6-tag)的编码序列,3’端加入了翻译终止密码子。构建好asfv-pa104r表达载体转化bl21大肠杆菌感受态细胞。单克隆接种到40mllb培养基中,培养12小时后转接到4l的lb培养基中,37℃培养至od600=0.6-0.8,加入iptg至终浓度0.2mm,16℃继续培养12小时。表达后将菌体收集,用蛋白缓冲液(10mmhepes,500mmnacl,ph7.4)重悬后超声破碎菌体,并获得可溶形式的pa104r蛋白。pa104r蛋白经镍离子亲和层析(histraptmhp(ge))和凝胶过滤层析(hiload16/60superdex75pg(ge))纯化后,通过sds-page鉴定蛋白纯度。如图1所示,经鉴定,可获得高纯度pa104r蛋白,大小约为14kda。
实施例2:hw2019001和hw2019002阻断asfv-pa104r结合dna的原理和阻断能力验证
将实施例1中纯化后的asfv-pa104r蛋白经蛋白质晶体学手段结晶,解析其高分辨率蛋白结构。通过软件autodockvina模拟表明,hw2019001或hw2019002(结构式如图2所示)能够结合于asfv-pa104r的结合槽底部。对复合物结构的分析表明,当hw2019001和hw2019002结合于由asfv-pa104r的氨基酸lys95、lys98、arg100和his106构成的dna结合槽底部时,能够通过空间位阻阻挡dna与asfv-pa104r互作,结果见图3。
合成5’端fam标记的30ntdna序列(30nt-f-fam),并与其未标记的互补链(30nt-r)在95℃条件下变性5分钟,而后梯度退火至室温,用以形成30bp的双链dna片段。dna序列见表1。取0.4μm实施例1中纯化好的asfv-pa104r蛋白与1μmfam标记的双链dna室温孵育30分钟,而后加入梯度稀释的不同浓度hw2019001或hw2019002,并于室温孵育30分钟,两种化合物的终浓度如图4所示。两种化合物购买于chembridge公司(货号分别为:5102751和5102836)。
孵育后的样品经native-page检测,结果见图4。emsa的结果表明,hw2019001和hw2019002都能在分子水平上阻断asfv-pa104r与dna的结合,其ic50分别为275μm和6.1μm。
表1.30ntdna序列
实施例3:hw2019001和hw2019002对pam细胞的毒性实验
细胞的毒性实验的目的是确定两个小分子是否对猪肺泡巨噬细胞(pam细胞)有细胞毒性,并确定其无毒性的最高剂量,以便为细胞水平的病毒抑制实验提供药物剂量参考。
将5×104个pam细胞接种于96孔细胞培养板中,37℃培养16小时。弃去培养基,每孔加入100μl用梯度稀释的hw2019001或hw2019002,浓度分别为1000μm、250μm、50μm、10μm、2μm、0.5μm、0.1μm、0.02μm、0.004μm,稀释液为含2%小牛血清的1640培养基,每个稀释度做3个重复孔。由于hw2019001和hw2019002溶解于dmso溶液中,因此同时用相同比例稀释的dmso溶液作为对照组。37℃培养48小时后,弃培养基,pbs溶液洗两次,加入100μl事先配制好的cck-8溶液(每100μl1640培养基加入10μlcck-8试剂)。将培养板在培养箱中孵育2小时,而后使用酶标仪测量450nm处的吸光度,结果见图5。
结果表明,hw2019001的给药量为10μm及以下时,给药48小时对pam细胞无细胞毒性。当hw2019001的给药量增加至50μm时,细胞存活率约为87%。由溶剂dmso的毒性数据可知,相同稀释度时dmso组的细胞存活率与hw2019001相似,约为84%。因此,hw2019001给药量为50μm时的细胞毒性主要来自于溶剂dmso,而非hw2019001本身。相比而言,hw2019002具有更低的细胞毒性,给药量为50μm及以下时,给药48小时对pam细胞无细胞毒性。因此,我们选用50μm作为最高的无毒剂量,用于病毒抑制实验。
实施例4:细胞水平上检测hw2019001和hw2019002对asfv感染的抑制能力
将5×105个pam细胞接种于24孔细胞培养板中,37℃培养16小时。将asfv病毒用1640培养基稀释至moi为0.5,加入到弃去培养基的pam细胞培养板中,37℃感染1小时。感染后弃掉病毒液,pam细胞用pbs洗一次以去掉残留的病毒。向pam细胞培养板中加入梯度稀释的hw2019001或hw2019002,浓度分别为50μm、5μm、0.5μm、0.05μm、0.005μm、0.0005μm、0,稀释液为含2%小牛血清的1640培养基。由于hw2019001和hw2019002溶解与dmso溶液中,因此本实验同时用dmso溶液作为对照组。37℃培养48小时后收集细胞上清,用试剂盒提取上清中病毒基因组dna,而后用荧光定量pcr法对上清中的病毒拷贝数进行绝对定量,其中检测的目标基因为asfv-vp72,引物和探针序列为见表2。
表2.引物探针序列
图6的结果表明,随着给药量的逐渐增加,两种化合物对asfv在pam细胞中的复制呈现出明显的抑制作用,其ic50值分别为2.93μm和0.45μm。当给药量为pam细胞最高无毒剂量50μm时,hw2019001和hw2019002能够将病毒的核酸拷贝数降低至对照组的22%和5%,其对病毒的抑制率分别为78%和95%。
实施例5
在实施例2的基础上,通过大量的化合物-蛋白复合物的结构拟合,发现具有
虽然本发明已以较佳实施例公开如上,但其并非用以限定本发明,任何熟悉此技术的人,在不脱离本发明的精神和范围内,都可做各种的改动与修饰,因此本发明的保护范围应该以权利要求书所界定的为准。
sequencelisting
<110>中国科学院微生物研究所
<120>一种小分子化合物在抗非洲猪瘟病毒感染中的新应用
<160>5
<170>patentinversion3.3
<210>1
<211>30
<212>dna
<213>人工序列
<400>1
ccaacttccctaacccagctgcgatccgta30
<210>2
<211>30
<212>dna
<213>人工序列
<400>2
tacggatcgcagctgggttagggaagttgg30
<210>3
<211>25
<212>dna
<213>人工序列
<400>3
ctgctcatggtatcaatcttatcga25
<210>4
<211>21
<212>dna
<213>人工序列
<400>4
gataccacaagatcaggccgt21
<210>5
<211>25
<212>dna
<213>人工序列
<400>5
ccacgggaggaataccaacccagtg25
- 还没有人留言评论。精彩留言会获得点赞!