C27H27N7O2S在制备抑制器官异体移植排斥药剂中的应用的制作方法
本发明涉及生物医药技术领域。更具体地,涉及c27h27n7o2s在制备抑制器官异体移植排斥药剂中的应用。
背景技术:
器官移植是目前治疗终末期器官功能丧失或衰竭最为理想的手段,但器官受者免疫系统往往产生针对外来移植物的排斥反应。同种异体移植抗原活化t细胞后引发的细胞免疫反应在急性排斥反应发生发展过程中起主导作用。比如在皮肤和心脏移植模型中,t细胞大量活化是引发免疫排斥的主要原因。所以为了提高器官移植的成功率,临床上常在手术前后使用免疫抑制剂,降低免疫系统活性,提高器官接受体的存活率。
fk506为临床最常使用的免疫抑制剂,通过抑制calcineurin的磷酸酶的功能,阻断t淋巴细胞活化信号传递,从而影响il-2的转录以及分泌。不过,临床数据显示长期使用免疫抑制剂的患者产生较大的毒副作用,比如肝肾毒性强及过敏等不良反应。基于临床上有多种作用于不同机制的免疫抑制药剂可以选择,目前的免疫抑制剂的使用倾向于多种药剂的联合应用,不仅可达到目标疗效,且可避免使用单一药剂所引起的副作用。因而研发新的针对器官移植排斥的药剂,尤其是心脏异体移植排斥药剂就显得尤为重要。
技术实现要素:
本发明为了解决上述现有技术的缺陷和不足,提供c27h27n7o2s在制备抑制器官异体移植排斥药剂中的应用。
本发明的上述目的是通过以下技术方案给予实现的:
c27h27n7o2s,2-(4-甲基-1,4-二氮杂基-1-基)-n-[(5-甲基吡嗪-2-基)甲基]-5-氧代-[1,3]苯并噻唑[3,2-a][1,8]萘啶-6-甲酰胺,其化学结构式如式(i)所示:
本发明从动物水平研究发现,c27h27n7o2s药剂处理小鼠后能明显推迟小鼠的心脏异体移植排斥反应;进一步通过检测基因表达水平变化,发现c27h27n7o2s能抑制nzymeb、tnf-α及il-12细胞因子的表达。
因此本发明首先请求保护所述c27h27n7o2s在制备抑制器官异体移植排斥药剂中的应用,或在抑制器官异体移植排斥反应中的应用。
优选地,所述c27h27n7o2s的用量为2.0~3.0mg·kg-1(优选2.0mg·kg-1)。
本发明还提供一种抑制器官异体移植排斥反应的药剂,所述药剂含有c27h27n7o2s。
优选地,所述药剂为片剂、胶囊剂、散剂、口服液、软胶囊、丸剂、酊剂、糖浆剂、栓剂或注射剂。
与现有技术相比,本发明具有以下有益效果:
本发明从动物水平研究发现,c27h27n7o2s药剂处理小鼠后能明显推迟小鼠心脏异体移植排斥反应;进一步检测基因表达水平变化,发现c27h27n7o2s能抑制nzymeb、tnf-α及il-12细胞因子的表达,表明c27h27n7o2s可用来制备抑制器官异体移植排斥反应药剂;本发明提供了c27h27n7o2s在制备抑制器官异体移植排斥药剂中的新用途,提供了一种新的高效安全的针对器官移植排斥的药剂。
附图说明
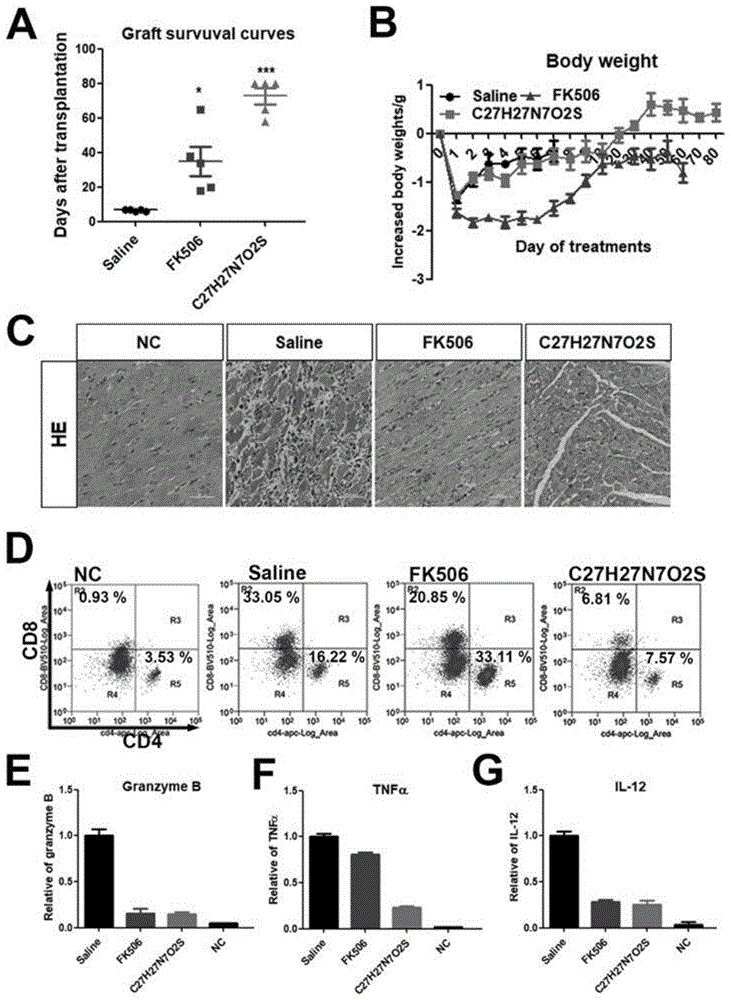
图1是在动物实验水平上检测c27h27n7o2s对心脏异体移植排斥的影响。
图1a中为心脏移植排斥评分(graftrejectionscore),依序为对照组(saline)、fk506药量为2.0mg·kg-1、c27h27n7o2s药量为2.0mg·kg-1。
图1b中为心脏移植中各组别处理后体重的变化,依序为对照组(saline)、fk506药量为2.0mg·kg-1、c27h27n7o2s药量为2.0mg·kg-1。
图1c为心脏病理切片,由左至右依序为对照组(saline)、fk506药量为2.0mg·kg-1、c27h27n7o2s药量为2.0mg·kg-1。
图1d为移植物心脏的cd4/cd8比例,由左至右依序为对照组(saline)、fk506药量为2.0mg·kg-1、c27h27n7o2s药量为2.0mg·kg-1。
图1e、f和g为实时定量pcr检测小鼠心脏移植后的granzymeb、tnf-α、il-12表达情况。由左至右依序为对照组(saline)、fk506药量为2.0mg·kg-1、c27h27n7o2s药量为2.0mg·kg-1。
具体实施方式
以下结合说明书附图和具体实施例来进一步说明本发明,但实施例并不对本发明做任何形式的限定。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。
除非特别说明,以下实施例所用试剂和材料均为市购。
实施例1c27h27n7o2s在动物实验水平上推迟心脏异体移植排斥的发生
1、小鼠心脏移植实验
(1)小鼠心脏移植模型建立
实验室用8~10周龄c57bl/6及c57bl/6购于中山大学动物中心,并饲养在中山大学动物中心的饲养室。balb/c小鼠c57bl/6小鼠经10%戊巴比妥钠麻醉后,将balb/c小鼠心脏取出接在将c57bl/6的颈动脉及静脉位置。小鼠分为4组,每组5只。
(2)药剂配制及给药
移植计为第0天,移植当天开始给药,给药方式采用腹腔注射,每天注射1次,连续注射直到移植心脏停跳,将c27h27n7o2s注射液根据给药剂量用生理盐水进行稀释。注射组别分为:空白对照组注射生理盐水;fk506药量为2.0mg·kg-1、c27h27n7o2s药量为2.0mg·kg-1。
(3)移植物存活情况
当心脏移植排斥发生时,其移植物的心脏将跳动减弱或停跳,通过肉眼观察及触摸来观察及记录其移植物心脏的存活情况。
(4)病理组织学检查
将移植皮肤取下,用4%的甲醛固定,石蜡包埋、切片、he染色后进行病理切片观察。与皮肤移植排斥评分方法一致,将移植皮肤坏死情况进行病理学评分。
(5)脾脏的granzymeb、tnf-α及il-12表达的测定
将小鼠于第七天处死,取出脾脏,经由trizol提取总rna,用primescriptrt-pcrkit(takara)进行反转录实验得到cdna。用荧光定量的方法检测granzymeb、tnf-α及il-12的转录水平,即granzymeb、tnf-α及il-12的mrna水平的变化。其中,荧光定量pcr检测以β-actin为内参基因;
荧光定量pcr检测内参β-actin基因的pcr引物序列为:
正向引物f:5’-ggctgtattcccctccatcg-3’;
反向引物r:5’-ccagttggtaacaatgccatgt-3’;
荧光定量pcr检测granzymeb的转录水平的引物为:
正向引物f:5’-tcgaccctacatggccttac-3’;
反向引物r:5-tggggaatgcattttaccat-3’;
荧光定量pcr检测tnf-α的转录水平的引物为:
正向引物f:5’-tctcatcagttctatggccc-3’;
反向引物r:5’-gggagtagacaaggtacaac-3’;
荧光定量pcr检测il-12的转录水平的引物为:
正向引物f:5’-cagcatgtgtcaatcagctac-3’;
反向引物r:5’-tgtggtcttcagcaggtttc-3’。
从实验结果中得到在c27h27n7o2s药剂处理后明显能推迟心脏移植的免疫排斥(图1a)。而在体重方面,在c27h27n7o2s处理后老鼠的体重并没有什么太大差异(图1b)。从he染色的结果发现(图1c),saline对照组移植心脏的组织中有大量炎症细胞浸润,主要为淋巴细胞和部分中性粒细胞,肌层有较大量炎症细胞广泛浸润。fk506组有部分淋巴细胞为主的炎症细胞浸润。c27h27n7o2s组只有轻度炎症细胞浸润,组织结构较紧密。从移植物心脏中分离t细胞经由流式细胞仪进行分析,结果显示,c27h27n7o2s能有效抑制cd4+及cd8+t细胞在移植物心脏中浸润。从脾脏中分离的rna经由实时定量pcr进行分析,结果显示,c27h27n7o2s都能抑制granzymeb、tnf-α及il-12细胞因子的表达。综上所述,c27h27n7o2s可以推迟心脏异体移植排斥的发生;表明c27h27n7o2s可用于制备推迟心脏异体移植排斥的药剂。同时,通过其他类型器官移植小鼠模型试验,发现所述c27h27n7o2s对肾脏、心脏、小肠、骨髓等器官或组织移植均具有良好的排斥反应抑制效果,表明c27h27n7o2s在抑制器官异体移植排斥中具有较大的应用前景。
- 还没有人留言评论。精彩留言会获得点赞!