姜黄素-茶叶制品的制备方法及其在抗肿瘤方面的应用与流程
本发明涉及含姜黄素的茶叶制品的制备方法和用途,具体而言涉及在茶叶提取物中加入天然产物姜黄素或其类似物。
背景技术:
研究背景:
茶是中国的一种传统饮料,通常将茶叶用水冲泡而成。目前在世界其他国家也深受人们的欢迎。按其产地和制作方法的不同,茶一般分为绿茶、红茶、白茶、黄茶、青茶、黑茶、乌龙茶、花茶等。由于茶中富含茶多酚、茶多糖、茶色素和γ-氨基丁酸等多种有益成分,适度饮茶具有显著的保健作用。据报道,茶能减低心脑血管发病和死亡风险、提高免疫力、降低胆固醇、降低血压、防治早老性痴呆、减肥瘦身等多种功能。近些年,大量的研究证明了茶也具有一定的抗肿瘤活性。但由于抗肿瘤所需要的摄入量远大于人们的日常饮用量,所以茶目前并没有作为抗肿瘤药物应用于临床。
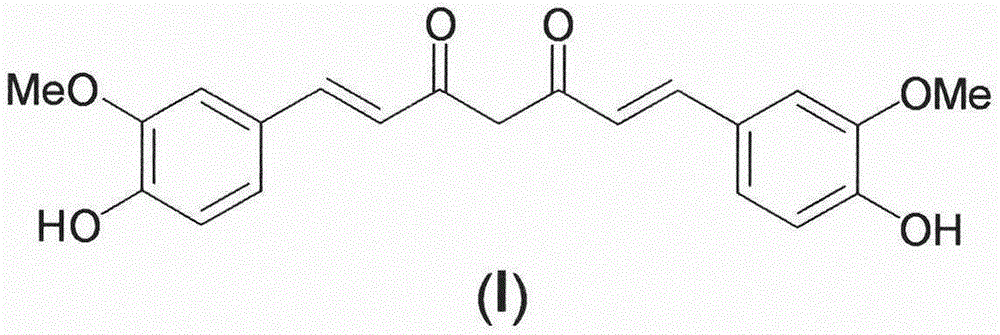
姜黄素(curcumin)是一种天然二酮类化合物,其结构如图1所示。姜黄素的主要生物来源为姜科和天南星科植物的根茎,如姜黄(c.longal.)、郁金(curcumaaromaticasalisb.)、莪术(c.zedoaria(berg.)rosc.)、和菖蒲(acoruscalamusl.)等。
作为一种安全的天然产物,姜黄素是联合国粮农组织食品法典委员会(fao/who-1995)批准、允许在食品中使用的食品添加剂之一。长期以来,姜黄素在食品工业中被广泛地应用,主要用于罐头、冷冻饮品、糖果、可可制品、方便米面制品、糕点、肠类制品、复合调味料、酱卤制品、碳酸饮料和人造黄油等各种食品形态。同时,姜黄素也被大量应用于一些非食品形态,如药丸、胶囊或片剂等。
对姜黄素大量的药理学研究,已发现其具有广泛的生物学活性,包括:抗氧化性、抗凝、抗炎、抗动脉粥样硬化、抗肝纤维化、抗病毒、和抗肿瘤等,且不良反应小、毒性低。特别是姜黄素的抗肿瘤活性,近些年已引起科研工作者日益深入的广泛研究。大量研究证明了姜黄素对多种恶性肿瘤细胞如口腔癌、胃癌、乳腺癌、肺癌、肝癌、直肠癌细胞等具有显著的抑制作用。
然而,通过大量临床试验证明,虽然姜黄素在细胞水平具有显著效果,但其在人体中却效果不显著。主要原因是姜黄素在人体内的生物利用度低,口服姜黄素被吸收从而进入血液的效率一般在1%-2%左右。姜黄素溶于乙醇、丙二醇,但其水溶性极差,约为20mg/l。其水溶性差的特征降低了其吸收效率,同时也限制了其静脉注射剂型的发展。为了提高姜黄素的水溶性,从而提高其生物利用度,水溶性氨基酸键合姜黄素、糖分子衍生物键合姜黄素、水溶性侧链衍生物键合姜黄素及脂质体包埋姜黄素等技术相继被开发出来。然而上述各种技术均步骤复杂,制备成本较高。因此开发一种制备简单、成本较低的方法来提高姜黄素的水溶性,进而提高其生物利用度和活性的方法将会极大的提高其药用价值。
技术实现要素:
本发明的目的是设计并制备一系列含姜黄素的茶叶制品来提高姜黄素的水溶性,同时增强茶叶的抗肿瘤活性,并就姜黄素-茶叶制品的抗肿瘤活性进行评价。
为了实现上述目的,本发明的第一方面,提供一系列含姜黄素及其衍生物的茶叶制品。所述茶叶制品包含茶叶或茶叶提取成分,同时包含姜黄素及其衍生物。
进一步的,所述茶叶制品包含绿茶、红茶、白茶、黄茶、青茶、黑茶、乌龙茶及其提取物。所述的姜黄素衍生物中包含姜黄素的化学结构衍生物及其在药学上可接受的盐。
本发明的第二方面,提供一种由所述的含姜黄素的茶叶制品作为活性成分制备的饮料、食品、药品和药学上可接受的赋形剂或载体。
本发明的第三方面,提供一种由所述的姜黄素-茶叶制品为原料生成的药物剂型,其特征在于,所述药物剂型包括散剂、片剂、颗粒剂、胶囊剂、溶液剂、乳剂、混悬剂、注射剂、冻干粉针剂。
本发明的第四方面,提供制备以上所述的姜黄素-茶叶制品和其类似物的方法,包括下列步骤:
以茶叶为原料提取茶叶水溶物;
按一定比例加入姜黄素制备姜黄素-茶叶制品。
本发明的第五方面,提供以上所述的姜黄素-茶叶制品在抑制癌细胞生长的应用。
在本发明实施例中,所述姜黄素-茶叶制品的水溶性比单体姜黄素提高了2倍。在所实验的肺癌,乳腺癌,前列腺癌,淋巴癌等多种肿瘤细胞中,所述姜黄素-茶叶制品的抗肿瘤活性均比茶叶有显著的提高。其中对淋巴癌细胞的半数抑瘤浓度(ic50)约为7.1mg/l。本发明解决了姜黄素的水溶性差,生物利用度低和茶叶产品抗肿瘤活性弱的技术问题。
附图说明
构成本发明的一部分的附图用来提供对本发明的进一步理解,使得本发明的其它特征、目的和优点变得更明显。本发明的示意性实施例附图及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
图1是姜黄素的结构图示;
图2是姜黄素-茶叶制品对淋巴癌细胞的抑制活性的实验结果;以及
图3是姜黄素-茶叶制品对多种肿瘤细胞的半数抑制浓度数据列表。
具体实施方式
为了使本技术领域的人员更好地理解本发明方案,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分的实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本发明保护的范围。
需要说明的是,本申请的说明书和权利要求书及上述附图中的术语“包括”和“具有”以及他们的任何变形,意图在于覆盖不排他的包含,例如,包含了一系列原料或步骤,不必限于清楚地列出的那些原料或步骤,而是可包括没有清楚地列出的或对于这些原料或步骤固有的其它原料或步骤。
如下给出以上所述的姜黄素-茶叶制品的制备方法的具体实施方式:
实施例1:绿茶提取物的制备
称量绿茶叶(程阳红韵,广西)2.02g,加入50ml去离子水,在80℃侵泡2h。用滤纸过滤除去固体残渣,高速离心(15,000g)10min,用0.2微米孔径的滤膜过滤,冷冻干燥,获得淡黄色固体产物0.15g,产率7.5%。
实施例2:红茶提取物的制备
称量红茶叶(程阳红韵,广西)2.52g,加入50ml去离子水,在80℃侵泡2h。用滤纸过滤除去固体残渣,高速离心(15,000g)10min,用0.2微米孔径的滤膜过滤,冷冻干燥,获得棕色固体产物0.16g,产率6.3%。
实施例3:姜黄素-绿茶提取物的制备
称量绿茶提取物固体100mg,溶于10ml去离子水,加入10.0mg姜黄素,室温搅拌10min,冷冻干燥,获得110mg姜黄素-绿茶制品。
实施例4:姜黄素-红茶提取物的制备
称量红茶提取物固体100mg,溶于10ml去离子水,加入10.0mg姜黄素,室温搅拌10min,冷冻干燥,获得110mg姜黄素-红茶制品。
实施例5:姜黄素在茶叶水溶液中的溶解度测定
(1)配置茶叶提取物的标准溶液
用分析天平分别准确称量绿茶和红茶提取物40.00mg,用去离子水配置浓度为0.4mg/ml的储备液。
(4)姜黄素溶解度测定
在100ml茶叶提取物水溶液中,加入100mg姜黄素固体,在室温振荡2h,15,000g离心5分钟,上层清液冷冻干燥,称重。获得的总重量减去茶叶提取物的重量即为姜黄素的溶解量。根据溶液的体积计算姜黄素在茶叶提取物水溶液的溶解度。
实验结果:姜黄素在绿茶提取物水溶液中的溶解度为41.5mg/ml。姜黄素在红茶提取物水溶液中的溶解度为41.1mg/ml。相比于姜黄素(20μg/ml),其水溶性提高了大约2倍。
实施例6抗肿瘤细胞活性测定
在37℃,5%co2培养箱中培养a549肺癌,bt474乳腺癌,mb231乳腺癌,du145前列腺癌,jurkat淋巴癌细胞。培养液为rpmi1640培养基,使用前加入10%胎牛血清(fbs)和1%抗生素-抗真菌混合抗生素。
收获指数生长的癌细胞,将其铺在96孔板中,浓度为2×104个细胞/孔。在37℃下孵育24小时后,用不同浓度的茶叶提取物和姜黄素-茶叶提取物处理细胞72小时。然后向每个孔中加入20μl的mtt(5mg/ml),将培养板在37℃下孵育2小时。弃去上清液,向各孔中加入100μldmso。15分钟后在490nm记录吸光度。通过下式获得细胞生长率:细胞生长率(%)=od处理×100%/od空白对照。数据报告为三次独立实验的平均值,每次实验均为三次。
实验结果:根据图3所示的mtt实验结果,茶叶提取物对a549肺癌,bt474乳腺癌,mb231乳腺癌,du145前列腺癌细胞的半数抑制浓度为126-398mg/l,而姜黄素-茶叶提取物这四种肿瘤细胞的半数抑制浓度为75.2-166mg/l。姜黄素-茶叶提取物的抗肿瘤活性比单纯茶叶提取物提高约为2倍左右。在所实验的肿瘤细胞中,姜黄素-茶叶提取物尤其对淋巴癌细胞具有高效的活性,其半数抑制浓度为7.1-9.2mg/l。
从实施例6的实验结果中,可以看出,所述的姜黄素-茶叶提取物具有显著地抑制癌细胞生长的作用。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!