左心室辅助设备调整和评估的制作方法
本申请要求于2018年3月29日提交的美国专利申请第62/649,929号的权益,其通过引用以其全文结合于此。
本文的公开内容涉及用于在使用体外电极装置调整和评估由左心室辅助设备(lvad)提供的心脏治疗中使用的系统和方法。
心脏辅助系统在患有心脏输出不足的患者体内提供附加的心脏输出。一个类型的心脏辅助系统被称为左心室辅助设备(lvad)。lvad可被描述为旨在用作增压泵以辅助患有慢性充血性心力衰竭的个体的心脏的辅助袋(auxiliarypouch)。慢性充血性心力衰竭可能经常是由于降低人类心脏的泵送能力的心脏病发作而引起的。通过增强这种虚弱的心脏的能力,患有此症状的个体可以被允许再次过上相对正常、有效的生活
正在经历外科手术的心力衰竭患者也可以被提供有lvad以急剧地卸除心室的负担从而促进恢复。使用lvad被治疗的患者中的约20%到30%可能产生对于医疗治疗而言是难治的右心室衰竭。作为由左心室和右心室之间的异常压力不平衡以及被观察为隔膜移位和游离壁异步鼓起(bulge)的异常壁运动产生的对右心室前负荷和后负荷的改变的结果,右心室功能可能下降。在右心室和左心室压力发展之间维持更大程度的同步可以防止在存在lvad的情况下右心室功能的消亡。
进一步地,植入式医疗设备(imd)(诸如,植入式起搏器、心脏复律器、除颤器、或起搏器-心脏复律器-除颤器)向心脏提供治疗性电刺激。imd可提供起搏以解决心动过缓,或提供起搏或电击以便于终止快速性心律失常,诸如心动过速或纤颤。在一些情况下,医疗设备可:感测心脏的固有去极化;基于固有去极化(或其缺失)检测心律失常;并且如果基于固有去极化检测到心律失常,则控制向心脏的电刺激的递送。
imd还可提供心脏再同步治疗(crt),其是一种形式的起搏。crt涉及向左心室、或左心室以及右心室两者的起搏的递送。向(多个)心室的起搏脉冲的递送的计时和位置可被选择以改进心室收缩的协调以及效率。
除植入式医疗设备本身之外,用于植入医疗设备的系统可包括工作台或其他装备。在一些情况中,这些其他各件装备协助医师或其他技术人员将心内引线放置在心脏上或心脏中的特定位置处。在一些情况下,装备向医师提供有关心脏的电活动以及心内引线的位置的信息。
技术实现要素:
本文描述的示例性系统、装置、方法和界面可以被配置成协助用户(例如,医师)评估患者和/或评估心脏治疗(例如,通过左心室心脏辅助设备(lvad)和/或植入式心脏治疗装置对患者执行的心脏治疗)。在一个或多个实施例中,系统、方法和界面可以被描述为非侵入式的。例如,在一些实施例中,系统、方法和界面可不需要或不包括植入式设备(诸如,引线、探针、传感器、导管、植入式电极等)来从患者的组织监测或获取多个心脏信号,以用于评估患者和/或由lvad和/或由植入式心脏治疗装置提供的心脏治疗。替代地,该系统、方法和界面可以使用采用例如多个体外电极和/或在患者的躯干周围附接到患者的皮肤的电极来非侵入式地获得的测量(例如,电测量,物理测量等)。
一个示例性系统可包括电极装置和计算装置,该电极装置包括多个体外电极以监测来自患者组织的心脏电活动,该计算装置包括处理电路系统并且被耦合到电极装置。计算装置可被配置成:至少在使用左心室辅助设备(lvad)递送心脏治疗期间使用多个体外电极监测心脏电活动,基于监测到的电活动生成电异质性信息,以及基于所生成的电异质性信息确定lvad的输出参数。
方法可包括:至少在使用左心室辅助设备(lvad)递送心脏治疗期间使用多个电极监测来自患者组织的电活动,基于监测到的电活动生成电异质性信息,以及基于所生成的电异质性信息确定lvad的输出参数。
本文所公开的示例性系统、装置和方法可被描述为用于滴定起搏参数以用于在心脏再同步治疗(crt)期间最大化心脏电同步的通用工具。更具体地,示例性系统、装置和方法可使用多个体外电极来在使用左心室辅助设备(lvad)的心脏治疗的使用期间测量和监测整体心脏激动模式,以供在例如lvad治疗评估、用于滴定lvad治疗的后续/编程(包括泵的速度和起搏治疗的伴随物(concomitant))中使用。本文所公开的示例性系统、装置和方法可进一步被描述为提供滴定lvad治疗以得到最优患者结果的即时、非侵入式手段。
在一个或多个实施例中,示例性系统、装置和方法可配备有或包括一个或多个附加传感器以协助lvad设备和患者管理。例如,可将声学传感器阵列结合到包括多个体外电极的电极装置中,并且声学信号可用于推断心脏的机械激动(例如,瓣膜打开和关闭)以及检测到与lvad的泵内的血栓积聚或lvad的其他机械问题相对应的声学特征(signature)。
进一步地,在一个或多个实施例中,包括,例如,信号放大器、电极阵列、分析过程或算法的示例性系统、装置和方法可被描述为与lvad系统的lvad控制器或lvad监测器集成。示例性系统、装置和方法可进一步包含或利用用于自动滴定用于最佳响应(例如,最低右心室(rv)不同步、最短rv激动时间等)和患者发展到rv衰竭的机会最小的参数的算法。
在一个或多个实施例中,示例性系统、装置和方法可被配置成仅滴定lvad泵速度或滴定lvad泵速度和起搏设备起搏参数(自动地或手动地)。进一步地,示例性系统、装置和方法还可包括或具有其他皮肤传感器和集成的相关联的信号处理(诸如,声学),集成的相关联的信号处理(诸如,声学)用于提供对心脏的机械功能的输入(例如,瓣膜打开和关闭)以及涉及泵功能本身的诊断(例如,泵内血栓的“积聚”等)。
以上发明内容不旨在描述本公开的每一个实施例或每一种实现方式。通过参考以下结合所附附图获得的具体实施方式以及权利要求书,更完整的理解将变得明显和可理解。
附图说明
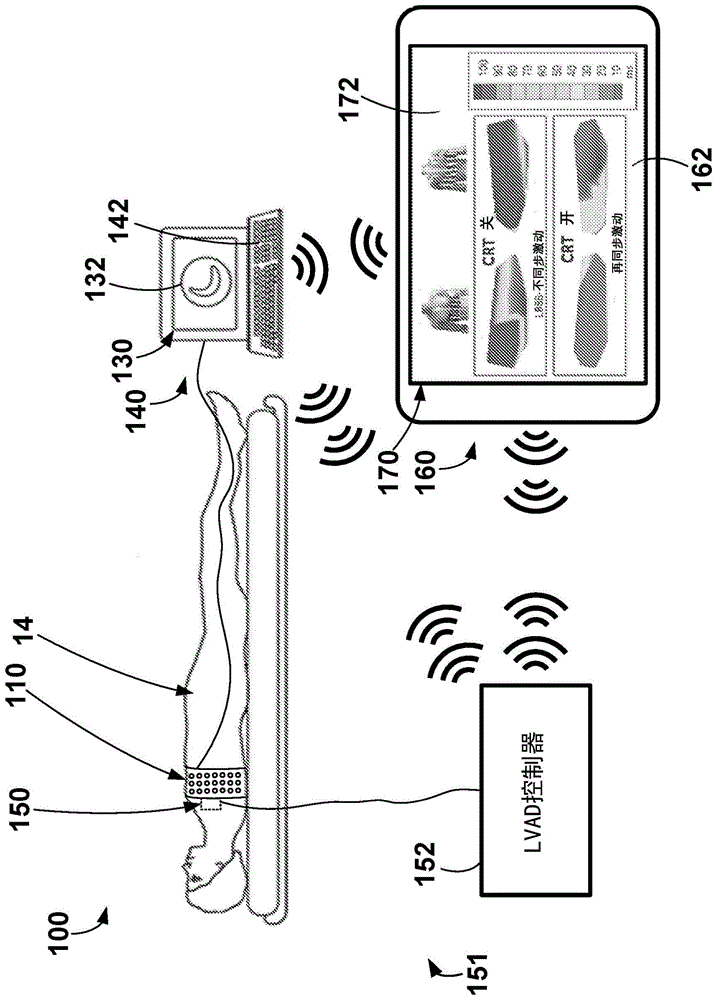
图1是包括电极装置、左心室辅助设备(lvad)装置、显示装置和计算装置的示例性系统的图。
图2-3是用于测量躯干表面电势的示例性体外电极装置的图。
图4是用于确定lvad输出参数的示例性方法的框图。
图5是用于调整lvad输出参数和起搏参数中的一者或两者的示例性方法的框图。
图6是用于基于电异质性信息和心音中的一者或两者调整lvad的示例性方法的框图。
图7是包括示例性植入式医疗设备(imd)的示例性系统的图。
图8是包括示例性lvad装置和图7的imd的示例性系统的图。
图9a是图7的示例性imd的图。
图9b是图9a的设置在左心室中的电引线的远侧端的放大视图的图。
图10a是示例性imd(例如图7-9的系统)的框图。
图10b是在图7-9的系统中采用的示例性imd(例如,植入式脉冲发生器)电路系统以及相关联的引线的另一框图。
具体实施方式
在以下对说明性实施例的详细描述中,参考了所附附图,这些附图形成实施例的一部分,并且在这些附图中以说明方式示出了可实践的具体实施例。应当理解,可以采用其他实施例,并且可以作出结构改变而不背离(例如,仍落入)在此所呈现的本公开的范围。
将参照图1-10来描述示例性系统和方法。对本领域技术人员将是显而易见的是,来自一个实施例的元件或过程可与其他实施例的元件或过程结合使用,并且使用本文中所阐述的特征的组合的此类方法和系统的可能的实施例不限于附图中所示和/或本文所描述的特定的实施例。进一步地,将认识到,本文中所描述的实施例可包括并不一定按比例示出的许多元件。更进一步地,将认识到,本文中的过程的时序以及各种元件的尺寸和形状可被修改但仍落在本公开的范围内,但是某些时序、一个或多个形状和/或尺寸、或元件的类型相对于其他时序、形状和/或尺寸、元件的类型可能是有利的。
可使用围绕患者的表面或皮肤定位的多个体外电极测得或监测多个心电图(ecg)记录或信号。ecg信号可被用于评估并且配置心脏治疗,诸如例如由lvad或crt提供的心脏治疗。如本文描述的,由于例如植入式电极可不被用于测量ecg信号,因此ecg信号可被非侵入式地收集或获取。进一步地,ecg信号可被用于确定心脏电激动时间,该心脏电激动时间可被用于生成各种度量(例如,电异质性信息),该各种度量可由用户(例如,医师)使用以优化起搏治疗(诸如crt)或由lvad提供的心脏治疗的一个或多个设置或参数。
不同的示例性系统以及方法可以被配置成使用包括体外电极的电极装置、显示装置和计算装置来在心脏健康的评估和/或心脏治疗的配置(例如,优化)中非侵入式地协助用户(例如,医师)。在图1中描绘了包括电极装置110、计算装置140、lvad装置151和远程计算设备160的示例性系统100。
示例性lvad装置151可被通常描述为包括lvad150和lvad控制器152,lvad150可操作地耦合到患者的心脏以执行左心室辅助心脏治疗,lvad控制器152可操作地耦合到lvad150以对lvad150进行控制和向lvad150提供电力。lvad150可被(例如,通过一个或多个有线电连接、无线地等)可操作地耦合到lvad控制器152。如所示的,lvad150通过使用有线连接或导线可操作地耦合到或连接到lvad控制器152。本文可参考图8进一步描述示例性lvad装置151。应当理解,lvad装置151可包括较低的输出流量(flow),部分心脏辅助系统可用于更宽范围的hf患者,所述更宽范围的hf患者包括症状较少的那些患者和具有其中高心脏充盈压可能导致hf症状的射血分数保留(hfpef)的那些患者。用于这些较低输出泵的植入方法可以使用微创技术来执行并且可包括各种放置(诸如左心房到主动脉循环支持)。为了本公开的目的,所有这样的完全或部分心脏辅助系统,包括治疗具有射血分数保留的hf的那些心脏辅助系统,都将被称为lvad。
所示的电极装置110包括多个电极,该多个电极被合并到、或被包括在围绕患者14的胸部或躯干而缠绕的带内。电极装置110被可操作地耦合到计算装置140(例如,通过一个或有线的电连接、无线地等)以将来自电极中的每一个电极的电信号提供到计算装置140以供分析、评估等。示例性电极装置可在于2014年3月27日提交并且于2016年3月26日颁布的题为“bioelectricsensordeviceandmethods(生物电传感器设备以及方法)”的美国专利第9,320,446号中被描述。进一步地,示例性电极装置110将参照图2-3被更详细地描述。
尽管在本文中未描述,但是示例性系统100可以进一步包括成像装置。该成像装置可以是被配置成以非侵入的方式对该患者的至少一部分进行成像或提供该患者的至少一部分的图像的任何类型的成像装置。例如,除了诸如造影剂之类的非侵入式工具之外,成像装置可不使用可被定位于患者体内以提供患者的图像的任何部件或部分。应当理解,本文描述的示例性系统和方法可以进一步使用成像装置来向用户(例如,医师)提供非侵入式辅助,以与配置心脏治疗相结合地将lvad150(或其一个或多个部分)或一个或多个起搏电极定位或放置在患者心脏附近。
例如,示例性系统和方法可以提供图像引导导航,该图像引导导航可用于在患者体内导航lvad150的一个或多个部分、引线(包括电极、无引线电极、无线电极、导管等),同时还提供非侵入性心脏治疗配置,包括确定有效或最优lvad参数、a-v间期等。使用成像装置和/或电极装置的示例性系统以及方法可在下述中描述:ghosh的于2014年12月18日公布的美国专利申请公开第2014/0371832号、ghosh等人的于2014年12月18日公开的美国专利申请公开第2014/0371833号、ghosh等人的于2014年10月30日公开的美国专利申请公开第2014/0323892号以及ghosh等人的于2014年10月20日公开的美国专利申请公开第2014/0323882号,上述专利申请公开中的每一个均以其整体通过引用并入本文。
示例性成像装置可以被配置成捕获x射线图像和/或任何其他替代成像模态。例如,该成像装置可以被配置成使用同心荧光镜检查、双平面荧光镜检查、超声、计算机断层成像术(ct)、多层面计算机断层成像术(msct)、磁共振成像(mri)、高频超声(hifu)、光学相干断层成像术(oct)、血管内超声(ivus)、二维(2d)超声、三维(3d)超声、四维(4d)超声、术中ct、术中mri等来捕获图像或图像数据。进一步地,应当理解的是,成像装置可以被配置成(例如,连续地)捕获多个连续图像以便提供视频帧数据。即,使用成像装置随时间拍摄的多个图像可提供视频帧、或动态影片、数据。额外地,还可以以二维、三维或四维获得并显示图像。在更为先进的形式中,还可通过结合来自图或来自由mri、ct或超声心动描记图模态捕获的术前图像数据的心脏数据或其他软组织数据,来实现心脏或身体的其他区域的四维表面呈现。来自混合模态(诸如正电子发射断层扫描(pet)与ct组合、或单光子发射计算机断层扫描(spect)与ct组合)的图像数据集也可提供叠加到解剖数据上的功能图像数据,例如,以被用于将植入式装置导航至心脏或其他感兴趣的区域内的目标位置。
可用于与本文描述的示例性系统和方法结合使用的系统和/或成像装置在以下各项中被描述:evron等人的于2005年1月13日公开的美国专利申请公开第2005/0008210号;zarkh等人的于2006年4月6日公开的美国专利申请公开第2006/0074285号;zarkh等人的于2014年5月20日公告的美国专利第8,731,642号;brada等人的于2014年10月14日公告的美国专利第8,861,830号;evron等人的于2005年12月27日公告的美国专利第6,980,675号;okerlund等人的于2007年10月23日公告的美国专利第7,286,866号;reddy等人的于2011年12月11日公告的美国专利第7,308,297号;burrell等人的于2011年12月11日公告的美国专利第7,308,299号;evron等人的于2008年1月22日公告的美国专利第7,321,677号;okerlund等人的于2008年3月18日公告的美国专利第7,346,381号;burrell等人的于2008年11月18日公告的美国专利第7,454,248号;vass等人的于2009年3月3日公告的美国专利第7,499,743号;okerlund等人的于2009年7月21日公告的美国专利第7,565,190号;zarkh等人的于2009年9月8日公告的美国专利第7,587,074号;hunter等人的于2009年10月6日公告的美国专利第7,599,730号;vass等人的于2009年11月3日公告的美国专利第7,613,500号;zarkh等人的于2010年6月22日公告的美国专利第7,742,629号;okerlund等人的于2010年6月29日公告的美国专利第7,747,047号;evron等人的于2010年8月17日公告的美国专利第7,778,685号;vass等人的于2010年8月17日公告的美国专利第7,778,686号;okerlund等人的于2010年10月12日公告的美国专利第7,813,785号;vass等人的于2011年8月9日公告的美国专利第7,996,063号;hunter等人的于2011年11月15日公告的美国专利第8,060,185号;verard等人的于2013年3月19日公告的美国专利第8,401,616号,这些专利中的每一个通过引用以其整体结合在此。
计算装置140和远程计算设备160可分别各自包括显示装置130、160,该显示装置130、160可被配置为显示和分析数据,诸如例如,电信号(例如,心电图数据)、电激动时间、电异质性信息等。例如,由通过电极装置110收集或监测的电信号表示的多个心动周期或多个心跳中的一个心动周期、或一个心跳可被分析并且评估,以得到一个或多个度量,包括激动时间以及电异质性信息,所述一个或多个度量可与关于心脏治疗的一个或多个参数的治疗性质相关,该一个或多个参数诸如例如,lvad泵速度、lvad泵功率/电流(例如,被递送到泵以影响泵速度和/或其他泵参数的电流)、lvad泵吞吐量、其他lvad操作参数、起搏参数、引线位置等。更具体地,例如,可针对一个或多个度量评估单个心动周期的qrs波群,该一个或多个度量诸如,例如qrs开始、qrs偏移(offset)、qrs峰、电异质性信息、电激动时间、左心室或胸电激动时间标准差(lved)、激动时间标准差(sdat)、平均左心室或胸替代电激动时间(lvat)(被参考为最早激动时间)、qrs持续时间(例如,qrs开始到qrs偏移之间的间期)、平均左替代激动时间和平均右替代激动时间之间的差、相对或绝对qrs形态、激动时间的较高百分位和较低百分位之间的差(较高百分位可以是90%、80%、75%、70%等,并且较低百分位可以是10%、15%、20%、25%和30%等)、集中趋势的其他统计测量(例如,中值或众数)、应用于所有激动时间或左替代激动时间或右替代激动时间等的离散度(dispersion)(例如,平均差、标准差、方差、四分位距、范围)。
在至少一个实施例中,计算装置140和远程计算设备160中的一者或两者可以是服务器、个人计算机、或者平板计算机。计算装置140可被配置成从输入装置142(例如,键盘)接收输入并向显示装置130传输输出,并且远程计算设备160可被配置成从输入装置162(例如,触摸屏)接收输入并向显示装置170传输输出。计算装置140和远程计算设备160两者可包括数据存储,该数据存储允许访问处理程序或例程和/或一个或多个其他类型的数据,例如,用于分析由电极装置110捕获的多个电信号,用于确定qrs开始、qrs偏移、中值、众数、平均值、峰值或最大值、谷值或最小值,用于确定电激动时间,用于驱动被配置成非侵入式地协助用户配置一个或多个lvad操作参数或设置(诸如,lvad泵速度、lvad泵吞吐量、lvad泵功率、lvad泵电流、泵流入万向架(gimbal)角度、对诸如泵抽吸、患者活动水平变化和生理参数输入之类的事件的自动算法响应、启用/禁止诸如拉瓦瑞(lavare)循环之类的周期性泵速度调节特征)的图形用户界面,用于驱动被配置成用于非侵入式地协助用户配置一个或多个起搏参数或设置(诸如例如,起搏频率、心室起搏频率、a-v间期、v-v间期、起搏脉宽、起搏向量、多点起搏向量(例如,左心室向量四引线)、起搏电压、起搏配置(例如,双心室起搏、仅右心室起搏、仅左心室起搏等)),以及心律失常检测和治疗、频率自适应设置和性能等的图形用户界面。
计算装置140可被可操作地耦合到输入装置142和显示装置130,从而例如向输入装置142和显示装置130中的每一个传输数据并从输入装置142和显示装置130中的每一个传输数据,并且远程计算设备160可被可操作地耦合到输入装置162和显示装置170,从而例如向输入装置162和显示装置170中的每一个传输数据并从输入装置162和显示装置170中的每一个传输数据。例如,可以使用例如模拟电气连接、数字电气连接、无线连接、基于总线的连接、基于网络的连接、基于互联网的连接等将计算装置140和远程计算设备160电耦合到输入装置142、162和显示装置130、170。如本文进一步描述的,用户可以向输入设备142、162提供输入,以查看和/或选择与由lvad装置151和植入式医疗设备中的一者或两者递送的心脏治疗相关的一条或多条配置信息。
尽管如所描绘的输入装置142是键盘并且输入装置162是触摸屏,但是应当理解,输入装置142可以包括能够向计算装置140提供输入以便执行在本文描述的功能、方法、和/或逻辑的任何装置。例如,输入装置142、162可包括键盘、鼠标、轨迹球、触摸屏(例如,电容触摸屏、电阻触摸屏、多点触摸屏等)等。同样地,显示装置130、170可包括能够向用户显示信息的任何装置,诸如包括如下各项的图形用户界面132、172:一个或多个心跳、qrs波群、lvad操作参数、lvad操作度量、起搏参数、电异质性信息、文本指令、电激动信息的图形描绘、人类心脏的解剖的图形描绘、患者心脏的图像或图形描绘、一个或多个电极的位置的图形描绘、人类躯干的图形描绘、患者躯干的图像或图形描绘、植入的电极和/或引线的图形描绘或实际图像等。进一步地,显示装置130、170可以包括液晶显示器、有机发光二极管屏、触摸屏、阴极射线管显示器等。
由计算装置140和远程计算设备160存储和/或执行的处理程序或例程可包括用于下述的程序或例程:计算数学、矩阵数学、分解算法、压缩算法(例如,数据压缩算法)、校准算法、图像构造算法、信号处理算法(例如,各种滤波算法、傅里叶变换、快速傅里叶变换等)、标准化算法、比较算法、矢量数学、或实现本文所描述的一个或多个示例性方法和/或过程所需的任何其他处理。由计算装置140和远程计算设备160存储和/或使用的数据可以包括例如来自电极装置110的电信号/波形数据(例如,多个qrs波群)、来自电极装置110的电激动时间、来自声学传感器120的心音/信号/波形数据、图形(例如,图形元素、图标、按钮、窗口、对话框、下拉菜单、图形区域、图形区、3d图形等)、图形用户界面、来自根据本文的公开采用的一个或多个处理程序或例程的结果(例如,电信号、电异质性信息等)、或可对于执行本文描述的一个和/或多个过程或方法所需的任何其他数据。
在一个或多个实施例中,可以使用在可编程计算机上执行的一个或多个计算机程序来实现示例性系统和方法,所述可编程计算机诸如包括例如处理能力、数据存储(例如,易失性或非易失性存储器和/或存储元件)、输入设备、和输出设备的计算机。本文中所描述的程序代码和/或逻辑可以应用于输入数据以便执行本文中所描述的功能并且生成所期望的输出信息。输出信息可以作为输入被应用于如本文中所描述的或如将以已知的方式被应用的一个或多个其他设备和/或方法。
可以使用任何可编程语言来提供用于实现本文中所描述的系统、装置、方法、和/或界面的一个或多个程序,所述可编程语言例如,适用于与计算机系统进行通信的高级程序化编程语言和/或面向对象的编程语言。任何这种程序可以例如被存储在由通用程序或专用程序可读的任何适当的设备(例如,存储介质)上,所述通用程序或专用程序在计算机系统(例如,包括处理装置)上运行以用于在读取适当的设备以执行本文中所描述的程序时对计算机系统进行配置和操作。换言之,至少在一个实施例中,可以使用配置有计算机程序的计算机可读存储介质来实现示例性系统和方法界面,其中,如此配置的存储介质使计算机以特定的且预定义的方式操作以便执行本文中所描述的功能。进一步地,在至少一个实施例中,示例性系统、装置、方法和界面可以被描述为由编码在一个或多个非瞬态介质中的逻辑(例如,目标代码)来实现,该一个或多个非瞬态介质包括用于执行的并且在由处理器执行时可操作用于执行诸如本文中所描述的方法、过程、和/或功能之类的操作的代码。
计算装置140和远程计算设备160可以是例如任何固定或移动的计算机系统(例如,控制器、微控制器、个人计算机、小型计算机、平板计算机等)。并不限制计算装置140和远程计算设备160的确切配置,并且本质上,能够提供合适的计算能力以及控制能力(例如,信号分析、数学功能(诸如,中值、众数、平均、最大值确定、最小值确定、斜率确定、最小斜率确定、最大斜率确定、图形处理等)的任何设备均可被使用。如本文描述的,数字文件可以是由本文描述的计算装置140和远程计算设备160可读和/或可写的包含数字字节(例如,以二进制、三进制等编码)的任何介质(例如,易失性或非易失性存储器、cd-rom、穿孔卡片、磁带等)。同样,如本文所描述的,用户可读格式的文件可以是由用户可读和/或可理解的在任何介质(例如,纸张、显示器等)上可呈现的任何数据表示(例如,ascii文本、二进制数、十六进制数、十进数、图解等)。
鉴于上述内容,将显而易见的是,如在根据本公开的一个或多个实施例中描述的功能可以以如将对于本领域技术人员所已知的任何方式来实现。由此,将用于实现本文中所描述的过程的计算机语言、计算机系统、或任何其他软件/硬件不应当限制于本文中所描述的系统、过程或程序(例如,由此类系统、过程或程序提供的功能)的范围。
示例性电极装置110可以被配置成用于测量患者14的身体表面电势,并且更具体地,患者14的躯干表面电势。如图2所示,示例性电极装置110可以包括一组电极112或电极112阵列、绑带113、和接口/放大器电路系统116。电极112可以被附连或耦合到绑带113并且绑带113可以被配置成围绕患者14的躯干缠绕,使得电极112环绕患者的心脏。如进一步所示的,电极112可以围绕患者14的外周定位,包括患者14的躯干的后部位置、侧面位置、后外侧位置、前外侧位置、和前部位置。
示例性电极装置110可以被进一步配置成测量或监测来自患者14和位于患者14体内或可操作地耦合到患者14的一个或多个设备(诸如lvad150)中的至少一者或两者的声音。如图2所示,示例性电极装置110可以包括一组声学传感器120或声学传感器120阵列,该声学传感器120被附接到或耦合到绑带113。绑带113可被配置成围绕患者14的躯干缠绕,使得声学传感器120围绕患者心脏。如进一步所示的,声学传感器120可以围绕患者14的外周定位,包括患者14的躯干的后部位置、侧面位置、后外侧位置、前外侧位置、和前部位置。
进一步地,电极112和声学传感器120可以经由有线连接118被电连接到接口/放大器电路系统116。接口/放大器电路系统116可被配置成放大来自电极112和声学传感器120的信号并且向计算装置140和远程计算设备160中的一者或两者提供信号。其他示例性系统可以使用无线连接来将由电极112感知到的信号传输到接口/放大器电路系统116,并且进而(例如,作为多通道数据)传输到计算装置140和远程计算设备160中的一者或两者。在一个或多个实施例中,可以使用例如模拟电连接、数字电连接、无线连接、基于总线的连接、基于网络的连接、基于互联网的连接等将接口/放大器电路116电耦合到计算装置140。
尽管在图2的示例中电极装置110包括绑带113,但是在其他示例中,可以采用多种机制中的任何一个(例如,胶带或粘合剂)来协助电极112和声学传感器120的间隔和放置。在一些示例中,绑带113可以包括弹性带、胶带条或布。进一步地,在一些示例中,绑带113可以是诸如例如t恤之类的一件衣服的一部分、或与诸如例如t恤之类的一件衣服集成在一起。在其他示例中,电极112和声学传感器120可以被单独放置在患者14的躯干上。进一步地,在其他示例中,电极112(例如,以阵列布置)和声学传感器120(例如,也以阵列布置)可以是贴片、背心的一部分或定位在贴片、背心内,和/或将电极112和声学传感器120紧固到患者14的躯干上的其他方式。又进一步地,在其他示例中,电极112和声学传感器120可以是两个材料部分或两个“贴片”的一部分,或被定位在两个材料部分或两个“贴片”内。两个部分或贴片中的一个可被定位在患者14的躯干的前侧上(例如,以监测表示患者心脏的前侧的电信号、测量表示患者心脏的前侧的替代心脏电激动时间、监测或测量患者的前侧的声音等),并且另一部分或贴片可被定位于患者14的躯干的后侧上(例如,以监测表示患者心脏的后侧的电信号、测量表示患者心脏的后侧的替代心脏电激动时间、监测或测量患者的后侧的声音等)。并且又进一步地,在其他示例中,电极112和声学传感器120可被布置在从患者14的前侧跨越患者14的左侧延伸至患者14的前侧的顶部列以及底部列中。又另进一步地,在其他示例中,电极112和声学传感器120可被布置在围绕腋窝区域的曲线中,并且可具有电极/传感器密度,该电极/传感器密度在右胸上比其他剩余区域更为稀疏。
电极112可以被配置成环绕患者14的心脏,并且在与心脏的去极化和复极化相关联的电信号已经传播通过患者14的躯干之后记录或监测这些电信号。电极112中的每一个可以以单极配置使用以感测反映心脏信号的躯干表面电势。接口/放大器电路系统116还可以被耦合到可以与每个电极112组合使用以用于单极感测的返回电极或中性电极(未示出)。
在一些示例中,可能存在在空间上围绕患者躯干分布的约12至约50个电极112和约12至约50个声学传感器120。其他配置可具有更多或更少的电极112和更多或更少的声学传感器120。应当理解,电极112和声学传感器120可不被布置或分布在完整围绕或完全围绕患者14延伸的阵列中。替代地,电极112和声学传感器120可被布置在仅围绕患者14的一部分延伸或部分地围绕患者14延伸的阵列中。例如,电极112和声学传感器120可被分布在患者的前部、后部、左侧上,其中右侧(包括右侧的后部区和前部区)附近的电极和声学传感器较少或没有电极和声学传感器。
计算装置140可以记录并分析由电极112和声学传感器120感知到的并且由接口/放大器电路116放大/调节的躯干表面电势信号。计算装置140可被配置为分析来自电极112的电信号以提供来自患者心脏的心电图(ecg)信号、信息或数据,如本文将进一步描述的。计算装置140可被配置为分析来自声学传感器120的电信号以提供来自患者身体和/或植入在患者体内的设备(诸如lvad150)的声音信号、、信息或数据,如本文将进一步描述的。
此外,计算装置140和远程计算设备160可被配置成提供图形用户界面132、172,该图形用户界面132、172描绘了包括使用电极装置110获取的qrs波群的ecg并且描绘了包括使用声学传感器120获取的声波,以及与其相关的其他信息。示例性系统以及方法可非侵入式地使用通过使用电极装置110收集的电信息和使用声学传感器120收集的声音信息,以评估患者的心脏健康并且评估以及配置被递送至患者的心脏治疗,以及评估植入的设备(诸如lvad150)的机械功能。
进一步地,电极装置110可进一步包括参考电极和/或驱动电极,该参考电极和/或驱动电机例如定位在患者14的下半躯干周围并且可进一步地由系统100使用。例如,电极装置110可包括三个参考电极,并且来自该三个参考电极的信号可被组合以提供参考信号。进一步地,电极装置110可使用三个尾部参考电极(例如,替代于威尔逊中心电端(wilsoncentralterminal)中使用的标准参考)以通过平均三个尾部定位的参考信号来获得具有较少噪声的“真实的”单极信号。
图3示出了包括多个电极112和多个声学传感器120的另一示例性电极装置110,该多个电极112被配置成环绕患者14的心脏,并且在与心脏的去极化和复极化相关联的电信号已经传播通过患者14的躯干之后记录或监测这些信号,多个声学传感器120被配置成环绕患者14的心脏,并且在与心脏和/或植入的设备(诸如lvad150)相关联的声音信号已经传播通过患者14的躯干之后记录或监测这些信号。电极装置110可以包括背心114,多个电极112和多个声学传感器120可以被附接在背心114上,或电极112和声学传感器120可以被耦合到背心114。在至少一个实施例中,多个电极112或电极112的阵列可以用来收集电信息,诸如,例如替代电激动时间。与图2的电极装置110类似,图3的电极装置110可包括接口/放大器电路系统116,接口/放大器电路系统116通过有线连接118被电耦合到电极112和声学传感器120中的每一个,并且被配置成用于将来自电极112和声学传感器120的信号传输到计算装置140。如所示的,电极112和声学传感器120可以被分布在患者14的躯干上,包括例如患者14的躯干的后部位置、侧面位置、后外侧位置、前外侧位置和前部位置。
背心114可以由编织物形成,其中电极112和声学传感器120附接到该编织物。背心114可被配置成维持电极112和声学传感器120在患者14的躯干上的位置和间隔。进一步地,背心114可被标记以协助确定患者14的躯干表面上的电极112和声学传感器120的位置。在一些示例中,可能存在围绕患者14的躯干分布的约25个至约256个电极112和约25个至约256个声学传感器120,尽管其他配置可具有更多或更少的电极112和更多或更少的声学传感器120。
示例性系统以及方法可被用于在评估患者的心脏健康和/或评估和配置(例如,通过lvad、通过植入式医疗设备等)当前被递送至患者的心脏治疗时向用户提供非侵入式协助。例如,示例性系统以及方法可被用于在配置和/或调整通过lvad150被递送到患者的左心室辅助心脏治疗的一个或多个心脏治疗设置时协助用户。进一步地,例如,示例性系统以及方法可提供对起搏治疗(例如,左单心室起搏治疗)的a-v间期或延迟的优化。仍进一步地,例如,示例性系统以及方法可被用于在配置和/或调整使用例如植入式医疗设备进行的lvad递送的心脏治疗和起搏治疗两者的一个或多个心脏治疗设置时协助用户。
进一步地,应当理解,计算装置140、远程计算设备160和lvad控制器152可以以多个不同的方式被可操作地耦合到彼此,以便执行或实行本文所述的功能。例如,在所描绘的实施例中,计算装置140可以被无线地可操作地耦合到远程计算设备160和lvad控制器152,如由在它们之间发出的无线信号线所描绘的。进一步地,例如,在所描绘的实施例中,远程计算设备160可以被无线地可操作地耦合到计算装置140和lvad控制器152,如由在它们之间发出的无线信号线所描绘的。进一步地,例如,与无线连接相反,计算装置140、远程计算设备160和lvad控制器152中的一个或多个可以通过一个或多个有线电连接可操作地耦合。
图4中描绘了使用例如图1-3和图7-10中所描绘的系统和装置确定lvad输出参数的示例性方法200。如所示,方法200包括使用多个体外电极(诸如例如,本文参考图1-3描述的电极装置110)监测患者的电活动202。可监测电活动202达多个心动周期或心跳。进一步地,可监测电活动202达所选择的时间段(诸如,例如,五秒钟)。可以在不存在lvad治疗的情况下或在lvad治疗期间通过多个电极监测电活动202。
方法200可以进一步包括根据所监测的电活动202生成电异质性信息204。可使用电异质性的度量生成电异质性信息。电异质性信息的度量可包括患者的躯干的右侧上的电极的右心室激动时间(rvat)的度量。可根据前表面和后表面两者上的电极确定rvat的度量。进一步地,rvat可以是基于来自患者躯干的右侧(例如,患者的右躯干)上的右电极组的电信号的平均值、中值、或其他统计复合值,或根据患者躯干的右侧(例如,患者的右躯干)上的右电极组的电信号计算的平均值、中值、或其他统计复合值。而且,电异质性信息的度量可包括指示隔膜不同步(septaldyssynchrony)的隔膜电异质性信息,该隔膜电异质性信息是使用由多个体外电极中定位在患者的胸骨或脊柱附近的中心体外电极组所监测的电活动而被生成的。更具体地,可以通过查看靠近胸骨和脊柱的电极子集来确定隔膜不同步,并且相对于右侧激动(或左侧激动)的隔膜计时可以有助于滴定lvad泵速度以避免抽吸、右心室衰竭等。
进一步地,电异质性的度量可包括患者的躯干的左侧上的电极的激动时间标准偏差(sdat)的度量和/或患者的躯干的左侧上的电极的平均左心室激动时间(lvat)的度量。可根据前表面和后表面两者上的电极确定lvat的度量。电异质性的度量可包括从来自患者的躯干两侧的多个电极信号获得的平均总激动时间(mtat)的度量,或它可以包括反映位于患者躯干的右侧或患者躯干的左侧上或组合患者躯干的右侧和左侧两者上的多个电极上的激动时间的范围或离散度的其他度量(例如,标准偏差、四分位偏差、最迟发的激动时间与最早发的激动时间之间的差异)。
附加地,隔膜复极化指数还可用于滴定(获得良好的心脏舒张或均匀性的机会),并且进一步可用于最小化rv激动时间(通过来自右侧胸电极的激动时间来测量)。进一步地,可以描述的是,可以使用本文所述的系统和方法通过例如测量右心室和左心室激动时间和模式来监测右心室或左心室重构。
如本文所描述的,可以在不存在lvad治疗的情况下或在lvad治疗期间通过多个电极监测202电活动。如果在不存在lvad治疗的情况下监测202电活动,则由其生成204的电异质性信息可以表示基线心脏健康值。如果在lvad治疗期间监测202电活动,则由其生成204的电异质性信息可以表示在一个或多个lvad输出参数处的lvad治疗的递送期间的心脏健康值,该一个或多个lvad输出参数可以是使用本文所述的示例性系统、装置、设备和方法可配置的或可调整的。
示例性方法200可以进一步包括基于生成的电异质性信息204确定lvad输出参数206。例如,为了确定lvad输出参数206,可以将隔膜中心电异质性信息与从患者的胸骨或脊柱的右侧或左侧的一组体外电极生成的其他电异质性信息进行比较。具体而言,如果当将隔膜中心电异质性信息与来自患者的胸骨或脊柱的右侧或左侧的一组体外电极的其他电异质性信息进行比较时,隔膜中心电异质性信息指示心室的电激动导致由lvad流速取代的机械脉动活动,则可减小或定制lvad输出参数(诸如例如,泵速度、rpm自适应算法、或用于控制周期性速度调节的参数)。
进一步地,例如,确定lvad输出参数206可包括将现在或当前生成的电异质性信息204与在不存在lvad治疗的情况下或使用先前的一个或多个lvad输出参数的先前生成的电异质性信息204进行比较。以此方式,如果所生成的电异质性信息204指示患者心脏的电和/或机械心脏功能的改善,则示例性方法200可以确定当前的一个或多个lvad输出参数206比不存在lvad治疗或先前的一个或多个lvad输出参数更有效。
以此方式,可以基于所生成的电异质性信息204滴定或调整一个或多个lvad输出参数210,直到找到最优lvad输出参数为止。例如,在确定一个或多个lvad输出参数206之后,示例性方法200可以基于或使用所确定的一个或多个lvad输出参数210来调整lvad(例如,用户可以手动地这样做或者系统可以自动地执行调整),并且随后方法200可以循环以再次在lvad治疗的递送期间监测电活动202、基于所监测的电活动生成电异质性信息204、以及基于此确定lvad输出参数。换言之,示例性方法200可以“尝试”多个不同的lvad输出参数,直到基于所生成的电异质性信息确定该多个不同的lvad输出参数中的哪些是适当的、可接受的和/或最优的。在一个或多个实施例中,可描述的是,方法200提供关于速度控制的反馈以避免右心室不同步或可能导致右心室衰竭(右心室到左心室不同步)的其他因素。
如本文所描述的,lvad输出参数可包括以下各项中的至少一项:lvad泵速度、lvad泵吞吐量、lvad泵功率、lvad泵电流、lvad泵电压、泵流入万向架角度、对诸如泵抽吸、患者活动水平变化和生理参数输入之类的事件的自动算法响应、启用/禁止诸如拉瓦瑞循环之类的周期性泵速度调节特征等。在至少一个实施例中,方法200可以被描述为基于根据使用多个体外电极监测的患者的电活动生成的电异质性信息的反馈来调整lvad泵速度。可以在多个不同的lvad泵速度期间监测电活动,并且可以针对在多个不同的lvad泵速度期间监测到的每一组电活动生成电异质性信息。由此,电异质性信息可以与多个不同的lvad泵速度中的每一个相关联。与最优或可接受的电异质性信息相关联的lvad泵速度,或具有最优或可接受的电异质性信息的lvad泵速度可以被确定为要与患者一起使用的lvad泵速度。在一个实施例中,可以选择具有最佳电异质性信息(例如,最低的不同步量、最低的右心室不同步量等)的lvad泵速度。
进一步地,其他因素也可以将一个lvad输出参数与另一个lvad输出参数(诸如例如用于促进原生心脏恢复的设置)区分开,该另一个lvad输出参数诸如是被选择为保留原生功能的流速或对rpm的周期性降低调整,所述对rpm的周期性降低调整用于将更多的心脏做功转移到原生心脏并且用于测试可允许或启用撤回对lvad的支持的恢复。换言之,虽然一个lvad输出参数可以提供最佳或最优电异质性信息,但是可以确定或选择不同的lvad输出参数,因为该电信息可以支持适当的设置以鼓励和加速原生心脏恢复,这可以导致lvad支持的停止和泵撤回而不会产生急性支持不足。
附加地,每当lvad输出参数被确定206时,可以将所确定的lvad输出参数显示208在计算装置或设备的图形用户界面上,诸如参考图1-3所示和所描绘的那些。用户可以看到所确定的lvad输出参数,并且随后可以根据所确定的lvad输出参数使用lvad控制器手动调整lvad。在其他实施例中,可以使用本文所述的系统和方法自动调整lvad输出参数。换言之,对于“单按钮(one-button)”速度滴定,对lvad的反馈可以是自动的。
使用lvad可以影响一个或多个心脏腔室的体积并且还可以影响心脏组织的拉伸。进一步地,心脏组织的传导可以进一步受到体积变化和心脏组织拉伸的影响。又进一步地,激动模式也可受到心脏形状的变化的影响,而不仅是不同步。因此,lvad可以影响还可以被递送到或施加到患者的起搏治疗。
lvad还可以与心脏起搏治疗结合使用,并且因此,lvad和心脏起搏治疗可以被同时调整或滴定,以向患者提供可接受的或最优的心脏治疗。图5中描绘了使用例如图1-3和图7-10中所描绘的系统和装置调整lvad输出参数和起搏参数中的一者或两者的示例性方法250。如所示的,示例性方法250可包括例如使用本文参考图1和图8描述lvad装置151来提供lvad治疗252,以及例如使用本文参考图7-10描述的系统和装置来提供起搏治疗254。lvad治疗252可包括可由本文所述的示例性系统和/或使用示例性系统的用户可调整的多个不同的输出参数。同样的,起搏治疗254可包括可由本文所述的示例性系统和/或使用示例性系统的用户可调整的多个不同的起搏参数。多个不同的起搏参数可包括a-v间期、v-v间期、起搏脉宽、起搏向量、多点起搏向量、起搏电压、起搏配置(例如,双心室起搏、仅左心室起搏、仅右心室起搏)、起搏频率、起搏频率响应参数等。
类似于方法200,示例性方法250可包括使用多个体外电极(诸如例如,本文参考图1-3描述的电极装置110)监测患者的电活动256。可监测电活动256达多个心动周期或心跳。进一步地,可监测电活动256达所选择的时间段(诸如,例如,五秒钟)。可以在不存在lvad治疗的情况下、在不存在心脏起搏治疗的情况下、在不存在lvad治疗和心脏起搏治疗两者的情况下、在lvad治疗期间、在心脏起搏治疗期间、在lvad治疗和心脏起搏治疗两者期间监测电活动256。而且,类似于方法200,方法250可以进一步包括根据所监测的电活动256生成电异质性信息258。所生成的电异质性信息258可以随后用于调整所提供的lvad治疗252的lvad输出参数和所提供的心脏起搏治疗254的心脏起搏治疗参数中的一者或两者。
例如,示例性方法250可以尝试lvad输出参数和心脏起搏参数的多个不同组合中的一个组合,并且可以根据在使用lvad输出参数和心脏起搏参数的“经尝试的”组合期间监测到的电活动来生成电异质性信息258。可以将所生成的电异质性信息与基线电异质性信息或在使用lvad输出参数和心脏起搏参数的不同组合期间生成的电异质性信息进行比较,以确定lvad输出参数和心脏起搏参数的现在或当前的组合是否导致患者的可接受或最优的治疗。
更具体地,例如,lvad泵的速度可以被配置为多个不同的泵速度,并且对于每个泵速度,心脏起搏治疗的右心室预激(preexcitation)可以被调整为多个不同的右心室预激。更具体地,可以将右心室(rv)预激与左心室计时进行比较以最小化隔膜运动,并且可以通过a-v或v-v间期的计时来调整右心室(rv)预激。在另一实施例中,一个或多个设备设置(其包括先前描述的不同设备参数的组合)可被调整成提供最优同步的(例如,最同步的)右心室激动(例如,通过最低rvat或右侧电异质性的其他度量来测得)而在不阻碍lvad操作(例如,在操作lvad速度下不导致抽吸)。由此,可以对lvad和/或rv预激进行编程以优化右心室的贡献。可以针对lvad泵速度和右心室预激的每个不同组合生成电异质性信息,使得可以确定导致可接受的(例如,最优的)电异质性信息的lvad泵速度和右心室预激。所确定的lvad泵速度和右心室预激可以随后被例如显示在图形用户界面上以使得从业者可以看到结果,和/或自动用于对lvad和心脏起搏装置进行编程。进一步地,例如,可以运用lvad响应算法(诸如例如,抽吸响应或速率适配)、周期性速度调节、和/或操作模式特征(诸如拉瓦瑞循环)以测试可能在走动操作期间发生的对电激动模式的急性影响。
还可以使用心音信息(诸如例如,使用如本文参考图1-3描述的声学传感器120捕获)来调整lvad输出参数。在图6中描绘了使用例如图1-3和图7-10中所描绘的系统和装置基于电异质性信息和心音中的一者或两者来调整lvad的示例性方法270。类似于方法250,示例性方法270可包括例如使用本文参考图1和图8描述的lvad装置151来提供lvad272。尽管未在图6中描绘,但是应当理解,方法270还可包括例如使用本文参考图7-10描述的系统和装置来提供起搏治疗,以及使用与方法270相同或类似的方法和过程调整起搏治疗。此外,可以基于电异质性信息和心音信息中的一者或两者与心脏起搏治疗一起或同时地调整或滴定在方法270中被调整或滴定的lvad心脏治疗。
类似于方法200,示例性方法270可包括使用多个体外电极(诸如例如,本文参考图1-3描述的电极装置110)监测患者的电活动274。可监测电活动274达多个心动周期或心跳。进一步地,可监测电活动274达所选择的时间段(诸如,例如,五秒钟)。可以在不存在lvad治疗或在lvad治疗期间监测电活动274。而且,类似于方法200,方法270可以进一步包括根据所监测的电活动274生成电异质性信息278。所生成的电异质性信息288可以随后用于调整280所提供的lvad治疗的lvad输出参数280。
还可以鉴于或基于心音信息调整lvad输出参数280。例如,示例性方法270可以进一步包括使用声学传感器监测心音276。可以使用多个不同类型的装置和系统来监测心音。在至少一个实施例中,可以使用例如本文参考图1-3描述的体外声学传感器120来监测心音。在其他实施例中,可以使用一个或多个植入式设备或不与电极装置110相关联(例如,耦合到电极装置110,是电极装置110的一部分等)的其他声音监测设备来监测心音。此外,在其他实施例中,可以使用不与患者组织接触(例如,不与患者皮肤接触,不附接到、耦合到或靠近心脏组织等)的声音捕获装置来测量或监测心音。
心音监测276可导致代表来自围绕患者的多个不同位置的心音的电信号。此类心音可用于确定lvad输出参数和心脏起搏参数中的一者或两者。心音可用于确定机械心脏功能(例如,力、计时、运动等),诸如但不限于:心脏瓣膜打开、心脏瓣膜关闭、心脏腔室收缩(例如,在去极化期间)、心脏瓣膜舒张(例如,在复极化期间)、瓣膜性回流、右心或左心衰竭的进展、心律失常(诸如,心房纤颤或心室快速性心律失常/纤颤)等。
示例性方法270可以进一步包括:基于所生成的电异质性信息278和监测到的心音276中的一者或两者来调整一个或多个lvad输出参数280。例如,如果心音指示主动脉瓣打开并且电异质性信息指示在左心室的血液动力学排空之前右心室激动,则可以增大lvad泵速度。进一步地,例如,如果存在可能指示左心或右心衰竭的进展的异常心音的证据,则可以改变lvad泵速度。例如,右心室第三心音可以指示右心室功能障碍并且可以将lvad速度滴定得更低和/或可以调整起搏参数以降低电异质性。
在至少一个实施例中,示例性方法200可包括:基于监测到的心音确定至少一个心脏瓣膜是打开还是关闭,并且随后调整lvad的输出参数以允许心脏瓣膜的至少一些打开。更具体地,可以分析声学信号上的第二心音的特征以检测主动脉瓣从打开到关闭的转变,并且可以针对各种lvad速度监测该第二心音特征中的改变以检测瓣膜不打开的速度。例如,可编程lvad速度的阈值可被设定为仍允许主动脉瓣打开的最大速度。
示例性方法270可以调整lvad,并且方法270可以循环,以再次在lvad治疗的递送期间监测电活动和心音274、276,基于监测到的电活动生成电异质性信息278,并且进一步基于此确定和调整lvad输出参数280。
本文所述的示例性系统、装置和方法还可用于滴定或调整药物,该药物可以与本文所述的lvad和起搏治疗一起使用。例如,某些药物可以影响心脏激动,并且由此,示例性系统、装置和方法可用于为具有例如具有射血分数保留的心力衰竭、具有降低的射血分数的心力衰竭等的患者在相同或相似的时间处滴定或调整lvad、心脏起搏治疗和药物。
进一步地,本文所述的示例性系统、装置和方法还可用于对具有心房不同步的患者的左心房相对(versus)右心房起搏的滴定或调整。
而且,本文所述的系统、装置和方法还可用于测量或监测患者的恢复,以例如协助评价是否可以将lvad从患者体内移除。换言之,示例性系统、装置和方法可协助确定患者是否仍需要lvad心脏治疗。
如本文所述的,本文所述的示例性系统和方法可参照植入式医疗设备(imd)和/或lvad的植入和配置来使用。例如,可以结合本文参照图7-10描述的示例性治疗系统10使用示例性系统和方法。
图7是示出了可用于向患者14递送起搏治疗的示例性治疗系统10的概念图。患者14可以是但不一定是人。治疗系统10可包括可以被耦合到引线18、20、22的植入式医疗设备16(imd)。imd16可以是例如植入式起搏器、心脏复律器和/或除颤器,其经由耦合到引线18、20、22中的一个或多个的电极向患者14的心脏12递送或提供电信号和/或从患者14的心脏12测量或监测电信号。
引线18、20、22延伸至患者14的心脏12中以感测心脏12的电活动和/或向心脏12递送电刺激。在图11中所示的示例中,右心室(rv)引线18延伸通过一个或多个静脉(未示出)、上腔静脉(未示出)和右心房26,并进入右心室28。左心室(lv)冠状窦引线20延伸通过一个或多个静脉、腔静脉、右心房26,并进入冠状窦30到达与心脏12的左心室32的游离壁相邻的区域。右心房(ra)引线22延伸通过一个或多个静脉和腔静脉,并且进入心脏12的右心房26。尽管系统10包括rv引线18,但是要理解的是,本文描述的示例性系统以及方法可不利用被定位在rv引线18上的用于感测和/或起搏的电极。进一步地,要理解的是,系统10仅是一个示例,并且本文描述的示例性系统和方法可利用不包括rv引线18(例如,用于感测和/或起搏)的系统。
imd16可经由耦合到引线18、20、22中的至少一个的电极来感测伴随于心脏12的去极化和复极化的电信号等。在一些示例中,imd16基于在心脏12内感知到的电信号来向心脏12提供起搏治疗(例如起搏脉冲)。imd16可以可操作用于调整与起搏治疗相关联的一个或多个参数,诸如,例如a-v延迟和其他各种计时、脉冲宽度、振幅、电压、脉冲串长度等。进一步地,imd16可以可操作用于使用各种电极配置来递送起搏治疗,所述电极配置可以是单极的、双极的、四极的、或进一步多极的。例如,多极引线可以包括可用于递送起搏治疗的若干电极。因此,多极引线系统可提供或供应多个电向量以从其起搏。起搏向量可以包括:至少一个阴极,该至少一个阴极可以是定位在至少一条引线上的至少一个电极;以及至少一个阳极,该至少一个阳极可以是定位在至少一条引线(例如,同一条引线或不相同的引线)上和/或在imd的壳体或罐上的至少一个电极。虽然由于起搏治疗引起的对心脏功能的改善可以主要取决于阴极,但是如阻抗、起搏阈电压、电流消耗、寿命等电参数可能更依赖于包括阴极和阳极两者的起搏向量。imd16还可经由位于引线18、20、22中的至少一个引线上的电极来提供除颤治疗和/或心脏复律治疗。进一步地,imd16可检测心脏12的心律失常(诸如,心室28、32的纤颤),并以电脉冲的形式将除颤治疗递送至心脏12。在一些示例中,可对imd16进行编程以递送累进的治疗(例如,具有增大的能量水平的脉冲),直到心脏12的纤颤停止为止。
图8是经由心脏引线耦合到imd16并且附加地耦合到示例性lvad150的患者心脏的局部剖视图。lvad150包括流入管道173,该流入管道173通过外科手术被植入到lv的心尖区域,使得正常充盈lv的血液体积被至少部分地卸载到lvad150的中心泵送腔室176。在致动时,泵送腔室176通过被耦合到动脉系统(通常耦合到升主动脉或降主动脉)的流出管道174喷射血液。流入管道173和流出管道174可包括阀门,以便控制血液流入和流出lvad150的方向。lvad150的致动可以是气动的、液压的、电磁的或通过本领域已知的其他方式。lvad控制器或控制和电力单元152可以提供用于致动lvad150的电力。控制器152可以附加地被配置成关于时间、压力、流速或其他操作因素来控制或执行lvad150的致动。控制器(例如,控制和电力单元)152可以在完全植入式系统中与lvad150结合,或者控制器152可以位于患者身体外部,具有用于致动lvad150的经皮设置的任何必要连接。
在图9所示的实施例中,压力换能器168跨心肌地定位在左心室中。压力换能器168由经由连接器耦合到imd16的引线166携载。在放置lvad期间,lv的暴露可以允许将压力传感器直接放置在lv中的机会。替代地,传感器可被定位在心脏静脉中(如先前描述的)或其他位置以用于测量lvp的关联(correlate)。
图8中的其他类似标记的部件对应于图7和图9-10中的那些部件。在该实施例中的imd14可以被描述为从引线18接收egm和rvp信号并且从引线166接收lvp信号。可以在imd16中存储和处理rvp和lvp信号以用于检测心室同步的度量。imd16以及图1的计算装置140和远程计算设备160可以与lvad控制器150遥测通信,使得可以根据从imd16、计算装置140和远程计算设备160接收的命令来调整lvad操作参数。进一步地,lvad控制器152可以接收从imd16传输的压力相关的数据,并且可以处理此类数据以确定心室同步的度量并基于该度量调整lvad致动时间。
图9a-9b是更详细地示出了图7的治疗系统10的imd16和引线18、20、22的概念图。引线18、20、22可经由连接器块34被电耦合到imd16的治疗递送模块(例如,以供递送起搏治疗)、感测模块(例如,以供从一个或多个电极感测一个或多个信号)和/或任何其他模块。在一些示例中,引线18、20、22的近侧端可包括电触头,这些电触头电耦合到imd16的连接器块34中的相应的电触头。另外,在一些示例中,引线18、20、22可借助于固定螺钉、连接销或另一种适当的机械耦合机构被机械地耦合到连接器块34。
引线18、20、22中的每根引线包括细长的绝缘引线体,该绝缘引线体可以携载通过隔离件(例如管状绝缘鞘)而彼此分开的多个导体(例如,同心盘绕导体、直导体等)。在示出的示例中,双极电极40、42被定位在引线18的远侧端附近。此外,双极电极44、45、46、47被定位于引线20的远侧端附近,并且双极电极48、50被定位于引线22的远侧端附近。
电极40、44、45、46、47、48可采用环形电极的形式,并且电极42、50可采用分别可伸缩地安装在绝缘电极头52、54、56内的可延伸螺旋尖端电极的形式。电极40、42、44、45、46、47、48、50中的每一个可被电耦合到其相关联的引线18、20、22的引线体内的导体(例如,缠绕的和/或直的)中的相应一个导体,并由此被耦合到引线18、20、22的近侧端上的电触头中的相应一个电触头。
此外,电极44、45、46和47可具有约5.3mm2到约5.8mm2的电极表面积。电极44、45、46和47还可以分别被称为lv1、lv2、lv3和lv4。引线20上的lv电极(即左心室电极1(lv1)44、左心室电极2(lv2)45、左心室电极3(lv3)46、左心室4(lv4)47等)可按可变的距离间隔开。例如,电极44可与电极45距离例如约21毫米(mm),电极45和46可以彼此间隔例如约1.3mm至约1.5mm的距离,并且电极46和47可以彼此间隔例如20mm至约21mm的距离。
电极40、42、44、45、46、47、48、50可进一步用于感测伴随心脏12的去极化和复极化的电信号(例如,电描记图(egm)内的形态波形)。感知电信号可被用于调整一个或多个起搏参数,诸如,例如a-v间期、v-v间期等,以提供最佳和/或有效的心脏功能。这些电信号经由相应的引线18、20、22而被传导至imd16。在一些示例中,imd16还可以经由电极40、42、44、45、46、47、48、50递送起搏脉冲以引起患者的心脏12的心脏组织的去极化。在一些示例中,如图9a中所示,imd16包括一个或多个壳体电极,诸如壳体电极58,其可与imd16的壳体60(比如气密密封壳体)的外表面一体地形成或以其他方式耦合到该壳体60。电极40、42、44、45、46、47、48、50中的任何电极可用于单极感测或与壳体电极58相组合地进行起搏。换言之,电极40、42、44、45、46、47、48、50、58中的任一者可向结合地用于形成感测向量,例如,可用于评估和/或分析起搏治疗的有效性的感测向量。本领域技术人员将理解的是,还可以选择其他电极来限定或用于起搏和感测向量。进一步地,当不被用于递送起搏治疗时,电极40、42、44、45、46、47、48、50、58中的任意电极可用于在起搏治疗期间感测电活动。
如参照图9a进一步详细描述的,壳体60可封围治疗递送模块,该治疗递送模块可包括用于生成心脏起搏脉冲和除颤或心脏复律电击的刺激发生器、以及用于监测患者心脏的电信号(例如,患者的心律)的感测模块。引线18、20、22还可以分别包括可采取线圈形式的细长电极62、64、66。imd16可以经由细长电极62、64、66和壳体电极58的任何组合来向心脏12递送除颤电击。电极58、62、64、66还可以用于向心脏12递送心脏复律脉冲。进一步地,电极62、64、66可以由任何适当的导电材料制成,诸如,但不限于铂、铂合金、和/或已知可用于植入式除颤电极的其他材料。由于电极62、64、66一般不被配置成递送起搏治疗,因此电极62、64、66中的任意电极可用于感测电活动(例如,用于确定电极有效性、用于分析起搏治疗有效性等)并且可与电极40、42、44、45、46、47、48、50、58中的任意电极组合使用。在至少一个实施例中,rv细长电极62可用于在起搏治疗的递送期间感测患者的心脏的电活动(例如,与壳体电极58组合,或与除颤电极至壳体电极向量组合)。
图7-10中所示出的示例性治疗系统10的配置仅为几个示例。在其他示例中,替代图9a所示的经静脉引线18、20、22或除了图9a所示的经静脉引线18、20、22之外,治疗系统可包括心外膜引线和/或贴片电极。额外地,在其他示例中,治疗系统10可被植入在心脏间隙(cardiacspace)中/周围,而不采用经静脉引线(例如,无引线/或无线起搏系统),或采用被植入(例如,经静脉植入或使用入路(approach)植入)到心脏的左腔室中的引线(除了如图9a所示的被放置到心脏右腔室中的经静脉引线之外或代替如图9a所示的被放置到心脏右腔室中的经静脉引线)。示例性无引线系统可在于2014年2月5日提交的并且题为“systemsandmethodsforleadlesscardiacresynchronizationtherapy(用于无引线心脏再同步治疗的系统以及方法)”的美国专利申请序列第14/173,288号中描述,该专利申请以其整体通过引用并入本文。进一步地,在一个或多个实施例中,imd16不需要被植入至患者14体内。例如,imd16可以经由延伸通过患者14的皮肤至心脏12内或外的多个位置的经皮引线向心脏12递送各种心脏治疗。在一个或多个实施例中,系统10可采用无线起搏(例如,使用经由超声、电感耦合、rf等的到心脏内的起搏部件(多个)的能量传输)和使用在罐/壳体上和/或在皮下引线上的电极感测心脏激动。
在向心脏12提供电刺激治疗的治疗系统的其他示例中,此类治疗系统可以包括耦合到imd16的任何适当数量的引线,并且该引线中的每条引线可以延伸至心脏12内或附近的任何位置。例如,治疗系统的其他示例可包括少于或多于三个的经静脉引线。在至少一个实施例中,向心脏12提供起搏或电刺激治疗的治疗系统可仅通过使用或包括被定位在左心室中的感测或起搏电极来提供左单心室起搏治疗。在这些左单心室起搏系统中,至少一个起搏和/或感测电极可被定位在患者的左心室中,并且至少一个起搏和/或感测电极可被定位在右心房以及左心房中的一个或两者中。另进一步地,其他治疗系统可包括从imd16延伸进入右心房26或右心室28的单个引线,或延伸进入右心房26和右心室28中的相应一个的两根引线。
图10a是imd16的一个示例性配置的功能框图。如所示的,imd16可以包括控制模块81、治疗递送模块84(例如,其可以包括刺激发生器)、感测模块86和电源90。
控制模块81可以包括处理器80、存储器82以及遥测模块88。存储器82可以包括计算机可读指令,当例如由处理器80执行时,这些计算机可读指令使imd16和/或控制模块81执行本文所描述的归因于imd16和/或控制模块81的各种功能。进一步地,存储器82可包括任何易失性、非易失性、磁的、光的、和/或电的介质,诸如随机存取存储器(ram)、只读存储器(rom)、非易失性ram(nvram)、电可擦除可编程rom(eeprom)、闪存存储器、和/或任何其他数字介质。示例性夺获管理模块可以是在2010年3月23日颁发的题为“lvthresholdmeasurementandcapturemanagement(lv阈值测量和夺获管理)”的美国专利第7,684,863号中描述的左心室夺获管理(lvcm)模块,该专利通过引用以其整体包含在此。
控制模块81的处理器80可包括以下各项中的任一项或多项:微处理器、控制器、数字信号处理器(dsp)、专用集成电路(asic)、现场可编程门阵列(fpga)、和/或等效的分立或集成的逻辑电路系统。在一些示例中,处理器80可包括多个部件,诸如以下各项的任意组合:一个或多个微处理器、一个或多个控制器、一个或多个dsp、一个或多个asic、和/或一个或多个fpga、以及其他分立或集成逻辑电路系统。归因于本文中的处理器80的功能可具体化为软件、固件、硬件、或它们的任意组合。
控制模块81可控制治疗递送模块84根据可存储在存储器82中的选定的一个或多个治疗程序向心脏12递送治疗(例如,诸如起搏之类的电刺激治疗)。此外,具体地,控制模块81(例如,处理器80)可控制由治疗递送模块84递送的电刺激的各种参数(诸如,a-v延迟、v-v延迟、具有振幅、脉冲宽度、频率的起搏脉冲、或电极极性等),其可由一个或多个所选择的治疗程序指定(例如,a-v和/或v-v延迟调整程序、起搏治疗程序、起搏恢复程序、夺获管理程序等)。如所示,治疗递送模块84例如经由相应引线18、20、22的导体或在壳体电极58的情况下经由设置在imd16的壳体60内的电导体而被电耦合到电极40、42、44、45、46、47、48、50、58、62、64、66。治疗递送模块84可以被配置用于生成诸如起搏治疗之类的电刺激治疗并使用电极40、42、44、45、46、47、48、50、58、62、64、66中的一个或多个电极向心脏12递送诸如起搏治疗之类的电刺激治疗。
例如,治疗递送模块84可经由耦合到引线18、20、22的环形电极40、44、45、46、47、48和/或经由引线18、22的螺旋尖端电极42、50来递送起搏刺激(例如,起搏脉冲)。进一步地,例如,治疗递送模块84可经由电极58、62、64、66中的至少两个来将除颤电击递送至心脏12。在一些示例中,治疗递送模块84可被配置成以电脉冲形式来递送起搏、心脏复律或除颤刺激。在其他示例中,治疗递送模块84可被配置成以其他信号的形式(诸如,正弦波、方波和/或其他基本上连续的时间信号)来递送这些类型的刺激中的一种或多种。
imd16可进一步包括开关模块85,并且控制模块81(例如,处理器80)可使用开关模块85来例如经由数据/地址总线来选择可用的电极中的哪些被用于递送治疗(诸如,用于起搏治疗的起搏脉冲),或可用的电极中的哪些被用于感测。开关模块85可包括开关阵列、开关矩阵、多路复用器、或适用于选择性地将感测模块86和/或治疗递送模块84耦合到一个或多个选定电极的任何其他类型的开关设备。更具体地,治疗递送模块84可包括多个起搏输出电路。可例如使用开关模块85来选择性地将多个起搏输出电路中的每一个起搏输出电路耦合到电极40、42、44、45、46、47、48、50、58、62、64、66中的一个或多个(例如,使用双极或多极起搏向量来递送治疗的一对电极)。即,可使用开关模块85来将每个电极选择性地耦合到治疗递送模块的起搏输出电路中的一个。
感测模块86被耦合(例如,电耦合)至感测装置,该感测装置以及额外的感测装置可以包括电极40、42、44、45、46、47、48、50、58、62、64、66以便监测心脏12的电活动,例如,心电图(ecg)/电描记图(egm)信号等。ecg/egm信号可用于测量或监测激动时间(例如,心室激动时间等)、心率(hr)、心率变异性(hrv)、心率震荡(hrt)、减速/加速能力、减速序列发生率、t波交替(twa)、p波到p波的间期(也被称为p-p间期或a-a间期)、r波到r波的间期(也被称为r-r间期或v-v间期)、p波到qrs波群的间期(也被称为p-r间期、a-v间期或p-q间期)、qrs波群形态、st段(即,连接qrs波群和t波的段)、t波改变、qt间期、电向量等。
开关模块85还可以与感测模块86一起用于选择使用或启用可用电极中的哪些可用电极来例如感测患者心脏的电活动(例如,使用电极40、42、44、45、46、47、48、50、58、62、64、66的任意组合感测患者心脏的一个或多个电向量)。同样地,开关模块85还可以与感测模块86一起用于选择不使用(例如,禁用)可用电极中的哪些可用电极来例如感测患者心脏的电活动(例如,使用电极40、42、44、45、46、47、48、50、58、62、64、66的任意组合感测患者心脏的一个或多个电向量)等。在一些示例中,控制模块81可经由感测模块86内的开关模块(例如,通过经由数据/地址总线来提供信号)来选择用作感测电极的电极。
在一些示例中,感测模块86包括通道,该通道包括具有比r波或p波放大器相对更宽的通带的放大器。可以向多路复用器提供来自选定感测电极的信号,并且之后由模数转换器将所述信号转换成多位数字信号以便例如作为电描记图(egm)而存储在存储器82中。在一些示例中,对此类egm在存储器82中的存储可处于直接存储器存取电路的控制下。
在一些示例中,控制模块81可作为中断驱动设备而操作,并且可对来自起搏器计时和控制模块的中断作出响应,其中,该中断可与感知到的p波和r波的出现以及心脏起搏脉冲的生成相对应。可由处理器80执行任何必要的数学计算,并且由起搏器计时和控制模块控制的值或间期的任何更新可在此类中断之后发生。存储器82的一部分可以被配置为能够保留一个或多个系列的测得间期(例如,固有a-v传导时间)的多个再循环缓冲器,可响应于起搏或感测中断的发生而通过例如处理器80分析所述一个或多个系列的测得间期以便确定患者心脏12当前是否正展现出房性或室性快速心律失常。
起搏计时和控制模块可包括可编程计数器,该可编程计数器控制与ddd、vvi、dvi、vdd、aai、ddi、dddr、vvir、dvir、vddr、aair、ddir以及单腔室起搏和双腔室起搏的其他模式相关联的基础时间间期。在前面提到的起搏模式中,“d”可指示双腔室,“v”可指示心室,“i”可指示被禁止的起搏(例如无起搏),而“a”可指示心房。起搏模式中的第一个字母可指示被起搏的腔室,第二个字母可指示在其中电信号被感知的腔室,而第三个字母可指示在其中提供对感测的响应的腔室。
控制模块81的遥测模块88可以包括用于与诸如编程器等另一设备通信的任何适当的硬件、固件、软件或其任何组合。例如,在处理器80的控制下,遥测模块88可以借助于天线(所述天线可以是内部和/或外部天线)来接收来自编程器的下行链路遥测并向编程器发送上行链路遥测。处理器80可例如经由地址/数据总线提供要通过上行链路传送至编程器的数据以及针对遥测模块88内的遥测电路的控制信号。在一些示例中,遥测模块88可经由多路复用器将所接收的数据提供至处理器80。
imd16的各种部件被进一步耦合到电源90,该电源90可包括可再充电的和不可再充电的电池。可选择不可再充电的电池以维持达若干年,而可再充电的电池可例如每天或每周感应地从外部设备进行充电。
图10b是imd16的功能框图的另一实施例。图10b描绘了双极ra引线22、双极rv引线18以及双极lvcs引线20,没有lacs起搏/感测电极,并且与植入式脉冲发生器(ipg)电路31耦合,该植入式脉冲发生器电路31具有起搏领域所公知的可编程模式以及双心室ddd/r类型的参数。进而,传感器信号处理电路91间接地耦合到计时电路43并且经由数据和控制总线耦合到微计算机电路系统33。在通常被划分成微计算机电路33和起搏电路21的功能框图中示出了ipg电路31。起搏电路21包括数字控制器/定时器电路43、输出放大器电路51、感测放大器电路55、rf遥测收发机41、活动传感器电路35以及以下描述的多个其他电路和部件。
晶体振荡器电路89为起搏电路21提供基本计时时钟,而电池29则提供电力。上电复位电路87响应于电路到电池的用于定义初始的操作条件的初始连接,并且类似地响应于检测到低电池条件而重置设备的操作状态。参考模式电路37为起搏电路21内的模拟电路生成稳定的电压参考以及电流。模数转换器(adc)以及多路复用器电路39数字化模拟信号以及电压,以提供例如来自感测放大器55的心脏信号的实时遥测,以用于经由rf发射器以及接收器电路41进行上行链路传输。电压参考和偏置电路37、adc和多路复用器39、上电复位电路87和晶体振荡器电路89可对应于示例性植入式心脏起搏器中使用的那些中的任一个。
如果ipg被编程为频率应答(rateresponsive)模式,则由一个或多个生理传感器输出的信号被用作频率控制参数(rcp)以导出生理逸搏间期。例如,与在描绘的、示例性ipg电路31中的患者活动传感器(pas)电路35中产生的患者的活动水平成比例地调整逸搏间期。患者活动传感器27被耦合到ipg壳体并且可以采取压电晶体换能器的形式。患者活动传感器27的输出信号可被处理并且被用作rcp。传感器27响应于感知到的身体活动而生成电信号,这些电信号由活动电路35处理并被提供给数字控制器/定时器电路43。活动电路35以及相关联的传感器27可与于1991年10月1日颁布的题为“methodandapparatusforimplementingactivitysensinginapulsegenerator(用于在脉冲发生器中实现活动感测的方法和装置)”的美国专利第5,052,388号以及于1984年1月31日颁发的并且题为“rateadaptivepacer(频率自适应起搏器)”的美国专利第4,428,378号中公开的电路系统对应,上述专利均通过引用以其整体包含在此。相似地,在本文描述的示例性系统、装置和方法可以结合替代类型的传感器(诸如,氧合传感器、压力传感器、ph传感器和呼吸传感器)来实践,以用于提供频率应答起搏功能。替代地,qt时间可用作频率指示参数,在这种情况下不需要额外的传感器。类似地,在本文描述的示例性实施例还可以在非频率应答起搏器中实践。
通过遥测天线57和相关联的rf收发器41完成向外部编程器或者从所述外部编程器的数据传输,该相关联的rf收发器41用于解调接收到的下行链路遥测并且用于传送上行链路遥测两者。上行链路遥测能力可包括用于传送所存储的数字信息(例如,操作模式和参数、egm直方图和其他事件、以及指示心房和心室中的感知到的和起搏的去极化的发生的心房和/或心室电活动和标记通道脉冲的实时egm)的能力。
微计算机33包含微处理器80和相关联的系统时钟,并且分别包含处理器上ram和rom芯片82a和82b。此外,微计算机电路33包括单独的ram/rom芯片82c以提供额外的存储器容量。微处理器80通常以减小的功率消耗模式来进行操作,并且是中断驱动的。微处理器80响应于限定的中断事件而被唤醒,该限定的中断事件可包括由数字定时器/控制器电路43中的定时器生成的a-触发(tirg)信号、rv-触发信号、lv-触发信号,以及由感测放大器电路55生成的a-事件信号、rv-事件信号和lv-事件信号等等。由微计算机电路33根据被编程写入的参数值和操作模式通过数据和控制总线来控制由数字控制器/定时器电路43进行倒计时(timeout)的间期和延迟的特定值。此外,如果被编程成作为频率应答起搏器来操作,则可以例如每周期或每两秒提供定时中断,以便允许微处理器分析活动传感器数据并更新基本a-a、v-a或v-v逸搏间期(如适用)。此外,微处理器80还可用于限定可变的、可操作的a-v延迟间期和/或v-v间期、以及被递送至心室和/或心房的能量。
在一个实施例中,微处理器80是适合于以常规方式取得并执行存储在ram/rom单元82中的指令的定制微处理器。然而,所设想的是,其他实现可适用于实践本发明。例如,现成的可购得的微处理器或微控制器、或者定制的专用硬接线逻辑或状态机型电路可以执行微处理器80的功能。
数字控制器/定时器电路43在微计算机33的总体控制下进行操作以便控制起搏电路321内的计时功能和其他功能,并且包括一组计时电路和相关联逻辑电路,描绘了该一组计时电路和相关联逻辑电路中的与本发明有关的某些电路。所描绘的计时电路包括uri/lri定时器83a、v-v延迟定时器83b、用于对过去的v-事件到v-事件间期或v-事件到a-事件间期或v-v传导间期进行计时的固有间期定时器83c、用于对a-a、v-a和/或v-v起搏逸搏间期进行计时的逸搏间期定时器83d、用于自在前的a-事件或a-触发的a-lvp延迟(或a-rvp延迟)进行计时的a-v延迟间期定时器83e、用于对心室后时间周期进行计时的心室后定时器83f、以及日期/时间时钟83g。
用一个心室腔的适当延迟间期(例如,a-rvp延迟或a-lvp延迟)来加载a-v延迟间期定时器83e,以便从在前的a-起搏或a-事件开始倒计时。间期定时器83e触发起搏刺激递送,并且可以基于一个或多个之前的心动周期(或来自针对给定患者根据经验导出的数据集)。
事件后定时器83f对rv-事件或lv-事件或rv-触发或lv-触发之后的心室后时间段以及a-事件或a-触发之后的心房后时间段进行倒计时。事件后时间段的持续时间还可以被选择作为存储在微计算机33中的可编程参数。心室后时间段包括pvarp、心房后心室消隐期(pavbp)、心室消隐期(vbp)、心室后心房消隐期(pvarp)和心室不应期(vrp),但是也可以至少部分地根据起搏引擎中采用的操作电路系统而适当地定义其他时段。心房后时间周期包括心房不应期(arp)(在心房不应期期间,为了重置任何a-v延迟的目的而忽略a-事件)以及心房消隐期(abp)(在该心房消隐期期间,禁用心房感测)。应当注意的是,心房后时间周期和a-v延迟的开始可与每个a-事件或a-触发的开始或结束基本上同时开始,或者在a-触发的情况下,在可以在a-触发之后的a-起搏结束时开始。类似地,心室后时间段和v-a逸搏间期的开始可以与v-事件或v-触发的开始或结束基本上同时开始,或者在v-触发的情况下,在可以在v-触发之后的v-起搏结束时开始。微处理器80还可选地计算a-v延迟、v-v延迟、心室后时间周期和心房后时间周期,它们随响应于(多个)rcp、固有a-v传导时间、固有心率和/或任何其他参数或度量而建立的基于传感器的逸搏间期而变化。
输出放大器电路51包含ra起搏脉冲发生器(以及la起搏脉冲发生器,如果提供la起搏的话)、rv起搏脉冲发生器、lv起搏脉冲发生器、和/或配置成提供心房和心室起搏的任何其他脉冲发生器。为了触发rv-起搏或lv-起搏脉冲的生成,数字控制器/定时器电路43在a-rvp延迟的超时(在rv预激的情况下)时生成rv-触发信号或在a-lvp延迟的超时(在lv预激的情况下)时生成lv-触发,所述a-rvp延迟的超时和a-lvp延迟的超时由av延迟间期定时器83e(或v-v延迟定时器83b)提供。类似地,在由逸搏间期定时器83d计时的v-a逸搏间期结束时,数字控制器/定时器电路43生成触发ra-起搏脉冲的输出的ra-触发信号(或触发la-起搏脉冲的输出的la-触发信号,如果提供的话)。
输出放大器电路51包括开关电路,以用于将来自引线导体与ind-罐(ind-can)电极20之间的所选择的起搏电极对耦合到ra起搏脉冲发生器(和la起搏脉冲发生器,如果提供的话)、rv起搏脉冲发生器和lv起搏脉冲发生器。起搏/感测电极对选择和控制电路53选择要与输出放大器电路51内的心房和心室输出放大器耦合的引线导体和相关联的起搏电极对,以用于完成ra、la、rv和lv起搏。
感测放大器电路55包含用于心房和心室起搏和感测的感测放大器。高阻抗p波和r波感测放大器可以被用于放大压差信号,该压差信号由心脏去极化波阵面的通过而在感测电极对两端生成的。高阻抗感测放大器使用高增益来放大低振幅信号,并且依赖于通带滤波器、时域滤波、以及振幅阈比较来从背景电噪声中区分p波或r波。数字控制器/定时器电路43控制心房和心室感测放大器55的灵敏度设置。
感测放大器通常在向起搏系统的起搏电极中的任一个起搏电极递送起搏脉冲之前、期间和之后的消隐期期间与感测电极解耦合,以避免感测放大器的饱和。感测放大器电路55包括消隐电路,该消隐电路用于在abp、pvabp和vbp期间将所选择的引线导体对和ind-罐电极20与ra感测放大器(以及la感测放大器(如果提供的话))、rv感测放大器和lv感测放大器的输入解耦合。感测放大器电路55还包括开关电路,该开关电路用于将所选择的感测电极引线导体和ind-罐电极20耦合到ra感测放大器(以及la感测放大器,如果提供的话)、rv感测放大器和lv感测放大器。同样,感测电极选择和控制电路53选择用来与输出放大器电路51和感测放大器电路55内的心房和心室感测放大器耦合的导体和相关联的感测电极对,以用于沿着所期望的单级和双极感测向量完成ra、la、rv和lv感测。
由ra感测放大器感知到的ra-感测信号中的右心房去极化或p波导致被传送至数字控制器/定时器电路43的ra-事件信号。类似地,由la感测放大器(如果提供的话)感知到的la-感测信号中的左心房去极化或p波导致被传送至数字控制器/定时器电路43的la-事件信号。由心室感测放大器感知到的rv-感测信号中的心室去极化或r波导致被传送至数字控制器/定时器电路43的rv-事件信号。类似地,由心室感测放大器感知到的lv-感测信号中的心室去极化或r波导致被传送至数字控制器/定时器电路43的lv-事件信号。rv-事件信号、lv-事件信号、以及ra-事件信号、la-感测信号可以是应答的(refractory)或不应的(non-refractory),并且可以不经意地由电噪声信号或异常传导的去极化波触发,而不是由真正的r波或p波触发。
本公开中描述的技术(包括归因于imd16、计算装置140、远程计算设备160和/或各种组成部件的技术)可以至少部分地在硬件、软件、固件或其任何组合中实现。例如,这些技术的各方面可在一个或多个处理电路系统和/或一个或多个处理器内实现,所述一个或多个处理电路系统和/或一个或多个处理器包括一个或多个微处理器、dsp、asic、fpga、或任何其他等效的集成或分立逻辑电路系统,以及具体化在编程器中的此类部件(诸如,医生编程器或患者编程器、刺激器、图像处理设备或其他设备)的任何组合。术语“模块”、“处理器”或“处理电路系统”一般可指独立的或结合其他逻辑电路系统的任何前述逻辑电路系统、或任何其他等效电路系统。
此类硬件、软件和/或固件可在相同的设备内或在分开的设备内实现以支持本公开所描述的各种操作和功能。此外,所描述的单元、模块或部件中的任一者可一起被实现,或可被单独地实现为分立但可互操作的逻辑设备。将不同的特征描绘为模块或单元旨在强调不同的功能方面,且并不一定暗示这种模块或单元必须由分开的硬件或软件部件来实现。而是,与一个或多个模块或单元相关联的功能可由分开的硬件或软件部件来执行,或可集成在共同或分开的硬件或软件部件内。
当在软件中实现时,归因于本公开中描述的系统、设备和技术的功能可具体化为计算机可读介质(诸如,ram、rom、nvram、eeprom、闪存存储器、磁数据存储介质、光数据存储介质,等等)上的指令。可由一个或多个处理器执行这些指令以支持本公开中所描述的功能的一个或多个方面。
说明性实施例
实施例1:一种系统,包括:
电极装置,该电极装置包括多个体外电极,用于监测来自患者的组织的心脏电活动;以及
计算装置,该计算装置包括处理电路系统并且被耦合到电极装置,并且该计算装置被配置成用于:
使用多个体外电极至少在使用左心室辅助设备(lvad)递送心脏治疗期间监测心脏电活动;
基于监测到的电活动生成电异质性信息;以及
基于所生成的电异质性信息确定lvad的输出参数。
实施例2:一种方法,包括:
使用多个体外电极至少在使用左心室辅助设备(lvad)递送心脏治疗期间监测来自患者组织的电活动;
基于监测到的电活动生成电异质性信息;以及
基于所生成的电异质性信息确定lvad的输出参数。
实施例3:如实施例1-2中任一项所述的系统或方法,其中,多个体外电极包括以阵列定位的体表电极,该体表电极被配置成位于患者的躯干的皮肤附近。
实施例4:如实施例1-3中任一项所述的系统或方法,其中,所述系统进一步包括显示器,其中,所述显示器包括图形用户界面,所述图形用户界面被配置成协助用户评估患者心脏健康,其中,所述计算装置被进一步配置成在所述图形用户界面上显示电异质性信息和lvad的所确定的输出参数。
实施例5:如实施例1-4中任一项所述的系统或方法,其中,所述计算装置被进一步配置成执行或所述方法进一步包括:根据所确定的输出参数来调整lvad。
实施例6:如实施例1-5中任一项所述的系统或方法,其中,所述电异质性信息包括指示右心室不同步的右心室电异质性信息,所述右心室电异质性信息是使用由多个体外电极中定位在患者的右躯干附近的右体外电极组监测到的电活动而被生成的。
实施例7:实施例6的系统或方法,其中,所述电异质性信息包括由右体外电极组监测到的右心室电激动时间的平均值。
实施例8:如实施例1-7中任一项所述的系统或方法,其中,所述电异质性信息包括指示隔膜不同步的隔膜电异质性信息,所述隔膜电异质性信息是使用由多个体外电极中定位在患者的胸骨或脊柱附近的中心体外电极组监测到的电活动而被生成的。
实施例9:实施例8的系统或方法,其中基于所生成的电异质性信息确定lvad的输出参数包括:将隔膜中心电异质性信息与从患者的胸骨或脊柱的右侧或左侧的一组体外电极生成的其他电异质性信息进行比较。
实施例10:如实施例1-9中任一项所述的系统或方法,其中,所述计算装置被进一步配置成执行或所述方法进一步包括:基于所生成的电异质性信息确定要在与lvad相结合的心脏起搏治疗中使用的一个或多个心脏起搏参数。
实施例11:实施例10的系统或方法,其中,所述一个或多个起搏参数包括右心室预激。
实施例12:如实施例1-11中任一项所述的系统或方法,进一步包括或提供声学传感器,该声学传感器包括至少一个换能器以监测患者的心音,其中所述计算装置被进一步配置成执行或所述方法进一步包括:基于在使用lvad递送心脏治疗期间监测到的患者的心音来确定lvad的输出参数。
实施例13:实施例12的系统或方法,其中,基于在使用lvad递送心脏治疗期间监测到的患者的心音来确定lvad的输出参数包括:
基于监测到的心音确定心脏瓣膜是打开还是关闭;以及
调整lvad的输出参数以允许心脏瓣膜的至少一些打开。
实施例14:如实施例12-13中任一项所述的系统或方法,进一步包括显示器或提供显示器,其中所述显示器包括配置成协助用户评估患者心脏健康的图形用户界面,其中所述计算装置被进一步配置成基于在使用lvad递送心脏治疗期间监测到的患者的心音来显示心音信息。
已经参照说明性实施例提供了本公开,并且本公开不旨在以限制性意义进行解释。如先前所述,本领域技术人员将会认识到,其他各种说明性应用可以使用本文所描述的技术来利用本文所描述的装置和方法的有益特性。说明性实施例的各种修改以及本公开的附加实施例在参照本说明书时将会是显而易见的。
- 还没有人留言评论。精彩留言会获得点赞!