直接AMPK活化剂化合物的制作方法
引言
amp-活化的蛋白激酶(ampk)是能量稳态的进化保守的主调节子,其协调代谢途径以便平衡营养物质供应与能量需求。ampk被认为是抵抗日益流行的代谢疾病诸如肥胖症、2型糖尿病、心血管疾病的关键药物目标。
ampk活性存在于所有组织中,包括肝脏、肾、肌肉、肺和脑(pmid:10698692)。就结构而言,ampk为由催化亚基(α)和两个调节亚基(β和γ)组成的异源三聚复合物。ampk复合物在进化上是保守的,并且也可见于酵母和植物中。哺乳动物ampk由不同同种型的亚基组成:α1、α2、β1、β2、γ1、γ2和γ3(pmid:11746230),从而产生12种可能的异源三聚物组合。α2同种型主要可见于骨骼肌和心肌ampk中;α1和α2同种型均可见于肝ampk中;而例如在脂肪细胞和t细胞中,α1同种型ampk占优势(pmid:16818670,pmid15878856)。
2型糖尿病是一种复杂且异质的障碍。没有普遍适用的单一解决方案来治疗该疾病,因此建议药物和生活方式干预的组合。寻找以限定的作用机制适度活化ampk(尤其是在肌肉和肝脏中)的天然分子可能提供模仿运动的作用并有助于维持/改善代谢健康。
尽管制药工业持续付出了大量努力,但没有可用于治疗代谢障碍的直接ampk活化药物。尚未有任何临床试验注册以测试ampk活化药物的作用。已鉴定/开发了几种合成ampk活化剂。然而,它们要么没有口服利用率/口服利用率差(pmid:16753576、pmid:24900234)要么担心它们的不利影响,因为慢性且强烈的ampk活化可能导致心脏糖原含量增加和肥大(pmid:11827995)。
已知有许多天然化合物/提取物可带来一些代谢健康有益效果,显示这些有益效果最有可能通过抑制线粒体呼吸来间接刺激ampk。然而,这些代谢作用是否由ampk介导在很大程度上难以捉摸,此外,还存在关于副作用/毒性作用(细胞/线粒体中毒)的担忧。
对直接活化ampk的新天然化合物存在明显未满足的需求。
技术实现要素:
本发明提供一种具有通式i的化合物,
其中r1、r2、r3、r4、r5、r6、r7和r8各自独立地为:h;oh;ome;o-糖苷;c-糖苷;酰化的o-糖苷;酰化的c-糖苷;硫酸化的o-糖苷;硫酸化的c-糖苷;卤素;伯醇、仲醇或叔醇;酮;醛;羧酸;酯;伯胺、仲胺或叔胺;伯酰胺或仲酰胺;氰基;硝基;磺酸酯(sulfonate);硫酸酯(sulfate);任选地被取代和/或任选地支化的c1至c20烷基;任选地被取代和/或任选地支化的c2至c20烯基;任选地被取代和/或任选地支化的c4至c20聚烯基;任选地被取代和/或任选地支化的c2至c20炔基,或任选地被取代和/或任选地支化的c4至c20多炔基,或它们的衍生物或类似物,所述化合物用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,r1、r2、r3、r6、r7和r8各自独立地为:h;oh;ome;o-糖苷;c-糖苷;酰化的o-糖苷;酰化的c-糖苷;硫酸化的o-糖苷;硫酸化的c-糖苷;卤素;伯醇、仲醇或叔醇;酮;醛;羧酸;酯;伯胺、仲胺或叔胺;伯酰胺或仲酰胺;氰基;硝基;磺酸酯;硫酸酯;任选地被取代和/或任选地支化的c1至c20烷基;任选地被取代和/或任选地支化的c2至c20烯基;任选地被取代和/或任选地支化的c4至c20聚烯基;任选地被取代和/或任选地支化的c2至c20炔基,或任选地被取代和/或任选地支化的c4至c20多炔基;r4和r5各自独立地为:h;oh;o-糖苷;c-糖苷;酰化的o-糖苷;酰化的c-糖苷;硫酸化的o-糖苷;硫酸化的c-糖苷;卤素;伯醇、仲醇或叔醇;酮;醛;羧酸;酯;伯胺、仲胺或叔胺;伯酰胺或仲酰胺;氰基;硝基;磺酸酯;硫酸酯;任选地被取代和/或任选地支化的c1至c20烷基;任选地被取代和/或任选地支化的c2至c20烯基;任选地被取代和/或任选地支化的c4至c20聚烯基;任选地被取代和/或任选地支化的c2至c20炔基,或任选地被取代和/或任选地支化的c4至c20多炔基,或它们的衍生物或类似物,所述化合物用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,r1、r2、r3、r4、r5、r6、r7和r8各自独立地为:h;oh;ome;o-糖苷;卤素;醛;羧酸;伯胺、仲胺或叔胺;伯酰胺或仲酰胺;氰基;硝基;磺酸酯;硫酸酯;任选地被取代和/或任选地支化的c1至c20烷基;任选地被取代和/或任选地支化的c2至c20烯基;任选地被取代和/或任选地支化的c4至c20聚烯基;任选地被取代和/或任选地支化的c2至c20炔基,或任选地被取代和/或任选地支化的c4至c20多炔基,或它们的衍生物或类似物,所述化合物用于ampk的活化。
在一个实施方案中,r2为:h;oh;ome;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,r4为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,r5为:h;ome;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,r5为:h;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,r6为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,r7为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,r2为:h;oh;ome;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基;r4为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基;并且r7为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,r2为:h;oh;ome;o-糖苷;任选地被取代和/或任选地支化的c1至c5烷基;任选地被取代和/或任选地支化的c2-c5烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c5炔基,或任选地被取代和/或任选地支化的c4至c5多炔基;r4为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c5烷基;任选地被取代和/或任选地支化的c2-c5烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c5炔基,或任选地被取代和/或任选地支化的c4至c5多炔基;并且r7为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c5烷基;任选地被取代和/或任选地支化的c2-c5烯基;任选地被取代和/或任选地支化的c4至c5聚烯基;任选地被取代和/或任选地支化的c2至c5炔基,或任选地被取代和/或任选地支化的c4至c5多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,r2为:h;oh;ome;o-糖苷;c1至c5烷基;c2至c5烯基;c4至c5聚烯基;c2至c5炔基,或c4至c5多炔基;r4为:h;oh;o-糖苷;c1至c5烷基;c2-c5烯基;c4至c5聚烯基;c2至c5炔基,或c4至c5多炔基;并且r7为:h;oh;o-糖苷;c1至c5烷基;c2至c5烯基;c4至c5聚烯基;c2至c5炔基;或c4至c5多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,烷基、烯基和炔基是未支化的。
在一个实施方案中,烷基、烯基和炔基是未取代的。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,r1、r2、r3、r6、r7和r8各自独立地为:h;oh;ome;o-糖苷;卤素;醛;羧酸;伯胺、仲胺或叔胺;伯酰胺或仲酰胺;氰基;硝基;磺酸酯;硫酸酯;任选地被取代和/或任选地支化的c1至c20烷基;任选地被取代和/或任选地支化的c2至c20烯基;任选地被取代和/或任选地支化的c4至c20聚烯基;任选地被取代和/或任选地支化的c2至c20炔基,或任选地被取代和/或任选地支化的c4至c20多炔基;r4和r5各自独立地为:h;oh;o-糖苷;卤素;醛;羧酸;伯胺、仲胺或叔胺;伯酰胺或仲酰胺;氰基;硝基;磺酸酯;硫酸酯;任选地被取代和/或任选地支化的c1至c20烷基;任选地被取代和/或任选地支化的c2至c20烯基;任选地被取代和/或任选地支化的c4至c20聚烯基;任选地被取代和/或任选地支化的c2至c20炔基,或任选地被取代和/或任选地支化的c4至c20多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,r1、r2、r3、r4、r5、r6、r7和r8各自独立地为:h;me;oh;ome;och2ch=ch2;o-糖苷;硫酸酯;卤素;cho;ch2oh;cooh,conh2,coch3;ch=ch2;ch2-ch=c(ch3)2;ch(ch3)2;ch=ch-cho;ch(ch3)-oh;ch(ch3)-ome;ch(ch3)-oc2h5;ch(ch3)-o-ch2-ch=c(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;4-羟基苯甲酰基糖苷,或它们的衍生物或类似物,其用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,r1、r2、r3、r6、r7和r8各自独立地为:h;me;oh;ome;och2ch=ch2;o-糖苷;硫酸酯;卤素;cho;ch2oh;cooh,conh2,coch3;ch=ch2;ch2-ch=c(ch3)2;ch(ch3)2;ch=ch-cho;ch(ch3)-oh;ch(ch3)-ome;ch(ch3)-oc2h5;ch(ch3)-o-ch2-ch=c(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;4-羟基苯甲酰基糖苷,r4和r5各自独立地为:h;me;oh;och2ch=ch2;o-糖苷;硫酸酯;卤素;cho;ch2oh;cooh,conh2,coch3;ch=ch2;ch2-ch=c(ch3)2;ch(ch3)2;ch=ch-cho;ch(ch3)-oh;ch(ch3)-ome;ch(ch3)-oc2h5;ch(ch3)-o-ch2-ch=c(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;4-羟基苯甲酰基糖苷,或它们的衍生物或类似物,其用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,r1、r2、r3、r4、r5、r6、r7和r8各自独立地为:h;me;oh;ome;och2ch=ch2;o-糖苷;硫酸酯;br;cho;ch2oh;cooh,conh2,coch3;ch=ch2;ch2-ch=c(ch3)2;ch(ch3)2;ch=ch-cho;ch(ch3)-oh;ch(ch3)-och3;ch(ch3)-oc2h5;ch(ch3)-o-ch2-ch=c(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;4-羟基苯甲酰基糖苷,或它们的衍生物或类似物,其用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,r1、r2、r3、r6、r7和r8各自独立地为:h;me;oh;ome;och2ch=ch2;o-糖苷;硫酸酯;br;cho;ch2oh;cooh,conh2,coch3;ch=ch2;ch2-ch=c(ch3)2;ch(ch3)2;ch=ch-cho;ch(ch3)-oh;ch(ch3)-och3;ch(ch3)-oc2h5;ch(ch3)-o-ch2-ch=c(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;4-羟基苯甲酰基糖苷,r4和r5各自独立地为:h;me;oh;och2ch=ch2;o-糖苷;硫酸酯;br;cho;ch2oh;cooh,conh2,coch3;ch=ch2;ch2-ch=c(ch3)2;ch(ch3)2;ch=ch-cho;ch(ch3)-oh;ch(ch3)-och3;ch(ch3)-oc2h5;ch(ch3)-o-ch2-ch=c(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;4-羟基苯甲酰基糖苷,或它们的衍生物或类似物,其用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,r1、r2、r3、r4、r5、r6、r7和r8各自独立地为:h;me;oh;ome;o-糖苷;硫酸酯;ch2-ch=c(ch3)2。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,r1、r2、r3、r6、r7和r8各自独立地为:h;me;oh;ome;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;r4和r5各自独立地为:h;me;oh;o-糖苷;硫酸酯;ch2-ch=c(ch3)2。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,r1为:h;ch3;oh;och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;或4-羟基苯甲酰基糖苷;r2和r7各自独立地为:oh;och3;o-ch=ch2;o-糖苷;或硫酸酯;r3为:h;ch3;oh;och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;或4-羟基苄基;r4和r5各自独立地为:oh,och3;o-糖苷;或硫酸酯;r6为ch3;oh;och3;o-糖苷;ch2-ch=c(ch3)2;4-羟基苄基;或ar;r8为:oh;och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;或4-羟基苄基,
在一个实施方案中,r1为:h;ch3;oh;och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;或4-羟基苯甲酰基糖苷;r2和r7各自独立地为:oh;och3;o-ch=ch2;o-糖苷;或硫酸酯;r3为:h;ch3;oh;och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;或4-羟基苄基;r4和r5各自独立地为:oh,o-糖苷;或硫酸酯;r6为ch3;oh;och3;o-糖苷;ch2-ch=c(ch3)2;4-羟基苄基;或ar;r8为:oh;och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;或4-羟基苄基。
在一个实施方案中,r1、r3、r5、r6和r8为h;r2为:oh;ome或o-糖苷;r4为oh或o-糖苷;并且r7为oh或o-糖苷。
在一个实施方案中,r1、r3、r5、r6和r8为h;r2为oh或ome;r4为oh;并且r7为oh。
在一个实施方案中,r1、r3、r5、r6和r8为h;r2为ome;r4为oh;并且r7为oh。
在一个实施方案中,所述化合物为被称为7-甲氧基-9,10-二氢菲-2,5-二醇的lusianthridin,cas号为87530-30-1。
在另一个实施方案中,所述化合物为被称为7-甲氧基-9,10-二氢菲-2,3,5-三醇的化合物2。
在另一个实施方案中,所述化合物为被称为2,5-菲二醇、9,10-二氢、9,10-二氢菲-2,5-二醇的化合物3,cas号为1071055-42-9。
在另一个实施方案中,所述化合物为被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢的化合物4,cas号为70205-52-6。
在另一个实施方案中,所述化合物为被称为cannithrene1、大麻二氢菲(cannabidihydrophenanthrene)、9,10-二氢-7-甲氧基-3,5-菲二醇、3,5-菲二醇、9,10-二氢-7-甲氧基、7-甲氧基-9,10-二氢菲-3,5-二醇的化合物5,cas号为71135-80-3。
在一个实施方案中,ampk的活化治疗或预防受试者的病症、障碍或疾病。
在一个实施方案中,受试者是人类或伴侣动物。
在一个实施方案中,受试者是人。
在一个实施方案中,受试者是中年人。
在一个实施方案中,受试者是老年人。
在一个实施方案中,受试者是伴侣动物。
在一个实施方案中,病症、障碍或疾病涉及心脏代谢健康、肥胖症、2型糖尿病、非酒精性脂肪肝疾病、心血管疾病和/或癌症。
在一个实施方案中,病症、障碍或疾病涉及2型糖尿病和/或非酒精性脂肪肝疾病。
在一个实施方案中,ampk的活化是直接活化机制。
在一个实施方案中,ampk的活化在肌肉和肝脏组织中。
在一个实施方案中,ampk包含α2亚基、β1亚基和γ1亚基。
在一个实施方案中,ampk包含α1亚基、β1亚基和γ1亚基。
在一个实施方案中,所述化合物从植物或植物提取物获得。
在一个实施方案中,所述化合物通过化学合成获得。
本发明还提供一种如本文所述的具有通式i的化合物,其用于制备用于响应于ampk活化的病症、障碍或疾病的药物、治疗或预防响应于ampk活化的病症、障碍或疾病。
在一个实施方案中,具有通式i的化合物用于制备治疗或预防2型糖尿病的药物。
在一个实施方案中,具有通式i的化合物用于制备治疗或预防非酒精性脂肪肝疾病的药物。
本发明还提供一种用于ampk的活化的组合物,该组合物包含如本文所述的具有通式i的化合物或其衍生物或类似物。
在一个实施方案中,该组合物为食物、饮料或饮食补充剂。
在一个实施方案中,该组合物为营养品。
在一个优选的实施方案中,具有通式i的化合物为被称为7-甲氧基-9,10-二氢菲-2,5-二醇的lusianthridin,cas号为87530-30-1。
在一个优选的实施方案中,具有通式i的化合物为被称为7-甲氧基-9,10-二氢菲-2,3,5-三醇的化合物2。
在一个优选的实施方案中,具有通式i的化合物为被称为2,5-菲二醇、9,10-二氢、9,10-二氢菲-2,5-二醇的化合物3,cas号为1071055-42-9。
在一个优选的实施方案中,具有通式i的化合物为被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢的化合物4,cas号为70205-52-6。
在一个优选的实施方案中,具有通式i的化合物为被称为cannithrene1、大麻二氢菲、9,10-二氢-7-甲氧基-3,5-菲二醇、3,5-菲二醇、9,10-二氢-7-甲氧基、7-甲氧基-9,10-二氢菲-3,5-二醇的化合物5,cas号为71135-80-3。
在一个实施方案中,该组合物还包含药学上可接受的载体。
本发明还提供一种用于ampk的活化的药物组合物,该药物组合物包含治疗有效量的如本文所述的具有通式i的化合物或其药学上可接受的盐或溶剂化物作为活性成分,以及药学上可接受的载体。
在一个优选的实施方案中,包含具有通式i的化合物的药物组合物为被称为7-甲氧基-9,10-二氢菲-2,5-二醇的lusianthridin,cas号为87530-30-1)。
在一个优选的实施方案中,包含具有通式i的化合物的药物组合物为被称为7-甲氧基-9,10-二氢菲-2,3,5-三醇的化合物2。
在一个优选的实施方案中,包含具有通式i的化合物的药物组合物为被称为2,5-菲二醇、9,10-二氢-、9,10-二氢菲-2,5-二醇的化合物3,cas号为1071055-42-9。
在一个优选的实施方案中,包含具有通式i的化合物的药物组合物为被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢的化合物4,cas号为70205-52-6)。
在一个优选的实施方案中,包含具有通式i的化合物的药物组合物为被称为cannithrene1、大麻二氢菲、9,10-二氢-7-甲氧基-3,5-菲二醇、3,5-菲二醇、9,10-二氢-7-甲氧基、7-甲氧基-9,10-二氢菲-3,5-二醇的化合物5,cas号为71135-80-3。
在一个实施方案中,该药物组合物为口服剂型。
本发明还提供一种施用治疗有效量的如本文所述的具有通式i的化合物用于治疗或预防响应于ampk活化的病症、障碍或疾病的方法。
在一个优选的实施方案中,具有通式i的化合物为被称为7-甲氧基-9,10-二氢菲-2,5-二醇的lusianthridin,cas号为87530-30-1)。
在一个优选的实施方案中,具有通式i的化合物为被称为7-甲氧基-9,10-二氢菲-2,3,5-三醇的化合物2。
在一个优选的实施方案中,具有通式i的化合物为被称为2,5-菲二醇、9,10-二氢、9,10-二氢菲-2,5-二醇的化合物3,cas号为1071055-42-9。
在一个优选的实施方案中,具有通式i的化合物为被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢的化合物4,cas号为70205-52-6)。
在一个优选的实施方案中,具有通式i的化合物为被称为cannithrene1、大麻二氢菲、9,10-二氢-7-甲氧基-3,5-菲二醇、3,5-菲二醇、9,10-二氢-7-甲氧基、7-甲氧基-9,10-二氢菲-3,5-二醇的化合物5,cas号为71135-80-3。
在一个实施方案中,响应于ampk活化的障碍为代谢障碍。
在一个实施方案中,代谢障碍为前驱糖尿病或糖尿病。
在一个实施方案中,糖尿病的代谢障碍伴随有可响应ampk活化的病症,例如糖尿病性肾病或糖尿病性神经病变。
在一个实施方案中,代谢障碍为血脂异常。
本发明还提供一种在对其有需要的受试者中活化ampk的方法,所述方法包括向对其有需要的受试者施用包含有效量的如本文所述的具有通式i的化合物的组合物。
在一个优选的实施方案中,具有通式i的化合物为被称为7-甲氧基-9,10-二氢菲-2,5-二醇的lusianthridin,cas号为87530-30-1。
在一个优选的实施方案中,具有通式i的化合物为被称为7-甲氧基-9,10-二氢菲-2,3,5-三醇的化合物2。
在一个优选的实施方案中,具有通式i的化合物为被称为2,5-菲二醇、9,10-二氢、9,10-二氢菲-2,5-二醇的化合物3,cas号为1071055-42-9。
在一个优选的实施方案中,具有通式i的化合物为被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢的化合物4,cas号为70205-52-6。
在一个优选的实施方案中,具有通式i的化合物为被称为cannithrene1、大麻二氢菲、9,10-二氢-7-甲氧基-3,5-菲二醇、3,5-菲二醇、9,10-二氢-7-甲氧基、7-甲氧基-9,10-二氢菲-3,5-二醇的化合物5,cas号为71135-80-3。
本发明还提供了一种活化ampk的体外方法,该方法包括使如本文所述的具有通式i的化合物或其衍生物或类似物与ampk接触。
在一个实施方案中,体外方法为无细胞的。
在一个实施方案中,体外方法为基于细胞的。
在一个优选的实施方案中,具有通式i的化合物为被称为7-甲氧基-9,10-二氢菲-2,5-二醇的lusianthridin,cas号为87530-30-1。
在一个优选的实施方案中,具有通式i的化合物为被称为7-甲氧基-9,10-二氢菲-2,3,5-三醇的化合物2。
在一个优选的实施方案中,具有通式i的化合物为被称为2,5-菲二醇、9,10-二氢、9,10-二氢菲-2,5-二醇的化合物3,cas号为1071055-42-9。
在一个优选的实施方案中,具有通式i的化合物为被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢的化合物4,cas号为70205-52-6。
在一个优选的实施方案中,具有通式i的化合物为被称为cannithrene1、大麻二氢菲、9,10-二氢-7-甲氧基-3,5-菲二醇、3,5-菲二醇、9,10-二氢-7-甲氧基、7-甲氧基-9,10-二氢菲-3,5-二醇的化合物5,cas号为71135-80-3。
具体实施方式
具有通式i的化合物
本发明涉及一种如本文所述的具有通式i的化合物,其具有如下所示的结构:
其中r1、r2、r3、r4、r5、r6、r7和r8各自独立地为:h;oh;ome;o-糖苷;c-糖苷;酰化的o-糖苷;酰化的c-糖苷;硫酸化的o-糖苷;硫酸化的c-糖苷;卤素;伯醇、仲醇或叔醇;酮;醛;羧酸;酯;伯胺、仲胺或叔胺;伯酰胺或仲酰胺;氰基;硝基;磺酸酯;硫酸酯;任选地被取代和/或任选地支化的c1至c20烷基;任选地被取代和/或任选地支化的c2至c20烯基;任选地被取代和/或任选地支化的c4至c20聚烯基;任选地被取代和/或任选地支化的c2至c20炔基,或任选地被取代和/或任选地支化的c4至c20多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r1、r2、r3、r6、r7和r8各自独立地为:h;oh;ome;o-糖苷;c-糖苷;酰化的o-糖苷;酰化的c-糖苷;硫酸化的o-糖苷;硫酸化的c-糖苷;卤素;伯醇、仲醇或叔醇;酮;醛;羧酸;酯;伯胺、仲胺或叔胺;伯酰胺或仲酰胺;氰基;硝基;磺酸酯;硫酸酯;任选地被取代和/或任选地支化的c1至c20烷基;任选地被取代和/或任选地支化的c2至c20烯基;任选地被取代和/或任选地支化的c4至c20聚烯基;任选地被取代和/或任选地支化的c2至c20炔基,或任选地被取代和/或任选地支化的c4至c20多炔基;r4和r5各自独立地为:h;oh;o-糖苷;c-糖苷;酰化的o-糖苷;酰化的c-糖苷;硫酸化的o-糖苷;硫酸化的c-糖苷;卤素;伯醇、仲醇或叔醇;酮;醛;羧酸;酯;伯胺、仲胺或叔胺;伯酰胺或仲酰胺;氰基;硝基;磺酸酯;硫酸酯;任选地被取代和/或任选地支化的c1至c20烷基;任选地被取代和/或任选地支化的c2至c20烯基;任选地被取代和/或任选地支化的c4至c20聚烯基;任选地被取代和/或任选地支化的c2至c20炔基,或任选地被取代和/或任选地支化的c4至c20多炔基,或它们的衍生物或类似物,所述化合物用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r1、r2、r3、r4、r5、r6、r7和r8各自独立地为:h;oh;ome;o-糖苷;卤素;醛;羧酸;伯胺、仲胺或叔胺;伯酰胺或仲酰胺;氰基;硝基;磺酸酯;硫酸酯;任选地被取代和/或任选地支化的c1至c20烷基;任选地被取代和/或任选地支化的c2至c20烯基;任选地被取代和/或任选地支化的c4至c20聚烯基;任选地被取代和/或任选地支化的c2至c20炔基,或任选地被取代和/或任选地支化的c4至c20多炔基,或它们的衍生物或类似物,所述化合物用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r2为:h;oh;ome;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r4为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r5为:h;ome;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r5为:h;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r6为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r7为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r2为:h;oh;ome;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基;r4为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基;并且r7为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c10烷基;任选地被取代和/或任选地支化的c2至c10烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c10炔基,或任选地被取代和/或任选地支化的c4至c10多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r2为:h;oh;ome;o-糖苷;任选地被取代和/或任选地支化的c1至c5烷基;任选地被取代和/或任选地支化的c2-c5烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c5炔基,或任选地被取代和/或任选地支化的c4至c5多炔基;r4为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c5烷基;任选地被取代和/或任选地支化的c2-c5烯基;任选地被取代和/或任选地支化的c4至c10聚烯基;任选地被取代和/或任选地支化的c2至c5炔基,或任选地被取代和/或任选地支化的c4至c5多炔基;并且r7为:h;oh;o-糖苷;任选地被取代和/或任选地支化的c1至c5烷基;任选地被取代和/或任选地支化的c2-c5烯基;任选地被取代和/或任选地支化的c4至c5聚烯基;任选地被取代和/或任选地支化的c2至c5炔基,或任选地被取代和/或任选地支化的c4至c5多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r2为:h;oh;ome;o-糖苷;c1至c5烷基;c2至c5烯基;c4至c5聚烯基;c2至c5炔基,或c4至c5多炔基;r4为:h;oh;o-糖苷;c1至c5烷基;c2-c5烯基;c4至c5聚烯基;c2至c5炔基,或c4至c5多炔基;并且r7为:h;oh;o-糖苷;c1至c5烷基;c2至c5烯基;c4至c5聚烯基;c2至c5炔基;或c4至c5多炔基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中烷基、烯基和炔基为未支化的。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中烷基、烯基和炔基为未被取代的。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r1、r2、r3、r4、r5、r6、r7和r8各自独立地为:h;me;oh;ome;och2ch=ch2;o-糖苷;硫酸酯;卤素;cho;ch2oh;cooh,conh2,coch3;ch=ch2;ch2-ch=c(ch3)2;ch(ch3)2;ch=ch-cho;ch(ch3)-oh;ch(ch3)-ome;ch(ch3)-oc2h5;ch(ch3)-o-ch2-ch=c(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;4-羟基苯甲酰基糖苷,或它们的衍生物或类似物,其用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r1、r2、r3、r4、r5、r6、r7和r8各自独立地为:h;me;oh;ome;och2ch=ch2;o-糖苷;硫酸酯;br;cho;ch2oh;cooh,conh2,coch3;ch=ch2;ch2-ch=c(ch3)2;ch(ch3)2;ch=ch-cho;ch(ch3)-oh;ch(ch3)-och3;ch(ch3)-oc2h5;ch(ch3)-o-ch2-ch=c(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)-(ch2)3-ch(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;4-羟基苯甲酰基糖苷,或它们的衍生物或类似物,其用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r1、r2、r3、r4、r5、r6、r7和r8各自独立地为:h;me;oh;ome;o-糖苷;硫酸酯;ch2-ch=c(ch3)2,或它们的衍生物或类似物,其用于ampk的活化。
在一些实施方案中,och3基团可与相邻的oh基团环化以形成亚甲基二氧基桥。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r1为:h;ch3;oh;och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;或4-羟基苯甲酰基糖苷;r2和r7各自独立地为:oh;och3;o-ch=ch2;o-糖苷;或硫酸酯;r3为:h;ch3;oh;och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;或4-羟基苄基;r4和r5各自独立地为:oh,och3;o-糖苷;或硫酸酯;r6为ch3;oh;och3;o-糖苷;ch2-ch=c(ch3)2;4-羟基苄基;或ar;r8为:oh:och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;或4-羟基苄基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r1为:h;ch3;oh;och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;4-羟基苄基;4-羟基-3-甲氧基苄基;4-羟基苯甲酰基;或4-羟基苯甲酰基糖苷;r2和r7各自独立地为:oh;och3;o-ch=ch2;o-糖苷;或硫酸酯;r3为:h;ch3;oh;och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;或4-羟基苄基;r4和r5各自独立地为:oh,och3;o-糖苷;或硫酸酯;r6为ch3;oh;och3;o-糖苷;ch2-ch=c(ch3)2;4-羟基苄基;或ar;r8为:oh:och3;o-糖苷;硫酸酯;ch2-ch=c(ch3)2;或4-羟基苄基,或它们的衍生物或类似物,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r1、r3、r5、r6和r8为h;r2为:oh;ome或o-糖苷;r4为oh或o-糖苷;并且r7为oh或o-糖苷,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r1、r3、r5、r6和r8为h;r2为oh或ome;r4为oh;并且r7为oh,其用于ampk的活化。
在一个实施方案中,本发明提供了一种具有通式i的化合物,其中r1、r3、r5、r6和r8为h;r2为ome;r4为oh;并且r7为oh,其用于ampk的活化。
在一个实施方案中,所述化合物为被称为7-甲氧基-9,10-二氢菲-2,5-二醇的lusianthridin,cas号为87530-30-1:
在另一个实施方案中,所述化合物为被称为7-甲氧基-9,10-二氢菲-2,3,5-三醇的化合物2:
在另一个实施方案中,所述化合物为被称为2,5-菲二醇、9,10-二氢、9,10-二氢菲-2,5-二醇的化合物3,cas号为1071055-42-9:
在另一个实施方案中,所述化合物为被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢的化合物4,cas号为70205-52-6:
在另一个实施方案中,所述化合物为被称为cannithrene1、大麻二氢菲、9,10-二氢-7-甲氧基-3,5-菲二醇、3,5-菲二醇、9,10-二氢-7-甲氧基、7-甲氧基-9,10-二氢菲-3,5-二醇的化合物5,cas号为71135-80-3:
定义
通用化学术语
术语“烷基”是指具有1至20个碳原子、或1至15个碳原子、或1至10个碳原子、或1至8个碳原子、或1至6个碳原子、或1至4个碳原子的支链或直链的饱和烃链。该术语通过诸如甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、正己基、正癸基、十四烷基的基团来举例说明。
术语“取代的烷基”是指:
1)如上定义的具有1、2、3、4或5个取代基(在一些实施方案中,1、2或3个取代基)的烷基链,这些取代基选自烯基、炔基、烷氧基、环烷基、环烯基、环烷氧基、环烯氧基、酰基、酰氨基、酰氧基、氨基、取代的氨基、氨基羰基、烷氧基羰基氨基、叠氮基、氰基、卤素、羟基、酮基、硫代羰基、羧基、羧烷基、芳硫基、杂芳硫基、杂环基硫基、硫醇、烷硫基、芳基、芳氧基、杂芳基、氨基磺酰基、氨基羰基氨基、杂芳氧基、杂环基、杂环氧基、羟氨基、烷氧基氨基、硝基、-s(o)-烷基、-s(o)-环烷基、-s(o)-杂环基、-s(o)-芳基、-s(o)-杂芳基、-s(o)2-烷基、-s(o)2-环烷基、-s(o)2-杂环基、-s(o)2-芳基和-s(o)2-杂芳基。除非定义另有限定,否则所有取代基可任选地进一步被1、2或3个取代基取代,这些取代基选自烷基、烯基、炔基、羧基、羧烷基、氨基羰基、羟基、烷氧基、卤素、cf3、氨基、取代的氨基、氰基、环烷基、杂环基、芳基、杂芳基和-s(o)nr<a>,其中r<a>为烷基、芳基或杂芳基,并且n为0、1或2;或
2)如上定义的间杂有1至10个原子(例如1、2、3、4或5个原子)的烷基链,这些原子独立地选自氧、硫和nr<a>,其中r<a>选自氢、烷基、环烷基、烯基、环烯基、炔基、芳基、杂芳基和杂环基。所有取代基可任选地被烷基、烯基、炔基、羧基、羧烷基、氨基羰基、羟基、烷氧基、卤素、cf3、氨基、取代的氨基、氰基、环烷基、杂环基、芳基、杂芳基和-s(o)nr<a>进一步取代,其中r<a>为烷基、芳基或杂芳基,并且n为0、1或2;或
3)如上定义的烷基链,其具有如上定义的1、2、3、4或5个取代基,并且还间杂有如上定义的1-10个原子(例如1、2、3、4或5个原子)。
术语“烯基”是指其中烷基基团的两个原子形成不是芳族基团的一部分的双键的一类烷基链。即,烯基链包含图案r-c(r)=c(r)-r,其中r是指烯基基团的其余部分,其可相同或不同。烯基链的非限制性示例包括-ch=ch2、-c(ch3)=ch2、-ch=chch3、-c(ch3)=chch3、-ch2-ch=c(ch3)2和–c(ch3)2-ch=ch2。烯基部分可为支链、直链或环状的(在这种情况下,其也将被称为“环烯基”基团)。烯基基团可任选地被取代。
术语“炔基”是指其中烷基基团的两个原子形成三键的一类烷基链。即,炔基基团包含图案r-c≡c-r,其中r是指炔基基团的其余部分,其可相同或不同。炔基基团的非限制性示例包括-c≡ch、-c≡cch3和-c≡cch2ch3。炔基部分的“r”部分可为支链、直链或环状的。炔基基团可任选地被取代。
术语“多不饱和的”是指
1)其中烷基基团的多于一对的原子形成不是芳族基团的一部分的双键的被称为聚烯基的链。即,聚烯基链包含若干r-c(r)=c(r)-r图案,其中r是指烯基基团的其余部分,其可相同或不同。聚烯基链的非限制性示例包括–ch=ch-ch=ch-、-ch2-ch=cch3-ch2-ch2-ch=c(ch3)2和-ch2-ch=cch3-ch2-ch2-ch=cch3--ch2-ch2-ch=c(ch3)2。聚烯基部分可以是支链或直链的。包含两个双键的聚烯基部分可为环状的(在这种情况下,其也将被称为“环二烯基”基团)。环二烯基基团的非限制性示例包括环戊二烯和环己二烯基团。聚烯基基团可任选地被取代。
2)其中烷基基团的多于一对的原子形成三键的被称为多炔基的链。即,多炔基基团包含若干图案r-c≡c-r,其中r是指炔基基团的其余部分,其可相同或不同。多炔基基团的非限制性示例包括-ch2-ch2-c≡c-c≡ch。多炔基部分的“r”部分可为支链、直链或环状的。炔基基团可任选地被取代。
3)其中烷基基团的至少一对原子形成双键并且烷基基团的一对原子形成三键的一种类型的烷基链。即,多不饱和链包含r-c(r)=c(r)-r和r-c≡c-r图案,其中r是指多不饱和链的其余部分,其可相同或不同。这种类型的多不饱和链的非限制性示例包括-ch2-ch=ch-c≡ch。多不饱和部分的“r”部分可为支链、直链或环状的。多不饱和的链可任选地被取代。
4)如上第1-3段中定义的间杂有1至10个原子(例如1、2、3、4或5个原子)的多不饱和链,这些原子独立地选自氧、硫和nr<a>,其中r<a>选自氢、烷基、环烷基、烯基、环烯基、炔基、芳基、杂芳基和杂环基。
如本文所用,术语“环”是指任何共价闭合的结构。环包括例如碳环(例如芳基和环烷基)、杂环(例如杂芳基和非芳族杂环)、芳族(例如芳基和杂芳基)、和非芳族(例如环烷基和非芳族杂环)。环可任选地被取代。环可形成环系的一部分。如本文所用,术语“环系”是指两个或更多个环,其中两个或更多个环是稠合的。术语“稠合的”是指其中两个或更多个环共享一个或多个键的结构。
术语“卤素原子”可指氟原子、氯原子、溴原子或碘原子。
术语“糖苷”是指其中至少一个糖经由糖苷键与另一个官能团结合的化合物。通常,糖苷链可包含1至4个糖单元。
术语“糖苷键”是指在糖的半缩醛或半缩酮基团与化合物的化学基团之间形成的键。化学基团可为-oh(o-糖苷)或-cr1r2r3(c-糖苷)。
术语“酰化的o-糖苷”和“酰化的c-糖苷”是指其中糖苷链的至少一个羟基被有机酸酯化的化合物。有机酸的典型示例可包括乙酸、取代的苯甲酸、肉桂酸(咖啡酸、阿魏酸、对香豆酸)和/或苯基丙酸(二氢咖啡酸)。
术语“硫酸化的o-糖苷”和“硫酸化的c-糖苷”是指其中糖苷链的至少一个羟基被硫酸酯化的化合物。
术语“亚甲基二氧基”可指具有结构式r-o-ch2-o-r'的官能团,其通过两个化学键连接至分子的其余部分。
如本文所用,术语“类似物”应理解为是指具有类似于另一种结构的结构,但在某些组分方面与之不同的化合物。“衍生物”是通过用另一个原子或原子基团取代一个或多个原子而产生或实际上由母体化合物合成的化合物。
本文所述的化学结构的组分可进一步定义如下:术语“不饱和的”是指其在碳原子之间包含至少一个、最多八个双键。“脱水”是指两个相邻碳之间的水损失,一个碳带有羟基,而另一个碳带有至少一个氢,从而导致双键的形成。“还原”是指将氢加成至双键,从而导致形成单键,通常将羰基还原为醇,或将不饱和链还原为饱和链。碳氧化可例如逐步从甲基氧化成醇,成醛,并且最终成羧酸。
如本文所用,术语“醛”表示具有通式结构-c-[c(=o)]n-h或h-[c(=o)]n-h的有机化合物(n为1或更大,并且其中与-[c(=o)]-n基团键合的碳原子不与氧、硫、硒或碲双键合,或与氮三键合。
如本文所用,术语“胺”表示具有与碳原子单键合或双键合的氮原子并且其中与氮原子键合的碳原子缺乏与氧、硫、硒或碲的双键合或与氮三键合的有机化合物。此外,其中相同氮原子键合至-c(=x)-基团(x为o、s、se或te)并且键合至未与氧、硫、硒或碲双键合的碳原子的那些化合物不被认为是胺,例如-c-nh-c(x=)-
如本文所用,术语“氰基”表示相邻碳原子和氮原子之间的三键。
如本文所用,术语“羧酸”表示-c(=o)oh基团的存在。
化合物或其组合物
应当理解,根据某些实施方案,本发明的化合物或其组合物可为营养品组合物、药物组合物、功能性食品、功能性营养产品、医疗食品、医疗营养产品或饮食补充剂。
术语“营养品”将词语“营养”和“药物”结合在一起。它是一种提供健康和医疗益处,包括预防和治疗病症、障碍或疾病的食物或食物产品。营养品是从一般以通常不与食物相关联的药物形式销售的食物中分离或纯化的产品。证实营养品具有生理有益效果或提供对慢性病症、障碍或疾病的预防。此类产品可在从分离的营养物质、饮食补充剂和特定饮食到经基因工程化的食物、草药产品和加工食品诸如谷物、汤和饮料的范围内。
如本文所用,术语“营养品”表示在营养和药物应用领域中的有用性。因此,新型营养组合物可用作食品和饮料的补充剂,并且可用作肠道或肠胃外施用的药物制剂,其可为固体制剂诸如胶囊或片剂,或液体制剂诸如溶液或悬浮液。
根据本发明的营养品组合物还可包含保护性亲水胶体(诸如胶类、蛋白质类、改性淀粉类)、粘合剂、成膜剂、包囊剂/材料、壁/壳材料、基质化合物、包衣、乳化剂、表面活性剂、增溶剂(油类、脂肪类、蜡类、卵磷脂类等)、吸附剂、载体、填充剂、共化合物、分散剂、润湿剂、加工助剂(溶剂)、流动剂、掩味剂、增重剂、胶凝剂、凝胶形成剂、抗氧化剂和抗微生物剂。
此外,可将复合维生素和矿物质补充剂添加到本发明的营养品组合物中,以获得足够量的在一些饮食中是缺失的必需营养物质。复合维生素和矿物质补充剂还可用于预防疾病以及防止由于生活方式模式导致的营养损失和缺乏。
本发明的营养品组合物可为适于施用于身体的任何盖仑剂型,尤其是常规用于口服施用的任何形式,例如为固体形式,诸如食品或饲料、食品或饲料预混物、强化食品或饲料、片剂、丸剂、颗粒剂、糖衣丸、胶囊剂和泡腾剂制剂诸如粉末和片剂;或者为液体形式,诸如溶液、乳液或悬浮液,如例如饮料、糊剂和油性悬浮液。可将糊剂掺入硬壳或软壳胶囊中,由此胶囊的特征在于例如(鱼、猪、家禽、牛)明胶、植物蛋白或木质素磺酸酯的基质。其它应用形式的示例是用于透皮、肠胃外或注射施用的那些。膳食和药物组合物可为受控(缓释)制剂的形式。
饮料涵盖非酒精饮料和酒精饮料以及待添加到饮用水和液体食品中的液体制剂。非酒精饮料为例如软饮料、运动饮料、果汁、茶和基于乳质的饮料。液体食品为例如汤和乳制品。可将包含本发明化合物的营养品组合物添加到软饮料、能量棒或糖果中。
如果营养品组合物是药物制剂,并且组合物还包含药学上可接受的赋形剂、稀释剂或佐剂,然后可对其制剂使用标准技术,如例如《雷明顿药物科学》,第20版,威廉斯·威尔金斯出版公司,美国宾夕法尼亚州(remington'spharmaceuticalsciences,20theditionwilliams&wilkins,pa,usa)中所公开的。对于口服施用,优选地使用包含合适粘合剂(例如明胶或聚乙烯吡咯烷酮)、合适填料(例如乳糖或淀粉)、合适润滑剂(例如硬脂酸镁)和任选的其它添加剂的片剂和胶囊剂。
“功能性食品”、“功能性营养产品”、“医疗食品”和“医疗营养产品”涉及声称具有除供给营养物质基本功能之外的健康状况提升或疾病预防特性的任何健康食品。功能性食品的一般类别包括加工食品或用提升健康状况的添加剂强化的食品,如“富含维生素”的产品。
术语“食物”、“食物产品”和“食物组合物”或“饮食产品”意指旨在供个体(诸如,人)摄入并且向个体提供至少一种营养物质的产品或组合物。本公开(包括本文所述的多个实施方案)的组合物可包含、由或基本上由以下要素组成:本文所公开的要素,以及本文所述的或者说可用于饮食中的任何另外的或任选的成分、组分或要素。
饮食补充剂也称为食品补充剂或营养补充剂,是旨在补充饮食并提供在人饮食中可能缺失或可能摄入量不足的营养物质(诸如维生素、矿物质、纤维、脂肪酸或氨基酸)的制剂。一些国家/地区将膳食补充剂定义为食品,而在其它国家/地区将膳食补充剂定义为药物或天然健康产品。包含维生素或膳食矿物质的补充剂作为一类食品包括在《国际食品法典》中,《国际食品法典》是国际公认的标准、实践规范、指南以及与食品、食品生产和食品安全相关的其它建议的集合。这些文本由国际食品法典委员会制定,国际食品法典委员会是受联合国粮食及农业组织(fao)和世界卫生组织(who)资助的组织。
旨在用于动物的组合物包括为动物、动物犒赏物(例如饼干)和/或饮食补充剂提供必要的饮食需求的食物组合物。组合物可以是干组合物(例如粗磨食物)、半湿组合物、湿组合物或它们的任何混合物。在一个实施方案中,组合物为饮食补充剂,诸如肉汁、饮用水、饮料、酸奶、粉末、颗粒、糊剂、悬浮液、咀嚼物、小块、犒赏物、小吃、食丸、丸剂、胶囊、片剂或任何其他合适的递送形式。饮食补充剂可包含高浓度的ufa和norc,以及b族维生素和抗氧化剂。这允许将补充剂以少量施用给动物,或者在另选方案中可以在施用给动物之前稀释。膳食补充剂可能需要混合,或者可在施用于动物之前与水或其他稀释剂混合。
“宠物食品”或“宠物犒赏物组合物”包含约15%至约50%的粗蛋白。粗蛋白材料可包含植物蛋白,诸如大豆粉、大豆浓缩蛋白、玉米蛋白粉、小麦谷蛋白、棉籽和花生粕,或者动物蛋白,诸如酪蛋白、白蛋白和肉蛋白。可用于本发明的肉蛋白质的示例包括猪肉、羊羔肉、马肉、禽肉、鱼肉以及它们的混合物。组合物还可包含约5%至约40%的脂肪。组合物还可包含碳水化合物源。组合物可包含约15%至约60%的碳水化合物。此类碳水化合物的示例包括谷粒或谷物,诸如水稻、玉米、芦粟、高粱、苜蓿、大麦、大豆、芥花、燕麦、小麦以及它们的混合物。组合物还可任选地包含其他材料,诸如干乳清和其他乳制品副产物。在一些实施方案中,组合物的灰分含量在小于1%至约15%的范围内,并且在一个方面,在约5%至约10%的范围内。
水分含量可根据组合物的性质而变化。在一个实施方案中,组合物可以是完全且营养平衡的宠物食品。在该实施方案中,宠物食品可以是“湿食品”、“干燥食品”或中等水分含量的食物。“湿食品”描述的是通常以罐或箔袋形式销售的宠物食品,并且其水分含量通常在约70%至约90%的范围内。“干燥食品”描述了与湿食品组成相似的宠物食品,但其含有的水分含量有限,通常在约5%至约15%或20%的范围内,因此呈现为例如小饼干类粗磨食品。在一个实施方案中,组合物具有约5%至约20%的水分含量。干燥食品包括各种含水量的各种食品,使得它们相对耐贮存并且抗微生物或真菌导致的变质或污染。还包括在内的是作为挤出食物产品的干燥食品组合物,诸如宠物食品,或用于伴侣动物的零食。
化合物或其组合物的施用的方法
本发明的化合物或其组合物优选地通过口服施用。在一些实施方案中,本发明的化合物或其组合物可通过以下方式施用:静脉注射施用、局部施用、肠胃外施用、腹膜内施用、肌内注射施用、鞘内注射施用、病灶内施用、颅内施用、鼻内施用、眼内施用、心脏内施用、玻璃体内施用、骨内施用、脑内施用、动脉内施用、关节内施用、真皮内施用、透皮施用、经粘膜施用、舌下施用、肠内施用、唇下施用、吹入施用、栓剂施用、吸入施用或皮下施用。
本发明的组合物可具有可在小于一个月内观察到的急性效应。附加地或另选地,组合物可具有长期效应,并且因此各种实施方案包括将组合物施用给个体(例如口服)持续至少一个月的时间段;优选至少两个月,更优选至少三个月、四个月、五个月或六个月;最优选至少一年。在该时间段期间,可将组合物施用给个体每周至少一天;优选每周至少两天,更优选每周至少三天、四天、五天或六天;最优选每周七天。组合物可每天以单次剂量或每天以多种单独剂量施用。在一个实施方案中,单剂量为不小于约100mg。在一个实施方案中,单剂量为不超过约1000mg。在一个实施方案中,单剂量为介于约100mg和约1000mg之间。
ampk活化术语
如本文所用,“ampk活化剂”是指增加(磷酸化的或非磷酸化的)ampk的下游底物的磷酸化的化合物和/或增加ampk的磷酸化的化合物。
如本文所用,“直接ampk活化剂”是指通过与其亚基中的至少一个直接相互作用来活化ampk的化合物。
如本文所用,“响应于ampk活化”的病症、障碍或疾病是指其中症状将通过ampk的活化而减轻或其过程将被有利地改变的病症、障碍或疾病,包括但不限于代谢障碍、糖尿病、血脂异常、高血压、超重和肥胖症。例如,糖尿病的代谢障碍伴随有可响应于ampk活化的病症,诸如糖尿病性肾病或糖尿病性神经病变。
医学术语
如本文所用,术语“糖尿病”包括胰岛素依赖性糖尿病(即,iddm,也称为1型糖尿病)、非胰岛素依赖性糖尿病(即,niddm,也称为2型糖尿病)和前驱糖尿病。1型糖尿病是胰岛素绝对缺乏的结果,胰岛素是调节葡萄糖利用率的激素。2型糖尿病通常在面临胰岛素水平正常或甚至升高的情况下发生,并且似乎是组织不能适当响应胰岛素的结果。这被称为“胰岛素抗性”。大多数2型糖尿病患者也超重或肥胖。诊断糖尿病的标准之一是空腹血浆葡萄糖水平。糖尿病受试者具有大于或等于126mg/dl的空腹血浆葡萄糖水平。前驱糖尿病受试者是患有前驱糖尿病的人。前驱糖尿病受试者是空腹血糖耐受性异常(空腹血浆葡萄糖水平大于或等于100mg/dl且小于126mg/dl);或葡萄糖耐受性异常(≥140mg/dl且<200mg/dl的2小时血浆葡萄糖水平);或胰岛素抗性的受试者,从而导致糖尿病发展的风险增加。预防2型糖尿病包括治疗前驱糖尿病。
如本文所用,术语“血脂异常”涵盖任何脂质级分的异常水平以及特异性脂蛋白异常。例如,它是指血浆胆固醇的升高和/或甘油三酯的升高和/或游离脂肪酸的升高和/或低高密度脂蛋白(hdl)水平和/或高低密度脂蛋白(ldl)水平和/或高极低密度脂蛋白(vldl)水平。血脂异常可例如导致动脉粥样硬化和最终症状性血管疾病(包括冠心病)的发展。血脂异常可与糖尿病相关或可不与糖尿病相关。
如本文所用,术语“代谢障碍”涵盖由于环境因素和遗传因素而破坏正常代谢的任何异常化学和酶反应(环境因素包括身体活动、营养),从而导致某些物质的过度水平或缺乏以及能量稳态的功能障碍。代谢障碍的非限制性示例包括糖尿病、血脂异常、高血压、超重、肥胖症、以及它们的任何组合。
如本文所用,“ampk相关疾病”包括其中ampk的活化提供有益作用的病理或病原学病症。此类疾病或病症的示例包括肥胖症、糖尿病、代谢综合征、急性炎性肺损伤、心脏病、再灌注局部缺血、癌症、衰老、视网膜变性、心脏肥大、非酒精性脂肪肝疾病、高血压、白蛋白尿、零星阿尔茨海默病、肌营养不良和骨关节炎。此外,“ampk相关病症”包括其中ampk的活化改善与原发性“ampk相关疾病”相关联的病症的病症。例如,糖尿病性肾病(salotto等人,(2017)j.pharma和exptthera361:303-311)或糖尿病性神经病变是可与糖尿病的“ampk相关疾病”相关联的“ampk相关病症”。
“预防”或“防止”包括降低病症、障碍或疾病的风险和/或严重程度。
术语“治疗”、“处理”、“减轻”和“缓解”既包括防止性或预防性治疗(预防和/或减缓目标病理学病症或障碍的发展)也包括治愈性、治疗性或疾病修饰治疗,包括治愈、减慢、减轻诊断的确诊的病理学病症或障碍的症状和/或中断其进展的治疗性措施;并且包括治疗存在染病风险或怀疑已染病的患者,以及治疗生病或已经诊断为患有疾病或医学病症的患者。该术语不一定表示受试者被治疗直至完全恢复。这些术语也指在未患有疾病但可能易于发展不健康状况的受试者中进行的健康维持和/或促进。这些术语还旨在包括强化或以其他方式增强一种或多种主要的防止性或治疗性措施。术语“治疗”、“减轻”和“缓解”还旨在包括疾病或病症的膳食管理或者防止或预防疾病或病症的膳食管理。治疗可为患者相关的或医生相关的。
肥胖症是相对于瘦体重而言体脂过量,是一种在现代社会中高度普遍的慢性疾病。它不仅与社交成见(socialstigma)相关联,而且还与寿命缩短和许多医学问题相关联,包括不利的心理发育、冠状动脉疾病、高血压、中风、糖尿病、高脂血症和一些癌症(参见例如nishina,etal.,metab.43:554-558,1994;grundyandbarnett,dis.mon.36:641-731,1990;rissanen,etal.,britishmedicaljournal,301:835-837,1990)。
“肥胖相关障碍”是指那些与疾病或病症的进展或抑制有关的体重过多或“体重指数(bmi)”过高的疾病或病症。肥胖症相关障碍的代表性示例包括但不限于糖尿病、糖尿病并发症、胰岛素敏感性、多囊卵巢疾病、高血糖症、血脂异常、胰岛素抗性、代谢综合征、肥胖症、体重增加、炎症性疾病、消化器官疾病、心绞痛、心肌梗塞、心绞痛或心肌梗塞的后遗症、老年性痴呆和脑血管痴呆。参见,harrison'sprinciplesofinternalmedicine,13thed.,mcgrawhillcompaniesinc.,newyork(1994)。炎性病症的示例包括但不限于消化器官的疾病(诸如溃疡性结肠炎、克隆氏病、胰腺炎、胃炎、消化器官的良性肿瘤、消化息肉、遗传性息肉综合征、结肠癌、直肠癌、胃癌和消化器官的溃疡性疾病)、心绞痛、心肌梗塞、心绞痛或心肌梗塞的后遗症、老年性痴呆、脑血管痴呆、免疫疾病和一般癌症。
术语“受试者”或“个体”意指可受益于本文所公开的化合物、组合物或方法中的一者或多者的任何动物,包括人类。一般来讲,受试者是人类或鸟类动物、牛科动物、犬科动物、马科动物、猫科动物、山羊类动物、狼类动物、鼠科动物、绵羊类动物和猪类动物。“伴侣动物”是任何驯养的动物,并且包括但不限于猫、狗、兔、豚鼠、雪貂、仓鼠、小鼠、沙鼠、马、牛、山羊、绵羊、驴、猪等。优选地,受试者是人类或伴侣动物,诸如狗或猫。在人类的背景中,术语“老年”是指自出生起的年龄为至少60岁,优选地63岁以上,更优选地65岁以上,并且最优选地70岁以上。在人的上下文中,术语“中老年”是指自出生起年龄为至少45岁,优选50岁以上,更优选55岁以上的年龄,并且包括老年个体。对于其他动物,“中老年”是指已超过其特定物种和/或物种内品种的平均寿命的50%。如果动物超过平均预期寿命的66%,则将其视为“老年”,优选超过平均预期寿命的75%,更优选超过平均预期寿命的80%。老年猫或狗自出生起的年龄为至少约7岁。
如本文所用,“有效量”是在受试者中预防缺陷、治疗障碍、病症或疾病的量,或更一般地讲,是减轻症状、管理疾病进展或向受试者提供营养、生理或医学有益效果的量。相对术语“改善”、“增加”、“增强”等是指本文所公开的组合物相对于缺乏一种或多种成分和/或具有不同量的一种或多种成分但以其他方式相同的组合物的效应。
1.5通用术语
如本文所用,单数形式“一个”、“一种”和“该”包括多个指代物,除非上下文明确地另外指明。因此,例如,提及“一种组分”或“所述组分”包括两种或更多种组分。
除非另有定义,否则本文所用的所有技术和科学术语具有与本发明所属领域的技术人员通常所理解的含义。本文参考了本领域的那些技术人员已知的各种方法和材料。阐述重组dna技术的一般原理的标准参考文献包括sambrooketal.,molecularcloning:alaboratorymanual,第2版,coldspringharborlaboratorypress,newyork(1989);kaufmanetal.,eds.,handbookofmolecularandcellularmethodsinbiologyinmedicine,crcpress,bocaraton(1995);mcpherson,ed.,directedmutagenesis:apracticalapproach,irlpress,oxford(1991)。阐述药理学的一般原理的标准参考文献包括goodman和gilman的thepharmacologicalbasisoftherapeutics,第10版,mcgrawhillcompaniesinc.,newyork(2001)。本文所用的标准医学术语具有stedman'smedicaldictionary,第27版中定义的含义,具有兽医学插入物。
本文中表示的所有百分数均以占组合物的总重量的重量计,除非另有表示。如本文所用,“约”、“大约”和“基本上”应理解为是指某一数值范围内的数字,例如该所提及数字的-10%至+10%的范围内,优选该所提及数字的-5%至+5%,更优选该所提及数字的-1%至+1%,最优选该所提及数字的-0.1%至+0.1%。本文中的所有数值范围都应理解为包括该范围内的所有整数或分数。另外,这些数值范围应理解为对涉及该范围内任何数字或数字子集的权利要求提供支持。例如,1至10的公开应理解为支持1至8、3至7、1至9、3.6至4.6、3.5至9.9等的范围。
如本说明书中所用,无论是在过渡短语中还是在权利要求的正文中,术语“包括”和“包含”都将被解释为具有开放式含义。即,该术语将与短语“具有至少”或“包括至少”同义地解释。在过程的上下文中使用时,术语“包含”意指该过程至少包括所述步骤,但可包括附加的步骤。当在化合物或组合物的上下文中使用时,术语“包含”意指该化合物或组合物至少包括所述的特征或化合物,但也可包括附加特征或化合物。在“x和/或y”的上下文中使用的术语“和/或”应被解释为“x”或“y”或“x和y”。在本文中使用的情况下,术语“示例”和“诸如”(尤其是当随后是术语列表时)仅仅是示例性和说明性的,并且不应被视为是排他性或全面性的。
下文详细参考本发明的具体实施方案。虽然将结合这些具体实施方案来描述本发明,但应当理解,并非旨在将本发明限制于此类具体实施方案。相反,其旨在涵盖可包括在由权利要求限定的本发明的实质和范围内的替代形式、修改形式和等同形式。在说明书中阐述了许多具体细节,以便提供对本发明的透彻理解。可在没有这些具体细节中的一些或全部的情况下实践本发明。在其他情况下,未详细描述熟知的方法和协议,以免不必要地模糊本发明。
附图说明
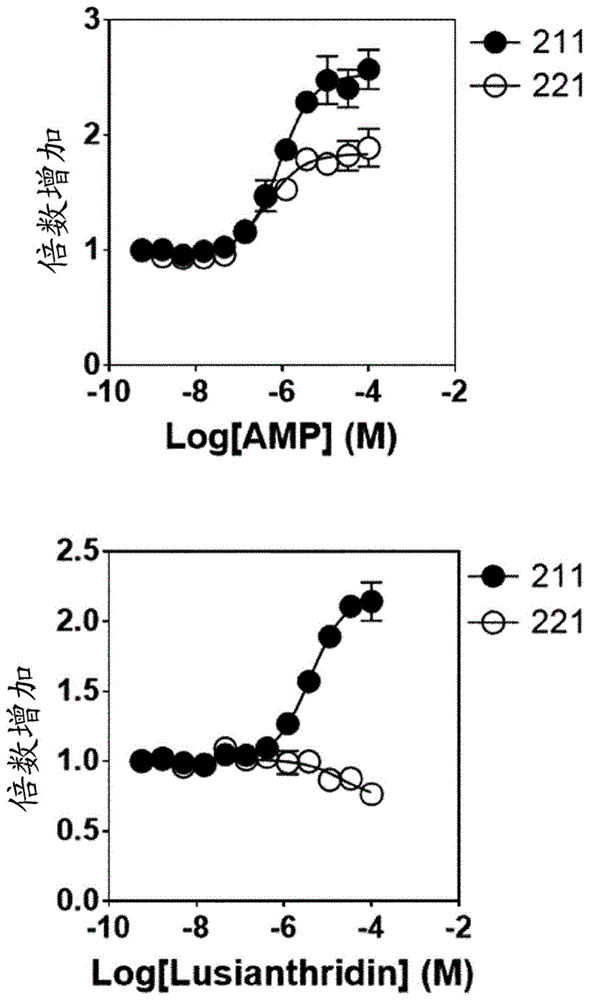
图1:amp和lusianthridin对细菌表达的ampkα2β1γ1(211)或α2β2γ1(221)复合物的活化。lusianthridin(7-甲氧基-9,10-二氢菲-2,5-二醇,cas号87530-30-1)不活化含β2的复合物。先前已报道ampk中的变构药物和代谢(adam)结合位点处的活化剂对含β2的ampk复合物的活化较弱。相比之下,amp-结合位点处的调节剂不受ampk的β-同种型组合物的影响。
图2:amp和lusianthridin对细菌表达的ampkα1β1γ1(111)或α2β1γ1(211)复合物的活化。lusianthridin活化含α1的复合物和含α2的复合物。
图3:amp和lusianthridin对细菌表达的ampkα2β1γ1(211)或α2β1γ1γ1r298g(211r298g)突变复合物的活化。lusianthridin仍活化在γ1amp结合口袋中带有突变的ampk复合物。相比之下,该突变体的amp调节受损。这表明lusianthridin不通过ampkγ亚基中的核苷酸结合位点活化ampk。
图4:amp和lusianthridin对细菌表达的ampkα2β1γ1(211)或其中碳水化合物结合模块(cbm)从复合物缺失(δcbm)的α2β1γ1复合物(211δcbm)的活化。lusianthridin不活化α2β1γ1δcbm突变体。cbm形成adam结合位点的整体部分并介导活化剂在该位点的结合。这些数据表明lusianthridin在该位点活化ampk。
图5:amp和lusianthridin对细菌表达的ampkα2β1γ1(211)或带有β1s108a突变的α2β1γ1复合物(211s108a)的活化。lusianthridin不活化具有s108a突变的ampk复合物。先前,已表明s108a突变干扰adam结合位点处ampk的调节。重要的是,磷酸化的s108残基在β1亚基的cbm和α亚基的激酶结构域之间形成重要相互作用。
图6:lusianthridin增加ampk底物即乙酰-coa羧化酶(acc)在u2osflp-int-rex哺乳动物细胞中的磷酸化。
(a)htrf测定
(b)蛋白质印迹分析
图7:lusianthridin增加ampk底物acc在小鼠原代肝细胞中的磷酸化。
图8:lusianthridin显示出对原代肝细胞中脂肪生成的剂量依赖性抑制。
图9:lusianthridin增加分化的c2c12细胞中的葡萄糖摄取。
图10:化合物2、化合物3、化合物4和化合物5对细菌表达的ampkα2β1γ1复合物的活化。
化合物2、化合物3、化合物4和化合物5活化ampkα2β1γ1复合物。
化合物2被称为7-甲氧基-9,10-二氢菲-2,3,5-三醇。
化合物3被称为2,5-菲二醇,9,10-二氢-,9,10-二氢菲-2,5-二醇,cas号为1071055-42-9。
化合物4被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢,cas号为70205-52-6。
化合物5被称为cannithrene1、大麻二氢菲、9,10-二氢-7-甲氧基-3,5-菲二醇、3,5-菲二醇、9,10-二氢-7-甲氧基、7-甲氧基-9,10-二氢菲-3,5-二醇,cas号为71135-80-3。
图11:化合物4对各种细菌表达的ampk复合物和突变体的活化。
211表示ampkα2β1γ1;221表示ampkα2β2γ1;111表示ampkα1β1γ1;
211s108a表示ampkα2β1γ1s108a突变体;
211δcbm表示ampkα2β1γ1δcbm突变体
化合物4被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢,cas号为70205-52-6。
化合物4活化含α1复合物和含α2复合物,但不活化含β2复合物、α2β1γ1δcbm突变体和具有s108a突变体的ampk复合物。总之,这表明化合物4通过结合到ampk的adam口袋来活化ampk。
图12:化合物2、化合物3、化合物4和化合物5增加ampk底物即乙酰-coa羧化酶(acc)在u2osflp-int-rex哺乳动物细胞中的磷酸化。
化合物2被称为7-甲氧基-9,10-二氢菲-2,3,5-三醇。
化合物3被称为2,5-菲二醇,9,10-二氢-,9,10-二氢菲-2,5-二醇,cas号为1071055-42-9。
化合物4被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢,cas号为70205-52-6。
化合物5被称为cannithrene1、大麻二氢菲、9,10-二氢-7-甲氧基-3,5-菲二醇、3,5-菲二醇、9,10-二氢-7-甲氧基、7-甲氧基-9,10-二氢菲-3,5-二醇,cas号为71135-80-3。
图13:化合物4显示出对原代肝细胞中脂肪生成的剂量依赖性抑制。
化合物4被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢,cas号为70205-52-6。
图14:化合物4增加分化的c2c12细胞中的葡萄糖摄取。
化合物4被称为9,10-二氢菲-2,4,7-三醇、9,10-二氢-2,4,7-菲三醇、2,4,7-三羟基-9,10-二氢菲、2,4,7-菲三醇、9,10-二氢,cas号为70205-52-6。
图15:lusianthridin不增加缺乏ampkα1/α2亚基的c2c12中的葡萄糖摄取。
图16:胰岛素可增加缺乏ampkα1/α2亚基的c2c12中的葡萄糖摄取。
图17:wortmanin不影响c2c12中的lusianthridin刺激的葡萄糖摄取。
图18:lusianthridin没有对小鼠原代肝细胞显示出细胞毒性效应。
将小鼠原代肝细胞用指定浓度的lusianthridin、寡霉素和fccp在37℃处理1小时。通过使用mtt测定法按照制造商的方案确定细胞活力。结果显示为用这些化合物处理后活细胞的百分比。
图19:如通过pacchtrf测定法所评估的,lusianthridin不活化稳定表达adam结合位点ampk突变体(β1s108a)的细胞中的ampk。
β1wt和β1s108a突变体在ampkβ1β2双敲除细胞中稳定表达,并且在37℃用不同浓度的lusianthridin处理30分钟。lusianthridin不增加表达β1s108a突变体的细胞中的pacc。相比之下,lusianthridin能够活化表达β1wt的细胞。
图20:如通过蛋白质印迹分析所评估的,lusianthridin不活化稳定表达adam结合位点ampk突变体(β1s108a)的细胞中的ampk。
与表达β1wt的细胞相比,lusianthridin不增加表达β1s108a突变体表达细胞的细胞中acc的磷酸化。总之,这展示出lusianthridin活化细胞中ampk的能力是通过其结合到adam位点而不是ampk的核苷酸结合位点的能力。
实施例
实施例1
通过(3-(苄氧基)-5-甲氧基苄基)三苯基溴化鏻和5-(苄氧基)-2-碘苯甲醛之间的维蒂希反应化学合成lusianthridin
部分1:(3-(苄氧基)-5-甲氧基苄基)三苯基溴化鏻的合成。
在合适的保护之后,将3,5-二羟基苯甲酸甲酯还原为伯醇,并且在与三苯基膦反应之前转化为其对应的卤代烷,以得到所需的三苯基鏻叶立德试剂(方案1)。
试剂和条件:(a)k2co3,bnbr,丙酮,60℃,31%;(b)k2co3,mel,丙酮,室温,94%;(c)lah,thf,室温,92%;(d)pbr3,1,4-二氧杂环己烷,40℃,80%;(e)pph3,甲苯,100℃,82%。
方案1:(3-(苄氧基)-5-甲氧基苄基)三苯基溴化鏻的合成。
步骤a:向3,5-二羟基苯甲酸甲酯1(300g,1784.12mmol)的丙酮(7200ml)溶液中加入碳酸钾(271.22g,1962.53mmol)。将悬浮液在室温搅拌10分钟。加入苄基溴(222.50mml,1873.32mmmol),并且将所得悬浮液在60℃加热12h。冷却至室温后,过滤悬浮液,用丙酮洗涤滤饼,并且将滤液浓缩成残余物。将残余物通过自动正相色谱法纯化并用乙酸乙酯/己烷洗脱,以得到3-(苄氧基)-5-羟基苯甲酸甲酯2,为灰白色固体。(144g,31%收率)。1hnmr(300mhz,dmso-d6)δppm:9.89(s,1h),7.33-7.46(m,5h),7.01(dd,j=6.30,0.90hz,2h),6.67(t,j=2.40hz,1h),5.11(s,2h),3.82(s,3h);ms(es+)m/z257.1[m-h]+;hplc-uv分析:保留时间=13.35分钟;检测:190-400nm:峰面积,99.81%;洗脱液a,0.1%tfa的水溶液;洗脱液b,乙腈;30分钟内等度/梯度为流速为1.0mlmin-1。
步骤b:向3-(苄氧基)-5-羟基苯甲酸甲酯2(140g,542.06mmol)的丙酮(7000ml)溶液中加入碳酸钾(224.74g,1626.20mmol)。将悬浮液在室温搅拌10分钟。加入碘甲烷(168.73ml,2710.34mmol),并且将所得悬浮液在室温搅拌16h。过滤悬浮液,用丙酮洗涤滤饼,并且将滤液浓缩成残余物。将残余物通过自动正相色谱法纯化并用乙酸乙酯/己烷洗脱,以得到3-(苄氧基)-5-甲氧基苯甲酸甲酯3,为液体。(125g,94%收率)。1hnmr(300mhz,dmso-d6)δppm:7.33-7.48(m,6h),7.16(t,j=2.10hz,1h),7.08(d,j=1.20hz,1h),6.87(t,j=2.40hz,1h),5.15(s,2h),3.84(s,3h),3.79(s,3h);ms(es+)m/z273.1[m+h]+;hplc-uv分析:保留时间=15.31分钟;检测:190nm-400nm:峰面积,99.78%;洗脱液a,0.1%tfa的水溶液;洗脱液b,乙腈;30分钟内等度/梯度为流速为1.0mlmin-1。
步骤c:在0℃,将氢化铝锂(16.86g,444.36mmol)的thf(605ml)溶液加入到3-(苄氧基)-5-甲氧基苯甲酸甲酯3(121g,444.36mmol)的thf(1600ml)溶液中。将悬浮液在0℃搅拌20min,在室温搅拌1h。将反应混合物用thf稀释,并且通过加入水淬灭。将所得混合物通过硅藻土垫过滤,并且用乙酸乙酯洗涤。将滤液真空浓缩,以得到(3-(苄氧基)-5-甲氧基苯基)甲醇4,为液体。(100g,92%收率)。1hnmr(300mhz,dmso-d6)δppm:7.30-7.46(m,5h),6.59(d,j=0.60hz,1h),6.51(s,1h),6.45(d,j=2.40hz,1h),5.19(t,j=5.70hz,1h),5.07(s,2h),4.44(d,j=5.70hz,2h),3.72(s,3h);ms(es+)m/z245.1[m+h]+;hplc-uv分析:保留时间=12.86分钟;检测:190nm-400nm:峰面积,99.64%;洗脱液a,0.1%tfa的水溶液;洗脱液b,乙腈;30分钟内等度/梯度为流速为1.0mlmin-1。
步骤d:向(3-(苄氧基)-5-甲氧基苯基)甲醇4(100g,409.34mmol)的1,4-二噁烷(1000ml)溶液中加入三溴化磷(50.54ml,532.15mmol)。将反应混合物在40℃搅拌1h,并且通过加入水淬灭。用乙酸乙酯萃取水相,并且将合并的有机萃取物用水、盐水洗涤并且浓缩,以得到1-(苄氧基)-3-(溴甲基)-5-甲氧基苯5,为浅黄色固体。(100g,80%收率)。1hnmr(300mhz,dmso-d6)δppm:7.33-7.46(m,5h),6.72(s,1h),6.63(s,1h),6.54(d,j=1.80hz,1h),5.09(d,j=5.40hz,2h),4.62(d,j=5.70hz,2h),3.74(s,3h);ms(es+)m/z309[m+2h]+;hplc-uv分析:保留时间=15.77分钟;检测:190nm-400nm:峰面积,99.71%;洗脱液a,0.1%tfa的水溶液;洗脱液b,乙腈;30分钟内等度/梯度为流速为1.0mlmin-1。
步骤e:向1-(苄氧基)-3-(溴甲基)-5-甲氧基苯5(100g,325.53mmol)的甲苯(2488ml)溶液中,加入三苯基膦(85.38g,325.53mmol)。将反应混合物在100℃搅拌6h,然后使其冷却至室温。通过过滤收集固体,用醚洗涤,并且真空干燥,以得到(3-(苄氧基)-5-甲氧基苄基)三苯基溴化鏻6,为灰白色固体。(150g,82%收率)。1hnmr(400mhz,dmso-d6)δppm:7.89-7.91(m,3h),7.65-7.75(m,12h),7.28-7.37(m,5h),6.51(s,1h),6.23(s,1h),6.12(s,1h)5.07(d,j=15.60hz,2h),4.82(s,2h),3.48(s,3h);ms(es+)m/z489.2[m-hbr]+;hplc-uv分析:保留时间=14.19分钟;检测:190nm-400nm:峰面积,95.51%;洗脱液a,0.1%tfa的水溶液;洗脱液b,乙腈;30分钟内等度/梯度为流速为1.0mlmin-1。
部分2:5-(苄氧基)-2-碘苯甲醛的合成
如方案2所示,在邻位碘化之前,对3-羟基苯甲醛进行了保护。
试剂和条件:(a)k2co3,bnbr,丙酮,60℃,96%;(b)cf3cooag,i2,chcl3,室温,59%;
方案2:5-(苄氧基)-2-碘苯甲醛的合成。
步骤a:向3-羟基苯甲醛7(25g,204.85mmol)的丙酮(250ml)溶液中加入碳酸钾(42.46g,307.27mmol)。将悬浮液在室温搅拌10分钟。加入苄基溴(31.38ml,264.25mmol),并且将所得悬浮液在60℃加热12h。冷却至室温后,过滤悬浮液,用丙酮洗涤滤饼,并且将滤液浓缩成残余物。将残余物通过自动正相色谱法纯化,并用乙酸乙酯/己烷洗脱,以得到3-(苄氧基)苯甲醛8,为灰白色固体。(42g,96%收率)。1hnmr(400mhz,dmso-d6)δppm:9.98(s,1h),7.27-7.50(m,5h),7.25-7.26(m,2h),5.14(s,2h);gcms:m/z212.1:(gcms条件:柱:hp-5(30m×320μm×0.25μm);梯度:120℃-300℃,40℃min-1;hplc-uv分析:保留时间=14.37分钟;检测:190nm-400nm:峰面积,99.58%;洗脱液a,0.1%tfa的水溶液;洗脱液b,乙腈;30分钟内等度/梯度为流速为1.0mlmin-1。
步骤b:向3-(苄氧基)苯甲醛8(42g,197.87mmol)的氯仿(1050ml)溶液中加入三氟乙酸银(65.56g,296.81mmol)。将悬浮液在0℃搅拌10分钟。在0℃加入碘(32.43g,126.90mmol),将所得悬浮液在室温搅拌12小时,并通过加入水淬灭。将所得混合物通过硅藻土垫过滤,用二氯甲烷洗涤。用二氯甲烷萃取水相,并且将合并的有机萃取物用水、盐水洗涤,并且浓缩成残余物。将残余物通过自动正相色谱法纯化,并且用乙酸乙酯/己烷洗脱,以得到5-(苄氧基)-2-碘苯甲醛9,为灰白色固体。(40g,59%收率)。1hnmr(400mhz,cdcl3)δppm:10.04(s,1h),7.83(d,j=8.40hz,1h),7.54(s,1h),7.37-7.53(m,5h),7.01(dd,j=8.80,3.20hz,1h),5.12(s,2h);gcmsm/z338:(gcms条件:柱:zb1ms(10m×100μm×0.1μm);梯度:120℃-300℃,40℃min-1;hplc-uv分析:保留时间=16.04分钟;检测:190nm-400nm:峰面积,99.84%;洗脱液a,0.1%tfa的水溶液;洗脱液b,乙腈;30分钟内等度/梯度为流速为1.0mlmin-1。
部分3:lusianthridin的合成。
如方案3所示,通过(3-(苄氧基)-5-甲氧基苄基)三苯基溴化鏻和5-(苄氧基)-2-碘苯甲醛之间的维蒂希反应,然后环化、脱保护和还原来制备lusianthridin。
试剂和条件:(a)kotbu,5-(苄氧基)-2-碘苯甲醛,thf,室温,86%;(b)bu3snh,aibn,甲苯,100℃,65%;(c)pd/c,acoh,thf,氢气球,室温,然后sfc
方案3:lusianthridin的合成。
步骤a:向5-(苄氧基)-2-碘苯甲醛9(36g,106.46mmol)的thf(3600ml)溶液中,加入(3-(苄氧基)-5-甲氧基苄基)三苯基溴化鏻6(127.32g,223.57mmol)。将悬浮液在0℃搅拌。在0℃加入叔丁醇钾(26.28g,234.08mmol),并且将所得悬浮液在室温搅拌12h。将反应混合物浓缩成残余物,并且将残余物通过自动正相色谱法纯化,并且用乙酸乙酯/己烷洗脱,以得到(z)-4-(苄氧基)-2-(3-(苄氧基)-5-甲氧基苯乙烯基)-1-碘苯10,为灰白色固体。(50g,86%收率)。1hnmr(400mhz,cdcl3)δppm:7.74(d,j=8.80hz,1h),7.26-7.42(m,8h),6.89(d,j=3.20hz,1h),6.49-6.65(m,4h),6.40(s,3h),6.33(t,j=1.60hz,1h),4.85(s,4h),3.62(s,3h);ms(es+)m/z549.1[m+h]+;hplc-uv分析:保留时间=18.74分钟;检测:190nm-400nm:峰面积,89.98%;洗脱液a,0.1%tfa的水溶液;洗脱液b,乙腈;30分钟内等度/梯度为流速为1.0mlmin-1。
步骤b:向(z)-4-(苄氧基)-2-(3-(苄氧基)-5-甲氧基苯乙烯基)-1-碘苯10(50g,91.17mmol)的甲苯(1250ml)溶液中加入氢化三丁基锡(49.14ml,182.34mmol)和偶氮二异丁腈(7.48g,45.58mmol)。用氮气将反应混合物曝气5分钟,并且在100℃加热16h。将反应混合物浓缩成残余物,并且将残余物通过自动正相色谱法纯化,并且用乙酸乙酯/己烷洗脱,以得到4,7-双(苄氧基)-2-甲氧基菲11a和2,7-双(苄氧基)-4-甲氧基菲11b的1∶1混合物,为灰白色固体。(25g,65%收率)。ms(es+)m/z421.3[m+h]+;hplc-uv分析:保留时间=(6.59&6.70)分钟;检测:190nm-400nm:峰面积,99.28%;洗脱液a,0.1%tfa的水溶液;洗脱液b,0.1%tfa的乙腈溶液;10分钟内等度/梯度为流速为2.0mlmin-1。
步骤c:向4,7-双(苄氧基)-2-甲氧基菲11a和2,7-双(苄氧基)-4-甲氧基菲11b(25g,59.45mmol)的乙酸(2000ml)和thf(250ml)溶液中加入10%pd/c(25g)。将反应混合物在室温在氢气球下搅拌2天。将所得混合物通过硅藻土垫过滤,用乙酸乙酯洗涤,并且将滤液浓缩,以得到区域异构体的1:1混合物。(11.50g,79%收率)。将该粗产物(11.50g,1:1混合物)通过sfc(sfc条件:柱:ymc直链淀粉-c;检测:210nm:助溶剂:0.5%异丙胺的甲醇溶液;流速为4.0mlmin-1)纯化,以得到7-甲氧基-9,10-二氢菲-2,5-二醇lusianthridin,为灰白色固体(1.1g)。1hnmr(400mhz,dmso-d6)δppm:9.60(s,1h),9.18(s,1h),8.08(d,j=8.80hz,1h),6.60(s,1h),6.59(d,j=7.20hz,1h),6.37(s,1h),6.32(s,1h),3.70(s,3h),2.60(s,4h);13cnmr(100mhz,dmso-d6)δppm:158.13,155.52,155.45,140.32,138.86,129.05,124.67,114.86,114.62,113.09,105.15,100.97,55.25,30.70,29.95;ms(es+)m/z243.1[m+h]+;c15h14o3+0.2ch3oh的元素分析计算值(%):c73.41,h6.00。实测值:c73.43,h5.84;hplc-uv分析:保留时间=11.84分钟;检测:190nm-400nm:峰面积,98.62%;洗脱液a,0.1%tfa的水溶液;洗脱液b,乙腈;30分钟内等度/梯度为流速为1.0mlmin-1。
实施例2
lusianthridin以剂量依赖性方式活化细菌表达的ampkα2β1γ1和α1β1γ1复合物。
lusianthridin(cas87530-30-1)是从笋兰(thuniaalba)果实中分离得到的。其源自analyticon(np-012362)。该植物于2003年通过analyticon的生物材料供应商购买。原产国家是尼泊尔。ampk异源三聚体在细菌中表达,并且通过镍纯化通过his-α亚基纯化。ampk复合物通过凝胶过滤纯化并通过与camkkβ温育磷酸化,并且通过最终凝胶过滤纯化步骤进一步纯化。使用来自htrf-kineasecisbio测定试剂盒(stks1试剂盒)的底物和试剂,将磷酸化纯化的ampk与不同浓度的配体一起温育30分钟。根据制造商的方案(和coulerieetal.,(2016)pmid:27792327),通过与供体和受体抗体在室温温育2h测量底物的磷酸化,并通过进行htrf检测磷酸化肽。确定665nm/620nm比率,并且将结果绘制为与不含任何化合物的相应ampk复合物相比的活化倍数。
图1至图5示出lusianthridin(7-甲氧基-9,10-二氢菲-2,5-二醇,cas号为87530-30-1)不活化含β2-亚基的ampk复合物。此外,它不活化在β1亚基中具有突变(s108a)或碳水化合物结合模块的缺失(δcbm)的ampk复合物。该活化特征图是通过adam(变构药物和代谢)位点介导其效应的活化剂的表征。表现出amp调节受损的ampkγ1r298g突变体对由lusianthridin活化没有影响。这些数据与在α亚基的激酶结构域和β亚基的cbm之间形成的ampk的adam结合口袋处的lusianthridin活化一致。
实施例3
lusianthridin增加ampk底物即乙酰-coa羧化酶(acc)在u2osflp-int-rex哺乳动物细胞中的磷酸化。
将u2osflp-int-rex细胞以100k接种于96孔板中,并在37℃置于补充有10%(体积/体积)fbs和100u/ml青霉素g以及100μg/ml链霉素的dmemglutamax(赛默飞世尔科技公司(thermofisherscientific))中过夜。根据制造商的方案(cisbio),在缺乏fbs的培养基中用不同浓度的lusianthridin处理细胞1小时,然后在50μl的补充有封闭溶液的cisbio裂解缓冲液#1中裂解细胞。将细胞在室温裂解30分钟,然后将16μl裂解物与4μlhtrf抗体(受体和供体(p)acc抗体的1:40稀释液,按照制造商的方案)一起温育。在使用moleculardevicesi3读板机(具有htrf柱添加)确定665nm/620nm比率之前,将裂解物与抗体温育过夜。对于蛋白质印迹分析,将sds-样品缓冲液添加至该裂解物的其余部分,在95℃变性,然后用磷酸特异性和总acc抗体(细胞信号传导)进行蛋白质印迹分析。将带通过与li-cor二抗温育而可视化,并在li-corodersey机上扫描。
图6(a)示出,使用pacchtrf测定试剂盒(cisbio),lusianthridin以剂量依赖性方式增加ampk底物acc在u2osflp-int-rex哺乳动物细胞中的磷酸化。acc的磷酸化广泛用作ampk活性的细胞指示剂。
图6(b)示出了用不同浓度的lusianthridin处理的u2osflp-int-rex裂解物的蛋白质印迹分析。使用磷酸特异性acc和总acc抗体(细胞信号传导)探测裂解物。这些数据表明,lusianthridin活化细胞中的ampk,并且这导致其下游底物之一磷酸化。
实施例4
lusianthridin增加ampk底物acc在小鼠原代肝细胞中的磷酸化。
肝细胞分离:首先用50ml灌注缓冲液(含有0.5μmedta的krebs-hepes缓冲液)灌注肝脏,然后用50ml胶原酶a缓冲液(含有5mmcacl2和0.5mg/ml胶原酶的krebs-hepes缓冲液)灌注肝脏。在通过100μm网孔之后,将细胞溶液用冷培养基洗涤若干次,最后将细胞培养沉淀物重悬于培养基(培养基199(m199)+glutamax,100u/ml青霉素g和100μg/ml链霉素,0.1%(wt/vol)bsa,10%fcs,10nm胰岛素,200nm三碘甲状腺原氨酸和500nm地塞米松)中。保留肝细胞附着(3-4小时)并在补充有抗生素和100nm地塞米松的m199中培养过夜。第二天早晨将细胞用于实验。
将原代肝细胞以15k细胞接种于96孔板中过夜。根据制造商的方案(cisbio),在培养基中用不同浓度的lusianthridin处理细胞1小时,然后在50μl的补充有封闭溶液的cisbio裂解缓冲液#1中裂解细胞。将细胞在室温裂解30分钟,然后将16μl裂解物与4μl的htrf抗体一起温育。在使用moleculardevicesi3读板机(具有htrf柱添加)确定665nm/620nm比率之前,将裂解物与抗体温育过夜。
图7示出使用pacchtrf测定试剂盒(cisbio),lusianthridin以剂量依赖性方式增加ampk底物acc在原代肝细胞中的磷酸化(在37℃温育1小时)。
实施例5
lusianthridin显示出对原代肝细胞中脂肪生成的剂量依赖性抑制。
对于原代肝细胞分离,参见实施例4。对于原代肝细胞中的脂肪生成测量,将细胞以600k细胞/孔接种于6孔板中过夜。在存在[1-14c]-乙酸酯的情况下,在37℃与不同浓度的lusianthridin一起温育1小时之前,用新鲜m199培养基单独替换培养基2小时。在与水相分离之后,在下有机层中确定[14c]向脂肪酸中的掺入。结果显示为每分钟崩解(dpm)每μg蛋白质。
脂肪生成受ampk底物acc控制,并且ampk对acc的磷酸化和抑制导致脂肪生成减少。通过确定14c-标记的乙酸盐向脂肪酸中的掺入,测量原代肝细胞中的脂肪生成。在37℃,在存在或不存在不同浓度的lusianthridin的情况下监测脂肪生成1小时。图8所示的结果以dpm每μg总蛋白质表示,表明lusianthridin能够以剂量依赖性方式抑制脂肪生成。该观察结果与其在肝细胞中活化ampk的能力一致,这导致acc的磷酸化和抑制。这些数据与先前通过htrf测定和蛋白质印迹分析(参见上文实施例)确定的lusianthridin活化细胞系和原代肝细胞两者中的ampk的能力一致。
实施例6
lusianthridin增加分化的c2c12细胞中的葡萄糖摄取。
将c2c12细胞维持在补充有10%(体积/体积)fbs和100u/ml青霉素g以及100μg/ml链霉素的dmemglutamax中。通过在补充有2%(体积/体积)马血清和抗生素的dmemglutamax中培养7天,c2c12成肌细胞分化成肌管。将细胞转移至无血清培养基保持24小时,然后在处理前与无碳酸氢盐的培养基进行平衡。在存在3h-2-脱氧葡萄糖的情况下(在含有丙酮酸钠的krebs-hepes缓冲液中),用对照(dmso1%最终浓度)或100μmlusianthridin处理细胞。将细胞裂解,并使用闪烁计数器确定这些样品中的3h的量。
先前已显示肌肉细胞中ampk的活化增加葡萄糖摄取。因此,测试分化的肌肉细胞系c2c12细胞中ampk的活化是否将导致葡萄糖摄取增加。将分化的c2c12细胞在37℃用对照或100μmlusianthridin处理4小时。通过监测细胞中3h-2-脱氧葡萄糖的摄取来确定葡萄糖摄取。图9中的结果显示为相对于对照孔的倍数增加。这些结果显示,lusianthridin导致c2c12细胞中的葡萄糖摄取增加约2倍。这些数据表明,lusianthridin活化肌肉中ampk的能力导致下游底物磷酸化,最终导致该肌肉细胞系中的葡萄糖摄取增加。这与ampk在介导肌肉中葡萄糖摄取中的重要作用一致。
实施例7
另外的二氢菲类似物直接变构活化ampk并增加细胞中的底物磷酸化。
对于ampk体外活性测定,参见实施例2。图10示出化合物2、化合物3、化合物4和化合物5活化细菌表达的ampkα2β1γ1复合物。与lusianthridin类似,化合物4不活化含β2的复合物、α2β1γ1δcbm突变体和具有s108a突变的ampk复合物(图11)。总之,这表明lusianthridin和化合物4共享共同的活化机制,并且该活性分布是通过结合到adam口袋来调节ampk的配体的特征。
对于u2osflp-int-rex细胞的处理,参见实施例3。图12示出使用pacchtrf测定试剂盒(cisbio),化合物2、化合物3、化合物4和化合物5以剂量依赖性方式增加ampk底物acc在u2osflp-int-rex哺乳动物细胞中的磷酸化。
实施例8
化合物4活化小鼠原代肝细胞中的ampk并减少肝脂肪生成,以及增加c2c12细胞中的葡萄糖摄取。
分离小鼠原代肝细胞(参见实施例4)并在确定脂肪生成速率(参见实施例5)之前用不同浓度的化合物4在37℃处理(参见实施例5)1小时。如图13所示,化合物4引起脂肪生成速率的剂量依赖性降低,这与采用lusianthridin时所见的效果相当。
在用化合物4处理之前,将c2c12细胞培养并分化成肌管(参见实施例6)。图14示出化合物4引起葡萄糖摄取增加约2倍,这与采用lusianthridin时所见的效果相当。
实施例9
lusianthridin增加c2c12肌管中葡萄糖摄取的能力取决于ampk
为了测试lusianthridin增加c2c12肌管中葡萄糖摄取的能力是否依赖于ampk,我们生成了缺乏催化ampkα亚基(ampkα1α2-/-)的两种同种型的c2c12细胞。通过用含有与绿色荧光蛋白表达连接的cas9酶和靶向鼠ampkα1亚基(sc-430618,santacruz)和鼠ampkα2亚基(sc-430803,santacruz)的cas9向导rna序列的质粒瞬时转染野生型细胞来产生c2c12ampkα1α2双敲除细胞系。通过流式细胞术将绿色荧光蛋白表达阳性的细胞单细胞分选到含有生长培养基的96孔板中,并在克隆扩增后分析ampk信号传导的损失。
将分化的c2c12ampkα1α2+/+和ampkα1α2-/-细胞在37℃用载体(0.2%dmso)、30μm或100μmlusianthridin处理1小时。此外,还通过在存在或不存在15nmwortmanin(一种胰岛素信号传导抑制剂)的情况下用300nm胰岛素处理c2c12细胞1小时来评估胰岛素依赖性/ampk非依赖性葡萄糖摄取。最后,将分化的c2c12ampkα1α2+/+和ampkα1α2-/-细胞在存在或不存在15nmwortmanin的情况下,在37℃用载体(0.2%dmso)或100μmlusianthridin处理1小时。对于wortmanin实验,在处理前将分化的c2c12细胞与dmso或wortmanin一起预温育1小时。
通过监测细胞中3h-2-脱氧葡萄糖的摄取来确定葡萄糖摄取。将c2c12ampkα1α2+/+和ampkα1α2-/-细胞维持在补充有20%(体积/体积)fbs和100u/ml青霉素g以及100μg/ml链霉素的dmemglutamax中。通过在补充有1%(体积/体积)马血清和抗生素的dmemglutamax中培养5-7天,c2c12成肌细胞分化成肌管。将细胞转移至无血清培养基保持24小时,然后在处理前与无碳酸氢盐的培养基进行平衡。在存在3h-2-脱氧葡萄糖的情况下(在含有丙酮酸钠的krebs-hepes缓冲液中),处理细胞。将细胞裂解,并使用闪烁计数器确定这些样品中的3h的量。通过将每种处理条件下获得的每分钟计数除以载体对照条件下获得的每分钟计数来确定葡萄糖摄取的倍数变化。
图15至图17中的结果显示为相对于对照孔的倍数变化。图15和图16中的结果表明,用lusianthridin和胰岛素处理c2c12ampkα1α2+/+细胞导致葡萄糖摄取增加。胰岛素刺激的葡萄糖摄取在ampkα1α2-/-细胞中未受影响,但如预期的那样,其效果通过用wortmanin处理而消除其作用(图16)。
相比之下,wortmanin对lusianthridin增加ampkα1α2+/+细胞中葡萄糖摄取的能力没有影响,表明该化合物不会通过胰岛素信号传导途径增加葡萄糖摄取(图17)。相比之下,ampkα1α2-/-细胞中lusianthridin刺激的葡萄糖摄取消失(图15)。总之,这些数据表明,lusianthridin增加c2c12细胞中的葡萄糖摄取的能力取决于其活化ampk的能力。
实施例10
lusianthridin不引起小鼠原代肝细胞中的细胞毒性。
对于原代肝细胞中的细胞毒性实验,将细胞以20k细胞/孔接种于96孔板中的m199培养基中过夜。将肝细胞与不同浓度的lusianthridin、寡霉素或fccp在37℃温育1h。在按照制造商的说明书(thermofisher,v131154)进行mtt测定之前,将培养基更换为不含酚红的培养基。mtt测定法是常规用于测量细胞中化合物的细胞毒性的量热测定法。图18中所示的结果表明,在所有测试的lusianthridin浓度下,细胞活力均无变化。相比之下,两种已知的毒性化合物寡霉素和fccp(羰基氰化物p-(三氟甲氧基)苯腙)导致细胞活力的稳健降低。总之,这表明在高达100μm的最终浓度时,lusianthridin对小鼠原代肝细胞不具有细胞毒性作用。
实施例11
lusianthridin不活化在细胞中的变构药物和代谢物(adam)位点处包含突变的复合物(s108a)。
ampkβ1/β2双敲除u2-osflp-intmt-rextm细胞系由horizondiscovery(cambridge,uk)生成。对细胞通过蛋白质印迹进行基因分析以确认ampkβ1/β2的完全敲除。我们采用这些ampkβ1/β2双敲除细胞,并将人类β1野生型(wt)或β1丝氨酸108的表达重新引入丙氨酸突变(s108a)。这是使用存在于该细胞系中的flp-intm系统(英杰公司(invitrogen))实现的,并且根据制造商的方案产生表达β1wt或β1s108a突变体的稳定细胞。通过蛋白质印迹分析确认β1亚基的再表达。
将稳定表达β1wt或β1s108a突变体的细胞用不同浓度的lusianthridin处理并进行pacchtrf(cisbio)测定或蛋白质印迹分析,以确定ampk底物acc在细胞裂解物中的磷酸化。蛋白质印迹使用li-cor奥德赛系统定量,并显示为来自pacc的抗体信号除以总acc的比率。
如图19和图20中所示,lusianthridin能够剂量依赖性地增加稳定表达β1wt的细胞中的pacc。相比之下,lusianthridin不能增加表达β1s108a突变体的细胞中的pacc。该细胞数据与我们的体外数据一致,体外数据示出lusianthridin不能在别构学上活化重组α2β1γ1s108a复合物。总之,我们表明,在体外和细胞中,lusianthridin通过与ampk的adam口袋结合来活化ampk,adam口袋与ampkγ亚基中的核苷酸结合位点分开。
- 还没有人留言评论。精彩留言会获得点赞!