用于关节软骨修复的带有胶粘剂的支架的制作方法
用于关节软骨修复的带有胶粘剂的支架
1.与相关申请的交叉引用
2.本申请要求2018年6月11日提交的美国临时申请62/683,358的优先权,所述临时申请的公开内容整体通过参考并入本文。
技术领域
3.在屏障组合物上方将基质植入物植入到关节软骨病变部位中,所述屏障组合物有效地抑制细胞、血液和其他材料从软骨下区域迁移到所述病变部位中。
背景技术:
4.关节软骨由包埋在包含水分子、胶原蛋白纤维和蛋白聚糖的大的细胞外基质中的软骨细胞构成。在活动的个体和老年人中,由于急性或重复性外伤损伤或衰老而发生对关节软骨的伤害。此类伤害导致疼痛,影响移动能力并可以导致残疾。当前存在许多正在使用的治疗方法。当前的手术治疗包括微骨折、灌洗、清创术、钻孔术和磨损软骨成形术。
5.灌洗包括用氯化钠、林格氏或林格氏和乳酸盐溶液冲洗关节。清创术包括使软骨的粗糙表面变得光滑并除去半月板的松散部分。这些技术提供暂时的疼痛缓解,但几乎没有或没有进一步愈合的潜力。所述暂时的疼痛缓解据信是由于除去变性的软骨碎片、蛋白水解酶和炎性介导物而引起的。
6.微骨折包括除去损伤的关节软骨,然后通过物理方式损坏下方的软骨下骨骼以暴露出骨髓并产生出血。微骨折通过在软骨下骨骼中钻出小孔以允许骨髓来源的干细胞迁移到软骨缺损部位中来进行。所述手术在清洁软骨缺损后通过关节镜来进行。外科医生可以使用尖锥在软骨下骨骼中产生许多细小骨折。含有干细胞的血液和骨髓从骨折处渗出并产生血凝块,其释放出软骨构建细胞。身体对微骨折的反应如同它对损伤的反应,这导致形成新的替换软骨。所述血凝块引入炎性细胞因子、生长因子和间充质干细胞(msc)以填补所述缺损。这些物质、特别是干细胞允许产生新的软骨。
7.软骨病变部位中修复组织与软骨下骨板之间的通讯可以促进软骨修复。vasara,a.i.等,osteoarthritis and cartilage,2006,14:1066
‑
1074。微骨折可以在7
‑
17年内提供长期改善。steadman,j.r.等,arthroscopy,2003,9(5):477
‑
484。同时,微骨折促进纤维软骨而不是透明软骨的形成。微骨折在治疗老年患者、超重患者和软骨病变部位大于2.5cm的患者中也不太有效。这些患者可能会在手术后仅仅一到两年由于纤维软骨磨损而恢复症状。在那时,这些患者可能不得不重新进行关节软骨修复手术。
8.其他选项包括骨骼软骨自体移植物移植(oat)和骨骼软骨同种异体移植物移植(oca)。然而,oat受到供体部位发病率和无法治疗大的病变部位的限制,oca具有疾病传播和软骨下骨骼塌陷的风险。将细胞或组织直接移植到缺损中和用生物或合成替代物替换所述缺损,目前仅占手术干预的一小部分。
附图说明
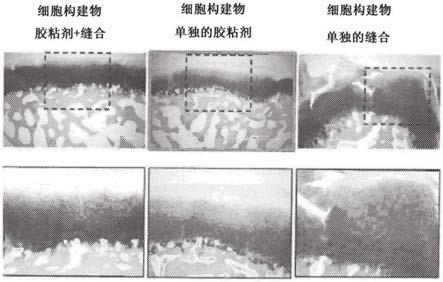
9.图1示出了在软骨下骨骼上方的植入物的组织学分析,其中将上图中的图像的一部分放大并显示在下图中。左图示出了在将缝合的细胞构建物植入到骨骼上方后的组织,其中胶粘剂被施加到所述细胞构建物下方。中图示出了在将细胞构建物植入到骨骼上方后的组织,其中胶粘剂被施加到所述细胞构建物下方。右图示出了在不具有胶粘剂的情况下将缝合的细胞构建物植入到骨骼上方后的组织。
技术实现要素:
10.一方面,提供了一种治疗关节软骨中的损伤或缺损的方法。所述方法包括制备基质植入物,将包含聚合物的屏障组合物施加到所述软骨病变部位的底部,以及将所述植入物植入到所施加的屏障组合物上方。在某些实施方式中,将所述屏障组合物施加到软骨下骨骼。
11.在某些实施方式中,所述屏障组合物有效地阻断细胞、血液或其他材料从所述软骨下区域迁移到所述软骨病变部位中。
12.在某些实施方式中,所述基质植入物是无细胞基质植入物。在某些实施方式中,所述无细胞基质植入物包含以下的一者或多者:i型胶原蛋白、ii型胶原蛋白、iv型胶原蛋白、含有蛋白聚糖的胶原蛋白、含有糖胺聚糖的胶原蛋白、含有糖蛋白的胶原蛋白、芳香族有机酸的聚合物、明胶、琼脂糖、透明质酸、纤连蛋白、层粘连蛋白、生物活性肽生长因子、细胞因子、弹性蛋白、纤维蛋白、由聚乳酸制成的聚合物、由聚乙醇酸制成的聚合物、聚(ε
‑
己内酯)、聚(乙烯醇)、聚(癸二酸)、聚(乳酸
‑
共
‑
乙醇酸)、聚(乳酸
‑
共
‑
ε
‑
己内酯)、聚(乳酸
‑
共
‑
乙烯醇)、聚(乳酸
‑
共
‑
癸二酸),聚(乙醇酸
‑
共
‑
ε
‑
己内酯)、聚(乙醇酸
‑
共
‑
乙烯醇)、聚(乙醇酸
‑
共
‑
癸二酸)、聚(ε
‑
己内酯
‑
共
‑
乙烯醇)、聚(ε
‑
己内酯
‑
共
‑
癸二酸)、聚(乙烯醇
‑
共
‑
癸二酸)、聚氨基酸、羟基聚酰胺、聚酰胺和多肽凝胶。美国专利号8,623,943、9,315,624和9,505,882中描述了示例性的羟基聚酰胺,所有这些专利通过参考并入本文。
13.在某些实施方式中,所述屏障组合物包含以下的一者或多者或由以下形成的聚合产物:明胶,i型胶原蛋白,高碘酸盐氧化的明胶,可光聚合的聚乙二醇
‑
共
‑
聚(
ɑ
‑
羟基酸)二丙烯酸酯大分子单体,用n
‑
(酰氧基)琥珀酰亚胺和硫醇衍生的4臂聚乙二醇加上甲基化胶原蛋白,用烷基化胶原蛋白交联的衍生的聚乙二醇(peg),四
‑
n
‑
羟基琥珀酰亚胺基或四
‑
硫醇衍生的peg(例如来自于covidien的spraygel粘附屏障系统或来自于baxter healthcare的coseal
tm
)以及用甲基化胶原蛋白交联的peg。
14.在某些实施方式中,所述屏障组合物包含密封剂。在某些实施方式中,在将所述屏障组合物施加到所述软骨下骨骼后所述密封剂形成水凝胶。
15.在某些实施方式中,所述屏障组合物或密封剂包含聚合物。在某些实施方式中,所述聚合物是明胶、聚乙二醇(peg)、衍生的peg、聚(氰基丙烯酸酯)、聚氨酯、聚(亚甲基丙二酸酯)、聚乙烯醇、聚酰胺、羟基聚酰胺、衍生的聚乙烯醇、丙烯酸聚合物、纤维蛋白、明胶、带有邻苯二酚侧链的聚苯乙烯、聚酯、包含二羟基酪氨酸的多肽、具有邻苯二酚侧链的聚(α
‑
氨基羧酸)、由沙堡虫(phragmatopoma californica)分泌的聚合物、聚乙二醇和聚丙交酯的共聚物、聚乙二醇和聚乙交酯的共聚物、聚醚、多糖、氧化的多糖、聚阳离子多胺、聚阴离子、聚(酯脲)、聚乙二醇与聚丙交酯或聚乙交酯的共聚物、4臂季戊四醇硫醇和聚乙二醇二
丙烯酸酯、4臂四
‑
n
‑
羟基琥珀酰亚胺酯或四
‑
硫醇衍生的peg、由明胶和氧化的淀粉形成的聚合物、由可光聚合的聚乙二醇
‑
共
‑
聚(a
‑
羟基酸)二丙烯酸酯大分子单体形成的聚合物、高碘酸盐氧化的明胶、血清白蛋白和用马来酰亚胺基、琥珀酰亚胺基、邻苯二甲酰亚胺基和相关的活性基团衍生的双功能聚乙二醇以及用琥珀酰亚胺酯和硫醇衍生的4臂聚乙二醇和甲基化胶原蛋白。在某些实施方式中,所述聚合物是明胶或纤维蛋白,并且所述屏障组合物包含凝血酶或交联剂。
16.在某些实施方式中,所述屏障组合物包含调节粘度的组分。
17.在某些实施方式中,所述屏障组合物包含稳定剂。
18.在某些实施方式中,所述屏障组合物包含有效提高所述屏障组合物的降解速率的酶。
19.在某些实施方式中,所述屏障组合物还包含结构性材料。在某些实施方式中,所述结构性材料包含以下的一者或多者:纤维、纤维蛋白、藻酸盐、透明质酸、明胶、纤维素或胶原蛋白。
20.在某些实施方式中,所述方法还包括在所述基质植入物上方引入顶部保护性生物可降解聚合物的层。
21.在某些实施方式中,所述基质组合物包括增强细胞附着和/或增殖的组分。
22.详细描述
23.定义:
24.除非另有定义,否则本文中使用的技术和科学术语具有与本发明所属领域的普通技术人员通常理解的相同的含义。
25.不带具体数目的指称不表示对数量的限制,而是表示存在“至少一个”所指称的项目。
26.当在本文中使用时,术语“软骨”是指特殊类型的结缔组织,其含有包埋在细胞外基质中的软骨细胞。软骨的生物化学组成根据类型而异,但通常包含胶原蛋白、主要是ii型以及其他次要类型(例如ix和xi型)软骨、蛋白聚糖、其他蛋白质和水。在本领域中已认识到几种类型的软骨,包括例如透明软骨、关节软骨、肋软骨、纤维软骨、半月板软骨、弹性软骨、耳软骨和黄色软骨。
27.当在本文中使用时,术语“软骨细胞”是指能够产生软骨组织的组分的细胞。
28.术语“支持基质”意味着生物学上可接受的溶胶
‑
凝胶或胶原海绵、支架、蜂巢、水凝胶、生物学上可接受的材料,其适合于接受活化的迁移软骨细胞或骨细胞,为软骨细胞的生长和三维繁殖、为形成新的透明软骨或为骨骼软骨细胞迁移到骨骼病变部位中提供结构性支持。
29.本发明人发现,通过在软骨病变部位中,在置于软骨下骨骼上的至少一层屏障组合物的上方配置可生物降解的无细胞基质植入物,有利于健康的透明软骨而不是纤维软骨的形成。不希望受到理论限制,所述屏障组合物有效地阻断细胞、血液或流体从所述软骨下区域迁移到所述病变部位中,它们中的任一者可能倾向于促进所述病变部位中纤维软骨的形成。本发明人已发现,所述阻断可以允许在健康的软骨组织周围的源自于所述植入物的软骨细胞和驻留在滑液或滑膜中的滑膜干细胞在所述植入物中发展出软骨。从滑膜或其他相邻组织迁移而来的细胞可以产生软骨硫酸化糖胺聚糖。所述屏障组合物中的密封剂和胶
粘剂组分可以防止所述软骨下骨骼的穿透,防止骨水肿,并允许所述软骨下骨骼以不依赖于植入物的方式充分愈合。骨水肿是疼痛和引起骨关节炎的变性的来源。本文中描述的方法相比于微骨折提供了优点,包括降低骨水肿的风险和相比于纤维软骨更多地促进透明软骨的形成。
30.基质
31.提供了一种用于治疗关节软骨中的损伤或缺损的基质植入物。所述基质植入物被配置成用于放置在包含聚合物的屏障组合物的上方,所述屏障组合物被施加到软骨病变部位的底部例如软骨下骨骼。
32.在各种不同实施方式中,所述基质是二维或三维结构性组合物或能够转变成二维或三维结构的组合物。在某些实施方式中,所述基质是海绵状结构或蜂巢状网格。
33.在某些实施方式中,所述基质是支持基质。在某些实施方式中,所述支持基质由以下的一者或多者制备:i型胶原蛋白、ii型胶原蛋白、iv型胶原蛋白、明胶、琼脂糖、含有蛋白聚糖、糖胺聚糖或糖蛋白的胶原蛋白、芳香族有机酸的聚合物、纤连蛋白、层粘连蛋白、生物活性肽生长因子、细胞因子、弹性蛋白、纤维蛋白、由聚酸例如聚乳酸、聚乙醇酸或聚氨基酸制成的聚合物、聚己内酯、由聚乳酸制成的聚合物、由聚乙醇酸制成的聚合物、聚(ε
‑
己内酯)、聚(乙烯醇)、聚(癸二酸)、聚(乳酸
‑
共
‑
乙醇酸)、聚(乳酸
‑
共
‑
ε
‑
己内酯)、聚(乳酸
‑
共
‑
乙烯醇)、聚(乳酸
‑
共
‑
癸二酸)、聚(乙醇酸
‑
共
‑
ε
‑
己内酯)、聚(乙醇酸
‑
共
‑
乙烯醇)、聚(乙醇酸
‑
共
‑
癸二酸)、聚(ε
‑
己内酯
‑
共
‑
乙烯醇)、聚(ε
‑
己内酯
‑
共
‑
癸二酸)、聚(乙烯醇
‑
共
‑
癸二酸)、聚氨基酸、羟基聚酰胺、聚酰胺、可吸收的ε
‑
己内酯聚合物、多肽凝胶、其共聚物及其组合。所述凝胶溶液基质可以是聚合热可逆胶凝水凝胶。所述支持基质可以具有下述性质中的一者或多者:生物相容性,生物可降解性,亲水性,非反应性,中性电荷,以及确定的结构。
34.在某些实施方式中,所述基质通过将多糖与包含聚乳酸、聚乙醇酸或包含聚乳酸、聚乙醇酸、聚乙二醇、聚乙烯醇和聚(癸二酸)的共聚物的聚酯温育或将多糖用所述聚酯缠绕来制备。所述多糖可以被氧化。
35.在某些实施方式中,所述基质包含胶原蛋白、透明质酸和硫酸软骨素中的一者或多者。
36.在某些实施方式中,所述屏障组合物包含以下的一者或多者或由以下形成的聚合产物:明胶,i型胶原蛋白,高碘酸盐氧化的明胶,可光聚合的聚乙二醇
‑
共
‑
聚(
ɑ
‑
羟基酸)二丙烯酸酯大分子单体,用n
‑
(酰氧基)琥珀酰亚胺和硫醇衍生的4臂聚乙二醇加上甲基化胶原蛋白,用烷基化胶原蛋白交联的衍生的聚乙二醇(peg),四
‑
n
‑
羟基琥珀酰亚胺基或四
‑
硫醇衍生的peg(例如来自于covidien的spraygel粘附屏障系统或来自于baxter healthcare的coseal
tm
)以及用甲基化胶原蛋白交联的peg。
37.在某些实施方式中,所述屏障组合物包含密封剂。在某些实施方式中,在将所述屏障组合物施加到所述软骨下骨骼后所述密封剂形成水凝胶,
38.在某些实施方式中,所述屏障组合物或密封剂包含聚合物。在某些实施方式中,所述聚合物是明胶、聚乙二醇(peg)、衍生的peg、聚(氰基丙烯酸酯)、聚氨酯、聚(亚甲基丙二酸酯)、聚乙烯醇、聚酰胺、羟基聚酰胺、衍生的聚乙烯醇、丙烯酸聚合物、纤维蛋白、明胶、带有邻苯二酚侧链的聚苯乙烯、聚酯、包含二羟基酪氨酸的多肽、具有邻苯二酚侧链的聚(α
‑
氨基羧酸)、由沙堡虫(phragmatopoma californica)分泌的聚合物、聚乙二醇和聚丙交酯的共聚物、聚乙二醇和聚乙交酯的共聚物、聚醚、多糖、氧化的多糖、聚阳离子多胺、聚阴离子、聚(酯脲)、聚乙二醇与聚丙交酯或聚乙交酯的共聚物、4臂季戊四醇硫醇和聚乙二醇二丙烯酸酯、4臂四
‑
n
‑
羟基琥珀酰亚胺酯或四
‑
硫醇衍生的peg、由明胶和氧化的淀粉形成的聚合物、由可光聚合的聚乙二醇
‑
共
‑
聚(a
‑
羟基酸)二丙烯酸酯大分子单体形成的聚合物、高碘酸盐氧化的明胶、血清白蛋白和用马来酰亚胺基、琥珀酰亚胺基、邻苯二甲酰亚胺基和相关的活性基团衍生的双功能聚乙二醇以及用琥珀酰亚胺酯和硫醇衍生的4臂聚乙二醇和甲基化胶原蛋白。在某些实施方式中,所述聚合物是明胶或纤维蛋白,并且所述屏障组合物包含凝血酶或交联剂。
39.在某些实施方式中,所述基质组合物包括增强细胞附着和/或增殖的组分。
40.在各种不同实施方式中,所述基质是三维有孔支架,其包含由大量纤维形成的生物相容的聚合物,所述纤维被配置成形成非织造三维开孔基质。所述开孔基质可以具有预定的形状。所述开孔基质可以具有预定的孔隙体积分数。所述开孔基质可以具有预定的孔隙形状。例如,所述基质中的孔隙可以形成蜂巢网格。所述开孔基质可以具有预定的孔隙尺寸。
41.在各种不同实施方式中,所述基质或支持基质具有确定的孔隙尺寸。不同的孔隙尺寸允许所述软骨细胞或快或慢地浸润到所述基质中,所述细胞或快或慢地生长和繁殖,并最终允许新的软骨构建物中或高或低的细胞密度,例如在通过参考并入本文的美国专利号8,906,686中所描述的。所述基质的孔隙尺寸可以通过例如改变所述凝胶溶液的ph、胶原蛋白浓度和冷冻干燥条件来调节。所述基质的孔隙尺寸可以是50至500μm、100至300μm或150至250μm。
42.在各种不同实施方式中,所述基质可以是或者可以不是多孔的,并且可以作为填料施加。此类基质可以包含聚合热可逆胶凝水凝胶(trgh)。所述填料可以使用患者自身的滑液来重构,这可以允许用细胞接种所述基质。海绵状材料也可以在植入之前用滑液浸泡。可以允许所述基质在施加后固化。
43.在某些实施方式中,所述基质包含至少一种治疗剂。所述治疗剂可以是例如抗感染剂、止痛药、镇痛剂或抗炎剂和免疫抑制剂。
44.屏障组合物
45.提供了一种用于治疗关节软骨中的损伤或缺损的屏障组合物。所述屏障组合物被施加到软骨病变部位的底部例如软骨下骨骼。基质植入物被放置在屏障组合物上方。在某些实施方式中,在所述基质植入物上方放置顶部保护性生物可降解聚合物。
46.如本文中所述将屏障组合物配置在软骨下骨骼上,可以允许在手术期间在清洁后保护所述病变部位的完整性,并且可以阻止软骨下细胞和细胞产物迁移到软骨缺损的部位中。不希望受到理论限制,这种迁移的阻止产生了用于形成健康的透明软骨的环境,同时也阻止由从骨髓通过软骨下骨骼迁移到所述基质的干细胞形成纤维软骨。
47.所述屏障组合物可以包含密封剂。密封剂是生物学上可接受的通常快速胶凝的制剂,具有指定范围内的粘附和内聚性质。所述密封剂可以是具有粘附和/或胶合性质的生物学上可接受的快速胶凝的合成化合物。在各种不同实施方式中,所述密封剂是水凝胶,例如衍生的聚乙二醇(peg),其优选地用胶原蛋白化合物、通常是烷基化胶原蛋白交联。所述水
凝胶可以在将所述屏障组合物施加到软骨下骨骼后形成。密封剂的实例包括但不限于四
‑
n
‑
羟基琥珀酰亚胺基或四
‑
硫醇衍生的peg或其组合,其可以在商品名coseal
tm
下从cohesion technologies,palo alto,calif.商购(j.biomed.mater.res appl.biomater.,58:545
‑
555(2001));快速形成基质的双组分聚合物组合物,其中所述化合物中的至少一者是聚合的,例如聚氨基酸、多糖、聚亚烷基氧化物或聚乙二醇,并且两个组分通过共价键相连(美国专利号6,312,725,通过参考并入本文);以及用甲基胶原蛋白交联的peg,例如用甲基胶原蛋白交联的聚乙二醇水凝胶。所述密封剂在与组织、特别是与软骨下骨骼接触后,可以快速胶凝或粘合。
48.在各种不同实施方式中,所述屏障组合物包含聚合物。所述屏障组合物中的示例性聚合物包括但不限于明胶和氧化的淀粉、4臂季戊四醇四
‑
硫醇和聚乙二醇二丙烯酸酯、由可光聚合的聚乙二醇
‑
共
‑
聚(a
‑
羟基酸)二丙烯酸酯大分子单体形成的聚合物、高碘酸盐氧化的明胶、血清白蛋白和用马来酰亚胺基、琥珀酰亚胺基、邻苯二甲酰亚胺基和相关的活性基团衍生的双功能聚乙二醇以及用琥珀酰亚胺酯和硫醇衍生的4臂聚乙二醇和甲基化胶原蛋白。
49.在某些实施方式中,所述屏障组合物包含聚乙二醇、基于聚乙二醇的材料或交联的聚乙二醇。示例性的基于聚乙二醇(peg)的材料包括但不限于ct
‑
3、(baxter)、(hyperbranch medical technology)和(ocular therapeutics)。在某些实施方式中,所述屏障组合物包含交联的聚乙二醇和甲基化胶原蛋白,例如ct
‑
3。在某些实施方式中,所述屏障组合物对细胞无毒性。
50.在某些实施方式中,所述屏障组合物包含氰基丙烯酸酯或基于氰基丙烯酸酯的胶粘剂。基于氰基丙烯酸酯的胶粘剂的实例包括但不限于(ethicon)、(kimberly clark)、(adhezion)、(aesculap)、actabond
tm
(bergen)和(covidien)。氰基丙烯酸酯可以在水或湿气存在下粘合到软骨下骨骼。氰基丙烯酸酯可以具有各种不同的链长,其能够影响结合程度和生物可降解性。在各种不同实施方式中,所述屏障组合物可以快速施加。在各种不同实施方式中,所述氰基丙烯酸酯或基于氰基丙烯酸酯的胶粘剂允许所述屏障组合物抵抗感染。
51.在某些实施方式中,所述屏障组合物包含聚氨酯或基于聚氨酯的胶粘剂。基于聚氨酯的胶粘剂的实例包括但不限于(cohera)。在某些实施方式中,例如通过用异佛尔酮二异氰酸酯修饰蓖麻油或通过将聚己内酯二醇与二异氰酸己二酯反应,使所述聚氨酯和基于聚氨酯的胶粘剂具有增强的生物可降解性。所述聚氨酯可以基于聚己内酯二醇。
52.在某些实施方式中,所述屏障组合物包含聚(亚甲基丙二酸酯)或基于聚(亚甲基丙二酸酯)的胶粘剂。基于聚(亚甲基丙二酸酯)的胶粘剂的实例包括但不限于(optmed)。可以将所述屏障组合物粘贴在软骨下骨骼上或使用涂药器施加到软骨下骨骼。所述包含聚(亚甲基丙二酸酯)或基于聚(亚甲基丙二酸酯)的胶粘剂的屏障组合物在所述胶粘剂凝固后可能具有快速的干燥时间。
53.在某些实施方式中,所述屏障组合物包含衍生的聚乙烯醇或基于衍生的聚乙烯醇的材料。基于衍生的聚乙烯醇的材料的实例是(pulmonx)。所述衍生的聚乙烯
醇可以例如通过添加水配制成水凝胶。此类基于衍生的聚乙烯醇的水凝胶可以具有与透明软骨相似的性质,使得所述屏障组合物的施加可以帮助减轻疼痛和改善关节功能。
54.在某些实施方式中,所述屏障组合物包含丙烯酸或基于丙烯酸的材料。
55.在某些实施方式中,所述屏障组合物包含纤维蛋白或基于纤维蛋白的密封剂。基于纤维蛋白的密封剂的实例包括但不限于(baxter)和(ethicon)。所述屏障组合物可以在两种分开的组合物例如基于纤维蛋白原的组合物和基于凝血酶的组合物的混合后形成,其中纤维蛋白在混合时形成。可以利用涂药器或具有两个或更多个仓室的注射器来促进混合和施加。基于纤维蛋白的密封剂与其他类型的密封剂相比可以具有低毒性。基于纤维蛋白的密封剂与其他类型的密封剂相比可以具有更高的可生物降解性和生物相容性。在各种不同实施方式中,对所述基于纤维蛋白的密封剂进行灭菌以除去病毒和其他病原体。在各种不同实施方式中,可以将所述包含纤维蛋白或基于纤维蛋白的密封剂的屏障组合物粘贴或喷涂在暴露的软骨下骨骼上。
56.在某些实施方式中,所述屏障组合物包含明胶和凝血酶或明胶与凝血酶的混合物。所述屏障组合物还可以包含纤维蛋白。这些屏障组合物的实例包括但不限于(ethicon)和(baxter)。所述屏障组合物可以在两种分开的组合物例如包含可流动的明胶和纤维蛋白原的组合物和包含凝血酶的组合物的混合后形成。可以利用涂药器或具有两个或更多个仓室的注射器来促进混合和施加。在某些实施方式中,90%的基于纤维蛋白的密封剂在8周内降解。在各种不同实施方式中,对所述基于纤维蛋白的密封剂进行灭菌以除去病毒和其他病原体。在各种不同实施方式中,可以将所述屏障组合物粘贴或喷涂在暴露的软骨下骨骼上。
57.在某些实施方式中,所述屏障组合物包含白蛋白和一种或多种化学交联剂。所述屏障组合物可以在两种分开的组合物例如包含白蛋白的组合物和包含化学交联剂例如戊二醛的组合物的混合后形成。可以利用涂药器或具有两个或更多个仓室的注射器来促进混合和施加。这些屏障组合物的实例包括但不限于(cryolife)、progel
tm
(neomend)和(mallinckrodt pharma)。
58.在各种不同实施方式中,所述屏障组合物包含在下述文献中的任一者中描述的聚合物:美国专利号6,312,725和6,624,245;wallace,d.g.等,j.biomed.mater.res.,2001,58:545
‑
555;hill,a.等,j.biomed.mater.res.,2001,58:308
‑
312;和wise,p.e.等,the american surgeon,68:553
‑
562(2002),所述文献全都通过参考并入本文。例如,所述ct
‑
3聚合物被描述在美国专利号6,312,725中。
59.在某些实施方式中,所述屏障组合物包含带有邻苯二酚侧链的聚苯乙烯,例如在美国专利公布号2009/0036611中所描述的,其整体通过参考并入本文。
60.在某些实施方式中,所述屏障组合物包含基于聚酯的密封剂或聚酯。基于聚酯的密封剂的实例是聚(甘油癸二酸酯丙烯酸酯),其描述在mahdavi等,proc.natl.acad.sci.usa,2008,vol.105,p.2307中。为了增强附着性,可以如mahdavi等人所描述的将聚(甘油
‑
共
‑
癸二酸酯丙烯酸酯)模压成基于在壁虎脚上发现的粘附性表面的图案。
61.在某些实施方式中,所述屏障组合物包含例如在美国专利公布号2016/0206300中
所描述的沙堡蠕虫胶。沙堡蠕虫(沙堡虫(phragmatopoma californica))可以合成聚合的胶粘性液体,其在几小时内固化形成胶粘剂。所述沙堡蠕虫胶可以包含多酚类蛋白。
62.在某些实施方式中,所述屏障组合物包含在美国专利号7,964,207中描述的kryptonite
tm
骨骼基质产品,所述专利整体通过参考并入本文。
63.在某些实施方式中,所述屏障组合物包含由包含明胶和氧化淀粉的凝胶制备而成的聚合物,所述凝胶通过将明胶和氧化淀粉的水性溶液混合来形成。所述凝胶可以通过淀粉分子上的醛基与组织的蛋白质上的氨基的反应粘合到组织。在某些实施方式中,胶粘剂粘合强度为约100n/m。在某些实施方式中,弹性模量为约8x106pa。所述胶凝的密封剂被切割明胶的肽键和淀粉的糖苷键的酶降解。在某些实施方式中,90%的所述屏障组合物在14年内降解。
64.在某些实施方式中,所述屏障组合物包含由聚乙二醇与聚丙交酯或聚乙交酯的共聚物制成、还含有丙烯酸酯侧链、并且在某些活化分子存在下被光胶凝的聚合物。
65.在某些实施方式中,所述屏障组合物包含含有水溶性聚合区的聚合物。示例性的聚合物包括聚醚例如聚亚烷基氧化物例如聚乙二醇(“peg”)、聚氧化乙烯(“peo”)、聚氧化乙烯
‑
共
‑
聚氧化丙烯(“ppo”)、共聚氧化乙烯嵌段或随机共聚物,以及聚乙烯醇(“pva”)、聚(乙烯吡咯烷酮)(“pvp”)、聚氨基酸、多糖例如葡聚糖、壳聚糖、藻酸盐、羧甲基纤维素、氧化纤维素、羟乙基纤维素和/或羟甲基纤维素、透明质酸和蛋白质例如白蛋白、胶原蛋白、酪蛋白和明胶。所述大分子单体的水溶性区(例如peg)可以具有约3,500道尔顿至约40,000道尔顿(例如约3,500道尔顿至约35,000道尔顿或约3,500道尔顿至约30,000道尔顿或约3,500道尔顿至约25,000道尔顿)的平均分子量。在某些实施方式中,所述peg具有约3,500道尔顿至约20,000道尔顿(例如约3,500至约15,000道尔顿或约3,500道尔顿至约10,000道尔顿或约3,500道尔顿至约5,000道尔顿)的平均分子量。例如,所述peg可以具有约35,000道尔顿或约25,000道尔顿的平均分子量。在某些实施方式中,所述peg可以具有约3,500道尔顿至约40,000道尔顿的平均分子量。例如,所述peg可以具有约25,000道尔顿的平均分子量。在其他实施方式中,所述peg可以具有约35,000道尔顿的平均分子量。
66.在某些实施方式中,所述屏障组合物包含基于peg的材料,例如duraseal
tm
(covidien)、(cohesion technologies)和advaseal
tm
(ethicon)。包含peg的屏障组合物和包含基于peg的材料的屏障组合物可以具有高的粘附强度、与软骨下骨骼的生物相容性和柔性。
67.所述屏障组合物可以包含聚阳离子多胺和至少一种聚阴离子,其中所述至少一种可生物降解的聚阳离子多胺包含改性明胶,例如在整体通过参考并入本文的美国专利号8,283,384中所描述的。在某些实施方式中,所述明胶用乙二胺改性。在某些实施方式中,所述聚阴离子是聚磷酸盐化合物。
68.所述屏障组合物可以包含基于聚(酯脲)(peu)的胶粘剂,其包含具有一个或多个包含磷酸酯基团的侧链的peu聚合物骨架和包含二甲金属盐的交联剂,例如在整体通过参考并入本文的国际专利公布号wo2017/189534中所描述的。在某些实施方式中,所述二价金属盐包含钙盐、镁盐、锶盐、钡盐、锌盐或钙、镁、锶、钡和锌的任何组合。
69.在各种不同实施方式中,所述屏障组合物包含硫酸软骨素。所述硫酸软骨素可以被修饰以包括官能团例如甲基丙烯酸酯基团和醛基。所述硫酸软骨素可以例如通过使用光
引发剂的uv交联来交联,以形成水凝胶。
70.在各种不同实施方式中,所述屏障组合物包含多种不同聚合物、密封剂和/或胶粘剂。所述屏障组合物中存在的每种聚合物、密封剂或胶粘剂的性质可以补偿存在的其他聚合物、密封剂或胶粘剂的优点和缺点。例如,所述屏障组合物可以用两种聚合物配制,其中一种聚合物与另一种聚合物相比具有更高的降解和生物再吸收速率但具有更低的粘附强度。这些屏障组合物可以具有可接受的降解、生物再吸收和粘附强度。
71.在各种不同实施方式中,所述屏障组合物可以为水凝胶的形式。所述水凝胶可以具有足够的厚度,使得所述屏障组合物有效地阻断细胞、血液、碎片和流体从软骨下空间迁移。示例性的水凝胶及其组分被描述在整体通过参考并入本文的美国专利号7,009,034中。水凝胶可以通过用壳聚糖交联peg来形成。另一种示例性的水凝胶可以通过在树枝块(dendron)的硫醇残基与peg大分子单体之间形成硫酯键来合成。
72.在某些实施方式中,所述屏障组合物包含氧化的多糖例如葡聚糖和/或壳聚糖。葡聚糖是一种具有一些支链结构的复杂多糖,并且与壳聚糖不同,不具有反应性氨基。氧化的葡聚糖与壳聚糖盐酸盐反应,形成可以附着到组织的凝胶。氧化的多糖可以与各种不同的材料交联或混合在一起。示例性的源自于氧化葡聚糖的密封剂描述在下述文献中:balakrishnan等,acta biomater.2017,vol 53,p.343;lisman等,j.biomater.appl.2014,vol.28,p 1386;araki等,j.torac.cardiovasc surg.2007,v.134,p.1241。示例性的源自于壳聚糖的密封剂描述在下述文献中:hoque等,mol.pharm.2017,vol.14,p.1218;nie等,carbohydr.polym.2013,vol 96,p.342;medina等,otolaryngol.head neck surg.2012,vol.147,p.357。源自于硫酸软骨素的密封剂的实例被描述在elisseeff等,mil.med.2014,vol.179,p.686中。
73.在各种不同实施方式中,所述屏障组合物包含调节粘度的组分。这些组分可以包括例如糖胺聚糖(例如透明质酸)、羧甲基纤维素(cmc)、二乙二醇二甲醚(“diglyme”)、二甲基甲酰胺(“dmf”)、琥珀酸二甲酯、戊二酸二甲酯、己二酸二甲酯、葡聚糖、硫酸葡聚糖、聚乙烯吡咯烷酮(pvp)、其组合等。可用于调节本公开的组合物的粘度的增稠剂包括聚氰基丙烯酸酯、聚乳酸、聚乙醇酸、乳酸
‑
乙醇酸共聚物、聚
‑3‑
羟基丁酸、聚原酸酯、聚酸酐、果胶、其组合等。
74.在各种不同实施方式中,所述屏障组合物包含稳定剂。适合的稳定剂可以包括防止过早聚合的稳定剂,例如醌、对苯二酚、受阻酚、对苯二酚单甲醚、邻苯二酚、连苯三酚、苯醌、2
‑
羟基苯醌、对甲氧基苯酚、叔丁基邻苯二酚、丁基化羟基苯甲醚、丁基化羟基甲苯、叔丁基对苯二酚、其组合等。适合的稳定剂还可以包括酸酐、甲硅烷基酯、磺酸内酯(例如α
‑
氯
‑
α
‑
羟基
‑
邻甲苯磺酸
‑
γ
‑
磺酸内酯)、二氧化硫、硫酸、磺酸、亚硫酸、内酯、三氟化硼、有机酸、烷基硫酸酯、烷基亚硫酸酯、3
‑
环丁砜、烷基砜、烷基亚砜、硫醇、烷基硫化物、其组合等。在某些实施方式中,酸酐例如马来酸酐、癸二酸酐和/或壬二酸酐可以用作稳定剂。在其他实施方式中,抗氧化剂例如维生素e、维生素k1、肉桂酸和/或黄烷酮可以用作稳定剂。
75.在各种不同实施方式中,所述稳定剂以所述屏障组合物的约0.01至约10重量%的量存在。在某些实施方式中,所述稳定剂以所述屏障组合物的约0.1至约2重量%的量存在。
76.在某些实施方式中,可以向所述屏障组合物添加酶以提高其降解速率。适合的酶包括例如肽水解酶例如弹性蛋白酶、组织蛋白酶g、组织蛋白酶e、组织蛋白酶b、组织蛋白酶
h、组织蛋白酶l、胰蛋白酶、胃蛋白酶、胰凝乳蛋白酶、γ
‑
谷氨酰转移酶(γ
‑
gtp)等;糖链水解酶例如磷酸化酶、神经氨酸酶、葡聚糖酶、淀粉酶、溶菌酶、寡糖酶等;寡核苷酸水解酶例如碱性磷酸酶、核糖核酸内切酶、脱氧核糖核酸内切酶等。在某些实施方式中,在添加酶的情况下,所述酶可以被包含在脂质体或微球中以控制其释放速率,从而控制所述屏障组合物的降解速率。
77.在各种不同实施方式中,所述屏障组合物还包含1型胶原蛋白。不希望受到理论限制,所述1型胶原蛋白可以允许细胞在所述屏障组合物的表面上迁移并刺激来自于所述软骨下骨骼的任何血液的凝结。
78.在各种不同实施方式中,所述屏障组合物为水合形式。
79.在某些实施方式中,所述屏障组合物可以允许所述基质植入物在植入后牢固保留在胶原蛋白病变部位或缺损中。不需要缝合所述基质植入物。
80.所述基质系统可以是无细胞基质。所述无细胞基质可以是已被去细胞化的组织,使得从结构性细胞外基质中去除了核和细胞组分。所述无细胞基质可以从组织、包括器官或分离的器官部分制备。示例性的组织包括心脏瓣膜、小肠粘膜下层、真皮、羊膜、膀胱、网膜、心包膜、韧带、血管等。在一个实施方式中,所述组织包括但不限于网膜和真皮。在另一个实施方式中,所述组织是真皮。所述组织可以从各种不同的哺乳动物来源获得,包括但不限于人、山羊、猪、牛、羊、马等。所述组织可以通过常规技术去细胞化,所述常规技术包括诸如组织保存、去细胞化、清洗、去污染和储存的步骤。
81.所述无细胞基质层可以通过将所述无细胞基质拆分成厚度通常为约50微米至约200微米的薄片来获得。
82.所述基质还可以包含至少一种生长因子,所述生长因子可以是上皮生长因子(egf)、血管内皮生长因子(vegf)、转化生长因子
‑
β(tgf
‑
β)、骨形态发生蛋白(bmp)、生长分化因子、抗背侧化形态发生蛋白1(admp
‑
1)、碱性成纤维细胞生长因子(bfgf)、酸性成纤维细胞生长因子(afgf)、刺猬蛋白、胰岛素样生长因子、血小板衍生生长因子(pdgf)、白介素(il)、集落刺激因子(csf)和/或激活素。另外,这些实施方式的基质还可以包含胶原蛋白。
83.在某些实施方式中,可以将所述基质紧固到所述软骨下骨骼。紧固的实例包括但不限于钉书钉、刺、别针、螺钉、缝线、胶水或大头钉。在其他方面,假体可以是假体板。
84.在某些实施方式中,所述基质还包含至少一种治疗剂。在各种不同实施方式中,治疗剂可以是但不限于抗感染剂、止痛药、镇痛剂或抗炎剂和免疫抑制剂。
85.在某些实施方式中,所述抗感染剂是抗生素,例如庆大霉素、地贝卡星、卡内多霉素、利维霉素、妥布霉素、阿米卡星、弗氏霉素、西索米星、盐酸四环素、盐酸土霉素、罗利环素、盐酸多西环素、氨苄青霉素、哌拉西林、羟基噻吩青霉素、头孢噻吩、头孢噻啶、头孢替安、头孢磺啶、头孢甲肟、头孢美唑、头孢唑啉、头孢噻肟、头孢哌酮、头孢唑肟、莫西内酰胺、拉氧头孢、噻烯霉素、磺胺星霉素、氨曲南或其组合。
86.在某些实施方式中,所述止痛药或镇痛剂是吗啡、非甾类抗炎(nsaid)药、羟考酮、吗啡、芬太尼、氢可酮、naproxyphene、可待因、对乙酰氨基酚、苯佐卡因、利多卡因、普鲁卡因、布比卡因、罗哌卡因、甲哌卡因、氯普鲁卡因、丁卡因、可卡因、依替卡因、丙胺卡因、普鲁卡因、可乐定、甲苯噻嗪、美托咪定、右美托咪定或vr1拮抗剂。
87.在某些实施方式中,所述屏障组合物具有20
‑
400gf/cm2范围内的胶粘强度。在某
些实施方式中,所述屏障组合物具有20
‑
100gf/cm2、40
‑
120gf/cm2、60
‑
150gf/cm2、80
‑
200gf/cm2、100
‑
300gf/cm2、200
‑
400gf/cm2、20
‑
40gf/cm2、30
‑
50gf/cm2、40
‑
60gf/cm2、50
‑
70gf/cm2、60
‑
80gf/cm2、70
‑
90gf/cm2、80
‑
100gf/cm2、90
‑
110gf/cm2、100
‑
120gf/cm2、110
‑
130gf/cm2、120
‑
150gf/cm2、140
‑
170gf/cm2、160
‑
200gf/cm2、180
‑
220gf/cm2、200
‑
240gf/cm2、220
‑
260gf/cm2、240
‑
280gf/cm2、260
‑
300gf/cm2、280
‑
320gf/cm2、300
‑
350gf/cm2、320
‑
370gf/cm2或350
‑
400gf/cm2范围内的胶粘强度。
88.在各种不同实施方式中,可以将所述屏障组合物和基质中的一者或两者注射或植入到软骨缺损的部位中。在各种不同配置中,需要组织生长的部位可以包括但不限于真皮、转轴肌腱、跟腱、韧带例如前交叉韧带(acl)、后交叉韧带(pcl)、内侧副韧带、外侧副韧带或牙周韧带、括约肌例如肛门括约肌、尿道括约肌、食道括约肌或胃窦括约肌、成疝组织例如腹疝、腹膜后疝、膈疝、上腹疝、股疝、切口疝、腹股沟疝、椎间盘突出、利特雷疝、闭孔疝、灯笼裤状疝、会阴疝、腹膜前疝、里希特氏疝、坐骨疝、滑动疝、半月线疝或脐疝、椎间盘髓核、椎间盘纤维环、骨膜组织、神经组织例如中枢神经系统组织(包括脊髓组织)和脱髓鞘神经组织、神经隧道例如穿越骨组织的神经隧道、二尖瓣、三尖瓣、主动脉瓣、肺动脉瓣、包含支架的血管组织、狭窄的心血管组织、肋软骨、半月板软骨、会厌软骨、喉头软骨例如杓状软骨、环状软骨、楔状软骨和小角软骨、外耳软骨或咽鼓管软骨。
实施例
89.本发明也通过下述实施例进行了描述和演示。然而,这些实施例和本说明书中别处的其他实施例的使用仅仅是说明性的,并且不以任何方式限制本发明或任何示例的条款的范围和含义。同样,本发明不限于本文中描述的任何特定优选实施方式。事实上,对于本领域技术人员来说,在阅读了本说明书后,对本发明的许多修改和变动可能是显而易见的,并且这些变动可以在不脱离本发明的精神或范围的情况下做出。因此,本发明只受随附的权利要求的条款以及那些权利要求所赋予的等同物的全部范围的限制。
90.实施例1
91.将猪分成至少两组,其中存在至少一个对照组。每个测试组被施加屏障组合物,而对照组不施加屏障组合物。在所有组中,在膝关节的股骨内侧髁的承重区中产生软骨缺损。
92.在每个测试组中,将屏障组合物施加到软骨下骨骼上。可以产生多个测试组,以测试各种不同的屏障组合物。在所有组中,在施加任何屏障组合物后施加相同的基质。在所有测试组和对照组中,与基质和基质上方的任何顶部聚合物屏障的施加相关的条件应该是一致的。
93.在一个月和另外的时间段时进行测试,以确定屏障组合物是否阻止了软骨下组分例如细胞和流体迁移到软骨病变部位中。这种测试可以包括组织学分析和纤维软骨形成程度的测定。
94.可以进行另外的测试,例如炎症的评估、组织学分级和测量手术后动物移动能力改善的速率和程度。
95.然后将提供了最佳的软骨下组分迁移的阻止、最少的炎症和最高的透明软骨与纤维软骨的相对形成的屏障组合物进行进一步测试,以在临床中应用于人类患者和动物患者。
96.实施例2
97.用于在猪中的测试的支架如下所述来制备。将蜂巢状多孔胶原蛋白海绵(直径5mm且厚度1mm,koken,tokyo,japan)浸泡在25μl冷0.3%中和胶原蛋白溶液(vitrogen,cohesion tech,palo alto,ca)中,然后在37℃温育1小时。所述中和胶原蛋白溶液固化,形成由海绵内的胶原蛋白凝胶构成的无细胞支架。
98.用胶粘剂和缝合线植入的工程化细胞构建物如下制备:从猪的关节软骨收获活检样品,将所述活检样品切碎,然后将它在溶解在含有100μg/ml青霉素和100单位/ml链霉素(p/s,invitrogen)的ham’s f
‑
12(f
‑
12,invitrogen)中的1.5mg/ml胶原酶(cls 1,worthington,freehold,nj)中,在旋转器上在37℃下消化18小时。使用细胞筛(70μm筛孔,bd biosciences,franklin lakes,nj)除去未消化的组织。将分离的猪关节软骨细胞(pac)通过以1000rpm离心10分钟用pbs清洗两次。使用血细胞计数器和锥虫蓝排除法对活细胞和死细胞进行计数。每个活检样品的细胞存活率高于95%。
99.将pac接种到单层培养皿(直径100mm),并在增补有10%胎牛血清(fbs,invitrogen)和p/s的dmem/f
‑
12中,在37℃、空气中的5%co2的条件下温育5天。在将所述pac接种到胶原蛋白凝胶/海绵支架中之前,使用0.05%胰蛋白酶
‑
edta(invitrogen)从培养皿收获pac。将0.3%的来自于猪皮的经胃蛋白酶消化的酸溶性胶原蛋白(cohesion,palo alto,ca)溶液用1/10体积的10x pbs和0.1n naoh中和。将悬浮在25μl这种中和胶原蛋白溶液中的300,000个pac置于特氟龙制成的培养皿(saint
‑
gobain performance plastics,courbevoie,france)上,以便凭借高的流体表面张力在所需区域内维持细胞悬浮。将由蜂巢状孔眼构成的圆形胶原蛋白海绵(直径5mm且厚度1.5mm,koken,tokyo,japan)置于所述细胞悬液上并允许其吸收所述溶液。将这些细胞构建物在37℃温育1小时,以允许胶原蛋白溶液固化成凝胶。然后向培养皿添加培养基。
100.在所述培养基中温育12小时后,将所述细胞构建物转移到附连到生物反应器的耐压培养箱(tep
‑
1,purpose,shizuoka,japan),并在0
‑
0.5mpa、0.5hz的循环静水压(hp)和0.05ml/min的培养基更新速率、37℃、空气中的5%co2的条件下温育7天。然后,将所述细胞构建物转移到常规的12孔培养板(每个孔含有2ml培养基中的一个细胞构建物),并在大气压、37℃和空气中的5%co2的条件下继续温育14天。每周两次更换培养基。在第21天收获用于植入的细胞构建物、包括代用品。所述代用品构建物的细胞存活率和细胞密度通过组织学进行评估。
101.实施例3
102.将5种不同的工程化细胞构建物植入到猪中并比较它们的性能。所述5种构建物是a)空白缺损对照(“空白”);b)用胶粘剂和缝合线植入的无细胞支架对照(“支架”);c)用胶粘剂和缝合线植入的工程化细胞构建物(“细胞构建物”);d)仅用胶粘剂植入的工程化细胞构建物(“胶粘的细胞构建物”);和e)仅用缝合线植入到软骨下骨骼上的工程化细胞构建物(“缝合的细胞构建物”)。
103.在猪中进行了两轮手术。用于动物研究的方案得到charles river laboratories的动物护理和使用管理委员会(worcester,ma)批准。在第一次手术之前,使16只阉割过的12至15月龄、体重为30至45kg的雄性猪(micro
‑
yucatan,charles river laboratories)适应环境超过一周。使用0.04mg/kg硫酸阿托品(patterson,devens,ma)、0.55mg/kg酒石酸布
托啡诺(patterson)、1.5mg/kg甲苯噻嗪(vedco,st.joseph,mo)和20mg/kg盐酸氯胺酮(vedco)的肌肉内注射引起动物麻醉,并使用异氟烷(patterson)吸入麻醉进行维持。将右漆关节在前外侧打开并将髌骨向内脱臼,以暴露出滑车和内侧髁。
104.在第一轮手术期间,从右膝的非承重部位收集软骨块用于产生细胞构建物,并在承重部位处产生两个全厚度软骨缺损。某些缺损被留空(以充当空白),其他缺损植入有无细胞支架(以充当支架)。在第二轮手术期间,在从相同动物收集软骨后4周将所述工程化细胞构建物植入到左膝承重部位处手术产生的缺损中。
105.在猪中,8个膝盖各自在其中产生两个空白,8个膝盖各自在其中植入有两个支架,8个膝盖各自在其中植入有两个细胞构建物,4个膝盖各自在其中植入有两个胶粘的细胞构建物,并且4个膝盖各自在其中植入有两个缝合的细胞构建物。在空白、支架和细胞构建物植入的每次手术后2周时,进行关节镜检查以评估关节间隙、缺损和植入物。在工程化细胞构建物植入后6个月(或用于空白缺损产生和无细胞支架植入的活检后7个月时),将动物安乐死,用于治疗部位的组织学评估。
106.在手术过程中,从滑车脊收获几块软骨组织(活检样品)。获得大约40mg活检样品,并将其保持在含有p/s的无ca
2+
且无mg
2+
的dulbecco磷酸盐缓冲盐水(dpbs;invitrogen,carlsbad,ca)中。
107.使用皮肤打孔器(5mm)、海狸刀片和刮匙在内侧和远端股骨踝的承重部位处产生两个直径为5mm的全厚度缺损,同时小心地避免损伤软骨下骨骼。将四只动物指定为空白对照,将四只动物指定为无细胞支架对照组。
108.为了植入细胞构建物,将左膝关节在前外侧打开并将髌骨向内脱臼,以暴露出股骨内侧髁。使用与用于空白缺损和无细胞支架对照相同的方法,在髁上产生两个软骨缺损(直径5mm)。将所述细胞构建物放置在所述缺损中,使用四条可吸收和两条不可吸收的彩色缝合线缝合每个构建物,并用胶粘剂覆盖构建物(ct
‑
3)。将髌骨还原并用可吸收缝合线(0pds
‑
ii)分层封闭伤口。然后允许动物自由笼中活动。
109.对于胶粘的细胞构建物植入来说,将所述细胞构建物放置在涂布有胶粘剂的缺损中,并只用胶粘剂覆盖所述细胞构建物。将每个构建物用两条不可吸收的彩色缝合线缝合,用于关节镜确认。将缝合的细胞构建物放置在没有胶粘剂的缺损中,并将每个构建物用四条可吸收和两条不可吸收的彩色缝合线缝合。
110.在无细胞支架对照组中,在动物膝盖的右侧中植入两个无细胞支架。简单来说,将无细胞支架植入到具有基于聚乙二醇(peg)/胶原蛋白的组织胶粘剂(ct
‑
3,angiotech,vancouver,canada)的缺损中,并将每个支架用四条可吸收的(8
‑
0 vicryl,ethicon,somerville,ny)和在关节镜评估期间充当标志物的两条不可吸收的蓝色缝合线(8
‑
0 proline,ethicon)进行六针缝合。在缝合后,将植入物的表面用ct
‑
3胶粘剂覆盖。在将髌骨还原后,用可吸收缝合线(0 pds
‑
ii,聚二氧杂环己酮,ethicon)分层封闭伤口。
111.将所述动物单独饲养在笼中并允许自由笼中活动。每个笼子中的地板覆盖有厚橡胶板,以防止打滑和手术后对膝关节的额外创伤。
112.在涉及空白缺损对照的产生、支架的植入、细胞构建物的植入、胶粘的细胞构建物的植入和缝合的细胞构建物的植入的每次开膝手术后两周,通过关节镜评估软骨表面以确认构建物牢固地保留在缺损中。如果任何植入物没有保留在部位处,将所述组织学样品从
评估中移除。此外,观察到的缺损为半透明白色,在外观上与邻近软骨的表面一致。事实上,未发现没有彩色标记的缝合线的植入的无细胞构建物或工程化构建物,表明所述胶粘剂和构建物没有抑制来自于邻近组织的细胞迁移。
113.通过在工程化细胞构建物植入后6个月(组织活检和无细胞支架植入后7个月)时对细胞构建物、胶粘的细胞构建物和缝合的细胞构建物组进行宏观和组织学评估,分析了手术胶粘剂的有效性。使用的动物在尸检之前被安乐死。
114.在总体解剖发现的基础上对所述空白缺损对照、植入的无细胞支架和植入的工程化细胞构建物所在的关节表面进行评估:与周围的宿主软骨相比,缺损中的填充组织的目测特征、填充率、颜色和与宿主组织的表面整合。使用数字相机(coolpix e
‑
995,nikon usa,ny)记录宏观图像。然后将修复的软骨与软骨下骨骼和邻近软骨一起收获,在4%聚甲醛(jt baker,phillipsburg,nj)中固定,并在4℃下在轻柔旋转器上在pbs(ph 7.4)中溶解7天。然后将固定的组织在5%甲酸和柠檬酸钠溶液(sigma
‑
aldrich)中脱钙处理1至2周,并包埋在石蜡中。切出4
‑
μm厚的纵向连续切片,然后用苏木精和曙红(h&e)或番红o
‑
固绿进行染色。
115.此外,进行了使用ii型胶原蛋白抗体的免疫染色。对于免疫组织化学分析来说,将切片在二甲苯中脱石蜡化,并用分级乙醇和pbs重新水合。为了高效暴露出表位,将所述切片在700u/ml牛睾丸透明质酸酶(sigma)和2u/ml链霉蛋白酶xiv(sigma)中在37℃温育1小时。然后将切片在针对ii型胶原蛋白的多克隆抗体(southern biotech,birmingham,al)中温育。
116.组织学数据示出在图1中。“细胞构建物胶粘剂+缝合”和“细胞构建物单独的胶粘剂”组在手术期间具有胶粘剂屏障(ct
‑
3密封剂),而“细胞构建物单独的缝合”组在手术期间未施加密封剂。在“细胞构建物胶粘剂+缝合”和“细胞构建物单独的胶粘剂”组中,存在软骨下骨骼与所述植入物的清楚划分,并且健康的骨骼组织出现在植入物下方。在“细胞构建物单独的缝合”组中,与其他组相比存在所述缝合的细胞植入物在骨骼中显著更大的穿透。
117.然后使用由sellers等,j.bone joint surg.am.,1997,79(10):1452
‑
63开发的组织分级量表的改良版本对组织学发现进行评分。三位调查人员使用下述标准对纵向切片进行盲评:1)缺损的填充;2)与宿主邻近软骨的整合;3)使用番红o
‑
固绿的基质染色(异染性);4)软骨细胞形态;5)整个缺损中的体系结构;6)表面的体系结构;和7)穿透。细胞构建物组具有胶粘剂和缝合线,缝合的细胞构建物组只具有缝合线,胶粘的细胞构建物组只具有胶粘剂。评分示出在下面的表1中。
118.表1
[0119][0120]
关于表1中的与邻近软骨的整合,对再生组织与邻近软骨之间的缝隙数目或缺乏连续性进行计数和分类。与空白中的缝隙相比,与所述细胞构建物整合的再生组织具有显著更少的缝隙数目(p<0.05)。胶粘的构建物和缝合的构建物的整合在缝隙数目方面与所述细胞构建物相近(表1)。
[0121]
番红o
‑
固绿染色指示作为关节软骨的主要组分的硫酸化软骨基质的品质。与邻近软骨相比,所述支架和细胞构建物内的再生组织在数量上略低。所述胶粘的细胞构建物和缝合的细胞构建物的基质染色揭示出它们的硫酸化软骨基质在品质上与所述细胞构建物相近(表1)。
[0122]
对所述再生组织内的软骨细胞形态进行了分析,这是因为这个特征指示了细胞外基质的健康的非致密核、软骨细胞形状和品质。所述胶粘的细胞构建物和缝合的细胞构建物与所述细胞构建物的软骨细胞在形态上相似(表1)。
[0123]
表1中的“整个缺损中的体系结构”分类是对所述再生组织的密度的评估,所述再生组织有时具有看起来像空隙或裂缝的松散质构。所述胶粘的细胞构建物和缝合的细胞构建物与所述细胞构建物在再生组织的密度上相近。
[0124]
在表1中,“缺损处表面的体系结构”分类描述了所述再生组织的表面抵抗承重和关节负荷应力的能力。所述细胞构建物内的再生组织的大部分表面一致地覆盖有多层组织并延伸到邻近软骨的浅表过渡区。所述胶粘的细胞构建物和缝合的细胞构建物与所述细胞构建物的表面的体系结构在等级上相近(表1)。
[0125]
表1中的“穿透”分类描述了软骨下骨骼中的水肿形成,并且对于确定缺损的完全恢复来说是重要的。与所述细胞构建物和胶粘的细胞构建物相比,所述缝合的细胞构建物向软骨下骨骼的穿透显著更高(p<0.05,表1)。
[0126]
所述胶粘的细胞构建物和缝合的细胞构建物与所述细胞构建物中的ii型胶原蛋
白在强度上相近。
[0127]
实施例4
[0128]
在膝盖中具有软骨缺损、软骨损伤或软骨病变部位的人类患者经历手术。如果尚未存在软骨病变部位,这种病变部位可以通过从所述软骨缺损或软骨损伤的部位除去软骨来产生。
[0129]
将包含聚乙二醇的屏障组合物的第一层引入到所述病变部位中,并配置在所述病变部位的底部例如软骨下骨骼处。所述屏障组合物被配制成使得它在3至15分钟内从可流动液体或糊状物快速胶凝成承重的凝胶。允许所述屏障组合物凝固或固化,以便有效地防止软骨下细胞或外加组分例如血液携带的因子、细胞和细胞碎片等进入并阻断它们迁移到空腔中。
[0130]
对支持基质进行切割以匹配所述软骨病变部位的尺寸。然后将所述支持基质植入到所述软骨病变部位中。不进行缝合。在所述植入的支持基质上添加至少一层密封剂。然后将伤口缝合。
[0131]
所述患者从一开始每两周进行检查,以评估疼痛和移动能力的改善。
[0132]
***
[0133]
本发明的范围不受本文中描述的具体实施方式的限制。事实上,对于本领域技术人员来说,根据上述描述和附图,除了本文中描述的之外的本发明的各种不同修改将变得显而易见。这些修改打算落于随附的权利要求书的范围之内。还应该理解,所有的值都是近似值,并且出于描述的目的而提供。
[0134]
在整个本申请中引用了专利、专利申请、出版物、产品说明和方案流程,其公开内容为所有目的整体通过参考并入本文。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1