治疗或抑制亨廷顿病发作的方法
治疗或抑制亨廷顿病发作的方法
1.本申请要求2018年6月21日提交的第62/688,174号美国临时专利申请序列的权益,所述申请通过引用整体并入本文。
发明领域
2.本申请涉及治疗或抑制亨廷顿病发作的方法。
3.发明背景
4.亨廷顿病(hd)是致命的常染色体显性神经退行性病症,其特征是进行性行为、认知和运动功能障碍。hd是由亨廷顿蛋白(htt)基因的第一外显子的cag三核苷酸重复序列引起的,该三核苷酸重复序列编码聚谷氨酰胺扩展。其发病年龄和严重程度与这种重复扩展的长度成比例,其中cag长度超过35不可避免地会导致临床疾病。这与突变型htt(mhtt)的细胞内积累和聚集相关联,这导致神经元丢失。虽然hd病理变化主要通过纹状体中棘状神经元(msn)的进行性丧失和随之而来的纹状体萎缩来反映,但mri研究已表明,hd的特征还在于早期出现脱髓鞘和白质丢失,这可能在症状出现之前出现(tabrizi等人,“potential endpoints for clinical trials in premanifest and early huntington's disease in the track
‑
hd study:analysis of 24 month observational data,”the lancet neurology 11:42
‑
53(2012)类似地,在hd小鼠模型中的研究已揭示了早期髓鞘形成障碍(teo等人,“structural and molecular myelination deficits occur prior to neuronal loss in the yac128 and bachd models of huntington disease,”human molecular genetics 25:2621
‑
2632(2016)),伴有关键髓鞘生成基因(myelinogenic gene)myrf的缺陷(huang等人,“mutant huntingtin downregulates myelin regulatory factor
‑
mediated myelin gene expression and affects mature oligodendrocytes,”neuron 85:1212
‑
1226(2015);jin等人,“early white matter abnormalities,progressive brain pathology and motor deficits in a novel knock
‑
in mouse model of huntington's disease,”human molecular genetics 24:2508
‑
2527(2015))。总之,这些观察表明hd病理变化与白质丢失相关联,白质丢失进而可能反映了产生髓鞘的少突细胞的功能障碍。
5.然而,尽管这些数据表明hd中存在白质异常和髓鞘形成障碍,并且平行研究表明胶质替代可以改善hd转基因小鼠的症状(benraiss等人,“human glia can both induce and rescue aspects of phenotype in huntington disease,”nature communications 7:11758(2016)),但人hd中胶质病理变化的细胞和分子基础都尚未得到很好的探索。
6.本公开旨在克服现有技术中的这些和其它缺陷。
技术实现要素:
7.本公开的第一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用胶质细胞分化调控基因的一种或多种调节剂,所述胶质
细胞分化调控基因选自由以下组成的组:bmp2、lingo1、mag、nkx2
‑
2、nr2e1、ntrk3、olig2、serpine2、sirt2和tcf7l2,或由其编码的蛋白质。
8.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用与髓鞘形成相关联的基因的一种或多种调节剂,所述与髓鞘形成相关联的基因选自由以下组成的组:fa2h、gal3st1、mag、mbp、myrf、nfasc、olig2、omg、pllp、pou3f2、sirt2、slc8a3、tcf7l2、tf和ugt8,或由其编码的蛋白质。
9.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用少突细胞分化基因的一种或多种调节剂,所述少突细胞分化基因选自由以下组成的组:fa2h、gli3、lingo1、myrf、nkx2
‑
2、olig1、olig2、omg、sirt2、slc8a3、sox10和tcf7l2,或由其编码的蛋白质。
10.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用胶质生成调控基因的一种或多种调节剂,所述胶质生成调控基因选自由以下组成的组:bmp2、lingo1、mag、myc、nkx2
‑
2、nr2e1、ntrk3、olig2、serpine2、sirt2、sox10、tcf7l2、tf和zcchc24,或由其编码的蛋白质。
11.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用神经元包鞘(neuron ensheathment)基因的一种或多种调节剂,所述神经元包鞘基因选自由以下组成的组:fa2h,gal3st1、mag、mbp、myrf、nfasc、olig2、omg、pllp、pou3f2、sirt2、slc8a3、tcf7l2、tf和ugt8,或由其编码的蛋白质。
12.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用轴突导向基因的一种或多种调节剂,所述轴突导向基因选自由以下组成的组:alcam、bcl11b、dscam、foxd1、gas1、gli3、hoxa1、hoxa2、mnx1、nfasc、plxnc1、prkcq、ptpro、robo2、sema6b、unc5a、vax1和wnt7b或由其编码的蛋白质。
13.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用神经元投射导向基因的一种或多种调节剂,所述神经元投射导向基因选自由以下组成的组:alcam、bcl11b、dscam、foxd1、gas1、gli3、hoxa1、hoxa2、mnx1、nfasc、plxnc1、prkcq、ptpro、robo2、sema6b、unc5a、vax1和wnt7b,或由其编码的蛋白质。
14.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用轴突生成基因的一种或多种调节剂,所述轴突生成基因选自由以下组成的组:adgrb1、alcam、bcl11b、cacna1a、dscam、foxd1、gas1、gli3、hoxa1、hoxa2、lingo1、lrrc4c、mag、mbp、mnx1、nfasc、nr2e1、ntng1、ntrk3、omg、plxnc1、pou3f2、prkcq、ptpro、robo2、sema6b、slitrk2、slitrk3、snap91、unc5a、vax1和wnt7b,或由其编码
的蛋白质。
15.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用轴突发育基因的一种或多种调节剂,所述轴突发育基因选自由以下组成的组:adgrb1、alcam、bcl11b、cacna1a、dscam、foxd1、gas1、gli3、hoxa1、hoxa2、lingo1、lrrc4c、mag、mbp、mnx1、nefm、nfasc、nr2e1、ntng1、ntrk3、omg、plxnc1、pou3f2、prkcq、ptpro、robo2、rtn4rl2、sema6b、slitrk2、slitrk3、snap91、unc5a、vax1和wnt7b,或由其编码的蛋白质。
16.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用细胞投射形态发生基因的一种或多种调节剂,所述细胞投射形态发生基因选自由以下组成的组:adgrb1、alcam、bcl11b、cacna1a、camk2a、dscam、ehd3、foxd1、gas1、gli3、hoxa1、hoxa2、kank1、lingo1、lrrc4c、mag、mbp、mnx1、nedd4l、neurl1、nfasc、nr2e1、ntng1、ntrk3、omg、pcdh15、plxnc1、pou3f2、prkcq、ptpro、robo2、sema6b、sgk1、slitrk2、slitrk3、snap91、snx10、ugt8、unc5a、vax1和wnt7b,或由其编码的蛋白质。
17.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用突触结构或活性调控基因的一种或多种调节剂,所述突触结构或活性调控基因选自由以下组成的组:adgrb1、adgrl3、bcan、calb1、camk2a、fgf14、lrrtim1、ncdn、neto1、neurl1、nr2e1、ntrk3、ppfia3、robo2、serpine2、shisa7、six4、slc8a3、slitrk2、slitrk3和syndig1或由其编码的蛋白质。
18.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用突触信号传导途径基因的一种或多种调节剂,所述突触信号传导途径基因选自由以下组成的组:bcan、cacna1a、cacna1g、calb1、camk2a、chrna4、fgf12、fgf14、gria2、gria4、grid2、grik4、kcnd2、lrrtm1、mbp、mpz、ncdn、neto1、neurl1、nova1、nr2e1、p2rx7、pde7b、plcl1、ppfia3、rapgef4、rgs8、rit2、s1pr2、serpine2、shisa7、slc18a1、slc1a1、slc1a2、slc8a3、snap91、snph和syt6或由其编码的蛋白质。
19.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用突触基因的一种或多种调节剂,所述突触基因选自由以下组成的组:adgrb1、bcan、bcas1、cacna1a、calb1、camk2a、chrna4、cttnbp2、dscam、gria2、grid1、grid2、grik4、hcn2、kcnd2、lgi3、lrrc4c、lrrtm1、neto1、neurl1、ntm、p2rx7、pcdh15、pde4b、ppfia3、prima1、prkcq、ptpro、rapgef4、serpine2、shisa7、slc17a8、slc18a1、slc1a1、slc1a2、slc8a3、snap91、snph、syndig1和syt6,或由其编码的蛋白质。
20.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用单价无机阳离子转运基因的一种或多种调节剂,所述单
价无机阳离子转运基因选自由以下组成的组:abcc9、asic4、cacna1a、chrna4、cngb1、cntn1、dpp10、dpp6、fgf12、fgf14、hcn2、kcnd2、kcnj9、kcnq1、kcns3、nalcn、nedd4l、nkain4、p2rx7、ptger3、serpine2、sgk1、slc10a4、slc17a8、slc18a1、slc22a3、slc2a13、slc5a9、slc8a3和slc9a7,或由其编码的蛋白质。
21.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用神经元投射基因的一种或多种调节剂,所述神经元投射基因选自由以下组成的组:adgrl3、alcam、bcan、bcl11b、cacna1a、cacna1g、calb1、camk2a、chrna4、cttnbp2、dscam、gria2、gria4、grid2、grik4、hcn2、kcnd2、lgi3、lrrtm1、mag、mbp、myc、ncam2、ncdn、nefm、neurl1、nfasc、ntm、pde4b、pik3r1、ptger3、ptpro、rapgef4、rgs8、robo2、sgk1、sirt2、slc17a8、slc1a2、slc8a3、snap91、snph、syndig1和unc5a,或由其编码的蛋白质。
22.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用tcf7l2靶基因的一种或多种调节剂,所述tcf7l2靶基因自由以下组成的组:bmp4、ccnd1、ccnd2、dock10、dock9、dusp15、enpp4、epas1、ephb1、erbb3、evi2a、evi2b、fa2h、gjb1、hapln2、hspa2、id3、lgi3、mbp、mog、myc、myrf、nfasc、nkain1、nkx6
‑
2、olig2、plekhb1、plp1、ppp1r16b、rab33a、rasgef1b、rtkn、sirt2、slc1a2、sox10、st18、tmem125、tmem2、tppp、tspan15、ugt8和aatk,或由其编码的蛋白质。
23.本公开的另一方面涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,以及向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用参与nkx2.2
→
olig2
→
sox10
→
myrf调控级联的基因或由其编码的蛋白质的一种或多种调节剂。
24.本公开检查了表达mhtt的人胶质祖细胞(hgpc)的基因表达模式是否可以反映细胞自主的分子病理变化,如果可以,则是否可以预测hd的白质疾病。双潜能少突细胞
‑
星形细胞hgpc最初是从源自亨廷顿蛋白突变型胚胎或其同胞对照的人胚胎干细胞(hesc)中产生的。然后使用荧光激活细胞分选术(facs),基于这些细胞的gpc选择性cd140a的表达来分离这些细胞(sim等人,“cd140a identifies a population of highly myelinogenic,migration
‑
competent and efficiently engrafting human oligodendrocyte progenitor cells,”nat.biotechnol.29:934
‑
941(2011);wang等人,“human ipsc
‑
derived oligodendrocyte progenitor cells can myelinate and rescue a mouse model of congenital hypomyelination,”cell stem cell 12:252
‑
264(2013),所述文献据此通过引用整体并入本文),随后进行全转录组rna测序(rna
‑
seq)分析以评估它们的基因表达中依赖于mhtt的变化。我们发现,在从源自三种不同hd胚胎的hesc产生的hgpc中,与星形胶质(astroglial)和少突胶质(oligodendroglial)分化以及与下游髓鞘生物合成相关联的一组连贯的关键转录因子相对于对照作为mhtt表达的函数而显著下调。因此,当hd hesc来源的hgpc被移植到新生的髓鞘缺乏(myelin
‑
deficient)的免疫缺乏的颤抖(shiverer)小鼠(mbp
shi/shi
)中时,所得到的胶质嵌合体的髓鞘形成比移植有源自正常对照hesc的hgpc的同窝出生对照更慢且更不完全。另外,相对于与正常同胞hgpc嵌合的小鼠,用
hd hgpc建立的嵌合体表现出星形细胞形态发生的显著延迟和破坏。总之,这些数据表明,人hd中的白质衰竭和髓鞘形成减少可能是表达mhtt的hgpc的终末胶质分化中的细胞自主缺陷的结果,而不是继发于神经元丢失,这种缺陷的发生可能是hd的发病机制和神经学表现的核心。
25.附图简述
26.图1a
‑
1g显示hd hesc衍生的hgpc表现出巨大的mhtt依赖性的基因表达变化。图1a示出了基于rv26,000转录物的表达的主成分分析(pca)。表达数据以百万分之转录物(tpm)示出,用后归一化(post
‑
normalization)来解释方差(risso等人,“normalization of rna
‑
seq data using factor analysis of control genes or samples,”nat.biotechnol.32:896
‑
902(2014),所述文献据此通过引用整体并入)。pca图示出了hd来源的人胶质祖细胞(hgpc)的独特转录组范围的表达特征(signature)。图1b是维恩图(venn diagram),其示出通过比较源自3个不同hd患者的hgpc与来自2个供体的汇集的对照hgpc获得的差异表达基因(deg)的列表的交集(绿色,下调;红色,上调;变化倍数[fc]>2.0,fdr 1%)。然后,通过与在患者hd20(genea20来源的)对比正常同胞ctr19(genea19)中发现的那些deg(fc>2.0,fdr1%)相交,过滤3名hd患者共享的deg列表;这一过滤步骤进一步增加了与mhtt相关联的deg的特异性。灰色突出显示的交集共同构成了所有hd系相对于它们的汇集的对照差异表达的整个基因集合。图1c示出基于图1b中突出显示的429个deg的tpm值的表达热图,其示出了根据疾病状态的hgpc的聚类。树形图示出了基于欧几里德距离的分层聚类,所述欧几里德距离是从来自三个hd
‑
esc系(hd
‑
17、hd
‑
18和hd
‑
20)和两个匹配的对照系(ctr19和ctr02)的log2
‑
tpm值计算得出的。图1d示出了图1b中突出显示的429个交集deg的功能注释的网络表示(基因本体:生物过程和细胞组分,bonferroni校正的p<0.01)。基因是圆形节点,边缘颜色代表其失调方向(绿色,下调;红色,上调)。圆角矩形节点代表注释术语(term)。节点按程度划分大小,并由通过社区检测(community detection)鉴定的紧密互联模块(m1
‑
m3)着色。对于每个模块,列出了按重要性和富集倍数列出的前3个注释。标记选定的基因节点,其包括编码关键hgpc谱系转录因子和阶段调控蛋白的基因。图1e是在m1中鉴定的63个保守deg的表达热图((图1d)中紫色),其具有与胶质细胞分化和髓鞘形成有关的注释。图1f是在m2中鉴定的56个保守deg的表达热图((图1d)中的浅紫色),其具有与轴突导向和轴突生成有关的注释。图1g是在m3中鉴定的68个保守deg的表达热图(图1d中的黄色),其具有与对突触结构和突触信号传导的调控有关的注释。所有差异表达的(de)结果均为1%fdr且fc>2;基因本体(go)注释结果被bonferroni修正为p<0.01。
[0027]
图2a
‑
图2d示出了在来源于不同hd hesc与汇集的对照的hgpc之间差异表达的基因。图2a
‑
图2b示出了通过将每种经cd140a分选的hd来源的gpc系(hd17、hd18和hd20)与汇集的对照来源的gpc相比较而获得的差异表达基因(图2a,上调的基因;图2b,下调的基因)的基因集合交集图。hd gpc中的差异表达基因在1%fdr下且fc>2.00时是显著的。图2c
‑
图2d示出经cd44分选的hd来源的apc系(hd17、hd18和hd20)与对照来源的apc的比较(图2c,上调;图2d,下调)。在5%fdr下,hd apc中的差异表达基因是显著的。在这两种情况下,20对比19表示hd系hd20(genea20)与其同胞对照系ctr19(genea19)的比较。横条表示基因集合的总体大小,竖条表示基因集合交集的大小。竖条首先按交集中基因集合的数量排序,然后按交集的大小排序。这些点对应于构成每个交集的那些基因集合。
[0028]
图3a
‑
图3b显示功能注释揭示了与hd相关联的胶质分化、髓鞘形成和突触传递相关基因的转录的损伤。基因本体(go)功能注释是针对3个mhtt hgpc系中的429个相对于汇集的对照hgpc的差异表达基因(deg)执行的(参见图1b
‑
1c)。用toppcluster注释工具(kaimal等人,“toppcluster:a multiple gene list feature analyzer for comparative enrichment clustering and network
‑
based dissection of biological systems,”nucleic acids res.38:w96
‑
w102(2010),所述文献据此通过引用整体并入本文)鉴定了50个显著相关联的go注释术语(生物过程和细胞组分,bonferroni校正的p<0.01)。通过网络分析,这些go术语及其相关联的deg一起被分为三个功能上有关的模块(m1至m3,参见图1d)。对于每个go术语,给定注释的deg的数目和术语中发现的人蛋白质编码基因的总数目,期望值假设为恒定的比率。富集倍数是在该术语中发现的观察到的deg数目与预期数目的比率。在每个功能模块中,go术语首先按p值排序,然后按富集倍数排序。三个go术语,go:0007268(化学突触传递)、go:0098916(顺行跨突触信号传导)和go:0099537(跨突触信号传导),在m3模块中分别排第3至第5位。它们含有一组相同的37个相关联的deg,其包含在与在m3中排名第二的go:0099536(突触信号传导)相关联的38个deg内。为了减少冗余,图中省略了这三个go术语。图3a是示出每个功能模块的前5个go术语的条形图。图3b是表格,其列出了每个排名靠前的术语的计算值和相关联的deg。相关联的deg是根据它们与对照来源的hgpc相比在hd来源的hgpc中的失调方向来着色的(绿色,下调;红色,上调)。
[0029]
图4a
‑
图4c显示逐渐增加的cag长度与减少的少突胶质基因表达相关。图4a示出了基于tpm值的表达热图,所述tpm值是通过将源自三个不同的hd患者中的每一个hd患者的hgpc与来自两个不同供体的汇集的对照hgpc进行比较,从在deg的交集中发现的429个deg(1%fdr,fc>2.0)的原始计数计算出的。行边的颜色示出了该基因相对于汇集的对照在每个hd来源的hgpc系中的fc与该hd系中相应的cag重复数目(hd17=40x cag,hd18=46x cag,hd20=48x cag)之间的皮尔逊相关(pearson’s correlation)系数(r)。列出了参与胶质分化和髓鞘形成的编码转录因子和阶段调控的蛋白的选定基因。图4b示出了具有线性拟合线的组合散点图,该线性拟合线是通过将图4a中热图中示出的429个deg中的每一个的变化倍数针对于相应的hgpc系中的cag重复数目作回归而获得的。图4c是直方图,其示出针对3个hd系中的deg的fc与相应的cag长度之间的相关性的皮尔逊系数(r)的分布。对于429个基因中的255个(|皮尔逊r|>0.75),相关分析表明,fc的绝对量值随cag重复数目的增加而增加;这些基因中的228个显示出基因表达水平与cag重复数目呈负相关,较长的重复与胶质基因表达减少相关联。
[0030]
图5a
‑
图5d显示人和小鼠胶质表现出在作为cag重复长度的函数失调的基因上的重叠。这些hgpc基因与被发现随着hgpc中cag重复长度的增加而逐渐失调,且被注意到在小鼠脑组织中随着cag重复长度而失调的本体之间存在高度的重叠(langfelder等人,“integrated genomics and proteomics define huntingtin cag length
‑
dependent networks in mice,”nat.neurosci.19:623
‑
633(2016),其据此通过引用整体并入)。图5a示出了将从hd来源的经cd140分选的gpc和hd来源的经cd44分选的apc获得的差异表达基因(deg),与来自(langfelder等人,“integrated genomics and proteomics define huntingtin cag length
‑
dependent networks in mice,”nat.neurosci.19:623
‑
633(2016),其据此通过引用整体并入本文)的小鼠mhtt等位基因系列(图5a和图5b)和6个月的
q175异形(profiled)组织(图5c和图5d)的差异表达结果进行比较获得的代表性列表。图5a和图5c中的网络图示出了cd140和cd44 hd genea来源的deg集合(黄色节点)与来自langfelder等人,“integrated genomics and proteomics define huntingtin cag length
‑
dependent networks in mice,”nat.neurosci.19:623
‑
633(2016)(其据此通过引用整体并入本文)的deg集合(分析(灰色节点))之间的重要的成对集合交集(fisher精确检验,p<0.05)。节点的大小是根据每个节点的括号中指示的deg总数目确定的。hd genea集合中的deg数目是在id转换为小鼠直向同源基因后获得的。边缘厚度表示基因集合交集的显著性,计算为
‑
log10(fisher精确检验p值)。边缘颜色和标签显示成对集合交集中的基因数量。来自langfelder等人,integrated genomics and proteomics define huntingtin cag length
‑
dependent networks in mice,”nat.neurosci.19:623
‑
633(2016)(其据此通过引用整体并入)的deg集合中只有与这两个hd genea集合中的任一个具有显著重叠的deg集合被示出。图5b和图5d中的点图分别示出了针对图5a和图5c中的deg集合的基因本体(go):生物过程注释结果的比较。点的大小是根据基因相对于deg集合的比例来确定的。点的颜色代表了关联对go术语的重要性。示出了所有具有重要注释(bh校正的p<0.01)的deg集合。相较于等位基因系列deg在cd140 deg集合与6个月纹状体q175样品中的deg之间(p=1.10e
‑
06;150个基因),以及在cd140 deg集合与q175组织的6个月q175小脑deg之间(p=9.86e
‑
13;85个基因)观察到最显著的相交。这些交集包括胶质调节剂nkx2
‑
2、olig1和olig2,以及编码参与髓鞘形成、离子通道活性和突触传递的蛋白质的基因。总的来说,对hd genea cd140 deg和来自langfelder等人,“integrated genomics and proteomics define huntingtin cag length
‑
dependent networks in mice,”nat.neurosci.19:623
‑
633(2016)(其据此通过引用整体并入)的牵涉到包括胶质生成、髓鞘形成、轴突发育和离子通道活性在内的功能的脑源性deg观察到了许多类似的重要注释。
[0031]
图6a
‑
图6b显示与胶质细胞分化相关联的基因在表达mhtt的gpc中失调。通过taqman低密度阵列(tlda)rt
‑
qpcr评估如通过rna
‑
seq分析鉴定的hd来源的gpc中失调的选定基因的表达,并将其与对照gpc进行比较。将表达数据针对18s和gapdh内源性对照作归一化。示出了平均ddct值和标准误差范围,所述ddct值和标准误差范围是由3个汇集的hd gpc系(对于genea17系和genea20系而言n=3,对于genea18而言n=5,总共n=11)与2个汇集的对照gpc系(对于genea02而言n=6,对于genea19线而言n=3,总共n=9)对比计算得出的。通过配对t检验以及随后进行的benjamini
‑
hochberg(bh)多重检验校正来评估在hd和对照gpc中的表达差异(***p<0.01,**p<0.05,*p<0.1)。在这两个阵列上测定的基因以粗体突出显示。tlda数据的分析是在expressionsuite软件1.1(applied biosciences)中执行的。大部分被rna
‑
seq鉴定为在hd来源的gpc中失调的基因被tlda证实为确实如此。图6a示出编码关键gpc谱系转录因子和阶段调控的与髓鞘有关的蛋白的基因。示出了44个基因,该44个基因不包括mobp和mog,它们被发现具有高比例的不可靠反应。图6b示出了如通过ipa中上游调控因子分析所预测的tcf7l2的转录靶标。总共示出了42个基因,该42个基因不包括具有高比例的不可靠反应的基因。
[0032]
图7显示hd来源的hgpc表现出钾通道基因的显著失调。每个hd来源的hgpc系与汇集的对照hgpc的差异基因表达比较(fdr为5%,无变化倍数阈值)揭示在3个hd来源的系中,至少有2个系中有25个钾通道基因失调。ns=不显著。
[0033]
图8a
‑
8n显示用表达mhtt的人gpc嵌合的小鼠中的髓鞘形成受损。通过将hgpc新生期注射到颤抖x rag2宿主中来建立人胶质嵌合小鼠,在第8周、13周和18周将小鼠处死。图8a和图8d显示,到新生期植入后的第8周,对照hgpc(genea19)的髓鞘碱性蛋白(mbp)表达是明显的(图8a),而植入有hd来源的表达mhtt的hgpc(genea20)的小鼠在该点几乎未表现出或未表现出mbp免疫标记(图8d)。图8b和图8e显示,到13周,植入有对照hgpc的小鼠表现出强劲的髓鞘产生(图8b),而在匹配的hd来源的gpc的受者中仅发现分散的mbp表达岛(图8e)。图8c和图8f显示,相对于mhtt gpc嵌合小鼠(图8f),对照gpc来源的髓鞘形成到18周时越来越强劲(图8c)。图8g
‑
图8i显示,所植入的人gpc的密度在对照组与mhtt hgpc之间在评估的任何时间点均没有差异(图8g),但在表达mhtt的hgpc中,那些分化为转铁蛋白(tf)+少突细胞的hgpc的分数显著较低(图8h),导致在植入有mhtt hgpc的嵌合体中tf界定的少突细胞较少(图8i)。图8j
–
8l显示,与植入了对照hgpc的嵌合脑相比,供体来源的少突细胞中如由人tf和mbp的mbp共表达界定的生成髓鞘的比例在植入了mhtt
‑
hgpc的嵌合脑中显著较低(图8j)。类似地,与植入了hd来源的hgpc的小鼠相比,所有供体细胞中出现mbp表达的比例在植入有对照hgpc的小鼠中显著较高(图8k)。因此,植入了对照的胼胝体中的如在mbp免疫染色切片上评估的髓鞘亮度显著高于相应的植入了mhtt gpc的白质中的髓鞘亮度(图8l)。图8m和图8n显示,无论是所植入的人gpc的密度(图8g)还是分布(图8m和图8n,点图)在对照与hd来源的hgpc之间都没有显著差异,表明植入了mhtt hgpc的脑中的髓鞘形成缺陷是由于受损的少突胶质分化和髓鞘生成所致,而不是由于差异植入所致。比例尺,50mm。根据双因素anova和bonferroni事后检验,数值表示为平均值扫
±
sem.**p<0.01且***p<0.001。
[0034]
图9a
‑
图9h显示植入了mhtt gpc的脑表现出轴突髓鞘形成的减少和延迟。图9a
‑
图9f是植入了hgpc的颤抖胼胝体的共聚焦图像,该图像显示与植入有表达genea20来源的mhtt的hgpc的小鼠(图9d
‑
图9f)相比,在植入有genea19对照hgpc的小鼠(图9a
–
图9c)中mbp表达更高且包鞘轴突的比例更高。图9d’和图9e’示出了共聚焦z堆栈,其中有供体来源的mbp+少突细胞的正交视图。图9f’示出了图9f的更高倍数的放大图,其示出了包鞘轴突周围的mbp免疫反应性。图9g和图9h示出了总的经mbp包鞘的nf+宿主轴突的比例(图9g),以及每个mbp+供体来源的少突细胞的经mbp包鞘的nf+宿主轴突的比例(图9h)。比例尺代表20mm(图9a
–
图9f)和5mm(图9a
’–
图9c’)。根据双因素anova和bonferroni事后检验,数值代表平均值
±
sem.**p<0.01且***p<0.001。
[0035]
图10显示了sox10
‑
myrf转导恢复了mhtt gpc中的髓鞘基因表达。该图显示了下表1中概述的qpcr数据的图形表示。
[0036]
表1.sox10
‑
myrf转导恢复mhtt gpc中的髓鞘基因表达
[0037][0038]
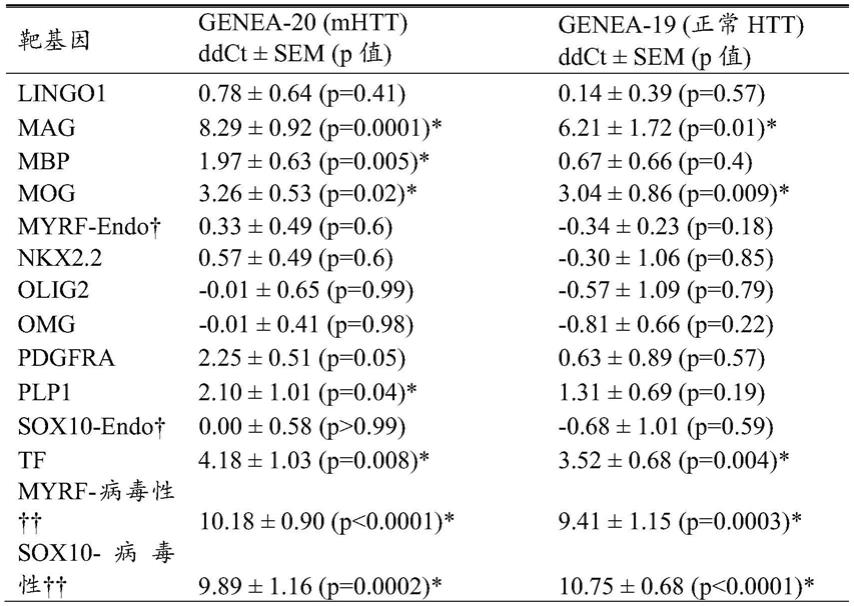
这些qpcr数据示出了在用表达sox10和myrf的双顺反子质粒转染后,正常hgpc和表达mhtt的hgpc中选定的少新生(oligoneogenic)基因和髓鞘生成基因的在以18s并随后以对照质粒转染的细胞作归一化后的ddct值,该值反映了相对mrna水平。welch’s t检验。位于编码序列上的引物;位于3’utr中的引物。endo:内源性基因;病毒:病毒转基因产品。*p<0.05。
[0039]
在用表达sox10和myrf的双顺反子质粒转染后,在正常hgpc(genea19,黑色条)和表达mhtt的(genea 20,红色)hgpc中,选定的少新生基因和髓鞘生成基因的以18s和对照质粒转染的细胞作归一化的表达值。welch t检验比较:1)针对每一个系独立进行的sox 10
‑
myrf
‑
转染对比egfp
‑
转染,显著性由星号表示;或2)sox10
‑
myrf转染的genea 20对比egfp对照转染的genea19(显著性由井字记号表示)。*/#p<0.05.**/##p<0.01.;***/###p<0.001.;****/####p<0.0001.位于编码序列上的引物;位于3’utr中的引物。
[0040]
图11a
‑
图11m显示了sox10和myrf通过mhtt gpc拯救了少突细胞分化和髓鞘生成。图11a显示了多西环素调控的双重载体慢病毒(lv)转导策略,该策略允许多西环素(dox)触发sox10和myrf的相互依赖的过表达以及cd4的同时表达以允许对sox10
‑
myrf转导的hgpc进行基于facs的免疫分离。图11b
‑
图11d示出了sox10和myrf过表达在表达mhtt的hgpc中的影响,其是通过用dox调控的慢病毒sox10/myrf转导匹配的180div genea20来源的hgpc集合,并将一些培养物暴露于dox中,而对匹配的对照培养物不予处理来评估的。在体外再待一周后,用识别少突细胞硫酸脑苷脂(oligodendrocytic sulfatide)的mab o4对细胞进行免疫染色。在dox不存在的情况下,mhtt hgpc得以稳定地维持,并且未表达可检测到的o4(图11b)。相比之下,以dox饲养的那些mhtt hgpc(图11c)具有上调的sox10和myrf表达,显示出少突细胞分化的急剧和显著增加(图11d)。该示意图概述了用于评估在存在和不存在sox10和myrf表达拯救的情况下hd来源的hgpc的体内髓鞘生成能力的实验设计。使所有细
胞在体外短暂地暴露于dox中,以便在移植到新生的免疫缺乏的颤抖小鼠中之前启动cd4表达并允许facs分离。在9周龄时,再向经受植入的小鼠给予dox 4周以启动sox10和myrf表达(+dox),或者不如此处理(
‑
dox,对照)。新生期植入了源自正常的表达htt的hesc的hgpc(genea19)的颤抖小鼠,在体内到第13周时产生了丰富的mbp表达和少突细胞形态。相比之下,植入有从hd hesc产生的表达mhtt的hgpc(genea20[g20])的小鼠在该时间点几乎没有产生可检测到的mbp。图11h和图11i显示,在9周龄时,向一些植入了genea20mhtt hgpc的小鼠口服给予dox以触发sox10和myrf表达(图11h),而不向匹配的对照给予dox(图11i)。dox(+)小鼠在经受植入的白质中显示出显著数量的mbp+髓鞘化少突细胞(图11h)。图11j和图11k显示,到同一时间点时,dox(
‑
)对照小鼠中没有供体细胞产生mbp表达(图11j),尽管有类似供体细胞植入(图11k)。图11l和图11m显示,在植入有sox10/myrf转导的genea20 hgpc的dox(+)小鼠中,供体来源的少突细胞诱导了朗维结(nodes of ranvier)的强劲形成(图11l),这由侧接有以结节架构为特点的caspr蛋白的βiv
‑
血影蛋白簇聚得到证明(图11m),该簇聚原本不存在于未处理的颤抖脑中。比例尺代表50mm(图11b、11c和11f
–
11i)、1mm(图11l)和0.5mm(图11m)。数值代表平均值
±
sem。***p<0.001(t检验)。
[0041]
图12a
‑
图12p显示在mhtt gpc中星形细胞分化延迟。图12a
‑
图12c显示在mhtt胶质嵌合体中星形细胞分化显著延迟。新生期移植有正常htt genea19来源的hgpc的小鼠到8周时开始发育出大量的供体来源的gfap+星形细胞(图12a),到13周时开始强劲地发育供体来源的gfap+星形细胞(图12b),到18周时胼胝体白质具有密集的星形细胞定殖(图12c)。图12d
‑
图12f显示,相比之下,源自genea20同胞hesc的表达mhtt的hgpc在8周(图12d)和13周(图12e)时更缓慢地发育星形细胞表型,具有几乎不明显的gfap表达,并且只有适度的gfap+星形细胞在18周时成熟(图12f)。图12g和图12h显示了对照(图12g)和表达mhtt(图12h)的星形细胞的成熟星形细胞形态的不同之处在于,mhtt星形细胞通常不能表现出它们的对照来源的对应物的径向对称度。图12i显示了与植入了对照的小鼠相比,所有供体细胞中表达gfap的细胞的比例在植入了mhtt hgpc的小鼠中始终较低。图12j
‑
图12m显示了在neurolucida中以3d模式追踪的细胞的sholl分析,该细胞在图12o和图12p中显示为扁平的,揭示了正常供体星形细胞与表达mhtt的星形胶质(astroglia)相比具有更大的纤维复杂性(图12j)和更多的初级突起(图12k),但具有更短的平均纤维长度和最大纤维长度(图12l和图12m)。图12n
–
图12p示出了体积占据率的扇入径向(fan
‑
in radial)分析(dang等人,“formoterol,a long
‑
actingβ2adrenergic agonist,improves cogntive function and promotes dendritic complexity in a mouse model of down syndrome,”biol.psychiatry 75:179
‑
188(2014),其据此通过引用整体并入),该分析揭示了mhtt星形细胞与对照星形细胞相比具有明显更多的未被胶质突起占据的区域(图12n)。图12o和图12p中的图示指示出它们的不连续结构域结构。数值代表平均值
±
sem.*p<0.05;**p<0.01;***p<0.001,采用双因素anova和bonferroni事后检验(图12i)、非线性回归的比较(p<0.0001)(图12j)以及比较所有被评分的细胞中每小鼠的平均值的非配对t检验(图12k
‑
图12n)(n=4个对照,7只mhtt小鼠)。比例尺代表25mm(图12a
–
图12f)和10mm(图12g、图12h、图12o和图12p)。
[0042]
图13a
‑
图13e显示表达mhtt的星形细胞表现出降低的复杂性和不完整的结构域结构。图13a示出了新生期植入后18周,人胶质嵌合体中gfap免疫染色的人细胞的sholl分析。
示出了作为分支顺序的函数的每个细胞线的径向交集的非线性回归曲线(洛伦兹曲线拟合)。对照组(n=7)对比mhtt小鼠(n=10)的比较;p<0.0001。图13b显示了正常htt对照系genea19和无关的正常htt hips细胞系c27均比表达mhtt的genea系(genea18和genea20)具有更多的初级突起。对照genea19和c27彼此没有区别,但genea18和genea20都与对照显著不同(单因素anova和dunnett事后t检验;p<0.0001)。图13c显示来源自两个对照系c27和genea19的星形细胞的纤维分布比这两种mhtt系中的任一种的纤维分布更加径向对称。采用单因素anova和dunnett事后检验,以c27为对照,p<0.0001。genea18和genea20均与c27显著不同,p<0.0001。图13a
‑
13c,对照:c27,灰色;和genea 19,黑色。hd来源的:genea 18,橙色;genea 20,红色。图13d示出了与移植有genea18来源的hgpc的小鼠的胼胝体的星形细胞的扁平三维冠状描迹(tracing)(图13e)相比较的来自移植有c27来源的对照hgpc的小鼠的胼胝体的星形细胞的扁平三维冠状描迹。比例尺:图13d,25μm。
[0043]
图14a
‑
图14h显示hd hesc来源的cd44+星形胶质表现出mhtt依赖性的基因表达变化。图14a示出如图1a中那样但使用经cd44分选的星形胶质及其前体执行的pca,验证了hd来源的细胞和正常细胞的分离的表达特征(signature)。图14b示出突出显示deg列表的交集的维恩图(绿色,下调;红色,上调;fdr 5%),该图是通过将源自3名hd患者的星形胶质与汇集的对照细胞进行比较并使用与图1中相同的细胞系和分析管道获得的。利用患者hd20(genea20)相对于其同胞供体ctr19(genea19)差异表达的那些基因对该3名hd患者共享的deg的列表进行过滤。图14c示出基于从(图14b)中突出显示的114个deg的原始计数计算出的经log2
‑
变换的tpm值的热图,该图示出了根据疾病状态的聚类。图14d示出了在(图14b)中突出显示的114个交集deg的功能注释的网络表示(基因本体:细胞组分,经fdr校正的p<0.1)。基因被指定为圆形节点(绿色,下调;红色,上调);圆角矩形节点代表注释术语。节点按程度划分大小,并分组为通过社区检测鉴定出的互连模块(m1
‑
m4)。对于每个着色模块,网络中会列出并标记三个最重要的注释。图14e示出了在m1中鉴定出的14个保守deg(图14d中为黄色)的表达热图,其具有与突触后和受体复合物组分有关的注释。图14f示出了在m2中鉴定出的针对核周和早期内体组分注释的9个保守deg的热图(图14d中为灰色)。图14g显示了在m3中鉴定出的11个保守deg(图14d中为蓝色)的热图,其具有与质膜、细胞
‑
细胞接合和桥粒组分有关的注释。图14h显示了在m4中鉴定出的8个deg的热图((图14d)中为橙色),其具有与细胞外基质成分有关的注释。
具体实施方式
[0044]
本文的公开内容总体上涉及治疗或抑制亨廷顿病发作的方法。这种方法涉及选择患有亨廷顿病或者有患亨廷顿病风险的受试者,并向所述受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用如表2或表3中所述的一种或多种基因或由其编码的蛋白质的一种或多种调节剂。
[0045]
[0046][0047]
[0048]
[0049]
[0050]
[0051]
[0052]
[0053]
[0054]
[0055]
[0056][0057]
[0058]
亨廷顿病是常染色体显性神经退行性疾病,其特征是持续进行性运动障碍,伴有毁灭性的精神和认知退化。亨廷顿病与新纹状体的持续严重萎缩相关联,所述新纹状体的持续严重萎缩与纹状体的主要输出神经元gaba能中型多棘投射神经元的显著丧失有关。亨廷顿病的特征是亨廷顿蛋白基因(“htt”)的第一外显子中异常长的cag重复扩增。突变型亨廷顿蛋白的编码的多聚谷氨酰胺扩增破坏了其正常功能和蛋白质
‑
蛋白质相互作用,最终产生广泛的神经病理变化,在新纹状体中最为明显。
[0059]
如本文中所用,术语“胶质细胞”是指提供支持和营养、维持体内平衡、形成髓鞘或促进髓鞘形成,并参与神经系统中的信号传递的非神经元细胞群。如本文中所用的“胶质细胞”包括胶质谱系中的完全分化的细胞,诸如少突细胞或星形细胞,以及胶质祖细胞。胶质祖细胞是具有分化为胶质谱系的细胞诸如少突细胞和星形细胞的潜力的细胞。
[0060]
如本文中所用,“治疗(treating)”或“治疗(treatment)”是指在改善损伤、病理变化或疾患上取得成功的任何迹象,包括任何客观或主观参数,诸如缓和;缓解;减少症状或者使所述损伤、病理变化或疾患变得更能被患者忍受;减慢退化或衰退的速度;使退化的最终点不那么虚弱;或者改善受试者的身体或精神健康。症状的治疗或改善可以基于客观或主观参数;包括身体检查、神经检查和/或精神评估的结果。“治疗”包括施用胶质祖细胞以预防或延迟、以减缓,或者以遏制或抑制与疾病、疾患或病症相关联的症状或病状的发展。“治疗效果”是指减轻、消除或预防受试者的疾病、疾病症状或疾病、疾患或病症的副作用。治疗可以是防治性的(以预防或以延迟疾病、疾患或病症的发作或恶化,或者以预防其临床或亚临床症状的表现),或者在疾病、疾患或病症表现后对症状的治疗性压制或减缓。
[0061]
根据本文所述方法的治疗的合适受试者包括患有亨廷顿病或者有患亨廷顿病风险的任何哺乳动物受试者。示例性哺乳动物受试者包括人、小鼠、大鼠、豚鼠和其它小型啮齿动物、狗、猫、绵羊、山羊和猴子。在一个实施方案中,受试者是人。
[0062]
用于本文所述方法的一种或多种调节剂可以是但不限于肽、核酸分子或小分子化合物。所述调节剂可以是例如天然存在的、半合成的或合成的剂。例如,调节剂可以是靶向一种或多种基因的特定功能的药物。在某些实施方案中,所述一种或多种调节剂可以是拮抗剂或激动剂。
[0063]
本发明的调节剂可以经口、肠胃外施用,例如皮下、静脉内、肌内、腹膜内施用,通过鼻内滴注来施用,或者通过施涂于粘膜,诸如鼻、喉和支气管的粘膜来施用。它们可以单独施用或与合适的药物运载体一起施用,并且可以是固体或液体形式,诸如片剂、胶囊、粉剂、溶液、悬浮液或乳剂。
[0064]
本发明的调节剂可以例如与惰性稀释剂,或与可同化的可食用运载体一起经口施用,或者它们可被包封在硬壳或软壳胶囊中,或者它们可被压制成片剂,或者它们可直接与饮食食物合并在一起。对于经口治疗施用,这些调节剂可与赋形剂合并在一起并且以片剂、胶囊、酏剂、混悬剂、糖浆剂等的形式使用。此类组合物和制品应该含有至少0.1%的活性化合物。这些组合物中化合物的百分比当然可以变化,并且可以方便地在该单位的重量的约2%至约60%之间。在此类治疗上有用的组合物中活性化合物的量使得可获得合适的剂量。根据本发明的优选组合物被制备成使得口服剂量单位含有介于约1mg与250mg之间的活性化合物。
[0065]
片剂、胶囊等还可含有粘合剂,诸如黄蓍胶、阿拉伯胶、玉米淀粉或明胶;赋形剂,
诸如磷酸二钙;崩解剂诸如玉米淀粉、马铃薯淀粉、海藻酸;润滑剂,诸如硬脂酸镁;和甜味剂诸如蔗糖、乳糖或糖精。当剂量单位形式是胶囊时,它除了含有上述类型的材料之外,还可含有液体运载体,诸如脂肪油。
[0066]
各种其它材料可以作为包衣存在或者为了改变剂量单位的物理形式而存在。例如,片剂可以用虫胶,糖或两者包衣。糖浆剂除了含有活性成分之外,还可含有作为甜味剂的蔗糖、作为防腐剂的对羟基苯甲酸甲酯和对羟基苯甲酸丙酯、染料以及诸如樱桃或橙子风味剂的调味剂。
[0067]
这些调节剂还可以肠胃外施用。还可在适当地与表面活性剂诸如羟丙基纤维素混合的水中制备这些调节剂的溶液或混悬剂。还可在甘油、液体聚乙二醇及其在油中的混合物中制备分散体。示例性油是石油、动物、植物或合成来源的油,例如花生油、大豆油或矿物油。一般来说,水、盐水、右旋糖水溶液和相关的糖溶液以及二醇诸如丙二醇或聚乙二醇是优选液体运载体,特别是对于可注射溶液而言。在常规储存和使用条件下,这些制品含有防腐剂以预防微生物的生长。
[0068]
适合注射使用的药物形式包括无菌水溶液或分散体以及用于临时制备无菌注射溶液或分散体的无菌粉末。在所有情况下,该形式必须是无菌的,并且必须是达到易注射程度的流体。它必须在制造和储存条件下是稳定的,并且必须被保存以防止微生物(诸如细菌和真菌)的污染作用。所述运载体可以是含有例如以下物质的溶剂或分散介质:水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇)、其合适的混合物和植物油。
[0069]
本发明的调节剂还可以以气溶胶的形式直接施用至气道。为了用作气雾剂,可将呈溶液或混悬液形式的本发明的化合物与合适的推进剂一起包装在加压气雾剂容器中,所述推进剂例如是具有常规助剂的烃推进剂,如丙烷、丁烷或异丁烷。本发明的材料还可以以非加压形式,诸如在喷雾器或雾化器中施用。
[0070]
如果要在dna水平上实现调节,这可通过使用基因疗法来敲除或破坏靶基因来实现。如本文中所用,“敲除”可以是基因敲低,或者可以通过包括但不限于逆转录病毒基因转移的本领域已知的技术,通过突变诸如点突变、插入、缺失、移码或错义突变来敲除基因。
[0071]
在一个实施方案中,所述一种或多种调节剂可通过锌指核酸酶阻抑本文所述的一种或多种基因的表达。锌指核酸酶(zfn)是通过使锌指dna结合结构域融合到dna切割结构域上而产生的人工限制性酶。锌指结构域可被工程改造成靶向期望的dna序列,这使得锌指核酸酶能够靶向复杂基因组中的独特序列(urnov等人,“genome editing with engineered zinc finger nucleases,”nat.rev.genet.11:636
‑
646(2010),其据此通过引用整体并入)。通过利用内源性dna修复机制,这些试剂可用于精确改变高等生物的基因组。
[0072]
所述一种或多种调节剂还可以是兆核酸酶和tal效应核酸酶(talens,cellectis bioresearch)(joung&sander,“talens:a widely applicable technology for targeted genome editing,”nat.rev.mol.cell biol.14:49
‑
55(2013),其据此通过引用整体并入)。由融合到引入双链断裂(dsb)的核酸内切酶的催化结构域上的用于序列特异性识别的tale dna结合结构域组成。的dna结合域能够以高精度靶向大的识别位点(例如17bp)。兆核酸酶是序列特异性内切核酸酶,天然存在的“dna剪刀”,源自各种单细胞生物,诸如细菌、酵母、藻类和一些植物细胞器。兆核酸酶具有介于12与30个之间的碱基对的长识别位点。兆核酸酶的识别位点可以被修饰,以便靶向天然基因组dna序列(诸如内源
基因)。
[0073]
在另一个实施方案中,所述一种或多种调节剂是crispr
‑
cas9导向核酸酶(wiedenheft等人,“rna
‑
guided genetic silencing systems in bacteria and archaea,”nature 482:331
‑
338(2012);zhang等人,“multiplex genome engineering using crispr/cas systems,”science 339(6121):819
‑
23(2013);和gaj等人,“zfn,talen,and crispr/cas
‑
based methods for genome engineering,”cell 31(7):397
‑
405(2013),其据此通过引用整体并入)。如同talen和zfn一样,crispr
‑
cas9干扰是遗传技术,其允许通过导向核酸酶双链dna切割对原核和真核细胞中的基因表达进行序列特异性控制。它基于细菌免疫系统来源的crispr(成簇的规律间隔的回文重复序列)途径。
[0074]
本文所述的一种或多种基因的调节也可以使用反义寡核苷酸(aso)进行。用于抑制本文所述的一种或多种基因的合适的治疗性aso包括但不限于反义rna、dna、rna/dna杂交体(例如,间隙体(gapmer))及其化学类似物,例如吗啉代类、肽核酸寡聚体、由锁核酸组成的aso。除rna寡聚体、pna和吗啉代类外,所有其它反义寡聚体都通过rna酶h介导的靶切割机制在真核细胞中发挥作用。pna和吗啉代类以高亲和力和特异性结合互补的dna和rna靶标,并因此通过简单的对rna翻译机制的空间阻断来起作用,并且似乎完全抵抗核酸酶攻击。
[0075]“反义寡聚体”是指包含长度为至少约10个核苷酸的寡聚物的反义分子或抗基因剂。在实施方案中,反义寡聚体包含至少15个、18个、20个、25个、30个、35个、40个或50个核苷酸。反义途径涉及对与本文鉴定的基因的多核苷酸序列编码的rna互补的寡核苷酸(dna、rna、dna/rna或其化学修饰衍生物)的设计。反义rna可以被引入到细胞中,从而通过与互补mrna进行碱基配对并从物理上阻碍该互补mrna的翻译或该互补mrna的活性来抑制该互补mrna的翻译或活性。因此,这种效应是化学计量的。绝对互补性虽然是优选的,但不是必须的。如本文中所提及的与一部分rna“互补”的序列意指具有足够的互补性从而能够与该rna杂交,形成稳定双链体的序列。在双链反义多核苷酸序列的情况下,因而可以测试双链dna的单链,或者可以测定三链体的形成。杂交能力将取决于互补程度和反义多核苷酸序列的长度。一般地,杂交多核苷酸序列越长,与其可能含有的rna的碱基错配就越多并且仍然形成稳定的双链体(或三链体,视具体情况而定)。本领域技术人员可通过使用标准程序确定杂交复合物的熔点来探知可容忍的错配程度。
[0076]
在一个实施方案中,所述一种或多种调节剂是反义寡核苷酸,其特异性地结合至本文所述的一种或多种基因并抑制本文所述的一种或多种基因的功能性表达。例如,用于增加双链体稳定性的aso的常见修饰包括5
‑
甲基
‑
dc、2
‑
氨基
‑
da、锁核酸和/或肽核酸碱基的并入。用于增强核酸酶抗性的常见修饰包括将正常的磷酸二酯键联转化为硫代磷酸酯或二硫代磷酸酯键联,或使用丙炔类似物碱基、2
’‑
o
‑
甲基或2
’‑
o
‑
甲氧基乙基rna碱基。
[0077]
使用小干扰rna(sirna)的rna干扰(rnai)是另一种形式的转录后基因沉默,其可用于调节如本文所述的受试者中的一种或多种基因。
[0078]
因此,在一个实施方案中,所述一种或多种调节剂是sirna。sirna是长度约为20
‑
25个核苷酸的双链合成rna分子,其两端具有短的2
‑
3个核苷酸的3’悬突。双链sirna分子代表靶mrna分子的一部分的有义链和反义链。sirna分子通常被设计成靶向起始密码子下游约50
‑
100个核苷酸的mrna靶标的区域。本发明的sirna可包含部分纯化的rna、基本上纯的
rna、合成的rna或重组产生的rna,以及通过添加、删除、取代和/或改变一个或多个核苷酸而不同于天然存在的rna的经改变的rna。此类改变可包括将非核苷酸物质添加至例如sirna的一个或多个末端上或者添加至sirna的一个或多个内部核苷酸上,包括使sirna对核酸酶消化具有抗性的修饰。在被引入到细胞中后,sirna复合物触发内源性rnai途径,从而导致靶mrna分子的切割和降解。sirna组合物的各种改进(诸如将经修饰的核苷或基序并入到sirna分子的一条或两条链中以增强稳定性、特异性和功效)已被描述并且适合于根据本发明的这一方面使用(参见例如,giese等人的wo2004/015107;mcswiggen等人的wo2003/070918;imanishi等人的wo1998/39352;jesper等人的美国专利申请公布第2002/0068708号;kaneko等人的美国专利申请公布第2002/0147332号;bhat等人的美国专利申请公布第2008/0119427号,这些文献据此通过引用整体并入)。
[0079]
在另一个实施方案中,所述一种或多种调节剂包含由内切核糖核酸酶制备的sirna(esirna),其包含由用内切核糖核酸酶(例如,rna酶iii或切丁酶(dicer))切割长双链rna而形成的sirna寡核苷酸的混合物。合成的长双链rna的消化产生长度在18
‑
25个碱基之间的短的重叠的sirna片段,它们都靶向相同的mrna序列。全部靶向相同mrna序列的许多不同sirna的复杂混合物导致沉默功效提高。本领域中已经描述了利用esirna技术靶向长非编码rna(theis等人,“targeting human long noncoding transcripts by endoribonuclease
‑
prepared sirnas,”j.biomol.screen 20(8):1018
‑
1026(2015),其据此通过引用整体并入)。
[0080]
所述一种或多种调节剂也可以是短的或小的发夹rna。短的或小的发夹rna分子在功能上与sirna分子类似,但包含形成紧密发夹弯的更长的rna序列。shrna被细胞机制切割成sirna,并且基因表达通过细胞rna干扰途径沉默。
[0081]
特异性地结合至本文所述的一种或多基因的核酸适体也可用于本发明的方法。核酸适体是单链、部分单链、部分双链或双链的核苷酸序列,有利地是可复制的核苷酸序列,能够通过除watson
‑
crick碱基配对或三链体形成以外的机制特异性地识别选定的非寡核苷酸分子或分子的组。适体包括但不限于限定的序列区段和序列,其包含核苷酸,核糖核苷酸,脱氧核糖核苷酸,核苷酸类似物,经修饰的核苷酸以及含有骨架修饰、分支点和非核苷酸残基、基团或桥的核苷酸。核酸适体包括部分和完全单链和双链的核苷酸分子和序列;合成的rna、dna和嵌合核苷酸;杂交体;双链体;异源双链体;以及任何核糖核苷酸、脱氧核糖核苷酸或其嵌合对应物以及/或者扩增、转录或复制适体分子或序列的全部或部分所需的相应互补序列、启动子或引物退火序列。
[0082]
在上述实施方案中,所述一种或多种调节剂可被包装在合适的递送媒介物或运载体中以用于递送至受试者。合适的递送媒介物包括但不限于病毒、病毒样颗粒、细菌、噬菌体、可生物降解的微球、微粒、纳米颗粒、外来体、脂质体、胶原小丸(minipellet)和脂质卷(cochleate)。这些和其它生物基因递送媒介物是本领域技术人员熟知的(参见,例如,seow和wood,“biological gene delivery vehicles:beyond viral vectors,”mol.therapy 17(5):767
‑
777(2009),其据此通过引用整体并入)。
[0083]
在一个实施方案中,调节剂被包装到治疗性表达载体中以促进递送。合适的表达载体是本领域公知的,包括但不限于病毒载体,诸如腺病毒载体、与腺相关联的病毒载体、逆转录病毒载体、慢病毒载体或疱疹病毒载体。病毒载体或其它合适的表达载体包含编码
mediates sirna tumor delivery,visualization and therapeutic tumor reduction in vivo,”j.control release 149(2):111
–
116(2011),其据此通过引用整体并入)。适用于本发明的其它纳米颗粒递送媒介物包括在prakash等人的美国专利公布第2010/0215724号(其据此通过引用整体并入)中公开的微胶囊纳米管装置。
[0088]
在另一个实施方案中,药物组合物包含在脂质体递送媒介物中。术语“脂质体”意指由排列在一个或多个球形双层中的两亲性脂质组成的囊泡(vesicle)。脂质体是单层或多层囊泡,其具有由亲脂性物质形成的膜和水性内部。该水性部分含有要递送的组合物。阳离子脂质体具有能够与细胞壁融合的优势。非阳离子脂质体虽然不能与细胞壁高效融合,但被体内巨噬细胞摄取。
[0089]
脂质体的几个优势包括:它们具有生物相容性和生物可降解性,能将广泛范围的水溶性和脂溶性药物并入;并且它们能保护封装的药物免受代谢和降解。在制备脂质体制剂时,重要的考虑因素是脂质表面电荷、囊泡尺寸和脂质体的含水体积(aqueous volume)。
[0090]
脂质体可用于将活性成分转移和递送至作用部位。因为脂质体膜在结构上类似于生物膜,所以当脂质体被施涂于组织时,脂质体开始与细胞膜融合,并且随着脂质体和细胞融合的进展,脂质体内容物被排空到细胞中,活性剂可以在细胞中起作用。
[0091]
用于制备用于本发明的脂质体的方法包括在以下文献中公开的那些:bangham等人,“diffusion of univalent ions across the lamellae of swollen phospholipids,”j.mol.biol.13:238
–
52(1965);hsu的美国专利第5,653,996号;lee等人的美国专利第5,643,599号;holland等人的美国专利第5,885,613号;dzau等人的美国专利第5,631,237号以及loughrey等人的美国专利第5,059,421号,所述文献通过引用整体并入。
[0092]
在一方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用胶质细胞分化调控基因的一种或多种调节剂,所述胶质细胞分化调控基因选自由以下组成的组bmp2、lingo1、mag、nkx2
‑
2、nr2e1、ntrk3、olig2、serpine2、sirt2和tcf7l2,或由其编码的蛋白质。
[0093]
针对这些基因的示例性调节剂包括但不限于:合成的非肽基小分子hh
‑
ag 1.1和相关分子hh
‑
ag 1.2、hh
‑
ag 1.3、hh
‑
ag 1.4和hh ag 1.5,它们影响hedegehog信号传导途径(frank
‑
kamenetsky等人,“small
‑
molecule modulators of hedgehog signaling:identification and characterization of smoothened agonists and antagonists,”j.biol.1(2):10(2002),其据此通过引用整体并入)以及wnt信号传导途径的激动剂,包括但不限于2
‑
氨基
‑4‑
(3,4
‑
亚甲二氧基)苄基氨基)
‑6‑
(3
‑
甲氧基苯基)嘧啶(2
‑
ambmp)、姜黄素(curcumin)和辛伐他汀(simvastatin),如blagodatski等人,“targeting the wnt pathways for therapies,”mol.cell ther.2:28(2014)(其据此通过引用整体并入)中所描述的;奥匹单抗(opicinumab);gsk
‑
249320;十二烷基硫酸钠;瑞格列奈(repaglinide);阿替拉替尼(altiratinib);chembl2007421;plx
‑
3397;根赤壳菌素(radicicol);甲状腺素;恩曲替尼(entrectinib);loxo
‑
101;cep
‑
2563;来他替尼(lestaurtinib);plx
‑
7486;azd
‑
6918;azd
‑
7451;米哚妥林(midostaurin)及其组合。
[0094]
在另一方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用与髓鞘形成相关联的基因的一种或多种调节剂,所述与髓鞘形成相关联的基因选
自由以下组成的组:fa2h、gal3st1、mag、mbp、myrf、nfasc、olig2、omg、pllp、pou3f2、sirt2、slc8a3、tcf7l2、tf和ugt8或由其编码的蛋白质。
[0095]
针对这些基因的示例性调节剂包括但不限于:wnt信号传导途径的激动剂,包括但不限于2
‑
氨基
‑4‑
(3,4
‑
(亚甲二氧基)苄氨基)
‑6‑
(3
‑
甲氧基苯基)嘧啶(2
‑
ambmp)、姜黄素和辛伐他汀,如blagodatski等人,“targeting the wnt pathways for therapies,”mol.cell ther.2:28(2014)(其据此通过引用整体并入)所述的;gsk
‑
249320;十二烷基硫酸钠、瑞格列奈;环孢菌素;干扰素β
‑
1a;泼尼松;槲皮素和芦丁及其组合。
[0096]
在又一方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用少突细胞分化基因的一种或多种调节剂,所述少突细胞分化基因选自由以下组成的组:fa2h、gli3、lingo1、myrf、nkx2
‑
2、olig1、olig2、omg、sirt2、slc8a3、sox10和tcf7l2,或由其编码的蛋白质。
[0097]
针对这些基因的示例性调节剂包括但不限于:合成的非肽基小分子hh
‑
ag 1.1和相关分子hh
‑
ag 1.2、hh
‑
ag 1.3、hh
‑
ag 1.4和hh ag 1.5,它们影响hedegehog信号传导途径(frank
‑
kamenetsky等人,“small
‑
molecule modulators of hedgehog signaling:identification and characterization of smoothened agonists and antagonists,”j.biol.1(2):10(2002),其据此通过引用整体并入),以及wnt信号传导途径的激动剂,包括但不限于2
‑
氨基
‑4‑
(3,4
‑
(亚甲二氧基)苄氨基)
‑6‑
(3
‑
甲氧基苯基)嘧啶(2
‑
ambmp)、姜黄素和辛伐他汀,如blagodatski等人,“targeting the wnt pathways for therapies,”mol.cell ther.2:28(2014)(其据此通过引用整体并入)中所述的;奥匹单抗;十二烷基硫酸钠;瑞格列奈;维莫非尼;以及它们的组合。
[0098]
在进一步的方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用胶质生成调控基因的一种或多种调节剂,所述胶质生成调控基因选自由以下组成的组:bmp2、lingo1、mag、myc、nkx2
‑
2、nr2e1、ntrk3、olig2、serpine2、sirt2、sox10、tcf7l2、tf和zcchc24,或由其编码的蛋白质。
[0099]
这些基因的示例性调节剂包括但不限于:合成的非肽基小分子hh
‑
ag 1.1和相关分子hh
‑
ag 1.2、hh
‑
ag 1.3;hh
‑
ag 1.4和hh ag 1.5,它们影响hedegehog信号传导途径(frank
‑
kamenetsky等人,“small
‑
molecule modulators of hedgehog signaling:identification and characterization of smoothened agonists and antagonists,”j.biol.1(2):10(2002)(其据此通过引用整体并入),以及wnt信号传导途径的激动剂,包括但不限于2
‑
氨基
‑4‑
(3,4
‑
(亚甲二氧基)苄氨基)
‑6‑
(3
‑
甲氧基苯基)嘧啶(2
‑
ambmp)、姜黄素和辛伐他汀,如blagodatski等人,“targeting the wnt pathways for therapies,”mol.cell ther.2:28(2014),其据此通过引用整体并入)中所述的;奥匹单抗;gsk
‑
249320;十二烷基硫酸钠;维莫非尼;瑞格列奈;那屈肝素钙;4
’‑
羟基他莫昔芬;阿扎胞苷;硫鸟嘌呤;激活素;阿多来新;氨磷汀;氨基蝶呤;抗生素;比折来新;溴隐亭;苔藓抑素;骨化三醇;二乙基己烯雌酚;依沙芦星;雌酮;叶酸;谷氨酰胺;次黄嘌呤;伊马替尼;西拉司丁(cilmostin);褪黑激素;甲基泼尼松龙;n
‑
甲基
‑
n
‑
亚硝基脲;新生霉素;chembl35482;佛波醇肉豆蔻酸酯乙酸酯;泼尼松;喹那普利;伏林司他(vorinostat);舒林酸;凝血酶;促甲状腺素;β
‑
烟酰胺腺嘌呤二核苷酸磷酸钠;曲格列酮;维拉帕米;chembl100014;chembl1213492;绒毛膜促性腺激素;紫苏醇(perillyl alcohol);amg
‑
900;alisertib;
dinaciclib;roniciclib;替莫唑胺;普列克斯替布(prexasertib);阿替拉替尼;chembl2007421;plx
‑
3397;根赤壳菌素(radicicol);甲状腺素;恩曲替尼;loxo
‑
101;cep
‑
2563;来他替尼;plx
‑
7486;azd
‑
6918;azd
‑
7451;米哚妥林;以及它们的组合。
[0100]
在本公开的另一个方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用神经元包鞘基因的一种或多种调节剂,所述神经元包鞘基因选自由以下组成的组:fa2h、gal3st1、mag、mbp、myrf、nfasc、olig2、omg、pllp、pou3f2、sirt2、slc8a3、tcf7l2、tf和ugt8,或由基编码的蛋白质。
[0101]
针对这些基因的示例性调节剂包括但不限于:wnt信号传导途径的激动剂,包括但不限于2
‑
氨基
‑4‑
(3,4
‑
(亚甲二氧基)苄氨基)
‑6‑
(3
‑
甲氧基苯基)嘧啶(2
‑
ambmp)、姜黄素和辛伐他汀,如blagodatski等人,“targeting the wnt pathways for therapies,”mol.cell ther.2:28(2014)(其据此通过引用整体并入)中所述的;gsk
‑
249320;环孢菌素;干扰素β
‑
1a;泼尼松;槲皮素;芦丁;十二烷基硫酸钠;瑞格列奈;以及它们的组合。
[0102]
在另一方面,向所选受试者在对治疗或抑制所述受试者亨廷顿病发作有效的条件下施用轴突导向基因的一种或多种调节剂,所述轴突导向基因选自由以下组成的组:alcam、bcl11b、dscam、foxd1、gas1、gli3、hoxa1、hoxa2、mnx1、nfasc、plxnc1、prkcq、ptpro、robo2、sema6b、unc5a、vax1和wnt7b,或由其编码的蛋白质。
[0103]
针对这些基因的示例性调节剂包括但不限于wnt信号传导途径的激动剂,包括但不限于2
‑
氨基
‑4‑
(3,4
‑
(亚甲二氧基)苄氨基)
‑6‑
(3
‑
甲氧基苯基)嘧啶(2
‑
ambmp)、姜黄素和辛伐他汀,如blagodatski等人,“targeting the wnt pathways for therapies,”mol.cell ther.2:28(2014)(其据此通过引用整体并入本文)中所述的;氟尿嘧啶;cep
‑
2563;星形孢菌素;chembl369507;右磷丝氨酸;噻氯匹定;gsk
‑
690693;索曲妥林;(7s)
‑
羟基
‑
星形孢菌素;米哚妥林;槲皮素;苔藓抑素;醋酸索曲妥林;巨大戟醇甲基丁烯酸酯(ingenol mebutate);卡铂;紫杉醇;以及它们的其组合。
[0104]
在又一方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用神经元投射导向基因的一种或多种调节剂,所述神经元投射导向基因选自由以下组成的组:alcam、bcl11b、dscam、foxd1、gas1、gli3、hoxa1、hoxa2、mnx1、nfasc、plxnc1、prkcq、ptpro、robo2、sema6b、unc5a、vax1和wnt7b,或由其编码的蛋白质。
[0105]
针对这些基因的示例性调节剂包括但不限于:wnt信号传导途径的激动剂,包括但不限于2
‑
氨基
‑4‑
(3,4
‑
(亚甲二氧基)苄氨基)
‑6‑
(3
‑
甲氧基苯基)嘧啶(2
‑
ambmp)、姜黄素和辛伐他汀,如blagodatski等人,“targeting the wnt pathways for therapies,”mol.cell ther.2:28(2014)(其据此通过引用整体并入本文)中所述的;氟尿嘧啶;cep
‑
2563;星形孢菌素;chembl369507;右磷丝氨酸;噻氯匹定;gsk
‑
690693;索曲妥林;(7s)
‑
羟基
‑
星形孢菌素;米哚妥林;槲皮素;苔藓抑素;醋酸索曲妥林;巨大戟醇甲基丁烯酸酯;卡铂;紫杉醇;以及它们的组合。
[0106]
在另一方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用轴突生成基因的一种或多种调节剂,所述轴突生成基因选自由以下组成的组:adgrb1、alcam、bcl11b、cacna1a、dscam、foxd1、gas1、gli3、hoxa1、hoxa2、lingo1、lrrc4c、mag、mbp、mnx1、nfasc、nr2e1、ntng1、ntrk3、omg、plxnc1、pou3f2、prkcq、ptpro、robo2、sema6b、slitrk2、slitrk3、snap91、unc5a、vax1和wnt7b,或由其编码的蛋白质。
[0107]
针对这些基因的示例性调节剂包括但不限于:wnt信号传导途径的激动剂,包括但不限于2
‑
氨基
‑4‑
(3,4
‑
(亚甲二氧基)苄氨基)
‑6‑
(3
‑
甲氧基苯基)嘧啶(2
‑
ambmp),姜黄素和辛伐他汀,如blagodatski等人,“targeting the wnt pathways for therapies,”mol.cell ther.2:28(2014)(其据此通过引用整体并入本文)中所述的;奥匹单抗;gsk
‑
249320;环孢菌素;干扰素β
‑
1a;泼尼松;槲皮素;芦丁;氟尿嘧啶;cep
‑
2563;星形孢菌素;chembl369507;右磷丝氨酸;噻氯匹定;gsk
‑
690693;索曲妥林;(7s)
‑
羟基
‑
星形孢菌素;米哚妥林;苔藓抑素;醋酸索曲妥林;巨大戟醇甲基丁烯酸酯;卡铂;紫杉醇;普瑞巴林;维拉帕米;苄普地尔;塞来昔布;尼索地平;加巴喷丁;加巴喷丁依那卡比;艾培三嗪;阿塔加巴林;盐酸苄普地尔;胺甲辛酸;阿替拉替尼;chembl2007421;plx
‑
3397;radicicola;甲状腺素;恩曲替尼;loxo
‑
101;cep
‑
2563;来他替尼;plx
‑
7486;azd
‑
6918;azd
‑
7451;以及它们的组合。
[0108]
在另一方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用轴突发育基因的一种或多种调节剂,所述轴突发育基因选自由以下组成的组:adgrb1、alcam、bcl11b、cacna1a、dscam、foxd1、gas1、gli3、hoxa1、hoxa2、lingo1、lrrc4c、mag、mbp、mnx1、nefm、nfasc、nr2e1、ntng1、ntrk3、omg、plxnc1、pou3f2、prkcq、ptpro、robo2、rtn4rl2、sema6b、slitrk2、slitrk3、snap91、unc5a、vax1和wnt7b,或由其编码的蛋白质。
[0109]
针对这些基因的示例性调节剂包括但不限于:wnt信号传导途径的激动剂,包括但不限于2
‑
氨基
‑4‑
(3,4
‑
(亚甲二氧基)苄氨基)
‑6‑
(3
‑
甲氧基苯基)嘧啶(2
‑
ambmp)、姜黄素和辛伐他汀,如blagodatski等人,“targeting the wnt pathways for therapies,”mol.cell ther.2:28(2014)(其据此通过引用整体并入本文)中所述的;奥匹单抗;右磷丝氨酸;氟尿嘧啶;cep
‑
2563;星形孢菌素;chembl369507;gsk
‑
249320;噻氯匹定;gsk
‑
690693;索曲妥林;(7s)
‑
羟基
‑
星形孢菌素;米哚妥林;槲皮素;苔藓抑素;醋酸索曲妥林;和巨大戟醇甲基丁烯酸酯;卡铂;紫杉醇;普瑞巴林;维拉帕米;苄普地尔;塞来昔布;尼索地平;加巴喷丁;加巴喷丁依那卡比;艾培三嗪;阿塔加巴林;盐酸苄普地尔;胺甲辛酸;阿替拉替尼;chembl2007421;plx
‑
3397;radicicola;甲状腺素;恩曲替尼;loxo
‑
101;cep
‑
2563;来他替尼;plx
‑
7486;azd
‑
6918;azd
‑
7451;环孢菌素;干扰素β
‑
1a;泼尼松;芦丁;以及它们的组合。
[0110]
在本公开的进一步方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用细胞投射形态发生基因的一种或多种调节剂,所述细胞投射形态发生基因选自由以下组成的组:adgrb1、alcam、bcl11b、cacna1a、camk2a、dscam、ehd3、foxd1、gas1、gli3、hoxa1、hoxa2、kank1、lingo1、lrrc4c、mag、mbp、mnx1、nedd4l、neurl1、nfasc、nr2e1、ntng1、ntrk3、omg、pcdh15、plxnc1、pou3f2、prkcq、ptpro、robo2、sema6b、sgk1、slitrk2、slitrk3、snap91、snx10、ugt8、unc5a、vax1和wnt7b,或由其编码的蛋白质。
[0111]
针对这些基因的示例性调节剂包括但不限于:wnt信号传导途径的激动剂,包括但不限于2
‑
氨基
‑4‑
(3,4
‑
(亚甲二氧基)苄氨基)
‑6‑
(3
‑
甲氧基苯基)嘧啶(2
‑
ambmp)、姜黄素和辛伐他汀,如blagodatski等人,“targeting the wnt pathways for therapies,”mol.cell ther.2:28(2014)(其据此通过引用整体并入本文)中所述的;奥匹单抗;gsk
‑
249320;环孢菌素;干扰素β
‑
1a;泼尼松;槲皮素;芦丁;右磷丝氨酸;氟尿嘧啶;cep
‑
2563;星
tosylate)、mibampator、布特萨、(r,s)
‑
ampa、chembl123132、茴拉西坦(aniracetam)、chembl136800、chembl1255648、环噻嗪(cyclothiazide)、chembl77862、chembl334920、chembl1097939、吡拉西坦(piracetam)、chembl320642、chembl265301、gyki
‑
52466、nbqx、chembl222418、替占帕奈(tezampanel)、(s)
‑
ampa、chembl594840、chembl121915、使君子氨酸(quisqualate)、chembl337577、chembl27130、dnqx、chembl333964、(s)
‑
willardiine、chembl28472、他仑帕奈(talampanel)、吡仑帕奈(perampanel)、依仑帕奈(irampanel)、cx1739、达兰帕奈(dasolampanel)、贝坎帕奈(becampanel)、法拉帕托(farampator)、mk
‑
8777、唑南帕奈(zonampanel)、戊巴比妥(pentobarbital)、pf
‑
04958242、舍路帕奈(selurampanel)、达伐吡啶(dalfampridine)、盐酸胍、替地沙米(tedisamil)、奈立吡啶(nerispirdine)、evt401、三磷酸腺苷、chembl335550、白屈菜红碱(chelerythrine)、醋丁洛尔(acebutolol)、吗氯贝胺(moclobemide)、伊维菌素(ivermectin)、chemb377219、chembl255787、甲氯噻嗪(methylclothiazide)、chembl550637、原钒酸钠(sodium orthovanadate)、chembl2338352、苯佐那酯(benzonatate)、gsk1482160、azd9056、ce224535、喘定(dyphylline)、chembl484928、双嘧达莫(dipyridamole)、盐酸黄酮哌酯(flavoxate hydrochloride)、己酮可可碱(pentoxifylline)、奎纳克林(quinacrine)、chembl2313646、chembl570352、奥扎尼莫德(ozanimod)、chembl225155、chembl1368758、盐酸芬戈莫德(fingolimod hydrochloride)、盐酸阿米西莫德(amiselimod hydrochloride)、利血平(reserpine)、去甲肾上腺素(norepinephrine)、chembl126506、甲基苯丙胺(methamphetamine)、酮色林(ketanserin)、四苯喹嗪(tetrabenazine)、l
‑
谷氨酸盐、二氢卡因酸盐(dihydrokainate)、2s,4r
‑4‑
甲基谷氨酸盐(2s,4r
‑4‑
methylglutamate)、o
‑
苄基
‑
l
‑
丝氨酸、chembl1628669,和美沙拉明(mesalamine)、替占帕奈(tezampanel)、软骨藻酸(domoic acid)、dysiherbaine、红藻氨酸(kainic acid)、美沙拉明(mesalamine)、托吡酯(topiramate)、天冬氨酸、氯氮平(clozapine)、酒精、氟哌啶醇(haloperidol)、渥曼青霉素(wortmannin)、奥氮平(olanzapine)、佛波醇肉豆蔻酸酯乙酸酯(phorbol myristate acetate)、利培酮(risperidone)、利多卡因(lidocaine)、普瑞巴林(pregabalin)、加巴喷丁依那卡比(gabapentin enacarbil)、二盐酸米贝拉地尔(mibefradil dihydrochloride)、三甲双酮(trimethadione)、桂利嗪(cinnarizine)、乙琥胺(ethosuximide)、唑尼沙胺(zonisamide)、大麻素(anandamide)、米贝拉地尔(mibefradil)、chembl1684954、氟桂利嗪(flunarizine)、甲琥胺(methsuximide)、盐酸苄普地尔(bepridil hydrochloride)、加巴喷丁(gabapentin)、苯琥胺(phensuximide)、甲乙双酮(paramethadione)、阿塔加巴林(atagabalin)、塞来昔布(celecoxib)、胺甲辛酸(imagabalin);以及它们的组合。
[0116]
在另一个方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用突触基因的一种或多种调节剂,所述突触基因选自由以下组成的组:adgrb1、bcan、bcas1、cacna1a、calb1、camk2a、chrna4、cttnbp2、dscam、gria2、grid1、grid2、grik4、hcn2、kcnd2、lgi3、lrrc4c、lrrtm1、neto1、neurl1、ntm、p2rx7、pcdh15、pde4b、ppfia3、prima1、prkcq、ptpro、rapgef4、serpine2、shisa7、slc17a8、slc18a1、slc1a1、slc1a2、slc8a3、snap91、snph、syndig1和syt6,或由其编码的蛋白质。
[0117]
针对这些基因的示例性调节剂包括但不限于:右磷丝氨酸、普瑞巴林、维拉帕米、
苄普地尔、塞来昔布、尼索地平、加巴喷丁、加巴喷丁依那卡比、艾培三嗪、阿塔加巴林、盐酸苄普地尔、胺甲辛酸、mibampator、布特萨、仲丁巴比妥、布他比妥、他布比妥、司可巴比妥、美沙比妥、硫喷妥、扑米酮、甲苯比妥、苯巴比妥、(r,s)
‑
ampa、chembl123132、茴拉西坦、chembl136800、chembl1255648、环噻嗪、chembl77862、chembl334920、chembl1097939、吡拉西坦、chembl320642、chembl265301、gyki
‑
52466、nbqx、chembl222418、替占帕奈、异戊巴比妥、阿普比妥、庚巴比妥、海索比妥、巴比妥、(s)
‑
ampa、chembl594840、chembl121915、使君子氨酸、chembl337577、chembl27130、dnqx、chembl333964、(s)
‑
willardiine、chembl28472、他仑帕奈、吡仑帕奈、依仑帕奈、cx1739、达兰帕奈、贝坎帕奈、法拉帕托、mk
‑
8777、唑南帕奈、托吡酯、戊巴比妥、pf
‑
04958242、舍路帕奈(selurampanel)、波拉克磷尼古丁、伐尼克兰、布特萨、帕扎克兰、金雀花碱、rivanicline、地棘蛙素、chembl1876219、chembl3103988、阿曲库铵、chembl490153、六甲铵、chembl407217、tc
‑
2216、abt
‑
560、异丙克兰、索菲尼克林、tc
‑
6499、azd1446、cp
‑
601927、右美卡拉明(dexmecamylamine)、尼古丁、酒石酸伐尼克兰、甲磺酸苯扎托品、喷托铵、azd0328、bradanicline、戊巴比妥、chembl1201135、右依法克生(dexefaroxan)、美卡拉明(chembl267936)、dianicline、阿替克林、咪噻吩(trimethaphan)、油酸、甲苯磺酸替巴克兰、波拉克磷尼古丁、卡铂、紫杉醇、l
‑
谷氨酸盐、达伐吡啶、盐酸胍、替地沙米、奈立吡啶、evt401、三磷酸腺苷、chembl335550、白屈菜红碱、醋丁洛尔、吗氯贝胺、伊维菌素、chemb377219、chembl255787、甲氯噻嗪、chembl550637、原钒酸钠、chembl2338352、苯佐那酯、gsk1482160、azd9056、ce224535、利血平、去甲肾上腺素、chembl126506、甲基苯丙胺、酮色林、四苯喹嗪、l
‑
谷氨酸盐、二氢卡因酸盐、2s,4r
‑4‑
甲基谷氨酸盐、o
‑
苄基
‑
l
‑
丝氨酸、chembl1628669、美沙拉明、替占帕奈、软骨藻酸、dysiherbaine、红藻氨酸、美沙拉明、托吡酯、cep
‑
2563、星形孢菌素、chembl369507、噻氯匹定、gsk
‑
690693、索曲妥林、(7s)
‑
羟基
‑
星形孢菌素、米哚妥林、槲皮素、苔藓抑素、醋酸索曲妥林、巨大戟醇甲基丁烯酸酯、磷酸腺苷、茶碱、喘定、己酮可可碱、恩丙茶碱、伊洛前列素(iloprost)、罂粟碱、可可碱、氨吡酮(inamrinone)、[r]
‑
美索普兰、罗氟司特、吡拉米司特、咯利普兰、非明司特、chembl1230617、chembl519827、西洛司特、(
‑
)
‑
咯利普兰、克立硼罗(crisaborole)、异丁司特、阿普司特、chembl521203、chembl74078、丙氧芬、cdp840、苯丁酸钠、chembl1232082、双嘧达莫、茶碱甘氨酸钠、盐酸黄酮哌酯、氨茶碱、白藜芦醇、咖啡因、胆茶碱、氨来占诺、依地唑酯、西洛雷定、扎替雷定、chembl2052019、chembl395336、环单磷酸腺苷、天冬氨酸、氯氮平、酒精、氟哌啶醇、渥曼青霉素、奥氮平、佛波醇肉豆蔻酸酯乙酸酯、利培酮、利多卡因,以及它们的组合。
[0118]
在又一个方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用单价无机阳离子转运基因的一种或多种调节剂,所述单价无机阳离子转运基因选自由以下组成的组:abcc9、asic4、cacna1a、chrna4、cngb1、cntn1、dpp10、dpp6、fgf12、fgf14、hcn2、kcnd2、kcnj9、kcnq1、kcns3、nalcn、nedd4l、nkain4、p2rx7、ptger3、serpine2、sgk1、slc10a4、slc17a8、slc18a1、slc22a3、slc2a13、slc5a9、slc8a3和slc9a7,或由其编码的蛋白质。
[0119]
针对这些基因的示例性调节剂包括但不限于:纳米尼地尔、三磷酸腺苷、格列本脲、沙拉卡林、吡那地尔水合物、米诺地尔、普瑞巴林、维拉帕米、苄普地尔、塞来昔布、尼索地平、加巴喷丁、加巴喷丁依那卡比、艾培三嗪、阿塔加巴林、盐酸苄普地尔、胺甲辛酸、
chembl549906、chembl550795、氯化钠、gsk
‑
650394、达伐吡啶、盐酸胍、替地沙米、奈立吡啶、evt401、三磷酸腺苷、chembl335550、白屈菜红碱、醋丁洛尔、吗氯贝胺、伊维菌素、chemb377219、chembl255787、甲氯噻嗪、chembl550637、原钒酸钠、chembl2338352、苯佐那酯、gsk1482160、azd9056、ce224535、氢氯噻嗪、chembl1229875、波拉克磷尼古丁、他布比妥、仲丁巴比妥、布他比妥、司可巴比妥、美沙比妥、硫喷妥、扑米酮、甲苯比妥、苯巴比妥、伐尼克兰、异戊巴比妥、阿普比妥、布特萨、庚巴比妥、海索比妥、巴比妥、帕扎克兰、金雀花碱、rivanicline、地棘蛙素、chembl1876219、chembl3103988、阿曲库铵、chembl490153、六甲铵、chembl407217、tc
‑
2216、abt
‑
560、异丙克兰、索菲尼克林、tc
‑
6499、西洛雷定、扎替雷定、chembl2052019、chembl395336、环单磷酸腺苷、chembl99951、氟吡汀、吲达帕胺、苄普地尔、阿齐利特、chembl2070953、甲芬那酸、chembl1907717、尼氟酸、chembl298475、chembl342375、chembl332826、多拉司琼、塞来昔布、奈立吡啶、埃佐加滨、吲哚美辛、他克莫司、盐酸胍、替地沙米、达伐吡啶、乙胺嘧啶、钴(ii)离子维拉帕米乙胺嘧啶钴(ii)离子、二氢卡因酸盐、比马前列素、地诺前列酮、米索前列醇、贝前列素、chembl1628262、卡巴环素、西卡前列素、氯前列烯醇(chembl2220404)、恩前列素、氟前列烯醇、伊洛前列素、地诺前列素、硫前列酮、曲前列环素、chembl357834、chembl1317823、chembl565591、chembl358653、sarcnu,以及它们的组合。
[0120]
在本公开的进一步方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用神经元投射基因的一种或多种调节剂,所述神经元投射基因选自由以下组成的组:adgrl3、alcam、bcan、bcl11b、cacna1a、cacna1g、calb1、camk2a、chrna4、cttnbp2、dscam、gria2、gria4、grid2、grik4、hcn2、kcnd2、lgi3、lrrtm1、mag、mbp、myc、ncam2、ncdn、nefm、neurl1、nfasc、ntm、pde4b、pik3r1、ptger3、ptpro、rapgef4、rgs8、robo2、sgk1、sirt2、slc17a8、slc1a2、slc8a3、snap91、snph、syndig1和unc5a,或由其编码的蛋白质。
[0121]
这对这些基因的示例性调节剂包括但不限于:磷酸腺苷、茶碱、喘定、己酮可可碱、恩丙茶碱、伊洛前列素、罂粟碱、可可碱、氨吡酮、[r]
‑
美索普兰、罗氟司特、吡拉米司特、咯利普兰、非明司特、chembl1230617、chembl519827、西洛司特、(
‑
)
‑
咯利普兰、克立硼罗(crisaborole)、异丁司特、阿普司特、chembl521203、chembl74078、丙氧芬、cdp840、苯丁酸钠、chembl1232082、双嘧达莫、茶碱甘氨酸钠、盐酸黄酮哌酯、氨茶碱、白藜芦醇、咖啡因、胆茶碱、氨来占诺、依地唑酯、普瑞巴林、维拉帕米、苄普地尔、塞来昔布、尼索地平、加巴喷丁、加巴喷丁依那卡比、艾培三嗪(elpetrigine)、阿塔加巴林、盐酸苄普地尔、胺甲辛酸、卡铂、紫杉醇、chembl549906、chembl550795、氯化钠、gsk
‑
650394、达伐吡啶、盐酸胍、替地沙米、奈立吡啶、l
‑
谷氨酸盐、二氢卡因酸盐、2s,4r
‑4‑
甲基谷氨酸盐、o
‑
苄基
‑
l
‑
丝氨酸、chembl1628669、美沙拉明、氟尿嘧啶、普瑞巴林、加巴喷丁依那卡比、二盐酸米贝拉地尔、三甲双酮、桂利嗪、乙琥胺、唑尼沙胺、大麻素、米贝拉地尔、chembl1684954、氟桂利嗪、甲琥胺、盐酸苄普地尔、加巴喷丁、苯琥胺、甲乙双酮、阿塔加巴林、塞来昔布,和胺甲辛酸、波拉克磷尼古丁、他布比妥、仲丁巴比妥、布他比妥、司可巴比妥、美沙比妥、硫喷妥、扑米酮、甲苯比妥、苯巴比妥、伐尼克兰、异戊巴比妥、阿普比妥、布特萨、庚巴比妥、海索比妥、巴比妥、帕扎克兰、金雀花碱、rivanicline、地棘蛙素、chembl1876219、chembl3103988、阿曲库铵、chembl490153、六甲铵、chembl407217、tc
‑
2216、abt
‑
560、异丙克兰、索菲尼克林、tc
‑
6499、
mibampator、(r,s)
‑
ampa、chembl123132、茴拉西坦、chembl136800、chembl1255648、环噻嗪、chembl77862、chembl334920、chembl1097939、吡拉西坦、chembl320642、chembl265301、gyki
‑
52466、nbqx、chembl222418、替占帕奈、(s)
‑
ampa、chembl594840、chembl121915、使君子氨酸、chembl337577、chembl27130、dnqx、chembl333964、(s)
‑
willardiine、chembl28472、他仑帕奈、吡仑帕奈、依仑帕奈、cx1739、达兰帕奈、贝坎帕奈、法拉帕托、mk
‑
8777、唑南帕奈、托吡酯、戊巴比妥、pf
‑
04958242、舍路帕奈(selurampanel)、环噻嗪、chembl334920、chembl1097939、joro蜘蛛毒素、软骨藻酸、dysherbacine、红藻氨酸、美沙拉明、2s,4r
‑4‑
甲基谷氨酸盐、chembl2313646、环孢菌素、干扰素β
‑
1a、泼尼松、槲皮素、芦丁、gsk
‑
249320、西洛雷定、扎替雷定、chembl2052019、chembl395336、环单磷酸腺苷、十二烷基硫酸钠、比马前列素、地诺前列酮、米索前列醇、贝前列素、chembl1628262、卡巴环素、西卡前列素、氯前列烯醇(chembl2220404)、恩前列素、氟前列烯醇、伊洛前列素、地诺前列素、硫前列酮、曲前列环素、chembl357834、chembl1317823、chembl565591、chembl358653、那屈肝素钙、4
’‑
羟基他莫昔芬、阿扎胞苷、硫鸟嘌呤、激活素、阿多来新、氨磷汀、氨基蝶呤、抗生素、比折来新、溴隐亭、苔藓抑素、骨化三醇、二乙基己烯雌酚、依沙芦星、雌酮、叶酸、谷氨酰胺、次黄嘌呤、伊马替尼、西拉司丁(cilmostin)、褪黑激素、甲基泼尼松龙、n
‑
甲基
‑
n
‑
亚硝基脲、新生霉素、chembl35482、佛波醇肉豆蔻酸酯乙酸酯、泼尼松、喹那普利、伏林司他、舒林酸、凝血酶、促甲状腺素、β
‑
烟酰胺腺嘌呤二核苷酸磷酸钠、曲格列酮、维拉帕米(verapamil)、chembl100014、chembl1213492、绒毛膜促性腺激素、紫苏醇、amg
‑
900、alisertib、dinaciclib、roniciclib、替莫唑胺、普列克斯替布、pf
‑
04691502、普喹替尼、pa
‑
799、异丙肾上腺素、sf
‑
1126、渥曼青霉素、gsk
‑
2636771、ds
‑
7423、奥米利塞、recilisib、pwt
‑
33587、rg
‑
7666、vs
‑
5584、copanlisib、gedatolisib、松里昔布、apitolisib、他塞利昔布、皮拉里昔布(chembl3360203)、沃塔里昔布、zstk
‑
474、阿尔琣昔布、pi
‑
103、皮拉里昔布(chembl3218575)、wx
‑
037、达托里昔布、bgt
‑
226(chembl3545096)、pictilisib、布帕里昔布、帕努里昔布、gsk
‑
1059615、azd
‑
6482、盐酸布帕里昔布(buparlisib hydrochloride)、ly
‑
3023414以及它们的组合。
[0122]
在另一方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用tcf7l2靶基因的一种或多种调节剂,所述tcf7l2靶基因自由以下组成的组:bmp4、ccnd1、ccnd2、dock10、dock9、dusp15、enpp4、epas1、ephb1、erbb3、evi2a、evi2b、fa2h、gjb1、hapln2、hspa2、id3、lgi3、mbp、mog、myc、myrf、nfasc、nkain1、nkx6
‑
2、olig2、plekhb1、plp1、ppp1r16b、rab33a、rasgef1b、rtkn、sirt2、slc1a2、sox10、st18、tmem125、tmem2、tppp、tspan15、ugt8和aatk,或由其编码的蛋白质。
[0123]
针对这些基因的示例性调节剂包括但不限于:wnt信号传导途径的激动剂,包括但不限于2
‑
氨基
‑4‑
(3,4
‑
(亚甲二氧基)苄氨基)
‑6‑
(3
‑
甲氧基苯基)嘧啶(2
‑
ambmp)、姜黄素和辛伐他汀,如blagodatski等人,“targeting the wnt pathways for therapies,”mol.cell ther.2:28(2014)(其据此通过引用整体并入)中所述的;三氧化二砷;对乙酰氨基酚;维生素e;阿糖胞苷;棉酚;roniciclib;瑞博西尼(ribociclib);帕布昔利布;甲氨蝶呤;霉酚酸;硝苯地平;他莫昔芬;曲格列酮;尿嘧啶;abemaciclib;布瑞昔利布(briciclib);abemaciclib;地西他滨;帕布昔利布;派罗酰胺;环孢菌素;干扰素β
‑
1a;泼尼松;槲皮素;芦丁;维莫非尼;那屈肝素钙;4
’‑
羟基他莫昔芬;阿扎胞苷;硫鸟嘌呤;阿西维
辛;阿多来新;氨磷汀;氨基蝶呤;抗生素;比折来新;溴隐亭;苔藓抑素;骨化三醇;二乙基己烯雌酚;依沙芦星;雌酮;叶酸;谷氨酰胺;次黄嘌呤;伊马替尼;吲哚美辛;锂;司莫司汀;褪黑激素;甲基泼尼松龙;n
‑
甲基
‑
n
‑
亚硝基脲;新生霉素、chembl35482;佛波醇肉豆蔻酸酯乙酸酯;泼尼松;喹那普利;伏林司他;舒林酸;凝血酶;促甲状腺素;β
‑
烟酰胺腺嘌呤二核苷酸磷酸钠;曲格列酮;维拉帕米;chembl100014;chembl1213492;促性腺激素;绒促性素(chorionic);紫苏醇;amg
‑
900;alisertib;dinaciclib;替莫唑胺;普列克斯替布;十二烷基硫酸钠;l
‑
谷氨酸盐;二氢卡因酸盐;2s,4r
‑4‑
甲基谷氨酸盐;o
‑
苄基
‑
l
‑
丝氨酸;chembl1628669;美沙拉明;派罗酰胺;以及它们的组合。
[0124]
在本公开的最后一个方面,向所选受试者在对治疗或抑制所述受试者的亨廷顿病发作有效的条件下施用参与nkx2.2
→
olig2
→
sox10
→
myrf调控级联的基因或由其编码的蛋白质的一种或多种调节剂。
[0125]
该途径中基因的示例性调节剂包括但不限于维莫非尼(vemurafenib)。
[0126]
本发明的示例性调节剂及其相应的基因靶标在下表4中给出。
[0127]
表4.
[0128]
[0129]
[0130]
[0131]
[0132]
[0133]
[0134]
[0135]
[0136]
[0137]
[0138]
[0139]
[0140]
[0141][0142]
表4中列出的所有参考文献据此通过引用整体并入。
[0143]
1 sim et al.,“p21 and cd166 as predictive markers of poor r esponse and outcome after fluorouracil
‑
based chemoradiotherapy for the patients with rectal cancer,”bmc cancer 14:241(2014);
2 overi ngton et al.,“how many drug targets are there?”nat.rev.drug.discov.5(12):993
‑
6(2006);
3 gazulla et al.,
cycle by fenr etinide in burkitt's lymphoma mutu i cell line accessed with bcl
‑
6down
‑
regulation,”biochem biophys res commun.276(3):1295
‑
1301(2000);
106
biton v.“clinical pharmacology and mechanism of action of zonisamide,”clin neuropharmacol.30(4):230
‑
240(2007);
107
hyun et a l.,“arsenic trioxide inhibits the growth of a498 renal cell carcino ma cells via cell cycle arrest or apoptosis,”biochem biophys res co mmun.300(1):230
‑
235(2003);
108
gadd et al.,“acetaminophen
‑
induced proliferation of estrogen
‑
responsive breast cancer cells is associated with increases in c
‑
myc rna expression and nf
‑
kappab activity,”t oxicol sci.66(2):233
‑
243(2002);
109
galli et al.,“the effect of alpha
‑
and gamma
‑
tocopherol and their carboxyethyl hydroxychroman meta bolites on prostate cancer cell proliferation,”arch biochem biophys.423(1):97
‑
102(2004);
110
siitonen et al,“the effect of alpha
‑
and gam ma
‑
tocopherol and their carboxyethyl hydroxychroman metabolites o n prostate cancer cell proliferation,”leuk res.29(11):1335
‑
1342(2005);
111
van poznak et al.,“oral gossypol in the treatment of patients with refractory metastatic breast cancer:a phase i/ii clinical trial,”b reast cancer res treat.66(3):239
‑
48(2001);
112
costea et al.,“the inf luence of cyclin d1(ccnd1)870a>g polymorphism and ccnd1
‑
thymidylate synthase(ts)gene
‑
gene interaction on the outcome of childhood acute lymphoblastic leukaemia,”pharmacogenetics.13(9):577
‑
580(2003);
113
saitoh et al.,“medroxyprogesterone acetate induces cell proliferation through up
‑
regulation of cyclin d1 expression via phosphatidylinositol 3
‑
kinase/akt/nuclear factor
‑
kappab cascade in hu man breast cancer cells,”endocrinology.146(11):4917
‑
4925(2005);
114
boutillier et al.,“depolarization regulates cyclin d1 degradation and neuronal apoptosis:a hypothesis about the role of the ubiquitin/pro teasome signalling pathway,”eur j neurosci.11(2):441
‑
448(1999);
115
han et al.,“cyclin d1 expression and patient outcome after tamoxi fen therapy in estrogen receptor positive metastatic breast cancer,”o ncol rep.10(1):141
‑
144(2003);
116
sharma et al.,“peroxisome prolifer ator
‑
activated receptor gamma activation modulates cyclin d1 transcr iption via beta
‑
catenin
‑
independent and camp
‑
response element
‑
bindi ng protein
‑
dependent pathways in mouse hepatocytes,”j biol chem.279(17):16927
‑
16938(2004);
117
ogawa et al.,“aberrant expression of p27(kip1)is associated with malignant transformation of the rat uri nary bladder epithelium,”carcinogenesis.21(1):117
‑
121(2000);
118
yu et al.,“absence of cyclin d2 expression is associated with promote r hypermethylation in gastric cancer,”br j cancer.88(10):1560
‑
1565(2003);
119
wyss et al.,“mitochondrial creatine kinase from chicken b rain.purification,biophysical characterization,and generation of hete rodimeric and heterooctameric molecules with subunits of other crea tine kinase isoenzymes,”j biol chem.265
133(2):250
‑
264(2008),所述文献据此通过引用整体并入。
[0149]
可将上述ipsc产生方法修改成包括提高重编程效率或甚至替代重编程因子的小分子。这些小分子包括但不限于表观遗传调节剂,诸如dna甲基转移酶抑制剂5
’‑
氮杂胞苷、组蛋白去乙酰化酶抑制剂vpa,及g9a组蛋白甲基转移酶抑制剂bix
‑
01294以及bayk8644(一种l型钙通道激动剂)。其它小分子重编程因子包括靶向信号转导途径的那些,诸如tgf
‑
β抑制剂和激酶抑制剂(例如,肯保隆(kenpaullone))(参见sommer和mostoslavsky的综述,“experimental approaches for the generation of induced pluripotent stem cells,”stem cell res.ther.1:26doi:10.1186/scrt26(2010年8月10日),其据此通过引用整体并入)。
[0150]
获得适合于本文所述方法的来自ipsc的高度富集的胶质祖细胞制品的方法公开于goldman和wang的wo2014/124087以及wang等人,“human ipsc
‑
derived oligodendrocyte progenitors can myelinate and rescue a mouse model of congenital hypomyelination,”cell stem cell 12(2):252
‑
264(2013),所述文献据此通过引用整体并入。
[0151]
在另一个实施方案中,人胶质祖细胞源自胚胎干细胞。人胚胎干细胞提供了潜在地可用于组织替代疗法的几乎无限的克隆/遗传修饰细胞来源。获得适合于在本公开的方法中使用的来自胚胎细胞的高度富集的胶质祖细胞制品的方法描述于wang等人,“human ipsc
‑
derived oligodendrocyte progenitor cells can myelinate and rescue a mouse model of congenital hypomyelination,”cell stem cell 12:252
‑
264(2013)(其据此通过引用整体并入)中。
[0152]
在另一个实施方案中,人胶质祖细胞源自人胎儿组织。胶质祖细胞可通过使用如goldman的美国专利申请公布第20040029269号和20030223972号中所描述的启动子特异性分离技术直接从含有混合细胞群的胎儿脑组织中提取,所述专利申请公布据此通过引用整体并入。这种方法涉及选择在胶质祖细胞中特异地发挥功能的启动子,并将在所述启动子控制下编码标志物蛋白的核酸引入到混合细胞群中。使所述混合细胞群表达标志物蛋白,并将表达标志物蛋白的细胞从细胞群中分离出来,经分离的细胞是胶质祖细胞。人胶质祖细胞可以从脑的脑室或脑室下区,或者从皮质下白质中分离出来。
[0153]
可用于从混合细胞群中分离胶质祖细胞的胶质特异性启动子包括cnp启动子(scherer等人,neuron 12:1363
‑
75(1994),其据此通过引用整体并入本文)、ncam启动子(holst等人,j.biol.chem.269:22245
‑
52(1994),其据此通过引用整体并入本文)、髓鞘碱性蛋白启动子(wrabetz等人,j.neurosci.res.36:455
‑
71(1993),其据此通过引用整体并入本文)、jc病毒最小核心启动子(krebs等人,j.virol.69:2434
‑
42(1995),其据此通过引用整体并入本文)、与髓鞘相关联的糖蛋白启动子(laszkiewicz等人,“structural characterization of myelin
‑
associated glycoprotein gene core promoter,”j.res.50(6):928
‑
36(1997),其据此通过引用整体并入本文),或蛋白脂质蛋白启动子(cook等人,“regulation of rodent myelin proteolipid protein gene expression,”neurosci.lett.137(1):56
‑
60(1992);wight等人,“regulation of murine myelin proteolipid protein gene expression,”j.neurosci.res.50(6):917
‑
27(1997);以及cambi等人,neurochem.res.19:1055
‑
60(1994),其据此通过引用整体并入本文)。还参见,
human glial progenitor cells can both remyelinate and rescue the otherwise lethally hypomyelinated shiverer mouse,”cell stem cell 2:553
‑
565(2008),所述文献据此通过引用整体并入。
[0156]
根据本文所述的方法,选定的施用的人胶质祖细胞的制品包含至少约80%的胶质祖细胞,包括例如约80%、85%、90%、95%、96%、97%、98%、99%、100%的胶质祖细胞。选定的胶质祖细胞的制品可以相对缺乏(例如,含有少于20%、15%、10%、9%、8%、7%、6%、5%、4%、3%、2%或1%)的其它细胞类型,诸如神经元或神经元谱系细胞、纤维性星形细胞和纤维性星形细胞谱系细胞,以及多能干细胞(如es细胞)。任选地,示例性细胞群是实质上纯的胶质祖细胞群。
[0157]
所施用的制品的胶质祖细胞可以任选地被遗传修饰成表达其它目标蛋白质。例如,胶质祖细胞可被修饰成表达治疗性生物分子、外源性靶向部分、外源性标志物(例如,用于成像目的)等。所述制品的胶质祖细胞可以任选地被修饰成过表达内源性生物分子、靶向部分和/或标志物。
[0158]
所施用的制品的胶质祖细胞可以是星形细胞偏向的胶质祖细胞、少突细胞偏向的胶质祖细胞、无偏向的胶质祖细胞或其组合。所施用的制品的胶质祖细胞表达胶质细胞谱系的一种或多种标志物。例如,在一个实施方案中,所施用的制品的胶质祖细胞可以表达a2b5
+
。在另一个实施方案中,所施用的制品的胶质祖细胞对pdgfαr标志物呈阳性。pdgfαr标志物任选地是pdgfαr胞外结构域,诸如cd140a。pdgfαr和cd140a是少突细胞偏向的胶质祖细胞的标志物。在另一个实施方案中,所施用的制品的胶质祖细胞是cd44
+
。cd44是星形细胞偏向的胶质祖细胞的标志物。在另一个实施方案中,所施用的制品的胶质祖细胞对cd9标志物呈阳性。cd9标志物任选地是cd9胞外结构域。在一个实施方案中,所述制品的胶质祖细胞是a2b5
+
、d140a
+
和/或cd44
+
。前述胶质祖细胞表面标志物可用于在施用前鉴定、分离和/或富集胶质祖细胞的制品。
[0159]
所施用的胶质祖细胞制品任选地对psa
‑
ncam标志物和/或其它神经元谱系标志物呈阴性,并且/或者对一种或多种炎性细胞标志物呈阴性,例如对cd11标志物呈阴性,对cd32标志物呈阴性,并且/或者对cd36标志物呈阴性(所述cd36标志物是小胶质细胞的标志物)。任选地,胶质祖细胞的制品对这些额外的标志物的任何组合或子集呈阴性。因此,例如,胶质祖细胞的制品对这些额外的标志物中的任一个、两个、三个或四个呈阴性。
[0160]
将细胞引入到受试者的纹状体、前脑、脑干和/或小脑中的合适方法是本领域技术人员熟知的,包括但不限于如本文所述的注射、沉积和植入。
[0161]
在一个实施方案中,胶质祖细胞如以下文献中所述的那样从双侧被移植到受试者的多个部位中:goldman,windrem等人的美国专利第7,524,491号,“neonatal chimerization with human glial progenitor cells can both remyelinate and rescue the otherwise lethally hypomyelinated shiverer mouse,”cell stem cell 2:553
‑
565(2008),han等人,“forebrain engraftment by human glial progenitor cells enhances synaptic plasticity and learning adult mice,”cell stem cell 12:342
‑
353(2013),and wang等人,“human ipscs
‑
derived oligodendrocyte progenitor cells can myelinate and rescue a mouse model of congenital hypomyelination,”cell stem cell 12:252
‑
264(2013),其据此通过引用以其全文并入)。用于将神经组织和
细胞移植到宿主脑中的方法描述于bjorklund和stenevi(编辑),neural grafting in the mammalian cns,ch.3
‑
8,elsevier,amsterdam(1985);gage等人的美国专利第5,082,670号;以及weiss等人的美国专利第6,497,872号中(所述文献据此通过引用整体并入本文)。典型的程序包括实质内、胼胝体内、脑室内、鞘内和静脉内移植。
[0162]
实质内移植是通过在宿主脑中注射或沉积组织以使其在移植时与脑实质贴合(apposed)来实现的。实质内移植的两个主要程序是:1)将供体细胞注射到宿主脑实质内,或者2)通过外科方式制备空腔以暴露宿主脑实质,然后将植入物沉积到空腔内((bjorklund和stenevi(编辑),neural grafting in the mammalian cns,ch.3,elsevier,amsterdam(1985),其据此通过引用整体并入)。这两种方法都使得植入时供体细胞与宿主脑组织之间实质贴合,并且两者都促进植入物与宿主脑组织之间的解剖整合。如果要求供体细胞成为宿主脑的不可分割的部分并在宿主的一生中存活,这一点非常重要。
[0163]
胶质祖细胞也可以如goldman的美国专利申请公布第20030223972号(其据此通过引用整体并入)中所述的那样在胼胝体内递送。胶质祖细胞还可被直接递送至前脑皮层下部,特别是胼胝体的前部和后部原基(anlagen)中。胶质祖细胞也可被递送到小脑脚白质(cerebellar peduncle white matter)上,以进入主要的小脑和脑干束。胶质祖细胞还可被递送至脊髓。
[0164]
替代地,可将该细胞置于室中,例如大脑室(cerebral ventricle)中。将细胞植入到室中可以通过以下方式来实现:注射供体细胞,或者使该细胞在基底诸如30%胶原中生长以形成固体组织塞,然后可将该固体组织塞植入到室中以防止植入细胞脱位。对于硬膜下植入,可在硬膜中开一个狭缝后将细胞注射到脑表面周围。
[0165]
胶质细胞递送的合适技术如上文所描述。在一个实施方案中,向受试者的纹状体、前脑、脑干和/或小脑施用所述胶质祖细胞制品。
[0166]
细胞向受试者的递送可包括直接注射到神经系统中的单步或多步注射。虽然成人和胎儿少突细胞前体细胞在移植受者的脑中广泛分布,但对于广泛的病症,可对多个注射部位进行注射以优化治疗。任选地直接注射到中枢神经系统的区域,诸如白质束如胼胝体(例如,注射到前部和后部原基中)、背柱(dorsal column)、小脑脚、大脑脚中。此类注射可使用精确的定位方法(诸如立体定位手术),任选地利用伴随的成像方法(例如,高分辨率mri成像)来从单侧或双侧进行。本领域技术人员认识到脑区域因物种的不同而有所变化;然而,本领域技术人员也认识到整个哺乳动物物种的脑区域是类似的(comparable)。
[0167]
细胞移植物任选地作为解离细胞来注射,但也可通过非离解细胞的局部放置来提供。在任一情况下,细胞移植物均任选地包含可接受的溶液。此类可接受的溶液包括避免不期望的生物活性和污染的溶液。合适的溶液包括适量的用于使制剂等渗的药学上可接受的盐。药学上可接受的溶液的实例包括但不限于盐水、林格氏溶液、右旋糖溶液和培养基。所述溶液的ph优选为约5至约8,更优选为约7至约7.5。
[0168]
离解的细胞移植物的注射可以是穿过注射装置(例如,套管、针或管)的入口路径、出口路径,或者入口和出口路径两者进行的流式注射(streaming injection)。可利用自动化来提供统一的进入和出口速度以及注射速度和体积。
[0169]
根据受者的大小和物种以及需要细胞替换的组织的体积,施用给受试者的胶质祖细胞的数量在每次施用(例如,注射部位)时可在约102‑
108的范围内。单次施用(例如,注射)
剂量可跨越103‑
105个、104‑
107个和105‑
108个细胞的范围,或用于移植物接受患者的任何总量。
[0170]
由于cns是免疫豁免部位(immunologically privileged site),因此包括异种细胞在内的所施用的细胞可以存活,并且任选地,在治疗方法中不使用免疫压制药物或典型的免疫压制剂方案。然而,任选地,也可向受试者施用免疫压制剂。免疫压制剂及其给药方案是本领域技术人员已知的,包括诸如硫唑嘌呤(azathioprine)、硫唑嘌呤钠、环孢菌素、达曲班(daltroban)、三盐酸胍立莫司(gusperimus trihydrochloride)、西罗莫司和他克莫司之类的剂。所述方案的剂量范围和持续时间可以根据以下方面而变化:所治疗的病症;排斥的程度;所采用的特定免疫压制剂的活性;受试者的年龄、体重、一般健康状况、性别和饮食;施用时间;施用途径;所采用的特定免疫压制剂的排泄速率;治疗的持续时间和频率;以及组合使用的药物。本领域技术人员可以确定免疫压制的可接受剂量和持续时间。在出现任何禁忌症或受试者状态发生变化的情况下,个体医生可以调整剂量方案。
[0171]
实施例
[0172]
下面的实施例旨在举例说明本公开的实施方案的实践,但绝不旨在限制其范围。
[0173]
用于实施例的材料和方法
[0174]
从人胚胎干细胞(hesc)生产gpc。使用先前描述的方案(wang等人,“human ipsc
‑
derived oligodendrocyte progenitor cells can myelinate and rescue a mouse model of congenital hypomyelination,”cell stem cell 12:252
‑
264(2013);windrem等人,“human ipsc glial mouse chimeras reveal glial contributions to schizophrenia,”cell stem cell 21:195
‑
208(2017),其据此通过引用整体并入)从人胚胎干细胞(esc)产生gpc,该方案在wang等人,“human ipsc
‑
derived oligodendrocyte progenitor cells can myelinate and rescue a mouse model of congenital hypomyelination,”cell stem cell 12:252
‑
264(2013)(其据此通过引用整体并入)中以非常详细的方法学进行了概述。在160与240之间收获细胞,此时大多数细胞通常表达双电位gpc标志物cd140a,而其余细胞主要由a2b5
+
/cd140a
‑
未成熟星形细胞组成。未检测到表达ssea4的细胞。人es细胞是从genea,inc.(sydney,australia)以以下形式获得的:genea02系和genea19系(正常htt:15/18cag)和genea 17、18和20(mhtt:分别为40/12、46/17和48/17cag)(bradley等人,“derivation of huntington's disease
‑
affected human embryonic stem cell lines,”stem cells dev 20:495
‑
502(2011),其据此通过引用整体并入)。genea02和17是男性的,而genea18、19和20是女性的。值得注意的是,genea 19和20是作为一对女性同胞姐妹(一位正常,一位患有hd)捐赠和衍生的。c27对照系是男性的。
[0175]
宿主。将纯合的颤抖小鼠(the jackson laboratory,bar harbor,me)与纯合的rag2基因敲除(null)免疫缺乏小鼠(shinkai等人,“rag
‑2‑
deficient mice lack mature lymphocytes owing to inability to inititate v(d)j rearrangement,”cell 68:855
‑
867(1992),其据此通过引用整体并入)在c3h本底(background)(taconic,germantown,ny,usa)上杂交,以产生shi/shi x rag2
‑
/
‑
髓鞘缺乏的免疫缺乏小鼠(windrem等人,“neonatal chimerization with human glial progenitor cells can both remyelinate and rescue the otherwise lethally hypomyelinated shiverer mouse,”cell stem cell 2:553
‑
565(2008),其据此通过引用整体并入)。将小鼠按照12:12小时光周期维持在置于无
病原体的栖息室内的温度和湿度受控的壳体(64
‑
79℉;30%
–
70%湿度)中。使它们随意摄取含有0.025%甲氧苄啶(trimethoprim)/0.124%磺胺甲氧基唑(sulfamethoxyzole)和经高压灭菌的酸性水(ph 2.5
‑
3.0)的mod labdiet 5p00。
[0176]
将单细胞或小簇的hesc来源的gpc的混悬液离心沉降至100,000个细胞/ml。通过冷却对新生动物进行麻醉,并如(windrem等人,“fetal and adult human oligodendrocyte progenitor cell isolates myelinate the congenitally dysmyelinated brain,”nat.med.10:93
‑
97(2004),其据此通过引用整体并入)中所述的那样在胼胝体中从双侧给该新生动物移植总共200,000个细胞。在8周龄、12
‑
13周龄或18周龄时,将经移植的小鼠用戊巴比妥麻醉,然后用冷hbss灌注固定,接着用4%多聚甲醛灌注固定。取出脑,并在冷的多聚甲醛中后固定2小时。
[0177]
所有程序均已根据协议2004
‑
129由university of rochester动物资源委员会(ucar)批准。
[0178]
用于移植的细胞制品。注射前,执行流式细胞术以确认cd140a在每种培养物中占优势。然后从孔中收集悬浮的细胞丛簇,离心,并将其重新悬浮在小体积的不含ca
2+
/mg
2+
‑
的hbss中。将重悬的细胞丛簇转移到100mm的细胞培养皿中,然后用11号手术刀切割以获得直径为100
‑
200mm的断片。然后收集这些碎片,离心,用不含ca
2+
/mg
2+
的hbss洗涤,并在不含ca2+/mg2+的hbss中重悬浮至近似105个细胞/ml的浓度。
[0179]
移植。在出生后第1天或第2天对颤抖x rag2基因敲除新生小鼠进行移植。将一窝幼崽的一半从母兽(dam)身边移出,并放入加湿的加热室中。为此,使用内衬为用汉克斯平衡盐溶液浸湿的无菌纱布并在加热块上加热的无菌塑料盒。然后用聚维酮碘擦拭待注射的幼崽,并将幼崽用无菌纱布包裹以防止与冰直接接触,然后根据尺寸冷冻麻醉2至6分钟。然后将幼崽从冰上取出,用酒精棉片(alcohol prep pad)清洁,然后放入由烘焙的模制粘土制成的定制新生小鼠夹持器(mouse holder)中。将幼崽直接通过皮肤和颅骨样骨注射到吻侧(rostral)(ap+1.0mm;ml
±
1.0mm,腹侧1.0mm)和尾侧(ap
‑
1.0,ml
±
1.0mm,腹侧0.9mm)胼胝体中。注射后,用酒精棉片清洁幼崽,并将其放回加温室进行恢复。恢复后,将一窝幼崽的第一个一半送回给母兽,而将第二个一半放入加湿室中。幼崽在21至28天之间断奶,然后分组圈养。
[0180]
组织切片的免疫标记。将脑冷冻保存,包埋在oct(tissue
‑
tek oct,sakura finetek,torrance,ca)中,并在低温恒温器上以20mm进行矢状或冠状切片。用小鼠抗人细胞核(克隆235
‑
1,1:800)(mab1281;emd millipore,billerica,ma)鉴定人细胞。以1:25用mbp大鼠抗mbp(ab7349;abcam,cambridge,ma)标记少突细胞,用抗人特异性gfapf(以1:1000的smi 21,covance,princeton,nj)标记星形细胞,以及以1:5000(smi
‑
311)或1:1000(smi
‑
312;covance,princeton,nj)用小鼠抗神经丝标记轴突。以1:400使用alexa fluor二抗,山羊抗小鼠和抗大鼠488、568、594和647(life technologies,carlsbad,ca)。
[0181]
使用的抗体和稀释液。
[0182]
表5
–
关键来源
[0183]
[0184]
[0185]
[0186]
[0187]
[0188][0189]
rna
‑
seq。首先使用facs aria iiiu(becton dickinson)如(sim等人,“cd140a identifies a population of highly myelinogenic,migration
‑
competent and efficiently engrafting human oligodendrocyte progenitor cells,”nat.biotechnol.29:934
‑
941(2011),其据此通过引用整体并入)所描述的那样,根据细胞表面标志物cd140a(bd pharmingen)通过荧光激活细胞分选术对就基因表达进行了评估的hgpc进行分选(图3)。通过polya
‑
选择方案从由源自3名hd患者(被指定为hd系17[n=5个独立细胞集合制品)、18[n=5]和20[n=6])和2名健康对照(被指定为ctr系02[n=6]和19[n=6],hd20的同胞)的人胚胎干细胞(es)产生的经facs
‑
分选的pdgfra阳性gpc系中分离出mrna。用illumina truseq rna v2试剂盒制备测序文库,并在illumina hiseq2500测序仪上对测序文库进行测序,对于所有细胞系(对照ctr02系除外,其测序深度相似,但以125bp的成对端读段模式进行),每个样品产生约4500万个100bp的单端读段。然后使用trimmomatic(bolger等人,“trimmomatic:a flexible trimmer for illumina sequence data,”bioinformatics 30:2114
‑
2120(2014),其据此通过引用整体并入),通过修剪掉衔接子和低质量序列来预处理测序数据。用fastqc评估预处理前后的读段质量。然后利用subread读段比对器(liao等人,“the subread aligner:fast,accurate and scalable read mapping by seed
‑
and
‑
vote,”nucleic acids res.41:e108(2013),其据此通过引用整体并入)将经预处理的读段与refseq ncbi参考人基因组版本grch38(pruitt等人,“ncbi reference sequences(refseq):a curated non
‑
redundant sequence database of genomes,transcripts and proteins,”nucleic acids res.35:d61
‑
d65(2007),其据此通过引用整体并入)进行比对。利用featurecounts(liao等人,“featurecounts:an efficient general purpose program for assigning sequence reads to genomic features,”bioinformatics 30:923
‑
930(2014),其据此通过引用整体并入)从bam比对文件获得原始基因计数。
[0190]
髓鞘形成的sox10/myrf拯救。对于该组实验,将sox10和myrf转录物克隆在两个独立的慢病毒载体:ptank
‑
tre
‑
myrf
‑
cag
‑
rtta3g
‑
wpre和ptank
‑
tre
‑
sox10
‑
p2a
‑
dc4
‑
wpre
中。在这种tet
‑
on系统中,选择性标记cd4的细胞表面表达需要来自这两种病毒的表达,从而确保myrf和sox10转基因的共表达。产生用水泡性口炎病毒g糖蛋白假型化的病毒颗粒,将其通过超速离心浓缩,并在293hek细胞上滴定。在胶质培养基中以1.0moi感染g20hgpc培养物。用hbss洗涤细胞,并将其在补充有1mg/ml dox(millipore
‑
sigma st.louis,mo)的胶质培养基中维持4天。然后如(windrem等人,“neonatal chimerization with human glial progenitor cells can both remyelinate and rescue the otherwise lethally hypomyelinated shiverer mouse,”cell stem cell 2:553
‑
565(2008),其据此通过引用整体并入),使用macs(miltenyi,germany)所描述的那样选择hgpc以进行cd4的膜表达。
[0191]
在体外对少突细胞分化的拯救。让macs分离的cd4+细胞在胶质培养基中附着过夜(wang等人,“human ipsc
‑
derived oligodendrocyte progenitor cells can myelinate and rescue a mouse model of congenital hypomyelination,”cell stem cell 12:252
‑
264(2013),其据此通过引用整体并入)。在整个分化诱导过程中,将dox维持在过表达状态下。第二天,将细胞在hbss洗涤一次,并转换到分化培养基(神经基础培养基(neurobasal medium)(gibco)、1x n2(thermo fisher)、1x b27(thermo fisher)、1x glutamax(thermo fisher)、20ng/ml bdnf(r&d systems)、0.2mm l
‑
抗坏血酸(sigma)、60ng/ml t3(sigma)、0.2mm二丁酰环amp(sigma)、100ng/ml生物素(sigma)、1x胰岛素
‑
转铁蛋白
‑
硒(thermofisher)、10ng/ml nt3(r&d)和100ng/ml igf1(r&d)中。固定前每隔一天更换培养基,持续2周。通过o4免疫染色定量少突细胞分化。
[0192]
在体外对少突细胞分化的拯救。制备用于移植的细胞,然后将其在单侧的两个部位注射到新生颤抖小鼠的胼胝体中。从9周龄开始,给一半的经移植的小鼠施用dox(2mg/ml,含有含5%蔗糖的水(chow等人,“a doxycycline
‑
inducible,tissue
‑
specific aromatase
‑
expressing transgenic mouse,”transgenic res.21:415
‑
428(2012),其据此通过引用整体并入))或它们的水瓶中的正常饮用水5周。然后在13周龄时处死对照小鼠和实验小鼠,并对其进行准备以针对mbp和人核抗原进行免疫标记,然后通过共聚焦成像来评估如上所述的表达mbp的少突细胞的轴突包鞘。
[0193]
成像和定量组织学。为了绘制人细胞核的分布图,在配备有nikon digital sight照相机ds
‑
fi1的nikon instruments ni
‑
e上对切片进行成像,并在nikon nis elements v4.5中进行计数评分。为了在低功率下拍摄髓鞘的分布,在leica lmd 6500上对整个脑切片进行成像。使用nikon c2+共聚焦获得髓鞘包鞘的更高功率共聚焦图像,并且使用100倍物镜,使用0.2mm步长获取图像。使用由stereo investigator软件(mbf,williston,vt)驱动的hammamatsu相机,在olympus bx51上对细胞类型特异性标志物进行成像。使用leica sp8共聚焦获取经受sholl分析的星形细胞的更高放大倍率的共聚焦堆栈(higher magnification confocal stack)。
[0194]
细胞计数。胼胝体中供体细胞密度的定量是基于中线外侧1mm的计数。针对人细胞核、dapi和其它表型特异性标志物(olig2、hgfap、tf和mbp)对随机启动的、均匀采样的脑冠状切片进行标记。对于olig2和hgfap定量,使用配备有hamamatsu相机的olympus bx51以40倍对每个切片的目标区域成像。z堆栈以1mm的步长获得。对于tf和mbp的定量,使用配备有ds
‑
fi1照相机的nikon ni
‑
e eclipse显微镜以20倍对目标区域成像。z堆栈以0.7
‑
1mm的步长获得。在nikon nis elements v.4.5中,使用z堆栈图像在每只小鼠的三个均匀间隔的冠
状切片上的高强度投影来计数免疫标记的细胞。
[0195]
星形细胞的形态测量。将颤抖x rag2基因敲除小鼠在18周龄时处死,评估它们的白质星形细胞形态。通过振动切片机(vibratome)从植入了对照(genea19)或hd(genea20)hgpc的小鼠的前囟
‑
1.0mm处获取150mm厚的冠状切片,将所述切片在4℃下于小鼠抗hgfap中孵育1周,然后在alexa 568山羊抗小鼠抗血清中孵育4小时。将切片安装在载玻片上,并通过共聚焦(leica sp8)以100倍成像。使用neurolucida 360(microbright field,inc.)追踪图像;所有的追踪都是由对治疗条件不知情的实验者完成的。
[0196]
从胼胝体中部在中间深度处选取单个星形细胞,以便完整地捕获细胞及其突起(process)。在中线500mm、1000mm和1500mm外侧取3个细胞/切片和3个切片/脑,通过neurolucida用sholl分析对细胞进行分析。评估了总共14个经受新生期植入的脑(genea18,n=21个细胞/3个脑;genea19,32个细胞/4个脑;genea20,42个细胞/7个脑),产生63个追踪的mhtt星形细胞(genea18来源的和genea20来源的),和32个对照(genea19)星形细胞。对于sholl分析,将直径依次增加5mm的同心壳置于细胞体的中心,并计算细胞突起与壳之间的交叉数量(sholl,“dendritic organization in the neurons of the visual and motor cortices of the cat,”j.anat.87:387
‑
406(1953),其据此通过引用整体并入)。对于星形细胞纤维3d结构的评估和定量描述,如先前针对树枝状拓扑研究(dang等人,“formoterol,a long
‑
actingβ2adrenergic agonist,improves cogntive function and promotes dendritic complexity in a mouse model of down syndrome,”biol.psychiatry 75:179
‑
188(2014),其据此通过引用整体并入)所述的那样使用扇入分析(mbf biosciences)。
[0197]
髓鞘亮度分析。为了测量前脑髓鞘形成,使用了基于mbp免疫荧光测量的亮度分析。如所描述的那样对均匀间隔和均匀采样的冠状切片进行mbp染色,并使用nikon ni
‑
e和nikon ds
‑
fi1照相机以10倍拍摄图像。选择胼胝体作为目标区域,并使用nis elements v.4.5获得平均强度值。
[0198]
组织学数据的统计分析。所有分析均利用v.7(graphpad软件)使用双向anova和bonferroni事后t检验进行。当p
‑
值小于0.05时,认为具有统计显著性。显著性表示为*p<0.05,**p<0.01以及***p<0.001。用prism 7制作和组装图表和图形,所有数据均以平均值(sem)
±
平均值的标准误差示出。
[0199]
生物信息学。在检查了用本机r函数(native r functions)(r core team,“r:a language and environment for statistical computing,”r foundation for statistical computing(2014),其据此通过引用整体并入)生成的主成分和层次聚类图后,从hd17系(genea17)的分析中移除了一个错误聚类的离群样品,也在hd20系(genea20)和ctr19系(genea19)中移除了2个离群值。在消除低表达的转录物后,留下那些在多于3个样品中具有至少5个读段的计数的转录物,计数数据使用ruvseq(risso等人,“normalization of rna
‑
seq data using factor analysis of control genes or samples,”nat.biotechnol.32:896
‑
902(2014),其据此通过引用整体并入)进行归一化。使用r生物导体包(gentleman等人,“bioconductor:open software development for computational biology and bioinformatics,”genome biol.5:r80(2004),其据此通过引用整体并入))说明差异。如ruvseq文献资料中所述的那样,归一化是通过以下三步程序
完成的:1)通过利用edger(robinson等人,“edger:a bioconductor package for differential expression analysis of digital gene expression data,”bioinformatics 26:139
‑
140(2010),其据此通过引用整体并入)和deseq2(love等人,“moderated estimation of fold change and dispersion for rna
‑
seq data with deseq2,”genome biol.15:550(2014),其据此通过引用整体并入)r生物导体包进行首过差异表达分析(first
‑
pass differential expression analysis)来确定阴性的经电脑模拟的对照基因,包括如通过这两种方法计算的经fdr调控的p值>0.75的那些基因;2)然后在ruvseq的ruvg函数中使用阴性的经电脑模拟的对照基因来计算方差因子;以及3)使用最初的原始计数并通过在edger和deseq2包中实现的多因子glm模型调整ruvg计算的方差因子,如此执行二过差异表达分析(second
‑
pass differential expression analysis)(1%fdr和log2倍数变化>1),以确定疾病失调基因。
[0200]
这种滤除了低表达和非表达的转录物的三步分析用于对每个hd来源的hgpc细胞系与汇集的ctr来源的hgpc进行比较,以及用于hd20与hd19的同胞对比较。在所有比较中,使用了一个ruvg计算的方差因子。所得的四个差异表达基因列表的交集被视为hd
‑
失调基因的保守代表性列表。为了获得所有三个hd来源的gpc系中失调基因的平均fc和p值,通过相同的工作流程和相同数量的方差因子对汇集的hd系和汇集的ctr系执行差异表达比较。
[0201]
对于所有差异表达的比较,在下游分析中仅使用了在edger与deseq2之间一致的显著结果。结果中报告的倍数变化和经fdr调整的p值是通过edger计算的。使用topcluster(kaimal等人,“toppcluster:a multiple gene list feature analyzer for comparative enrichment clustering and network
‑
based dissection of biological systems,”nucleic acids res.38:w96
‑
w102(2010),其据此通过引用整体并入)和独创性途径分析(ingenuity pathway analysis)(ipa)(qiagen)(kramer等人,“causal analysis approaches in ingenuity pathway analysis,”bioinformatics 30:523
‑
530(2014),其据此通过引用整体并入)对一组保守的hd失调基因进行功能注释。
[0202]
用于基因表达验证的taqman rt
‑
qpcr阵列。使用基于ribo
‑
spia基全转录组的扩增(nugen)对提取的总rna进行扩增。使用48
‑
基因taqman低密度阵列(tlda(applied biosystems),通过实时聚合酶链反应(rt
‑
pcr)评估细胞类型标志物和途径特异性基因的表达。通过ddct分析来计算转录物表达的相对丰度,并将表达数据针对作为内源对照的18s和gapdh的平均值作归一化。通过配对t检验,并随后通过用benjamini
‑
hochberg(bh)程序(benjamini和hochberg,“controlling the false discovery rate:a practical and powerful approach to multiple testing,”j.r.stat.soc.series b stat.methodol.57:289
‑
300(1995),其据此通过引用整体并入)进行多重检验校正来评估在hd和对照gpc中表达的差异。tlda数据的分析在applied biosciences提供的expressionsuite软件1.1版中执行。
[0203]
髓鞘生成基因表达的sox10/myrf拯救。用在组成型启动子ef1α(ptank
‑
ef1α
‑
sox10
‑
p2a
‑
myrf
–
t2a
‑
egfp
‑
wpre)的调控控制下表达串联的sox10和myrf的质粒,或仅表达egfp(ptank
‑
ef1α
‑
egfp
‑
wpre)的对照质粒转染mhtt和正常同胞hesc来源的hgpc。按照制造商的方案使用核转染剂(lonza,germany)使用ca205转染程序在p3缓冲液中执行转染。转染后72小时收集细胞,用于潜在的sox10和myrf靶基因的rt
‑
qpcr。使用qiagen rneasy micro
list feature analyzer for comparative enrichment clustering and network
‑
based dissection of biological systems,”nucleic acids res.38:w96
‑
w102(2010),其据此通过引用整体并入)。注释结果通过toppcluster的网络生成器导出,作为表示网络边缘的术语
‑
基因关联列表。对于所有随后的网络可视化和分析,将术语
‑
基因关联网络输入到gephi图形可视化软件(jacomy等人,“forceatlas2,a continuous graph layout algorithm for handy network visualization designed for the gephi software,”plos one 9:e98679(2014),其据此通过引用整体并入)中。计算基本节点中心度度量和节点度,并使用默认参数利用force atlas布局来排列网络。对于cd140a来源的注释网络使用1.3的随机化和分辨率参数,对于cd44来源的注释网络使用2.0的随机化和分辨率参数,利用内置的社区检测算法(blondel等人,“fast unfolding of communities in large networks,”arxiv arxiv:0803.0476(2008),其据此通过引用整体并入)确定紧密互连的节点模块,以便优化社区的分组和数量。
[0210]
实施例1
–
mhtt opc下调胶质谱系进展的转录决定子
[0211]
为了解决胶质转录异常在hd发病机制中的作用,首次评估了源自亨廷顿蛋白突变型hesc的双潜能hgpc的差异基因表达。为此,制取并纯化从表达mhtt的胚泡获得的三个不同的hesc系(genea17、genea18和genea20;genea biocells)以及两个对照系(genea02和genea19)的gpc(bradley等人,“derivation of huntington's disease
‑
affected human embryonic stem cell lines,”stem cells dev 20:495
‑
502(2011),其据此通过引用整体并入)。使用先前描述的方法(wang等人,“cd133/cd140a
‑
based isolation of distinct human multipotent neural progenitor cells and oligodendrocyte progenitor cells,”stem cells and development 22:2121
‑
2131(2013),其据此通过引用整体并入)从hesc制取gpc,然后使用基于cd140a的facs分离所得到的gpc级分(>99%cd140a
+
)(sim等人,“cd140a identifies a population of highly myelinogenic,migration
‑
competent and efficiently engrafting human oligodendrocyte progenitor cells,”nature biotechnology 29:934
‑
941(2011),其据此通过引用整体并入)。重要的是,对照之一(genea19;18cag)是表达mhtt的系中的一个(genea20;48cag)的同胞;这些由同一双亲捐赠的系是异卵女性双胞胎。
[0212]
在分别为190
±
16天和174
±
14天的平均繁殖时间后,收获mhtt和对照hgpc作为稳定扩增的hgpc。流式细胞术揭示54%
±
3.4%的正常细胞(genea02和genea19;n=12次培养运行)和44%
±
3.3%的亨廷顿蛋白突变细胞(genea17、18和20;n=16)在这些时间点表达cd140a(平均值
±
sem)。然后通过facs将每种培养物的cd140a级分分离至接近纯净,并使用illumina hiseq 2500测序仪执行rna
‑
seq,所述rna
‑
seq显示,相对于汇集的对照hesc gpc,源自三个hd系的hgpc中存在严重的转录失调。主成分分析(pca)显示,表达mhtt的hgpc和对照hgpc明显分离(图1a)。作为一个组,使用2倍变化(fc)截止值和1%的假发现率(fdr),相对于对照,mhtt hgpc中有239个基因上调,530个基因下调(图1b)。为了进一步完善差异表达的基因的结果列表,然后将genea20(mhtt)来源的hgpc的差异表达与其同胞genea19
‑
来源的对照进行比较,并将该同胞比较添加到总体比较中;这充当了额外的过滤器,并产生了更紧密的差异表达的基因列表,该基因列表由源自所有hd来源的hgpc细胞系的hgpc中相对于汇集的对照hgpc的64个上调的基因和365个下调的基因组成(图1b和1c)。
[0213]
使用这种基因集合,使用来自基因本体(go)的注释执行功能分析,通过该功能分析,我们鉴定出了50个显著相关联的go注释术语(bonferroni校正的p<0.01,在生物学过程和细胞成分go域的术语中),其代表了429个差异调控的基因中的187个(图2和图3a
‑
3b)。通过网络分析,这些注释术语,连同它们的相关联基因,被进一步分组为三个功能上有关的模块,其中的每个模块均以其最重要的注释术语为特征(图1d)。这三个模块代表了与(1)胶质细胞分化和髓鞘形成,(2)轴突导向和轴突生成,以及突触结构和突触信号传导的调控有关的基因和功能(图1d)。第一模块和第二模块紧密互连,并含有一系列关键少突细胞谱系转录因子(包括sox10、sirt2、myrf、nkx2.2、tcf7l2、olig1和olig2),以及阶段调控的与髓鞘相关联的蛋白(包括tf、mbp、mag、omg、ugt8和fa2h);所有这些在hd hgpc中都显著下调。第三模块含有与突触传递组分的调控有关的基因,最显著的是syndig1、bcan、neto1和snph,以及编码谷氨酸盐受体信号传导蛋白gria2、gria4、grid1、grid2和grik4的基因和由kcnd2、kcnj9、kcnq1和kcns3编码的钾通道;所有这些都显著下调(图1e
‑
图1g)。总之,这些hd失调基因及其相关联功能揭示了hgpc向成熟少突胶质的分化受到hd依赖性压制。
[0214]
实施例2
–
mhtt hgpc下调髓鞘生成的转录决定子
[0215]
如由差异表达分析所揭示的,与少突胶质分化和髓鞘生物合成相关联的关键转录因子集合作为mhtt表达的函数显著且大幅下调。这些包括早期的少突胶质调控因子nkx2.2、olig2和sox10,它们中的每一种在表达mhtt的hgpc中均急剧下调(图1e)。此外,在mhtt压制的少突胶质谱系转录因子的下游,mhtt hgpc表达的myrf(髓鞘调控因子)水平急剧降低。myrf协同地激活髓鞘形成所必需的许多基因(bujalka等人,“myrf is a membrane
‑
associated transcription factor that autoproteolytically cleaves to directly activate myelin genes,”plos biology 11:e1001625(2013),其据此通过引用整体并入),并且myrf的产生量已被发现在小鼠mhtt
‑
转基因少突细胞中是缺乏的(huang等人,“mutant huntingtin downregulates myelin regulatory factor
‑
mediated myelin gene expression and affects mature oligodendrocytes,”neuron 85:1212
‑
1226(2015),其据此通过引用整体并入)。在人esc来源的hgpc中,myrf调控的髓鞘生成转录物mbp、mag、omg、plp1和mog都显著下调(图1e)。此外,当直接比较来源于具有最小的背景遗传变异的同胞对(针对mhtt的genea20和针对正常htt的genea19)的hgpc的表达模式时,再次注意到与髓鞘生成相关联的那些基因在mhtt hgpc中的差异下调。这些包括myrf(
‑
4.04(在mhtt hgpc中下降的倍数);log2标度)、mag(
‑
6.78)、mbp(5.14)、mog(
‑
10.35)、omg(
‑
5.15)和plp1(
‑
2.22),表明与髓鞘生成相关联的转录物在hd hgpc中广泛下调。重要的是,当比较源自三种不同mhtt hesc系(genea17、genea18和genea20,它们的htt基因分别具有40个、46个和48个cag重复序列)的hgpc的rna表达模式时,注意到较长的cag重复序列长度与这些相同的与分化和髓鞘生成相关联的基因的进行性下调密切相关(图4a
‑
图4c)。重要的是,这些基因与本体之间存在高度的重叠,发现随着hgpc中cag重复长度的增加,这些基因和本体失调的程度越来越高,而在hd转基因小鼠中,这些基因和本体的失调随着cag重复长度的增加而增加(langfelder等人,“integrated genomics and proteomics define huntingtin cag length
‑
dependent networks in mice,”nat.neurosci.19:623
‑
633(2016),其据此通过引用整体并入)(图5a
‑
图5d)。
[0216]
为了验证这些基于rna
‑
seq的表达数据,然后使用带有taqman低密度阵列(tlda)
的qrt
‑
pcr来在mhtt与对照hgpc之间比较这些与分化相关联的基因的表达水平。在rna
‑
seq分析中被鉴定为在mhtt hgpc中差异失调的那些基因中的大多数被证实确实如此(图6a
‑
图6b)。这些基因包括关键的少突胶质谱系转录因子myrf、sox10和olig2,以及它们下游的与髓鞘生成相关联的靶标,包括plp1、mog和mbp。基于这个宽泛的与髓鞘形成相关联的基因集合的下调,预测mhtt hgpc对髓鞘生物发生和维持都有显著的破坏。
[0217]
实施例3
–
与mhtt相关联的分化遏制受压制的钾通道表达
[0218]
在功能上有关的基因当中,受mhtt表达差异失调最大的是那些编码离子通道和转运蛋白,特别是钾通道的基因。这一大组基因包括人基因组中的117个已知成员(pruitt等人,“ncbi reference sequences(refseq):a curated non
‑
redundant sequence database of genomes,transcripts and proteins,”nucleic acids research 35:d61
‑
d65(2006),其据此通过引用整体并入),其中93个被hgpc可检测到地表达(数据集内至少3个样品的原始计数>5)。其中,在93个已鉴定的k
+
通道和转运蛋白基因中,有25个在hd hgpc中相对于它们的汇集的hesc gpc对照失调(使用>2.0的fc截止值和5%的fdr阈值);这些基因中有23个即使在1%fdr下仍存在明显的失调(图7)。这些基因包括许多内向整流k
+
通道,该通道的协同压制揭示了hd脑的钾缓冲被破坏的基础(tong等人,“astrocyte kir4.1 ion channel deficits contribute to neuronal dysfunction in huntington's disease model mice,”nat neurosci 17:694
‑
703(2014),其据此通过引用整体并入)。为了在这一大组协同失调的k
+
通道基因中进一步完善和优先排序,将genea20对比genea19同胞对的比较作为额外的过滤包括在内。通过这种最严格的分析,4个基因(kcnd2、kcnj9、kcnq1和kcns3)在所有hd hgpc系中相对于汇集的对照以及在mhtt和正常hesc来源的hgpc的同胞集合中保持强烈且显著的下调。总之,这些k
+
通道基因的失调表达具有特殊的意义,因为它们在维持稳定的间质k
+
水平和确定动作电位阈值方面起着重要作用。因此,与mhtt相关联的hgpc k
+
通道的压制,除其它作用以外,介导突触k
+
的胶质再摄取,可能是导致在hd中在纹状体神经元中观察到的神经元过度兴奋的原因(benraiss等人,“human glia can both induce and rescue aspects of phenotype in huntington disease.nature communications 7:11758(2016);shin等人,“expression of mutant huntingtin in glial cells contributes to neuronal excitotoxicity,”j cell biol 171:1001
‑
1012(2005);tong等人,“astrocyte kir4.1 ion channel deficits contribute to neuronal dysfunction in huntington's disease model mice,”nat neurosci 17:694
‑
703(2014),其据此通过引用整体并入)。
[0219]
鉴于胶质分化以及k
+
通道表达的同时失调以及后者对前者的依赖性,要提出的问题是是否可能存在一种共同的上游调控因子,其自身由于mhtt表达的功能而失调。使用独创性途径分析(ipa),发现tcf7l2被预测为各种各样的与胶质分化相关联的基因的正调控因子,所述与胶质分化相关联的基因包括已被报道能调控k
+
通道基因表达的几种基因,诸如sox10调节的kcnb1(liu等人,“chromatin landscape defined by repressive histone methylation during oligodendrocyte differentiation,”j neurosci 35:352
‑
365(2015),其据此通过引用整体并入),其在源自所有三种测试的hd系的hgpc中都下调。在这些与胶质分化相关联的基因中,有一些在mhtt胶质中的表达相对于它们的对照是明显缺乏的(图6a)。在此基础上,对rna
‑
seq数据集进行了tcf7l2和tcf7l2调控转录物的查询,发现
tcf7l2在hd中相对于正常hgpc确实差异地下调,而tcf7l2调控的基因伴随地下调(图6b)。由于tcf7l2与胶质分化(尤其是少突胶质分化)密切的牵连,因此这些结果进一步强调了hd中胶质分化阻滞的细胞内在性质。
[0220]
实施例4
–
hd hgpc在体内表现出受损的髓鞘生成
[0221]
由于mhtt hgpc在获取代表少突细胞成熟和髓鞘生成的基因表达模式上似乎是不足的,因此要提出的问题是植入有hd gpc的低髓鞘小鼠是否相对于植入有来自正常同胞的gpc的小鼠缺乏髓鞘形成能力。为此,使用利用双侧半球注射的所述多部位注射方案,将分别源自配对培养物中的同胞雌性genea20系和genea19系的表达mhtt的hgpc和对照hgpc新生期移植到免疫缺乏的颤抖小鼠中。当使用正常多能干细胞来源的或组织来源的hgpc时,该方案在宿主脑中产生了供体来源的髓鞘形成的定型模式和时间过程(wang等人,“human ipsc
‑
derived oligodendrocyte progenitor cells can myelinate and rescue a mouse model of congenital hypomyelination,”cell stem cell 12:252
‑
264(2013b);windrem等人,“neonatal chimerization with human glial progenitor cells can both remyelinate and rescue the otherwise lethally hypomyelinated shiverer mouse,”cell stem cell 2:553
‑
565(2008),其据此通过引用整体并入)。在这种情况下,虽然是非等基因的(正常和突变亨廷顿蛋白的真正等基因系尚未被报道),但在该实验中使用同胞系尽可能地减少了遗传变异。使用这些配对系和这种体内模型,在8、13和18周龄时评估经受植入的小鼠的少突细胞分化和髓鞘形成模式(每个时间点n=3
‑
5只小鼠,总共12只植入了hd hgpc的小鼠和10只植入了对照hgpc的小鼠)。对这些小鼠的脑进行冷冻切片,对少突胶质和髓鞘抗原进行免疫标记,并进行共聚焦成像以比较hd和对照来源的hesc hgpc在体内的分化和髓鞘形成效率。
[0222]
发现,相对于植入了hd hgpc的动物,植入了对照hgpc的小鼠中出现少突胶质表型标志物和髓鞘蛋白产生指数的时间明显提前。然而在新生期植入后8周,使用对照hgpc时轴突接合的髓鞘碱性蛋白的表达是明显的,但植入有hd hgpc的小鼠在该时间点没有表现出明显的mbp免疫标记(图8a和图8d)。到12
‑
13周龄时(到此时植入有对照hgpc的小鼠表现出强劲的髓鞘产生),只有未成熟少突胶质表达的分散的mbp岛出现在匹配的hd gpc受者中(图8b和图8e)。植入了hd gpc的白质的相对延迟的髓鞘形成持续至少4个月;然而,到第18周,植入了对照gpc的小鼠表现出密集的胼胝体和包膜髓鞘形成,而mbp界定的髓鞘形成的汇合区域仅出现在植入了mhtt的脑中(图8c和图8f)。因此,在植入有genea19对照gpc的小鼠中,分化为转铁蛋白
+
少突细胞(图8h和图8i)及其衍生物、mbp
+
髓鞘化少突细胞(图8j和图8k)的人供体细胞的分数显著高于植入有genea20 mhtt gpc的小鼠中的所述人供体细胞的分数。类似地,如在mbp免疫染色切片上评估的髓鞘亮度,在植入了对照gpc的胼胝体中在这两个时间点上都显著高于它们的植入了mhtt gpc的对应物中的所述髓鞘亮度(图8l)。尽管如此,在对照细胞和hd来源的细胞之间,人gpc的植入密度和分布都没有显著差异(图8g、图8m、图8n),这表明植入了hd hgpc的脑中的髓鞘形成缺陷是由于与mhtt相关联的供体细胞少突细胞分化和髓鞘产生上的障碍所致,而不是由于差异植入所致。
[0223]
与mhtt相关联的髓鞘形成延迟对轴突髓鞘形成的速率和效率有显著影响。当通过对单个胼胝体轴突的高分辨率共聚焦成像来分析胼胝体髓鞘形成时,很明显,在植入了mhtt
‑
hgpc的脑中轴突包鞘受损(图9a
‑
图9f)。在第13周和第18周时间点,mhtt hgpc嵌合脑
显示出较少的有髓鞘轴突(图9g);沿着可视化轴突的长度,那些有髓鞘轴突中有较大比例确实是如此不完全的,而对于每个鉴定出的mbp
+
人少突细胞,有较少的轴突被包鞘(图9h)。总之,这些数据表明,被制作成针对表达mhtt的hgpc嵌合的颤抖小鼠未能像植入有正常hesc hgpc的小鼠一样快速或者同样好地形成髓鞘,产生存在轴突包鞘不足的相对低髓鞘动物。因此,由mhtt hgpc表达谱(expression profile)所揭示的与mhtt相关联的分化阻滞似乎反映在它们在导致体内髓鞘形成减少的少突细胞分化能力方面的相对缺乏上。
[0224]
实施例5
–
体内髓鞘基因表达和髓鞘生成可通过sox10和myrf拯救
[0225]
鉴于sox10和myrf在调控髓鞘合成中的首要地位(bujalka等人,“myrf is a membrane
‑
associated transcription factor that autoproteolytically cleaves to directly activate myelin genes,”plos biology 11:e1001625(2013);emery等人,“myelin gene regulatory factor is a critical transcriptional regulator required for cns myelination,”cell 138:172
‑
185(2009);lopez
‑
anido等人,“differential sox10 genomic occupancy in myelinating glia,”glia 63:1897
‑
1914(2015),其据此通过引用整体并入)及其作为髓鞘基因表达的末端效应子的作用,数据表明sox10和myrf的转录激活可能足以拯救hd的髓鞘形成缺陷。在此基础上,接下来要问的是在表达mhtt的hgpc中强制表达sox10和myrf是否能拯救mag、mbp和其它参与髓鞘生物合成的关键基因的表达。为此,使用双顺反子质粒通过质粒转染在mhtt和正常对照hesc来源的hgpc(分别为genea20和genea19)中诱导sox10和myrf的表达,在所述双顺反子质粒中这两个基因都被置于组成型ef1a启动子的控制之下。然后使用qpcr将它们的表达与sox10
‑
myrf和对照质粒转染细胞中的下游髓鞘生成基因(包括mag、mbp、mog、pdgfra、plp1、tf和lingo1)的表达进行比较。发现sox10
‑
myrf的过表达确实拯救了转染的mhtt hgpc中大多数与髓鞘相关联的基因的表达(表1;图10)。
[0226]
基于这些数据,接下来要问的是sox10和myrf过表达是否足以拯救下游少突细胞分化和髓鞘生成。为此,开发了多西环素调控的双重载体慢病毒转导策略,该策略允许多西环素(dox)触发的sox10和myrf的相互依赖的过表达以及cd4的同时表达,以允许对sox10
‑
myrf转导的hgpc进行基于facs的免疫分离(图11a)。首先,通过用dox调控的慢病毒sox10/myrf转导匹配的180天体外(div)genea20来源的hgpc的集合,然后将一些培养物暴露于dox中,而对匹配的对照培养物不予处理,如此来评估sox10和myrf过表达在表达mhtt的hgpc中的影响。已经证实,在dox不存在的情况下饲养的细胞中,sox10和myrf表达与未转导的genea20来源的hgpc的sox10和myrf表达没有区别。在体外再待一周后,然后针对被o4识别的少突细胞硫酸脑苷脂对细胞进行免疫染色,所述少突细胞硫酸脑苷脂是由谱系限制的,主要是有丝分裂后的人少突细胞表达的。在dox不存在的情况下,mhtt hgpc保持原样,并且不表达可检测到的o4。相比之下,那些在dox中饲养的具有上调的sox10和myrf表达的mhtt hgpc表现出少突细胞分化的急剧和显著的增加,其中表达o4免疫反应性的超过15%(图11b
‑
图11d)。
[0227]
由于sox10和myrf表达的诱导似乎足以在体外拯救少突细胞从mhtt hgpc的分化,接下来要问的是sox10和myrf表达是否类似地足以拯救体内髓鞘生成。为此,使用籍以用cd4表达报告sox10和myrf的同时表达的载体系统,用如上所述的dox调控的慢病毒sox10/myrf转导genea20来源的hd hgpc,在cd4上分选细胞,并将sox10/myrf转导的mhtt hgpc移
植到新生颤抖小鼠中。在9周龄时,一些经移植的小鼠被给予dox(口服,被引到入它们随意饮用的水中)以触发sox10和myrf表达,而其它小鼠未被给予dox,从而用作匹配的对照(图11e)。在13周龄时(正常hgpc通常开始髓鞘形成的时间点,而未经处理的mhtt hgpc尚未开始髓鞘形成;图11f和图11g),处死小鼠,将它们的脑切片并进行mbp的免疫染色。发现在其中诱导了供体来源的hgpc sox10和myrf的dox(+)小鼠,在宿主的经受植入的白质中显示出大量的mbp
+
髓鞘化少突细胞。在数量上,植入有sox10/myrf转导的、dox调控的genea20 gpc的dox(+)小鼠表现出强劲的髓鞘生成:到13周时,28.6%
±
0.8%(n=3只小鼠;平均值
±
sem)的供体细胞表达mbp,而在经受相同植入的dox(
‑
)小鼠(n=6只小鼠)中供体细胞未出现可检测到的mbp表达(p<0.0001)。相比之下,18.1%
±
2.1%(n=5)的正常genea19来源的gpc在同一时间点出现mbp表达,表明sox10/myrf转导的hd hgpc在体内mbp界定的髓鞘生成中至少与正常hgpc一样高效。
[0228]
在植入有sox10/myrf
‑
转导的genea20 hgpc的dox(+)小鼠中,所得少突细胞被证明足以诱导常驻的颤抖轴突形成朗维结(nodes of ranvier),其表现出典型的侧接有以结节架构为特征的caspr1的βiv
‑
血影蛋白簇聚(图11l和图11m)。相反,在同一时间点,在dox(
‑
)对照小鼠中供体细胞都未出现mbp表达(图11h
‑
图11j),也没有观察到明确的结节,尽管有类似的供体细胞植入(图11k)。这些数据表明,sox10和myrf的强制表达足以拯救表达mhtt的hgpc的少突细胞分化和髓鞘形成。
[0229]
实施例7
–
mhtt损害体内人星形胶质分化
[0230]
由于hgpc产生星形细胞和少突细胞,因此,少突胶质谱系进展中的与mhtt相关联的缺陷,以及提示对星形细胞
‑
少突细胞命运选择上游的胶质分化造成转录障碍的rna表达数据揭示对星形细胞分化的类似障碍。在此基础上,接下来的问题是,新生期注射了表达mhtt的hgpc(genea20来源的)的小鼠与注射了正常htt同胞对照hgpc(genea19)的小鼠相比,是否表现出体内星形细胞分化的任何差异。为此,使用早期用于检查hd基因型对髓鞘生成的影响的相同小鼠来评估其对胶质纤维酸性蛋白(gfap)界定的白质星形细胞的成熟的影响。在新生期植入后的第8周、第13周和第18周,使用物种特异性抗人gfap抗体对植入了对照和hd hgpc的颤抖脑进行免疫染色。
[0231]
已发现,相对于植入了对照(genea19)hgpc的对应物(n=10)而言,来自所植入的hgpc的星形细胞成熟在所评估的植入了hd(genea20)hgpc的脑(共12个,跨越3个时间点)中是明显缺乏的。聚焦于经受最快速的大量植入的胼胝体和内囊的白质区室,发现由hd hgpc产生的gfap界定的星形细胞分化相对于对照gpc显著减少,并且直至18周的观察点一直如此(图12a
‑
图12f)。为了定量地验证这一观察结果,对在第13周和第18周处死的那些脑进行了评分。在第13周时,植入了对照hgpc的小鼠显示出明显的gfap
+
星形细胞成熟,使得胼胝体中5.9%
±
0.5%的人供体细胞表达gfap(n=4只小鼠;总共2,669个被评分的供体细胞中包含有170个gfap
+
细胞);相比之下,在植入了mhtt gpc的胼胝体中,只有3.3%
±
0.3%的人细胞是gfap
+
细胞(n=5只小鼠;2,153个被评分的供体细胞中有60个gfap
+
)(p=0.026)(图12i)。到18周时,mhtt依赖性的星形细胞成熟压制仍然显著;到该时间点时,8.5%
±
1.0%的对照来源的细胞已经发育出gfap
+
星形细胞表型(n=3只小鼠;2452个被评分的供体细胞中有209个gfap
+
),而表达mhtt的人供体细胞中只有4.9%
±
0.8%如此(n=4只小鼠;3,522个被评分的供体细胞中有147个gfap
+
)(p<0.005)(图12i)。总之,这些数据表明表
达mhtt的hesc gpc的星形细胞分化相对于正常的hesc gpc显著延迟(f=16.31[1,16自由度(df)],双因素anova;总体上p=0.0009)。因此,人们可能会预料到,hd可能会损害发育中的回路整合(circuit integration)以及星形细胞的成年功能。
[0232]
实施例8
–
mhtt gpc白质星形细胞形成异常纤维分布和结构域
[0233]
鉴于在植入了mhtt
‑
hgpc的小鼠中注意到的星形细胞分化减少和延迟,接下来的问题是,那些确实成熟的hd星形细胞发育出的形态是否正常,或者它们的成熟架构最终是否不同于它们的更快速发育的对照hgpc来源的对应物。粗略评估显示,表达mhtt的星形细胞和对照星形细胞的成熟星形细胞形态的不同之处在于,表达mhtt的hd来源的星形细胞通常不能表现出它们的对照来源的对应物的径向对称程度(图12g和图12h)。为了调查这一观察结果,将sholl分析用来评估个体星形胶质形态的复杂性;sholl分析是基于细胞过程与依次地被置于更远半径上的同心圆的交集的数量(sholl,d.a.,“dendritic organization in the neurons of the visual and motor cortices of the cat,”j anat 87:387
‑
406(1953),其据此通过引用整体并入)。通过在150
‑
mm切片的z堆栈中对抗人gfap免疫染色细胞成像并在neurolucida(mbf biosciences)中重建这些细胞,将植入有两种不同系的mhtt hesc hgpc(genea18和genea20)的小鼠的白质中供体来源的星形细胞的纤维架构与植入有源自两种对照hesc系(c27ipsc和genea19 hesc,后者是genea 20的同胞)的hgpc的小鼠的白质中供体来源的星形细胞的纤维架构进行比较。sholl分析显示,表达mhtt的星形细胞的纤维复杂性相对于源自它们的同胞对照hgpc的星形细胞显著降低(图13a
‑
图13d)。这种影响在源自genea20 hesc的mhtt星形细胞与源自它们的匹配的genea19同胞的正常星形细胞的比较中特别明显(图12j
‑
图12p)。植入了mhtt
‑
hgpc的嵌合体中的人星形细胞与植入了正常gpc的小鼠中的那些显著不同,其中纤维网络复杂性较低(图12j)并且具有突起更少但更长的特点(图12k
‑
图12m)。当通过扇入径向分析额外评估3维neurolucida描迹(图12o和图12p)以评估每个细胞的纤维结构域占据其直接体积环境的程度时(dang等人,“formoterol,a long
‑
acting beta2 adrenergic agonist,improves cognitive function and promotes dendritic complexity in a mouse model of down syndrome,”biol psychiatry 75:179
‑
188(2014),其据此通过引用整体并入),发现mhtt星形细胞与对照来源的星形细胞相比,显示出明显更多的未被胶质突起占据的区域(图12n
‑
图12p),这表明结构域结构是不连续的和不完整的。
[0234]
为了更好地理解星形细胞形态中这些与hd相关联的形态异常的转录伴随物,接下来评估了hd对比对照来源的星形细胞的基因表达模式。为此,按照标准方案制取cd140a界定的hgpc,然后通过将该细胞转换到补充有20ng/ml bmp4的含血清培养基中来引导该细胞向星形细胞分化。然后根据cd44对该细胞进行分选,所述cd44在脑细胞中被星形细胞及其定型的前体细胞差异表达(cai等人,“cd44
‑
positive cells are candidates for astrocyte precursor cells in developing mouse cerebellum,”cerebellum 11:181
‑
193(2012);liu等人,“chromatin landscape defined by repressive histone methylation during oligodendrocyte differentiation,”j neurosci 35:352
‑
365(2015),其据此通过引用整体并入)。然后对提取的hd和对照来源的cd44界定的星形细胞的rna执行rna
‑
seq分析,这因此通过它们实际上一致的gfap表达来证实。该分析揭示了表达mhtt的星形胶质相对于对照来源的cd44
+
星形胶质在基因表达上的显著差异(图14a
‑
图
14c)。网络分析揭示了四个离散模块的差异表达,该离散模块包括与(1)突触基因、突触后基因及与受体相关联的基因,(2)内体转录物,(3)桥粒和细胞
‑
细胞接合基因相关的功能本体;以及细胞外基质成分(图14d
‑
图14h)。其中,最大的差异表达的基因集合是与突触和受体调节有关的那些基因集合;这些基因集合包括许多调控纤维长出和运动的基因,包括myl7和mylk2,肌球蛋白轻链
‑
7和肌球蛋白轻链激酶
‑
2(它们是在表达mhtt的星形细胞中相对于对照都急剧下调的基因)(图14e)。重要的是,胶质肌球蛋白及其激酶不仅参与胶质纤维的细化(elaboration),还参与星形胶质的钙信号传递(cotrina等人,“cytoskeletal assembly and atp release regulate astrocytic calcium signaling,”j.neurosco.18:8794
‑
8804(1998),其据此通过引用整体并入本文)。它们在hd星形胶质中的表达的缺乏然后可能会导致hd星形细胞的异常形态发育(khakh等人,“unravelling and exploiting astrocyte dysfunction in huntington’s disease,”trends neurosci.40:422
‑
437(2017);octeau等人,“an optical neuron
‑
astrocyte proximity assay at synaptic distance scales,”neuron 98:49
‑
66(2018),其据此通过引用整体并入本文),同时预测hd脑的胶质合胞体内的异常信号传导(jiang等人,“dysfunctional calcium and glutamate signaling in striatal astrocytes from huntington’s disease model mice,”j.neurosci.36:3453
‑
3470(2016),其据此通过引用整体并入本文)。总之,这些数据强调hd与星形细胞分化和功能发育的不足以及少突细胞成熟和髓鞘形成的受损相关联。
[0235]
实施例讨论
[0236]
这些实验表明,hd中的白质衰竭是受影响的hgpc的分化中mhtt依赖性阻滞的产物,因此编码一组关键胶质谱系转录因子的mrna在表达mhtt的hgpc中差异下调。特别是如nkx2.2、olig2和sox10的表达下调所表现的与mhtt相关联的对少突胶质分化的抑制伴随着sox10调控的髓鞘调控因子myrf的表达减少。这导致了髓鞘形成的压制,髓鞘形成需要与髓鞘生物发生相关联的关键mrna(诸如mag和mbp)的myrf依赖性转录(bujalka等人,“myrf is a membrane
‑
associated transcription factor that autoproteolytically cleaves to directly activate myelin genes,”plos biology 11:e1001625(2013);emery等人,“myelin gene regulatory factor is a critical transcriptional regulator required for cns myelination,”cell 138:172
‑
185(2009),其据此通过引用整体并入本文)。有趣的是,在表达特别长的cag重复序列(150q和250q)的hd转基因小鼠的成熟少突细胞中,也类似地注意到myrf的下调(jin等人,“early white matter abnormalities,progressive brain pathology and motor deficits in a novel knock
‑
in mouse model of huntington’s disease,”hum.mol.genet.24:2508
‑
2527(2015),其据此通过引用并入本文)。这些数据表明,在人中,与mhtt相关联的胶质细胞分化阻滞发生在比以前认为的阶段更早的阶段,并且在产生星形细胞以及少突细胞的双潜能hgpc中是明显的。因此,已发现mhtt显著阻碍了hd中这两种胶质谱系的发育,更重要的是,这种发育遏制发生在表达40
‑
48q的cag重复扩增长度(这是人hd的典型特征)的人gpc中。
[0237]
这些表达数据暗示在hd的白质缺乏症中nkx2.2、olig2和sox10的mhtt依赖性压制表明,使sox10和myrf过表达或者以其它方式激活sox10和myrf的转录可能足以缓解该疾病的髓鞘形成缺陷。结果发现,在表达mhtt的hgpc中sox10和myrf的强制表达拯救了参与髓鞘生物发生的关键基因的表达,并且恢复了体内hd来源的神经胶质细胞的髓鞘形成。因此,靶
向激活或上调sox10和myrf可用作恢复hd中表达mhtt的少突细胞的髓鞘形成能力的一种手段。
[0238]
除了与mhtt相关联的少突细胞成熟和髓鞘形成的缺陷之外,还注意到星形细胞的分化也受到损害,这可能是预期的,因为早在接近星形细胞
‑
少突细胞的命运选择的nkx2.2和olig2阶段,胶质转录就出现了失调。hd hgpc的此种缺陷性星形细胞成熟表明hd表型可能具有重要的发育成分,因为表达mhtt的hgpc的星形细胞分化的任何延迟都可能损害发育性突触发生和回路形成,其中的每一者均依赖于星形细胞导向(clarke等人,“glia keep synapse distribution under wraps,”cell 154:267
‑
268(2013);ullian等人,“control of synapse number by glia,”science(new york,ny)291:657
‑
661(2001),其据此通过引用整体并入本文)。另外,预计任何此种疾病依赖性的星形细胞成熟延迟都可能导致hd的延迟(并最终导致hd的髓鞘形成不足),因为少突细胞对局部星形细胞具有代谢依赖性)(amaral等人,“metabolic aspects of neuron
‑
oligodendrocyte
‑
astrocyte interactions,”front endocrinol(lausanne)4:54(2013),其据此通过引用整体并入)。hd来源的hgpc对星形细胞成熟的拯救是否可能减轻这些对突触发育和组织的影响仍有待观察;如果能减轻的话,我们可以预测以少突细胞的分化拯救似乎足以缓解hd的髓鞘形成缺陷的方式,星形细胞的替代可能足以拯救hd的突触病理变化。
[0239]
除了对神经网络形成和突触架构的贡献之外,hgpc和星形细胞都密切参与维持成年间质离子体内平衡并且参与调控神经元兴奋性。因此,令人感兴趣的是,表达mhtt的hgpc的终末分化受遏制与几个胶质钾通道家族的广泛压制相关联。这些包括kcnj家族的内向整流k
+
通道,包括kcnj8和kcnj9,等等。这种与mhtt相关联的内向整流k
+
通道(其负责将钾离子输入到细胞中)的压制可能有助于通过抑制突触释放的k
+
的胶质再摄取而导致hd神经元的过度兴奋性(shin等人,“expression of mutant huntingtin in glial cells contributes to neuronal excitotoxicity,”j cell biol 171:1001
‑
1012(2005),其据此通过引用整体并入)。在这方面,khakh及其同事已经报告了hd小鼠模型中向内整流通道kir4.1(kcnj10)的星形细胞表达不足(tong等人,“astrocyte kir4.1 ion channel deficits contribute to neuronal dysfunction in huntington's disease model mice,”nat neurosci 17:694
‑
703(2014),其据此通过引用整体并入),这可能类似地反映了破坏的胶质成熟对钾通道表达和胶质k
+
摄取的影响。在于星形细胞终末成熟前的一个阶段被遏制的表达mhtt的人gpc中,似乎大量的k
+
通道转录物被协同地压制,这表明抑制了k
+
通道基因表达的共享上游激活物。虽然这些钾通道基因的上游调控因子尚未被鉴定,但可以合理地假设,mhtt依赖性的终末胶质分化压制可能会导致胶质钾体内平衡机制的开展失败,否则所述机制将会调控和保护神经元活性。
[0240]
总之,这些观察结果表明,预计hd hgpc对星形细胞成熟的任何破坏都可能会显著影响hd中神经网络的发育和成年表现。重要的是,这些发现的一个推论是,用野生型或遗传校正的对应物替换表达mhtt的hgpc可能足以恢复受影响的hd脑的功能性星形细胞和少突胶质。这种可能性最初是由新生期递送的野生型hgpc在先天性髓鞘形成减少的模型中战胜患病hgpc的能力提出的(windrem等人,“neonatal chimerization with human glial progenitor cells can both remyelinate and rescue the otherwise lethally hypomyelinated shiverer mouse,”cell stem cell 2:553
‑
565(2008),其据此通过引用
整体并入),同样值得注意的是新生期胶质替代也足以纠正hd转基因小鼠中钾体内平衡的不足(benraiss等人,“human glia can both induce and rescue aspects of phenotype in huntington disease.nature communications 7:11758(2016),其据此通过引用整体并入)。健康细胞对比患病细胞的这种竞争优势是否会在成年hd中出现仍有待确定,但如果这被证明是可行的,此种胶质替代策略就可能被证明是hd疾病改善的一种现实的治疗途径。
[0241]
应当理解,上述公开的变型和其它特征和功能,或其替代物可以组合到许多其它不同的系统或应用中。本领域技术人员随后可以做出各种目前未预见或未预料到的替代、修改、更改或改进,它们也旨在被所附权利要求书所涵盖。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1