用于近实时定位的具有多个X射线成像仪的辐射治疗系统的制作方法
相关申请的交叉引用
本申请要求于2018年7月28日提交的美国临时申请号62/711,483和于2019年6月25日提交的美国非临时申请号16/452,505的权益。
背景技术:
除非本文中另外指出,否则本节中描述的方法不是本申请中的权利要求的现有技术,并且不能由于包括在本节中而被承认是现有技术。
辐射治疗是一种针对诸如癌性肿瘤的具体靶标组织(计划靶标体积)的局部处理。在理想情况下,对计划靶标体积执行辐射治疗,该辐射治疗使周围的正常组织免于接收高于指定公差的剂量,从而将损害健康组织的风险最小化。在辐射治疗的输送之前,通常采用成像系统来提供靶标组织和周围区域的三维图像。从这样的成像,可以估计靶标组织的尺寸和质量,并且生成适当的处理计划并且确定计划靶标体积。
为了在辐射治疗期间将设定剂量正确地供应给计划靶标体积(即,靶标组织),患者应当相对于提供辐射治疗的线性加速器正确定位。通常,在处理之前和处理期间检查剂量和几何数据,以确保正确的患者放置,并且确保所给予的放疗处理与先前计划的处理相匹配。该过程称为图像指导辐射治疗(igrt),并且涉及在辐射处理被输送给计划靶标体积的同时使用成像系统查看靶标组织。igrt并入了来自处理计划的成像坐标,以确保患者正确对准以在辐射治疗设备中进行处理。
技术实现要素:
根据本公开的至少一些实施例,一种辐射治疗系统被配置为使得能够在单次患者屏气期间对靶标体积进行成像和处理。具体地,在实施例中,辐射系统包括旋转机架,在旋转机架上安装处理输送x射线源、以及多个成像x射线源和对应的x射线成像设备。多个成像x射线源和x射线成像设备使得能够在相对较短的旋转弧(例如,30度或更小)之上获取针对靶标体积的体积图像数据。结果,可以近实时地(例如,在大约一秒钟或更少的时间内)检测分次内运动(在单次患者屏气期间发生的解剖变化,例如由于蠕动、气泡运动、失去屏气等)。因此,辐射治疗系统可以执行图像指导辐射治疗(igrt),该igrt使用x射线成像而不是磁共振成像(mri)来监测分次内运动。然后可以经由患者重新定位和/或处理修改,来补偿检测到的解剖变化,或者可以中止当前处理。
在一些实施例中,例如经由锥形束计算机断层摄影(cbct)在患者屏气开始时执行更高质量的建立扫描,而在屏气的剩余部分期间采用数字断层合成(dts),以监测分次内运动。与基于mri的igrt不同,根据实施例,在屏气期间在包含计划靶标体积的三维(3d)区域内,监测这样的分次内运动。因此,可以在包括所有计划靶标体积的区域内,而不是在计划靶标体积的单个二维(2d)切片内,监测分次内运动。另外,为了在屏气期间在处理已经开始之后生成计划靶标体积的更高质量的3d成像,利用在处理已经开始之后(即,经由dts扫描)获取的3d成像数据,来修改在处理开始之前(即,经由cbct扫描)获取的3d图像数据。
前述发明内容仅是说明性的,并不旨在于以任何方式进行限制。除了上述说明性方面、实施例和特征,通过参考附图和以下具体实施方式,进一步的方面、实施例和特征将变得明显。
附图说明
根据结合附图进行的以下描述和所附权利要求,本公开的前述和其他特征将变得更加充分明显。这些附图仅描绘了根据本公开的几个实施例,因此不应当被视为对其范围的限制。通过使用附图,将利用附加具体性和细节来描述本公开。
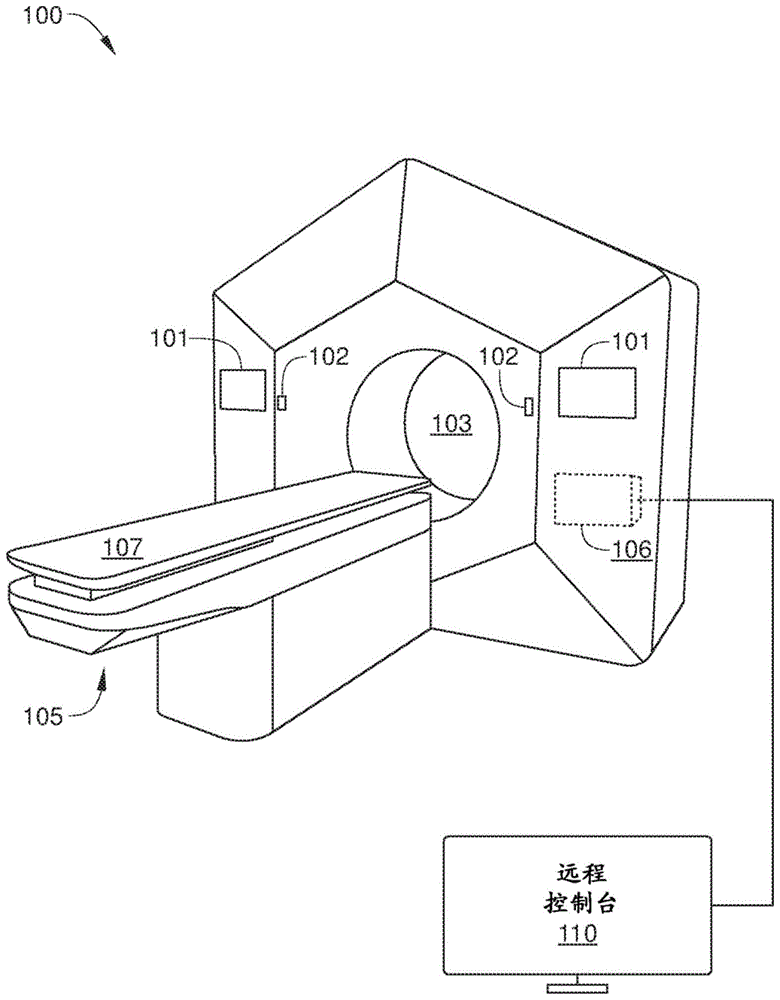
图1是根据本公开的一个或多个实施例的辐射治疗系统的透视图。
图2示意性地图示了根据当前公开的各种实施例的、图1的辐射治疗系统的机架。
图3a和图3b示意性地图示了根据当前公开的各种实施例的、安装在图2的机架上的x射线生成和成像部件。
图4示意性地图示了根据当前公开的各种实施例的、基于通过第一x射线源和第二x射线源生成的投影图像而构造的数字体积。
图5示意性地图示了根据当前公开的各种实施例的、在机架旋转45度之后的、安装在机架上的x射线生成和成像部件。
图6示意性地图示了根据当前公开的各种实施例的、安装在机架上的x射线生成和成像部件。
图7a示意性地图示了根据当前公开的各种其他实施例的、安装在机架上的x射线生成和成像部件。
图7b示意性地图示了根据当前公开的各种实施例的、安装在机架上的x射线生成和成像部件。
图8示意性地图示了根据当前公开的各种其他实施例的、安装在机架上的x射线生成和成像部件。
图9阐述了根据本公开的一个或多个实施例的辐射治疗过程的流程图。
图10阐述了根据本公开的一个或多个实施例的示例性的计算机实现的辐射治疗方法的流程图。
图11a和图11b是根据本公开的一个或多个实施例的旋转时间线,它们示意性地图示了某些方法步骤在机架旋转中的什么点处发生。
图12是根据本公开的一个或多个实施例的旋转时间线,其示意性地图示了某些方法步骤在机架旋转中的什么点处发生。
图13是根据本公开的一个或多个实施例的旋转时间线,其示意性地图示了在机架旋转期间的重叠图像获取弧。
图14阐述了根据本公开的一个或多个实施例的示例性的计算机实现的辐射治疗方法的流程图。
具体实施方式
在以下具体实施方式中,参考形成其部分的附图。在附图中,除非上下文另外指出,否则相似的符号通常标识相似的部件。在具体实施方式、附图和权利要求中描述的说明性实施例并不意在是限制性的。在不脱离此处呈现的主题的精神或范围的情况下,可以利用其他实施例,并且可以进行其他改变。将容易理解的是,如本文中总体上描述的以及在图中图示的本公开的方面可以以各种各样的不同配置来布置、替换、组合和设计,所有这些都被明确地构想并且构成本公开的部分。
图像指导辐射治疗(igrt)用于处理诸如肺部的进行自愿移动、或诸如受蠕动影响的器官的进行非自愿移动的身体区域中的肿瘤。igrt涉及在向靶标组织输送辐射处理的同时,使用成像系统查看靶标组织(还称为“靶标体积”)。在igrt中,将来自先前确定的处理计划的、靶标体积的基于图像的坐标与在施加处理束期间确定的、靶标体积的基于图像的坐标进行比较。以这种方式,可以检测靶标体积相对于辐射治疗系统的运动或变形,并且可以调整患者的位置和/或处理束,以将辐射剂量更精确地靶向肿瘤。
在一些常规igrt辐射系统中,经由诸如金种子的基准标记物,在施加处理束期间,检测软组织的运动。然而,基准标记物的使用具有众多缺点,特别是放置标记物所需要的侵入性外科手术。具体地,基准标记物的腹腔镜插入需要附加的时间和临床资源,诸如手术室、麻醉、抗生素、以及众多附加的医学专家的参与。
替代地,在一些常规igrt辐射系统中,在施加处理束期间经由磁共振成像(mri)来检测软组织的运动。然而,基于mri的igrt也有缺点。首先,基于mri的igrt系统一般比采用x射线成像的辐射治疗系统更大、更复杂且更昂贵。其次,经由mri来检测靶标体积的运动或变形一般涉及监测与穿过靶标体积的2d切片相关联的图像。结果,难以检测在被监测的2d切片之外(或垂直于该2d切片)的任何地方发生的靶标体积运动或变形,这可能会严重影响所施加的辐射剂量的准确性。
鉴于上述情况,本领域中需要改进的系统和技术,以确保在将处理束输送到靶标体积的同时,将靶标体积保持适当地定位以在辐射治疗系统中进行处理。根据本文中描述的各种实施例,辐射系统被配置为使用x射线成像技术,在没有基准标记物的情况下并且近实时地检测分次内运动。在图1中图示了一个这样的实施例。
图1是根据本公开的一个或多个实施例的辐射治疗系统100的透视图。辐射治疗(rt)系统100被配置为针对身体中的指示辐射处理的任何地方的病变、肿瘤和病情,提供立体定向放射外科和精确放疗。这样,rt系统100可以包括以下中的一项或多项:生成高能x射线的兆伏(mv)处理束的线性加速器(linac)、千伏(kv)x射线源、x射线成像仪、以及在一些实施例中的mv电子射野成像设备(epid)(为清楚起见而未示出)。通过示例的方式,本文中描述了配置有圆形机架的辐射治疗系统100。
一般地,rt系统100能够在施加mv处理束期间对靶标体积进行kv成像,使得可以使用x射线成像而不是mri来执行igrt过程。rt系统100可以包括一个或多个触摸屏101、卧榻运动控件102、孔103、基座定位组件105、设置在基座定位组件105上的卧榻107、以及图像获取和处理控制计算机106,所有这些都设置在处理室内。rt系统100进一步包括远程控制台110,远程控制台110被设置在处理室外部,并且使得能够从远程位置进行处理输送和患者监测。基座定位组件105被配置为相对于孔103精确地定位卧榻107,并且运动控件102包括诸如按钮和/或开关的输入设备,该输入设备使得用户能够操作基座定位组件105,以相对于孔103将卧榻107自动且精确地定位到预定位置。运动控件102还使得用户能够将卧榻107手动地定位到预定位置。在一些实施例中,rt系统100进一步包括在处理室中的用于患者监测的一个或多个相机(未示出)。
图2示意性地图示了根据当前公开的各种实施例的rt系统100的驱动机座200和机架210。图2中为清楚起见而省略了盖、基座定位组件105、卧榻107以及rt系统100的其他部件。驱动机座200是用于rt处理系统110的部件的固定支撑结构,该部件包括机架210和用于可旋转地移动机架210的驱动系统201。驱动机座200搁置在支撑表面上和/或固定到该支撑表面,该支撑表面在rt处理系统110外部,诸如为rt处理设施的地板。机架210旋转地耦合到驱动机座200,并且是rt系统100的各种部件安装在其上的支撑结构,该各种部件包括线性加速器(linac)204、mv电子射野成像设备(epid)205、第一成像x射线源206、第一x射线成像仪207、第二成像x射线源208和第二x射线成像仪209。在rt处理系统110的操作期间,机架220在由驱动系统201致动时围绕孔103旋转。
驱动系统201旋转地致动机架210。在一些实施例中,驱动系统201包括线性电机,该线性电机可以固定到驱动机座200,并且与安装在机架210上的磁道(未示出)相互作用。在其他实施例中,驱动系统201包括用于使机架210围绕孔103精确地旋转的另一合适的驱动机构。linac204生成高能x射线(或在一些实施例中,电子)的mv处理束230,并且epid205被配置为利用处理束230获取x射线图像。第一成像x射线源206被配置为将x射线(在本文中称为成像x射线231)的锥形束,穿过rt系统100的等角点203引导到第一x射线成像仪207。类似地,第二成像x射线源208被配置为将x射线(在本文中称为成像x射线232)的锥形束,穿过rt系统100的等角点203引导到第二x射线成像仪209。等角点203通常对应于待处理的靶标体积的位置。第一x射线成像仪207接收成像x射线231,并且从其生成合适的投影图像,并且第二x射线成像仪209接收成像x射线232,并且从其生成合适的投影图像。根据某些实施例,然后,可以采用这样的投影图像,以针对与包括靶标体积的3d区域相对应的数字体积,构造或更新成像数据的部分。在实施例中,可以使用锥形束计算机断层摄影(cbct)和数字断层合成(dts),来处理由第一x射线成像仪207和第二x射线成像仪209生成的投影图像。
在图2所图示的实施例中,第一x射线成像仪207和第二x射线成像仪209被描绘为平面设备。在其他实施例中,第一x射线成像仪207和/或第二x射线成像仪209可以具有弯曲配置。另外,在图2所图示的实施例中,rt系统100包括两个x射线成像仪和对应成像x射线源。在其他实施例中,rt系统100可以包括三个或更多x射线成像仪和对应成像x射线源,这进一步便于使用x射线成像技术近实时地检测分次内运动。
在不同实施例中,linac204、epid205、第一成像x射线源206、第一x射线成像仪207、第二成像x射线源208和第二x射线成像仪209可以以各种配置来布置。下面结合图3a和图3b描述一个这样的实施例。
图3a示意性地图示了根据当前公开的各种实施例的安装在机架210上的x射线生成和成像部件。为了清楚起见,在图3a和图3b中将机架210描绘为单虚线。如图所示,linac204被定位为将处理束230穿过rt系统100的等角点203引导到epid205。另外,第一x射线源206被定位为将成像x射线231从与第一x射线源206相关联的源点301朝向第一x射线成像仪207引导,并且第二x射线源208被定位为将成像x射线232从与第二x射线源208相关联的源点302朝向第二x射线成像仪209引导。在图3a和图3b所图示的实施例中,第一x射线源206和第二x射线源208相对于linac204和epid205对称地定位。在其他实施例中,第一x射线源206和第二x射线源208可以相对于linac204和epid205非对称地定位在机架210上。类似地,第一x射线成像仪207和第二x射线成像仪209可以相对于linac204和epid205对称地或非对称地定位在机架210上。
由第一x射线源206和第二x射线源208生成的投影图像用于针对包括靶标体积的3d区域内的患者解剖结构的数字体积,来构造成像数据。替代地或附加地,这样的投影图像可以用于更新针对与3d区域相对应的数字体积的现有成像数据的部分。下面结合图4描述这样的数字体积的一个实施例。
图4示意性地图示了根据当前公开的各种实施例的数字体积400,数字体积400是基于通过第一x射线源206和第二x射线源208生成的投影图像而构造的。数字体积400包括解剖图像数据的多个体素401(虚线),其中每个体素401对应于数字体积400内的不同位置。为清楚起见,在图4中仅示出了单个体素401。数字体积400对应于包括靶标体积410的3d区域。在图4中,数字体积400被描绘为8×8×8体素立方体,但是实际上,数字体积400一般包括更多体素,例如比图4所示的多几个数量级。
为了讨论的目的,靶标体积410可以是指针对特定处理的大体肿瘤体积(gtv)、临床靶标体积(ctv)或计划靶标体积(ptv)。gtv描绘了大体肿瘤的位置和范围,大体肿瘤例如是可以看到或成像的东西;ctv包括gtv和针对亚临床疾病传播的附加余裕,亚临床疾病传播一般是不可成像的;并且ptv是几何概念,其被设计为确保将合适的放疗剂量实际输送到ctv,而不会对附近的有风险器官造成不利影响。因此,ptv一般大于ctv,但在一些情形下,ptv也可以在一些部分中减小,以在有风险器官周围提供安全余裕。ptv通常基于在处理时间之前执行的成像来确定,并且通过本发明的实施例,便于ptv与在处理时患者解剖结构的当前位置的对准。
根据下面描述的各种实施例,经由通过第一x射线源206和第二x射线源208经由cbct过程生成的投影图像,构造与数字体积400的每个体素401相关联的图像信息。例如,可以紧接在将处理束230输送到靶标体积410之前,采用这样的cbct过程,使得可以在处理开始之前确认靶标体积410的位置和形状。另外,根据下面描述的各种实施例,经由通过第一x射线源206和第二x射线源208经由dts过程生成的投影图像,更新与数字体积400的一些或全部体素401相关联的图像信息。例如,在计划处理的部分开始之后,并且在计划处理完成之前,可以采用这样的dts过程。以这种方式,可以在进行处理的同时确认靶标体积410的位置和形状。因此,如果检测到靶标体积410的足够部分延伸到阈值区域之外(例如,由于呼吸、蠕动、失去屏气等),则处理可以被中止或修改。在这种实例中,可以通过调整患者位置和/或处理束,来实行对处理的修改。在一些实施例中,对处理的修改在处理弧之间执行。在其他实施例中,对处理的修改在处理弧期间、在正在施加处理束的同时执行。
在使用期间,处理束230通常在所有方向上生成大量散射辐射,包括从患者、处理台和机器部件发出的散射辐射、以及从linac204泄漏的散射辐射。结果,大量mv散射可以入射在第一x射线成像仪207和第二x射线成像仪209上。在一些实例中,这样的x射线散射的量可能超过入射在第一x射线成像仪207和第二x射线成像仪209上的成像x射线231和成像x射线232的大小。相应地,在一些实施例中,处理束230与成像x射线231和成像x射线232的时域交错可以被采用于:利用对成像x射线231和成像x射线232的检测,来减少或消除来自处理束230的x射线散射的干扰。在这样的实施例中,成像x射线231、成像x射线232和处理束230被脉冲化或以其他方式被间歇性地激活,使得在成像x射线231和成像x射线232被引导到靶标体积410时,处理束230未被输送到靶标体积410。也就是说,在这样的实施例中,当处理束230开启时,成像x射线231和成像x射线232关闭。
在一些实施例中,典型的kv脉冲的持续时间大约为10ms(毫秒),其中近似每30ms获取图像。在这样的实施例中,处理束230的典型mv脉冲的持续时间可以显著短于上述kv脉冲的持续时间,例如处理束230的典型mv脉冲的持续时间为5μs(微秒)。在这样的实施例中,当成像x射线231和成像x射线232关闭时,可以大约每1-10ms输送处理束230的脉冲。因此,在这种境况下,如果将成像x射线231和成像x射线232与处理束230的mv脉冲同时输送,则可以在kv脉冲内输送处理束230的几个mv脉冲。
在一些实施例中,在成像x射线231和成像x射线232的每个kv脉冲之间,输送处理束230的多个mv脉冲的系列。在其中kv脉冲的持续时间为大约10ms,x射线图像近似每30ms被获取,并且处理束230的mv脉冲的持续时间大约为1μs到10μs的一个这样的实施例中,kv脉冲之间有20ms的窗口用于输送处理束230的mv脉冲。替代地,在一些实施例中,成像x射线231和成像x射线232的kv脉冲的持续时间被缩短,和/或处理束230的mv脉冲在时间上的分离被延长,使得kv成像脉冲适配在多个mv脉冲的系列之间。例如,在其中在大约1ms到5ms中获取x射线图像的实施例中,可以在处理束230的某些mv脉冲之间执行成像。
返回到图3a和图3b所图示的实施例,第一x射线源206和第二x射线源208被定位为使得:第一成像束路径303(在源点301处开始并且在第一x射线成像仪207处结束)与第二成像束路径304(在源点302处开始并且在第二x射线成像仪209处结束)以成像仪分离角309分离。在各种实施例中,成像仪分离角309可以小到大约30度并且大到大约120度。在一些实施例中,为了在法向于处理束230的方向上提供增强的定位准确性,rt系统100被配置为具有显著小于90度的成像仪分离角309。在一些实施例中,为了提供增强的各向同性分辨率,如图3a和图3b所示,rt系统100被配置为具有90度的成像仪分离角309。
在图3a和图3b所图示的实施例中,第一成像束路径303垂直于第二成像束路径304。此外,第一成像束路径303和第二成像束路径304可以各自穿过等角点203。因此,在第一成像束路径303与第二成像束路径304之间的成像仪分离角309为90度。在这样的实施例中,与第一x射线源206和第二x射线源208被定位为使得成像仪分离角309小于或大于90度时相比,一般可以在机架210的较短旋转弧之上收集图像信息,该图像信息被生成用于构造或更新数字体积400的体素401。
例如,在图3a和图3b所图示的实施例中,当机架210旋转通过大约30度的获取弧角时,第一x射线成像仪207和第二x射线成像仪209可以生成阈值成像数据集,其中阈值成像数据集是用于填充或更新数字体积400的部分的成像数据集,数字体积400的该部分足够大并且具有足够的准确性,使得可以在要求公差内,准确地确定靶标体积410的当前形状和位置。在这样的实施例中,由第一x射线成像仪207和第二x射线成像仪209以投影图像形式生成成像数据,对该成像数据执行dts过程。相比之下,在其中成像仪分离角309大于或小于90度的实施例中,可能需要大于30度的机架旋转,以用于第一x射线成像仪207和第二x射线成像仪209生成阈值成像数据集。此外,在包括单个kvx射线源和对应kvx射线成像仪的常规rt系统中,可能需要60度或更大的机架旋转,以用于单个kvx射线成像仪生成阈值成像数据集。因为处理期间的机架旋转速度通常限制为每分钟少量旋转(例如,每分钟2-5个旋转),因此对于接收针对靶标体积410的当前位置和形状的反馈来说,机架旋转通过60度的弧可能是过分长的时间,例如几秒钟。相反,在图3a和图3b所图示的实施例中,这样的反馈成像可以近实时地(例如在机架旋转大约一秒钟之后)提供。在图5中图示了机架旋转的一个实例。
图5示意性地图示了根据当前公开的各种实施例的、在机架210旋转45度之后的、安装在机架210上的x射线生成和成像部件。如图所示,linac204、epid205、第一成像x射线源206、第一x射线成像仪207、第二成像x射线源208和第二x射线成像仪209围绕等角点203一起旋转。在图5所图示的实例中,机架210和安装在其上的上述部件已经旋转通过获取弧角501,从初始旋转位置旋转到当前旋转位置,其中获取弧角501为45度。为了参考,在图5中还示出了linac204的初始位置204a、epid205的初始位置205a、第一成像x射线源206的初始位置206a、第一x射线成像仪207的初始位置207a、第二成像x射线源208的初始位置208a和第二x射线成像仪209的初始位置209a(虚线)。
注意,因为rt系统100包括两个成像x射线源和对应x射线成像仪,所以获取弧角501的有效断层摄影角近似是两倍。针对典型的cbct获取,理想地,机架210在图像数据获取期间旋转通过的断层摄影角足够大,使得至少大约180度的射线以足够的采样密度与2d图像的每个像素相交,该2d图像是从重构视场中的数字体积生成的。例如,在一些实例中,用于完整cbct扫描的最小旋转被认为是180度加上kv扇形角(通常大约为30度),这表示最小旋转大约为210度。因此,因为rt系统100包括两个(或更多)成像x射线源和对应x射线成像仪,所以可以利用近似90度的获取弧角501,来实现与每个像素相交的射线的近似180度的cbct要求。此外,在其中rt系统100包括三个成像x射线源和对应x射线成像仪的实施例中,获取弧角501的有效断层摄影角近似是三倍,并且可以利用近似60度的获取弧角501,来实现与每个像素相交的射线的近似180度的cbct要求。
同样,由rt系统100执行的dts获取也受益于rt系统100中包括的多个成像x射线源和对应x射线成像仪。根据各种实施例,dts获取(也称为“部分弧cbct获取”)被采用于经由减小的获取弧角501生成针对数字体积400的图像数据。具体地,跨大约5度与大约45度之间的获取弧角501取得的dts获取可以生成针对数字体积400的足够准确的数据,使得可以在正在将处理束施加到靶标体积410的同时,可靠地检测靶标体积410的运动和变形。注意,因为需要大量时间将机架210旋转通过较大获取弧角501,因此在获取用于更高质量图像的足够图像数据与生成具有足够时间分辨率的这种图像之间存在权衡。然而,根据本文中描述的各种实施例,结合包括多个成像x射线源和x射线成像仪的rt系统而采用的dts获取可以向igrt过程提供靶标体积410的足够的时间分辨率和定位准确性。
因为获取弧角501是可以依赖于正在执行的特定igrt过程而变化的获取参数,所以在一些实施例中,获取弧角501可以基于多个因素来选择。这样的因素包括:靶标体积410的准确定位需要多少断层摄影信息、需要多么频繁地更新的定位信息、患者特定特性(诸如屏气的能力)、解剖靶标的尺寸和位置等。
在一些实施例中,成像仪分离角309基于与成像不直接相关的因素来选择。例如,为了适应机架210上其他部件的定位,与图3a、图3b和图5所图示的相比,第一成像x射线源206、第一x射线成像仪207、第二成像x射线源208和第二x射线成像仪209相对于linac204和epid205被不同地定位。在图6中图示了一个这样的实施例。
图6示意性地图示了根据当前公开的各种实施例的安装在机架210上的x射线生成和成像部件。如图所示,第一成像x射线源206接近epid205并且在epid205的第一侧上被安装在机架210上,而第二成像x射线源208接近epid205并且在epid205的第二侧上被安装在机架210上。结果,第一成像束路径303与第二成像束路径304之间的成像仪分离角609小于90度。
在一些实施例中,rt系统100包括以全扇形配置定位在机架210上以用于生成成像x射线的一个或多个成像x射线源。替代地或附加地,在一些实施例中,rt系统100包括以半扇形配置定位在机架210上以用于生成成像x射线的一个或多个成像x射线源。在图7a中图示了一个这样的实施例。
图7a示意性地图示了根据当前公开的各种其他实施例的安装在机架210上的x射线生成和成像部件。如图所示,第一成像x射线源706和第一x射线成像仪707以用于生成成像x射线731的全扇形配置,定位在机架210上。也就是说,第一x射线成像仪707定位在机架210上,使得第一x射线成像仪707的穿刺点701在第一x射线成像仪707的中心点702处或附近,其中x射线成像仪的穿刺点被定义为成像仪上与穿刺射线(从x射线源开始并且延伸穿过旋转等角点(诸如等角点203)的线段)相交的点。因此,第一x射线成像仪707定位在机架210上,使得穿刺射线在由第一成像x射线源706生成的x射线束的锥形中基本上居中。另外,第二成像x射线源708和第二x射线成像仪709以用于生成成像x射线732的半扇形配置,定位在机架210上。也就是说,第二x射线成像仪709定位在机架210上,使得成像x射线732的穿刺点703在第二x射线成像仪709的边缘704处或附近,而不是在第二x射线成像仪709的中心点705处或附近。因此,第二x射线成像仪709定位在机架210上,使得穿刺射线设置在由第二成像x射线源708生成的x射线束的锥形的边缘处或附近。因此,在图7a所图示的实施例中,第一x射线成像仪707和第二x射线成像仪709可以相对于linac204和epid205非对称地定位在机架210上。
成像x射线源和x射线成像仪的全扇形(或“中心检测器”)配置具有使得能够使用较短获取弧角(诸如图5所示的获取弧角501)的优点。因此,使用全扇形配置可以减少获取时间,但与半扇形配置相比,导致显著更小的视场。通过说明的方式,在图7a中示出了用于第一成像x射线源706和第一x射线成像仪707的全扇形视场721、和用于第二成像x射线源707和第二x射线成像仪709的半扇形视场722。根据各种实施例,与多个成像x射线源和对应x射线成像仪结合使用全扇形配置可以进一步减少获取时间。在这样的实施例中,通过选择等于(180+x射线扇形角719)/2的成像仪分离角(诸如图3a和图3b所示的成像仪分离角309),可以最小化或以其他方式减少获取时间。当可以产生充足的视场时,可以在cbct获取中有利地采用上述全扇形配置。另外,在分次内dts获取中,一般不需要大视场。因此,由于减少了获取时间,因此上述全扇形配置还可以有利地在分次内dts获取中被采用。结果,使得能够在处理期间更快地反馈靶标体积的当前位置和变形。
成像x射线源和x射线成像仪的半扇形(或“偏移检测器”)配置具有较大的所得视场的优点,但一般要求较大获取弧角。因此,在检测靶标体积的运动或变形中,使用半扇形配置可能增加获取时间和相关联的延时。然而,根据各种实施例,使用多个成像x射线源和对应x射线成像仪可以进一步减少获取时间。例如,在其中rt系统100具有半扇形配置以及90度或更小的成像仪分离角309的实施例中,为了获取完整的cbct数据集,将获取弧角501从360度减小到180度加上成像仪分离角309。在其中rt系统100具有半扇形配置以及大于90度的成像仪分离角309的实施例中,为了获取完整的cbct数据集,将获取弧角501从360度减小到360度减去成像仪分离角309。
在一些实施例中,可调整准直仪(未示出)设置在成像x射线源与x射线成像仪之间。在这样的实施例中,基于准直仪的位置,选择成像x射线源和x射线成像仪的全扇形配置和半扇形配置。例如,在全扇形配置中,可调整准直仪被定位为允许来自成像x射线源的成像x射线入射在x射线成像仪的全部或基本上全部上。相比之下,在半扇形配置中,可调整准直仪被定位为允许来自成像x射线源的成像x射线入射在x射线成像仪的近似一半上。
在图7a所图示的实施例中,rt系统100包括以全扇形配置和/或半扇形配置定位在机架210上以用于生成成像x射线的一个或多个成像x射线源。替代地,在一些实施例中,rt系统100包括不以全扇形配置或半扇形配置定位在机架210上的一个或多个成像x射线源。取而代之,rt系统100中包括的一个或多个成像x射线源和x射线成像仪以移位扇形配置定位在机架210上。在移位扇形配置中,x射线成像仪和对应x射线源定位在机架210上,使得来自x射线源的x射线的穿刺点设置在x射线成像仪的边缘与x射线成像仪的中心点之间。结果,提供了视场中的某些优点。在图7b中图示了一个这样的实施例。
图7b示意性地图示了根据当前公开的各种实施例的、安装在机架210上的x射线生成和成像部件。如图所示,第一成像x射线源756和对应的第一x射线成像仪757以及第二成像x射线源758和对应的第二x射线成像仪759以移位扇形配置定位在机架210上,以用于生成成像x射线761和成像x射线762。也就是说,第一x射线成像仪757定位在机架210上,使得第一x射线成像仪757的穿刺点751设置在第一x射线成像仪757的中心点752与第一x射线成像仪757的边缘753之间。因此,成像x射线761的穿刺射线763在成像x射线761的锥形内移位,以更靠近成像x射线761的近边缘射线764,而不是更靠近成像x射线761的远边缘射线765。类似地,第二x射线成像仪759定位在机架210上,使得第二x射线成像仪759的穿刺点754设置在第二x射线成像仪759的中心点755与第二x射线成像仪759的边缘760之间。因此,成像x射线762的穿刺射线766在成像x射线762的锥形内移位,以更靠近成像x射线762的近边缘射线767,而不是更靠近成像x射线762的远边缘射线768。
在一些实施例中,为了使得能够如上所述使成像x射线761的穿刺射线763和成像x射线762的穿刺射线766移位,第一成像x射线源756和第二成像x射线源758被如下定位,其中穿刺射线763与穿刺射线766之间的成像仪分离角710大于90度,例如在大约110度至140度的量级。较大的成像仪分离角710适应第一成像x射线源756和第二成像x射线源758在机架210上的定位,而不会机械地干扰epid205。替代地或附加地,较大的成像仪分离角710适应第一x射线成像仪757和第二x射线成像仪759在机架210上的定位,而不会机械地干扰linac204。
因为随着机架210在成像过程期间旋转,成像x射线761的穿刺射线763在成像x射线761的锥形内移位,所以近边缘射线764定义较小视场771的外界线(或与之重合),并且远边缘射线765定义较大视场772的外界线(或与之重合)。类似地,因为随着机架210在成像过程期间旋转,成像x射线762的穿刺射线766在成像x射线762的锥形内移位,所以近边缘射线767也定义较小视场771的外界线/与之重合,而远边缘射线768定义较大视场772的外界线/与之重合。因此,在图7b所示的实施例中,由rt系统100生成的x射线图像的视场大于由其中采用成像x射线源和x射线成像仪的全扇形配置的实施例生成的视场,并且小于由其中采用成像x射线源和x射线成像仪的半扇形配置的rt系统100的实施例生成的视场。
鉴于上述情况,在成像期间,在机架210在任何旋转位置处的情况下,较小视场771内的所有区域接收成像x射线761和成像x射线762。相比之下,在成像期间在机架210的任何旋转位置处,较大视场772的仅一部分接收成像x射线761,并且较大视场772的仅一部分接收成像x射线762。结果,为了生成较大视场772的指定质量的x射线图像,与用于生成较小视场771的相同质量的x射线图像的成像弧相比,机架210旋转通过显著更长的成像弧。
因为较短的成像弧要求较短的获取时间,所以图7b所示的实施例可以用于在相对较短的时间间隔(例如,在大约3秒至5秒的量级,其中机架速度约为6rpm至8rpm)中生成较小视场771的x射线图像。这种短的获取时间减少了在成像期间接近靶标体积的运动伪影的可能性,这对igrt非常有益。相反,较长的成像弧要求较长的获取时间,并且使用图7b所示的实施例生成较大视场772的x射线图像可能花费显著较长的时间,例如,在大约8秒至12秒的量级,其中机架速度约为6rpm至8rpm。这样的持续时间的获取时间对于在igrt期间在具有大量运动的解剖区域中使用是有问题的。然而,因为较大视场772的直径可以约为50cm到75cm,因此在大多数或所有方向上,对于大多数或所有患者,较大视场772的所生成的x射线图像可以从靶标体积延伸到皮肤表面。因此,较大视场772的x射线图像对于以下应用可能非常有益:其中与消除或减少成像期间靶标体积的不受控制的运动相比,了解确切的患者尺寸和患者内靶标体积的相对位置更为重要。因此,图7b所示的实施例可以用于代替使用专用ct仿真成像系统,来对较大视场772进行成像。
在图7a所示的实施例中,rt系统100包括:以半扇形配置定位的一个成像x射线源和对应x射线成像仪、以及以全扇形配置定位的一个成像x射线源和对应x射线成像仪。在其他实施例中,两个成像x射线源和对应x射线成像仪都以半扇形配置定位。在其他实施例中,两个成像x射线源和对应x射线成像仪都以全扇形配置定位。在又一些其他实施例中,成像x射线源中的一个或多个成像x射线源和对应x射线成像仪可以选择性地以半扇形配置或全扇形配置部署。在图8中图示了一个这样的实施例。
图8示意性地图示了根据当前公开的各种其他实施例的安装在机架210上的x射线生成和成像部件。如图所示,第一成像x射线源806被配置为在两个位置之间可调整:半扇形位置801和全扇形位置802。如图所示,第一成像x射线源806在半扇形位置801(断线)与全扇形位置802之间的运动(例如,倾斜和/或侧向移位)导致:穿过等角点203的成像x射线831的穿刺矢量811的位置在对应的第一x射线成像仪807上移位。也就是说,在全扇形位置802,穿刺矢量811近似地被引导到第一x射线成像仪807的中心点812,而在半扇形位置801,穿刺矢量811被引导到第一x射线成像仪807的边缘区域813。因此,在由第一成像x射线源806和第一x射线成像仪807所图示的实施例中,x射线源806的运动使得能够在半扇形位置801与全扇形位置802之间进行选择。第一成像x射线源806在半扇形位置801与全扇形位置802之间的运动可以被电动化,经由气动致动器实现,手动调整,或者通过任何其他合适的调整机制执行。替代地或附加地,第一成像x射线源806中包括的可调整准直仪(未示出)可以被采用于在第一成像x射线源806的半扇形配置与全扇形配置之间进行选择。
在替代实施例中,第二x射线成像仪809在半扇形位置803(断线)与全扇形位置804之间的运动导致:穿过等角点203的成像x射线832的穿刺矢量814的位置在第二x射线成像仪809上移位。在这样的实施例中,成像x射线832是由对应的第二成像x射线源808生成的。在全扇形位置804,穿刺矢量814近似地被引导到第二x射线成像仪809的中心点815,而在半扇形位置803,穿刺矢量814被引导到第二x射线成像仪809的边缘区域816。第二x射线成像仪809在半扇形位置803与全扇形位置804之间的运动可以被电动化,经由气动致动器实现,手动调整,或者通过任何其他合适的调整机制执行。
图9阐述了根据本公开的一个或多个实施例的辐射治疗过程的流程图。该方法可以包括如框901-930中的一个或多个框所图示的一个或多个操作、功能或动作。尽管框以相继顺序被图示,但是这些框可以并行地、和/或以与本文中描述的顺序不同的顺序来执行。而且,基于期望实现,各种框可以被组合成更少的框,被划分成附加的框,和/或被消除。尽管该方法结合图1-图8的系统进行描述,但是本领域技术人员将理解,任何合适配置的辐射治疗系统在本公开的范围内。
当获取针对包括靶标体积410的数字体积400的诊断体积(3d)图像数据,并且生成基于诊断体积图像数据的患者图像时,方法在步骤901处开始。通常,诊断体积图像数据包括针对数字体积400中的每个体素401的图像信息,并且可以从诊断计算机断层摄影(ct)、cbct或mri系统被获取。当通过ct或cbct过程产生时,诊断体积图像数据可以包括数字体积400的数百个有区别的数字x射线投影图像。在步骤902中,执行癌症诊断。如果诊断出癌症,则该方法进行到步骤903;如果否,则该方法进行到步骤930并且终止。在步骤903中,基于在步骤901中生成的ct或mri图像,创建处理计划。通常,处理计划指定分次(对处理设施的访问)的数目和每分次的剂量(包括处理弧的数目)。另外,处理计划一般指定肿瘤靶标的几何形状、有风险器官和处理束的定向角。如所描述的,如果例如由于胃、膀胱或结肠充填而导致靶标体积的位置和/或形状随后改变,则可以对应地修改计划的这种细节。
在步骤904中,当患者到达处理设施并且位于rt系统上(诸如rt系统100的卧榻107上)时,启动分次的执行。步骤904通常在关于在步骤903中创建的处理计划执行各种qa检查之后发生,例如在步骤903之后多达几周之后发生。在步骤905中,在患者位于rt系统100的卧榻107上的同时,rt系统100中包括的kv成像系统获取体积图像数据。在一些实施例中,然后执行数字体积的自动分割和可变形配准,之后进行患者位置调整(步骤906)。自动分割包括数字体积400内的靶标体积和有风险器官的界定。可变形配准调整在较早的计划阶段中针对靶标体积410和有风险的任何器官而生成的轮廓。可变形配准过程补偿例如由于胃、结肠和膀胱充填、肿瘤收缩和其他因素而导致的、靶标体积410和有风险器官的形状和相对位置的改变。在步骤906中,根据在步骤905中获取的体积成像信息,来调整卧榻107的位置。因此,在适用时,调整患者的当前位置,以将靶标体积410与现在已修改的计划靶标体积精确对准。例如,卧榻107的位置可以被自动和/或手动地调整,以使靶标体积410与已修改计划靶标体积对准。在步骤907中,将靶标体积的图像(基于在步骤905中获取的体积图像数据)与在步骤901中获取的靶标体积的计划图像进行比较。在步骤908中,调整处理计划,以考虑在某些器官形状中检测到的改变。
在步骤909中,当患者屏气开始时,启动当前分次的一个处理弧的执行。在步骤910中,根据本公开的实施例,执行处理弧,其中在处理弧期间采用来自多个x射线成像仪的成像信息,以近实时地检测分次内运动。在单次患者屏气期间,执行处理弧。下面结合图10更详细地描述步骤910。在步骤911中,患者恢复呼吸,并且在步骤912中,计算靶标体积410和周围的有风险器官的剂量,并且临床工作人员查看累积的剂量、热斑和冷斑。“热斑”是已经接收多于预定允许剂量的靶标体积410或有风险器官的部分,而“冷斑”是已经接收少于针对处理中的当前点的计划剂量水平的靶标体积410的部分。注意,根据本公开的实施例,基于在步骤910期间从第一x射线成像仪207和第二x射线成像仪209获取的成像信息,来执行步骤911。通常,步骤911和912同时执行,但也可以串行执行。在步骤913中,做出是否已经达到针对当前分次的靶标体积的所要求的剂量的确定。在一些实施例中,临床工作人员做出这样的确定,并且在其他实施例中,这样的确定可以是自动化过程。如果已经达到针对当前分次的所要求的剂量,则该方法进行到步骤920;如果尚未达到针对当前分次的所要求的剂量,则该方法进行到步骤914。
在步骤914中,做出在步骤913中检测到的任何热斑或冷斑是否超过指定位置和/或剂量公差的确定。如果超过这样的公差,则该方法进行到步骤915;如果否,则该方法返回回到步骤909,并且当另一患者屏气开始时,启动当前分次的下一处理弧的执行。在步骤915中,响应于在先前的处理弧中超过指定的位置和/或剂量公差,做出一个或多个调整。在一些实施例中,卧榻107被重新定位,以使检测到的热斑和/或冷斑在指定公差内。替代地或附加地,在一些实施例中,修改处理计划,以使检测到的热斑和/或冷斑在指定公差内。例如,可以修改处理束230的计划的场形状和/或强度,以补偿检测到的热斑和/或冷斑。在做出这样的调整之后,该方法回到步骤909,并且当另一患者屏气开始时,启动当前分次的下一处理弧的执行。在替代实施例中,可以在步骤910中的处理弧的执行期间,执行在步骤915中执行的调整。
在确定已经达到针对当前分次的所要求的剂量时发生的步骤920中,当前分次完成。在步骤921中,患者离开处理设施。在步骤922中,做出是否已经达到针对整个处理的指定剂量的确定。如果是,则该方法进行到步骤924并且处理完成;如果否,则方法进行到步骤923。在步骤923中,临床工作人员查看总剂量以及检测到的热斑和冷斑,并且相应地调整处理计划。然后该方法返回到904,并且当患者再次到达处理设施时,启动处理的下一分次的执行。
图10阐述了根据本公开的一个或多个实施例的示例性的计算机实现的辐射治疗方法的流程图。该方法可以包括如由框1001-1040中的一个或多个框所图示的一个或多个操作、功能或动作。尽管框以相继顺序被图示,但是这些框可以并行地、和/或以与本文中描述的顺序不同的顺序来执行。而且,基于期望实现,各种框可以被组合成更少的框,被划分成附加的框,和/或被消除。尽管该方法结合图1-图9的系统进行描述,但是本领域技术人员将理解,任何合适配置的辐射治疗系统在本公开的范围内。图11a、图11b和图12是根据本公开的一个或多个实施例的旋转时间线1100和1200,旋转时间线1100和1200各自示意性地图示了某些方法步骤在机架210的旋转中的什么点处发生。具体地,图11a和图11b图示了:当实现包括步骤1010和1011的过程分支时,某些方法步骤在机架210的旋转中的什么点处发生,其中图11b图示了当响应于失去屏气而执行图10的方法步骤时机架210的旋转。图12图示了:当实现包括步骤920和921的过程分支时,某些方法步骤在机架210的旋转中的什么点处发生。在图11a、图11b和图12中,“12点钟”位置1101对应于机架210的0度旋转。
当患者开始屏气时,方法在步骤1001处开始。在一些实施例中,用光学标记块和相机监测患者的呼吸。在这样的实施例中,当操作员要求患者屏住他/她的呼吸时,相机将指示何时最终屏住呼吸,并且步骤901开始。替代地,在步骤901中可以采用本领域中已知的监测患者呼吸的其他手段,诸如光学主块、腰带传感器、光学标记块、呼吸管等。
在步骤1001中,与rt系统100相关联的计算设备(诸如图像获取和处理控制计算机106)使得:在机架210旋转通过初始成像弧1102的同时,发生从第一x射线成像仪207和第二x射线成像仪209的体积图像数据的获取。例如,在使得机架210在第一方向1103上从第一成像位置1104向第一处理输送位置1105旋转的同时,计算设备使得第一成像x射线源206引导成像x射线231穿过靶标体积410,并且计算设备使得第二成像x射线源208引导成像x射线232穿过靶标体积410。在一些实施例中,成像x射线231和成像x射线232的脉冲交错,以减少或消除由kvx射线散射产生的噪声。另外,计算设备从第一x射线成像仪207接收第一体积图像数据,并且从第二x射线成像仪209接收第二体积图像数据。在一些实施例中,第一体积图像数据和第二体积图像数据的组合对应于针对靶标体积410的完整cbct数据集。因为rt系统100包括两个或更多成像x射线源和对应x射线成像仪,所以如图12所示,当机架210旋转通过大约90度的获取弧角501(即,初始成像弧1102)时,可以生成这样的完整cbct数据集。替代地,在一些实施例中,可以在初始成像弧1102期间生成dts图像,并且初始成像弧可以是显著更短的弧,诸如当靶标体积设置在腹部中时大约为30度,并且当靶标体积设置在胸部中时小到大约5-10度。在一些实施例中,rt系统100被配置为使机架210以比输送处理束230时更高的旋转速度旋转通过初始成像弧1102,即,旋转通过每个后续获取弧角501。
在步骤1002中,基于在步骤1001中接收的第一体积图像数据和第二体积图像数据,计算设备确定靶标体积410的当前形状和位置。注意,靶标体积410的这样的定位在3d体素集、而不是2d体素集内执行的,2d体素集诸如为在基于mr的igrt中采用的体素的单个2d“层”的平面阵列。因此,靶标体积410的任何部分的移动和/或变形可以由计算设备检测到。也就是说,这样的对移动或变形的检测并不取决于靶标体积410的某个平面区域(诸如在基于mr的igrt中监测的2d体素层)内发生的移动或变形。
在步骤1003中,基于在步骤1002中确定的偏移,计算设备确定靶标体积410的当前形状和位置从针对靶标体积410的计划处理位置的位置偏移。例如,在一些实施例中,计算设备确定靶标体积410的部分从针对靶标体积410的该部分的计划处理位置的位置偏移。此外,在一些实施例中,计算设备确定靶标体积410的多个部分中的每个部分从针对靶标体积410的那些部分的相应计划处理位置的位置偏移。注意,靶标体积410的当前形状和位置从已修改计划靶标体积的偏移可以在围绕靶标体积410的3d数字体积中确定,而不是在穿过靶标体积410的平面区域的2d表示中确定。
在步骤1004中,基于在步骤1003中确定的偏移,计算设备确定靶标体积410的部分距针对靶标体积410的该部分的计划处理位置是否小于第一阈值距离。此外,在一些实施例中,计算设备确定靶标体积410的多个部分中的每个部分距针对靶标体积410的该部分的相应计划处理位置是否小于第一阈值距离。在这样的实施例中,确定靶标体积410的部分距针对该部分的计划处理位置是否小于第一阈值距离包括:确定靶标体积410的任何部分是否超过中止处理阈值,使得触发当前处理的中止。例如,靶标体积410可能由于蠕动、气泡运动、失去患者屏气等而显著移动。在一些实施例中,中止处理阈值可以是靶标体积410的部分从在已修改计划靶标体积中针对该部分而指出的位置的总允许位移。因此,在这样的实施例中,当该部分从在已修改计划靶标体积中指示的位置的位移多于中止处理阈值时,中止当前处理,并且该方法进行到步骤1040;如果该部分的位移小于中止处理阈值,则该方法进行到步骤1005。替代地或附加地,在一些实施例中,中止处理阈值包括延伸到已修改计划靶标体积之外的靶标体积410的允许总体积。替代地或附加地,在一些实施例中,中止处理阈值包括针对靶标体积410相对于已修改计划靶标体积的位移的任何其他可量化度量。因此,步骤1004确保了:如果靶标体积410在处理期间改变位置和/或变形太多,则处理中止。
在步骤1005中,计算设备确定是否响应于先前的处理弧中的失去呼吸而正在执行当前处理弧。如果否,则该方法进行到步骤1007;如果是,则方法100进行到步骤1006。
在步骤1006中,计算设备使得机架210旋转到如下位置,该位置对应于先前处理弧期间的、失去患者屏气并且处理束230关闭的机架位置。然后该方法进行到步骤1007。
在步骤1007中,在计算设备使得机架210继续在第一方向1103上(例如,从第一处理输送位置1105向第二处理输送位置1106)旋转的同时,计算设备根据当前处理计划启动处理束230到靶标体积410的输送。在一些实施例中,处理束230被连续地输送到靶标体积410,并且在其他实施例中,处理束230不被连续地输送,例如处理束230可以间歇地和/或经由多个脉冲的系列被输送。
在步骤1008中,在机架210继续在第一方向1103上旋转的同时,计算设备确定当前临床方案是否指示要在整个处理弧中避免kv成像。例如,在一些实例中,依赖于解剖部位(例如,肺部对腹部)和linac204的最大剂量率,临床方案可以指示应当最小化或以其他方式减少由kv成像引起的剂量。如果当前临床方案指示要在整个处理弧中避免kv成像,则该方法进行到步骤1010(参见图11);如果当前临床方案未指示要在整个处理弧中避免kv成像,则该方法进行到步骤1020(参见图12)。
在步骤1010中,在机架210从第一处理输送位置1105向最终处理输送位置1108旋转的同时,计算设备使得处理束230被引导到靶标体积410,其中最终处理输送位置1108是旋转弧中的最终位置,在该旋转弧期间,处理束230被引导到靶标体积410(参见图11)。在步骤1011中,计算设备确定机架210是否已经旋转通过所有处理位置,即,机架210是否已经到达最终处理输送位置1108。如果否,则该方法进行到步骤1012;如果是,则该方法进行到步骤1013。在步骤1012中,计算设备在向靶标体积410施加处理束230期间确定是否发生失去屏气。如果是,则该方法进行到步骤1030;如果否,则该方法返回回到步骤1010,并且随着机架210继续朝向最终处理输送位置1108旋转,处理束230继续被输送到靶标体积410。在一些实施例中,使用在步骤1001中在机架210旋转通过初始成像弧1102的同时启动从第一x射线成像仪207和第二x射线成像仪209获取体积图像数据的相同传感器,确定失去呼吸。例如,光学标记块、肺活量计等可以被采用于检测患者失去屏气。
在响应于机架210旋转通过所有处理位置并且到达最终处理输送位置1108而发生的步骤1013中,当机架旋转通过处理之后的成像弧1109时,计算设备使得经由第一x射线源206、第二x射线源208、第一x射线成像仪207和第二x射线成像仪209生成弧后x射线图像。注意,因为采用多个x射线成像仪来生成弧后x射线图像,所以处理之后的成像弧1109的长度可以显著小于180度、或者甚至小于90度,并且仍然使得能够生成足够清晰的投影图像以检测靶标体积410的分次内运动。例如,当靶标体积410位于腹部中时,处理之后的成像弧1109可以为大约30度的量级,而当靶标体积410位于胸部中时,处理之后的成像弧1109可以为大约1度到10度的量级。
在步骤1014中,计算设备将在步骤1013中生成的弧后图像与在步骤1001中生成的处理前x射线图像进行比较。然后,计算设备基于靶标体积410的运动,计算到有风险器官(oar)(例如,接近靶标体积410的器官)和到大体肿瘤体积(gvt)(即,靶标体积410)的剂量的上限和下限。这样计算出的信息设置在处理期间可能已经发生的可能的热斑和冷斑的上限和下限。例如,在一些实施例中,假定当机架210在第一处理输送位置1105处时发生靶标体积410的运动(通过弧后图像与处理前x射线图像的比较来指示),执行第一剂量计算,并且假定当机架210在最终处理输送位置1108处时发生由图像比较所指示的靶标体积410的运动,执行第二剂量计算。因此,即使在机架210旋转通过处理位置的同时未监测到靶标体积410的运动,也针对靶标体积410的运动计算最佳情况剂量方案和最坏情况剂量方案。然后,该方法进行到作为当前处理弧的结束的步骤1040。
在确定当前临床方案未指示要在整个处理弧中避免kv成像后发生的步骤1020中,在机架210在第一方向1103上从第一处理输送位置1205向第二处理输送位置1206旋转的同时,计算设备根据计划处理使得处理束230被引导到靶标体积410(参见图12)。另外,计算设备使得第一成像x射线源206引导成像x射线231穿过靶标体积410,并且使得第二成像x射线源208引导成像x射线232穿过靶标体积410。在一些实施例中,成像x射线231和成像x射线232的脉冲与处理束230的脉冲交错,以减少或消除由处理束230生成的mvx射线散射所产生的噪声。此外,计算设备从第一x射线成像仪207接收第三体积图像数据,并且从第二x射线成像仪209接收第四体积图像数据。因此,在步骤1020中,在其中处理束230被输送给靶标体积410的相同的旋转弧之上,获取体积图像数据。
在一些实施例中,在步骤1020中执行dts获取。在这样的实施例中,当在具体获取弧角501之上被获取时,第三体积图像数据和第四体积图像数据的组合对应于针对靶标体积410的dts数据集,该dts数据集包括足够的信息来进行靶标体积410的定位。在步骤1020中采用的具体获取弧角501可以依赖于各种因素而变化,该各种因素包括靶标体积410中包括的组织类型、靶标体积410的尺寸和解剖位置、第一x射线成像仪207和第二x射线成像仪209的特性等。另外,在其中在步骤1020中执行dts获取的实施例中,与生成完整cbct数据集所要求的获取弧角相比较,具体获取弧角501被显著减小。此外,因为rt系统100包括两个(或更多)成像x射线源和对应x射线成像仪,所以获取足够的数据来进行靶标体积410的定位所需要的具体获取弧角501是具有单个kv成像仪的rt系统所要求的获取弧角的一半(或更小)。例如,在其中在步骤1020中采用dts获取的实施例中,获取足够的第三体积图像数据和第四体积图像数据来进行靶标体积410的定位所需要的具体获取弧角501可以在大约5度到大约45度之间。在图10所图示的实施例中,第一处理输送位置1205与第二处理输送位置1206之间的具体获取弧角501被描绘为大约45度的旋转。
在一些实施例中,除了从第一x射线成像仪207获取第三体积图像数据和从第二x射线成像仪209获取第四体积图像数据之外,在步骤1020中,计算设备还基于第三体积图像数据和第四体积图像数据,更新针对数字体积400的现有体积图像数据。因此,在步骤1020之后,数字体积400反映如基于在机架通过获取弧角501的旋转期间所获取的体积图像数据而确定的、靶标体积410的当前位置和形状。在其中针对数字体积400的现有体积图像数据包括在机架210旋转通过初始成像弧1102时获取的cbct生成的图像数据的实例中,可以在步骤1020中采用mckinnon-bates(mkb)算法,以利用在步骤1020中获取的dts生成的图像数据来更新现有体积图像数据。
在步骤1021中,计算设备确定机架210是否已经旋转通过所有处理位置,即,是否已经旋转到最终处理束输送位置1208。通常,计划在整个360度弧上施加处理束230,例如从第一处理输送位置1205到最终处理输送位置1208。因此,除非该方法中止,否则计算设备使得机架210旋转通过360度弧,同时处理束230被施加到靶标体积410。如果机架210已经旋转通过所有处理位置,则该方法进行到步骤1023;如果否,则该方法进行到步骤1022。
在步骤1022中,在将处理束230施加到靶标体积410期间,计算设备确定是否发生失去屏气。如果是,则该方法进行到步骤1030;如果否,则该方法返回回到步骤1020,并且随着机架210继续从第二处理输送位置1206朝向最终处理输送位置1208旋转,处理束230继续被输送到靶标体积410。在步骤1023中,计算设备更新或生成在当前处理弧期间已经发生的靶标体积410的运动记录。该记录可以用于计算靶标体积410和有风险器官中的累积剂量。然后,该方法进行到作为当前处理弧的结束的步骤1040。
在上述方法中,在具体获取弧角501之上,执行体积图像数据的dts获取,其中选择获取弧角501,使得足够的体积图像数据被生成,以使得能够确定靶标体积410的当前位置和/或形状。因此,每次机架210旋转通过具体获取弧角501时,计算设备都会执行靶标体积410的定位(即,确定靶标体积410的当前位置和/或形状)。例如,在图12所图示的实施例中,计算设备在360度处理弧期间,在每30度旋转之后,执行靶标体积410的定位。在其他实施例中,计算设备经由包括“滑动弧”或“滑动窗口”方法的数字体积400的dts重构,更频繁地执行靶标体积410的定位。更具体地,计算设备利用新获取的体积图像数据来更新针对数字体积400的现有体积图像数据,该新获取的体积图像数据本身可以不包括足够的成像信息以使得能够对靶标体积410进行定位。在图13中图示了一个这样的实施例。
图13是根据本公开的一个或多个实施例的旋转时间线1300,其示意性地图示了在机架210的旋转期间的重叠图像获取弧。图13示出了机架210的旋转的部分,该部分包括初始成像弧1002和多个处理中成像弧1321-1323。如上面所指出的,初始成像弧1002在将处理束230施加到靶标体积410之前发生。在初始成像弧1002期间,进行靶标体积410的投影图像的cbct获取,以用于确定靶标体积410的初始位置。相比之下,每个处理中成像弧1321-1323对应于处理弧1320的不同部分,处理弧1320是处理束230通过其被施加到靶标体积410的旋转弧。处理弧1320通常是360度旋转弧,但是为了清楚起见,在图13中仅示出了其初始和最终部分。
根据各种实施例,在机架210旋转通过处理中成像弧1321-1323之一期间,获取针对数字体积400的体积图像数据的第一集。然后使用体积图像数据的第一集来更新针对数字体积400的现有体积图像数据,基于针对数字体积400的更新的体积数据来执行靶标体积410的定位,并且然后在适当时,执行对靶标体积和/或处理束230的位置的修改。以这种方式,在机架210已经旋转通过足够大小的获取弧角501以生成针对靶标体积410的完整的体积图像数据集之前,生成关于靶标体积410的位置和变形的反馈。取而代之,关于靶标体积410的位置和变形的反馈可以以如下频率来生成,该频率显著高于在基于(在机架210旋转通过完整的获取弧角501时生成的)完整的体积图像数据集执行靶标体积410的定位时的频率。例如,在图13所示的实施例中,获取弧角501包括三个处理中成像弧1321-1323。在这样的实施例中,基于用在单个处理中成像弧(诸如处理中成像弧1321)期间获取的体积图像数据来更新现有体积图像数据(诸如在初始成像弧1002期间获取的cbct图像数据),可以生成定位反馈。结果,在这样的实施例中,以基于在完整获取弧角501期间获取的数据来生成反馈数据的频率的三倍的频率,来接收定位反馈。
图14阐述了根据本公开的一个或多个实施例的示例性计算机实现的辐射治疗方法的流程图。该方法可以包括如由框1401-1410中的一个或多个框所示出的一个或多个操作、功能或动作。尽管框以相继顺序示出,但是这些框可以并行地、和/或以与本文中描述的顺序不同的顺序来执行。而且,基于期望实现,各种框可以被组合成更少的框,被划分成附加的框,和/或被消除。尽管该方法结合图1-图13的系统进行描述,但是本领域技术人员将理解,任何合适配置的辐射治疗系统在本公开的范围内。
当患者开始屏气时,方法1400在步骤1401处开始。在步骤1401中,与rt系统100相关联的计算设备(诸如图像获取和处理控制计算机106)使得:在机架210旋转通过初始成像弧1002的同时,发生从第一x射线成像仪207和第二x射线成像仪209的体积图像数据的获取。例如,在步骤1401期间,进行靶标体积410的投影图像的cbct获取,以生成使得能够定位靶标体积410的完整的体积图像数据集。
在步骤1402中,计算设备基于在步骤1401中获取的体积图像数据,确定靶标体积410的初始位置。
在步骤1403中,计算设备开始将处理束230施加到靶标体积410。
在步骤1404中,计算设备确定机架210是否已经旋转通过所有处理位置,例如,在处理束230开启的情况下旋转360度。如果是,则方法1400进行到步骤1410,并且处理结束;如果否,则方法1400进行到步骤1405。
在步骤1405中,在机架210继续旋转通过当前处理中成像弧(即,处理中成像弧1321-1323之一)时,计算设备使得进行靶标体积410的投影图像的dts获取。也就是说,计算设备使得针对数字体积400获取dts体积图像数据的部分集。
在步骤1406中,通过利用在步骤1405中获取的dts体积图像数据的部分集来更新针对数字体积400的当前体积图像数据,计算设备生成更新的体积图像数据。在步骤1406的第一迭代中,针对数字体积400的当前体积图像数据对应于在步骤1401中获取的完整的体积图像数据集。在步骤1406的后续迭代中,数字体积400的当前体积图像数据对应于先前已经用在机架210旋转通过较早的处理中成像弧时获取的dts体积图像数据而更新的体积图像数据。
在步骤1410中,计算设备结束当前处理,并且患者可以释放屏气。
上述实施例的实现使得能够在使用x射线成像技术的辐射治疗期间近实时地反馈解剖变化。例如,用于靶标体积的3d定位的x射线成像数据可以以大约每秒一次或多次的量级进行刷新。因此,在可以持续10秒、20秒、30秒或更长时间的单次屏气期间,可以在施加处理束期间重复确定靶标体积的位置和变形。结果,可以在igrt期间采用x射线成像以准确定位靶标体积,并且可以执行剂量计算,该剂量计算量化在处理期间产生的热斑和冷斑的可能位置限。
各种实施例的描述已经给出以用于说明目的,但非旨在穷举或限于所公开的实施例。在不脱离所描述的实施例的范围和精神的情况下,很多修改和变型对于本领域普通技术人员将是很清楚的。
本实施例的方面可以体现为系统、方法或计算机程序产品。因此,本公开的方面可以采取以下形式:完全硬件实施例、完全软件实施例(包括固件、驻存软件、微代码等)、或将一般在本文中全都可以称为“电路”、“模块”或“系统”的软件和硬件方面组合的实施例。此外,本公开的方面可以采取体现在一个或多个计算机可读介质中的计算机程序产品的形式,该一个或多个计算机可读介质具有体现在其上的计算机可读程序代码。
可以利用一种或多种计算机可读介质的任何组合。计算机可读介质可以是计算机可读信号介质或计算机可读存储介质。计算机可读存储介质可以是例如但不限于:电子、磁性、光学、电磁、红外或半导体的系统、装置或设备、或前述各项的任何合适的组合。计算机可读存储介质的更具体示例(非详尽列表)将包括以下:具有一根或多根接线的电连接、便携式计算机磁盘、硬盘、随机存取存储器(ram)、只读存储器(rom)、可擦除可编程只读存储器(eprom或闪存)、光纤、便携式紧凑盘只读存储器(cd-rom)、光学存储设备、磁存储设备、或前述各项的任何合适的组合。在本文档的上下文中,计算机可读存储介质可以是任何有形介质,其可以包含或存储供指令执行系统、装置或设备使用或与其结合使用的程序。
尽管本文中已经公开了各种方面和实施例,但是其他方面和实施例对于本领域技术人员将是很清楚的。本文中公开的各种方面和实施例是出于说明的目的,而不是旨在进行限制,其中真实的范围和精神由所附权利要求指示。
- 还没有人留言评论。精彩留言会获得点赞!