用于经由身体引流或注射进行治疗的系统和方法与流程
相关申请的交叉引用
本申请要求2018年8月14日提交的标题为“systemandmethodfortreatmentviathoracicductdrainageorinjection”的临时专利申请序列号62/718,863、2018年10月11日提交的标题为“systemandmethodfortreatmentviathoracicductdrainageorinjection”的临时专利申请序列号62/744,577、2018年10月18日提交的标题为“systemandmethodfortreatmentviathoracicductdrainageorinjection”的临时专利申请序列号62/747,644、2019年2月12日提交的标题为“thoracicductlymphaticdrainage”的临时专利申请序列号62/804,675以及2019年5月15日提交的标题为“pleuralandlymphaticdrainagesystems”的临时专利申请序列号62/848,468的权益和优先权,此处据此以引证的方式将所有申请全文并入。
背景技术:
慢性和急性充血性心力衰竭(chf)通常发生在心脏不能向身体循环充足的血液供应时。这通常是由于心输出量不足,心输出量不足有许多原因。在chf代偿失调中,液体通过肺和全身静脉/淋巴系统沿逆行方向回流,这引起不适和器官功能障碍。许多疾病可能损害心脏的泵送效率,从而导致充血性心力衰竭,诸如冠状动脉疾病、高血压和心脏瓣膜病症。
除了疲劳之外,充血性心力衰竭的一个突出特征是液体在体内的潴留。通常,重力导致保持的液体积聚到下肢,包括腹腔、肝脏和其他器官,这导致许多相关并发症。液量限制和盐摄入的减少可有助于管理液体潴留,但利尿药物是主要的治疗选择,包括呋塞米、布美他尼和氢氯噻嗪。另外,血管扩张剂和强心药也可用于治疗。
虽然利尿剂可能是有帮助的,但是它们也经常对肾有毒性,并且如果不小心使用,则可能导致急性和/或慢性肾衰竭。这要求在医院中时进行仔细的医疗管理,这消耗大量的时间和资源。因此,在不需要有毒剂量的利尿剂的情况下治疗充血性心力衰竭的液体潴留的能力将可能以显著较少的成本导致更好的患者结果。
液体潴留并不仅限于chf。诸如器官衰竭、肝硬化、肝炎、癌症和感染的病症可能引起在肺附近的液体积聚,称为胸腔积液。空间由两个薄膜(脏胸膜和壁层胸膜)加衬,这两个薄膜对肺的表面和胸壁的内部加衬。通常,仅有几茶匙液体位于该空间中,以便帮助肺在患者的胸腔中平滑地移动,但是潜在的疾病可能增加该量。患有胸腔积液的患者可能需要经由直接引入胸膜的引导针和导管进行频繁的直接引流。这些手术是昂贵的、创伤性的,并且需要住院治疗。
在这点上,需要一种改进的治疗选择,用于体内液体积聚,无论该积聚是由chf、肝硬化、器官衰竭、癌症、感染还是其它潜在疾病引起的。
技术实现要素:
本发明总体涉及治疗由充血性心力衰竭或其它导致胸腔积液、水肿、淋巴水肿或显著液体潴留(例如,深静脉血栓形成、蜂窝织炎、静脉停滞不足或淋巴网络损伤)的病症引起的液体潴留的装置和方法。具体地,治疗装置用于直接地或经由插管在淋巴系统(或其他区域,诸如肺周围的脏胸膜和壁层胸膜)与外部引流装置之间产生临时或永久通道,该外部引流装置可以是主动的(抽吸)或被动的(内部流体动力学压力或重力)。该装置可以临时位于患者体内或者可以植入患者体内更长的时间段。医生可以经由装置安全且可靠地从淋巴系统中去除过多液体,并且在一些实施例中,注射其他治疗剂(例如,电解质、化学治疗剂、强心药、类固醇、抗生素或其他心力衰竭、感染或癌症治疗剂)。
附图说明
本发明的实施例能够实现的这些和其他方面、特征以及优点将参照附图根据本发明的实施例的以下描述而是显而易见的并且被阐明,附图中:
图1、图2和图3例示了根据本发明的引流系统的一个实施例。
图4例示了根据本发明的引流系统的另一实施例。
图5、图6和图7例示了根据本发明的引流系统的另一实施例。
图8、图9、图10、图11和图12例示了根据本发明的可部分植入的引流系统的另一实施例。
图13和图14例示了根据本发明的可植入引流系统的另一实施例。
图15例示了根据本发明的可植入引流系统的另一实施例。
图16例示了根据本发明的可植入引流系统的另一实施例。
图17例示了根据本发明的可植入引流系统的另一实施例。
图18例示了根据本发明的弯曲引导导管的实施例。
图19例示了根据本发明的可植入引流系统的另一实施例。
图20例示了根据本发明的可植入引流系统的另一实施例。
图21例示了根据本发明的可植入引流系统的另一实施例。
图22例示了根据本发明的可植入引流系统的另一实施例。
图23、图24、图25和图26例示了根据本发明的可植入引流系统的另一实施例。
图27例示了根据本发明的可植入引流系统的另一实施例。
图28例示了根据本发明的可植入引流系统的另一实施例。
具体实施方式
现在将参照附图描述本发明的特定实施例。然而,本发明可以以许多不同的形式来具体实施,并且不应被解释为限于本文阐述的实施例;相反,这些实施例被提供为使得本公开将全面且完整,并且将向本领域技术人员完全传达本发明的范围。在附图中例示的实施例的详细描述中使用的术语不旨在限制本发明。在附图中,同样的附图标记提及同样的元件。
淋巴系统是血管系统的一部分和免疫系统的重要组成部分,包括将淋巴朝向心脏定向运送的淋巴管网络。人循环系统通常经由毛细过滤每天平均处理10升血液到淋巴管内,毛细过滤去除血浆而留下血细胞。大部分过滤的血浆被直接再吸收入血管,而剩余的血浆保留在身体的间质液中。淋巴系统为这种未吸收的血浆以及其它生物材料(称为淋巴)提供了到血液的辅助返回路径。一些疾病,诸如充血性心力衰竭,可能导致淋巴水肿或淋巴/液体在淋巴系统内的积聚、以及液体在身体的其他部分中的积聚。
本发明总体涉及治疗由充血性心力衰竭或其它导致胸腔积液、水肿、淋巴水肿或显著液体潴留(例如,深静脉血栓形成、蜂窝织炎、静脉停滞不足或淋巴网络损伤)的病症引起的液体潴留的装置和方法。具体地,治疗装置用于直接地或经由插管在淋巴系统与外部引流装置之间产生临时或永久通道,该外部引流装置可以是主动的(抽吸)或被动的(内部流体动力学压力或重力)。该装置可以临时位于患者体内或者可以植入患者体内更长的时间段。医生可以经由装置安全且可靠地从淋巴系统(或从其它位置,诸如肺)中去除过多液体,并且在一些实施例中,注射其他治疗剂(例如,电解质、化学治疗剂、强心药、类固醇、抗生素或其他心力衰竭、感染或癌症治疗剂)。
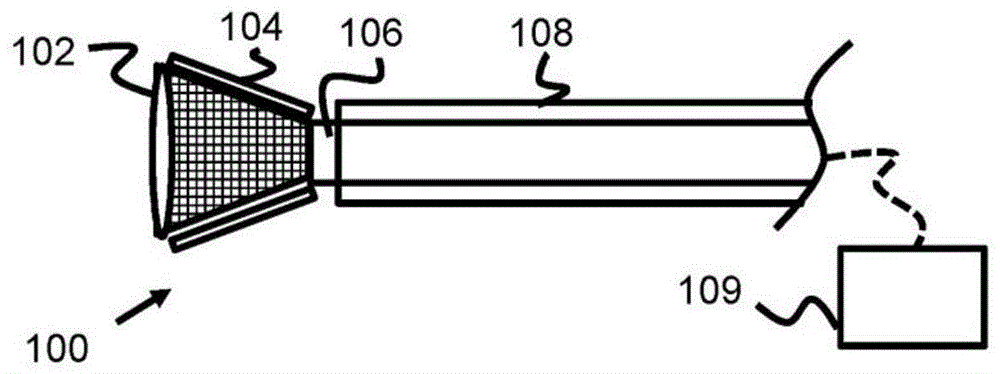
图1例示了淋巴治疗装置100的一个实施例,该淋巴治疗装置可以用于施加引流以去除患者淋巴系统中的淋巴。装置100包括插管主体106,该插管主体为细长的、圆柱形的,并具有穿过其中的内部通道。插管主体106的远端具有径向可扩张部分102,而插管主体106的近端与引流装置109连通以通过插管主体106抽取淋巴。
在一个实施例中,径向可扩张部分102由编织的形状记忆丝(例如镍钛诺)组成,这些线被热定型以扩张为圆锥形状。为了增强高效流动,膜或液体不可渗透层104(例如pet或弹性聚合物)布置在编织丝的上方。可扩张部分102和插管主体106两者均可由单个管状编织形状记忆层组成,使得仅远端部分在不受约束时径向扩张(例如,插管主体106可具有约束其径向扩张的一个或多个聚合物层)。另选地,只有可扩张部分102可由附接到插管主体106的远端的编织的形状记忆丝组成。另选地,径向可扩张部分102可由激光切割管、编织的、非形状记忆丝、可扩张聚合物套管或本领域已知的各种其它结构组成。可扩张部分102可以是圆柱形、圆锥形或其它3d形状。
装置100还可包括控制可扩张部分102的扩张的机构。例如,可纵向移动的外鞘108可最初定位在可扩张部分102上以提供限制。向近端移动鞘108暴露可扩张部分102以允许扩张,而随后向远端移动鞘108将使部分102塌缩。另选地,装置100内可以包括拉丝以控制可扩张部分102的扩张/收缩,或者球囊扩张技术。
装置100以及本说明书中描述的任何其它装置可以连接或定位在淋巴系统10的各种不同位置处,并且经由多种不同的途径连接或定位。一个特别期望的治疗位置是在胸导管12内,参见图2。胸导管12具有所有淋巴系统的最大直径之一,并且可以相对容易地进入。例如,胸导管12将淋巴在胸导管瓣膜/口12a处递送到左锁骨下静脉14中。左锁骨下静脉14可以通过患者的肩部、腿部进入,或者经由导管/导丝系统经由任何其它中心静脉进入部位进入,这允许装置然后穿过胸导管瓣膜/口12a并进入胸导管12中。
装置100可用于经由该左锁骨下静脉途径(或者另选地经由股静脉、颈内静脉、右锁骨下静脉、贵要静脉和肱静脉)进行治疗。例如,导丝可以插入左锁骨下静脉14和胸导管12中。也可以使用其它常用于血管内手术的装置。例如,进入鞘可以前进到左锁骨下静脉14中,引导导管可以在第一导丝上前进,如果必要,第一导丝可以被去除并且用第二、较小直径的导丝替换,并且装置100可以在第二导丝上并且通过引导导管递送。
如图3中看到的,一旦装置的远端定位在胸导管12中的期望位置(诸如在或刚好超过胸导管12的口12a),外鞘108就可以向近端移动以暴露可扩张部分102。可扩张部分102径向扩张至圆锥形,并且外层104允许可扩张部分102在患者体外与胸导管12形成连续通道。然后施加经由引流装置109的引流(例如,吸取、抽吸),这允许淋巴进入可扩张部分102、插管主体106的通道,并且最终到患者体外。当已经执行了期望量的淋巴去除时,外鞘108可以向远端前进(或者插管主体106可以向近端抽出),以使得可扩张部分102径向压缩到外鞘108中。
图4例示了淋巴治疗装置180的另选实施例,该淋巴治疗装置可以用于施加引流以去除患者淋巴系统中的淋巴。与定位到胸导管12中的现有装置100不同,装置180在淋巴去除过程期间可以大部分或完全保持在左锁骨下静脉14内。
装置180包括具有远端可扩张部分184的导管主体182,该可扩张部分使引流开口186(其可以另选地用于输注)抵靠胸导管12的开口或口12a扩张,这允许淋巴引流到延伸穿过导管主体182的引流通道188中。在一个示例中,远端可扩张部分184包括远端圆形球囊184a和近端圆形球囊184b,它们都是可膨胀的以引起远端可扩张部分184的径向扩张。优选地,球囊184a、184b定位在胸导管开口的近端和远端以及左锁骨下静脉14内,这允许它们扩张并隔离胸导管12的开口。一旦扩张,血液继续通过在远端可扩张部分184的各个端开口的灌注通道184c,并且通过将左锁骨下静脉14扩张到比其自然具有的直径更大的直径,可以使该血液灌注最大化。
装置180还可包括在口12a处打开胸导管12的瓣叶的结构。在一个示例中,该结构187可以是形成管状形状或相对于装置180的轴线垂直突出的一个或多个细长形状的可膨胀球囊结构187。在另一示例中,结构187可以是由形状记忆丝(例如,垂直编织管状结构或垂直丝环)组成的自扩张结构。
虽然图中未示出,但是膨胀通道优选地延伸穿过导管主体182和远端可扩张部分184以连接到两个球囊184a、184b。该设计的一个优点是,不一定需要诸如荧光透视法的高保真度成像,而可能只潜在地需要经胸廓超声(tte)。另一个优点是,球囊可以帮助为静脉提供刚性支撑,从而防止其在引流过程期间塌缩,尤其是在施加吸取时。
虽然远端可扩张部分184被例示为具有单个孔口186,但是也可以具有径向地围绕远端可扩张部分184定位并且在球囊184a、184b之间的多个孔口。这可以消除对特定旋转取向的需要。
远端可扩张部分184被例示为具有外膜184d,引流开口186位于其上。在另选的示例中,外膜184d可以不存在,并且引流开口186可以位于近端圆形球囊184b的内侧上。换言之,远端可扩张部分184将由两个球囊184a、184b、灌注通道184c和穿过近端球囊184b的引流管组成。在这点上,球囊在灌注通道184c与静脉14的内表面之间产生封闭的空间。在另一示例中,远端可扩张部分184可以由沿着远端可扩张部分184的整个长度延伸的单个管状球囊组成。
装置180可以可选地包括一个或多个探头(例如,从装置的远端延伸的细长丝),以提供触觉响应,用于实现期望的定位。深度标记物也可以沿着导管主体182的长度存在,以进一步帮助相对于接入点瞄准期望的位置。
图5至图7例示了淋巴治疗装置190的另选实施例,该装置仅部分地被植入以施加引流以去除患者淋巴系统中的淋巴。装置190包括支架部分192和连接到支架部分192的细长导丝194,导丝提供用于定位引流导管196的引导或跟踪系统。支架部分192可以是在胸导管12内扩张的自扩张或球囊扩张的支架状结构(例如,如图6中看到的,或者靠近环12a或者更深地进入管12中)。导丝194可以打结、成环、焊接、胶粘或以其它方式永久地固定到支架部分192,并延伸出管12进入左锁骨下静脉14中。导丝194的近端可以盘绕或附接到更大的取回结构;两者都可以放置在皮下。由于导丝194可在患者体内保持延长的时间,因此其优选地具有防止凝血或组织向内生长的涂层。
当患者需要治疗时,可以进入导丝194的近端的经皮位置,并且可以使引流导管在导丝194上前进并进入胸导管12中以开始引流。装置190可以留在患者体内用于将来的治疗环节。另选地,装置190可以用于单个治疗环节,并且在去除引流导管196之后从患者去除,和/或引流导管可以永久地连接/植入患者。在一个实施例中,经皮进入部位可以包括便于引流导管的多次进入的端口或类似装置。
本发明还设想一种方法,该方法临时或永久地保持靠近口12a的胸导管12的瓣叶打开,以允许一些慢性引流在引流环节之间进入静脉系统。该方法包括以下步骤:将可植入装置递送到胸导管12中;将装置定位通过胸导管瓣膜,以便将瓣膜维持在部分打开的位置并允许液体从胸导管12移动到左锁骨下静脉14中。
在一个实施例中,装置190可以允许在利用引流导管196的引流环节之间进入静脉系统中的一些长期引流。例如,支架部分192可以定位在淋巴口12a的小叶处或附近,以便保持通向管12的瓣膜部分地打开,以允许被动引流到静脉系统中。另选地,引流导管196可以包括多个引流孔口,这些引流孔口位于引流导管196的近端部分中,使得它们可以定位在静脉系统中并且允许引流到静脉系统中。这些孔口可以被选择性地阻塞(例如,通过使另一个导管或引流构件直接穿过导管196以便阻塞这些孔口)。在另一实施例中,导丝194可以包括扩大构件,该扩大构件固定到导丝194或在导丝194上滑动并且定位在管14的瓣膜内以将其维持在部分打开的位置。应当理解,本说明书的其它实施例也可以用于在短时间内(例如,在手术期间1-2小时)或经由植入装置慢性地(例如,数周、数月或数年)执行该慢性引流的方法。
图8至图12例示了淋巴治疗装置100的另一实施例,该装置包括支架112,该支架植入患者体内并且可以选择性地重新连接到插管118,该插管118联接到引流装置109以去除淋巴。如图11中看到的,支架112可以经由肩部和左锁骨下静脉14以及本说明书中其它地方描述的其它部位递送到胸导管12。首先使支架递送导管116在胸导管12内前进,直到其远端位于期望的支架递送位置,诸如刚好超过胸导管12的口12a和瓣叶。然后使支架112在胸导管12内暴露并扩张。这可能是因为支架是径向自扩张的(例如,由编织的、热定形的、形状记忆丝组成)并前进到导管116外,或者从与支架一起在其中扩张的集成的或单独的可膨胀球囊和/或球囊导管扩张。
然后,从患者体内抽出递送导管116,使插管118在胸导管12内前进,并且将插管118的远端附接到支架112的近端。另选地,可以将支架112放置在胸导管12的瓣膜上,以将其维持在打开位置,以在附接递送导管之间的时间内实现慢性引流,如前面其它实施例讨论的。在该实施例中,支架112和/或螺纹部分114可以包括可由医师选择性打开的瓣膜。
在一个实施例中,支架包括近端螺纹部分114。螺纹部分114可以具有沿着其内径(如图9中看到的)或者在其外径上的螺纹114a。插管118包括远端螺纹部分119,该远端螺纹部分在其外径上具有多个配合螺纹,如图10中看到的,或者沿着其内径具有多个配合螺纹,并且这些配合螺纹定位和构造成与螺纹114a接合。当远端螺纹部分119接触近端螺纹部分114时,医师旋转插管118,将二者连接在一起。螺纹部分114在直径上可相对接近扩张的支架112或可具有较小的直径,这使得支架形成圆锥形近端。在螺纹部分114的较小直径的情况下,可能期望包括液体密封的外层或膜(例如,聚合物)以增强引流。一旦已经去除期望量的淋巴,医师可以沿相反方向旋转插管118以旋开支架112,并且可以从患者体内去除插管118。优选地,不透射线的标记物至少位于螺纹部分114处/附近,以向医师提供关于支架位置的指导(尽管对于随后的穿刺,也可能期望沿着支架的其它位置处的标记物)。
用于支架112的其它附接机构也是可能的。例如,支架的近端可以包括一个或多个钩,这些钩可以闩锁到插管118的其它特征上。在另一示例中,支架112可在其远端上具有环形柔性环,该环允许插管118的远端压靠。当启动引流时,来自插管118的引流力将使插管118的远端压靠支架112的近端。因此,不需要物理闩锁/连接机构。
图20中可以看到附接系统的另一示例,该附接系统使用多个磁体来连接支架和插管/导管123。具体地,植入的支架112包括多个位于其近端、暴露端的磁体112a。导管123具有沿着其侧面(或另选地在其端部)的开口123a,多个磁体123b和软聚合物材料123c围绕其圆周。当磁体112a和123b定位在彼此的接近度内时,它们彼此吸引,软聚合物材料123c帮助与支架112(以及可选地与支架可具有的任何内/外套管或层)建立密封。可选地,在任一装置上仅需要一组磁体,并且另一材料可包括被吸引到磁体的含铁金属。磁体123b可以直接位于导管123的主体上,或者可以定位在软聚合物材料123c上以允许少量的移动。类似的聚合物材料布置也可位于支架112的端部上。
图21例示了与图20类似的磁性附接系统的另一示例。然而,代替仅定位在瓣膜/口12a处的支架112,支架170延伸到左锁骨下静脉14中。具体地,支架170包括:第一部分170a,该第一部分具有大体笔直的轮廓,该轮廓抵靠口12a扩张;和弯曲的第二部分170b,该第二部分从第一部分170a的近端延伸。弯曲的第二部分170b可以是大体管状结构,如图中看到的,或者可以是开口的曲面或凹面。第二部分170b的近端包括多个磁体170c,这些磁体可以吸引引流导管172的远端上的多个磁体172b。多个磁体172b可以安装在有助于密封第二部分170b的近端的软聚合物材料172a(以及第二部分可以由其组成的任何内/外套管或材料)上或附近。在一个示例中,软聚合物材料172a在扩张时形成圆锥形。因此,与植入支架的可去除连接可发生在导管的一侧(图20)或导管的远端(图21)。
图20和图21的任一实施例可以包括传感器系统,该传感器系统确定支架和导管的磁体何时彼此连接。例如,这可以通过允许磁体的连接完成通过导管、进入支架、并回到导管中的电路路径来实现。导管可以包括在其近端上的电源,该电源既为电路供电又在电路完成时启动指示器。
可选地,具有可膨胀球囊125a的导管125可经由导管125(或本文所述的其它类似导管)插入穿过支架112,如图22中看到的。使该球囊125a快速膨胀可帮助增加淋巴系统内的驱动压力,从而增加引流速率。可选地,使该球囊125a快速缩小可以帮助降低胸导管最近端部分的压力,从而将淋巴液从主胸导管中拉出。可选地,如果球囊125a被导航得更深、更远端地进入主胸导管,然后扩张,然后朝向胸导管的开口拉回,则这将产生真空效应,从而用球囊抽出淋巴液。
图13例示了可植入淋巴装置120的一个实施例,该淋巴装置具有细长管状部分126,该细长管状部分在其远端连接到可扩张锚定部分122并在其近端连接到端口128。另选的构造可以是在支架上具有倒钩或钩,这些倒钩或钩可以通过抓握周围组织并且保持装置牢固地附接到组织壁来用于将支架稳定在胸导管内。如图14中最佳看到的,可扩张锚定部分122可扩张并锚定在淋巴系统10的一部分内,诸如胸导管12内。细长管状部分126朝向皮肤延伸,诸如靠近肩部延伸,并被端口128密封。在一个示例中,细长管状部分126具有占据胸导管12的直径的约40-60%的扩张直径,以允许装置120周围的正常淋巴引流。通常,胸导管12在被支持时和在压力下可以扩张到15mm大的直径,因此,细长管状部分126的直径可以在5.5mm至8.5mm的范围内,或大约7.5mm以允许其正常引流。
在一种构造中,端口128位于皮肤下面,如图14中看到的。在另一构造中,细长管状部分126延伸出皮肤,使得端口128位于身体外部。外部定位对于装置的相对较快的临时使用可能特别有用,诸如仅当患者入院时。细长管状部分126的远端包括向外渐缩至锚定部分122的圆锥形状。另选地,锚定部分122可具有近端,该近端向近端渐缩至细长管状部分126的直径。
可扩张锚定部分122可具有圆柱形状,该圆柱形状可从较小的压缩直径径向扩张至较大的扩张直径。锚定部分122可由多个织造/编织金属丝或由激光切割的圆柱形成。锚定部分122可由形状记忆材料组成,例如镍钛诺,该材料在不受约束时自扩张至其径向扩张直径。作为自扩张的另选方案或除此之外,当锚定部分122定位在胸导管12内时,可以使用球囊导管来扩张锚定部分122。在一个示例中,锚定部分12扩张到3mm至8mm范围内的直径。
锚定部分122可以可选地包括圆柱形盖104,该盖布置在锚定部分122的外表面上。该盖104可以减少锚定部分122与递送装置(例如,递送导管)之间的摩擦,并且进一步覆盖存在于锚定部分122中的任何孔口(例如,由编织的丝引起的),以增强引流压力。在一个示例中,盖124由诸如pet或弹性聚合物的生物相容聚合物膜组成。
细长管状部分126优选地被结构化成既柔性又抗扭。在一个实施例中,管状部分126由附接、嵌入或夹在防止液体泄漏的生物相容性聚合物层之间的螺旋丝卷126a(单丝或多丝)组成。例如,可以将丝紧紧地织造在圆柱形心轴周围并热定形,然后可以将一个或多个液体不可渗透层附接到卷。使用螺旋卷126a提供了附加的壁强度,当应用抽吸时,该附加的壁强度可以相对于为无丝加强的管更好地抵抗塌缩。在另一实施例中,代替丝卷126a或除此之外,可以使用管状编织丝结构。可选地,除了在管状部分126的远端处的开口之外或者代替远端开口,多个引流孔126b可以沿着管状部分126的长度以各种间隔隔开,与内部引流通道一起延伸,从而允许管状部分126吸入液体。在一个示例中,多个孔口可以包括在围绕管状部分的圆周的位置处,并且可以以1cm至3cm的增量彼此纵向隔开。在一个示例中,管状部分126具有2cm到64cm之间的长度,且具有沿着其整个长度间隔一定距离的孔口126b。
管状部分126的远端连接到锚定部分122的近端,并且至少部分地定位在胸导管12内,以便在管12与其近端处的端口128之间形成连续通道。在一个示例中,管状部分106具有0.5m至1m范围内的长度。
端口128可由刚性管状或圆形结构组成,该结构具有允许注射器针头穿透的自密封中间或内部部分。例如,自密封部分可由柔性硅树脂或类似聚合物组成。如前所述,端口128可以具有相对薄的形状以允许植入患者的皮肤下,或者如果定位在皮肤外部,可以具有相对窄的形状。在端口128位于身体外部或旨在通过切割患者的皮肤以便治疗而直接接近的示例性使用中,端口128可以包括能够由医师打开/关闭的阀(例如,陶西-博斯特(tuohy-borst)式阀)。
如图13中看到的,装置120还可包括沿其长度的导丝通道130,该导丝通道用于允许导丝132通过。该通道120可以帮助将装置120递送到胸导管12。可能期望在植入装置132之后将导丝132留在患者体内,以帮助防止通道130被蛋白质和其它材料堵塞。
在端口128位于身体外部或旨在通过切割患者的皮肤以便治疗而直接接近的示例性使用中,装置可包括可去除的管心针121,该管心针在不使用时阻塞装置100的通道,但可在治疗过程期间去除。管心针121防止蛋白质和其它材料积聚和堵塞装置120的通道。优选地,管心针121具有细长的柔性主体,该主体符合植入装置120的位置/构造。管心针121的远端包括环形密封件121a,该密封件优选地由弹性的可压缩材料组成,该材料抵靠装置120的内表面扩张。例如,海绵材料、硅树脂甚至水凝胶材料可以用于密封件121a。管心针121可具有一定长度,以便将密封件121a定位在锚定部分122、细长管状部分126的远端圆锥形部分中,或定位在细长管状部分126的更均匀部分中。
在单独的构造中,如果或当装置留在适当位置较长的时间段时,中心插管可以从近端到远端沿着液体管腔向下前进并且留在适当位置以阻塞流动并且限制随后的堵塞。插管/管心针可以制造有柔软的远端,该远端能够在管腔中时压缩,使得主动地排除液体。在另一实施例中,阻挡管心针可以前进到远端导管之外,这允许扩张,并且当被逆行拉向远尖端时阻挡液体。如果装置长时间保持植入,其中维持通畅是重要的考虑因素,则可以使用该构造。
如同本说明书的任何实施例,装置120可通过借助肩部或任何其它路径进入左锁骨下静脉14到达中央静脉系统然后前进到胸导管12来递送。递送过程可包括:首先将第一导丝前进到期望的胸导管位置,将鞘插入左锁骨下静脉14中,使引导导管在第一导丝上前进,用较小的第二导丝代替导丝,以及经由递送导管(诸如递送导管116)通过引导导管递送装置120。如果端口128要保持在患者的皮肤下,则可以在患者的肩部内挖空/产生空间。
图16例示了可植入的淋巴治疗装置140的另选实施例,该装置大体类似于前述装置120,包括递送技术。然而,代替端口,细长部分126的近端连接到其中积聚淋巴的贮存器142。贮存器142可以由液体不可渗透的材料组成,该材料在用针头穿透之后完全封闭并且自密封(例如,用于引流或递送治疗药物)。例如,贮存器142可由柔性聚合物组成,诸如硅橡胶、聚乙烯、聚氨酯、聚醚醚酮(peek)等。贮存器也可以由3维金属长丝或纤维织物制成,该织物被涂布以使其不透液体。贮存器142还优选地被植入在皮肤附近,使得当需要治疗时,医师可以容易地用针头穿过皮肤接近它。
图17例示了可植入淋巴治疗装置150的另一类似变型,该装置包括与细长部分126连通的端口128和贮存器142。在这方面,医师可以使用针头经由贮存器142去除/添加以进行治疗,或者可以接近端口128以进行治疗(例如,尤其是在端口128在患者外部时,这允许更大的胸导管进入)。
如前所述,在手术期间,可能期望使引导导管在放置在左锁骨下静脉14和胸导管12中的导丝上前进。图18例示了放置在导丝155上的一个这种引导导管156,该导丝具有被偏置成弯曲形状的远端部分156b。该弯曲形状有助于引导导管156从进入左锁骨下静脉14移动和过渡并进入胸导管12的瓣膜/口12a中。在一个示例中,远端部分156b在大约1-3cm范围内的长度上具有大约90度范围内的弯曲。
本说明书的任何实施例还可以包括用于监测患者的各个方面的传感器,诸如压力传感器、流量传感器、细胞物质传感器、蛋白质含量传感器和基因分析传感器。例如,图19例示了与前述实施例类似的可植入淋巴装置160。然而,它包括远端传感器162。传感器162可以位于锚定部分122中、细长部分126的远端处、端口128处、或沿着装置并在装置内的任何其它位置处。
虽然传感器162可以测量胸导管12内的环境,但是第二传感器166也可以沿着装置160的外部定位在一定距离处,以测量左锁骨下静脉14(或者装置定位在其中以到达胸导管12的任何血管)内的数据。再次,这里可以使用压力传感器、流量传感器、细胞物质传感器、蛋白质含量传感器和基因分析传感器。在这方面,装置160可以测量例如胸导管压力和血压两者。
传感器162和166例如经由嵌入的线连接到端口128中的通信装置164。通信装置164可以包括微控制器(或类似的处理器)、用于数据存储的存储器、以及无线通信收发器(例如,蓝牙、wifi),这允许通信装置接收并至少临时存储传感器数据,然后将该数据发送到外部装置。
装置160允许多种不同的使用方法。例如,如果传感器162是压力传感器,则医师可以在监测压力的同时抽出淋巴液。一旦淋巴压力达到期望的水平,液体抽出过程就可以停止。
在另一示例中,患者可以通过将装置160连接到他们的电话或类似装置来在家监测他们的压力。然后,装置/电话上的应用程序可以用于警告患者他们的淋巴压力已经达到需要抽出的水平,和/或可以发送到护理站或云站点,以便医师或护士确定是否需要进一步的治疗。然后,可以通过监测压力的医疗设施联系患者以安排液体抽出预约。
虽然许多患者可以受益于如前所述的淋巴引流,但是这种类型的引流受到蛋白质和淋巴细胞损失的挑战,这可能导致免疫功能受损。减少该蛋白质损失同时仍提供引流的一种方法是创建从患者淋巴系统到其身体的低压区的分流器。例如,分流器可以连接到膀胱、小肠、右心房或右心室。
图23至图26例示了一个示例分流器200的各个方面及其在患者体内的使用。首先转到图23,经由股静脉进入患者的下腔静脉22,这允许导管204前进到淋巴系统的乳糜池20附近的位置。接着,使针头206在刺穿下腔静脉和乳糜池20的方向上前进离开导管204。一旦针头206到位,就使分流器或透析导管200在针头206上前进,使得其远端位于乳糜池内。导管的远端可具有允许导管的远端固定在淋巴系统的乳糜池或另一部分内的几何形状或锚。例如,远端可以包括可膨胀球囊锚或支架状自扩张锚。接着,将分流器200的远端植入体内的引流位置。该位置可以是膀胱(如图25中看到的)、十二指肠、肠、皮下端口或人工皮下贮存器、或类似位置。类似地,导管的这一端可能需要允许导管在体内引流位置内固定和止血的几何形状或锚。例如,远端可以包括可膨胀球囊锚或支架状自扩张锚。在用于膀胱24或十二指肠的情况下,可以在分流器200的近端附近包括单向阀202,以仅允许液体进入该位置,而不能回流到淋巴系统。
在图26中看到的一个实施例中,分流器200包括本领域通常已知的多根透析纤维200a。在一个示例中,这些纤维是中空的并且具有约200微米的直径,这允许中空纤维的壁充当透析膜。纤维可由各种材料组成,例如纤维素基材料和合成聚合物。
分流器200的外管状壁200b优选由防水/防液体材料(例如聚氨酯)组成,该材料防止非淋巴液体被吸收。壁200b也可由多孔结构(例如,75-100微米直径)组成,该结构可帮助与周围组织产生动脉内皮和新内膜生长。分流器200可以临时地、短期地或长期地被植入。在该示例中,外管状壁200b被构造为进入与脆弱的天然组织和管的界面中的慢性植入物。在该示例中,管状壁200b由多孔的圆柱形结构组成,该结构具有防止其塌缩的强径向分量。它还具有高度的顺应性,并且可以是允许弯曲和防止塌缩的任何弹簧结构或交叉编织构造,75-100微米直径有助于允许在壁200b周围形成血管翳,形成内皮,由此产生完全生物表面。
图27例示了分流器200在患者体内将患者的淋巴系统引流到右肺静脉34中的另一个示例使用。分流器200的一端可以包括可扩张的支架部分102,并且可以如本说明书前述的那样固定在胸导管12内。分流器200通过左锁骨下静脉12定位并进入上腔静脉30,刚好在心脏32上方。然后分流器200通过上腔静脉30的壁定位并进入右肺静脉34。在淋巴引流不良的患者中,右肺静脉34中的压力可能相对低于胸导管12中的压力,因此可提供更好的淋巴系统引流。可选地,分流器中还可以包括单向阀以帮助维持液体流入右肺静脉34。可以在分流器的端部添加特征以帮助止血和锚定。这些特征可包括由金属或聚合物制成的自扩张或球囊扩张支架状结构。
图28例示了分流器200的另一示例使用,其类似于图27,但相反引流到左心房32b中。再次,分流器200经由支架部分102锚定在胸导管12中,并通过左锁骨下静脉14定位并进入上腔静脉30。从那里,分流器200进入右心房32a,通过隔膜定位,并终止于左心房32b。因此,胸导管12可以引流到左心房32b的相对较低压力区域中。可以在分流器的端部添加特征以帮助锚定。这些特征可包括由金属或聚合物制成的自扩张或球囊扩张支架状结构。
虽然本说明书的实施例主要是针对淋巴系统的引流进行描述的,但是应当理解,这些实施例和方法可以用于其它状况的引流。一个示例是胸腔积液,胸腔积液是由于许多不同的潜在医疗状况,在肺周围和胸膜空间内累积了非常大量的液体。该空间由两个薄膜(脏胸膜和壁层胸膜)加衬,这两个薄膜对肺的表面和胸壁的内部加衬。通常,仅有几茶匙液体位于该空间中,以便帮助肺在患者的胸腔中平滑地移动,但是潜在的疾病可能增加该量。胸腔积液通常由器官衰竭、癌症和感染引起。患有胸腔积液的患者可能需要经由直接引入胸膜的引导针和导管进行频繁的直接引流。这些手术是昂贵的、创伤性的,并且需要住院治疗。
图29例示了用于胸腔积液的另一种治疗方法,其中,分流器200或另选地植入的引流导管用于将胸膜引流到皮下端口128或身体中的另一位置,诸如膀胱或小肠。在一个实施例中,递送导管通过股静脉前进并进入腔静脉。导管的针头或位于导管中的针头前进到下腔静脉的接合处的正上方并朝向隔膜进入胸膜空间中。
一旦递送导管位于胸膜空间内,分流器200或引流导管就可前进到胸膜空间42中(并且尤其是进入保留过多液体的区域中)。取决于液体如何被保持以及被保持在哪里,分流器200可以沿着肺40下方的隔膜的底部(例如,以环路形式)或仅沿着胸膜空间的一部分被来回定位。
分流器200的结构可以根据分流器200引流到哪里而变化。例如,如果分流器200引流到皮下端口128,则它可以具有大体中空的管状通道,该管状通道具有沿着定位于肺40下方的部分定位的多个引流孔口。在另一示例中,如果分流器200引流到肠、膀胱或其它内部位置,则分流器200可以由透析纤维组成,如图27的实施例所讨论的,并且可以进一步包括单向阀以限制液体直接移动。这些分流器200实施例的任一个都可允许引流过多液体,而且可允许否则将损失的液体中的重要生物物质的再吸收。
在任何前述实施例中,锚定部分122或支架112可包括抗血栓和/或抗细胞涂层。这些可以帮助减少装置的阻塞或细胞过度生长。
虽然本说明书的实施例主要是就从淋巴系统中去除淋巴进行描述,但是应当理解,治疗剂也可以经由任何所述装置加入淋巴系统中。一旦装置已经插入和/或植入,治疗剂就可以相应地注射到装置中(例如,注射到导管、端口或管腔中)。例如,治疗剂可以包括电解质、化学治疗剂、类固醇、抗生素或其它心力衰竭或癌症治疗剂。
在包括可植入装置的任何实施例中,应当理解,它们可以在以后的日期去除。例如,可以使恢复鞘在植入物上前进,这使其压缩。然后,可以从患者体内去除鞘和装置。
虽然本说明书的实施例已经被描述为经由肩部和左锁骨下静脉植入,但是其它进入点也是可能的。例如,装置可经由腹股沟前进到锁骨下静脉和胸导管。
在本发明的另一方面,本说明书的任何装置可用于抽出淋巴以筛选恶性细胞或指示诸如转移癌的内部疾病状态的其它细胞。
尽管已经根据特定实施例和应用描述了本发明,但是本领域普通技术人员根据该示教可以在不脱离所要求保护的发明的精神或超出所要求保护的发明的范围的情况下生成附加实施例和修改。因此,应当理解,本文的附图和描述是通过示例的方式提供的,以便于理解本发明,而不应被解释为限制本发明的范围。
- 还没有人留言评论。精彩留言会获得点赞!