包含双特异性抗CD37抗体的药物组合物的制作方法
包含双特异性抗cd37抗体的药物组合物
发明领域
1.本发明涉及包含特异性结合人cd37抗原的双特异性抗体的药物组合物。本发明特别涉及包含结合人cd37抗原的不同表位的cd37特异性双特异性抗体分子的药物组合物,其中该双特异性抗体分子与细胞表面上的cd37结合后具有增强的fc
‑
fc相互作用,因此具有增强的效应器功能。本发明还涉及含有这些分子的药物组合物用于治疗癌症和其他疾病的用途。
2.发明背景
3.白细胞抗原cd37(“cd37”),也称为gp52
‑
40、四跨膜蛋白(tetraspanin)26或tspan26,是四跨膜蛋白超家族的跨膜蛋白(maecker et al.,faseb j.1997;11:428
‑
442)。在正常生理中,cd37在前b至外周成熟b细胞阶段期间在b细胞上表达,但据报道在浆细胞上缺乏(link et al.,j pathol.1987;152:12
‑
21)。cd37抗原仅在t细胞和髓样细胞如单核细胞、巨噬细胞、树突细胞和粒细胞上弱表达(schwartz
‑
albiez et al.,j.immunol1988;140(3):905
‑
914)。cd37在多种b细胞白血病和淋巴瘤,包括非何杰金淋巴瘤(nhl)和慢性淋巴样白血病(cll)中的恶性细胞上广泛表达(moore et al.j immunol.1986;137(9):3013)。
4.正在评估几种基于抗体的cd37靶向药物作为b细胞恶性肿瘤和其他恶性肿瘤的潜在治疗剂。这些包括例如放射免疫缀合物如抗体
‑
药物缀合物如imgn529和ags
‑
67e和重整或fc工程化的抗体如otlertuzumab和bi 836826(robak and robak,expert opin biol ther 2014;14(5):651
‑
61)。已经提出抗cd37抗体以上述形式和其他形式用作治疗剂(参见例如wo 2012/135740,wo 2012/007576,wo 2011/112978,wo 2009/126944,wo 2011/112978和ep 2 241 577)。
5.betalutin是一种与177
‑
镥缀合的小鼠抗cd37抗体lilotomab(以前为hh1/tetulomab)。betalutin迅速内在化,在体外抑制b细胞生长,并在i.v.daudi
‑
scid模型中延长存活(dahle et al 2013,anticancer res 33:85
‑
96)。
6.imgn529是一种由经由smcc接头与美登素类化合物(maytansinoid)dm1缀合的k7153a抗体组成的adc。据报道,在没有交联的情况下k7153抗体对表达cd37的ramos细胞诱导凋亡。它也能在伯基特淋巴瘤细胞系中诱导cdc和adcc,尽管与利妥昔单抗相比,诱导cdc的能力要低得多(deckert et al,blood 2013;122(20):3500
‑
10)。在缀合有dm
‑
1的抗体中保留了k7153a的这些fc介导的效应器功能。
7.agensys正在开发ags
‑
67e,一种与单甲基澳瑞他汀e(monomethyl auristatin e)缀合的人抗cd37 igg2 mab。ags67e诱导有力的细胞毒性和凋亡(pereira et al,mol cancer ther 2015;14(7):1650
–
1660)。
8.otlertuzumab(最初称为tru
‑
016)是一种smip(小模块免疫药物;smips是单链蛋白质的二硫化物连接的二聚体,其包含一个抗原结合vh/vl、连接铰链区和fc(片段,可结晶)区(ch2
‑
ch3))。它的作用机制是诱导凋亡和adcc,而不是cdc(zhao et al 2007,blood 110(7),2569
‑
2577)。
9.mab37.1/bi 836826是一种经工程化改造而与fcγriiia(cd16a)高亲和力结合的
嵌合抗体(heider et al 2011,blood 118:4159
‑
4168)。它具有不依赖于igg fc交联的促凋亡活性,尽管促凋亡活性通过交联而增加。它显示了cd37+b细胞系和原代cll细胞的有力adcc。
10.尽管本领域有这些和其他进展,但是仍然需要用于治疗癌症和其他疾病的改良的抗cd37抗体和其稳定的药物配制剂。
11.发明概述
12.pct/ep2018/058479(未公开)(其通过引用并入本文)提供了用于治疗癌症和/或其他疾病的抗cd37抗体,包括具有从两个亲本抗体中获得的结合臂的双特异性抗体,所述结合臂结合cd37上的不同表位并且所述双特异性抗体与结合所述不同表位的两个亲本单克隆抗体的组合和/或单独的任一亲本单克隆抗体相比具有增加的cdc和/或adcc。此外,pct/ep2018/058479提供了结合cd37上的两个不同表位的双特异性抗体,并且所述双特异性抗体与相同同种型且与所述双特异性抗体具有相同结合臂的双特异性抗体相比在结合质膜上的cd37后具有增强的fc
‑
fc相互作用。
13.本发明提供了稳定的药物组合物,其包含具有结合cd37上的不同表位的结合臂的双特异性抗体。
14.因此,一方面,本发明涉及药物组合物,其包含:
15.a)双特异性抗体,
16.b)组氨酸缓冲剂,
17.c)50至300mm的糖和/或50至300mm的多元醇,和
18.d)0.01至0.1%的聚山梨酯80,
19.其中所述组合物的ph在4.5和6.8之间,并且
20.其中所述双特异性抗体包含结合具有seq id no:62的序列的人cd37的第一和第二抗原结合区和人免疫球蛋白的第一和第二fc区,其中所述第一和第二fc区包含一个或多个氨基酸突变,所述氨基酸突变与没有所述突变的双特异性抗体之间的fc
‑
fc相互作用相比增强结合膜结合的靶物后所述双特异性抗体之间的所述fc
‑
fc相互作用,
21.其中所述第一抗原结合区包含cdr序列:
22.以seq id no:16所示的vh cdr1序列
23.以seq id no:17所示的vh cdr2序列
24.以seq id no:18所示的vh cdr3序列,
25.以seq id no:20所示的vl cdr1序列,
26.vl cdr2序列:kas,和
27.以seq id no:21所示的vl cdr3序列,
28.并且其中所述第二抗原结合区包含cdr序列:
29.以seq id no:23所示的vh cdr1序列,
30.以seq id no:24所示的vh cdr2序列,
31.以seq id no:25所示的vh cdr3序列,
32.以seq id no:27所示的vl cdr1序列,
33.vl cdr2序列:yas,和
34.以seq id no:31所示的vl cdr3序列。
35.在本发明的一个实施方案中,药物组合物包含:
36.e)双特异性抗体,
37.f)组氨酸缓冲剂,
38.g)50至300mm的糖和/或50至300mm的多元醇,和
39.h)0.01至0.1%的聚山梨酯80,
40.其中所述组合物的ph在4.5和6.8之间,和
41.其中所述双特异性抗体包含第一抗原结合区,其包含以seq id no:124所示的重链和以seq id no:119所示的轻链,并且其中第二抗原结合区包含以seq id no:125所示的重链和以seq id no:126所示的轻链。
42.本发明还提供了稳定的药物组合物,其包含具有结合cd37的结合臂的抗体。
43.因此,一方面,本发明涉及药物组合物,其包含:
44.a)抗体,
45.b)组氨酸缓冲剂,
46.c)50至300mm的糖和/或50至300mm的多元醇,和
47.d)0.01至0.1%的聚山梨酯80,
48.其中所述组合物的ph在4.5和6.8之间,和
49.其中所述抗体包含结合具有seq id no:62的序列的人cd37的第一抗原结合区和人免疫球蛋白的第一和第二fc区,其中所述第一和第二fc区包含一个或多个氨基酸突变,所述氨基酸突变与没有所述突变的双特异性抗体之间的fc
‑
fc相互作用相比增强结合膜结合的靶物后所述抗体之间的所述fc
‑
fc相互作用,其中所述第一抗原结合区包含cdr序列:
50.以seq id no:16所示的vh cdr1序列
51.以seq id no:17所示的vh cdr2序列
52.以seq id no:18所示的vh cdr3序列,
53.以seq id no:20所示的vl cdr1序列,
54.vl cdr2序列:kas,和
55.以seq id no:21所示的vl cdr3序列。
56.在另一方面,本发明涉及药物组合物,其包含:
57.e)抗体,
58.f)组氨酸缓冲剂,
59.g)50至300mm的糖和/或50至300mm的多元醇,和
60.h)0.01至0.1%的聚山梨酯80,
61.其中所述组合物的ph在4.5和6.8之间,和
62.其中所述抗体包含结合具有seq id no:62的序列的人cd37的第二抗原结合区和人免疫球蛋白的第一和第二fc区,其中所述第一和第二fc区包含一个或多个氨基酸突变,所述氨基酸突变与没有所述突变的双特异性抗体之间的fc
‑
fc相互作用相比增强结合膜结合的靶物后抗体之间的所述fc
‑
fc相互作用,其中所述第二抗原结合区包含cdr序列:
63.以seq id no:23所示的vh cdr1序列,
64.以seq id no:24所示的vh cdr2序列,
65.以seq id no:25所示的vh cdr3序列,
66.以seq id no:27所示的vl cdr1序列,
67.vl cdr2序列:yas,和
68.以seq id no:31所示的vl cdr3序列。
69.在其他方面,本发明涉及本发明的药物组合物用于制备药物的用途以及涉及治疗方法,包括施用本发明的药物组合物。
70.附图简述
71.图1:原代cll肿瘤细胞上由g28.1变体介导的cdc。在体外测定(a)igg1
‑
g28.1
‑
k409r
‑
delk,igg1
‑
g28.1
‑
e345r或igg1
‑
b12
‑
e345r(细胞:患者衍生,新诊断/未治疗(pb=外周血衍生))和(b)igg1
‑
g28.1,igg1
‑
g28.1
‑
e430g或igg1
‑
b12(细胞:患者衍生,新诊断/未治疗(bm=骨髓衍生))诱导对原代cll肿瘤细胞的cdc的能力。显示的数据是通过流式细胞术测量死细胞(对应于pi阳性细胞)的百分比确定的裂解%。
72.图2:定量测定cll肿瘤细胞上cd37,cd46,cd55和cd59表达水平。通过流式细胞术测定来自一名患者(新诊断/未治疗的患者vm
‑
pb0005)的cll细胞上的cd37,cd46,cd55和cd59的表达水平。抗原量显示为分子/细胞。migg1是小鼠igg1,κ同种型对照。
73.图3:人源化cd37抗体及其变体与daudi细胞的结合。通过流式细胞术测定igg1
‑
004
‑
h5l2,igg1
‑
004
‑
h5l2
‑
e430g,igg1
‑
005
‑
h1l2,igg1
‑
005
‑
h1l2
‑
e430g,igg1
‑
010
‑
h5l2,igg1
‑
010
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2和igg1
‑
016
‑
h5l2
‑
e430g与daudi细胞的结合。所示数据为一项代表性实验的平均荧光强度(mfi)值。
74.图4:g28.1和37.3及其变体与daudi细胞的结合。通过流式细胞术测定igg1
‑
g28.1,igg1
‑
g28.1
‑
e430g,igg1
‑
37.3和igg1
‑
37.3
‑
e430g与daudi细胞的结合。所示数据为一项代表性实验的平均荧光强度(mfi)值。
75.图5:人源化的cd37抗体igg1
‑
016
‑
h5l2的变体与daudi细胞的结合。通过流式细胞术测定igg1
‑
016
‑
h5l2,igg1
‑
016
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g和igg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430g与daudi细胞的结合。所示数据为一项代表性实验的平均荧光强度(mfi)值。
76.图6:cd37抗体变体与表达食蟹猴cd37的cho细胞的结合。通过流式细胞术测定igg1
‑
004
‑
h5l2
‑
e430g,igg1
‑
005
‑
h1l2
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2
‑
e430g,igg1
‑
g28.1和igg1
‑
g28.1
‑
e430g的结合。所示数据为一项代表性实验的平均荧光强度(mfi)值。
77.图7:测定cd37抗体之间的结合竞争和raji细胞上由人源化cd37抗体,其变体以及cd37抗体的组合介导的cdc。(a)通过流式细胞术测定igg1
‑
37.3
‑
e430g,igg1
‑
g28.1
‑
e430g,igg1
‑
004
‑
h5l2
‑
e430g,igg1
‑
005
‑
h1l2
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g和igg1
‑
016
‑
h5l2
‑
e434g之间的结合竞争。将raji细胞与未标记的抗体温育以进行一级结合,然后与经alexa fluor 488标记的探测抗体温育。与单独的经a488标记的抗体的结合相比,与未标记的抗体预温育后经a488标记的探测抗体的结合丧失指示经a488标记的抗体与未标记的抗体之间的结合竞争。显示的数据是一项代表性实验的当量可溶性荧光染料分子(mesf)的重复值。(b
‑
g)在体外测定具有或没有e430g突变的igg1
‑
004
‑
h5l2,igg1
‑
005
‑
h1l2,igg1
‑
010
‑
h5l2,igg1
‑
016
‑
h5l2和igg1
‑
37.3或这些的组合诱导对raji细胞的cdc的能力。显示的数据是通过流式细胞术测量死细胞(对应于pi阳性细胞)的百分比测定的裂解%。
78.图8:cd37抗体之间结合竞争的示意性概述。使用未标记的抗体进行一级结合并且使用经alexa fluor 488标记的探测抗体来检测竞争性抗体的后续结合,通过流式细胞术测定igg1
‑
37.3
‑
e430g,igg1
‑
g28.1
‑
e430g,igg1
‑
004
‑
h5l2
‑
e430g,igg1
‑
005
‑
h1l2
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g和igg1
‑
016
‑
h5l2
‑
e4340g之间对raji细胞的结合竞争。颜色指示:黑色;同时结合,白色;结合竞争,灰色;关联抗体。
79.图9:在daudi细胞上由人源化cd37抗体及其变体介导的cdc。在体外测定igg1
‑
004
‑
h5l2,igg1
‑
004
‑
h5l2
‑
e430g,igg1
‑
005
‑
h1l2,igg1
‑
005
‑
h1l2
‑
e430g,igg1
‑
010
‑
h5l2,igg1
‑
010
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2和igg1
‑
016
‑
h5l2
‑
e430g诱导对daudi细胞的cdc的能力。显示的数据是通过流式细胞术测量死细胞(对应于pi阳性细胞)的百分比测定的裂解%。
80.图10:daudi细胞上由g28.1和37.3及其变体介导的cdc,以及由具有不同fc
‑
fc相互作用增强突变的人源化cd37抗体介导的daudi细胞中的cdc。(a)在体外测定igg1
‑
g28.1,igg1
‑
g28.1
‑
e430g,igg1
‑
37.3和igg1
‑
37.3
‑
e430g诱导对daudi细胞的cdc的能力。显示的数据是通过流式细胞术测量死细胞(对应于pi阳性细胞)的百分比测定的裂解%。(b
‑
c)在体外测定(a)igg1
‑
010
‑
h5l2
‑
k409r
‑
e430g,igg1
‑
010
‑
h5l2
‑
e345r
‑
k409r,igg1
‑
010
‑
h5l2
‑
e345k
‑
k409r,igg1
‑
010
‑
h5l2
‑
k409r
‑
e430s,igg1
‑
010
‑
h5l2
‑
rrgy和(b)igg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430g,igg1
‑
016
‑
h5l2
‑
e345k
‑
f405l,igg1
‑
016
‑
h5l2
‑
f405l
‑
e430s和igg1
‑
016
‑
h5l2
‑
e345r
‑
f405l诱导对daudi细胞的cdc的能力。显示的数据是一项代表性实验的通过流式细胞术测量死细胞(对应于pi阳性细胞)的百分比测定的裂解%(在10μg/ml的抗体浓度下,最大杀伤)。误差棒指示实验(一式两份进行)内的变化。
81.图11:在daudi细胞上由人源化抗体igg1
‑
016
‑
h5l2的变体介导的cdc。在体外测定igg1
‑
016
‑
h5l2,igg1
‑
016
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g和igg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430g诱导对daudi细胞的cdc的能力。显示的数据是通过流式细胞术测量死细胞(对应于pi阳性细胞)的百分比测定的裂解%。
82.图12:daudi细胞上由具有fc
‑
fc相互作用增强突变的双特异性cd37抗体,具有fc
‑
fc相互作用增强突变的cd37抗体(的组合)和具有fc
‑
fc相互作用增强突变的单价cd37结合抗体介导的cdc;和具有fc
‑
fc相互作用增强突变的cd37抗体变体及其组合对oci
‑
ly
‑
7细胞的cdc活性。(a)在体外测定bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g,igg1
‑
005
‑
h1l2
‑
e430g,igg1
‑
016
‑
h5l2
‑
e430g,igg1
‑
005
‑
h1l2
‑
k409r
‑
e430g加上igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g的组合,bsigg1
‑
b12
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g和bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g和(b)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g的组合,bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g和bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g诱导对daudi细胞的cdc的能力。显示的数据是通过流式细胞术测量死细胞(对应于pi阳性细胞)的百分比测定的裂解%。(c)体外测定cd37双特异性抗体bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g,cd37单特异性二价(单克隆)抗体igg1
‑
010
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g的组合,单价cd37抗体bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g,bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g和bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g加上bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g的组合诱导oci
‑
ly
‑
7细胞的能力。显示的数据是通过流式细胞术测量死细胞(对应于pi阳性细胞)的百分比测定的裂解%。(d)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g加上bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g和igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g的cdc诱导的ec50值,如在2个独立实验中测定。(e)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g和igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g的cdc诱导的ec50值,如在3个独立实验中测定。
83.图13:在daudi细胞上由双特异性cd37抗体和具有fc
‑
fc相互作用增强突变的双特异性cd37抗体介导的cdc。体外测定(a)bsigg1
‑
016
‑
h5l2
‑
f405lx005
‑
h1l2
‑
k409r和bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g,和(b)bsigg1
‑
016
‑
h5l2
‑
f405lx010
‑
h5l2
‑
k409r和bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g诱导对daudi细胞的cdc的能力。显示的数据是通过流式细胞术测量死细胞(对应于pi阳性细胞)的百分比测定的裂解%。
84.图14:原代cll肿瘤细胞上由具有fc
‑
fc相互作用增强突变的双特异性cd37抗体,具有fc
‑
fc相互作用增强突变的cd37抗体(的组合)和具有fc
‑
fc相互作用增强突变的单价结合cd37抗体介导的cdc。在体外测定(a)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g,igg1
‑
005
‑
h1l2
‑
k409r
‑
e430g,igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g,igg1
‑
005
‑
h1l2
‑
k409r
‑
e430g加上igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g的组合,bsigg1
‑
b12
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g和bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g和(b)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g的组合,bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g和bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g诱导对原代cll肿瘤细胞(患者:vm
‑
bm0091新诊断/未治疗(bm=骨髓衍生))的cdc的能力。显示的数据是通过流式细胞术测量死细胞(对应于pi阳性细胞)的百分比测定的裂解%。
85.图15:在b细胞淋巴瘤细胞系上具有fc
‑
fc相互作用增强突变的双特异性cd37抗体介导的cdc。体外测定10μg/ml浓度的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g诱导对一批b细胞淋巴瘤细胞系的cdc的能力。通过定量流式细胞术测定cd37的表达水平,并显示为分子/细胞,2次实验的平均值
±
sd。白色棒指示对由bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g介导的cdc易感(>10%裂解,2个实验的平均值),黑色棒指示对由bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g介导的cdc不易感(<10%裂解,2个实验的平均值)。
86.图16:在daudi和raji细胞上由具有fc
‑
fc相互作用增强突变的双特异性cd37抗体,具有fc
‑
fc相互作用增强突变的cd37抗体(的组合)和具有fc
‑
fc相互作用增强突变的单价结合cd37抗体介导的adcc。使用铬释放测定法在体外测定在daudi细胞上(a)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g,igg1
‑
005
‑
h1l2
‑
k409r
‑
e430g,igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g和igg1
‑
005
‑
h1l2
‑
k409r
‑
e430g加上igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g的组合和在daudi细胞上(b)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2
‑
e430g和igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g的组合,和在raji细胞上(c)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g的组合,bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g和bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g诱导adcc的能力。显示的数据是特异性裂解%;误差棒表示测定法内的变化,每个数据点5个重复(a,b)或6个重复(c)。
87.图17:(a)cll,(b)fl,(c)mcl或(d)dlbcl肿瘤细胞上的cd37,cd46,cd55和cd59表达水平的定量测定。通过流式细胞术测定肿瘤细胞上的表达水平。抗原量显示为抗体结合能力。
88.图18:在具有cll、fl、mcl、dlbcl或b
‑
nhl(未进一步规定)的患者的原代肿瘤细胞上由具有fc
‑
fc相互作用增强突变的双特异性cd37抗体介导的cdc。通过流式细胞术测定bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405lx010
‑
h5l2
‑
k409r
‑
e430g诱导对源自(a)cll,(b)fl和(c)mcl,dlbcl或b
‑
nhl(未进一步规定)的患者的肿瘤细胞的cdc的能力。cdc诱导表示为使用100μg/ml(a和b)或10μg/ml(c)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405lx010
‑
h5l2
‑
k409r
‑
e430g,通过7
‑
aad阳性肿瘤细胞的分数测定的裂解百分比。
89.图19:具有fc
‑
fc相互作用增强突变的双特异性cd37抗体与人或食蟹猴血液中b细胞的结合。通过流式细胞术测定经alexa
‑
488标记的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g与(a)人或(b)食蟹猴血液中的b细胞的结合。将经alexa
‑
488标记的igg1
‑
b12用作阴性对照抗体。数据显示为一种代表性供体/动物的几何平均a488荧光强度值。误差棒显示实验内的变化(重复测量)。
90.图20:具有fc
‑
fc相互作用增强突变的双特异性cd37抗体和fcγr相互作用增强的单克隆cd37特异性抗体对人或食蟹猴血液中b细胞的细胞毒性。在全血细胞毒性测定法中测定(a)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g和igg1
‑
cd37
‑
b2
‑
s239d
‑
i332e对人血液中的b细胞和(b)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g对食蟹猴血液中的b细胞的细胞毒性。igg1
‑
b12用作阴性对照抗体。数据显示为一项代表性供体/动物的b细胞消减%。误差棒显示实验内的变化(重复测量)。
91.图21:由具有fc
‑
fc相互作用增强突变的双特异性cd37抗体,cd20特异性抗体或其组合介导的cdc。(a
‑
d)离体测定指定浓度的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g、奥法木单抗(ofatumumab)或其组合诱导对源自2名cll患者的肿瘤细胞的cdc的能力。数据显示为活b细胞的%。
92.图22:在jvm
‑
3模型中三次每周剂量的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g的剂量
‑
效应关系。(a)用不同剂量的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g或同种型对照抗体(igg1
‑
b12)处理后jvm
‑
3异种移植物的肿瘤生长。每个时间点显示每组的平均值和sem(n=10)。(b)在第25天每只小鼠的肿瘤大小。每个处理组指示平均值和sem。通过mann whitney检验分析差异。统计学显著差异如下指示:**:p<0.01;***:p<0.001。
93.图23:在daudi
‑
luc模型中三次每周剂量的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g的剂量
‑
效应关系。(a)用不同剂量的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g或同种型对照抗体(igg1
‑
b12)处理后的daudi
‑
luc异种移植物的肿瘤生长(通过萤光素酶活性,生物发光测量)。每个时间点显示每组的平均值和sem(n=9)。(b)在第36天每只小鼠的萤光素酶活性。每个处理组指示平均值和sem。差异由单向anova,未校正的费舍尔(fisher)lsd分析。统计学显著差异如下指示:**:p<0.01;***:p<0.001。
94.图24:在scid小鼠中静脉注射后bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g和igg1
‑
b12的血浆浓度。
95.给scid小鼠注射单剂i.v.的(a
‑
b)100μg(5mg/kg)或(c
‑
d)500μg(25mg/kg)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g或igg1
‑
b12。
96.图25:cd37抗体与胞外域中具有丙氨酸突变的cd37变体的结合分析。z得分(zscore)(倍数变化)定义为(标准化gmfi[aa位置]
‑
μ)/σ,其中μ和σ是所有突变体的标准化gmfi的平均值和标准差(sd)。z得分低于
‑
1.5(虚线表示)的残基认为是“结合丧失突变体”。x轴上方的数字是指氨基酸位置。注意,x轴是不连续的:轴的左侧部分(直到带状线)代表人cd37的小细胞外环中的aa残基,其不是丙氨酸或半胱氨酸。轴的右侧部分代表人cd37的大细胞外环中的aa残基,其不是丙氨酸或半胱氨酸。虚线表示
‑
1.5的z得分(倍数变化)。
[0097]
图26:raji细胞上由具有fc
‑
fc相互作用增强突变的cd37抗体加上临床建立的cd20抗体产品的混合物介导的cdc。具有fc
‑
fc相互作用增强突变的cd37抗体加上护理标准cd20抗体产品mabthera(利妥昔单抗)、arzerra(奥法木单抗)和gazyva(奥滨尤妥珠单抗,ga101)的1:0,3:1,1:1,3:1和0:1抗体混合物(10μg/ml终浓度)的抗体浓度稀释系列的cdc介导的对raji细胞的杀伤(%裂解表示为pi阳性细胞分数,如通过流式细胞术测定):(a)与igg1
‑
37.3
‑
e430g的混合物,(b)与igg1
‑
g28.1
‑
e430g的混合物,(c)与igg1
‑
004
‑
e430g的混合物,(d)与igg1
‑
005
‑
e430g的混合物,(e)与igg1
‑
010
‑
e430g的混合物和(f)与igg1
‑
016
‑
e430g的混合物。
[0098]
图27:抗体配制剂的浊度。使用浊度计确定的以比浊法浊度单位(ntu)计的浊度。闭合圆代表igg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430g(d1)。开放圆代表igg1
‑
010
‑
h5l2
‑
k409r
‑
e430g(e1)。
[0099]
图28:抗体配制剂中的亚可见颗粒计数。如使用hiac仪测定的两次冷冻
‑
融化循环后各种配制剂中的亚可见颗粒。计数超过2、5、10或25微米的颗粒。
[0100]
发明详述
[0101]
定义
[0102]
如本文所用,术语“cd37”是指白细胞抗原cd37,也称为gp52
‑
40、四跨膜蛋白26和tspan26,其是具有四个跨膜域(tm)和一个小的胞外域和一个大的胞外域的重度糖基化的跨膜蛋白。智人(即人)cd37蛋白由编码seq id no:62所示氨基酸序列(人cd37蛋白:uniprotkb/swissprot p11049)的核酸序列编码。在此氨基酸序列中,残基112至241对应于大的胞外域,残基39至59对应于小的胞外域,而剩余的残基对应于跨膜和胞质域。食蟹猕猴(macaca fascicularis)(即食蟹猴)cd37蛋白由编码seq id no:63所示的氨基酸序列(食蟹猴cd37蛋白:genbank登录号xp_005589942)的核酸序列编码。除非上下文矛盾,术语“cd37”是指“人cd37”。术语“cd37”包括由细胞(包括肿瘤细胞)天然表达或在用cd37基因或cdna转染的细胞上表达的cd37的任何变体、同种型和物种同源物。
[0103]
术语“人cd20”或“cd20”是指人cd20(uniprotkb/swiss
‑
prot no p11836),并且包括由细胞(包括肿瘤细胞)天然表达或在用cd20基因或cdna转染的细胞上表达的cd20的任何变体、同种型和物种同源物。物种同源物包括恒河猴(rhesus monkey)cd20(普通猕猴(macaca mulatta);uniprotkb/swiss
‑
prot no h9yxp1)和食蟹猴cd20(食蟹猕猴)。
[0104]
在本文中可以互换使用的术语“结合cd37的抗体”、“抗cd37抗体”、“cd37结合抗体”、“cd37特异性抗体”、“cd37抗体”是指结合cd37的胞外部分上的表位的任何抗体。
[0105]
在本发明的上下文中,术语“抗体”(ab)是指具有在典型的生理条件下以相当长的时间段的半衰期,例如至少约30分钟,至少约45分钟,至少约1小时,至少约2小时,至少约4小时,至少约8小时,至少约12小时,约24小时或更多,约48小时或更多,约3、4、5、6、7或更多天等,或任何其他相关的功能定义的时段(例如足以诱发,促进,增强和/或调节与抗体与抗原的结合相关的生理应答的时间和/或足以使抗体募集效应器活性的时间)与抗原特异性结合的能力的免疫球蛋白分子、免疫球蛋白分子的片段或其任一者的衍生物。免疫球蛋白分子的重链和轻链的可变区包含与抗原相互作用的结合域。抗体(ab)的恒定区可以介导免疫球蛋白与宿主组织或因子的结合,包括免疫系统的各种细胞(例如效应细胞)和补体系统的成分(例如c1q),即补体激活的经典途径中的第一成分。如上所述,除非另有说明或与上下文明显矛盾,否则本文中的术语抗体包括作为抗原结合片段,即,保留与抗原特异性结合的能力的抗体片段。已经显示抗体的抗原结合功能可以通过全长抗体的片段进行。术语“抗体”中涵盖的抗原结合片段的实例包括(i)fab'或fab片段,由v
l
,v
h
,c
l
和c
h
1域组成的单价片段或如wo2007059782(genmab)中所述的单价抗体;(ii)f(ab')2片段,包含在铰链区处通过二硫键连接的两个fab片段的二价片段;(iii)基本上由v
h
和c
h
1域组成的fd片段;(iv)基本上由抗体单臂的v
l
和v
h
域组成的fv片段,(v)基本上由v
h
域组成,也称为域抗体(holt et al;trends biotechnol.2003nov;21(11):484
‑
90)的dab片段(ward et al.,nature 341,544
‑
546(1989));(vi)骆驼科抗体或纳米抗体(revets et al;expert opin biol ther.2005jan;5(1):111
‑
24)和(vii)分离的互补决定区(cdr)。此外,尽管fv片段的两个域v
l
和v
h
由不同的基因编码,但可以使用重组方法通过合成接头将它们连接起来,所述合成接头使它们能够制备成单一蛋白链,其中v
l
区和v
h
区配对以形成单价分子(称为单链抗体或单链fv(scfv),参见例如bird et al.,science 242,423
‑
426(1988)和huston et al.,pnas usa 85,5879
‑
5883(1988))。除非另有说明或上下文明确指出,否则此类单链抗体涵盖在术语抗体内。尽管此类片段通常包括在抗体的含义内,但是它们共同且各自独立地是本发明的独特特征,表现出不同的生物学特性和效用。在本发明的上下文中,这些和其他有用的抗体片段以及此类片段的双特异性形式在本文中进一步讨论。对于本发明的药物组合物内包含的双特异性抗体,此类片段与fc域连接。还应理解,除非另有说明,术语抗体还包括多克隆抗体、单克隆抗体(mab)、抗体样多肽,例如嵌合抗体和人源化抗体,以及可通过任何已知技术,例如酶促裂解,肽合成和重组技术提供的保留与抗原特异性结合的能力的抗体片段(抗原结合片段)。产生的抗体可以具有任何同种型。
[0106]
术语“双特异性抗体”是指对至少两个不同的,通常是非重叠的表位具有特异性的抗体。此类表位可以在相同或不同的靶物上。对于本发明,表位在相同靶物,即cd37上。包含fc区的不同类别的双特异性抗体的实例包括但不限于:不对称双特异性分子,例如具有互补ch3域的igg样分子;和对称的双特异性分子,例如重组igg样双重靶向分子,其中分子的
每个抗原结合区结合至少两个不同的表位。
[0107]
双特异性分子的实例包括但不限于(trion pharma/fresenius biotech,wo/2002/020039)、突出
‑
进入
‑
空穴(genentech,wo 1998/50431)、crossmabs(roche,wo 2009/080251,wo 2009/080252,wo 2009/080253)、静电匹配fc
‑
异二聚体分子(amgen,ep1870459和wo2009089004;chugai,us201000155133;oncomed,wo 2010/129304)、luz
‑
y(genentech)、dig
‑
body、pig
‑
body和tig
‑
body(pharmabcine)、链交换工程化域抗体(strand exchange engineered domain body)(seedbody)(emd serono,wo2007110205)、双特异性igg1和igg2(pfizer/rinat,wo 2011/143545)、azymetric支架(zymeworks/merck,wo2012058768)、mab
‑
fv(xencor,wo 2011/028952)、xmab(xencor)、二价双特异性抗体(roche,wo 2009/080254)、双特异性igg(eli lilly)、分子(genmab a/s,wo 2011/131746)、duetmab(medimmune,us2014/0348839)、biclonics(merus,wo 2013/157953)、novimmune(κλbodies,wo 2012/023053)、fcδadp(regeneron,wo 2010/151792)、(dt)
‑
ig(gsk/domantis)、二合一抗体或双重作用fab(genentech,adimab)、mab2(f
‑
star,wo 2008/003116)、zybody
tm
分子(zyngenia)、covx
‑
body(covx/pfizer)、fynomabs(covagen/janssen cilag)、dutamab(dutalys/roche)、imab(medimmune)、双重可变域(dvd)
‑
igtm(abbott)、双重域双头部抗体(unilever;sanofi aventis,wo 2010/0226923)、ts2ab(medimmune/az)、bsab(zymogenetics)、hercules(biogen idec,us 7,951,918)、scfv
‑
融合物(genentech/roche,novartis,immunomedics,changzhou adam biotech inc,cn 102250246)、tvab(roche,wo2012/025525,wo2012/025530)、scfv/fc融合物、scorpion(emergent biosolutions/trubion,zymogenetics/bms)、interceptor(emergent)、双重亲和力重新靶向技术(dual affinity retargeting technology)(fc
‑
darttm)(macrogenics,wo2008/157379,wo2010/080538)、beat(glenmark)、二
‑
双抗体(di
‑
diabody)(imclone/eli lilly)和化学交联的单抗(karmanos cancer center)和共价融合的单抗(aimm therapeutics)。
[0108]
如本文所用,术语“全长抗体”是指含有对应于该类别或同种型的野生型抗体中通常发现的那些域的所有重链和轻链恒定和可变域的抗体(例如,亲本或变体抗体)。
[0109]
如本文所用,术语“嵌合抗体”是指可变区源自非人类物种(例如源自啮齿动物)且恒定区源自不同物种(例如人)的抗体。嵌合抗体可以通过抗体工程化产生。“抗体工程化”是用于抗体的不同种类修饰的通用术语,并且是技术人员熟知的方法。特别地,可以通过使用sambrook et al.,1989,molecular cloning:a laboratory manual,new york:cold spring harbor laboratory press,第15章中所述的标准dna技术产生嵌合抗体。因此,嵌合抗体可以是遗传或酶工程化重组抗体。产生嵌合抗体在技术人员的知识范围内,因此,可以通过除本文所述之外的方法来进行嵌合抗体的产生。开发用于治疗应用的嵌合单克隆抗体以降低抗体的免疫原性。它们通常可以包含对目标抗原具有特异性的非人(例如鼠)可变区以及人恒定抗体重链和轻链域。如在嵌合抗体的上下文中使用的术语“可变区”或“可变域”是指包含免疫球蛋白的重链和轻链的cdr和框架区的区域。
[0110]
如本文所用,术语“寡聚物”是指与至少在原则上由无数个单体组成的聚合物相反,由多于一个但数量有限的单体单元(例如抗体)组成的分子。示例性的寡聚物是二聚体,三聚体,四聚体,五聚体和六聚体。同样地,如本文所用,“寡聚化”诸如例如“六聚化”是指包
含靶物结合区的抗体和/或其他二聚体蛋白向寡聚物,如六聚体的分布增加。寡聚物如六聚体的形成增加是由于结合膜结合靶物后fc
‑
fc相互作用增加所致。
[0111]
如本文所用,术语“抗原
‑
结合区”、“抗原结合区”、“结合区”或抗原结合域是指能够与抗原结合的抗体区域。此结合区通常由抗体的vh和vl域定义,它们可以进一步细分为高变性区(或高变区,它们在序列和/或结构限定环的形式上是高变的),也称为互补决定区(cdr),散布着更保守的区域,称为框架区(fr)。抗原可以是任何分子,例如多肽,例如存在于细胞、细菌或病毒体上或溶液中。除非上下文矛盾,否则术语“抗原”和“靶物”可以在本发明的上下文中互换使用。
[0112]
如本文所用,术语“靶物”是指抗体的抗原结合区结合的分子。靶物包括产生的抗体所针对的任何抗原。就抗体而言,术语“抗原”和“靶物”可以互换使用,并且就本发明的任何方面或实施方案而言,构成相同的含义和目的。
[0113]
如本文所用,术语“人源化抗体”是指遗传工程化的非人抗体,其含有人抗体恒定域和经修饰以与人可变域含有高水平序列同源性的非人可变域。这可以通过将6个一起形成抗原结合位点的非人抗体互补决定区(cdr)移植到同源人受体框架区(fr)上来实现(参见wo92/22653和ep0629240)。为了完全重建亲本抗体的结合亲和力和特异性,可能需要将亲本抗体(即非人抗体)的框架残基替换为人构架区(回复突变)。结构同源性建模可以帮助鉴定框架区中对于抗体的结合特性重要的氨基酸残基。因此,人源化抗体可包含非人cdr序列,主要是人框架区(其任选地包含一个或多个向非人氨基酸序列的氨基酸回复突变),以及完全人恒定区。任选地,可以应用不一定是回复突变的其他氨基酸修饰,以获得具有优选特性,例如亲和力和生物化学特性的人源化抗体。
[0114]
可以使用经免疫的兔,使用种系人源化(cdr植入)技术使兔抗体进行人源化,并在必要时通过将可能对抗体结合特性至关重要的残基(如在结构建模中鉴定)回复突变成兔残基来产生人源化抗体。可以应用潜在的t细胞表位的筛选。
[0115]
如本文所用,术语“人抗体”是指具有源自人种系免疫球蛋白序列的可变区和恒定区的抗体。人抗体可包括不由人种系免疫球蛋白序列编码的氨基酸残基(例如,由体外随机或位点特异性诱变或体内体细胞突变引入的突变)。然而,如本文所用,术语“人抗体”不意图包括其中源自另一哺乳动物物种,例如小鼠的种系的cdr序列已被植入到人框架序列上的抗体。人单克隆抗体可以通过多种技术产生,包括常规的单克隆抗体方法,例如,kohler and milstein,nature 256:495(1975)的标准体细胞杂交技术。尽管体细胞杂交程序是优选的,但是原则上可以采用其他产生单克隆抗体的技术,例如,使用人抗体基因文库的b淋巴细胞的病毒或致癌转化或噬菌体展示技术。
[0116]
用于制备分泌人单克隆抗体的杂交瘤的合适的动物系统是鼠系统。在小鼠中产生杂交瘤是一种非常完善建立的程序。用于分离经免疫的脾细胞用于融合的免疫方案和技术是本领域已知的。融合配偶体(例如鼠骨髓瘤细胞)和融合程序也是已知的。
[0117]
因此,人单克隆抗体可以例如使用携带部分的人免疫系统而非小鼠或兔系统的转基因或转染色体小鼠或大鼠产生。
[0118]
术语“免疫球蛋白”是指由两对多肽链,一对轻(l)低分子量链和一对重(h)链(所有四者通过二硫键相互连接)组成的一类结构相关的糖蛋白。免疫球蛋白的结构已得到充分表征。例如参见fundamental immunology第7章(paul,w.编,第2版raven press,n.y.
(1989))。简而言之,每条重链通常由重链可变区(本文缩写为v
h
或vh)和重链恒定区(本文缩写为c
h
或ch)组成。重链恒定区通常由三个域c
h
1,c
h
2和c
h
3构成。每个轻链通常由轻链可变区(在本文中简称为v
l
或vl)和轻链恒定区(在本文中简称为c
l
或cl)构成。轻链恒定区通常由一个域c
l
构成。v
h
和v
l
区可进一步细分为高变性区(或高变区,它们在序列和/或结构限定环的形式上是高变的),也称为互补决定区(cdr),散布着更保守的区域,称为框架区(fr)。每个v
h
和v
l
通常由三个cdr和四个fr构成,从氨基端到羧基端按以下顺序排列:fr1,cdr1,fr2,cdr2,fr3,cdr3,fr4(还参见chothia and lesk j.mol.biol.196,901
‑
917(1987))。除非另有说明或与上下文矛盾,否则本文的cdr序列是根据imgt规则(brochet x.,nucl acids res.2008;36:w503
‑
508 and lefranc mp.,nucleic acids research 1999;27:209
‑
212;还见因特网http地址http://www.imgt.org/)鉴定的。参见除非另有说明或与上下文矛盾,否则在本发明中对恒定区中氨基酸位置的引用是根据eu编号(edelman et al.,proc natl acad sci u s a.1969may;63(1):78
‑
85;kabat et al.,sequences of proteins of immunological interest,fifth edition.1991nih publication no.91
‑
3242)。
[0119]
当在本文中使用时,除非上下文矛盾,术语“fab
‑
臂”或“臂”是指一个重链
‑
轻链对,并且在本文中与“半分子”互换使用。因此,“fab臂”包括重链和轻链的可变区以及轻链的恒定区和重链的恒定区,其包含免疫球蛋白的ch1区,铰链,ch2区和ch3区。“ch1区”是指例如对应于根据eu编号的氨基酸118
‑
215的人igg1抗体区域。因此,fab片段包含免疫球蛋白的结合区。
[0120]
在本文中可以互换使用的术语“片段可结晶区”、“fc区”、“fc片段”或“fc域”是指至少包含从氨基端至羧基端排列的铰链区、ch2域和ch3域的抗体区域。igg1抗体的fc区可以例如通过用木瓜蛋白酶消化igg1抗体来产生。抗体的fc区可以介导免疫球蛋白与宿主组织或因子的结合,包括免疫系统的各种细胞(例如效应细胞)和补体系统的成分,例如c1q,经典补体激活途径中的第一个成分。如本文所用,术语“铰链区”意图指免疫球蛋白重链的铰链区。因此,例如,人igg1抗体的铰链区对应于根据eu编号的氨基酸216
‑
230。
[0121]
如本文所用,术语“核心铰链”或“核心铰链区”是指对应于人igg1抗体的位置226
‑
229的四个氨基酸。
[0122]
如本文所用,术语“ch2区”或“ch2域”意图指免疫球蛋白重链的ch2区域。因此,例如,人igg1抗体的ch2区对应于根据eu编号的氨基酸231
‑
340。但是,ch2区也可以是如本文所述的任何其他同种型或同种异型。
[0123]
如本文所用,术语“ch3区”或“ch3域”意图指免疫球蛋白重链的ch3区。因此,例如,人igg1抗体的ch3区对应于根据eu编号的氨基酸341
‑
447。然而,ch3区也可以是如本文所述的任何其他同种型或同种异型。
[0124]
如本文所用,术语“同种型”是指由重链恒定区基因编码的免疫球蛋白类别(例如igg1,igg2,igg3,igg4,igd,iga,ige或igm)。
[0125]
在本发明的上下文中,术语“单价抗体”是指抗体分子能够结合抗原的单个分子,因此不能进行抗原交联。
[0126]“cd37抗体”或“抗cd37抗体”是结合抗原cd37特异性的如上所述的抗体。
[0127]“cd37xcd37抗体”或“抗cd37xcd37抗体”是包含两个不同的抗原结合区的双特异
性抗体,其中一个特异性结合抗原cd37上的第一表位,而第二个特异性结合cd37上的不同表位。
[0128]
在一个实施方案中,本发明的药物组合物内包含的双特异性抗体是分离的。如本文所用,“分离的双特异性抗体”是指基本上不含具有不同抗原性特异性的其他抗体的双特异性抗体(例如,特异性结合cd37的分离的双特异性抗体基本上不含特异性结合cd37的单特异性抗体)。
[0129]
术语“表位”是指能够结合抗体的抗原结合区(“互补位”)的蛋白质决定簇。表位通常由诸如氨基酸或糖侧链等的分子的表面分组组成,并且通常具有特定的三维结构特征以及特定的电荷特征。构象性和非构象性表位的区别在于,在存在变性溶剂的情况下,与前者的结合而非后者的结合丧失。表位定位技术可以确定“结构表位”或“功能性表位”。结构表位定义为与抗体直接接触的结构内的那些残基,并且可以例如通过基于结构的方法如x射线晶体学进行评估。结构表位可以包含直接参与抗体结合的氨基酸残基以及不直接参与结合的其他氨基酸残基,例如被抗体有效阻断或覆盖的氨基酸残基(换言之,氨基酸残基在抗体的足迹内)。功能性表位定义为对抗原
‑
抗体结合相互作用作出有力贡献的那些残基,并且可以例如通过定点诱变例如丙氨酸扫描(cunningham,b.c.,&wells,j.a.(1993)journal of molecular biology;clackson,t.,&wells,j.(1995)science,267(5196),383
–
386)来评估。功能性表位可包含直接参与抗体结合的氨基酸残基,以及不直接参与结合的其他氨基酸残基,例如引起参与直接相互作用的残基的位置发生构象变化的氨基酸残基(greenspan,n.s.,&di cera,e.(1999)nature biotechnology,17(10),936
–
937)。在抗体
‑
抗原相互作用的情况下,功能性表位可用于彼此区分抗体分子。可以通过使用如实施例17中所述的丙氨酸扫描方法来确定功能性表位。因此,蛋白质中的氨基酸可以用丙氨酸取代,从而产生一系列突变体蛋白,与野生型蛋白质相比,抗体的抗原结合区与突变体蛋白质的结合降低;如实施例17中所述,降低的结合确定为所述抗体的结合的标准化log(倍数变化)(表示为z得分)小于
‑
1.5。
[0130]
如本文所用,术语“单克隆抗体”是指基本上具有单一分子组成的抗体分子的制剂。单克隆抗体组合物显示对特定表位的单一结合特异性和亲和力。因此,术语“人单克隆抗体”是指显示单一结合特异性的抗体,其具有源自人种系免疫球蛋白序列的可变区和恒定区。人单克隆抗体可以由杂交瘤产生,所述杂交瘤包含与永生化细胞融合的获自转基因或转染色体非人类动物(例如转基因小鼠)的具有包含人重链转基因和轻链转基因的基因组的b细胞。
[0131]
如本文所用,在抗体与预定抗原结合的上下文中,术语“结合”通常当通过例如使用抗体作为配体和抗原作为分析物的octet htx仪中的biolayer干扰量度法(bli)技术测定时以对应于约10
‑6m或更小,例如10
‑7m或更小,例如约10
‑8m或更小,例如约10
‑9m或更小,约10
‑
10
m或更小,或约10
‑
11
m或甚至更小的k
d
的亲和力结合,并且其中抗体以对应于k
d
的亲和力与预定抗原结合,所述k
d
比其结合除预定抗原以外的非特异性抗原(例如bsa,酪蛋白)或紧密相关抗原的k
d
低至少10倍,例如低至少100倍,例如低至少1,000倍,例如低至少10,000倍,例如低至少100,000倍。结合k
d
较低的量取决于抗体的k
d
,因此,当抗体的k
d
非常低时,与抗原结合的k
d
低于与非特异性抗原的结合k
d
的量可以是至少10,000倍(即,抗体是高度特异性的)。
[0132]
如本文所用,术语“k
d”(m)是指特定抗体
‑
抗原相互作用的解离平衡常数。
[0133]
如本文所用,“亲和力”和“k
d”成反相关,即,较高的亲和力意图表示较低的k
d
,而较低的亲和力意图表示较高的k
d
。
[0134]
如本文所用,“竞争”或“交叉竞争”的抗体与“阻断”或“交叉阻断”另一种抗体(即参考抗体)的抗体互换使用,并且指抗体和参考抗体竞争与人cd37的结合,例如如本文实施例7所述的测定法中确定。在一个实施方案中,在竞争性参考抗体的存在下,抗体以其最大结合的小于50%,例如小于20%,例如小于15%结合。
[0135]
如本文所用,与另一种抗体(即参考抗体)“不竞争”或“不交叉竞争”或“不阻断”另一种抗体(即参考抗体)的抗体是指抗体和参考抗体不竞争对人cd37的结合,例如如本文实施例7所述的测定法中确定。对于几对抗体和参考抗体,仅当一种抗体结合到细胞上的抗原而另一种用于竞争时才观察到在实施例7的测定法中的非竞争,反之则不然。当在本文中使用时,术语“不竞争”或“非竞争”或“非阻断”也意图涵盖抗体的此类组合。在一个实施方案中,在参考抗体的存在下,抗体以其最大结合的至少75%,例如至少80%,例如至少85%结合。
[0136]
如本文所用,术语“fc
‑
fc相互作用增强突变”是指增强与细胞表面靶物结合的相邻igg抗体之间的fc
‑
fc相互作用的igg抗体中的突变。这可以导致增强的寡聚物形成,如例如靶物结合抗体的六聚化,而抗体分子在溶液中保持为单体,如记载于wo 2013/004842和wo 2014/108198,两者均通过引用并入本文。
[0137]
如本文所用,术语“fc效应器功能”或“fc介导的效应器功能”意图指由于多肽或抗体与其在细胞膜上的靶物(例如抗原)结合以及igg fc域与先天免疫系统分子(例如可溶性分子或膜结合分子)的后续相互作用而产生的功能。fc效应器功能的实例包括(i)c1q结合,(ii)补体激活,(iii)补体依赖性细胞毒性(cdc),(iv)抗体依赖性细胞介导的细胞毒性(adcc),(v)fc
‑
gamma受体结合,(vi)抗体依赖性细胞性吞噬作用(adcp),(vii)补体依赖性细胞性细胞毒性(cdcc),(viii)补体增强的细胞毒性,(ix)由抗体介导的经调理的抗体对补体受体的结合,(x)调理(opsonisation)和(xi)(i)至(x)中任一项的组合。
[0138]
当在本文中使用时,术语“第一和第二ch3区之间的异二聚体相互作用”是指第一
‑
ch3/第二
‑
ch3异二聚体蛋白中的第一fc
‑
区的第一ch3区和第二fc
‑
区的第二ch3区之间的相互作用。双特异性抗体是异二聚体蛋白的实例。
[0139]
当在本文中使用时,术语“第一和第二ch3区的同二聚体相互作用”是指第一
‑
ch3/第一
‑
ch3同二聚体蛋白中的第一ch3区和另一个第一ch3区之间的相互作用以及第二ch3/第二ch3同二聚体蛋白中的第二ch3区和另一个第二ch3区之间的相互作用。单克隆抗体是同二聚体蛋白的实例。
[0140]
术语“还原条件”或“还原环境”是指底物,诸如例如抗体铰链区中的半胱氨酸残基比被氧化更可能被还原的条件或环境。
[0141]
本发明还提供了包含双特异性抗体的药物组合物,所述双特异性抗体是实施例的双特异性抗体的v
l
区或v
h
区的功能变体。在双特异性抗体的上下文下使用的v
l
区,v
h
区或cdr的功能变体仍允许双特异性抗体的每个臂至少保留相当大比例(至少约50%,60%,70%,80%,90%,95%或更多)的亲本双特异性抗体的亲和力和/或特异性/选择性,并且在某些情况下,此类双特异性抗体可以比亲本双特异性抗体以更大的亲和力、选择性和/或特
异性缔合。此类功能性变体通常与亲本双特异性抗体保持显著的序列同一性。两个序列之间的同一性百分比是该序列共享的相同位置数的函数(即,%同源性=相同位置数/位置总数x 100),其中要考虑到缺口的数量和每个缺口的长度,所述缺口需要被引入以实现两个序列的最佳比对。两个核苷酸或氨基酸序列之间的同一性百分数可以例如使用已经并入align程序(第2.0版)中的e.meyers and w.miller,comput.appl.biosci 4,11
‑
17(1988)的算法,使用pam120权重残基表,缺口长度罚分12和缺口罚分4确定。此外,两个氨基酸序列之间的同一性百分比可以使用needleman and wunsch,j.mol.biol.48,444
‑
453(1970)算法确定。
[0142]
示例性的变体包括那些主要通过保守取代而与亲本双特异性抗体序列的vh和/或vl和/或cdr区不同的变体;例如,变体中的10个,例如9、8、7、6、5、4、3、2或1个取代是保守的氨基酸残基取代。优选地,变体在亲本抗体的vh和/或vl区中含有至多10个氨基酸取代,例如至多9、8、7、6、5、4、3、2或至多1个氨基酸取代。优选地,此类取代是保守取代,尤其是如果取代是在cdr序列中。
[0143]
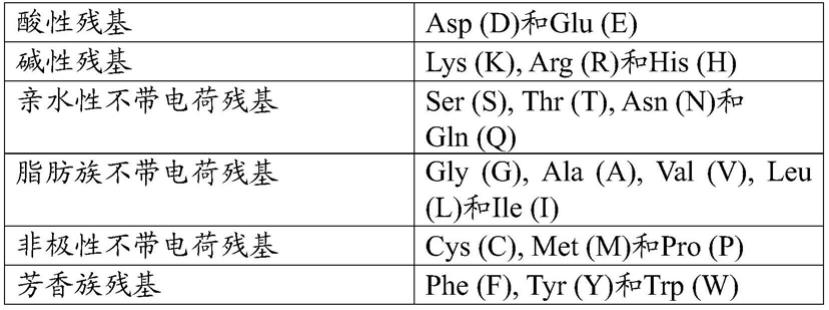
在本发明的上下文中,保守取代可以通过下表中反映的氨基酸类别内的取代来定义:
[0144]
保守取代的氨基酸残基类别
[0145][0146]
在本发明的上下文中,除非另外指出,否则以下标记用于描述突变;i)将给定位置的氨基酸取代写为例如k409r,其意指用精氨酸取代位置409上的赖氨酸;并且ii)对于特定的变体,使用特定的三字母或单字母代码,包括代码xaa和x表示任何氨基酸残基。因此,在位置409处用精氨酸取代赖氨酸称为:k409r,并且在位置409处用任何氨基酸残基取代赖氨酸称为k409x。若在位置409中缺失赖氨酸,则它用k409*表示。
[0147]
如本文所用,术语“重组宿主细胞”(或简称为“宿主细胞”)意图指已将引入有表达载体,例如编码本发明中使用的抗体的表达载体的细胞。重组宿主细胞包括例如转染瘤,例如cho,cho
‑
s,hek,hek293,hek
‑
293f,expi293f,per.c6或ns0细胞以及淋巴细胞。
[0148]
术语“治疗/处理”是指施用有效量的本发明的药物组合物,以缓解,改善,阻止或消除(治愈)症状或疾病状态。
[0149]
术语“有效量”或“治疗有效量”是指在必需的剂量和时间段内有效实现期望治疗结果的量。双特异性抗体的治疗有效量可以随诸如个体的疾病状态,年龄,性别和体重以及双特异性抗体在个体中引起期望的应答的能力等因素而变化。治疗有效量也是抗体或抗体部分的任何毒性或有害作用均被治疗有益作用超过的量。
[0150]
本发明的实施方案
[0151]
如上所述,在一个主要方面,本发明涉及药物组合物,其包含:
[0152]
a)双特异性抗体,
[0153]
b)组氨酸缓冲剂,
[0154]
c)50至300mm的糖和/或50至300mm的多元醇,和
[0155]
d)0.01至0.1%的聚山梨酯80,
[0156]
其中所述组合物的ph在4.5和6.8之间,并且
[0157]
其中所述双特异性抗体包含结合具有seq id no:62的序列的人cd37的第一和第二抗原结合区和人免疫球蛋白的第一和第二fc区,其中所述第一和第二fc区包含一个或多个氨基酸突变,所述氨基酸突变与没有所述突变的双特异性抗体之间的fc
‑
fc相互作用相比增强结合膜结合的靶物后所述双特异性抗体之间的所述fc
‑
fc相互作用,其中所述第一抗原结合区包含cdr序列:
[0158]
以seq id no:16所示的vh cdr1序列
[0159]
以seq id no:17所示的vh cdr2序列
[0160]
以seq id no:18所示的vh cdr3序列,
[0161]
以seq id no:20所示的vl cdr1序列,
[0162]
vl cdr2序列:kas,和
[0163]
以seq id no:21所示的vl cdr3序列,
[0164]
并且其中所述第二抗原结合区包含cdr序列:
[0165]
以seq id no:23所示的vh cdr1序列,
[0166]
以seq id no:24所示的vh cdr2序列,
[0167]
以seq id no:25所示的vh cdr3序列,
[0168]
以seq id no:27所示的vl cdr1序列,
[0169]
vl cdr2序列:yas,和
[0170]
以seq id no:31所示的vl cdr3序列。
[0171]
本发明的药物组合物内包含的双特异性抗cd37抗体结合cd37上的两个不同的表位。这两个表位使得这两个结合臂可以结合相同的蛋白质分子,并且因此使得每个结合臂不阻断另一个臂的结合和/或不与双特异性分子的另一个结合臂竞争结合。而且,双特异性抗体包含增强两个或更多个双特异性抗体分子之间的fc
‑
fc相互作用的突变。这具有以下效果:双特异性分子在结合靶细胞质膜上表达的cd37后形成寡聚物。与除突变外相同的分子相比,fc
‑
fc相互作用得到增强。优选地,突变在双特异性分子的fc区中。在一个实施方案中,它是双特异性分子的fc区中的单个氨基酸取代。优选地,对称取代是指两个半分子(亲本抗体)均具有突变。双特异性抗体的另一个优点是,与不具有fc
‑
fc相互作用增强突变的相同双特异性分子相比,其具有增强的cdc和/或adcc效应器功能。令人惊讶的是,与突变为具有增强的fc
‑
fc相互作用的两种亲本单克隆抗cd37抗体的组合相比,双特异性分子也具有改善的cdc和/或adcc,并且与单独的突变为具有增强的fc
‑
fc相互作用的任一亲本单克隆抗cd37抗体相比,双特异性分子也具有改善的cdc和/或adcc。因此,双特异性抗体比具有第一抗原结合区的抗体和具有第二抗原结合区的第二抗体的组合且其中这两种抗体均包含fc
‑
fc相互作用增强突变,或与具有第一或第二抗原结合区且包含fc
‑
fc相互作用增强突
变的单个单克隆抗cd37抗体相比更有力诱导cdc和/或adcc。
[0172]
本发明还提供了稳定的药物组合物,其包含具有结合cd37的结合臂的抗体。
[0173]
因此,一方面,本发明涉及药物组合物,其包含:
[0174]
i)抗体,
[0175]
j)组氨酸缓冲剂,
[0176]
k)50至300mm的糖和/或50至300mm的多元醇,和
[0177]
l)0.01至0.1%的聚山梨酯80,
[0178]
其中所述组合物的ph在4.5和6.8之间,和
[0179]
其中所述抗体包含结合具有seq id no:62的序列的人cd37的第一抗原结合区和人免疫球蛋白的第一和第二fc区,其中所述第一和第二fc区包含一个或多个氨基酸突变,所述氨基酸突变与没有所述突变的双特异性抗体之间的fc
‑
fc相互作用相比增强结合膜结合的靶物后抗体之间的所述fc
‑
fc相互作用,其中所述第一抗原结合区包含cdr序列:
[0180]
以seq id no:16所示的vh cdr1序列
[0181]
以seq id no:17所示的vh cdr2序列
[0182]
以seq id no:18所示的vh cdr3序列,
[0183]
以seq id no:20所示的vl cdr1序列,
[0184]
vl cdr2序列:kas和
[0185]
以seq id no:21所示的vl cdr3序列。
[0186]
在另一方面,本发明涉及药物组合物,其包含:
[0187]
m)抗体,
[0188]
n)组氨酸缓冲剂,
[0189]
o)50至300mm的糖和/或50至300mm的多元醇,和
[0190]
p)0.01至0.1%的聚山梨酯80,
[0191]
其中所述组合物的ph在4.5和6.8之间,并且
[0192]
其中所述抗体包含结合具有seq id no:62的序列的人cd37的第二抗原结合区和人免疫球蛋白的第一和第二fc区,其中所述第一和第二fc区包含一个或多个氨基酸突变,所述氨基酸突变与没有所述突变的双特异性抗体之间的fc
‑
fc相互作用相比增强结合膜结合的靶物后抗体之间的所述fc
‑
fc相互作用,其中所述第一抗原结合区包含cdr序列:
[0193]
以seq id no:23所示的vh cdr1序列,
[0194]
以seq id no:24所示的vh cdr2序列,
[0195]
以seq id no:25所示的vh cdr3序列,
[0196]
以seq id no:27所示的vl cdr1序列,
[0197]
vl cdr2序列:yas,和
[0198]
以seq id no:31所示的vl cdr3序列。
[0199]
在一个实施方案中,本发明的药物组合物包含5至100mg/ml的双特异性抗体,例如10至50mg/ml的双特异性抗体,例如10至30mg/ml的双特异性抗体,例如20mg/ml的双特异性抗体。
[0200]
在一个实施方案中,本发明的药物组合物包含5至100mg/ml的抗体,例如10至50mg/ml的抗体,例如,10至30mg/ml的抗体,例如20mg/ml的抗体。
[0201]
在一个实施方案中,本发明的药物组合物包含10至100mm的组氨酸,例如10至50mm组氨酸,例如10至30mm组氨酸,例如20mm组氨酸。在一个实施方案中,组氨酸是组氨酸
‑
hcl。
[0202]
在一个实施方案中,本发明的药物组合物包含糖,例如蔗糖或海藻糖。在一个实施方案中,糖为蔗糖,并且药物组合物包含75至275mm的蔗糖,例如100至250mm,例如100mm蔗糖或250mm蔗糖。在本发明的另一个实施方案中,药物组合物不包含多元醇。
[0203]
在另一个实施方案中,本发明的药物组合物包含多元醇,其中所述多元醇是山梨糖醇或甘露醇,其中所述药物组合物优选包含75至275mm山梨糖醇或75至275mm甘露醇,例如100至250mm山梨糖醇或100至250mm甘露醇,例如100mm山梨糖醇或100mm甘露醇或250mm山梨糖醇或100mm甘露醇。在本发明的另一个实施方案中,药物组合物不包含糖。
[0204]
在一个实施方案中,本发明的药物组合物包含0.01%至0.05%的聚山梨酯80(tween 80),例如0.01%到0.04%的聚山梨酯80,例如0.02%的聚山梨酯80或0.04%的聚山梨酯80。
[0205]
在一个实施方案中,本发明的药物组合物的ph为5.5至6.5,例如,5.5或6.5。
[0206]
在一个实施方案中,本发明的药物组合物的ph为5.5至6.5,例如,诸如5.6至6.4,或5.7至6.3,例如5.8至6.2,例如5.9至6.1。
[0207]
在一个实施方案中,本发明的药物组合物具有约6的ph。
[0208]
在本发明的药物组合物的一个实施方案中,组合物还包含氯化钠,例如25至250mm氯化钠,例如100至150mm氯化钠,例如100mm或150mm氯化钠。
[0209]
在一个实施方案中,本发明的药物组合物还包含精氨酸,例如25至200mm的精氨酸,例如50至100mm的精氨酸,例如75mm精氨酸。在一个实施方案中,精氨酸为精氨酸
‑
hcl。
[0210]
在一个实施方案中,本发明的药物组合物包含:
[0211]
a)20mg/ml双特异性抗体,20mm组氨酸,250mm蔗糖和0.02%或0.04%的聚山梨酯80,ph 5.5至6.5,或
[0212]
b)20mg/ml双特异性抗体,20mm组氨酸,100mm蔗糖,0.02%或0.04%的聚山梨酯80和100
‑
150mm,优选100mm的氯化钠,ph 5.5至6.5,或
[0213]
c)20mg/ml双特异性抗体,20mm组氨酸,100mm蔗糖,0.02%或0.04%的聚山梨酯80,75mm精氨酸和100
‑
150mm,优选100mm氯化钠,ph 5.5至6.5,或
[0214]
d)20mg/ml双特异性抗体,20mm组氨酸,100mm蔗糖,0.02%或0.04%的聚山梨酯80和75mm精氨酸,ph 5.5至6.5。
[0215]
在另一个实施方案中,本发明的药物组合物由水溶液中的以下组分组成:
[0216]
a)20mg/ml双特异性抗体,20mm组氨酸,250mm蔗糖和0.02%或0.04%的聚山梨酯80,ph 5.5至6.5,或
[0217]
b)20mg/ml双特异性抗体,20mm组氨酸,100mm蔗糖,0.02%或0.04%的聚山梨酯80和100
‑
150mm,优选100mm的氯化钠,ph 5.5至6.5,或
[0218]
c)20mg/ml双特异性抗体,20mm组氨酸,100mm蔗糖,0.02%或0.04%的聚山梨酯80,75mm精氨酸和100
‑
150mm,优选100mm氯化钠,ph 5.5至6.5,或
[0219]
d)20mg/ml双特异性抗体,20mm组氨酸,100mm蔗糖,0.02%或0.04%的聚山梨酯80和75mm精氨酸,ph 5.5至6.5。
[0220]
在本发明的另一个实施方案中,双特异性抗体的第一抗原结合区包含vh和vl序
列:
[0221]
i)以seq id no:15所示的vh序列和以seq id no:19所示的vl序列或
[0222]
ii)与seq id no 15和19的vh序列和vl序列具有至少90%同一性,例如至少95%同一性,例如至少98%同一性,例如至少99%同一性的vh序列和具有至少90%同一性,例如至少95%同一性,例如至少98%同一性,例如至少99%同一性的vl序列,条件是保留如下的第一抗原结合区的vh cdr1,vh cdr2,vh cdr3,vl cdr1,vl cdr2和vl cdr3序列:
[0223]
以seq id no:16所示的vh cdr1序列,
[0224]
以seq id no:17所示的vh cdr2序列,
[0225]
以seq id no:18所示的vh cdr3序列,
[0226]
以seq id no:20所示的vl cdr1序列,
[0227]
vl cdr2序列:kas和
[0228]
以seq id no:21所示的vl cdr3序列。
[0229]
在本发明的另一个实施方案中,双特异性抗体的第一抗原结合区包含vh和vl序列:
[0230]
iii)以seq id no:15所示的vh序列和以seq id no:127所示的vl序列或
[0231]
iv)与seq id no 15和19的vh序列和vl序列具有至少90%同一性,例如至少95%同一性,例如至少98%同一性,例如至少99%同一性的vh序列和具有至少90%同一性,例如至少95%同一性,例如至少98%同一性,例如至少99%同一性的vl序列,条件是保留如下的所述第一抗原结合区的vh cdr1,vh cdr2,vh cdr3,vl cdr1,vl cdr2和vl cdr3序列:
[0232]
以seq id no:16所示的vh cdr1序列,
[0233]
以seq id no:17所示的vh cdr2序列,
[0234]
以seq id no:18所示的vh cdr3序列,
[0235]
以seq id no:20所示的vl cdr1序列,
[0236]
vl cdr2序列:kas和
[0237]
以seq id no:21所示的vl cdr3序列。
[0238]
在本发明的另一个实施方案中,双特异性抗体的第二抗原结合区包含选自包含以下的组的vh和vl序列:
[0239]
i)以seq id no:22所示的vh序列和以seq id no:29所示的vl序列或
[0240]
ii)与seq id no 22和29的vh序列和vl序列具有至少90%同一性,例如至少95%同一性,例如至少98%同一性,例如至少99%同一性的vh序列和具有至少90%同一性,例如至少95%同一性,例如至少98%同一性,例如至少99%同一性的vl序列,条件是保留如下的第一抗原结合区的vh cdr1,vh cdr2,vh cdr3,vl cdr1,vl cdr2和vl cdr3序列:
[0241]
以seq id no:23所示的vh cdr1序列,
[0242]
以seq id no:24所示的vh cdr2序列,
[0243]
以seq id no:25所示的vh cdr3序列,
[0244]
以seq id no:27所示的vl cdr1序列,
[0245]
vl cdr2序列:yas,以及
[0246]
以seq id no:31所示的vl cdr3序列。
[0247]
因此,在本发明的另一个实施方案中,双特异性抗体包含第一和第二抗原结合区,
其中双特异性抗体的第一抗原结合区包含抗体010的vh和vl序列(即seq id no 15和19)并且其中双特异性抗体的第二抗原结合区包含抗体016的vh和vl序列(即seq id no 22和29)。
[0248]
在本发明的一个实施方案中,双特异性抗体包含第一和第二抗原结合区,其中双特异性抗体的第一抗原结合区包含抗体010的vh和vl序列(即seq id no 15和127)并且其中双特异性抗体的第二抗原结合区包含抗体016的vh和vl序列(即seq id no 22和29)。
[0249]
在本发明的一个优选的实施方案中,双特异性抗体包含第一和第二抗原结合区,其中双特异性抗体的第一抗原结合区包含分别以seq id no 15和127所示的vh和vl序列,并且其中双特异性抗体的第二抗原结合区包含分别以seq id no 22和29所示的vh和vl序列。
[0250]
在一个实施方案中,双特异性抗体的第一抗原结合区具有功能性表位,该功能性表位包含seq id no:62(cd37)的氨基酸y182,d189,t191,i192,d194,k195,v196,i197和p199中的一个或多个。在另一个实施方案中,所述第一抗原结合区结合功能性表位,其包含一个或多个选自seq id no:62(cd37)的y182,d189,t191,i192,d194,k195,v196,i197和p199的氨基酸。在另一个实施方案中,双特异性抗体的第一抗原结合区结合cd37上的功能性表位,其中与具有seq id no:62所示的氨基酸序列的野生型cd37相比对突变体cd37的结合降低,在所述突变体cd37中对应于seq id no 62(cd37)的位置y182,d189,t191,i192,d194,k195,v196,i197和p199的位置处的任何一个或多个氨基酸残基已经用丙氨酸取代;降低的结合确定为所述抗体的结合的z得分(倍数变化)低于
‑
1.5,其中如实施例17所述计算结合的z得分(倍数变化)。
[0251]
在一个实施方案中,双特异性抗体的第二抗原结合区具有功能性表位,该功能性表位包含seq id no:62(cd37)的氨基酸e124,f162,q163,v164,l165和h175中的一个或多个。在另一个实施方案中,所述第二抗原结合区结合功能性表位,所述功能性表位包含选自下组的一个或多个氨基酸:seq id no:62(cd37)的e124,f162,q163,v164,l165和h175。在另一个实施方案中,双特异性抗体的第二抗原结合区结合cd37上的功能性表位,其中与具有seq id no:62所示的氨基酸序列的野生型cd37相比对突变体cd37的结合降低,在所述突变体cd37中对应于seq id no:62(cd37)的位置e124,f162,q163,v164,l165和h175的位置处的任何一个或多个氨基酸残基已经用丙氨酸取代;降低的结合确定为所述抗体的结合的z得分(倍数变化)低于
‑
1.5,其中如实施例17所述计算结合的z得分(倍数变化)。
[0252]
fc
‑
fc增强突变
[0253]
在本发明的一个实施方案中,双特异性抗体的所述第一和第二fc区中的一个或多个fc
‑
fc相互作用增强突变是氨基酸取代。可以说双特异性抗体的fc区包含两个不同的fc区,来自每个亲本抗cd37抗体的一个。双特异性抗体可在每个半分子中包含一个或多个fc
‑
fc相互作用增强突变。在一个实施方案中,fc
‑
fc相互作用增强突变是对称的,即,在两个fc区中产生相同的突变。
[0254]
在一个实施方案中,本发明的药物组合物包含双特异性抗体,其中在所述第一和第二fc区中的一个或多个fc
‑
fc相互作用增强突变是在对应于使用eu编号系统时人igg1中氨基酸位置430、440和345的一个或多个位置处的氨基酸取代。在一个实施方案中,本发明的药物组合物包含双特异性抗体,其中在所述第一和第二fc区中的一个或多个fc
‑
fc相互
作用增强突变是在对应于使用eu编号系统时人igg1中的氨基酸位置430、440和345的一个或多个位置处的氨基酸取代,条件是440中的取代是440y或440w。
[0255]
在另一个实施方案中,本发明的药物组合物包含双特异性抗体,所述双特异性抗体在所述第一和第二fc区中包含选自包含以下的组的至少一个取代:e430g,e345k,e430s,e430f,e430t,e345q,e345r,e345y,s440y和s440w。在特别优选的实施方案中,双特异性抗体在所述第一和第二fc区中包含至少一个取代,其选自e430g或e345k,优选e430g。因此,提供了双特异性抗体,其在具有所述突变的不同抗体之间具有增强的fc
‑
fc相互作用。认为此突变导致抗体在靶细胞上形成寡聚物,从而增强cdc。
[0256]
优选地,在所述第一和第二fc区中的fc
‑
fc相互作用增强突变是在所述第一和第二fc区中的相同取代。因此,在一个优选的实施方案中,双特异性抗体具有两个fc区中相同的fc
‑
fc相互作用增强突变。fc区也可以描述为fc链,使得抗体具有两条fc链,它们构成了抗体的共同fc区。因此,在一个优选的实施方案中,两条fc链各自包含选自下组的位置的取代:对应于当使用eu编号系统时的人igg1中的氨基酸位置430、440和345。在一个实施方案中,两条fc链各自包含e430g取代,从而双特异性抗体包含两个e430g取代。在另一个实施方案中,两条fc链各自包含e345k取代,从而双特异性抗体包含两个e345k取代。
[0257]
在本发明的一个实施方案中,双特异性抗体是igg1同种型。
[0258]
在本发明的一个实施方案中,双特异性抗体是igg2同种型。
[0259]
在本发明的一个实施方案中,双特异性抗体是igg3同种型。
[0260]
在本发明的一个实施方案中,双特异性抗体是igg4同种型。
[0261]
在本发明的一个实施方案中,双特异性抗体是igg同种型。
[0262]
在本发明的一个实施方案中,双特异性抗体是同种型igg1,igg2,igg3和igg4的组合。例如,从第一亲本抗体获得的第一半抗体可以是igg1同种型,而从第二亲本抗体获得的第二半抗体可以是igg4同种型,使得双特异性抗体是igg1和igg4的组合。在另一个实施方案中,它是igg1和igg2的组合。在另一个实施方案中,它是igg1和igg3的组合。在另一个实施方案中,它是igg2和igg3的组合。在另一个实施方案中,它是igg2和igg4的组合。在另一个实施方案中,它是igg3和igg4的组合。通常,核心铰链将是具有序列cppc的igg1型核心铰链,但它也可以是其他稳定且不允许在体内进行fab臂交换的铰链,对于具有序列cpsc的igg4核心铰链就是这种情况。
[0263]
在一个优选的实施方案中,双特异性抗体是全长抗体。
[0264]
在本发明的另一个实施方案中,双特异性抗体是人抗体。在本发明的另一个实施方案中,双特异性抗体是人源化抗体。在本发明的另一个实施方案中,双特异性抗体是嵌合抗体。在本发明的一个实施方案中,双特异性抗体是人,人源化和嵌合的抗体的组合。例如,从第一亲本抗体获得的第一半抗体可以是人抗体,而从第二亲本抗体获得的第二半抗体可以是人源化抗体,使得双特异性抗体是人和人源化的抗体的组合。
[0265]
在本发明的一个优选实施方案中,双特异性抗体结合人和食蟹猴cd37,其分别具有seq id no 62和63所示的序列。这是一个优点,因为这将允许在食蟹猴中使用相同的双特异性分子进行临床前毒理学研究,随后所述双特异性分子将在人中进行测试。在针对人靶物的抗体不也结合动物模型中的靶物的情况下,很难进行分子的临床前毒理学研究和非临床安全性剖析,这是监管机构的要求。
[0266]
双特异性抗体形式
[0267]
本发明提供了包含双特异性cd37
×
cd37抗体的药物组合物,所述双特异性cd37
×
cd37抗体有效促进cdc和/或adcc介导的对表达cd37的肿瘤细胞例如b细胞来源的肿瘤的杀伤。根据具体用途的期望功能特性,可以从本文描述的抗体或抗原结合区的组选择具体的抗原结合区。双特异性抗体的许多不同形式和用途是本领域已知的,并且已由kontermann;drug discov today,2015jul;20(7):838
‑
47和mabs,2012mar
‑
apr;4(2):182
‑
97进行了综述。
[0268]
本发明的背景中的双特异性抗体不限于任何特定的双特异性形式或生产它的方法,然而双特异性抗体应当具有完整的fc域以诱导增强的fc
‑
fc相互作用。
[0269]
可用于本发明的双特异性抗体分子的实例包括:(i)具有包含不同抗原结合区的两个臂的单一抗体;和(ii)双重可变域抗体(dvd
‑
ig),其中每个轻链和重链含有通过短肽连接串联的两个可变域(wu et al.,generation and characterization of a dual variable domain immunoglobulin(dvd
‑
ig
tm
)molecule,于:antibody engineering,springer berlin heidelberg(2010));(iii)基于蛋白质激酶a中“二聚化和对接域”的所谓“对接和锁定”分子。
[0270]
在一个实施方案中,双特异性抗体是通过受控fab臂交换获得的交叉抗体(cross
‑
body)或双特异性抗体(例如wo2011131746(genmab)中所述)。
[0271]
不同类别的双特异性抗体的实例包括但不限于:(i)具有互补ch3域以迫使异二聚化的igg样分子;(ii)重组igg样双重靶向分子,其中分子的两侧各含有至少两种不同抗体的fab片段或fab片段的部分;(iii)igg融合分子,其中全长igg抗体与额外的fab片段或fab片段的部分融合;(iv)fc融合分子,其中单链fv分子或稳定化的双抗体与重链恒定域、fc区或其部分融合;(v)fab融合分子,其中不同的fab片段融合在一起,融合至重链恒定域,fc区或其部分;和(vi)基于scfv和双抗体的重链抗体(例如,域抗体,纳米抗体),其中不同的单链fv分子或不同的双抗体或不同的重链抗体(例如,域抗体,纳米抗体)与fc融合。
[0272]
具有互补ch3域分子的igg类分子的实例包括但不限于triomab/quadroma分子(trion pharma/fresenius biotech;roche,wo2011069104)、所谓的突出
‑
入
‑
空穴分子(genentech,wo9850431)、crossmabs(roche,wo2011117329)和静电操纵分子(amgen,ep1870459和wo2009089004;chugai,us201000155133;oncomed,wo2010129304)、luz
‑
y分子(genentech,wranik et al.j.biol.chem.2012,287(52):43331
‑
9,doi:10.1074/jbc.m112.397869.epub 2012nov 1)、dig
‑
body和pig
‑
body分子(pharmabcine,wo2010134666,wo2014081202)、链交换工程化域体(seedbody)分子(emd serono,wo2007110205)、biclonics分子(merus,wo2013157953)、fcδadp分子(regeneron,wo201015792)、铰链工程化双特异性igg1和igg2分子(pfizer/rinat,wo11143545)、azymetric支架分子(zymeworks/merck,wo2012058768)、mab
‑
fv分子(xencor,wo2011028952)、二价双特异性抗体(wo2009080254)和分子(genmab a/s,wo2011131746)。
[0273]
重组igg类双重靶向分子的实例包括但不限于双重靶向(dt)
‑
ig分子(wo2009058383)、二合一抗体(genentech;bostrom,et al 2009.science 323,1610
–
1614.)、交联的mab(karmanos cancer center)、mab2(f
‑
star,wo2008003116)、zybody分子
(zyngenia;lafleur et al.mabs.2013mar
‑
apr;5(2):208
‑
18)、采用共同轻链的方法(crucell/merus,us7,262,028),κλbodies(novimmune,wo2012023053)和covx
‑
body(covx/pfizer;doppalapudi,v.r.,et al 2007.bioorg.med.chem.lett.17,501
–
506.)。
[0274]
igg融合分子的实例包括但不限于双重可变域(dvd)
‑
ig分子(abbott,us7,612,181)、双重域双头抗体(unilever;sanofi aventis,wo20100226923)、igg类双特异性分子(imclone/eli lilly,lewis etal.nat biotechnol.2014feb;32(2):191
‑
8)、ts2ab(medimmune/az;dimasi et al.j mol biol.2009oct30;393(3):672
‑
92)和bsab分子(zymogenetics,wo2010111625)、hercules分子(biogen idec,us007951918)、scfv融合分子(novartis)、scfv融合分子(changzhou adam biotech inc,cn 102250246)和tvab分子(roche,wo2012025525,wo2012025530)。
[0275]
fc融合分子的实例包括但不限于scfv/fc融合体(pearce et al.,biochem mol biol int.1997sep;42(6):1179
‑
88)、scorpion分子(emergent biosolutions/trubion,blankenship jw,et al.aacr 100th annual meeting 2009(abstract#5465);zymogenetics/bms,wo2010111625)、双重亲和力重新靶向技术(fc
‑
dart)分子(macrogenics,wo2008157379,wo2010080538)和dual(scfv)2
‑
fab分子(national research center for antibody medicine
–
china)。
[0276]
fab融合双特异性抗体的实例包括但不限于f(ab)2分子(medarex/amgen;deo et al j immunol.1998feb 15;160(4):1677
‑
86.)、双重作用或bis
‑
fab分子(genentech,bostrom,et al 2009.science 323,1610
–
1614.)、锁定对接(dnl)分子(immunomedics,wo2003074569,wo2005004809)、二价双特异性分子(biotecnol,schoonjans,j immunol.2000dec 15;165(12):7050
‑
7.)和fab
‑
fv分子(ucb
‑
celltech,wo 2009040562 a1)。
[0277]
基于scfv,基于双抗体的抗体和域抗体的实例包括但不限于双重亲和力重新靶向技术(dart)分子(macrogenics,wo2008157379,wo2010080538)、combody分子(epigen biotech,zhu et al.immunol cell biol.2010aug;88(6):667
‑
75.)和双重靶向纳米抗体(ablynx,hmila et al.,faseb j.2010)。
[0278]
一方面,本发明的药物组合物内包含的双特异性抗体包括包含第一ch3区域的第一fc区和包含第二ch3区域的第二fc区,其中第一和第二ch3区域的序列不同并且使得所述第一和第二ch3区域之间的异二聚体相互作用比所述第一和第二ch3区域的每个同二聚体相互作用更强。在wo2011131746和wo2013060867(genmab)(其通过引用并入本文)中提供了关于这些相互作用以及可以如何实现它们的更多细节。
[0279]
如本文进一步所述,基于一种同二聚体起始cd37抗体和在ch3区中仅含有几个相当保守的不对称突变的另一种同二聚体起始cd37抗体,可以使用特定方法以高收率获得稳定的cd37xcd37双特异性抗体。不对称突变是指所述第一和第二ch3区的序列在不同位置处含有氨基酸取代,从而第一和第二ch3区具有不同的氨基酸序列。
[0280]
在一方面,双特异性抗体包含第一和第二fc区,其中所述第一和第二fc区各自至少包含铰链区、ch2和ch3区,其中在所述第一fc区中,已经取代了对应于选自下组的位置的位置中的氨基酸中的至少一个:人igg1重链中的t366、l368、k370、d399、f405、y407和k409,并且在所述第二fc区中,已经取代了对应于选自下组的位置的位置中的氨基酸中的至少一
个:人igg1重链中的t366、l368、k370、d399、f405、y407和k409,且其中所述第一和所述第二fc区未在相同位置中取代。
[0281]
因此,在本发明的优选的实施方案中,双特异性抗体的第一fc区包含对应于人igg1中位置f405的氨基酸的突变,并且双特异性抗体的第二fc区包含对应于人igg1中的位置k409的氨基酸的进一步突变。因此,这些突变与上文提及的fc
‑
fc相互作用增强突变相比是不对称的。
[0282]
在一个实施方案中,第一fc区具有位置366处的氨基酸取代,并且所述第二fc区具有选自下组的位置处的氨基酸取代:368、370、399、405、407和409。在一个实施方案中,位置366处的氨基酸取代选自ala、asp、glu、his、asn、val或gln。
[0283]
在一个实施方案中,第一fc区具有位置368处的氨基酸取代,并且所述第二fc区具有选自下组的位置处的氨基酸取代:366、370、399、405、407和409。
[0284]
在一个实施方案中,第一fc区具有位置370处的氨基酸取代,并且所述第二fc区具有选自下组的位置处的氨基酸取代:366、368、399、405、407和409。
[0285]
在一个实施方案中,第一fc区具有位置399处的氨基酸取代,并且所述第二fc区具有选自下组的位置处的氨基酸取代:366、368、370、405、407和409。
[0286]
在一个实施方案中,第一fc区具有位置405处的氨基酸取代,并且所述第二fc区具有选自下组的位置处的氨基酸取代:366、368、370、399、407和409。
[0287]
在一个实施方案中,第一fc区具有位置407处的氨基酸取代,并且所述第二fc区具有选自下组的位置处的氨基酸取代:366、368、370、399、405和409。
[0288]
在一个实施方案中,第一fc区具有位置409处的氨基酸取代,并且所述第二fc区具有选自下组的位置处的氨基酸取代:366、368、370、399、405和407。
[0289]
因而,在一个实施方案中,所述第一和第二fc区的序列含有不对称突变,即两个fc区中的不同位置处的突变,例如fc区之一中位置405处的突变和另一个fc区中的位置409处的突变。
[0290]
在一个实施方案中,第一fc区具有409位置处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys并且所述第二fc区具有选自下组的位置处的氨基酸取代:366、368、370、399、405和407。在一个此类实施方案中,所述第一fc区具有409位置处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys,并且所述第二fc区具有405位置处的除phe外的氨基酸,例如gly、ala、val、ile、ser、thr、lys、arg、his、asp、asn、glu、gln、pro、trp、tyr、cys、lys或leu。在本文的进一步的实施方案中,所述第一fc区具有409位置处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys,并且所述第二fc区具有405位置处的除phe、arg或gly以外的氨基酸,例如leu、ala、val、ile、ser、thr、met、lys、his、asp、asn、glu、gln、pro、trp、tyr或cys。
[0291]
在另一个实施方案中,所述第一fc区包含405位置处的phe和409位置处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys并且所述第二fc区包含405位置处的除phe以外的氨基酸,例如gly、ala、val、ile、ser、thr、lys、arg、his、asp、asn、glu、gln、pro、trp、tyr、leu、met或cys和409位置
处的lys。在本文的进一步实施方案中,所述第一fc区包含405位置处的phe和409位置处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr,或cys并且所述第二fc区包含405位置处的除phe、arg或gly以外的氨基酸,例如leu、ala、val、ile、ser、thr、met、lys、his、asp、asn、glu、gln、pro、trp、tyr或cys和409位置处的lys。
[0292]
在另一个实施方案中,所述第一fc区包含405位置处的phe和409位置处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys并且所述第二fc区包含位置405处的leu和位置409处的lys。在本文的进一步的实施方案中,所述第一ch3区包含位置405处的phe和位置409处的arg并且所述第二fc区包含位置405处的除phe、arg或gly以外的氨基酸,例如leu、ala、val、ile、ser、thr、lys、met、his、asp、asn、glu、gln、pro、trp、tyr或cys和位置409处的lys。在另一个实施方案中,所述第一fc区包含位置405处的phe和位置409处的arg并且所述第二ch3区包含位置405处的leu和位置409处的lys。
[0293]
在另一个实施方案中,所述第一fc区包含位置409处的除lys、leu或met外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys并且所述第二fc区包含位置409处的lys、位置370处的thr和位置405处的leu。在另一个实施方案中,所述第一fc区包含位置409处的arg并且所述第二fc区包含位置409处的lys、位置370处的thr和位置405处的leu。
[0294]
在另一个实施方案中,所述第一fc区包含位置370处的lys、位置405处的phe和位置409处的arg,并且所述第二fc区包含位置409处的lys、位置370处的thr和位置405处的leu。
[0295]
在另一个实施方案中,所述第一fc区包含位置409处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys并且所述第二fc区包含位置409处的lys和:a)位置350处的ile和位置405处的leu,或b)位置370处的thr和位置405处的leu。
[0296]
在另一个实施方案中,所述第一fc区包含位置409处的arg并且所述第二fc区包含位置409处的lys和:a)位置350处的ile和位置405处的leu,或b)位置370处的thr和位置405处的leu。
[0297]
在另一个实施方案中,所述第一fc区包含位置350处的thr、位置370处的lys、位置405处的phe和位置409处的arg并且所述第二fc区包含位置409处的lys和:a)位置350处的ile和位置405处的leu,或b)位置370处的thr和位置405处的leu。
[0298]
在另一个实施方案中,所述第一fc区包含位置350处的thr、位置370处的lys、位置405处的phe和位置409处的arg,并且所述第二fc区包含位置350处的ile、位置370处的thr、位置405处的leu和位置409处的lys。
[0299]
在一个实施方案中,所述第一fc区具有位置409处的除lys、leu或met以外的氨基酸并且所述第二fc区具有位置405处的除phe以外的氨基酸,诸如除phe、arg或gly以外;或者所述第一ch3区具有位置409处的除lys、leu或met以外的氨基酸并且所述第二ch3区具有位置407处的除tyr、asp、glu、phe、lys、gln、arg、ser或thr以外的氨基酸。
[0300]
在一个实施方案中,双特异性抗体包含具有位置409处的除lys、leu或met以外的
氨基酸的第一fc区和具有位置407处的除tyr、asp、glu、phe、lys、gln、arg、ser或thr以外的氨基酸的第二fc区。
[0301]
在一个实施方案中,双特异性抗体包含具有位置407处的tyr和位置409处的除lys、leu或met以外的氨基酸的第一ch3区和具有位置407处的除tyr、asp、glu、phe、lys、gln、arg、ser或thr以外的氨基酸和位置409处的lys的第二ch3区。
[0302]
在一个实施方案中,双特异性抗体包含具有位置407处的tyr和位置409处的arg的第一fc区和具有位置407处的除tyr、asp、glu、phe、lys、gln、arg、ser或thr以外的氨基酸和位置409处的lys的第二fc区。
[0303]
在另一个实施方案中,所述第一fc区具有位置409处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys并且所述第二fc区具有位置407处的除tyr、asp、glu、phe、lys、gln、arg、ser或thr以外的氨基酸,例如leu、met、gly、ala、val、ile、his、asn、pro、trp或cys。在另一个实施方案中,所述第一fc区具有位置409处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys并且所述第二fc区具有位置407处的ala、gly、his、ile、leu、met、asn、val或trp。
[0304]
在另一个实施方案中,所述第一fc区具有位置409处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr,或cys并且所述第二fc区具有位置407处的gly、leu、met、asn或trp。
[0305]
在另一个实施方案中,所述第一fc区具有位置407处的tyr和位置409处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys并且所述第二fc区具有位置407处的除tyr、asp、glu、phe、lys、gln、arg、ser或thr以外的氨基酸,例如leu、met、gly、ala、val、ile、his、asn、pro、trp或cys和位置409处的lys。
[0306]
在另一个实施方案中,所述第一fc区具有位置407处的tyr和位置409处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys,并且所述第二fc区具有位置407处的ala、gly、his、ile、leu、met、asn、val或trp和位置409处的lys。
[0307]
在另一个实施方案中,所述第一fc区具有位置407处的tyr和位置409处的除lys、leu或met以外的氨基酸,例如gly,ala,val,ile,ser,thr,phe,arg,his,asp,asn,glu,gln,pro,trp,tyr或cys,并且所述第二fc区具有位置407处的gly,leu,met,asn或trp和位置409处的lys。
[0308]
在另一个实施方案中,所述第一fc区具有位置407处的tyr和位置409处的arg并且所述第二fc区具有位置407处的除tyr,asp,glu,phe,lys,gln,arg,ser或thr以外的氨基酸,例如leu,met,gly,ala,val,ile,his,asn,pro,trp或cys和位置409处的lys。
[0309]
在另一个实施方案中,所述第一fc区具有位置407处的tyr和位置409处的arg并且所述第二fc区具有位置407处的ala,gly,his,ile,leu,met,asn,val或trp和位置409处的lys。
[0310]
在另一个实施方案中,所述第一fc区具有位置407处的tyr和位置409处的arg,并且所述第二fc区具有位置407处的gly、leu、met、asn或trp和位置409处的lys。
[0311]
在另一个实施方案中,所述第一fc区具有位置409处的除lys、leu或met以外的氨基酸,例如gly、ala、val、ile、ser、thr、phe、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys并且第二fc区具有
[0312]
(i)位置368处除phe、leu和met以外的氨基酸,例如gly、ala、val、ile、ser、thr、lys、arg、his、asp、asn、glu、gln、pro、trp、tyr或cys,或
[0313]
(ii)位置370处的trp,或
[0314]
(iii)位置399处的除asp、cys、pro、glu或gln以外的氨基酸,例如phe、leu、met、gly、ala、val、ile、ser、thr、lys、arg、his、asn、trp、tyr或cys,或
[0315]
(iv)位置366处的除lys、arg、ser、thr或trp以外的氨基酸,例如phe、leu、met、ala、val、gly、ile、asn、his、asp、glu、gln、pro、tyr或cys。
[0316]
在一个实施方案中,第一fc区具有位置409处的arg,ala,his或gly,并且第二fc区具有
[0317]
(i)位置368处的lys、gln、ala、asp、glu、gly、his、ile、asn、arg、ser、thr、val或trp,或
[0318]
(ii)位置370处的trp,或
[0319]
(iii)位置399处的ala、gly、ile、leu、met、asn、ser、thr、trp、phe、his、lys、arg或tyr,或
[0320]
(iv)位置366处的ala、asp、glu、his、asn、val、gln、phe、gly、ile、leu、met或tyr。
[0321]
在一个实施方案中,第一fc区具有位置409处的arg,并且第二fc区具有:
[0322]
(i)位置368处的asp、glu、gly、asn、arg、ser、thr、val或trp或
[0323]
(ii)位置370处的trp,或
[0324]
(iii)位置399处的phe、his、lys、arg或tyr,或
[0325]
(iv)位置366处的ala、asp、glu、his、asn、val、gln。
[0326]
除了上述规定的氨基酸取代外,相对于野生型fc序列,所述第一和第二fc区可进一步含有氨基酸取代、缺失或插入。
[0327]
在本发明的优选实施方案中,当使用eu编号时,双特异性抗体的第二fc区包含对应于人igg1中的f405的突变,并且第一fc区包含对应于人igg1中的k409的突变。
[0328]
在一个实施方案中,在位置f405和k409处的突变是取代。在一个特定的实施方案中,在位置f405处的取代是f405l取代。在另一个实施方案中,在位置k409处的取代是k409r取代。
[0329]
在一个优选的实施方案中,使用eu编号时
[0330]
a)第一fc区包含对应于人igg1中的f405l的进一步突变,并且第二fc区包含对应于人igg1中的k409r的进一步突变,或
[0331]
b)第二fc区包含对应于人igg1中的f405l的进一步突变,并且第一fc区包含对应于人igg1中的k409r的进一步突变。
[0332]
在双特异性抗体是igg4同种型的实施方案中,第一fc区可进一步包含f405l取代和r409k取代。在此类实施方案中,第二fc区在405和409氨基酸位置中的任一处不被取代。
[0333]
应当理解,除非明确说明,否则在公开的位置处所有提及的氨基酸突变都是相对于人igg1的突变,并且是使用人igg1使用eu编号系统进行编号。
[0334]
在本发明的一个实施方案中,第一或第二fc区包含选自下组的序列:seq id no 128,seq id no 129,seq id no 130,seq id no 131,seq id no 132,seq id no 133,seq id no 134和seq id no 135。在本发明的一个实施方案中,第一和第二fc区包含选自下组的序列:seq id no 128,seq id no 129,seq id no 130,seq id no 131,seq id no 132,seq id no 133,seq id no 134和seq id no 135。
[0335]
在本发明的一个实施方案中,第一fc区包含以seq id no:128所示的序列,并且第二fc区包含seq id no:129所示的序列,反之亦然。在本发明的一个实施方案中,第一fc区包含以seq id no:130所示的序列,并且第二fc区包含以seq id no:133所示的序列,反之亦然。在本发明的一个实施方案中,第一fc区包含以seq id no:131所示的序列,并且第二fc区包含以seq id no:134所示的序列,反之亦然。在本发明的一个实施方案中,第一fc区包含以seq id no:132所示的序列,并且第二fc区包含以seq id no:135所示的序列,反之亦然。
[0336]
在一个实施方案中,所述第一fc区和所述第二fc区在核心铰链区中都不包含cys
‑
pro
‑
ser
‑
cys序列。
[0337]
在另一个实施方案中,所述第一和第二fc区两者在核心铰链区中均包含cys
‑
pro
‑
pro
‑
cys序列。
[0338]
因此,提供了双特异性抗体,其可以以高产率产生并且在体内是稳定的。
[0339]
在另一个实施方案中,与没有fc
‑
fc相互作用增强突变的相同双特异性抗体相比,双特异性抗体具有增加的cdc和/或adcc效应器功能。在另一个实施方案中,与具有双特异性抗体的第一或第二结合区的结合区并且与本发明中使用的双特异性抗体具有相同的fc
‑
fc增强突变的单克隆亲本抗体相比,本发明中使用的双特异性抗体具有增加的cdc和/或adcc效应器功能。
[0340]
在本发明的药物组合物的一个实施方案中,所述双特异性抗体由以seq id no:118和120所示的重链和以seq id no:119和121所示的轻链组成,其中以seq id no:118中所示的重链与以seq id no:119所示的轻链形成抗原结合区,并且其中以seq id no:120所示的重链与以seq id no:121所示的轻链形成抗原结合区。
[0341]
在本发明的药物组合物的一个优选实施方案中,所述双特异性抗体由以seq id no:124和125所示的重链和以seq id no:119和126所示的轻链组成,其中以seq id no:124中所示的重链与以seq id no:119所示的轻链形成抗原结合区,并且其中以seq id no:125所示的重链与以seq id no:126所示的轻链形成抗原结合区。
[0342]
制备双特异性抗体的方法
[0343]
传统方法诸如杂交杂交瘤和化学缀合方法(marvin and zhu(2005)acta pharmacol sin 26:649)可以用于制备本发明的药物组合物内包含的双特异性抗体。除了期望的双特异性抗体外,在宿主细胞中共表达两种抗体(它们由不同的重链和轻链组成)导致可能的抗体产物的混合物,其然后可以通过例如亲和层析或类似方法分离。
[0344]
当共表达不同抗体构建体时,也可以使用有利于形成功能性双特异性产物的策略,例如,lindhofer et al.(1995j immunol 155:219)所述的方法。产生不同抗体的大鼠和小鼠杂交瘤的融合导致有限数量的异二聚体蛋白,这是由于优先的物种限制的重/轻链配对。相对于同二聚体促进异二聚体形成的另一种策略是“突出
‑
入
‑
空穴”策略,其中在第
一重链多肽中引入突出,并且在第二重链多肽中引入相应的腔,使得该突出可以位于这两个重链的界面处的腔中,从而促进异二聚体的形成并阻碍同二聚体的形成。通过用较大的侧链替换来自第一多肽的界面的小的氨基酸侧链来构建“突出”。通过用较小的氨基酸侧链替换大的氨基酸侧链在第二多肽的界面中创建与突出相同或相似大小的补偿“腔”(美国专利5,731,168)。ep1870459(chugai)和wo2009089004(amgen)描述了有利于在宿主细胞中不同抗体域共表达后异二聚体形成的其他策略。在这些方法中,构成这两个ch3域中ch3
‑
ch3界面的一个或多个残基替换为带电荷的氨基酸,使得同二聚体的形成在静电上是不利的,而异二聚化在静电上是有利的。wo2007110205(merck)描述了另一种策略,其中利用iga和igg ch3域之间的差异来促进异二聚化。
[0345]
wo2008119353(genmab)中已经描述了另一种产生双特异性抗体的体外方法,其中双特异性抗体通过还原条件下温育后两个单特异性抗体igg4
‑
或igg4
‑
样抗体之间的“fab臂”或“半分子”交换(交换重链和连接的轻链)形成。所得的产物是具有两个可以包含不同序列的fab臂的双特异性抗体。
[0346]
用于制备双特异性cd37xcd37抗体的优选方法包括wo2011131746和wo2013060867(genmab)中所述的方法,包括以下步骤:
[0347]
a)提供包含fc区的第一抗体,所述fc区包含第一ch3区;
[0348]
b)提供包含第二fc区的第二抗体,所述fc区包含第二ch3区,其中所述第一抗体是cd37抗体,而所述第二抗体是不同的cd37抗体;
[0349]
其中所述第一和第二ch3区域的序列不同,并且使得所述第一和第二ch3区域之间的异二聚体相互作用强于所述第一和第二ch3区域的每个同二聚体相互作用;
[0350]
c)在还原条件下将所述第一抗体与所述第二抗体一起温育;和
[0351]
d)获得所述双特异性抗体。
[0352]
在一个实施方案中,在足以使铰链区中的半胱氨酸经历二硫键异构化的还原条件下将所述第一抗体与所述第二抗体一起温育,其中在所得异二聚体抗体中所述第一抗体和第二抗体之间的异二聚体相互作用使得在37℃的24小时后在0.5mm gsh未发生fab臂交换。
[0353]
不受理论的限制,在步骤c)中,亲本抗体的铰链区中的重链二硫键被还原,然后所得的半胱氨酸能够与另一个亲本抗体分子(最初具有不同的特异性)的半胱氨酸残基形成重链间的二硫键。在此方法的一个实施方案中,步骤c)中的还原条件包括添加还原剂,例如选自下组的还原剂:2
‑
巯基乙胺(2
‑
mea)、二硫苏糖醇(dtt)、二硫丁四醇(dte)、谷胱甘肽、三(2
‑
羧乙基)膦(tcep)、l
‑
半胱氨酸和β
‑
巯基
‑
乙醇,优选选自下组的还原剂:2
‑
巯基乙胺、二硫苏糖醇和三(2
‑
羧乙基)膦。在另一个实施方案中,步骤c)包括恢复条件以变为非还原性的或还原性较小的,例如通过除去还原剂,例如通过脱盐。
[0354]
对于此方法,可以使用本文所述的任何cd37抗体,包括第一和第二cd37抗体,其包含第一和/或第二fc区。此类第一和第二fc区的实例(包括此类第一和第二fc区的组合)可以包括本文所述的任何那些。
[0355]
在此方法的一个实施方案中,所述第一和/或第二抗体是全长抗体。
[0356]
第一和第二抗体的fc区可以是任何同种型,包括但不限于igg1,igg2,igg3或igg4。在此方法的一个实施方案中,所述第一和第二抗体两者的fc区均为igg1同种型。在另一个实施方案中,所述抗体的fc区之一是igg1同种型,而另一个是igg4同种型。在后一个实
施方案中,所得的双特异性抗体包含igg1的fc区和igg4的fc区,因此就效应器功能的激活而言可以具有令人感兴趣的中间性质。
[0357]
在另一个实施方案中,已经将抗体起始蛋白之一工程化改造为不结合蛋白a,从而允许通过使产物通过蛋白a柱而将异二聚体蛋白与所述同二聚体起始蛋白分离。
[0358]
如上所述,同二聚体起始抗体(亲本抗体)的第一和第二ch3区的序列是不同的,并且使得所述第一和第二ch3区之间的异二聚体相互作用强于所述第一和第二ch3区的每个同二聚体相互作用。在wo2011131746和wo2013060867(genmab)(其在此通过引用完整并入)中已经提供了关于这些相互作用以及如何可以实现它们的更多细节。
[0359]
特别地,稳定的双特异性cd37xcd37抗体可以使用上述方法,基于结合cd37的不同表位并且在ch3区中仅含有几个相当保守的不对称突变的两个同二聚体起始抗体以高产率获得。不对称突变是指所述第一和第二ch3区的序列在不同位置处含有氨基酸取代。
[0360]
双特异性抗体也可以通过在单一细胞中共表达编码第一和第二多肽的构建体来获得。此类方法可以包括以下步骤:
[0361]
a)提供第一核酸构建体,其编码包含第一抗体重链的第一fc区和第一抗原结合区的第一多肽,所述第一fc区包含第一ch3区,
[0362]
b)提供第二核酸构建体,其编码包含第二抗体重链的第二fc区和第二抗原结合区的第二多肽,所述第二fc区包含第二ch3区,
[0363]
其中所述第一和第二ch3区的序列不同,并且使得所述第一和第二ch3区域之间的异二聚体相互作用强于所述第一和第二ch3区域的每个同二聚体相互作用,
[0364]
任选地,其中所述第一和第二核酸构建体编码所述第一和第二抗体的轻链序列
[0365]
c)在宿主细胞中共表达所述第一和第二核酸构建体,和
[0366]
d)从细胞培养物中获得所述异二聚体蛋白。
[0367]
在一个实施方案中,如本文公开的任何实施方案中所定义的双特异性抗体包含第一fc区和第二fc区,其中所述第一fc区和所述第二fc区在铰链区中都不包含cys
‑
pro
‑
ser
‑
cys序列。
[0368]
在一个实施方案中,如本文公开的任何实施方案中所定义的双特异性抗体包含第一fc区和第二fc区,其中所述第一fc区和所述第二fc区两者在铰链区中都包含cys
‑
pro
‑
pro
‑
cys序列。
[0369]
在一个实施方案中,如本文公开的任何实施方案中所定义的双特异性抗体包含第一fc区和第二fc区,其中所述第一fc区和第二fc区是人抗体fc区。
[0370]
在一个实施方案中,如本文公开的任何实施方案中所定义的双特异性抗体包含第一fc区和第二fc区,其中第一和第二抗原结合区包含人抗体vh序列和任选地人抗体vl序列。
[0371]
在一个实施方案中,如本文公开的任何实施方案中所定义的双特异性抗体包含第一fc区和第二fc区,其中第一和第二抗原结合区包含第一和第二轻链。
[0372]
合适的表达载体,包括启动子,增强子等,以及适合于产生抗体的宿主细胞是本领域中公知的。宿主细胞的实例包括酵母,细菌和哺乳动物细胞,例如cho或hek细胞。
[0373]
因此,在本发明的上下文中,表达载体可以是任何合适的载体,包括染色体,非染色体和合成核酸载体(包含合适的表达控制元件组的核酸序列)。此类载体的实例包括sv40
的衍生物,细菌质粒,噬菌体dna,杆状病毒,酵母质粒,源自质粒和噬菌体dna的组合的载体,以及病毒核酸(rna或dna)载体。在一个实施方案中,编码cd37抗体的核酸包含在裸dna或rna载体中,所述裸dna或rna载体包括例如线性表达元件(例如如记载于sykes and johnston,nat biotech 17,355 59(1997)),紧实的核酸载体(例如如记载于us6,077,835和/或wo 00/70087),质粒载体,例如pbr322,puc 19/18或puc118/119,“蚊(midge)”最小程度尺寸的核酸载体(如schakowski et al.,mol ther3,793
‑
800(2001)中所述),或作为沉淀的核酸载体构建体,如cap04沉淀的构建体(如例如wo200046147,benvenisty and reshef,pnas usa 83,9551
‑
55(1986),wigler et al.,cell 14,725(1978)和coraro and pearson,somatic cell genetics 7,603(1981)中所述)。此类核酸载体及其用途是本领域公知的(参见例如us 5,589,466和us 5,973,972)。
[0374]
载体可以适合于在细菌细胞中表达抗体。
[0375]
此类载体的实例包括表达载体,例如bluescript(stratagene),pin载体(van heeke&schuster,j biol chem 264,5503
‑
5509(1989),pet载体(novagen,madison wi)等。
[0376]
此外/或者,表达载体可以是适合在酵母系统中表达的载体。可以采用适合在酵母系统中表达的任何载体。合适的载体包括例如包含组成型或诱导型启动子,例如α因子,醇氧化酶和pgh的载体(综述于:f.ausubel et al.编current protocols in molecular biology,greene publishing and wiley interscience new york(1987)和grant et al.,methods in enzymol 153,516
‑
544(1987))。
[0377]
此外/或者,表达载体可以是适合在哺乳动物细胞中表达的载体,例如包含谷氨酰胺合成酶作为选择标志物的载体,例如bebbington(1992)biotechnology(ny)10:169
‑
175中描述的载体。
[0378]
核酸和/或载体也可以包含编码分泌/定位序列的核酸序列,所述分泌/定位序列可以将诸如新生多肽链的多肽靶向到周质空间或进入细胞培养基中。此类序列是本领域已知的,并且包括分泌前导序列或信号肽。
[0379]
表达载体可以包含任何合适的启动子,增强子和其他表达促进元件或与之相关。此类元件的实例包括强表达启动子(例如人cmv ie启动子/增强子以及rsv,sv40,sl3
‑
3,mmtv和hiv ltr启动子),有效的多聚(a)终止序列,大肠杆菌中质粒产物的复制起点,作为选择标志物的抗生素抗性基因和/或便利的克隆位点(例如,多接头)。与组成型启动子例如cmv ie相反,核酸还可以包含诱导型启动子。
[0380]
在一个实施方案中,可将编码cd37抗体的表达载体通过病毒载体定位在宿主细胞或宿主动物中和/或递送至宿主细胞或宿主动物。
[0381]
本发明的其他实施方案
[0382]
在另一个实施方案中,本发明涉及组合物,其包含本发明的双特异性抗体并且进一步包含单特异性抗cd37抗体,优选地具有双特异性抗体的第一或第二抗原结合区的抗原结合区的抗cd37抗体。
[0383]
在另一个实施方案中,本发明涉及用作药物的本发明的药物组合物。
[0384]
在一个实施方案中,本发明涉及用于治疗癌症,自身免疫疾病或炎性病症的本发明的药物组合物。
[0385]
在另一个实施方案中,本发明涉及本发明的药物组合物,其用于治疗变态反应,移
植排斥或b细胞恶性疾病,例如非何杰金淋巴瘤(nhl),慢性淋巴细胞性白血病(cll),滤泡性淋巴瘤(fl),套细胞淋巴瘤(mcl),浆细胞白血病(pcl),弥漫性大b细胞淋巴瘤(dlbcl)或急性成淋巴细胞性白血病(all)。
[0386]
在一个实施方案中,胃肠外施用,例如皮下,肌肉内或静脉内施用根据本发明使用的药物组合物。
[0387]
在另一个实施方案中,本发明涉及本发明的药物组合物,用于治疗类风湿性关节炎,例如急性关节炎,慢性类风湿关节炎,痛风或痛风性关节炎,急性痛风性关节炎,急性免疫性关节炎,慢性炎性关节炎,变性关节炎,ii型胶原诱导的关节炎,传染性关节炎,莱姆关节炎,增生性关节炎,银屑病关节炎,斯蒂尔氏病,椎骨关节炎和青少年型类风湿关节炎,骨关节炎,慢性进行性关节炎(arthritis chronica progrediente),变形性关节炎,慢性原发性关节炎(polyarthritis chronica primaria),反应性关节炎,和强直性脊柱炎,系统性红斑狼疮(sle),例如皮肤性sle或亚急性皮肤性sle,新生儿狼疮综合征(nle)和播散性红斑狼疮,多发性硬化症,炎性肠病(ibd),包括溃疡性结肠炎和克罗恩氏病,慢性阻塞性肺疾病(copd),银屑病,iga肾病,igm多发性神经病,重症肌无力,糖尿病,雷诺氏综合征(reynaud’s syndrome)和肾小球肾炎,掌足脓疱疹(pustulosis palmoplantaris,ppp),糜烂性扁平苔藓(erosive lichen planus),大疱性天疱疮(pemphigus bullosa),大疱性表皮松解(epidermolysis bullosa),接触性皮炎和特应性皮炎,多神经根炎,包括格
‑
巴二氏综合征(guillain
‑
barre syndrome)。
[0388]
在另一个实施方案中,本发明涉及用于治疗变态反应,移植排斥或b细胞恶性疾病的本发明的药物组合物。
[0389]
在另一个实施方案中,本发明涉及与一种或多种进一步治疗剂组合使用的本发明的药物组合物。一种或多种进一步治疗剂可以例如选自包含以下的组:多柔比星、顺铂、博来霉素、卡莫司汀、环磷酰胺、苯丁酸氮芥、苯达莫司汀、长春新碱、氟达拉滨、依鲁替尼和抗cd 20抗体,如利妥昔单抗、奥法木单抗、奥滨尤妥珠单抗(obinutuzumab)、维妥珠单抗(veltuzumab)、ocaratuzumab、奥瑞珠单抗(ocrelizumab)或tru
‑
015。
[0390]
在一个优选的实施方案中,另一种治疗剂是抗cd20抗体。在一个实施方案中,抗cd20抗体能够结合具有以seq id no:72所示的序列的人cd20。在一个实施方案中,抗cd20抗体能够结合具有以seq id no:73所示的序列的食蟹猴cd20。在一个实施方案中,抗cd20抗体能够结合具有分别以seq id no 72和73所示的序列的人和食蟹猴cd20。
[0391]
在一个实施方案中,抗cd20抗体能够结合人cd20上的表位,该表位不包含或不需要seq id no.72的170位的氨基酸残基丙氨酸或172位的脯氨酸,但是包含或需要163位的氨基酸残基天冬酰胺和166位的天冬酰胺。此类抗体的实例是如wo2004035607(genmab)中公开的表示为2f2和7d8的抗体和如wo2005103081(genmab)中公开的表示为2c6的抗体。表1公开了7d8的cdr序列。
[0392]
在一个实施方案中,抗cd20抗体能够结合人cd20上的表位,该表位不包含或不需要seq id no.72的170位的氨基酸残基丙氨酸或172位的脯氨酸。此类抗体的实例是11b8,如wo2004035607(genmab)中公开的。表1中公开了11b8的cdr序列。
[0393]
在一个实施方案中,抗cd20抗体能够结合人cd20上的不连续表位,其中表位包含第一小细胞外环的一部分和第二细胞外环的一部分。
[0394]
在一个实施方案中,抗cd20抗体能够结合人cd20上的不连续表位,其中表位具有小的第一细胞外环的残基agiyap和第二细胞外环的残基meslnfirahtpy。
[0395]
抗cd20抗体可以表征为i型和ii型抗cd20抗体。i型抗cd20抗体具有较高的cdc和adcc活性,但是较低的凋亡活性,例如奥法木单抗(2f2)和利妥昔单抗,而ii型抗cd20抗体具有低cdc活性或无cdc活性,但具有较高的adcc和凋亡活性,例如,奥滨尤妥珠单抗和11b8。i型抗体也诱导cd20重新分配到较大的洗涤剂抗性的微域(筏)中,而ii型抗体不然。
[0396]
在一个实施方案中,抗cd20抗体包含能够结合人cd20的抗原结合区,其中抗原结合区与包含分别如seq id no 74和seq id no 78所示的可变重链(vh)序列和可变轻链(vl)的抗cd20抗体竞争结合人cd20。
[0397]
在一个实施方案中,抗cd20抗体包含能够结合人cd20的抗原结合区,其中抗原结合区与包含分别如seq id no 81和seq id no 109所示的可变重链(vh)序列和可变轻链(vl)的抗cd20抗体竞争结合人cd20。
[0398]
在一个实施方案中,抗cd20抗体包含能够结合人cd20的抗原结合区,其中抗原结合区与包含分别如seq id no 94和seq id no 98所示的可变重链(vh)序列和可变轻链(vl)的抗cd20抗体竞争结合人cd20。
[0399]
在一个实施方案中,抗cd20抗体包含能够结合人cd20的抗原结合区,其中抗原结合区与包含分别如seq id no 87和seq id no 91所示的可变重链(vh)序列和可变轻链(vl)的抗cd20抗体竞争结合人cd20。
[0400]
在一个实施方案中,抗cd20抗体包含能够结合人cd20的抗原结合区,其中抗原结合区与包含分别如seq id no 101和seq id no 105所示的可变重链(vh)序列和可变轻链(vl)的抗cd20抗体竞争结合人cd20。
[0401]
在一个实施方案中,抗cd20抗体包含能够结合人cd20的抗原结合区,其包含cdr序列:
[0402]
以seq id no:75所示的vh cdr1序列,
[0403]
以seq id no:76所示的vh cdr2序列,
[0404]
以seq id no:77所示的vh cdr3序列,
[0405]
以seq id no:79所示的vl cdr1序列,
[0406]
vl cdr2序列das,和
[0407]
以seq id no:80所示的vl cdr3序列。[7d8]
[0408]
在一个实施方案中,抗cd20抗体包含能够结合人cd20的抗原结合区,其包含cdr序列:
[0409]
以seq id no:82所示的vh cdr1序列,
[0410]
以seq id no:83所示的vh cdr2序列,
[0411]
以seq id no:84所示的vh cdr3序列,
[0412]
以seq id no:85所示的vl cdr1序列,
[0413]
vl cdr2序列das,和
[0414]
以seq id no:86所示的vl cdr3序列。[118b]
[0415]
在一个实施方案中,抗cd20抗体包含能够结合人cd20的抗原结合区,其包含cdr序列:
[0416]
以seq id no:95所示的vh cdr1序列,
[0417]
以seq id no:96所示的vh cdr2序列,
[0418]
以seq id no:97所示的vh cdr3序列,
[0419]
以seq id no:99所示的vl cdr1序列,
[0420]
vl cdr2序列ats,和
[0421]
以seq id no:100所示的vl cdr3序列。[利妥昔单抗]
[0422]
在一个实施方案中,抗cd20抗体包含能够结合人cd20的抗原结合区,其包含cdr序列:
[0423]
以seq id no:88所示的vh cdr1序列,
[0424]
以seq id no:89所示的vh cdr2序列,
[0425]
以seq id no:90所示的vh cdr3序列,
[0426]
以seq id no:92所示的vl cdr1序列,
[0427]
vl cdr2序列das,和
[0428]
以vl cdr3序列在seq id no:93所示。[奥法木单抗]
[0429]
在一个实施方案中,抗cd20抗体包含能够结合人cd20的抗原结合区,其包含cdr序列:
[0430]
以seq id no:102所示的vh cdr1序列,
[0431]
以seq id no:103所示的vh cdr2序列,
[0432]
以seq id no:104所示的vh cdr3序列,
[0433]
以seq id no:106所示的vl cdr1序列,
[0434]
vl cdr2序列qms,和
[0435]
以seq id no:107所示的vl cdr3序列。[奥滨尤妥珠单抗]
[0436]
在一个实施方案中,抗cd20抗体包含能够结合人cd20的抗原结合区,其包含选自下组的cdr序列:
[0437]
i)以seq id no:75所示的vh cdr1序列,
[0438]
以seq id no:76所示的vh cdr2序列,
[0439]
以seq id no:77所示的vh cdr3序列,
[0440]
以seq id no:79所示的vl cdr1序列
[0441]
vl cdr2序列das,和
[0442]
以seq id no:80所示的vl cdr3序列。[7d8];
[0443]
ii)以seq id no:82所示的vh cdr1序列,
[0444]
以seq id no:83所示的vh cdr2序列,
[0445]
以seq id no:84所示的vh cdr3序列,
[0446]
以seq id no:85所示的vl cdr1序列,
[0447]
vl cdr2序列das,以及
[0448]
以seq id no:86所示的vl cdr3序列。[118b];
[0449]
iii)以seq id no:95所示的vh cdr1序列,
[0450]
以seq id no:96所示的vh cdr2序列,
[0451]
以seq id no:97所示的vh cdr3序列,
[0452]
以seq id no:99所示的vl cdr1序列,
[0453]
vl cdr2序列ats,和
[0454]
以seq id no:100所示的vl cdr3序列。[利妥昔单抗];
[0455]
iv)以seq id no:88所示的vh cdr1序列,
[0456]
以seq id no:89所示的vh cdr2序列,
[0457]
以seq id no:90所示的vh cdr3序列,
[0458]
以seq id no:92所示的vl cdr1序列,
[0459]
vl cdr2序列das,和
[0460]
以seq id no:93所示的vl cdr3序列。[奥法木单抗];和
[0461]
v)以seq id no:102所示的vh cdr1序列,
[0462]
以seq id no:103所示的vh cdr2序列,
[0463]
以seq id no:104所示的vh cdr3序列,
[0464]
以seq id no:106所示的vl cdr1序列,
[0465]
vl cdr2序列qms,和
[0466]
以seq id no:107所示的vl cdr3序列。[奥滨尤妥珠单抗]
[0467]
在另一方面,本发明涉及本发明的药物组合物用于制备药物的用途。在本文的另一个实施方案中,用途是用于制备药物,所述药物用于治疗癌症,自身免疫性疾病或炎性疾病如变态反应,移植排斥或b细胞恶性肿瘤,如非何杰金淋巴瘤(nhl),慢性淋巴细胞性白血病(cll),滤泡性淋巴瘤(fl),套细胞淋巴瘤(mcl),浆细胞白血病(pcl),弥漫性大b细胞淋巴瘤(dlbcl)或急性成淋巴细胞性白血病(all),类风湿性关节炎,例如急性关节炎,慢性类风湿关节炎,痛风或痛风性关节炎,急性痛风性关节炎,急性免疫性关节炎,慢性炎性关节炎,变性关节炎,ii型胶原诱导的关节炎,传染性关节炎,莱姆关节炎,增生性关节炎,银屑病关节炎,斯蒂尔氏病,椎骨关节炎和青少年型类风湿关节炎,骨关节炎,慢性进行性关节炎,变形性关节炎,慢性原发性关节炎,反应性关节炎,和强直性脊柱炎,系统性红斑狼疮(sle),例如皮肤性sle或亚急性皮肤性sle,新生儿狼疮综合征(nle)和播散性红斑狼疮,多发性硬化症,炎性肠病(ibd),包括溃疡性结肠炎和克罗恩氏病,慢性阻塞性肺疾病(copd),银屑病,iga肾病,igm多发性神经病,重症肌无力,糖尿病,雷诺氏综合征和肾小球肾炎,掌足脓疱疹(ppp),糜烂性扁平苔藓,大疱性天疱疮,大疱性表皮松解,接触性皮炎和特应性皮炎,多神经根炎,包括格
‑
巴二氏综合征。
[0468]
在本发明这些用途的一个实施方案中,药物组合物用于胃肠外施用,例如皮下,肌肉内或静脉内施用。
[0469]
在本发明的这些用途的另一个实施方案中,治疗包括与一种或多种进一步治疗剂的联合疗法,所述治疗剂例如选自包括以下的组:多柔比星,顺铂,博来霉素,卡莫司汀,环磷酰胺,苯丁酸氮芥,苯达莫司汀,长春新碱,氟达拉滨,依鲁替尼和抗cd20抗体,如利妥昔单抗或奥法单抗。
[0470]
在另一方面,本发明涉及诱导表达cd37的肿瘤细胞的细胞死亡或抑制其生长和/或增殖的方法,该方法包括向有此需要的个体施用有效量的本发明的药物组合物。在某些实施方案中,该方法用于治疗具有变态反应,移植排斥或b细胞恶性疾病,例如非何杰金淋巴瘤(nhl),慢性淋巴细胞性白血病(cll),滤泡性淋巴瘤(fl),套细胞淋巴瘤(mcl),浆细胞
性白血病(pcl),弥漫性大b细胞淋巴瘤(dlbcl)或急性成淋巴细胞性白血病(all)的个体,包括向所述个体施用有效量的本发明的药物组合物。在某些实施方案中,该方法包括与所述抗体或所述双特异性抗体组合的一种或多种进一步治疗剂,诸如例如多柔比星,顺铂,博来霉素,卡莫司汀,环磷酰胺,苯丁酸氮芥,苯达莫司汀,长春新碱,氟达拉滨,依鲁替尼或抗cd20抗体,如利妥昔单抗、奥法木单抗、奥滨尤妥珠单抗、维妥珠单抗、ocaratuzumab、奥瑞珠单抗或tru
‑
015。
[0471]
在一个实施方案中,胃肠外施用,例如皮下,肌肉内或静脉内施用药物组合物。
[0472]
在本发明的一个实施方案中,进一步治疗剂选自包含以下的组:环磷酰胺、苯丁酸氮芥、苯达莫司汀、异环磷酰胺、顺铂、卡铂、奥沙利铂、卡莫司汀、泼尼松、地塞米松、氟达拉滨、喷司他丁、克拉屈滨、氟尿嘧啶、吉西他滨、阿糖胞苷、甲氨蝶呤、普拉曲沙(pralatrexate)、吉西他滨、长春新碱、紫杉醇、多西他赛、多柔比星、米托蒽醌、依托泊苷、拓扑替康、伊立替康、博来霉素、cd20特异性利妥昔单抗、奥滨尤妥珠单抗和奥法木单抗、cd52特异性阿仑珠单抗、cd30特异性本妥昔单抗(brentuximab)、jnj
‑
63709178、jnj
‑
64007957、humax
‑
il8、抗dr5、抗vegf、抗cd38、抗pd
‑
1、抗pd
‑
l1、抗ctla4、抗cd40、抗cd137、抗gitr、抗vista、对其他免疫调节性靶物特异性的抗体、brentuximab vedotin、humax
‑
tac
‑
adc、干扰素、沙利度胺、来那度胺(lenalidomide)、axicabtagene ciloleucel、硼替佐米、罗米地辛(romidepsin)、贝利司他(belinostat)、伏立诺他(vorinostat)、依鲁替尼(ibrutinib)、阿卡替尼(acalabrutinib)、艾代拉利司(idelalisib)、copanlisib、索拉非尼、舒尼替尼、依维莫司、重组人trail、birinapant和维纳妥拉(venetoclax)。
[0473]
在本发明的一个实施方案中,进一步治疗剂选自包含以下的组:依鲁替尼,利妥昔单抗,维纳妥拉,chop(环磷酰胺,多柔比星,长春新碱和泼尼松),苯达莫司汀,氟达拉滨,环磷酰胺和苯丁酸氮芥。
[0474]
在本发明的一个实施方案中,进一步治疗剂选自:依鲁替尼,利妥昔单抗和维纳妥拉。
[0475]
序列
[0476]
表1:
[0477]
[0478]
[0479]
[0480]
[0481]
[0482]
[0483]
[0484]
[0485]
[0486]
[0487]
[0488]
[0489]
[0490]
[0491]
实施例
[0492]
实施例1:在兔中产生cd37特异性抗体
[0493]
cd37的表达构建体
[0494]
产生了以下用于表达全长cd37变体的经密码子优化的构建体:人(智人)cd37(genbank登录号np_001765)(seq id no:62),食蟹猴(macaca fascicularis)cd37((mfcd37)(seq id no:63)。此外,产生了以下用于表达各种cd37 ecd变体的经密码子优化的构建体:信号肽编码序列,接着是人cd37的第二个胞外域(ec2)(aa 112
‑
241),融合到具有c端his标签的人igg的fc(ch2
‑
ch3)域(cd37ec2
‑
fchis,seq id no:64),以及mfcd37的类似构建体(cd37mfec2
‑
fchis,seq id no:65)。构建体包含适合于克隆的限制性位点和最佳kozak(gccgccacc)序列[kozak et al.(1999)gene 234:187
‑
208]。将该构建体在哺乳动物表达载体pcdna3.3(invitrogen)或等同载体中克隆。
[0495]
在cho和hek细胞中瞬时表达
[0496]
在freestyle 293
‑
f(hek293f)细胞(life technologies,usa)中使用293fectin(life technologies)基本上如制造商所述或者在freesyle cho
‑
s细胞(cho)(life technologies)中通过使用freestyle max试剂(life technologies)基本上如制造商所述瞬时转染膜蛋白。通过使用expifectamine 293试剂(life technologies)基本上如制造商所述在expi293细胞(life technologies)中瞬时表达可溶性蛋白。使用蛋白a亲和层析从细胞培养上清液中纯化fc融合蛋白(cd37mfec2
‑
fchis和cd37ec2
‑
fchis)。
[0497]
兔的免疫
[0498]
在mab discovery gmbh(neuried,germany)进行兔的免疫。用瞬时表达人或mfcd37的cd37ec2
‑
fchis和cd37mfec2
‑
fchis或hek293f细胞的混合物对兔重复进行免疫。收集这些动物的血液并分离b淋巴细胞。使用mab discovery专有工艺,将单个b细胞分选到微量滴定板的孔中并进一步繁殖。对这些单个b细胞的上清液分析与瞬时表达cd37(cho
‑
cd37)和mfcd37(cho
‑
mfcd37)的cho
‑
s细胞的特异性结合。
[0499]
重组抗体生产
[0500]
分析初步筛选结果后,选择主要命中进行测序,重组mab生产和纯化。基因合成独特的可变重链(vh)和轻链(vl)编码区,并克隆到含有人igg1恒定区编码序列(ig kappa链和igg1同种异型g1m(f),其含有e430g突变(eu编号)重链)的哺乳动物表达载体中。在此过程期间,某些抗体轻链中不利的未配对的半胱氨酸用丝氨酸取代。
[0501]
通过在tecan freedom evo平台上使用自动化程序瞬时共转染编码重链(hc)和轻链(lc)的表达载体,在hek 293细胞中产生重组嵌合抗体。在dionex ultimate 3000hplc系统上使用亲和纯化(蛋白a)从细胞上清液中纯化免疫球蛋白。
[0502]
针对对cho
‑
cd37或cho
‑
mfcd37细胞的结合重新分析所产生的含有突变e430g的嵌合(vh兔,fc人)单克隆抗体(mab)的反应性。另外,分析了对人淋巴瘤细胞系daudi的结合以
及在daudi细胞上的cdc测定法中的功能性。
[0503]
实施例2:兔嵌合抗体的人源化
[0504]
人源化抗体序列的产生
[0505]
在antitope(cambridge,uk)生成来自兔抗体兔抗cd37
‑
004,
‑
005,
‑
010和
‑
016的人源化抗体序列。使用种系人源化(cdr植入)技术生成人源化抗体序列。基于与兔和鼠抗体的vh和vκ氨基酸序列具有最接近的同源性的人种系序列,设计了人源化的v区基因。为每种兔抗体设计了4至6个vh和4或5个vκ(vl)种系人源化v区基因的系列。
[0506]
使用swiss pdb产生兔抗体v区的结构模型并进行分析,以鉴定v区框架中对抗体的结合特性可能重要的氨基酸。记录掺入一种或多种植入有变体cdr的抗体中的这些氨基酸。
[0507]
将重链和轻链v区氨基酸序列与人种系v和j区段序列的数据库进行比较,以鉴定具有最大同源性程度的重链和轻链人序列,以用作人可变域框架。表2中显示了用作人源化设计基础的种系序列。
[0508]
表2:最接近匹配的人种系v区段和j区段序列。
[0509][0510][0511]
然后,通过将cdr植入到框架上,并在必要时通过将对于抗体结合特性可能至关重要的残基(如结构建模中鉴定)回复突变成兔残基来设计一系列人源化的重链和轻链v区。然后,使用antitope专有的计算机技术itope
tm
和tced
tm
(t细胞表位数据库)(perry,l.c.a,jones,t.d.and baker,m.p.new approaches to prediction of immune responses to therapeutic proteins during preclinical development(2008).drugs in r&d 9(6):385
‑
396;bryson,c.j.,jones,t.d.and baker,m.p.prediction of immunogenicity of therapeutic proteins(2010).biodrugs 24(1):1
‑
8)选择具有潜在t细胞表位的最低发生的变体序列。最后,对设计的变体的核苷酸序列进行了密码子优化。
[0512]
对于抗体igg1
‑
016
‑
h5l2,产生了在可变域中具有点突变的变体,以替换游离的半胱氨酸:igg1
‑
016
‑
h5l2
‑
lc90s(也在具有额外的f405l和e430g突变的情况下产生)。通过基因合成(geneart)产生此突变体。
[0513]
在本文的序列表和上面的表1中显示了人源化cd37抗体的可变区序列。
[0514]
实施例3:双特异性抗体的产生
[0515]
通过在受控的还原条件下进行fab臂交换产生双特异性igg1抗体。此方法的基础是使用互补的ch3域,其在特定的测定条件下促进异二聚体的形成,如wo2011/131746中所述。将f405l和k409r(eu编号)突变引入cd37抗体中,以创建具有互补ch3域的抗体对。在某些情况下,将f405l和k409r突变与e430g突变组合。
[0516]
为了生成双特异性抗体,将两种亲本互补抗体(每种抗体终浓度为0.5mg/ml)与
75mm 2
‑
巯基乙胺
‑
hcl(2
‑
mea)在31℃在100μl te的总体积中温育5小时。使用旋转柱(microcon离心滤器,30k,millipore)根据生产商的方案除去还原剂2
‑
mea,从而停止还原反应。
[0517]
实施例4:抗体的表达构建体、瞬时表达和纯化
[0518]
为了进行抗体表达,将vh和vl序列在表达载体(pcdna3.3)中克隆,所述表达载体在vh的情况下含有相关的恒定重链(hc),在某些情况下含有f405l或k409r突变和/或e345r或e430g突变,并且在vl的情况下含有轻链(lc)区。
[0519]
将抗体表达为igg1,κ。使用293fectin(life technologies)基本上如vink et al.(vink et al.,methods,65(1),5
‑
10 2014)所述在expi293f细胞(life technologies,usa)中瞬时转染编码抗体重链和轻链两者的质粒dna混合物。接下来,通过固定化的蛋白g层析纯化抗体。
[0520]
在实施例中使用了以下抗体:
[0521]
野生型igg1抗体:
[0522]
igg1
‑
004
‑
h5l2(具有以seq id no:1和seq id no:5所示的vh和vl序列)
[0523]
igg1
‑
005
‑
h1l2(具有以seq id no:8和seq id no:12所示的vh和vl序列)
[0524]
igg1
‑
010
‑
h5l2(具有以seq id no:15和seq id no:19所示的vh和vl序列)
[0525]
igg1
‑
016
‑
h5l2(具有以seq id no:22和seq id no:26所示的vh和vl序列)
[0526]
igg1
‑
g28.1(具有以seq id no:39和seq id no:43所示的vh和vl序列
–
基于ep2241577中的seq id no 1和3)
[0527]
igg1
‑
g28.1
‑
k409r
‑
delk(也含有c端重链突变445
‑
pg
‑
446)
[0528]
igg1
‑
37.3(具有以seq id no:46和seq id no:50所示的vh和vl序列
–
基于wo2011/112978中的seq id no 55和72)
[0529]
igg1
‑
b12((具有以seq id no:32和seq id no:36所示的vh和vl序列
‑
基于gp120特异性抗体b12[barbas,cf.j mol biol.1993apr 5;230(3):812
‑
23])
[0530]
具有fc
‑
fc相互作用增强突变e430g的igg1抗体:
[0531]
igg1
‑
004
‑
h5l2
‑
e430g
[0532]
igg1
‑
005
‑
h1l2
‑
e430g
[0533]
igg1
‑
010
‑
h5l2
‑
e430g
[0534]
igg1
‑
016
‑
h5l2
‑
e430g
[0535]
igg1
‑
g28.1
‑
e430g
[0536]
igg1
‑
37.3
‑
e430g
[0537]
igg1
‑
b12
‑
e430g
[0538]
igg1
‑
005
‑
h1l2
‑
k409r
‑
e430g
[0539]
igg1
‑
010
‑
h5l2
‑
k409r
‑
e430g
[0540]
igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g
[0541]
igg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430g
[0542]
igg1
‑
004
‑
e430g
[0543]
igg1
‑
005
‑
e430g
[0544]
igg1
‑
010
‑
e430g
[0545]
igg1
‑
016
‑
e430g
[0546]
具有fc
‑
fc相互作用增强突变e430s的igg1抗体:
[0547]
igg1
‑
010
‑
h5l2
‑
k409r
‑
e430s
[0548]
igg1
‑
016
‑
h5l2
‑
f405l
‑
e430s
[0549]
具有fc
‑
fc相互作用增强突变e345k的igg1抗体:
[0550]
igg1
‑
010
‑
h5l2
‑
k409r
‑
e345k
[0551]
igg1
‑
016
‑
h5l2
‑
f405l
‑
e345k
[0552]
具有fc
‑
fc相互作用增强突变e345r的igg1抗体:
[0553]
igg1
‑
g28.1
‑
e345r
[0554]
igg1
‑
b12
‑
e345r
[0555]
igg1
‑
010
‑
h5l2
‑
k409r
‑
e345r
[0556]
igg1
‑
016
‑
h5l2
‑
f405l
‑
e345r
[0557]
双特异性抗体
[0558]
bsigg1
‑
016
‑
h5l2
‑
f405lx
‑
igg1
‑
005
‑
h1l2
‑
k409r
[0559]
bsigg1
‑
016
‑
h5l2
‑
f405lxigg1
‑
010
‑
h5l2
‑
k409r
[0560]
具有fc
‑
fc相互作用增强突变e430g的双特异性抗体:
[0561]
bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g
[0562]
bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g
[0563]
bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g
[0564]
bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g
[0565]
bsigg1
‑
b12
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g
[0566]
具有fcγr相互作用增强突变s239d
‑
i332e的igg1抗体:
[0567]
igg1
‑
g28.1
‑
s239d
‑
i332e
[0568]
实施例5:将fc
‑
fc相互作用增强突变引入cd37抗体导致增强的诱导补体依赖性细胞毒性(cdc)的从头能力
[0569]
补体依赖性细胞毒性(cdc)的测定
[0570]
在第一个实验中,将源自未治疗的cll患者的肿瘤细胞(allcells,california,usa)重悬于含有0.2%bsa(牛血清白蛋白)的rpmi中,然后以密度0.2x105个细胞/孔(40μl/孔)分配到聚苯乙烯96孔圆底板(greiner bio
‑
one cat#650101)中,并且添加40μl igg1
‑
g28.1
‑
k409r
‑
delk,igg1
‑
g28.1
‑
e345r或igg1
‑
b12
‑
e345r浓度系列(最终抗体浓度0.003
‑
10μg/ml)。igg1
‑
b12
‑
e345r(基于gp120特异性抗体b12[barbas,cf.j mol biol.1993apr 5;230(3):812
‑
23])用作阴性对照。对于igg1
‑
g28.1
‑
k409r
‑
delk,应当注意,k409r突变对结合能力或诱导cdc的能力没有影响。类似地,已引入抗体中以促进生化分析的delk(445
‑
pg
‑
446)突变不影响靶物结合或诱导cdc的能力(见下文)。
[0571]
温育(室温,摇动情况下10分钟)后,将20μl合并的正常人血清(nhs cat#m0008 sanquin,amsterdam,the netherlands)作为补体来源添加到每个孔,并将板在37℃温育45分钟。通过在冰上冷却板来终止反应。接下来,添加碘化丙啶(pi;10μl的10μg/ml溶液;sigma
‑
aldrich chemie b.v.,zwijndrecht,the netherlands),并且通过流式细胞术(facs canto ii;bd biosciences)测量死细胞(对应于pi阳性细胞)的百分比来检测裂解。
在graphpad prism v6.04软件(graphpad software,san diego,ca,usa)中使用具有对数转换浓度的非线性剂量响应拟合的最佳拟合值生成图。
[0572]
在第二个实验中,将来自另一位未治疗的cll患者的肿瘤细胞(allcells,california,usa)重悬于含有0.2%bsa的rpmi中,并以密度0.5x105个细胞/孔(30μl/孔)分配到聚苯乙烯96孔圆底板(greiner bio
‑
one cat#650101),并且添加50μl igg1
‑
g28.1,igg1
‑
g28.1
‑
e430g或igg1
‑
b12的浓度系列(最终抗体浓度0.003
‑
10μg/ml,以3.33x连续稀释)。温育(室温,15分钟)后,将20μl合并的正常人血清(nhs cat#m0008 sanquin,amsterdam,the netherlands)作为补体来源添加到每个孔,并将板在37℃温育45分钟。通过在冰上冷却板来终止反应。接下来,加入碘化丙啶(pi;20μl的10μg/ml溶液;sigma
‑
aldrich chemie b.v.,zwijndrecht,the netherlands),并通过流式细胞术(facs canto ii;bd biosciences)测量死细胞(对应于pi阳性细胞)的百分比来检测裂解。在graphpad prism v6.04软件(graphpad software,san diego,ca,usa)中使用具有对数转换浓度的非线性剂量响应拟合的最佳拟合值生成图。
[0573]
图1a和b显示没有fc
‑
fc相互作用增强e345r或e430g突变的cd37抗体g28.1(igg1
‑
g28.1或igg1
‑
g28.1
‑
k409r
‑
delk)不诱导对来自cll患者的原代肿瘤细胞的cdc,而具有fc
‑
fc相互作用增强突变e345r或e430g的g28.1(igg1
‑
g28.1
‑
e345r或igg1
‑
g28.1
‑
e430g)诱导对原代cll细胞的深度的剂量依赖性cdc。
[0574]
通过流式细胞术(qifi)定量测定细胞表面抗原
[0575]
使用人igg校准试剂盒(biocytix cat#cp010)测定cll肿瘤细胞上的cd37和膜补体调节蛋白(mcrp;cd46,cd55和cd59)表达水平。简言之,将来自cll患者的肿瘤细胞(如在上文所述的第一个实验中)重悬于含有0.2%bsa的rpmi中,然后以密度0.5x105细胞/孔(30μl/孔)分配到聚苯乙烯96孔圆底板(greiner bio
‑
one cat#650101)中,离心,并且添加50μl cd37(abcam,产品目录编号76522)或对照小鼠抗体(纯化的小鼠igg1,κ同种型对照,克隆mopc
‑
21;bd产品目录编号555746)。温育(4℃,30分钟)后,将50μl校准珠添加到单独的孔中。两次洗涤珠和细胞(150μl facs缓冲液,在洗涤步骤之间在4℃以300xg离心3分钟)后,添加如人igg校准试剂盒中提供的50μl/孔二抗(fitc缀合)稀释液。在黑暗中(4℃,45分钟)温育后,将细胞用facs缓冲液洗涤两次,并将细胞重悬于35μl facs缓冲液中,并通过流式细胞术(intellicyt iquetm筛选器)进行分析。根据制造商的指南,通过根据校准曲线计算抗体结合能力来测定抗原量。
[0576]
图2显示了cd37在来自此cll患者的原代肿瘤细胞上是高表达的。患者显示mcrp的正常表达水平。
[0577]
实施例6:cd37抗体及其变体对细胞表面表达的cd37的结合
[0578]
通过流式细胞术测定对细胞表面表达的cd37(daudi细胞,表达食蟹猴cd37的cho细胞)的结合。将细胞重悬于含有0.2%bsa的rpmi中,以100,000个细胞/孔接种在聚苯乙烯96孔圆底板(greiner bio
‑
one cat#650101)中,并在4℃以300xg离心3分钟。添加cd37或对照抗体的连续稀释液(最终抗体浓度0.003
‑
10μg/ml,以3.33x连续稀释),并将细胞在4℃温育30分钟。使用facs缓冲液(pbs/0.1%bsa/0.01%叠氮化钠)将板洗涤/离心两次。接下来,将细胞与pbs/0.1%bsa/0.01%叠氮化钠中稀释1/100的缀合有r
‑
藻红蛋白(pe)的山羊抗人igg f(ab’)2(jackson immunoresearch laboratories,inc.,west grove,pa;cat#:
109
‑
116
‑
098)在4℃一起温育30分钟。使用facs缓冲液洗涤/离心细胞两次,重悬于30μl facs缓冲液中,并使用intellicyt iquetm筛选器(westburg)通过测定平均荧光强度进行分析。在graphpad prism v6.04软件(graphpad software,sand diego,ca,usa)中使用非线性回归(具有可变斜率的s形剂量响应)分析生成结合曲线。
[0579]
对daudi细胞的结合
[0580]
图3显示了人源化的cd37抗体igg1
‑
004
‑
h5l2,igg1
‑
005
‑
h1l2,igg1
‑
010
‑
h5l2和igg1
‑
016
‑
h5l2显示对daudi细胞的剂量依赖性结合。将fc
‑
fc相互作用增强e430g突变和对于igg1
‑
005
‑
h1l2还有k409r突变引入这些抗体并不影响结合。
[0581]
图4显示将e430g突变引入igg1
‑
g28.1或igg1
‑
37.3不影响对daudi细胞的结合。
[0582]
对于抗体igg1
‑
016
‑
h5l2,产生了在可变域中具有点突变以替换轻链中的游离半胱氨酸的变体:igg1
‑
016
‑
h5l2
‑
lc90s。还产生具有额外的f405l和e430g突变的此变体,以前显示所述突变不影响靶物结合特性。图5显示了igg1
‑
016
‑
h5l2,igg1
‑
016
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g和igg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430g均显示相当的对daudi细胞的结合,因此lc90s突变不影响结合。
[0583]
对表达食蟹猴cd37的cho细胞的结合
[0584]
使用如上所述的方法通过流式细胞术测定对表达食蟹猴cd37的cho细胞的结合。图6显示了igg1
‑
004
‑
h5l2
‑
e430g,igg1
‑
005
‑
h1l2
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g和igg1
‑
016
‑
h5l2
‑
e430g显示对表达食蟹猴cd37的cho细胞的剂量依赖性结合。igg1
‑
g28.1和igg1
‑
28.1
‑
e430g不结合表达食蟹猴cd37的cho细胞。
[0585]
实施例7:鉴定不竞争对cd37的结合的cd37抗体
[0586]
(缺乏)结合竞争
–
通过流式细胞术测定
[0587]
用alexa fluor 488nhs酯(琥珀酰亚胺酯)标记cd37抗体。将1mg cd37抗体(溶于pbs)转移到1ml微量离心管小瓶(反应小瓶)中。通过添加10%体积的1m碳酸氢钠缓冲液(ph 9)提高ph。在即将使用之前,将1mg alexa fluor488nhs酯(调整至室温)溶解在100μl dmso中。通过每mg抗体添加10μl新鲜alexa染料溶液来启动标记反应。将反应小瓶加盖并通过倒置轻轻混合。在室温温育1小时后,通过向每个反应瓶添加50μl 1m tris淬灭反应。使用用硼酸盐盐水缓冲液平衡的biorad pdp10柱根据生产商的指示通过凝胶过滤从经alexa标记的抗体中除去未反应的染料。将经alexa标记的抗体在4℃避光贮存。
[0588]
通过流式细胞术测定不同cd37抗体之间的结合竞争。以浓度1x107个细胞/ml将raji细胞(atcc,ccl
‑
86)重悬于raji培养基(rpmi 1640,10%fbs,100u/ml青霉素,100μg/ml链霉素,10mm hepes和1mm丙酮酸)中。接下来,将30μl细胞悬液等分试样与30μl未标记的抗体溶液的等分试样(终浓度40μg/ml)一起转移到facs管。在轻轻摇动的情况下将混合物在37℃温育15分钟。接下来,制备经a488标记的抗体稀释液,并且温育后,将10μl的经标记的抗体(最终抗体浓度4μg/ml)转移到含有未标记的抗体和细胞的facs管。在轻轻摇动的情况下将混合物在37℃温育15分钟。温育后,通过添加4ml冰冷的pbs淬灭样品,在4℃以2000rpm离心3分钟,抽吸两次,然后重悬于125μl pbs中。通过使用bd facscalibur(bd biosciences)测定平均荧光强度来分析结合竞争。将荧光强度转换为当量可溶性荧光分子(mesf)进行定量。
[0589]
图7a和图8显示了raji细胞与igg1
‑
005
‑
h1l2
‑
e430g和igg1
‑
010
‑
h5l2
‑
e430g的预
温育阻断igg1
‑
005
‑
h1l2
‑
e430g和igg1
‑
010
‑
h5l2e430g,而非igg1
‑
37.3
‑
e430g,igg1
‑
g28.1
‑
e430g,igg1
‑
004
‑
h5l2
‑
e430g和igg1
‑
016
‑
h5l2
‑
e430g的后续结合。
[0590]
raji细胞与igg1
‑
004
‑
h5l2
‑
e430g的预温育大大减少igg1
‑
37.3
‑
e430g,igg1
‑
g28.1
‑
e430g,igg1
‑
004
‑
h5l2
‑
e430g和igg1
‑
016
‑
h5l2
‑
e430g而非igg1
‑
005
‑
h1l2
‑
e430g和igg1
‑
010
‑
h5l2
‑
e430g的后续结合。
[0591]
raji细胞与igg1
‑
016
‑
h5l2
‑
e430g的预温育阻断igg1
‑
37.3
‑
e430g,igg1
‑
g28.1
‑
e430g,igg1
‑
004
‑
h5l2
‑
e430g和igg1
‑
016
‑
h5l2
‑
e430g而非igg1
‑
005
‑
h1l2
‑
e430g和igg1
‑
010
‑
h5l2
‑
e430g的后续结合。
[0592]
细胞与igg1
‑
37.3
‑
e430g的预温育阻断所有测试抗体的后续结合。然而,如上所讨论,与igg1
‑
005
‑
h1l2
‑
e430g或igg1
‑
010
‑
h5l2
‑
e430g中的任一者的预温育不阻断igg1
‑
37.3
‑
e430g的结合。
[0593]
细胞与igg1
‑
g28.1
‑
e430g的预温育阻断igg1
‑
37.3
‑
e430g,igg1
‑
g28.1
‑
e430g,igg1
‑
004
‑
h5l2
‑
e430g和igg1
‑
016
‑
h5l2
‑
e430g而非igg1
‑
005
‑
h1l2
‑
e430g和igg1
‑
010
‑
h5l2
‑
e430g的后续结合。
[0594]
(缺乏)结合竞争
–
通过使用cdc测定法的功能筛选测定
[0595]
为了确定非交叉阻断cd37抗体在组合时是否显示增强的cdc并确认在功能上组合非交叉阻断cd37抗体的潜力,使用个别cd37抗体及其组合进行了cdc测定法。
[0596]
将重悬于含有0.2%bsa的rpmi中的raji细胞以1x105个细胞/孔(30μl/孔)的密度分配到聚苯乙烯96孔圆底板(greiner bio
‑
one cat#650101)中,并且添加50μl人源化cd37抗体,其变体,其组合或对照抗体igg1
‑
b12(最终抗体浓度10μg/ml,组合5+5μg/ml)。温育(室温,摇动的情况下15分钟)后,将20μl合并的正常人血清(nhs cat#m0008 sanquin,amsterdam,the netherlands)添加到每个孔,并将板在37℃温育45分钟。将板离心(3分钟,1200rpm),并丢弃上清液。添加碘化丙啶(pi;30μl的1.67μg/ml溶液;sigma
‑
aldrich chemie b.v.,zwijndrecht,the netherlands),并通过流式细胞术(intellicyt iquetm筛选器,westburg)测量死细胞(对应于pi阳性细胞)的百分比来检测裂解。使用graphpad prism软件(graphpad software,san diego,ca,usa)分析数据。
[0597]
图7b和c显示了igg1
‑
004
‑
h5l2加上igg1
‑
010
‑
h5l2(有或没有e430g突变)的组合和igg1
‑
005
‑
h1l2加上igg1
‑
016
‑
h5l2(有或没有e430g突变)的组合与其个别的对应物相比诱导增强的cdc。igg1
‑
004
‑
h5l2加上igg1
‑
016
‑
h5l2(有或没有e430g突变)的组合与其个别的对应物相比不诱导增强的cdc。
[0598]
图7d和e显示了igg1
‑
004
‑
h5l2加上igg1
‑
005
‑
h1l2(有或没有e430g突变)的组合和igg1
‑
010
‑
h5l2加上igg1
‑
016
‑
h5l2(有或没有e430g突变)的组合与其个别的对应物相比诱导增强的cdc。igg1
‑
005
‑
h1l2加上igg1
‑
010
‑
h5l2(有或没有e430g突变)的组合与其个别的对应物相比不诱导增强的cdc。
[0599]
图7f和g显示了igg1
‑
37.3加上igg1
‑
005
‑
h1l2(有或没有e430g突变)的组合和igg1
‑
37.3加上igg1
‑
010
‑
h5l2(有或没有e430g突变)的组合与其个别的对应物相比诱导增强的cdc。
[0600]
因此,功能组合研究确认了所描述的cd37抗体的结合竞争研究的结果,并显示非交叉阻断cd37抗体可以在功能上进行组合。
[0601]
实施例8:将fc
‑
fc相互作用增强突变引入人源化cd37抗体导致增强的诱导补体依赖性细胞毒性(cdc)的从头能力
[0602]
将重悬于含有0.2%bsa的rpmi中的raji细胞以1x105个细胞/孔(30μl/孔)的密度分配到聚苯乙烯96孔圆底板(greiner bio
‑
one cat#650101)中,并且添加50μl人源化cd37抗体和其变体或对照抗体igg1
‑
b12的浓度系列(最终抗体浓度0.003
‑
10μg/ml,以3.33x连续稀释)。温育(室温,15分钟)后,将20μl合并的正常人血清(nhs,cat#m0008 sanquin,amsterdam,the netherlands)添加到每个孔,并将板在37℃温育45分钟。将板离心(3分钟,1200rpm),并弃去上清液。添加碘化丙啶(pi;30μl的1.67μg/ml溶液;sigma
‑
aldrich chemie b.v.,zwijndrecht,the netherlands),并通过流式细胞术(intellicyt iquetm筛选器,westburg)测量死细胞(对应于pi阳性细胞)的百分比来检测裂解。在graphpad prism v6.04软件(graphpad software,san diego,ca,usa)中使用具有对数转换浓度的非线性剂量响应拟合的最佳拟合值生成图。
[0603]
图9显示了igg1
‑
004
‑
h5l2,igg1
‑
005
‑
h1l2,igg1
‑
010
‑
h5l2和igg1
‑
016
‑
h5l2在daudi细胞中不诱导cdc。引入fc
‑
fc相互作用增强e430g突变后,这些抗体(igg1
‑
004
‑
h5l2
‑
e430g,igg1
‑
005
‑
h1l2
‑
e430g,igg1
‑
010
‑
h5l2
‑
e430g和igg1
‑
016
‑
h5l2
‑
e430g)诱导daudi细胞的深度的剂量依赖性cdc。
[0604]
图10a显示了igg1
‑
g28.1和igg1
‑
37.3不诱导对daudi细胞的cdc。引入fc
‑
fc相互作用增强e430g突变后,这些抗体(igg1
‑
g28.1
‑
e430g和igg1
‑
37.3
‑
e430g)诱导daudi细胞的深度的剂量依赖性cdc。
[0605]
对于抗体igg1
‑
016
‑
h5l2,产生了在可变域中具有点突变以替换轻链中的游离半胱氨酸的变体:igg1
‑
016
‑
h5l2
‑
lc90s。此外,还产生了具有f405l突变(先前显示不影响靶物结合或cdc)和fc
‑
fc相互作用增强e430g突变的变体。图11显示了igg1
‑
016
‑
h5l2
‑
e430g,igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g和igg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430g在体外cdc测定法中均显示相当的活性,因此lc90s突变不影响诱导cdc的能力。igg1
‑
016
‑
h5l2不诱导对daudi细胞的cdc。
[0606]
在igg1
‑
010
‑
h5l2和igg1
‑
016
‑
h5l2中引入其他fc
‑
fc相互作用增强突变e345k,e345r,e430s和rrgy也导致daudi细胞的深度cdc。图10b和c显示了对于所有测试的fc
‑
fc相互作用增强突变,daudi细胞的最大裂解是相当的。
[0607]
实施例9:由于单价结合和双重表位靶向,具有fc
‑
fc相互作用增强突变的双特异性cd37抗体比具有fc
‑
fc相互作用增强突变的单特异性双价cd37抗体更有力诱导cdc。
[0608]
将f405l或k409r突变引入含有e430g突变的人源化cd37抗体中,以允许生成具有两个不竞争对cd37结合的cd37特异性fab臂的双特异性抗体(bsigg1)。如上所述测定了含有e430g突变的双特异性cd37抗体诱导cdc的能力,并且与含有e430g突变的cd37单特异性二价抗体、两个不竞争对cd37的结合的含有e430g突变的cd37单特异性二价抗体的组合(组合抗体的终浓度一起等于个别双特异性抗体的浓度)、含有e430g突变的单价cd37抗体(即,含有一个cd37特异性fab臂和一个源自igg1
‑
b12且含有e430g突变的非结合fab臂的双特异性抗体)或两个不竞争对cd37的结合的含有e430g突变的单价cd37抗体的组合的能力进行比较。
[0609]
对daudi细胞的cdc
[0610]
图12a显示了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g比igg1
‑
005
‑
h1l2
‑
e430g或igg1
‑
016
‑
h5l2
‑
e430g在诱导对daudi细胞的cdc中更有力。双特异性bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g也比igg1
‑
005
‑
h1l2
‑
k409r
‑
e430g加上igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g的组合更有力。单价cd37结合抗体bsigg1
‑
b12
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g和bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g也诱导对daudi细胞的cdc,但效率不如bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g。
[0611]
图12b显示了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g比igg1
‑
010
‑
h5l2
‑
e430g或igg1
‑
016
‑
h5l2
‑
e430g在诱导对daudi细胞的cdc中更有力。双特异性bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g也比igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g的组合更有力。单价结合抗体bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g和bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g也诱导对daudi细胞的cdc,与bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g相比,bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g不太有力并且bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g同等有力。
[0612]
还比较了含有e430g突变的双特异性cd37抗体诱导cdc的能力与没有e430g突变的双特异性cd37抗体诱导cdc的能力。图13显示了bsigg1
‑
016
‑
h5l2
‑
f405lx005
‑
h1l2
‑
k409r以及bsigg1
‑
016
‑
h5l2
‑
f405lx010
‑
h5l2
‑
k409r能够诱导对daudi细胞的cdc,但与其含有e430g的对应物bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g和bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g相比在诱导对daudi细胞的cdc上效力较低。
[0613]
对oci
‑
ly
‑
7细胞的cdc
[0614]
图12c显示了单价结合抗体bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g和bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g与其单特异性二价结合对应物igg1
‑
016
‑
h5l2
‑
e430g和igg1
‑
010
‑
h5l2
‑
e430g相比在诱导对oci
‑
ly
‑
7细胞的cdc上更有力。单价结合抗体的组合(bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g加上bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g)比二价抗体的组合(igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g)更有力,如两个独立实验中一致的较低ec50证明(图12d)。bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g也比二价抗体的组合(igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g)在对oc i
‑
ly
‑
7细胞诱导cdc上更有力,如在三个独立实验中一致的较低的ec50所证明(图12e)。
[0615]
单价结合抗体的组合(bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g加上bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g)和bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g在对oci
‑
ly
‑
7细胞诱导cdc中的效力是相当的。
[0616]
对原代cll肿瘤细胞的cdc
[0617]
如上所述测定了含有e430g突变的双特异性cd37抗体对源自cll患者的肿瘤细胞诱导cdc的能力,并与含有e430g突变的cd37抗体或含有e430g突变的cd37抗体的组合或包含e430g突变的单价cd37抗体的能力进行比较。
[0618]
图14a显示了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g在诱
导对原代cll肿瘤细胞的cdc上比igg1
‑
005
‑
h1l2
‑
k409r
‑
e430g或igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g更有力。双特异性bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g也比igg1
‑
005
‑
h1l2
‑
k409r
‑
e430g加上igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g的组合更有力。单价结合抗体bsigg1
‑
b12
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g和bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g也对原代cll肿瘤细胞诱导cdc,但在此方面效率不如bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g。
[0619]
图14b显示了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g比igg1
‑
010
‑
h5l2
‑
e430g或igg1
‑
016
‑
h5l2
‑
e430g在诱导对原代cll肿瘤细胞的cdc上更有力。双特异性bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g也比igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g的组合更有力。单价结合抗体bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g和bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g也对原代cll肿瘤细胞诱导cdc,与bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g相比,bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g不太有力并且bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g是同等有力的。
[0620]
实施例10:具有fc
‑
fc相互作用增强突变的双特异性cd37抗体对具有广泛cd37表达的多种b细胞淋巴瘤细胞系诱导cdc
[0621]
对源自多种b细胞淋巴瘤亚型的一批b细胞淋巴瘤细胞系测定了浓度10μg/ml的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g诱导cdc的能力(如上所述)。如上所述,通过定量流式细胞术测定这些细胞系的细胞表面上cd37分子的表达水平。
[0622]
表3给出测试的细胞系的概述。
[0623]
表3:b细胞淋巴瘤细胞系。
[0624][0625]
[0626]
图15显示了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g对源自各种b细胞淋巴瘤类型的一大批b细胞淋巴瘤细胞系诱导cdc。
[0627]
实施例11:具有fc
‑
fc相互作用增强突变的双特异性cd37抗体在诱导抗体依赖性细胞介导的细胞毒性(adcc)中更有力
[0628]
靶细胞标记
[0629]
通过铬释放测定法测定cd37抗体诱导adcc的能力。将daudi或raji细胞(5x106个细胞/ml)收集在1ml培养基(rpmi 1640,其补充有10%含铁的供体牛血清(dbsi;thermofischer,cat#10371029)和青霉素链霉素混合物(pen/strep),向其添加100μci 51cr(铬
‑
51;perkinelmer,cat#nez030005mc)。将细胞在37℃水浴中摇动温育1小时,洗涤细胞(在pbs中两次,1500rpm,5分钟)后,将细胞重悬于rpmi 1640/10%dbsi/pen/strep中,并用锥虫蓝排除计数,将细胞稀释至1x105个细胞/ml的密度。
[0630]
效应细胞的制备
[0631]
通过ficoll密度离心(bio whittaker;淋巴细胞分离介质,cat 17
‑
829e)根据生产商的用法说明从45ml新鲜抽取的肝素血液(血沉棕黄层)分离来自健康志愿者(sanquin,amsterdam,the netherlands)的外周血单个核细胞。将细胞重悬于rpmi 1640/10%dbsi/pen/strep中后,通过锥虫蓝排除对细胞计数,并稀释至1x107个细胞/ml的密度。
[0632]
adcc测定法程序
[0633]
将50μl经
51
cr标记的靶细胞移液到96孔圆底微量滴定板(greiner bio
‑
one;cat#650101)中,然后添加rpmi 1640/10%dbsi/pen/strep中稀释的50μl的cd37或对照抗体的浓度系列(1.5
‑
5,000ng/ml终浓度,以3倍稀释)。将细胞在室温(rt)温育15分钟,并添加50μl效应细胞,产生效应物与靶物比率100:1。将细胞在37℃和5%co2温育4小时。为了测定最大裂解,将50μl经51cr标记的daudi细胞(5.000细胞)与100μl 5%triton
‑
x100温育;为了确定自发裂解(背景裂解),将5,000个经51cr标记的daudi细胞在不含任何抗体或效应细胞的150μl培养基中温育。通过在没有抗体的情况下将5,000个daudi细胞与500,000个pbmc温育来确定不依赖于抗体的细胞裂解水平。将板离心(1200rpm,10分钟),并且将25μl上清液转移至96孔板中的100μlmicroscint
‑
40溶液(packard,cat#6013641)中。将板密封并以800rpm摇动15分钟,并使用闪烁计数器(perkinelmer)对释放的51cr进行计数。
[0634]
特异性裂解的百分比计算如下:
[0635]
%特异性裂解=(cpm样品
‑
cpm自发裂解)/(cpm最大裂解
‑
cpm自发裂解),其中cpm是每分钟计数。
[0636]
图16a显示了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx005
‑
h1l2
‑
k409r
‑
e430g比igg1
‑
005
‑
h1l2
‑
k409r
‑
e430g或igg1
‑
016
‑
h5l2
‑
f409l
‑
e430g或比igg1
‑
005
‑
h1l2
‑
k409r
‑
e430g加上igg1
‑
016
‑
h5l2
‑
f405l
‑
e430g的组合在诱导对daudi细胞的adcc中更有力。
[0637]
图16b显示了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g比igg1
‑
010
‑
h5l2
‑
e430g或igg1
‑
016
‑
h5l2
‑
e430g或igg1
‑
010
‑
h5l2
‑
e430g加上igg1
‑
016
‑
h5l2
‑
e430g的组合在诱导对daudi细胞的adcc中更有力。
[0638]
图16c显示了来自不同供体的pbmc的与图16b相似的结果,并且另外显示bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g比单价结合抗体bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g和bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g在诱导对raji细胞的adcc中更有力。
[0639]
实施例12:具有fc
‑
fc相互作用增强突变的双特异性cd37抗体在来自患有各种b细胞恶性肿瘤的患者的原代肿瘤细胞中诱导有力的离体cdc
[0640]
使用来自五种不同b细胞恶性肿瘤的患者衍生的原代肿瘤细胞分析了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405lx010
‑
h5l2
‑
k409r
‑
e430g的cdc效力:慢性淋巴细胞性白血病(cll),滤泡性淋巴瘤(fl),弥漫性大b细胞淋巴瘤(dlbcl),套细胞淋巴瘤(mcl)和非何杰金淋巴瘤(未进一步规定)。所有患者样品均在书面知情同意书后获得,并按照赫尔辛基声明,使用vumc医学伦理委员会批准的方案进行贮存。通过密度梯度离心(ficoll
‑
paque plus,ge healthcare)从患者的骨髓穿刺物或外周血样品中分离患者的骨髓单个核细胞(bmnc)或外周血单个核细胞(pbmc)。细胞可以直接使用或者贮存在液氮中直至进一步使用。
[0641]
将患者淋巴结组织切成小碎片,并收集在含有1%青霉素
‑
链霉素,0.2%肝素和5%血小板裂解物的α
‑
mem培养基(thermofischer scientific,waltham,ma)中,并于37℃放置过夜。温育后,收集上清液(包括肿瘤细胞的非基质细胞区室),并使用70μm easy strainer(greiner bio
‑
one)过滤细胞。对细胞计数,重悬于包含25%热灭活的fbs和10%dmso的rpmi 1640培养基中,并在液氮中冷冻直至进一步使用。
[0642]
使用qifikit(dako,产品目录编号k007811)测定分离的患者细胞上的cd37和膜补体调节蛋白(mcrp;cd46,cd55和cd59)表达水平。将细胞与纯化的抗体cd37(bd,产品目录编号555456),cd46(biolegend,产品目录编号352404),cd55(biolegend,产品目录编号311302),cd59(biolegend,产品目录编号304702),和b12(genmab)在4℃温育30分钟。此后,使用qifikit制造商提供的方法。在qifi试剂盒程序的最后一步后,将细胞与淋巴瘤细胞特异性标志物一起温育,以实现肿瘤细胞鉴定。图17显示了每种适应症的表达水平。
[0643]
用10μg/ml或100μg/ml bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405lx010
‑
h5l2
‑
k409r
‑
e430g调理患者衍生的肿瘤细胞,并在存在20%合并nhs的情况下评估cdc诱导。使用以下细胞标志物来鉴定不同的细胞群体:cd45
‑
ko(beckman coulter b36294),cd19
‑
pc7(beckman coulter,产品目录编号im3628),cd3
‑
v450(bd,产品目录编号560365),cd5
‑
apc(bd,产品目录编号345783),cd5
‑
pe(dako,产品目录编号r084201),cd10
‑
apc
‑
h7(bd,产品目录编号655404),cd10
‑
pe(dako,产品目录编号r084201),cd23
‑
fitc(biolegend,产品目录编号338505),lambda
‑
apc
‑
h7(bd,产品目录编号656648),kappa
‑
pe(dako,产品目录编号r043601)和lambda
‑
fitc(emelca bioscience cyt
‑
lambf)。在cd45+细胞群体中,根据适应症通过不同标志物限定恶性b细胞:cd3
‑
/cd19+/cd5+(cll),cd3
‑
/cd19+/cd10+(fl,dlbcl),cd3
‑
/cd19+/cd5+/cd23
‑
(mcl)。在无法根据这些标志物鉴定恶性b细胞的情况下,可以使用kappa/lambda染色根据克隆性鉴定恶性细胞。在几个样品中,基于克隆性也无法鉴定出恶性b细胞;在这些情况下,评估了总的b细胞群体,不区分正常b细胞和恶性b细胞。以通过lsrfortessa流式细胞仪(bd biosciences,san jose,ca)测定的7
‑
氨基放线菌素d(7
‑
aad;bd,产品目录编号555816)阳性恶性b细胞的分数(%)计算杀伤。
[0644]
图18显示了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405lx010
‑
h5l2
‑
k409r
‑
e430g在源自cll,fl,mcl,dlbcl或b
‑
nhl(未进一步规定)的患者的肿瘤细胞中诱导cdc中高度有力(超过50%裂解)。在来自一名患有复发性/难治性fl的患者的细胞中,bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405lx010
‑
h5l2
‑
k409r
‑
e430g的cdc诱导能力较弱。
[0645]
实施例13:具有fc
‑
fc相互作用增强突变的双特异性cd37抗体对全血中的人或食蟹猴b细胞的结合,以及全血中的b细胞中的细胞毒性的诱导
[0646]
对人或食蟹猴b细胞的结合
[0647]
在全血结合测定法中测定对人或食蟹猴b细胞的结合。来自健康志愿者的经肝素处理的人血液源自umc utrecht(utrecht,the netherlands),来自食蟹猴的经水蛭素处理的血液源自covance(m
ü
nster,germany)。将血液等分取样到96孔圆底板的孔(greiner bio
‑
one,产品目录编号65010;35μl/孔)。通过添加100μl rbc裂解缓冲液(10mm khco3[sigma p9144],0.1mm edta[fluka 03620]和0.15mm nh4cl[sigma a5666])裂解红细胞(rbc),并在冰上温育直至rbc裂解完成。以300xg离心3分钟后,将细胞在4℃与经alexa
‑
488标记的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g或经alexa
‑
488标记的对照igg1(igg1
‑
b12)和直接标记的抗体的连续稀释(0.014
‑
30μg/ml终浓度,以3x连续稀释)温育30分钟以鉴定b细胞(在抗体的混合物中以进一步鉴定血液细胞亚组):
[0648]
对于人血b细胞,使用了以下抗体
[0649]
靶蛋白克隆标记靶细胞公司cat.no.cd19hib19bv711b细胞biolegend302245
[0650]
对于食蟹猴血b细胞,使用了以下抗体
[0651][0652]
将细胞沉淀并在150μl facs缓冲液中洗涤两次,并且重悬于150μl to
‑
pro
‑
3(终浓度0.2μm;molecular probes,产品目录编号t3605)。使用lsr fortessa流式细胞仪通过流式细胞术测量样品。结合表示为活的to
‑
pro
‑3‑
/cd14
‑
/cd19
+
b细胞(人)或活的to
‑
pro
‑3‑
/cd14
‑
/cd19
+
/cd20
+
b细胞(食蟹猴)的a488荧光强度的几何平均值。使用graphpad prism中非线性剂量响应拟合的最佳拟合值分析经对数转换的数据。
[0653]
图19显示了对于一个代表性供体/动物,bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g对(a)人和(b)食蟹猴血液中b细胞的浓度依赖性结合。对人和食蟹猴b细胞的结合的平均ec
50
值在相同范围内(分别为[基于对来自6名人供体的血液中b细胞的结合0.85μg/ml
±
0.284]和[基于对来自4只动物的血液中的b细胞的结合0.63μg/ml
±
0.228]),指示了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g显示相当的对人和食蟹猴cd37的结合。
[0654]
对人或食蟹猴b细胞的细胞毒性
[0655]
在全血细胞毒性测定法中测定了对人或食蟹猴b细胞的细胞毒性。来自健康志愿者的水蛭素处理过的人血来自umc utrecht(utrecht,the netherl ands),来自食蟹猴的经水蛭素处理的血液源自covance(m
ü
nster,germany)。将血液等分取样至96孔圆底板的孔,35μl/孔。
[0656]
添加了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g或igg1
‑
b12的连续稀释液(0.0005
‑
10μg/ml最终抗体浓度,以3x连续稀释;最终体积100μl/孔)。在
使用人全血的细胞毒性测定法中,将单克隆fcγr相互作用增强的cd37特异性抗体igg1
‑
g28.1
‑
s239d
‑
i332e包括在内作为参考。将样品在37℃温育4小时。此后,如上所述裂解红细胞,并如上所述对样品染色以鉴定b细胞。将细胞沉淀并在150μl facs缓冲液中洗涤两次,然后重悬于150μl to
‑
pro
‑
3(终浓度0.2μm;molecular probes,产品目录编号t3605)。使用lsrfortessa流式细胞仪通过流式细胞术测量样品。排除双联体后,测定活的to
‑
pro
‑3‑
/cd14
‑
/cd19
+
b细胞(人)或活的to
‑
pro
‑3‑
/cd14
‑
/cd19
+
/cd20
+
b细胞(食蟹猴)百分比。b细胞消减百分比计算如下:b细胞消减%=100*[(无抗体对照的b细胞%
‑
b细胞样品%)/(无抗体对照的b细胞%)]。使用graphpad prism中非线性剂量响应拟合的最佳拟合值分析经对数转换的数据。
[0657]
图20显示了对于一个代表性供体/动物,bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g对(a)人和(b)食蟹猴血液中b细胞的浓度依赖性细胞毒性。
[0658]
基于ec
50
,bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g在人和食蟹猴b细胞中诱导细胞毒性的能力相当:对人b细胞(来自6个供体的血液中)的细胞毒性的平均ec
50
为0.077μg/ml
±
0.039;对食蟹猴b细胞(来自4只动物的血液中)的细胞毒性的平均ec
50
为0.043μg/ml
±
0.019。
[0659]
图20a还显示了fcγr相互作用增强的单克隆cd37抗体igg1
‑
g28.1
‑
s239d
‑
i332e对代表性响应供体的人b细胞的细胞毒性,其显示比bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g低的细胞毒性。在来自3个响应供体的b细胞中,测量到igg1
‑
g28.1
‑
s239d
‑
i332e的50%的最大b细胞消减,而在其他3个供体中,未测量到此抗体对b细胞的细胞毒性。bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g在6/6供体的93
‑
99%b细胞中诱导细胞毒性。igg1
‑
g28.1
‑
s239d
‑
i332e对daudi细胞上表达的cd37的结合与bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g的结合相当(数据未显示)。
[0660]
实施例14:具有fc
‑
fc相互作用增强突变的双特异性cd37抗体与cd20特异性抗体的组合的有力cdc活性
[0661]
在从conversantbio(huntsville,alabama,usa)获得的患者衍生的cll肿瘤细胞上测试bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g和抗cd20抗体(igg1
‑
cd20
‑
ofa;奥法木单抗)的组合诱导cdc的能力。将患者衍生的pbmc重悬浮在含0.2%bsa(牛血清白蛋白)的rpmi中,并以0.1x106个细胞/孔(30μl/孔)的密度分配到聚苯乙烯96孔圆底板(greiner bio
‑
on e cat#650101)中,并以2倍稀释添加50μl bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g(0.0625
‑
0.05μg/ml)和igg1
‑
cd20
‑
ofa(1
‑
8μg/ml)的浓度系列。通过将平均而言分别达到相同效果的两种浓度混合以基于每种抗体的相对效力(ec50的差异)的抗体浓度来组合bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g和igg1
‑
cd20
‑
ofa。igg1
‑
b12用作阴性对照。
[0662]
温育(室温,摇动15分钟)后,将20μl合并的正常人血清(nhs cat#m0008sanquin,amsterdam,the netherlands)作为补体来源添加到每个孔,并将板在37℃温育45分钟。通过在冰上冷却板来终止反应。以300xg离心3分钟后,将细胞用150μl facs缓冲液洗涤两次,并在4℃与经r
‑
藻红蛋白(pe)标记的小鼠抗人igg1
‑
cd19抗体(克隆j3
‑
119,beckman coulter,产品目录编号a07769,从储液以1:50稀释)温育30分钟以测定肿瘤b细胞和to
‑
pro
‑
3(终浓度为0.2μm;molecular probes,产品目录编号t3605)进行死细胞鉴定。将细胞沉淀并在150μl facs缓冲液中洗涤两次,并使用lsrfortessa流式细胞仪通过流式细胞术测量。活细胞的百分比计算如下:活细胞%=100*(to
‑
pro
‑
3阴性事件数目)/(总事件数目)。
[0663]
图21a
‑
d显示了bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g和奥法木单抗两者诱导源自2名cll患者的肿瘤细胞中的cdc,cd c活性随剂量水平的增加而增加。将bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g与奥法木单抗组合对于测试的两名cll患者在所有测试浓度下导致增强的cdc活性,尽管这些效果在较高的抗体浓度不太明显,其中单一药剂几乎诱导完全的细胞杀伤(图21a和b)。这些结果指示对bs igg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g添加奥法木单抗可以改善从cll患者获得的恶性b细胞中cdc介导的肿瘤细胞杀伤。
[0664]
实施例15:在b细胞恶性肿瘤的异种移植模型中具有fc
‑
fc相互作用增强突变的双特异性cd37抗体的抗肿瘤活性
[0665]
皮下jvm
‑
3人慢性b细胞白血病异种移植模型中的抗肿瘤活性
[0666]
将jvm
‑
3细胞(1x107)接种到cb17.scid小鼠的右体侧中,并且当肿瘤达到约158mm3的平均体积时开始抗体处理(三次每周剂量的0.1、0.3、1、3或10mg/kg,静脉内注射;igg1
‑
b12用作阴性对照,以10mg/kg给药)。每周两次使用测径器在两个维度上测量肿瘤体积,并使用以下公式以mm3表示体积:v=(l x w x w)/2,其中v是肿瘤体积,l是肿瘤长度(最长的肿瘤维度),并且w是肿瘤宽度(垂直于l的最长肿瘤维度)。
[0667]
图22a显示了随时间的每个剂量组的肿瘤体积,图22b显示了当所有组仍完整时第25天的每个剂量组的每只小鼠的肿瘤体积。三次每周剂量的1,3或10mg/kg的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g显著降低jvm
‑
3细胞肿瘤生长,而以0.1或0.3mg/kg给药不影响肿瘤生长(mann whitney检验,p<0.01)。
[0668]
静脉内daudi
‑
luc伯基特氏淋巴瘤异种移植物模型中的抗肿瘤活性
[0669]
在第0天,给scid小鼠(c.b
‑
hsd
‑
prkdcscid;harlan)静脉内注射daudi
‑
luc细胞(经萤光素酶转染的daudi细胞,2.5x106个细胞/小鼠)。在第14、21和28天,给小鼠腹膜内注射0.1、0.3、1、3或10mg/kg的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g。igg1
‑
b12用作阴性对照抗体,以10mg/kg给药。每周(从第2天开始)通过生物发光成像(bli)评估肿瘤生长。给小鼠腹膜内注射100μl萤火虫d
‑
萤光素(30mg/ml;caliper lifesciences,产品目录编号119222),并且在异氟烷麻醉下使用biospace生物发光成像系统(perkinelmer;从背部部位对小鼠成像)测量生物发光(以p/s/cm2/sr[每平方弧度每cm2每秒的光子]计的辐射率)。
[0670]
图23a显示了随时间的每个剂量组的萤光素酶活性(生物发光,作为肿瘤体积的测量),图23b显示了当所有组仍完整时第36天的每个剂量组的每只小鼠的萤光素酶活性。每周三剂0.1、0.3、1、3或10mg/kg的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g显著降低daudi
‑
luc细胞的体内生长(单向anova,未校正的费舍尔lsd)。
[0671]
实施例16:在scid小鼠中评估具有fc
‑
fc相互作用增强突变的双特异性cd37抗体的血浆清除
[0672]
给11
‑
12周龄的雌性scid小鼠(c.b
‑
hsd
‑
prkdcscid;harlan)(每组3只
小鼠)静脉内(i.v.)注射单剂100μg(5mg/kg)或500μg(25mg/kg)bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g或igg1
‑
b12。建立实验以研究在没有靶物介导的清除的情况下的抗体清除,因为bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g和igg1
‑
b12均未显示与小鼠的交叉反应性。
[0673]
在抗体施用后10分钟,4小时,24小时,2天,7或8天,14天和21天从隐静脉收集50
‑
100μl血液样品。将血液收集到含有肝素的小瓶中,并以10,000g离心5分钟。对于以5mg/kg给药的小鼠以1:50(在980μl pbsa(补充有0.2%牛血清白蛋白(bsa)的pbs)中20μl样品)以及对于以25mg/kg给药的小鼠以1:20(在380μl pbsa中20μl样品)稀释血浆样品,并于
‑
20℃贮存直至测定单抗浓度。
[0674]
使用夹心elisa测定人igg浓度。以2μg/ml的浓度在100μl中于4℃过夜包被到96孔microlon elisa板(greiner,germany)的小鼠单抗抗人igg
‑
kappa克隆mh16(clb sanquin,the netherlands;产品目录编号m1268)用作捕获抗体。在室温(rt)用pbsa封闭板1小时后,添加样品,在pbsa中连续稀释,并在平板摇动器上于室温温育1小时。将板用300μl pbst(补充有0.05%tween 20的pbs)洗涤3次,然后在室温与山羊抗人igg免疫球蛋白(jackson,west grace,pa;产品目录编号109
‑
035
‑
098;补充有0.2%bsa的pbst中1:10.000)一起温育1小时。将板再次用300μl pbst洗涤3次,然后与2,2
’‑
连氮基
‑
双(3
‑
乙基苯并噻唑啉
‑6‑
磺酸)(abts;roche,mannheim,germany)一起避光温育。通过添加100μl 2%草酸终止反应。在微板阅读器(biotek,winooski,vt)中在405nm处测量吸光度。通过使用注射的材料作为参考曲线来计算人igg浓度。作为板对照,包括纯化的人igg1(the binding site,产品目录编号bp078)。绘制人igg浓度(以μg/ml计)(图24a和c),并使用graphpad prism 6.0计算曲线下面积(auc)。用公式d*1.000/auc测定直到血液取样的最后一天(第21天)的igg清除,其中d是注射剂量(1mg/kg)(图24b和d)。
[0675]
bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g和igg1
‑
b12的血浆清除率之间没有实质性差异,证明bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g显示在没有靶物结合的情况下与野生型人igg1相当的药动学概况。
[0676]
实施例17:使用丙氨酸扫描测定cd37氨基酸残基对cd37抗体结合的贡献
[0677]
文库设计
[0678]
合成了cd37单残基丙氨酸文库(geneart),其中除了已经含有丙氨酸或半胱氨酸的位置外,将人cd37(uniprot p11049)胞外域中的所有氨基酸(aa)残基个别突变为丙氨酸。未将半胱氨酸突变以使抗原的结构破坏的机会最小化。将文库在含有cmv/tk
‑
polya表达盒,amp抗性基因和pbr322复制起点的pmac表达载体中克隆。
[0679]
文库产生和筛选
[0680]
在freestyle hek293细胞中根据制造商的用法说明(thermo scientific)个别表达野生型cd37和丙氨酸突变体。转染后一天,收获细胞。将约100,000个细胞与facs缓冲液(pbs+0.1%(w/v)牛血清白蛋白(bsa)+0.02%(w/v)叠氮化钠)中20μl 3μg/ml浓度的缀合有alexa488的bsigg1
‑
b12
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g(单价结合010)或缀合有alexa488的bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gxb12
‑
k409r
‑
e430g(单价结合016)温育。将细胞在室温温育1小时。随后,通过添加150μl facs缓冲液并且在离心后除去上清液来洗涤细胞两次。将细胞重悬于20μl新鲜facs缓冲液中,并在4℃贮存,直到使用ique筛选器
(intellicyt)通过流式细胞术进行分析。整个实验进行两次。
[0681]
数据分析
[0682]
对于每个样品,将每个细胞的平均抗体结合测定为未门控细胞群体的荧光强度的几何平均值(gmfi)。gmfi受抗体对cd37突变体的亲和力和每个细胞cd37突变体表达水平的影响。由于特定的丙氨酸突变可以影响突变体cd37的表面表达水平,并且通常校正每个cd37突变体的表达差异,因此使用以下方程式相对于非竞争性cd37特异性对照抗体的结合强度将数据标准化(在此实施例中抗体单价结合010和单价结合016是非竞争性抗体,并且使用一种抗体作为另一种抗体的对照):
[0683][0684]
其中“aa位置”指cd37或野生型(wt)cd37中的特定丙氨酸突变体位置。
[0685]
为了表示抗体结合的丧失或获得,根据以下计算测定标准得分:
[0686][0687]
其中,μ和σ是所有突变体的标准化gmfi的平均值和标准差(sd)。
[0688]
在大多数情况下,结合获得将由参考抗体对特定ala突变体的结合的丧失引起。使用这些计算,用丙氨酸替换氨基酸后没有特定抗体结合的丧失或获得的氨基酸位置将给出“0”的z得分,结合获得将导致“z得分>0”而结合丧失将导致“z得分<0”。为了校正样品变化,仅z得分低于
–
1.5的cd37氨基酸残基认为是“结合丧失突变体”。在针对特定cd37突变体的对照抗体的gmfi低于平均gmfi
对照抗体
的平均gmfi
‑
2.5xsd的情况下,从分析中排除数据(对于那些cd37突变体,假定表达水平不足)。
[0689]
图25显示了cd37抗体对位置42至131(根据seq id no 94)处具有ala突变的cd37变体的“z得分(倍数变化)”。结果指示:
[0690]
·
抗体010的结合至少依赖于人cd37的氨基酸y182,d189,t191,i192,d194,k195,v196,i197和p199,
[0691]
·
抗体016的结合至少依赖于人cd37的氨基酸e124,f162,q163,v164,l165和h175。
[0692]
汇总
[0693]
总之,由具有fc
‑
fc相互作用增强突变的不竞争靶物结合的两个cd37特异性抗体构成的双特异性抗体在cd37阳性肿瘤细胞中显示了cdc效力和adcc效力的最有利组合。对于这两种效应器机制,与两个含有fc
‑
fc相互作用增强突变的非竞争性cd37抗体的组合或与单一具有fc
‑
fc相互作用增强突变的cd37抗体相比,具有fc
‑
fc相互作用增强突变的双特异性抗体显示优异的效力。
[0694]
实施例18:在raji细胞上体外评估新型六聚化增强的cd37抗体与临床建立的cd20抗体产品的混合物的cdc活性。
[0695]
使用伯基特氏淋巴瘤raji细胞在体外测试具有fc
‑
fc相互作用增强突变的cd37抗体igg1
‑
37.3
‑
e430g,igg1
‑
g28.1
‑
e430g,igg1
‑
004
‑
e430g,igg1
‑
005
‑
e430g,igg1
‑
010
‑
e430g和igg1
‑
016
‑
e430g(后4种是嵌合兔/人的),加上临床上建立的cd20靶向性单克隆抗体产品mabthera(利妥昔单抗;roche,h0124b08)、arzerra(奥法木单抗;novartis;
c656294)和gazyva(奥滨尤妥珠单抗,ga101;roche,d287
‑
41a gacd20)的混合物的cdc活性。将raji细胞(atcc,产品目录编号ccl
‑
86)在补充有10%热灭活的fbs,1u/ml青霉素,1μg/ml链霉素和4mm l
‑
谷氨酰胺的rpmi 1640中培养。在室温将0.1x106个raji细胞在每孔的总体积80μl rpmi/0.2%bsa中与抗体一起温育15分钟。接下来,将nhs添加至预温育的细胞至终体积100μl(最终抗体浓度10μg/ml;20%nhs),并在37℃温育45分钟。对于所有测试的总抗体浓度,测试了混合物中两种抗体的不同比率(1:0
–
3:1
–
1:1
–
1:3
–
0:1)。对板进行离心,并且将细胞重悬于30μl pi(2μg/ml)中。以通过在ique筛选器(intellicyt)上进行流式细胞术测定的pi阳性细胞分数(%)来计算杀伤。使用graphpad prism软件分析数据并作图。
[0696]
在raji细胞上与相同浓度的单一抗体相比具有fc
‑
fc相互作用增强突变的测试cd37抗体和临床建立的cd20抗体产品的混合物显示增强的剂量依赖性cdc活性(图8)。在混合物中两种抗体的不同测试比率(1:3、1:1或3:1),cdc活性几乎没有差异。这些数据指示具有fc
‑
fc相互作用增强突变的六聚化增强cd37抗体加上临床建立的cd20抗体产品例如mabthera,arzerra(i型cd20抗体)或gazyva(ii型cd20抗体)的混合物可以改善b细胞恶性肿瘤患者的治疗潜力,所述b细胞恶性肿瘤通常对单独的标准cd20靶向疗法变得难治。
[0697]
实施例19:抗体配制剂研究。
[0698]
将抗体igg1
‑
010
‑
h5l2
‑
k409r
‑
e430g(e1)和igg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430g(d1)各自配制成具有以下组成的三种不同配制剂:
[0699]
表4
[0700][0701]
根据usp<791>ph进行ph值的测定。在每种配制剂中,将1.95ml转移到nalgene冷冻管中,并进行两个由以下组成的冷冻
‑
融化循环:在
‑
65℃冷冻12h,然后在25℃融化12h。在时间0和两个冷冻/融化循环之后测试样品。
[0702]
可见颗粒
[0703]
针对黑色背景和针对白色背景以2000和3750勒克斯之间的最小强度照明进行可见颗粒计数。
[0704]
在时间0和冷冻
‑
融化循环之后,两种抗体中每种的所有三种配制剂实际上都不含可见颗粒(0
‑
3个颗粒/ml)。因此,样品在可见颗粒形成方面是稳定的。
[0705]
浊度
[0706]
通过使用浊度计针对药典参考标准溶液进行测量来进行浊度测试。将样品溶液的结果(以比浊法浊度单位(ntu)计)与最接近的参考溶液的结果进行比较。若样品结果在各自参考溶液的ntu值的[
‑
10%至+10%]之内,则结果报告为与参考溶液相等。
[0707]
图27中显示了两个冷冻
‑
融化循环后确定的浊度值。在参考悬浮液ii和iii内,所有浊度值都是低的。f1显示最低的浊度,f1中抗体igg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430g(d1)的浊度略高于抗体igg1
‑
010
‑
h5l2
‑
k409r
‑
e430g(e1)的浊度。浊度随nacl的增加而略有增加。
[0708]
亚可见颗粒
[0709]
使用hiac仪通过光遮蔽原理检测两个冷冻
‑
融化循环后的亚可见颗粒。计数超过2、5、10或25微米的颗粒。
[0710]
图28显示两种抗体的所有三种配制剂仅含有很少的亚可见颗粒,特别是很少的超过10或25微米的颗粒。在配制剂f2中,亚可见颗粒的数量最小。
[0711]
尺寸排阻层析(sec)
[0712]
使用尺寸排阻uplc(se
‑
uplc)来确定样品中存在的单体,高分子量种类(hmws/聚集体)和低分子量种类(lmws/片段)的量。在连接到(u)hplc系统的acquity uplc protein beh sec或等同的柱上进行方法。通过在280nm处的吸光度检测洗脱峰。主峰,hmws和lmws以相对峰面积(%)的百分比表示。
[0713]
数据在下表中给出(loq表示低于定量限)
[0714]
表5
[0715]
样品总hmws(%)主峰(%)总lmwsd1 f1 t00.499.6低于loqd1 f2 t00.499.6低于loqd1 f3 t00.599.5低于loqd1 f1冷冻
‑
融化0.599.5低于loqd1 f2冷冻
‑
融化0.499.6低于loqd1 f3冷冻
‑
融化0.499.6低于loq
[0716]
表6
[0717]
样品总hmws(%)主峰(%)总lmwse1 f1 t01.498.6低于loqe1 f2 t01.598.5低于loqe1 f3 t01.698.4低于loqe1 f1冷冻
‑
融化1.498.6低于loqe1 f2冷冻
‑
融化1.698.4低于loqe1 f3冷冻
‑
融化1.598.5低于loq
[0718]
数据显示,两种抗体的总hmws和lmws均较低,并且两次冷冻
‑
融化循环后未发现hmws和lmws的显著增加。三种配制剂之间没有重大差异。
[0719]
动态光散射(dls)
[0720]
通过动态光散射(dls)使用dynapro读板仪ii(带有软件dynamics;wyatt)在384孔板中进行扩散相互作用参数kd(ml/g)的评估。制备不同缓冲剂中蛋白质的连续稀释液。将d
m
(m2/s;来自dls的互扩散系数)对蛋白质浓度c(g/ml)作图。当将来自线性拟合的计算斜率除以截距时得到kd,所述截距是d0(m2/s;无限溶质浓度下的扩散系数)。
[0721]
d
m
=d0(1+kd*c)
[0722]
下表中显示了样品(尚未经历两个冷冻
‑
融化循环)的kd值。
[0723]
表7
[0724]
配制剂kd d1(ml/g)kd e1(ml/g)
f1
‑
6.15
‑
5.52f2
‑
8.95
‑
6.93f3
‑
9.05
‑
8.46
[0725]
数据仅显示三种配制剂中抗体的略有吸引力的行为。
[0726]
总体上,这两种抗体的三种配制剂表现出适合于药用用途的特征。
[0727]
实施例20:在应激条件下评估ph、赋形剂和表面活性剂。
[0728]
评估具有不同ph和离子强度的6种配制剂(f4
‑
f9)的ph和赋形剂筛选。
[0729]
化学品和赋形剂
[0730]
表8
[0731][0732]
表9
[0733][0734]
下表列出了评估的配制剂。
[0735]
表10
[0736][0737]
·
蛋白质是双特异性cd37抗体(bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g)。
[0738]
方法
[0739]
对如表20.1中规定的双特异性cd37抗体进行缓冲剂交换和浓缩以制备表20.3中
所列的配制剂。通过如下制备配制剂:1)交换缓冲剂以达到目标缓冲剂浓度和ph,然后2)浓缩至目标浓度以上。在加工蛋白质后确定蛋白质浓度,ph值和密度,并且用于通过使用标准稀释程序进行每种配制剂的所需要的计算。测定并确认最终混合溶液的蛋白质浓度和ph。使用0.22μm聚偏二氟乙烯(pvdf)膜滤器过滤所有配制剂溶液。
[0740]
适当地准备主要包装材料,并按照无菌技术,以目标填充体积2.4ml手动将每种配制剂填充到6r/20mm i型玻璃小瓶中,用20mm溴丁基橡胶塞(注射塞)塞住并用20mm铝制翻转式(flip
‑
off)密封件密封。标记所有配制剂的样品并在每种条件下保存,以进行稳定性研究。
[0741]
过滤后的配制剂
[0742]
测定过滤后的液体配制剂(f4至f9)的混合溶液的ph,蛋白质浓度和重量摩尔渗透压浓度。还包括在短期稳定性研究期间的初始时间点通过uv分光光度计(a280)确定的蛋白质浓度。
[0743]
·
过滤后,混合溶液中无可见颗粒。
[0744]
短期稳定性研究
[0745]
储存两周后的分析结果:
[0746]
在长期条件(2
‑
8℃)下,在加速条件(25℃)下观察到所有配制剂的良好稳定性,在储存长达2周后观察到变性,并且在应激条件(40℃)下更显著。根据hp
‑
sec,最显著影响的质量属性是电荷异质性和单体含量。在应激条件下储存2周后,在caliper ce
‑
sds结果中也观察到了轻微的削峰(clipping)。
[0747]
所有配制剂在应激条件下均显示聚集体含量的增加。对于f4,观察到异常高的聚集体水平。应激储存后,对所有配制剂也观察到片段的微小增加。
[0748]
在应激条件下观察到电荷变体的变化。尽管与配制剂f4的t0样品(ph 5.0)相比仍观察到10%的增加,但低ph似乎降低碱性变体增加的速率。在f7(ph6.0)中观察到最高的碱性变体含量。
[0749]
储存四周后的分析结果:
[0750]
可以确认在储存两周的样品中观察到的趋势。对于电荷变体,特别地,碱性变体在ph 5.0的情况下显示明显的ph依赖性,即,f4显示出最少的碱性变体形成。然而,在其他质量属性如聚集和削峰中,f4配制剂不太有利。具有ph 6.0及以上的配制剂显示出高的碱性变体形成。
[0751]
具有ph 5.5的配制剂显示出可接受的质量属性,并且在配制剂中,f5显示出最低的碱性变体形成。
[0752]
bsigg1
‑
016
‑
h5l2
‑
lc90s
‑
f405l
‑
e430gx010
‑
h5l2
‑
k409r
‑
e430g具有琥珀酰亚胺的序列倾向。在这项研究中做出了努力以开发可保护双特异性cd37抗体在长期储存条件下免于降解的配制剂。来自8个研究的结果能够显示出琥珀酰亚胺形成的ph依赖性(反映为稳定性样品中碱性电荷变体的增加),其中ph 5.0配制剂(f4)显示随储存时间的碱性变体含量的最小增加。然而,由于就如聚集和断裂等属性而言的较差的稳定性行为,认为此配制剂是不合适的。此外,结果显示了具有较高ph,例如ph 5.5的配制剂在所有测试的质量属性上提供了更好的稳定性。
[0753]
实施例20的稳定性研究结果示于下表11至18中。
[0754]
表11
[0755][0756]
表12
[0757][0758]
表13
[0759][0760]
ice:图像毛细管电泳
[0761]
表14
[0762][0763]
ice:图像毛细管电泳
[0764]
表15
[0765][0766]
表16
[0767][0768]
表17
[0769][0770]
表18
[0771]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1