一种抗敏组合物及其制备方法和应用与流程
本发明属于化妆品领域,具体涉及一种抗敏组合物及其制备方法和应用。
背景技术:
皮肤敏感,是指对多种因素易感而诱发的主观感觉症状的皮肤状态,即皮肤反应性高、耐受性差,甚至易过敏。敏感皮肤主要发生于面部,还有手脚、头皮等其他部位。就日常状态而言,敏感皮肤并无客观皮损或皮肤疾病证据,主要特点是更为干燥、容易紧绷和发红;受到轻微刺激,即可产生瘙痒、脱屑甚至烧灼和刺痛等感觉,严重者可产生不良情绪或精神症状。
敏感皮肤的成因并不是特定物质的接触和作用,而是皮肤自身结构和感受神经的既定状态。主要包括以下因素:(1)皮肤屏障功能受损,角质层薄弱的皮肤渗透能力强,刺激物更容易进入而引起皮肤的炎性反应;(2)神经因素;(3)炎症反应。气候变化、空气污染及化妆品种类与成分复杂化,提高了敏感皮肤出现的可能性。但是,由于敏感皮肤成因和机制的复杂性,目前仍无特效治疗的方法。
因此,希望提供有一种抗敏组合物,能够有效改善皮肤过敏。
技术实现要素:
本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明提出一种抗敏组合物,能够有效改善皮肤过敏。
一种抗敏组合物,主要由倒地铃和蓝蓟制得。
一种抗敏组合物的制备方法,包括以下步骤:
(1)分别取倒地铃和蓝蓟,粉碎,得倒地铃粉和蓝蓟粉;
(2)将步骤(1)制得的倒地铃粉和蓝蓟粉混合,加入溶剂,浸泡,提取,过滤,得滤液即为所述抗敏组合物。
步骤(1)中所述倒地铃和所述蓝蓟的质量比为(1-3):(3-1)。
优选的,步骤(1)所述粉碎的过程为:先粉碎过40-80目筛,再于-20至-10℃下超微粉20-90min,制得倒地铃超微粉和蓝蓟超微粉;所述倒地铃超微粉和所述蓝蓟超微粉的粒径≤25μm。倒地铃和蓝蓟中抗敏成分主要存在于细胞内,在细胞完整无损的情况下,抗敏成分只有透过细胞膜后才能被利用。经过超微粉碎后,细胞破壁,其细胞内的抗敏成分被暴露出来,效果有大幅度的提高。超微粉碎技术的利用,一方面可使抗敏成分溶出阻力减小;另一方面,微细化的物料具有很强的表面吸附力、亲和力、分散性和溶解性,从而提高了抗敏成分的溶出速度及溶出率。同时在超微粉碎时,通过在低温状态下进行,避免产生过热现象,更利于保留抗敏成分物质的活性,从而提高抗敏效果。
优选的,步骤(2)中所述溶剂为水和/或乙醇;进一步优选的,所述溶剂为质量分数为70%-90%的乙醇水溶液。蓝蓟和倒地铃中所含的抗敏物质在醇类的溶解度大于水中的溶解度,蓝蓟和倒地铃的醇提取物的抗敏能力大于水提取物的抗敏能力。当采用溶剂为质量分数为70%-90%的乙醇水溶液,蓝蓟和倒地铃中抗敏物质的含量高,抗敏效果好。
优选的,步骤(2)中所述溶剂的质量为所述倒地铃超微粉和所述蓝蓟超微粉的总质量的4-10倍。
优选的,步骤(2)提取为超声波提取;进一步优选的,所述超声波提取的时间为15-45min。当超声波提取时间小于10min时,蓝蓟和倒地铃中抗敏物质为能充分溶解于溶剂中;当提取时间过长,超声波会影响抗敏物质的活性。
优选的,步骤(2)中超声波的功率为150-250w。
具体的,一种抗敏组合物的制备方法,包括以下步骤:
(1)分别取干制的倒地铃和蓝蓟药材,倒地铃和蓝蓟整株均可入药,打碎,先用万能粉碎机粉碎,过筛,得倒地铃粉和蓝蓟粉;也可以在进一步粉碎得超微粉,即再采用振动式药物超微粉碎机在振幅5.5mm,工作温度为-20至-10℃下,粉碎20-60min,即得倒地铃超微粉和蓝蓟超微粉。
(2)称取地铃粉或超微粉和蓝蓟粉或超微粉,加4-10倍量溶剂浸泡10-24h,超声波提取20-30min,过滤,残渣加2倍量溶剂,超声波提取2次,每次20-30min。合并提取液液,过滤,得滤液,减压浓缩。
所述抗敏组合物在化妆品领域中的应用。
一种化妆水,包括水和所述抗敏组合物。
优选的,所述化妆水还包括氨基酸、维生素、二醇、六肽或对羟基苯乙酮中的至少一种。
优选的,所述氨基酸为蛋氨酸、苏氨酸、缬氨酸、异亮氨酸中的至少两种。
优选的,所述维生素为视黄醇、硫胺素、烟酰胺、泛醇中的至少两种。
优选的,所述二醇为己二醇和丙二醇。
相对于现有技术,本发明的有益效果如下:
本发明所述抗敏组合物,主要由蓝蓟提取物与倒地铃提取物组成;透明质酸酶是ⅰ型过敏反应的参与者,透明质酸酶与炎症、过敏有强相关性;所述抗敏组合物对透明质酸酶的抑制率高达95%,二者协同增效,能够改善皮肤过敏、炎症现象。
附图说明
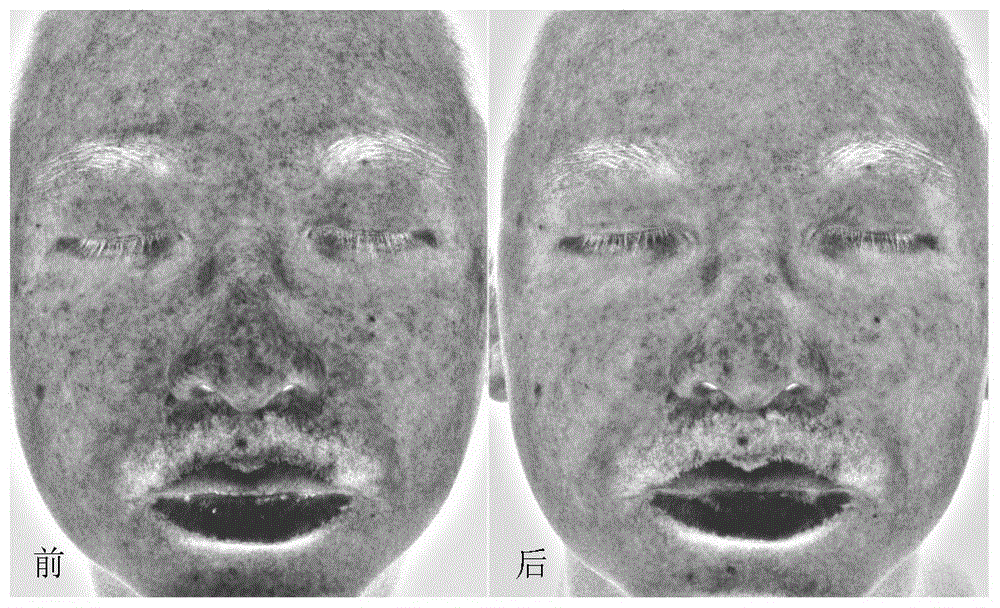
图1为敷化妆水a前后的面部状态图;
图2为敷化妆水b前后的面部状态图;
图3为敷化妆水c前后的面部状态图;
图4为敷化妆水d前后的面部状态图。
具体实施方式
为了让本领域技术人员更加清楚明白本发明所述技术方案,现列举以下实施例进行说明。需要指出的是,以下实施例对本发明要求的保护范围不构成限制作用。
实施例1
分别取倒地铃、蓝蓟药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目倒地铃粉、蓝蓟粉各500g,混合,加8倍量水浸泡24h,超声波(200w)提取30min,过滤,残渣加6倍量水,超声波(200w)提取2次,每次30min。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例2
分别取倒地铃、蓝蓟药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目倒地铃粉、蓝蓟粉各500g,混合,加8倍量85%乙醇浸泡24h,超声波(200w)提取30min,过滤,残渣加2倍量乙醇,超声波(200w)提取2次,每次30min。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例3
分别取倒地铃、蓝蓟药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目倒地铃粉、蓝蓟粉各500g,混合,加8倍质量分数为70%的乙醇水溶液浸泡24h,超声波(150w)提取15min,过滤,残渣加2倍量质量分数为70%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例4
分别取倒地铃、蓝蓟药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目倒地铃粉、蓝蓟粉各500g,混合,加8倍质量分数为80%的乙醇水溶液浸泡24h,超声波(250w)提取30min,过滤,残渣加2倍量质量分数为80%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例5
分别取倒地铃、蓝蓟药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目倒地铃粉、蓝蓟粉各500g,混合,加8倍质量分数为90%的乙醇水溶液浸泡24h,超声波(200w)提取45min,过滤,残渣加2倍量质量分数为90%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例6
分别取倒地铃和蓝蓟药材,打碎,先用万能粉碎机粉碎,过80目筛,再采用振动式药物超微粉碎机在振幅5.5mm,工作温度为-20至-10℃下,粉碎40min,即得倒地铃超微粉和蓝蓟超微粉。取过200目筛(约74μm)的倒地铃粉、蓝蓟粉各500g,混合,加8倍质量分数为70%的乙醇水溶液浸泡24h,超声波(200w)提取30min,过滤,残渣加2倍量质量分数为70%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例7
分别取倒地铃和蓝蓟药材,打碎,先用万能粉碎机粉碎,过80目筛,再采用振动式药物超微粉碎机在振幅5.5mm,工作温度为-20至-10℃下,粉碎40min,即得倒地铃超微粉和蓝蓟超微粉。取过200目筛的倒地铃粉、蓝蓟粉各500g,混合,加8倍质量分数为80%的乙醇水溶液浸泡24h,超声波(150w)提取45min,过滤,残渣加2倍量质量分数为80%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例8
分别取倒地铃和蓝蓟药材,打碎,先用万能粉碎机粉碎,过80目筛,再采用振动式药物超微粉碎机在振幅5.5mm,工作温度为-20至-10℃下,粉碎40min,即得倒地铃超微粉和蓝蓟超微粉。取过200目筛的倒地铃粉、蓝蓟粉各500g,混合,加8倍质量分数为90%的乙醇水溶液浸泡24h,超声波(250w)提取15min,过滤,残渣加2倍量质量分数为90%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例9
分别取倒地铃和蓝蓟药材,打碎,先用万能粉碎机粉碎,过80目筛,再采用振动式药物超微粉碎机在振幅5.5mm,工作温度为-20至-10℃下,粉碎40min,即得倒地铃超微粉和蓝蓟超微粉。取过1250目(约10μm)筛的倒地铃超微粉、蓝蓟超微粉各500g,混合,加8倍质量分数为70%的乙醇水溶液浸泡24h,超声波(250w)提取45min,过滤,残渣加2倍量质量分数为70%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例10
分别取倒地铃和蓝蓟药材,打碎,先用万能粉碎机粉碎,过80目筛,再采用振动式药物超微粉碎机在振幅5.5mm,工作温度为-20至-10℃下,粉碎40min,即得倒地铃超微粉和蓝蓟超微粉。取过1250目筛的倒地铃超微粉、蓝蓟超微粉各500g,混合,加8倍质量分数为80%的乙醇水溶液浸泡24h,超声波(200w)提取15min,过滤,残渣加2倍量质量分数为80%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例11
分别取倒地铃和蓝蓟药材,打碎,先用万能粉碎机粉碎,过80目筛,再采用振动式药物超微粉碎机在振幅5.5mm,工作温度为-20至-10℃下,粉碎40min,即得倒地铃超微粉和蓝蓟超微粉。取过1250目筛的倒地铃超微粉、蓝蓟超微粉各500g,混合,加8倍质量分数为90%的乙醇水溶液浸泡24h,超声波(150w)提取30min,过滤,残渣加2倍量质量分数为90%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例12
分别取倒地铃和蓝蓟药材,打碎,先用万能粉碎机粉碎,过80目筛,再采用振动式药物超微粉碎机在振幅5.5mm,工作温度为-20至-10℃下,粉碎40min,即得倒地铃超微粉和蓝蓟超微粉。取过1250目筛的倒地铃超微粉、蓝蓟超微粉各500g,混合,加8倍质量分数为60%的乙醇水溶液浸泡24h,超声波(150w)提取30min,过滤,残渣加2倍量质量分数为60%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例13
分别取倒地铃和蓝蓟药材,打碎,先用万能粉碎机粉碎,过80目筛,再采用振动式药物超微粉碎机在振幅5.5mm,工作温度为-20至-10℃下,粉碎40min,即得倒地铃超微粉和蓝蓟超微粉。取过1250目筛的倒地铃超微粉、蓝蓟超微粉各500g,混合,加8倍质量分数为90%的乙醇水溶液浸泡24h,超声波(150w)提取10min,过滤,残渣加2倍量质量分数为90%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例14
分别取倒地铃、蓝蓟药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目倒地铃粉、蓝蓟粉各500g,混合,加8倍质量分数为90%的乙醇水溶液浸泡24h,超声波(150w)提取30min,过滤,残渣加2倍量质量分数为90%的乙醇水溶液,超声波提取2次,每次超声时间与第一次超声时间一致。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例15
取倒地铃、蓝蓟药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目倒地铃、蓝蓟各500g,混合,加8倍量水浸泡24h,回流提取60min,过滤,残渣加6倍量水,回流提取2次,每次30min。合并提取液,过滤,得滤液,减压浓缩至500ml。
实施例16
取倒地铃、蓝蓟药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目倒地铃、蓝蓟各500g,混合,加8倍量85%乙醇溶液浸泡24h,回流提取60nin,过滤,残渣加2倍量乙醇溶液,回流提取2次,每次30min。合并提取液,过滤,得滤液,减压浓缩至500ml。
对比例1
取蓝蓟药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目蓝蓟粉1000g,加8倍量水浸泡24h,超声波(200w)提取30min,过滤,残渣加6倍量水,超声波(200w)提取2次,每次30min。合并提取液,过滤,得滤液,减压浓缩至500ml。
对比例2
取倒地铃药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目倒地铃粉1000g,加8倍量水浸泡24h,超声波(200w)提取30min,过滤,残渣加6倍量水,超声波(200w)提取2次,每次30min。合并提取液,过滤,得滤液,减压浓缩至500ml。
对比例3
取蓝蓟药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目蓝蓟粉1000g,加8倍量85%乙醇浸泡24h,超声波(200w)提取30min,过滤,残渣加2倍量85%乙醇,超声波(200w)提取2次,每次30min。合并提取液,过滤,得滤液,减压浓缩至500ml。
对比例4
取倒地铃药材,打碎,用万能粉碎机粉碎,过80目筛;称取80目倒地铃粉1000g,加8倍量85%乙醇浸泡24h,超声波(200w)提取30min,过滤,残渣加2倍量85%乙醇,超声波提取2次,每次30min。合并提取液,过滤,得滤液,减压浓缩至500ml。
产品效果测试
透明质酸酶是ⅰ型过敏反应的参与者,透明质酸酶与炎症、过敏有强相关性。采用透明质酸酶体外抑制率测试,检测各样品的抗敏效果。
1.透明质酸酶体外抑制率测试
(1)实验原理
透明质酸酶能够不加选择地水解透明质酸中的β-n-乙酰葡萄糖胺与d-葡萄糖醛酸之间的1,4-糖苷键,而得到β-n-乙酰葡萄糖胺。β-n-乙酰葡萄糖胺在碱性条件下可以与乙酰丙缩合生成生色原2-甲基-3-乙酰吡咯衍生物,生色原与对二甲氨基苯甲醛在浓盐酸乙醇中生色。
(2)实验所需溶液配制
0.5mol/l氢氧化钾乙醇溶液:将4gkoh和2.5g铝片置于500ml乙醇中,在95℃水内回流1h后立即蒸馏,将14gkoh溶解在蒸馏出的乙醇中,静置数天后取上清液。
醋酸缓冲溶液(ph=5.6):量取1155μl冰乙酸稀释至100ml混匀后取其中4.8ml为a溶液;称取2.72g结晶乙酸钠加水溶解定容至100ml,混匀后取其中45.2ml为b溶液;混合溶液a、b,以水定容至100ml混匀。精密测定其ph值,用溶液a或b调至5.6即可。
透明质酸酶溶液:称取透明质酸酶0.0100g置于烧杯中加入4ml醋酸缓冲溶液,最终工作浓度为1250u/ml。
0.5mg/ml透明质酸钠溶液:称取透明质酸钠0.0050g置于烧杯中,加入10m醋酸缓冲溶液。
埃尔利希试剂(ehrlichreagent):称取0.8g对二甲氨基苯甲醛溶于15ml浓盐酸和15ml无水乙醇中,可保存两个月。
乙酰丙酮溶液:取乙酰丙酮3.5ml溶于50ml1.0mol/l的碳酸钠溶液中,此溶液在用前配制。
(3)测定抗过敏活性:采用透明质酸酶体外抑制实验elson-morgan法进行。取0.1ml0.25mmo/lcacl2溶液和0.5ml透明质酸酶液37℃保温培养20min;分别加入样品液0.5ml;继续在37℃下保温培养20min;再加入0.5ml透明质酸钠液,于37℃下保温30min,常温放置5min;加入0.1ml0.4mol/lnaoh溶液和0.5ml乙酰丙酮溶液,置于沸水浴中加热15min后立即用冰水进行冷却5min;加入埃尔利希试剂1.0ml,并用3.0ml无水乙醇进行稀释,放置20min显色,用分光光度计测定其吸光度值。
抗过敏活性计算公式:
透明质酸酶的抑制率=[(a-b)-(c-d)]/(a-b)
式中,a表示对照溶液abs值(用醋酸缓冲溶液代替样品液);b表示对照空白溶液的abs值(用醋酸缓冲溶液代替样品液及酶液);c表示实验组abs值;d表示试样对照组abs值(用醋酸缓冲溶液代替酶液)。
实验前,先对对照溶液(用醋酸缓冲溶液代替样品液)进行450-700mm范围的波长扫描,以确定最大吸收波长,在该最大吸收波长处分别进行对照空白溶液和各提取物其他组的abs值测定。测定结果表明,在450-700mm波长范围内出现一个波峰,此时波长λ=547nm,吸光度为0.282最大,因此,确定最终测定吸光度时在λ=547nm处进行。
a.提取物浓度与抗敏效果之间的关系
分别取实施例1、2制得的抗敏组合物和对比例1-4制得的提取液10、20、40、60、80、120mg于50ml烧杯中,加去25ml离子水搅拌,配制成待测样品,进行透明质酸酶体外抑制率测试。测定结果见表1。
表1不同浓度下透明质酸酶体外抑制率
透明质酸酶抑制率越高,说明该物质的抗过敏效果越好,反之则效果越差,通过表1可知,蓝蓟提取物和倒地铃提取物具有一定的抗敏作用,但随着提取物浓度的增加上升趋势不明显,甚至在到达一定的浓度之后,倒地铃提取物对透明质酸酶的抑制呈减弱的趋势。抗敏效果差。而实施例1、2中蓝蓟、倒地铃提取物的组合物对透明质酸酶抑制率大大增加,高于蓝蓟提取物与倒地铃提取物对透明质酸酶抑制率的加和,蓝蓟与倒地铃提取物对透明质酸酶的抑制具有协同作用。
b.实施例1-16和对比例1-4制得的提取液在相同浓度下的抗敏效果
分别取实施例1-16和对比例1-4制得的提取液80mg于50ml烧杯中,加去25ml离子水搅拌,配制成待测样品液,进行透明质酸酶体外抑制率测试。
对实施例1-16和对比例1-4的各样品液进行测定,结果见下表2:
表2各实施例和对比例的透明质酸酶体外抑制率
实施例1-16制得的抗敏组合物的透明质酸酶体外抑制率明显高于对比例1-4,实施例1-16制得的抗敏组合物的透明质酸酶体外抑制率均大于50%,具有明显的抗敏效果,而对比例1-4的透明质酸酶体外抑制率小于40%,不能达到良好抗敏效果。
2.皮肤刺激修复试验
a.取蒸馏水99g升温至85℃,保温30min,搅拌降温至45℃,取复合氨基酸(蛋氨酸0.04g、苏氨酸0.04g、缬氨酸0.04g、异亮氨酸0.04g、赖氨酸0.04g)、复合维生素(视黄醇0.05g、盐酸硫胺素0.05g、烟酰胺0.05g、泛醇0.05g)、六肽-10.1g(浓度为1000ppm)、己二醇0.3g、实施例11制得的抗敏组合物(浓度为3.2mg/ml)0.2g,搅拌5分钟,制得混合液;再将对羟基苯乙酮0.4g、丙二醇1g加热至70℃,搅拌至溶解,降温至45℃,加入上述混合液中,混合,充分溶解,制得化妆水a。
b.取蒸馏水99g升温至85℃,保温30min,搅拌降温至45℃,取复合氨基酸(蛋氨酸0.04g、苏氨酸0.04g、缬氨酸0.04g、异亮氨酸0.04g、赖氨酸0.04g)、复合维生素(视黄醇0.05g、盐酸硫胺素0.05g、烟酰胺0.05g、泛醇0.05g)、六肽-10.1g(浓度为1000ppm)、己二醇0.3g、对比例2制得的提取液(浓度为3.2mg/ml)0.2g,搅拌5分钟,制得混合液;再将对羟基苯乙酮0.4g、丙二醇1g加热至70℃,搅拌至溶解,降温至45℃,加入上述混合液中,混合,充分溶解,制得化妆水b。
c.取蒸馏水99g升温至85℃,保温30min,搅拌降温至45℃,取复合氨基酸(蛋氨酸0.04g、苏氨酸0.04g、缬氨酸0.04g、异亮氨酸0.04g、赖氨酸0.04g)、复合维生素(视黄醇0.05g、盐酸硫胺素0.05g、烟酰胺0.05g、泛醇0.05g)、六肽-10.1ml(浓度为1000ppm)、己二醇0.3ml、对比例3制得的提取液(浓度为3.2mg/ml)0.2g,搅拌5分钟,制得混合液;再将对羟基苯乙酮0.4g、丙二醇1g加热至70℃,搅拌至溶解,降温至45℃,加入上述混合液中,混合,充分溶解,制得化妆水c。
d.取蒸馏水99.2g升温至85℃,保温30min,搅拌降温至45℃,取复合氨基酸(蛋氨酸0.04g、苏氨酸0.04g、缬氨酸0.04g、异亮氨酸0.04g、赖氨酸0.04g)、复合维生素(视黄醇0.05g、盐酸硫胺素0.05g、烟酰胺0.05g、泛醇0.05g)、六肽-10.1g(浓度为1000ppm)、己二醇0.3ml,搅拌5分钟,制得混合液;再将对羟基苯乙酮0.4g、丙二醇1g加热至70℃,搅拌至溶解,降温至45℃,加入上述混合液中,混合,充分溶解,制得化妆水d。
取化妆水a-d各50ml,将压缩面膜浸泡其中至完全浸湿,待用。
选面部皮肤完整,无皮损;年龄为25~35岁;至少4周内未经任何医美手段进行治疗;至少4周内未使用任何强烈刺激性功效产品;自愿加入研究项目中治疗并签署知情同意书的受试者80名。
如有以下情况之一的不得参加试验:a.妊娠及计划妊娠或哺乳期妇女;b.合并有各大脏器系统严重的原发性疾病、内分泌系统疾病患者、恶性肿瘤患者、精神病患者等;c.4周内曾使用其他方刺激性美容方法;d.无法判断疗效或资料不全影响疗效判断者;e.面部患有其他皮肤疾病;f.不符合纳入标准的其他案例;g.治疗过程中有严重不良反应者;h.对高浓度烟酰胺不敏感者。
过敏反应的早期阶段是血管扩张,血流速度加快导致流体静力压升高,毛细血管通透性增强,会直接导致毛细血管内部物质从血浆到达血管外间质,存在于皮肤真皮乳头层中血管和血红素被visia皮肤检测仪检测到,并赋予这些组织红颜色,红色面积越大,红色越深即表示过敏反应越剧烈。
受试者分成4组,每20人一组,选择受试者面部作为受试部位,用清水清洗面部,受试者静坐10min,随后进入涂抹实验阶段;用质量分数为15%的烟酰胺水溶液30g浸透压缩面膜,面部湿敷浸透15%烟酰胺的压缩面膜对受试区域进行刺激;持续刺激30min后,用visia7.0皮肤检测仪进行数值采集,数据采集结束后,每一组受试者分别立即使用化妆水a-d完全浸湿的压缩面膜,湿敷20min,湿敷后受试者静坐10min,用visia7.0皮肤检测仪进行数值采集;统计受试者实验部位每次测得的数值,分析红值的变化。
其中第一组20名受试者脸部在烟酰胺的刺激下,变红,再敷化妆水a完全浸湿的压缩面膜后,20名受试者脸部过敏变红的情况得到明显好转,选取一名受试者的数据采集,结果见如图1,图1分别为敷化妆水a前后的状态图(其中面部过敏变红部分即图中阴影部分)。可见使用含有抗敏组合物的化妆水后,能够有效改善过敏现象。
第二组20名受试者脸部在烟酰胺的刺激下,变红,再敷化妆水b完全浸湿的压缩面膜后,未出现明显好转的现象,选取一名受试者的数据采集,结果见如图2,图2分别为敷化妆水b前后的状态图(其中面部过敏变红部分即图中阴影部分)。
第三组20名受试者脸部在烟酰胺的刺激下,变红,再敷化妆水c完全浸湿的压缩面膜后,有轻微好转的现象,但效果明显不如第一组;选取一名受试者的数据采集,结果见如图3,图3分别为敷化妆水c前后的状态图(其中面部过敏变红部分即图中阴影部分)。
第四组20名受试者脸部在烟酰胺的刺激下,变红,再敷化妆水d完全浸湿的压缩面膜后,未出现好转的现象,选取一名受试者的数据采集,结果见如图4,图4分别为敷化妆水d前后的状态图(其中面部过敏变红部分即图中阴影部分)。
- 还没有人留言评论。精彩留言会获得点赞!