一种含艾草提取物的免洗手部消毒制剂及其制备方法与流程
本发明属于卫生清洁用品技术领域,具体涉及一种含艾草提取物的免洗手部消毒制剂及其制备方法。
背景技术:
在日常生活中,人体接触外部最频繁的部位是手部,极容易沾染上各种细菌,手上的细菌根据手部寄生的深度不同分为两类,一类是暂居菌,暂居菌有一部分是致病菌或条件致病菌,这些细菌的滋生和接触传播导致了很多疾病的发生,但是暂居菌在皮肤上的存活时间不足24h,用抑菌洗手液或消毒液就可以清除约98%的暂居菌,而另一类是常居菌,其种类和数量相对固定,且多为非致病菌。因此,有效地对手部进行消毒有利于防止疾病的发生。
目前,用于手部消毒的消毒液种类繁多,其组成成分及性能各不相同,而市售免洗手部消毒类产品多考虑产品杀菌功效,若不及时进行正确的护理和保湿,长期、频繁使用容易造成皮肤伤害,加速皮肤衰老。艾叶的化学成分复杂,根据研究及有关文献可知其药效源于所富含的各种化学物质,除主要含有挥发油,还有黄酮类、鞣质类、萜类、多糖类及微量元素等,这些成分大都具有抑制微生物、抗过敏、抗炎镇痛、免疫调节、止血、抗衰老等的药理活性,可缓解酒精对皮肤刺激性的副作用。艾草用超临界萃取精油后得到残渣,本发明人经过分析残渣后,发现残渣中含有大量未被萃取的黄酮类、鞣质类成分等有效成分,若将残渣中的有效成分充分提取,可以增加艾草的使用效率,做到高效环保。
技术实现要素:
本发明旨在提供一种含艾草提取物的免洗手部消毒制剂及其制备方法,本发明的免洗手部消毒制剂具有安全高效的消毒效果,能够减少对皮肤的刺激。
为了达到上述目的,本发明采用以下技术方案:
一种含艾草提取物的免洗手部消毒制剂,包括以下质量分数的原料:
艾草提取物85%~97%;
水1%~5%;
甘油1%~3%;
透明质酸钠0.05%~0.5%;
增稠剂0%~1.5%;
ph调节剂0.02%~5%。
优选地,包括以下质量分数的原料:
艾草提取物95.33%;
水1.5%;
甘油2.5%;
透明质酸钠0.05%;
增稠剂0.6%;
ph调节剂0.02%。
优选地,所述增稠剂为卡波、丙烯酰二甲基牛磺酸铵/vp共聚物、黄原胶中的一种或几种。
优选地,所述黄原胶与卡波的质量比为1:(5~8)或黄原胶与丙烯酰二甲基牛磺酸铵/vp共聚物的质量比为1:(5~8)。
优选地,ph调节剂为三乙醇胺或氨甲基丙醇。
优选地,所述艾草提取物的制备方法为:
s1)取艾草粉碎,超临界萃取后得到艾渣,干燥,得到艾渣粉末;
s2)将步骤s2中的艾渣粉末加入到60%~90%乙醇溶液中,浸泡,过滤,即得艾草提取物。
优选地,所述步骤s2中的浸泡时间为0.5h~4h。
优选地,所述含艾草提取物的免洗手部消毒制剂的制剂类型为液体剂、凝胶剂、喷雾剂中的一种。
本发明还提供上述含艾草提取物免洗手部消毒制剂的制备方法,包括以下步骤:
取配方量的甘油、透明质酸钠和增稠剂混合均匀,得到混合物;将艾草提取物加入到混合物中搅拌均匀,得到制剂;将水和ph调节剂混合得到ph调节剂;测量制剂的ph值,再加入ph调节剂调节制剂ph到4.5~6.5,灌装,质检,即得。
与现有技术相比,本发明具有以下有益效果:
(1)本发明含艾草提取物的免洗手部消毒制剂中的艾草提取物采用的原料为艾草超临界萃取后得到艾渣,能够提高艾草的使用率,且艾渣的有效成分与艾草的有效成分接近,具有强大的经济效益。
(2)本发明含艾草提取物的免洗手部消毒制剂可以用于手部消毒,经过实验四后发现,消毒制剂在乙醇挥发后,仍有具有消毒效果好,消毒持续时间长,安全高效。
(3)本发明含艾草提取物的免洗手部消毒制剂添加的艾草提取物、甘油、透明质酸钠和增稠剂能够共同作用,滋养皮肤,保持手部滋润。经过实验五后发现,艾草提取物的加入减少了对皮肤的刺激。
附图说明
图1为本发明艾草粉末在不同浸提溶剂的紫外吸收光谱图。
图2为本发明艾渣粉末在不同浸提溶剂的紫外吸收光谱图。
图3为本发明艾草粉末、艾渣粉末在不同浸提时间的紫外吸收光谱。
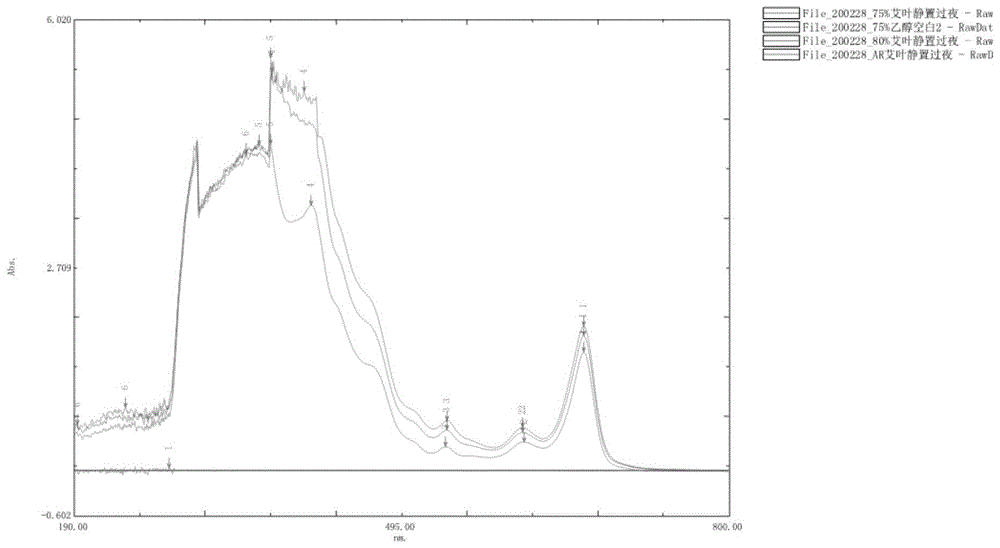
图4为本发明艾草粉末与艾渣粉末用75%乙醇浸提24h紫外吸收光谱图。
图5为本发明艾渣粉末与艾草粉末的280nm高效液相色谱图。
图6为本发明消毒制剂对大肠杆菌的抗菌效果图。
图7为本发明消毒制剂对金黄色葡萄球菌的抗菌效果图。
图8为本发明消毒制剂对白色念珠菌的抗菌效果图。
具体实施方式
以下通过实施例形式的具体实施方式,对本发明的上述内容作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下实施例。
实验一、不同浸提剂对艾草粉末、艾渣粉末的影响
1.1实验对象
艾草粉末(艾叶):将艾草干燥后粉碎即得;
艾渣粉末:取艾草粉碎,超临界萃取后得到艾渣,干燥,得到艾渣粉末。
1.2实验方法:分别取2.5g艾草粉末及艾渣粉末置于100ml锥形瓶中,然后分别加入50ml的75%乙醇溶液、80%乙醇溶液、无水乙醇溶液,浸提24h,用0.45μm微孔滤膜过滤待测溶液,再用紫外-可见分光光度计扫描。
设定紫外-可见分光光度计设备参数如下:比色皿为1cm;扫描范围:190nm-800nm;扫描速度:中速;扫描间隔:0.5nm,响应时间为:0.2s。
1.3结论:图1为艾草粉末在不同浸提溶剂的紫外吸收光谱图,图2为艾渣粉末在不同浸提溶剂的紫外吸收光谱图。鞣质在400-1000nm波长下均有吸收,其中鞣质含量最大吸收波长为760nm。黄酮类成分在紫外吸收光谱中主要由300-400nm(吸收带i)和240-280nm(吸收带ii)组成。从图1和图2可以看出,艾草粉末和艾渣粉末分别在以75%乙醇溶液为浸提剂时,浸提效果最佳。
实验二、不同浸提时间对艾草粉末、艾渣粉末的影响
2.1实验对象:艾草粉末(艾叶)、艾渣粉末
2.2实验方法:分别取2.5g艾草粉末及艾渣粉末置于100ml锥形瓶中,然后分别加入50ml的75%乙醇,对比浸泡15min、30min、60min、90min、120min、24h的溶液190nm-800nm范围内紫外光谱变化。
2.3结论:图3为艾草粉末、艾渣粉末在不同浸提时间的紫外吸收光谱。从图3可以看出,艾渣粉末在浸提15min后的黄酮类成分和鞣质的含量优于艾草粉末。
实验三、艾草粉末和艾渣粉末的对比实验
3.1紫外光谱对比
3.1.1实验对象:艾草粉末(艾叶)、艾渣粉末
3.1.2分别取2.5g艾草粉末和艾渣粉末置于50ml锥形瓶中,分别加入50ml的75%乙醇,浸提24h,用0.45μm微孔滤膜过滤待测溶液,设定紫外-可见分光光度计设备参数如下:比色皿为1cm;扫描范围:190-400;扫描速度:中速;扫描间隔:0.5nm,响应时间为:0.2s。对比吸收光谱变化。
3.2高效液相色谱对比
3.2.1实验对象:艾草粉末(艾叶)、艾渣粉末
3.2.2实验方法:分别取2.5g艾草粉末及艾渣粉末置于100ml锥形瓶中,加入50ml的75%乙醇溶液,称定重量,振荡浸泡24h,再称定重量,用75%乙醇不足减失的重量,振荡5min,静置过滤取续滤液,即得上机溶液。以十八烷键合硅胶为填充剂,以下表甲醇-水比例为流动相,检测波长为280nm。分别精密吸取艾渣浸提液和艾草浸提液各10μl,注入液相色谱仪,测定即得。
流动相比例:
3.3结论:图4为艾草粉末与艾渣粉末用75%乙醇浸提24h紫外吸收光谱图,图5为艾渣粉末与艾草粉末的280nm高效液相色谱图。从图4和图5可以看出,经超临界提取挥发性成分后剩余的艾渣粉末与艾草粉末在75%乙醇中的成分差异不明显,部分物质成分含艾草原植物中含量略低。因此,在超临界提取挥发性成分后的艾渣粉末具有较大的经济效益。
实施例1~5、含艾草提取物的免洗手部消毒制剂
表1:实施例1~5的配方
其中,实施例1的艾草提取物的制备方法为:
s1)取2.5g艾草粉碎,超临界萃取后得到艾渣,干燥,得到艾渣粉末;
s2)将步骤s2中的艾渣粉末加入到70%乙醇溶液中,浸泡1h,过滤,即得艾草提取物。
实施例2的艾草提取物的制备方法为:
s1)取2.5g艾草粉碎,超临界萃取后得到艾渣,干燥,得到艾渣粉末;
s2)将步骤s2中的艾渣粉末加入到75%乙醇溶液中,浸泡1h,过滤,即得艾草提取物。
实施例3的艾草提取物的制备方法为:
s1)取2.5g艾草粉碎,超临界萃取后得到艾渣,干燥,得到艾渣粉末;
s2)将步骤s2中的艾渣粉末加入到75%乙醇溶液中,浸泡2h,过滤,即得艾草提取物。
实施例4的艾草提取物的制备方法为:
s1)取2.5g艾草粉碎,超临界萃取后得到艾渣,干燥,得到艾渣粉末;
s2)将步骤s2中的艾渣粉末加入到80%乙醇溶液中,浸泡1.5h,过滤,即得艾草提取物。
实施例5的艾草提取物的制备方法为:
s1)取2.5g艾草粉碎,超临界萃取后得到艾渣,干燥,得到艾渣粉末;
s2)将步骤s2中的艾渣粉末加入到80%乙醇溶液中,浸泡2h,过滤,即得艾草提取物。
上述含艾草提取物免洗手部消毒制剂的制备方法为:取配方量的甘油、透明质酸钠和增稠剂混合均匀,得到混合物;将艾草提取物加入到混合物中搅拌均匀,得到制剂;将水和ph调节剂混合得到ph调节剂;测量制剂的ph值,再加入ph调节剂调节制剂ph到6.3,灌装,质检,即得。
对比例1、含艾草提取物的免洗手部消毒制剂
与实施例2相比,区别在于,将艾草提取物替换成75%乙醇溶液。
对比例2、含艾草提取物的免洗手部消毒制剂
与实施例2相比,区别在于,不添加黄原胶。
对比例3、含艾草提取物的免洗手部消毒制剂
与实施例2相比,区别在于,黄原胶与丙烯酰二甲基牛磺酸铵/vp共聚物的质量比为1:1。
对比例4、含艾草提取物的免洗手部消毒制剂
与实施例2相比,区别在于,黄原胶与丙烯酰二甲基牛磺酸铵/vp共聚物的质量比为1:15。
实验四、消毒效果实验
1)杀菌效果评价
1.1实验方法:
a.将大肠杆菌、金黄色葡萄球菌和白色念珠菌(大肠杆菌8099、金黄色葡萄球菌atcc6538和白色念珠菌atcc10231)增菌培养和划线分离培养,选择单个典型菌落接种普通琼脂培养基(白色念珠菌用沙堡琼脂培养基)斜面,在37℃下于烘箱培养24h,再用含蛋白胨10g/l的磷酸缓冲液稀释配制成试验菌悬液,回收菌数为1×104cfu/ml~9×104cfu/ml;
b.将水解酶蛋白琼脂(或沙堡琼脂)用蒸馏水加热至融化,118℃灭菌13min,冷却至60℃倒入无菌培养皿后,冷却,得到平板。
c.取实施例2的消毒制剂5ml置于灭菌试管中,一式三管,20℃恒温5min。取步骤a中的三种悬菌液,在三个试管中分别滴加100微升,混合均匀后开始计时,作用1min时分别吸取0.5ml加入含4.5ml灭菌pbs的试管内充分混匀,静置10mi,吸取0.1ml(或作2~3个稀释度)混匀样液涂布琼脂平板,每稀释度至少2个平板,培养24h~48h后计数。以pbs代替受试样品,重复上述操作,作为对照样品;做两个平行试验,求平均值。
计算公式:杀菌率:
杀菌率(%)=(a-b)/a×100…………………………………………(1)
式中:
a——对照样品平均菌落数;
b——试验样品平均菌落数。
1.2实验结果表1受试样品对白色念珠菌、金黄色葡萄球菌及大肠杆菌的抗菌平板计数
注:表中符号“-”表示多不可数。
从表1结合图5、图6和图7可以看出,消毒剂对大肠杆菌的杀菌率为100%,对金黄色葡萄球菌的杀菌率为100%,对白色念珠菌的杀菌率为100%。含艾草提取物的免洗手部消毒制剂具有较好的杀菌作用。
2)抑菌效果评价
2.1实验方法:
a.将大肠杆菌、金黄色葡萄球菌和白色念珠菌(大肠杆菌8099、金黄色葡萄球菌atcc6538和白色念珠菌atcc10231)增菌培养和划线分离培养,选择单个典型菌落接种普通琼脂培养基(白色念珠菌用沙堡琼脂培养基)斜面,在37℃下于烘箱培养24h,再用含蛋白胨10g/l的磷酸缓冲液稀释配制成试验菌悬液;
b.将水解酶蛋白琼脂(或沙堡琼脂)用蒸馏水加热至融化,118℃灭菌13min,冷却至60℃倒入无菌培养皿后,冷却,得到平板。
c.分别取实施例和对比例的消毒制剂各5ml置于灭菌试管中,一式三管。取步骤a中的三种悬菌液,在三个试管中分别滴加100微升,混合均匀后开始计时,作用15min、60min、240min时分别吸取0.5ml加入含4.5mlpbs的试管内充分混匀,用倾柱法做活菌培养计数,实验环境温度控制在19~25℃,重复3次实验,计算平均抑菌率。阳性对照组吸取100微升悬菌液加入5mlpbs中,作用240min后吸取0.5ml加至4.5mlpbs的试管中同样用倾柱法做活菌培养计数。阴性对照组为空白营养琼脂平板。
2.2实验结果
表2:实施例和对比例的消毒效果实验结果
注:大肠杆菌:阳性对照组作用240min回收的平均菌落数为39500cfu/ml;阴性对照组无大肠杆菌菌落。
金黄色葡萄球菌:阳性对照组作用240min回收的平均菌落数为36700cfu/ml;阴性对照组无金黄色葡萄球菌菌落。
白色念珠菌:阳性对照组作用240min回收的平均菌落数为38200cfu/ml;阴性对照组无白色念珠菌菌落。
从表3可以看出,实施例和对比例在15min时,抑菌效果相近,而随着时间延长到60min、240min时,抑菌效果发生变化,对比例的抑菌效果下降,而实施例仍保持较好的抑菌效果,且实施例1和实施例2的抑菌效果最优。
实验五、皮肤感调查比较
实验方法:随机从社会志愿者中选取30人,平均年龄为25~40岁,其中男性11人,女性19人,分成6组分别使用实施例2和对比例1~4的含艾草提取物的免洗手部消毒制剂,用后在外观、有无刺激感、有无紧绷感和用后舒适度上以每项25分为满分进行评价,再求平均分。
表3:调查评分标准表
表4:肤感调查结果
从表4可以看出,实施例2外观好,肤感较为舒适。
上述实施例仅例示性说明本发明的原理及其功效,而非用于限制本发明。任何熟悉此技术的人士皆可在不违背本发明的精神及范畴下,对上述实施例进行修饰或改变。因此,举凡所属技术领域中具有通常知识者在未脱离本发明所揭示的精神与技术思想下所完成的一切等效修饰或改变,仍应由本发明的权利要求所涵盖。
- 还没有人留言评论。精彩留言会获得点赞!