PDE4抑制剂在制备抑制胶质瘤增殖的药物中的应用的制作方法
pde4抑制剂在制备抑制胶质瘤增殖的药物中的应用
技术领域
1.本技术属于抗肿瘤药物特别是胶质瘤药物领域,具体地,本技术提供了pde4抑制剂zl-n-91在制备治疗胶质瘤增殖的药物中的应用。
背景技术:
2.中枢神经系统癌症(cns)一直是我国十大高发病率、高死亡率的恶性肿瘤之一。2016年,我国中枢神经系统(cns)癌症新发106,207例,死亡59,120例,是全世界cns癌症新发和死亡人数最多的国家,我国cns癌症防治任重而道远。在原发性cns癌症中最常见的是胶质瘤,一种胶质细胞恶性肿瘤,根据其恶性程度分为4个等级(whoⅰ至ⅳ级),胶质母细胞瘤(gbm,ⅳ级)是胶质瘤中最常见、恶性程度最高、侵袭性最强的肿瘤,占胶质瘤的大部分(56.6%),发病率为3.21/10万。尽管在其诊断和标准治疗如手术、放疗、化疗方面取得了进展,但由于gbm发病的复杂性、肿瘤耐辐射和化疗等,导致其预后仍效果很差,患者在确诊后生存期仅有12-15个月。由于目前治疗胶质瘤的药物种类远不及其他实体瘤,疗效和耐药性性能也普遍有限,寻求高效的治疗药物具有重要意义。
3.磷酸二酯酶(简称pdes)具有水解细胞内第二信使camp或cgmp的功能,从而影响这些第二信使所介导的信号通路,调节细胞功能。pdes共分为11个亚型,其中磷酸二酯酶4(pde4)特异性水解camp。pde4主要分布于各种炎性细胞内,包括肥大细胞、巨噬细胞淋巴细胞、上皮细胞等,参与了促进单核细胞与巨噬细胞活化、中性粒细胞浸润、血管平滑肌的增殖、血管扩张以及心肌收缩等相关生理病理过程,对中枢神经系统功能、心血管功能、炎症/免疫系统、细胞黏附等都有影响。研究显示,pde4抑制剂(pde4i)具有抗炎、抗过敏、抗血小板活化作用。其作用机制主要涉及:1)抑制多种炎症介质/细胞因子的释放,能够抑制il-4、il-5基因的表达;2)抑制白细胞的激活(如呼吸爆发),抑制白细胞游走;3)抑制细胞粘附因子(cam)的表达或上调;4)诱导产生具有抑制活性的细胞子,如il-6;5)诱导细胞凋亡;6)刺激内源性激素和儿茶酚胺类物质的释放。已经开发或正在开发的pde4抑制剂针对的疾病主要是慢性阻塞性肺疾病(copd)、哮喘、炎症性肠疾病、关节炎等。但是,很多研究表明pde4抑制剂对于恶性肿瘤也有显著的抑制作用。patricia goldhoff给裸鼠异种移植入人脑星形胶质母细胞瘤细胞u87后,使用pde4抑制剂可以延长小鼠生存期。2006年motoshi narita发现pde4i可以抑制人黑色素瘤细胞的生长,petros x.e.mouratidis发现在胰腺癌细胞中加入pde4抑制剂cc-8075和cc-8062后,可以使其细胞增殖降低和细胞凋亡增加。
4.现有的pde4抑制剂主要有咯利普兰(rolipram)、西洛司特(cilomilast)、罗氟司特(roflumilast)等。由于rolipram和cilomilast引发头晕、头痛和恶心、呕吐等胃肠道不良反应,影响了药物在临床中推广应用。导致胃肠道不良反应的可能原因之一是pde4抑制剂特异性差,从而中度选择性地抑制了整个pde家族。如cilomilast对pde4的ki=92nm,仅是pde1、2、3、5的ki的500到1000倍。因此使用较高剂量cilomilast会与其他pde家族成员发生作用从而产生副作用。事实上,大多数pde4抑制剂,在高剂量时产生呕吐的副作用是普遍现象。roflumilast虽然已经通过美国fda批准上市用于治疗copd,降低肺部的炎症、抵抗氧
化应激、有效的缓解肺部的纤维化、增强粘膜的清除能力以及气道的重塑等等。但是也有不良反应,主要表现为腹泻、体重下降、恶心、心房纤颤及精神方面疾病的加重(如失眠、焦虑、抑郁)等。
5.针对上述问题已经开发多种新型pde4选择性抑制剂,如北卡罗来纳大学柯衡明开发的zl-n-91:
[0006][0007]
其ic
50
达到18nm,国内外已经尝试其用于治疗肺部疾病,如copd乃至肺癌和前列腺癌,取得了良好的效果。在进一步扩展该pde4抑制剂治疗pde4相关疾病的过程中,其对于其他癌症,例如胶质瘤是否有效,尚无任何研究验证。
技术实现要素:
[0008]
发明人在前期pde4抑制剂zl-n-91治疗肺部疾病和恶性实体瘤的基础上,尝试将用于治疗胶质瘤。体外细胞学实验表明本发明所述磷酸二酯酶4抑制剂zl-n-91可以显著抑制胶质瘤细胞的增殖,使其周期受阻并诱导细胞凋亡。体内皮下瘤模型表明zl-n-91可显著抑制肿瘤增长,预示该磷酸二酯酶4抑制剂zl-n-91有望成为抗胶质瘤增殖研究的重要靶点,为制备抗胶质瘤增殖药物提供了基础,具有良好的开发应用前景。
[0009]
一方面,本发明提供了zl-n-91在制备治疗实体瘤的药物中的应用。
[0010]
进一步地,所述实体瘤为胶质瘤。
[0011]
进一步地,所述胶质瘤包括胶质母细胞瘤。
[0012]
进一步地,所述药物抑制胶质瘤增殖。
[0013]
进一步地,所述药物为口服、注射或雾化剂型。
[0014]
另一方面,本发明提供了一种治疗胶质瘤的药物组合物,其包含zl-n-91作为唯一活性成分。
[0015]
进一步地,所述胶质瘤包括胶质母细胞瘤。
[0016]
另一方面,本发明提供了使用zl-n-91抑制胶质瘤增殖的方法。
[0017]
进一步地,所述胶质瘤包括胶质母细胞瘤。
[0018]
进一步地,所述胶质瘤细胞为u87、snb19和u251细胞。
[0019]
进一步地,所述体内动物学实验使用胶质瘤皮下荷瘤模型。
[0020]
本技术中所述的zl-n-91的化学结构已经公开,本领域技术人员可以参考现有技术文献(如ruihong ma,bin-yan yang,chang-you wu.a selective phosphodiesterase 4(pde4)inhibitor zl-n-91suppresses il-17production by human memory th17 cells.international immunopharmacology,2008,8(10):1408-1417.)和有机化学领域常规技术使用合成、购买、申请赠予等方式获取适合纯度的zl-n-91。
[0021]
本技术中所述的胶质瘤包括星形细胞来源、少突细胞来源、混合性、室管膜来源、
脉络丛来源、其他神经上皮来源、神经元及混合来源的,各种恶性程度/分期的胶质瘤。
[0022]
本发明可采用的剂型包括但不限于片剂、胶囊剂、口服液、注射液、粉针剂、雾化液等,除常用的口服、注射、雾化剂型外,本领域技术人员也可以根据需要和药剂领域常识设计或选用其他剂型。
[0023]
根据剂型的需要和药剂学常识,所制备的药物中可以包含各种药学可接受的辅料、赋形剂,包括但不限于包衣材料、溶剂、增溶剂、粘合剂、稳定剂、抗氧化剂、ph调节剂、矫味剂等。
[0024]
本发明要求保护的技术方案中不排斥使用其他已知的治疗胶质瘤的中西药物/疗法,这些药物包括但不限于化学化疗药物、生物靶向药物、放射治疗、免疫治疗、干细胞治疗,zl-n-91可以与这些药物制备于同一药物组合物中或者以单独药物的形式联合使用。
[0025]
本发明所述的选择性pde4抑制剂zl-n-91,可以显著抑制胶质瘤的增殖,预示该磷酸二酯酶4抑制剂zl-n-91有望成为抗胶质瘤研究的重要靶点,为制备抗胶质瘤增殖药物提供了基础,具有良好的开发应用前景。zl-n-91对pde4b和pde4d的抑制剂强度是其他pde家族成员的5000倍以上。相比其他pde4抑制剂,该化合物对pde4b和pde4d具有更高的选择性,特异性强,产生的呕吐等副作用小,扩展用于胶质瘤治疗时具有良好的临床适应性和安全性。
附图说明
[0026]
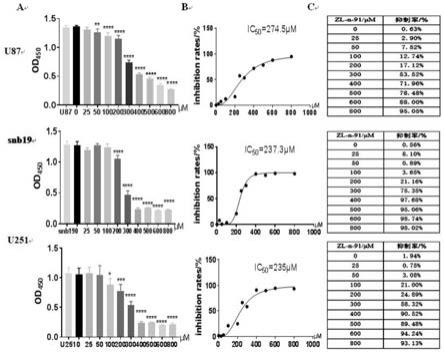
图1是zl-n-91对胶质瘤细胞的增殖抑制作用(a)不同浓度的zl-n-91处理u87、snb19、u251细胞48h后,细胞增殖结果图;(b)不同浓度的zl-n-91处理后,对u87、snb19、u251细胞抑制率的影响;(c)不同浓度的zl-n-91所对应的u87、snb19、u251的抑制率情况。所有数据均用平均值
±
标准偏差表示。(n=3),*p<0.05,**p<0.01,***p<0.001and****p<0.0001均与溶剂对照组0μm组相比。
[0027]
图2是zl-n-91对胶质瘤细胞周期分布的影响(a)不同浓度的zl-n-91处理u87、snb19、u251细胞24h后的细胞周期流式检测图;(b)不同浓度的zl-n-91处理后,u87、snb19、u251中周期各个阶段的百分比。所有数据均用平均值
±
标准偏差表示。(n=3),*p<0.05,**p<0.01,***p<0.001and****p<0.0001均与溶剂对照组相比。
[0028]
图3是zl-n-91诱导胶质瘤细胞凋亡情况(a)不同浓度的zl-n-91处理u87、snb19、u251细胞48h后的细胞凋亡流式检测图;(b)不同浓度的zl-n-91处理后,u87、snb19、u251细胞中,不同组别的总凋亡率。所有数据均用平均值
±
标准偏差表示。(n=3),*p<0.05,**p<0.01,***p<0.001and****p<0.0001均与溶剂对照组相比。
[0029]
图4是zl-n-91抑制裸鼠胶质瘤皮下瘤的生长情况(a)给药治疗后裸鼠体重变化图;(b)给药治疗后裸鼠肿瘤体积变化图;(c)肿瘤重量图;(d)肿瘤体积大小图。所有数据均用平均值
±
标准偏差表示。(n=5),*p<0.05,**p<0.01,均与溶剂对照组相比。
具体实施方式
[0030]
根据下述实施例,可以更好地理解本发明。然而,本领域的技术人员容易理解,实施例所描述的内容仅用于说明本发明,而不应当也不会限制权利要求书中所详细描述的本发明。
[0031]
实施例1:cck8法检测zl-n-91对胶质瘤细胞增殖抑制的影响。
[0032]
1)取对数生长期的胶质瘤细胞u87、snb19、u251,制备单细胞悬液。按每孔100μl细胞悬液(含2~3
×
103个细胞)接种于96孔板中,共分为9组:细胞完全对照组,溶剂对照组0μm,25μm、50μm、100μm、200μm、250μm、300μm、400μm、500μm、600μm、800μm,每组3个副孔;
[0033]
2)铺板后24h待细胞完全贴壁后,各组分别加入不同浓度的zl-n-91,将细胞继续培养48h;
[0034]
3)向每孔加入10ul cck-8溶液,避免产生气泡;
[0035]
4)将细胞继续孵育1-2h,将培养板取出,用酶标仪测定在450nm处的测细胞吸光度。并计算细胞增殖率和细胞抑制率,采用graphpad 7.0软件计算ic50结果。细胞增殖率(%)=(od450实验组-od450本底)/(od450溶剂对照组-od450本底)
×
100%;细胞抑制率(%)=1-细胞增殖率(%)
[0036]
结果如图1所示:随着zl-n-91浓度的升高,胶质瘤细胞u87、snb19、u251的抑制能力显著性增强。
[0037]
实施例2:流式细胞术检测zl-n-91对胶质瘤细胞周期分布的影响
[0038]
1)取对数生长期的u87、snb19、u251细胞,用无血清的基础培养基重悬,以2*105个/ml接种于6孔培养板,放在培养箱培养,饥饿处理24h;
[0039]
2)24h后,分别加入血清和实验药物浓度zl-n-91(150μm,200μm),同时设溶剂对照组,将细胞继续培养24h;
[0040]
3)24h后收集细胞,预冷pbs洗涤2次,用pbs制备成1
×
106个/ml的细胞悬液,加入1ml 70%的无水乙醇,置于4℃或者-20℃固定24h以上;
[0041]
4)离心,冷pbs洗涤2次,按试剂盒说明书加入500μl pe染色,轻柔的涡旋细胞,室温避光孵育15min,在1h内上机检测,用modifit lt5.0软件进行细胞周期分析。
[0042]
结果如图2所示:药物处理细胞生长周期阻滞在g0/g1时期,且药物浓度越高阻滞越显著,处于s时期分裂的细胞均有不同程度的下降。
[0043]
实验例3:流式细胞术检测zl-n-91对胶质瘤细胞凋亡的诱导作用
[0044]
1)取对数生长期的u87、snb19、u251胶质瘤细胞,以1.5~2*105个/ml接种于6孔培养板;
[0045]
2)铺板后24h待细胞完全贴壁后,分别加入实验浓度zl-n-91(150μm,200μm、300μm),同时设溶剂对照组,将细胞继续培养48h;
[0046]
3)48h后收获细胞,预冷pbs洗涤2次,用1
×
binding buffer制备成1
×
106个/ml的细胞悬液,取100μl于流式管中,按试剂盒说明书加入5ul 7-aad和5ul pe染色,轻柔的涡旋细胞,室温避光孵育15min,再200ul 1
×
binding buffer于管中,1h内进行流式细胞检测,用flow jo v10分析软件分析结果。
[0047]
结果如图3所示:zl-n-91诱导u87、snb19、u251胶质瘤细胞凋亡且呈剂量依赖性。
[0048]
实验例4:zl-n-91抑制裸鼠胶质瘤皮下瘤的生长情况
[0049]
为了在体内研究zl-n-91对胶质瘤u87细胞增殖抑制作用,我们将u87细胞种植于6周龄裸鼠皮下。待肿瘤体积长至100mm3左右,将荷瘤小鼠随机分为两组:溶剂对照组和给药组(5mg/kg),每天灌胃治疗,每两天称量小鼠体重、测量肿瘤体积。
[0050]
结果如图4所示:给药组和对照组相比体重没有明显差异,给药24天开始,给药组
小鼠肿瘤体积明显小于对照组。剥离肿瘤,称重,给药组肿瘤重量(182.6
±
109.4mg)明显小于对照组肿瘤重量(813.6
±
511.6mg)。这些结果表明,zl-n-91不但能显著抑制胶质瘤的增长,而且对小鼠副作用较小。
[0051]
以上研究结果表明,本发明所采用的磷酸二酯酶4抑制剂zl-n-91能抑制胶质瘤细胞增殖,具有良好的抗肿瘤效果。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1