一种预防或治疗疟疾的青蒿素类增强型药物组合物的制作方法
本发明属于生物医药领域,涉及一种预防或治疗疟疾的青蒿素类增强型药物组合物,具体涉及双氢青蒿素与促进pfemp1表达的试剂的联合应用在制备治疗疟疾的药物组合物中的应用。
背景技术:
疟疾是严重威胁人类健康和生命安全的重大传染病,在全世界91个国家和地区传播流行,为世界三大公共卫生问题之一。据who2017年11月发布的“世界疟疾报告”,2016年全球约有2.16亿疟疾病例,44.5万人死于重症疟疾。疟疾高风险人群包括婴儿、5岁以下儿童、孕妇及免疫力低下人群,三分之二以上的疟疾死亡病例发生在5岁以下儿童。虽2010-2015年全球5岁以下儿童疟疾死亡率下降了29%,但每2分钟仍有1名儿童死于重症疟疾。
恶性疟原虫(plasmodiumfalciparum)是致病性最强的疟原虫,在人体内分红外期和红内期2个发育阶段,红内期是主要的致病阶段,疟疾的临床症状多发生在此期,自然感染后的获得性免疫保护也发生在这个阶段。通过杀死或减少致病的红内期疟原虫可有效减少疟疾病发率或死亡率,因此,针对疟疾红内期的基础研究和疫苗研发始终是抗疟研究领域的研究热点。
既往研究认为,青蒿素类药物可选择性杀灭红内期疟原虫,其作用主要是干预疟原虫的膜系结构,影响表膜及线粒体功能,阻断宿主红细胞为其提供足够的营养,从而达到抗疟目的。青蒿素类药物对疟原虫配子体也具有杀灭作用,能够快速杀灭早期配子体,抑制各期配子体,对未成熟配子体可起到中断其发育过程的作用。
双氢青蒿素(dihydroartemisinin,dha)对疟原虫有快速高效的杀灭作用,其可以杀死红细胞内早期疟原虫,从而阻止疟原虫发展到更成熟的阶段。
恶性疟原虫红细胞膜蛋白1(pfemp1,plasmodiumfalciparumerythrocytemembraneprotein1)是一个相对分子质量在200000-400000之间的蛋白家族,其分子包含1个氨基末端区段(n-terminalsegment,nts)、若干个duffy结合样结构域(duffybindinglikedomain,dbl)、若干个富含半胱氨酸间隔区、1个跨膜区、1个c2结构域和1个c-末端区段。pfemp1由恶性疟原虫的var基因编码,1个恶性疟原虫染色体基因组有多达60个var基因拷贝,但每个生长周期仅有1个var基因最终获得表达,var基因可分为a、b、c3大群,众多的var基因导致pfemp1的高度变异。寄生恶性疟原虫的红细胞与正常红细胞之间会发生黏附,产生所谓的“玫瑰花结(rosetting)”现象,这是造成患者微血管阻塞进而导致重症疟疾(如脑型疟)的一个重要原因,pfemp1作为疟原虫的一个配体参与了“玫瑰花结”的形成。pfemp1能与血液中多个蛋白以及红细胞膜上的一些受体结合,如纤维蛋白原、白蛋白、血型a和b抗原、硫酸乙酰肝素和补体受体1等,从而使细胞间发生黏附,pfemp1氨基端的nts-dbl1α片段在“玫瑰花结”形成中起关键作用。研究显示,能够瓦解“玫瑰花结”的抗体与抗重症疟疾具有相关性,发生重症疟疾的患者体内缺乏瓦解“玫瑰花结”的抗体,而nts-dbl1α片段所激发的抗体就具有这种瓦解“玫瑰花结”的能力,且对寄生红细胞具有调理作用。
至今还未见双氢青蒿素与pfemp1蛋白在治疗疟疾中的联合作用。
技术实现要素:
本发明利用var基因过表达虫株8d5,该虫株是敲除3d7虫株pfsetvs基因的虫株,其可做为pfemp1过表达虫株。本发明利用该虫株检测了dha的杀伤作用:dha处理后,var基因过表达株ic50较野生型降低,说明pfemp1过表达可增强dha的抗疟效果。基于此,本发明的目的在于提供一种包括促进pfemp1表达的试剂、双氢青蒿素的治疗疟疾的药物组合物。
为了实现上述目的,本发明采用了如下技术方案:
根据本发明的一个方面,本发明提供了一种预防或治疗疟疾的药物组合物,所述药物组合物包括促进pfemp1表达的试剂、青蒿素或其衍生物。
进一步,本发明的药物组合物还包括药学上可接受的载体。作为有效成分的促进pfemp1表达的试剂和青蒿素或其衍生物与药学上可接受的载体按照常规制备工艺制备成本发明的药物组合物。
根据本发明,药学上可接受的载体可以是稀释剂、粘合剂、崩解剂、稳定剂、甜味剂、调味剂、增味剂、着色剂、助流剂和润滑剂中的一种或多种。
稀释剂,包括但不限于蔗糖、甘露醇、木糖醇、安赛蜜、阿斯巴甜、葡萄糖、果糖、糖精、糖精钠、山梨醇及其混合物都可以使用。
本发明的稀释剂还可以具有其他功能,如作为甜味剂。
粘合剂包括但不限于纤维素、烷基纤维素例如甲基纤维素、羟烷基纤维素例如羟丙基纤维素、低取代的羟丙基纤维素和羟丙基甲基纤维素、羧甲基纤维素钠或其混合物、预凝胶化玉米淀粉或聚乙烯吡咯烷酮。可以使用微晶纤维素,例如可以以商品名ph301购自asahikasei的微晶纤维素。
崩解剂,包括但不限于交联聚维酮、乙醇酸淀粉钠、淀粉例如玉米淀粉和干淀粉、交联羧甲基纤维素钠和纤维素产品例如微晶纤维素、超细(microfine)纤维素、低取代的羟丙基纤维素等可以单独使用或混合使用。
稳定剂,包括但不限于三代磷酸钠、无水碳酸钠、甘氨酸、柠檬酸等或其混合物。
甜味剂,包括但不限于糖例如果糖、葡萄糖、蔗糖、糖醇如甘露醇、山梨醇或其混合物,以及人工甜味剂如糖精钠、环氨酸钠和阿斯巴甜。
调味剂指能够增加混合物味道的物质或其混合物。代表性的调味剂包括但不限于桔子香料、香蕉香料、柠檬薄荷香料、草莓香料、葡萄香料和奶油香料。
增味剂包括但不限于氯化钠、甘氨酸、柠檬酸、酒石酸等及其混合物。
着色剂包括但不限于二氧化钛颜料、色淀颜料和二氧化铁颜料。
助流剂包括但不限于胶体二氧化硅、滑石粉和表面活性剂,其中表面活性剂单独使用或作为和其他助流剂的混合物使用。也可以使用胶体二氧化硅和一种或多种表面活性剂的混合物。
润滑剂包括但不限于硬脂酸镁、硬脂酸钙、硬脂酸锌、氧化镁、富马酸硬脂酸钠、氢化植物油、十二烷基硬脂酸钠、硬脂酸、玉米淀粉、胶体二氧化硅、滑石及其混合物。
本发明的药物组合物可根据需要制备成各种剂型。包括但不限于,经皮、粘膜、鼻、口颊、舌下或经口使用的片剂、溶液剂、颗粒剂、贴剂、膏剂、胶囊剂、气雾剂或栓剂。
本发明的药物组合物的施用途径不受限制,只要它能发挥期望的治疗效果或预防效果即可,包括但不限于静脉内,腹膜内,眼内,动脉内,肺内,口服,小泡内,肌肉内,气管内,皮下的,通过皮肤,通过胸膜,局部的,吸入,通过粘膜,皮肤,肠胃,关节内,心室内,直肠,阴道,颅骨内,尿道内,肝内,瘤内。在某些情况下,可以系统地给药。在某些情况下是局部地给药。
本发明的药物组合物的剂量不受限制,只要获得期望的治疗效果或者预防效果即可,可以依据症状、性别、年龄等来恰当的确定。本发明的治疗药物或预防药物的剂量可以使用例如对疾病的治疗效果或者预防效果作为指标来确定。
本发明的药物组合物对于疟疾的治疗是药物组合物中的两种有效成分促进pfemp1表达的试剂、青蒿素或其衍生物的联合应用治疗。可以分别单独配制和使用促进pfemp1表达的试剂、青蒿素或其衍生物,也可以通过在单一配制物中施用促进pfemp1表达的试剂、青蒿素或其衍生物可达到联合治疗的目的。通过联合治疗也涵盖其他组合,例如,可连同包含第三种试剂的单独配制物一起配制和施用促进pfemp1表达的试剂、青蒿素或其衍生物。尽管在联合治疗中两种有效成分可同时施用,但是不需要一定如此。例如,第一种有效成分的施用可以在第二种活性成分的施用之前数分钟、数小时、数天或数周。因此,两种活性成分可在相隔数分钟内、或者在相隔1、2、3、6、9、12、15、18、或24小时、或者相隔1、2、3、4、5、6、7、8、9、10、12、14天、或者相隔2、3、4、5、6、7、8、9、或10周施用。在一些情况下,更久的间隔是可能的。尽管在一些情况下,在患者的体内可同时存在联合治疗使用的两种有效成分,但是不需要一定如此。
将本发明的药物组合物的给药至个体的时间为约1周至约2周的期间。在治疗期间可间歇给药或持续给药。
本发明的药物组合物可以在一天中任意时间与食物一起施用、在一天中任意时间不与食物一起施用、在空腹一晚之后与食物(例如早餐)一起施用。
本发明的药物组合物可以在每天一次、一天两次、一天三次、一天四次、一天五次或一天六次施用。
根据本发明的另一个方面,本发明提供了pfemp1在制备增强青蒿素或其衍生物的抗疟效果的药物中的应用。
进一步,所述药物是前面所述的药物组合物。
根据本发明的又一个方面,本发明提供了青蒿素或其衍生物在制备前面所述的药物组合物中的应用。
根据本发明的又一个方面,本发明提供了pfemp1和青蒿素或其衍生物在制备预防或治疗疟疾的药物中的应用。
进一步,所述药物是前面所述的药物组合物。
根据本发明的又一个方面,本发明提供了一种增强青蒿素或其衍生物的抗疟效果的药物,所述药物包括促进pfemp1表达的试剂。
根据本发明的又一个方面,本发明提供了一种预防或治疗疟疾的方法,所述方法包括向有需要者施用促进pfemp1表达的试剂和青蒿素或其衍生物。
本发明的青蒿素衍生物包括青蒿琥酯、蒿甲醚、蒿乙醚、双氢青蒿素。在本发明的具体实施方案中,所述青蒿素衍生物是指双氢青蒿素。
本发明的促进pfemp1表达的试剂包括pfemp1基因、pfemp1过表达载体、pfemp1蛋白、促进型mirna、促进型转录调控因子、或促进型靶向小分子化合物、抑制var基因启动子甲基化的试剂。
进一步,抑制var基因启动子甲基化的试剂包括抑制组蛋白赖氨酸甲基化酶的试剂。
优选地,所述组蛋白赖氨酸甲基化酶是pfsetvs。
抑制pfsetvs的试剂包括抑制pfsetvs基因mrna的试剂、抑制pfsetvs蛋白的试剂。所述抑制pfsetvs基因mrna的试剂包括抑制mrna稳定性的试剂、抑制mrna翻译活性的试剂。所述抑制pfsetvs蛋白的试剂包括抑制pfsetvs蛋白稳定性的试剂、抑制pfsetvs蛋白活性的试剂、抑制pfsetvs蛋白功能的试剂。
进一步,抑制pfsetvs基因mrna的试剂包括针对pfsetvs基因mrna的双链核糖核酸;抑制pfsetvs蛋白功能的试剂包括抑制tmed2蛋白功能的抗体。所述抗体可以是多克隆抗体,或是单克隆抗体。
所述针对pfsetvs基因mrna的双链核糖核酸可以是sirna。为了确保pfsetvs基因能够被高效剔除或沉默,根据pfsetvs基因的mrna序列设计sirna特异性片段。sirna的设计根据已发表的通用设计原则(elbashiret.al2001,schwarzet.al2003,khvorovaet.al2003,reynoldset.al2004,hsiehet.al2004,ui-teiet.al2004),通过在线工具完成设计,该在线工具为:sirnaselectionprogramofwhiteheadinstitute(bingbingyuanet.al2004,http://jura.wi.mit.edu/bioc/sirnaext/)和block-ittmrnaidesignerofinvitrogen(winnerofthe2004frost&sullivanexcellenceinresearchaward,https://rnaidesigner.invitrogen.com/sirna/)。为了进一步提高sirna片断的有效性,综合两个在线设计工具的优点来设计用于筛选的sirna片断。最后,通过同源性比对(ncbiblast)来过滤sirna序列,以提高sirna片断的特异性并减少rnai干扰的脱靶效应。
术语“治疗”指减少或减轻受治疗者的症状,防止症状的恶化或发展,或防止疾病的发展。对于给定的受治疗者,症状的改善、恶化、恢复或发展可以由本领域技术人员通常采用的主或客观测量方法来确定。因此,有效的治疗应该包括对已有疾病的治疗、通过减缓疾病的发展或使其停止来控制疾病、预防疾病的出现、降低症状数量或严重程度或其组合。使用一或多个统计上显著的标准,治疗效果可以在有对照的研究中表现出来。
术语“预防”的意思是指某种不具有某种疾病之前,就施加试剂对该种疾病进行预防。
本发明优点和有益效果:
本发明的药物组合物组分简单,毒性低,疗效确切,符合现代医学研究理论。本发明的药物组合物中的两种有效成分在防治疟疾中具有明显的协同增效作用。
附图说明
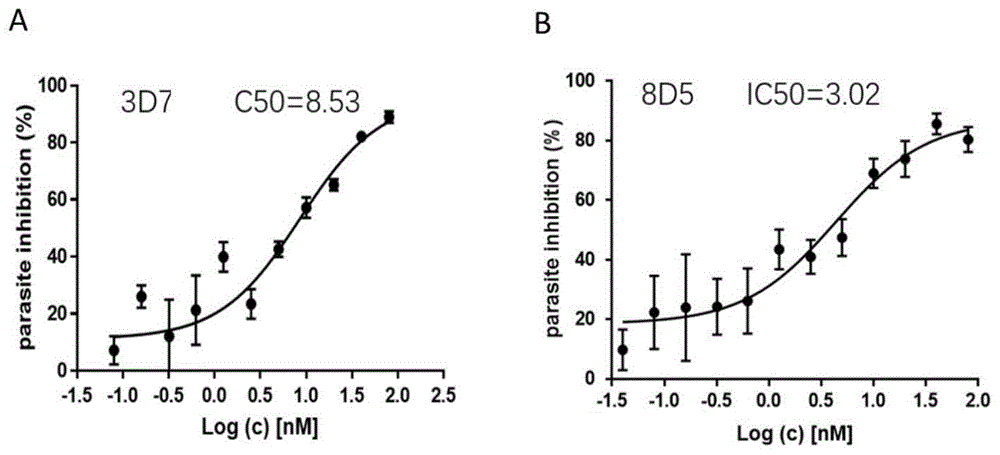
图1显示dha抗疟的ic50检测结果图。
具体实施方式
为了使本领域的技术人员更好的理解本发明的技术方案,下面结合附图及具体实施方式对本发明所述技术方案作进一步的详细说明。
实施例1pfemp1表达对dha的抗疟效果的影响
1、材料
恶性疟原虫国际标准株3d7由吉林大学人兽共患病研究所人兽共患病教育部重点实验室陈启军教授馈赠,本实验室传代保种。
恶性疟原虫国际标准株3d7敲除pfsetvs基因后的虫株,命名为8d5,由中科院上海巴斯德研究所江陆斌实验室馈赠(该虫株的构建过程参见文献:pfsetvsmethylationofhistoneh3k36repressesvirulencegenesinplasmodiumfalciparum.nature.2013jul11;499(7457):223-7),本实验室传代保种。江陆斌研究组成功地找到了控制var基因沉默的关键因子pfsetvs。pfsetvs作为果蝇ash1的同源蛋白,是一种组蛋白赖氨酸甲基化酶。研究人员证明,pfsetvs可在var基因的启动子区域产生一类特异性的组蛋白修饰h3k36me3,进而抑制var基因家族的转录。研究首次证明了真核生物中组蛋白修饰h3k36me3对基因沉默的介导作用;研究中通过敲除pfsetvs基因产生的可表达全部pfemp1蛋白的转基因恶性疟原虫株8d5,即其可做为pfemp1过表达虫株。本申请利用该虫株检测了dha的杀伤作用。
2、步骤
2.1虫株培养
根据trager和jensen建立的方法(参见文献:tragerw,jensenjb.humanmalariaparasitesincontinuousculture[j].jparasitol,1976,2005,91(3):484),采用0.5%albumaxⅱ替代人血清,配置1l完全培养基:1640粉末1袋,albumaxⅱ5g,l-谷氨酞胺0.3g,葡萄糖2g,hepes5.98g,次黄嘌呤0.025g,庆大霉素0.2g;将上述试剂溶于1l三蒸水中,搅拌均匀后加入碳酸氢钠2.56g混匀,将培养基经灭菌滤器过滤后分装使用。使用人o型血红细胞调整压积比在2%;将培养皿置于三气培养箱(环境5%co2,5%o2,90%n2,湿度95%,温度37℃)中培养。
2.2同步化
根据谷利维等(参见文献:谷利维,李玉洁,蔡维艳,等.双氢青蒿素对体外疟原虫感染人红细胞膜通透性的影响研究)的研究,使用5%d-山梨醇溶液可以较好的选择疟原虫实现同步化。涂薄血膜片观察,当虫株感染率为5%-10%且环状体期占绝大多数(>60%)时进行环期同步化操作。将培养皿中培养基及红细胞混匀,1900r·min-1室温离心2min,吸弃上清。加入37℃预热的8ml5%d-山梨醇溶液,混匀,37℃孵育10min,1900r·min-1室温离心2min,吸弃上清。加入适当体积的完全培养基,使用新鲜人o型血红细胞调整压积比在2%,置于三气培养箱中继续恒温培养。
2.3分组与加药
连续进行3次同步化处理后进行加药处理。双氢青蒿素以二甲基亚砜(dmso)配制成浓度为1μmol·l-1储存液(dmso浓度≤0.1%),-20℃避光保存,加药前稀释至所需浓度。在末次同步化6h后加药,每48h更换培养基,每组4个复孔。
2.4ic50计算
方法:于状体期恶性疟原虫(疟原虫感染红细胞后4-8小时)加药,培养至约72小时(至疟原虫为滋养体期),轻轻弃去100μl上清,加入100μl/孔裂解液(含荧光染料sybrgreen1),混匀。室温避光孵育1.5-2h,多功能酶标仪检测ex=485nm;em=525nm。计算生长抑制率:percentageinhibitiongrowth=(1-(awell–aneg/apos–aneg))x100),采用非线性回归分析方法统计ic50值。
结果如图1所示,dha处理后,8d5虫株ic50较3d7虫株降低,说明pfemp1过表达可增强dha的抗疟效果。
- 还没有人留言评论。精彩留言会获得点赞!