一种阿莫西林克拉维酸钾干混悬剂及其制备方法与流程
1.本发明涉及药物制剂领域,具体涉及一种阿莫西林克拉维酸钾干混悬剂的处方组成及其制备工。
背景技术:
2.阿莫西林化学名称为:(2s,5r,6r)-3,3-二甲基-6-[(r)-(-)-2-氨基-2-(4-羟基苯基)乙酰氨基]-7-氧代-4-硫杂-1-氮杂双环[3.2.0]庚烷-2-甲酸三水合物,其化学结构式为:
[0003][0004]
克拉维酸钾化学名称为:(z)-(2r,5r)-3-(2-羟亚乙基)-7-氧代-4-氧杂-1-氮杂双环[3.2.0]庚烷-2-羧酸钾,其化学结构式为:
[0005][0006]
阿莫西林为白色或类白色结晶性粉末,在水中微溶,在乙醇中几乎不溶,在各ph值溶出介质中的溶解度(37℃):ph1.2:30.7mg/ml、ph4.0:3.8mg/ml、ph 6.8:4.9mg/ml、水:3.6mg/ml,可见阿莫西林溶解度随着溶液ph值的增大呈下降趋势,溶液ph值增大到4.0以后阿莫西林溶解度基本保持不变。
[0007]
克拉维酸钾为白色至微黄色结晶性粉末,微臭;极易引湿,在水中极易溶解,在甲醇中易溶,在乙醇中微溶,在乙醚中不溶,在各ph值溶出介质中的溶解度(37℃):ph1.2:2.5g/ml、ph4.0:2.5g/ml、ph 6.8:2.5g/ml、水:2.5g/ml,不具有ph依赖性。
[0008]
阿莫西林克拉维酸钾干混悬剂,适应症为用于怀疑由产β-内酰胺酶的耐阿莫西林的细菌造成所致感染的短期治疗。细菌耐药性主要是由于细菌可产生β-内酰胺酶,该酶在抗生素作用于病原菌前即可将抗生素破坏。
[0009]
阿莫西林为半合成的广谱抗菌素,对许多革兰阳性菌和革兰阴性菌发生作用。然而β-内酰胺酶会降低阿莫西林的作用,因此单在阿莫西林发挥作用的菌谱中不包括产β-内酰胺酶的细菌。克拉维酸为一种β-内酰胺,结构与青霉素相似,对存在于微生物中的耐青霉素及头孢菌素常见β-内酰胺酶有抑制作用。特别是克拉维酸对有重要临床意义的由质粒介导的,可引起交叉耐药的β-内酰胺酶有较强的抑制作用。因此,克拉维酸的存在可以保护阿莫西林免受β-内酰胺酶的降解作用,进而扩大阿莫西林的抗菌谱。其中包括在通常情况下对阿莫西林和其它青霉素及头孢菌素耐药的许多细菌。所以本品具有显著的广谱抗菌作
用,同时又是一个β-内酰胺酶抑制剂。
[0010]
目前,阿莫西林克拉维酸钾复方制剂以口服固体制剂为主,包括片剂、胶囊剂和干混悬剂。由于片剂和胶囊剂不利于儿童、老年人和吞咽困难患者服用,因此干混悬剂就体现出了强有力的临床顺应性,可分剂量给药、服用方便、溶出速率高。但阿莫西林、克拉维酸钾在酸碱介质中稳定性均较差,患者服用后易出现不良反应,因此保证产品质量稳定性是该制剂开发的难点。
[0011]
专利cn103127099a公开了一种阿莫西林克拉维酸钾干混悬剂(4:1)及其生产工艺,由阿莫西林、克拉维酸钾、羟丙基甲基纤维素等混合而成,但其制备工艺复杂,需将克拉维酸钾和磷脂溶于氯仿中,加入二氧化硅,搅拌,在40℃以下减压蒸干氯仿,再过筛与其他物料混合,制得。
[0012]
专利cn110859801a公开了一种阿莫西林克拉维酸钾干混悬剂及其制备方法,所述阿莫西林克拉维酸钾干混悬剂由如下份数的原辅料组成:阿莫西林16-18份,阿莫西林克拉维酸钾混合粉10-12份,蔗糖70-85份,黄原胶1-9份,羟丙甲纤维素2-10份,阿司帕坦2-3份,二氧化硅1-12份,果奶香精1-2份;其中阿莫西林克拉维酸钾混合粉中阿莫西林、克拉维酸钾质量比为2:1。本品采用粉末直接灌装。但该专利只比较了ph5.0缓冲液中的溶出情况且药品单剂量重量大约1.2g/袋,成本高。
技术实现要素:
[0013]
基于现有技术的不足,本发明提供一种阿莫西林克拉维酸钾干混悬剂的处方及其制备方法。
[0014]
本发明所述阿莫西林克拉维酸钾干混悬剂含有以下组分:阿莫西林、克拉维酸钾、矫味剂、稀释剂、增稠剂、稳定剂、助悬剂、ph调节剂、芳香剂。
[0015]
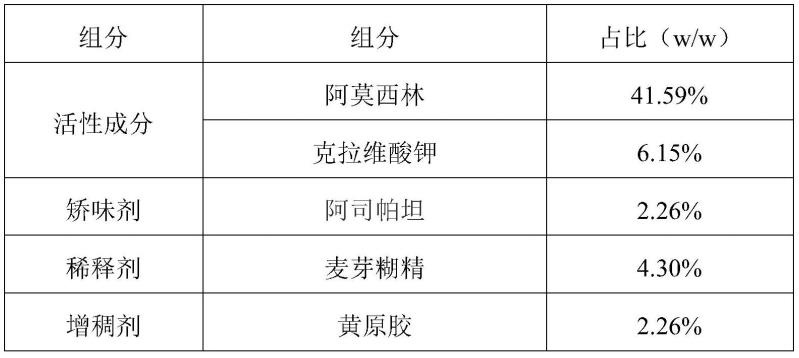
具体的,所述阿莫西林克拉维酸钾干混悬剂含有以下组分:
[0016]
阿莫西林30%~60%、克拉维酸钾5%~15%、矫味剂1%~5%、稀释剂3%~10%、增稠剂1%~5%、稳定剂10%~25%、助悬剂10%~30%、ph调节剂0.1%~0.5%、芳香剂0.01%~10%;
[0017]
优选的,所述阿莫西林克拉维酸钾干混悬剂含有以下组分:
[0018]
阿莫西林42%~56%、克拉维酸钾6%~8%、矫味剂2%~3%、稀释剂4%~6%、增稠剂2%~3%、稳定剂14%~18%、助悬剂12%~22%、ph调节剂0.1%~0.2%、芳香剂0.02%~10%。
[0019]
上述阿莫西林克拉维酸钾干混悬剂中:
[0020]
矫味剂选自阿司帕坦、蔗糖、海藻酸钠、阿拉伯胶、明胶、甲基纤维素、羧甲基纤维素钠中的一种或多种;
[0021]
稀释剂选自麦芽糊精、淀粉、预胶化淀粉、乳糖、微晶纤维素、甘露醇、山梨醇中的一种或多种;
[0022]
助悬剂选自胶态二氧化硅、阿拉伯胶、海藻酸钠、琼脂、淀粉浆、羧甲基纤维素钠、羟丙基纤维素中的一种或多种;
[0023]
稳定剂为微晶纤维素-羧甲基纤维素钠;增稠剂选自黄原胶、海藻酸钠、琼脂、卡拉胶中的一种或多种;
[0024]
ph调节剂选自琥珀酸、柠檬酸、乳酸、酒石酸、富马酸、乙酸、盐酸、磷酸、苹果酸中的一种或多种;
[0025]
芳香剂选自薄荷香精、甜橙香精、覆盆子香精、柠檬香精、姜油香精中的一种或多种;
[0026]
优选的,所述矫味剂选自阿司帕坦、蔗糖、海藻酸钠中的一种或多种;
[0027]
所述稀释剂选自麦芽糊精、淀粉、乳糖、微晶纤维素中的一种或多种;
[0028]
所述助悬剂选自胶态二氧化硅、阿拉伯胶、羟丙基纤维素中的一种或多种;
[0029]
所述ph调节剂选自琥珀酸、柠檬酸、酒石酸、乳酸中的一种或多种;
[0030]
所述芳香剂为甜橙香精、覆盆子香精的混合。
[0031]
进一步优选的,所述矫味剂为阿司帕坦;
[0032]
所述稀释剂为麦芽糊精;
[0033]
所述助悬剂为胶态二氧化硅;
[0034]
所述ph调节剂为琥珀酸;
[0035]
所述甜橙香精、覆盆子香精的比例为1:0.1-5;更优选的,所述甜橙香精、覆盆子香精的比例为1:0.5-3。
[0036]
本发明还提供了上述阿莫西林克拉维酸钾干混悬剂的制备工艺,所述制备工艺主要包括以下步骤:
[0037]
步骤1:将ph调节剂与增稠剂混合,加入矫味剂、稀释剂、稳定剂混合,得混合粉ⅰ;将阿莫西林、克拉维酸钾与助悬剂混合,得混合粉ⅱ;
[0038]
步骤2::将混合粉ⅰ和ⅱ混合后,加入芳香剂混合,即得。
[0039]
具体的,所述制备方法包括以下步骤:
[0040]
步骤1、烘干:黄原胶、麦芽糊精(先过80目筛)、阿司帕坦、微晶纤维素-羧甲基纤维素钠,105℃烘干4小时,控制辅料水分≤2.0%;
[0041]
步骤2、混合过筛:环境温度18~26℃,环境湿度≤35%,先将琥珀酸与黄原胶进行混合过80目筛,再加入阿司帕坦进行混合过80目筛,再加入麦芽糊精混合过80目筛,再加入微晶纤维素-羧甲基纤维素钠混合过80目筛,得混合粉ⅰ;将阿莫西林、克拉维酸钾与胶态二氧化硅混合过80目筛,得混合粉ⅱ;最后将混合粉ⅰ和ⅱ混合过80目筛,混合均匀;
[0042]
步骤3、总混:将s2所得混粉与香精混合均匀;
[0043]
步骤4、检测混合粉含量,并计算理论装量
[0044]
步骤5、根据生产需求,进行混合粉多剂量装瓶或单剂量装复合袋,即得。
[0045]
与现有技术相比,本发明所制备的阿莫西林克拉维酸钾干混悬剂的溶出曲线、粒度分布、粉体学性质与原研产品相似,质量稳定性优于原研产品,且制备方法简单可行,适合大规模生产,满足市场需求。
具体实施方式
[0046]
下面结合实施例对本发明进一步描述,给出的实例仅为了阐述本发明,但并不为实施例所限制。
[0047]
实施例1
[0048][0049][0050]
制备方法:
[0051]
1、烘干:黄原胶、麦芽糊精(先过80目筛)、阿司帕坦、微晶纤维素-羧甲基纤维素钠,
[0052]
105℃烘干4小时,控制辅料水分≤2.0%;
[0053]
2、混合过筛:环境温度18~26℃,环境湿度≤35%,先将琥珀酸与黄原胶进行混合过80目筛,再加入阿司帕坦进行混合过80目筛,再加入麦芽糊精混合过80目筛,再加入微晶纤维素-羧甲基纤维素钠混合过80目筛,得混合粉ⅰ;将阿莫西林、克拉维酸钾与胶态二氧化硅混合过80目筛,得混合粉ⅱ;最后将混合粉ⅰ和ⅱ混合过80目筛,混合均匀;
[0054]
3、总混:将s2所得混粉与香精混合均匀;
[0055]
4、检测混合粉含量,并计算理论装量
[0056]
5、混合粉按14个剂量装玻璃瓶;单剂量装铝塑复合袋,即得。
[0057]
实施例2
[0058][0059]
制备方法:参考实施例1。
[0060]
实施例3
[0061][0062]
制备方法:参考实施例1。
[0063]
实施例4
[0064][0065][0066]
制备方法:参考实施例1。
[0067]
实施例5
[0068][0069]
制备方法:参考实施例1。
[0070]
实施例6
[0071][0072][0073]
制备方法:参考实施例1。
[0074]
实施例7
[0075]
[0076]
制备方法:参考实施例1。
[0077]
实施例8
[0078][0079][0080]
制备方法:参考实施例1。
[0081]
实施例9
[0082][0083]
制备方法:参考实施例1。
[0084]
实施例10
[0085][0086][0087]
制备方法:参考实施例1。
[0088]
实施例11
[0089][0090]
制备方法:参考实施例1。
[0091]
实施例12
[0092][0093]
[0094]
制备方法:参考实施例1。
[0095]
实施例13
[0096][0097]
制备方法:参考实施例1。
[0098]
实施例14
[0099]
[0100][0101]
制备方法:参考实施例1。
[0102]
验证实施例:
[0103]
一、质量、粒径分布、粉体学性质检测
[0104]
取实施例1~4制得的阿莫西林克拉维酸钾干混悬剂进行质量、粒径分布、粉体学性质检测,结果见表1、2.
[0105]
表1:实施例1~4阿莫西林克拉维酸钾干混悬剂与原研药质量检测结果
[0106][0107]
表2:实施例1~4阿莫西林克拉维酸钾干混悬剂与原研药质量检测结果
[0108][0109][0110]
注1:以水为溶出介质,30分钟的溶出量,限度为标示量的80%。
[0111]
由检测结果可以看出,按实施例1~4处方和工艺制备的产品,无论是外观性状、粒度分布、粉体学性质及产品的含量、溶出度、有关物质等质量指标均与原研制剂一致。
[0112]
二、稳定性考察
[0113]
为比较按本发明处方和工艺制备的产品与原研质量的一致性,本发明对按照实施例2处方及工艺制备的三批样品(批号分别为:180501、180502、180503)与原研制剂(批号:t84a,生产企业:葛兰素史克),进行了加速稳定性考察,考察条件:温度30℃,相对湿度:65%
±
5%。考察结果见表3、4。
[0114]
表3:阿莫西林克拉维酸钾干混悬剂加速稳定性试验结果
[0115][0116][0117]
表4:阿莫西林克拉维酸钾干混悬剂加速稳定性试验结果
[0118][0119]
由上表可以看出,实施例2所得阿莫西林克拉维酸钾干混悬剂及原研品在加速留样条件下,阿莫西林、克拉维酸钾含量、溶出度基本没有变化,有关物质及荧光物质无明显变化,总杂仅0.2%的增加。
[0120]
三、溶出曲线比较
[0121]
取实施例2阿莫西林克拉维酸钾干混悬剂(批号:180501)及原研品阿莫西林克拉维酸钾干混悬剂(批号:t84a),参照中国药典2015年版四部0931溶出度测定法第二法的试验装置,分别以水、ph1.2盐酸溶液、ph4.5醋酸盐缓冲液及ph6.8磷酸盐缓冲液为溶出介质,转速为每分钟75转,计算药物的累积溶出量,并绘制溶出曲线,结果见表5、6。
[0122]
表5:180501与t84a阿莫西林溶出曲线对比结果
[0123][0124]
表6:180501与t84a克拉维酸钾溶出曲线对比结果
[0125][0126][0127]
由溶出曲线数据可知,自制品及原研品,阿莫西林及克拉维酸钾在15分钟的溶出度均≥85%,因此与参比制剂在体外的溶出行为相似。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1