一种环烯醚萜苷化合物抗特发性肺纤维化的用途
1.本发明属于医药及保健品领域,具体涉及一种环烯醚萜苷化合物抗特发性肺纤维化的用途。
背景技术:
2.特发性肺纤维化(idiopathic pulmonary fibrosis,ipf)是一种病因不明的进行性加重的慢性致纤维化性间质性肺病,据统计特发性肺纤维化全球患病率为(2-29)/10万,多发于50岁以上的老年人。疾病进展具有不可预测性,约50%ipf患者在确诊后的2-3年内死亡,5年生存率低于30%,比大多数癌症的生存率都低。目前有数据表明,全球ipf的发病率已与胃癌、肝癌、睾丸癌和宫颈癌等多种恶性肿瘤的发病率相当。
3.临床上针对发病率高、病情严重、预后极差的肺纤维化的治疗选择有限。ipf治疗国际指南表明除了肺移植以外,尚无确切有效的治疗措施。常用药物包括糖皮质激素、免疫抑制剂、抗凝药物等。但这些药物对ipf治疗效果不明显。截至目前fda仅批准尼达尼布(nintedanib)和吡非尼酮(pirfenidone)两种口服药用于ipf的治疗,但前者存在高比率腹泻(62.4%),后者常见胃肠道副作用,且29.2%出现光敏性皮疹,以至在患者中存在较高的停药率。
4.可用药少、现有药物不良反应大、在研合成药物大多针对单一靶点等缺点迫使我们亟需寻找及开发一种治疗ipf更加安全有效的药物。
技术实现要素:
5.本发明的主要目的在于提供一种相比现有在研合成药更安全有效的治疗ipf的药物。具体地,本发明提供了一种提取自中药桅子的有效活性成分,京尼平1-β-d-龙胆双糖苷,其具有药理活性范围广,多靶点调控的特点,相比于在研药物能够更有效地治疗和/或缓解ipf。
6.在本发明的第一方面,提供了一种式i化合物,或其药学上可接受的盐、溶剂化物、光学纯异构体、立体异构体或其混合物的用途,用于制备a)肺成纤维细胞转分化的抑制剂;b)预防和/或治疗特发性肺纤维化的药物;
[0007][0008]
式中,
[0009]
r1为双糖基或多糖基;
[0010]
r2选自:氢、c1-c4烷基、取代的c1-c4烷基、c2-c4烯基、取代的c2-c4烯基、c2-c4炔基、取代的c2-c4炔基、c6-c10芳基、取代的c6-c10芳基、3-8元杂芳基、取代的3-8元杂芳基、
单糖基、双糖基或多糖基;
[0011]
r3选自:coor4或者conhr4,r4为氢、c1-c4烷基、取代的c1-c4烷基、c2-c4烯基、取代的c2-c4烯基、c2-c4炔基、取代的c2-c4炔基、c6-c10芳基、取代的c6-c10芳基、3-8元杂芳基、取代的3-8元杂芳基、杂环基或取代的杂环基。
[0012]
在另一优选例中,所述式i化合物为式2所示的化合物,
[0013][0014]
式中,
[0015]
r5为双糖基。
[0016]
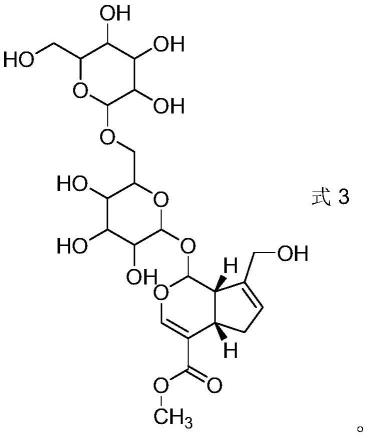
在另一优选例中,所述式i化合物为式3所示的化合物
[0017][0018]
在另一优选例中,所述式i化合物为京尼平1-β-d龙胆双糖苷。
[0019]
在另一优选例中,所述京尼平1-β-d龙胆双糖苷包括人工合成的和自然提取物。
[0020]
在另一优选例中,所述提取物包括但不限于栀子提取物、美洲格尼帕树提取物。
[0021]
在另一优选例中,所述式i化合物,或其药学上可接受的盐、溶剂化物、光学纯异构体、立体异构体或其混合物用于制备以下一种或多种用途的药物:
[0022]
(a1)降低肺脏胶原面积;
[0023]
(a2)降低细胞内胶原col1a1和/或col3a1水平;
[0024]
(a3)降低肺脏纤维粘连蛋白fibronectin的水平;
[0025]
(a4)降低平滑肌肌动蛋白α-sma水平;
[0026]
(a5)抑制肺脏炎症因子tnf-α和/或ifn-γ的表达;
[0027]
(a6)降低肺脏系数;
[0028]
(a7)改善肺组织损伤和/或肺泡结构破坏;
[0029]
(a8)减少肺组织炎症和/或肺纤维化。
[0030]
在另一优选例中,所述化合物的施用方式选自:口服、直肠、肠胃外,或其组合。
[0031]
在另一优选例中,所述肠胃外施用方式包括但不限于:静脉内、肌肉内或皮下施用。
[0032]
在另一优选例中,所述口服施用方式包括但不限于:胶囊剂、片剂、丸剂、散剂、颗粒剂、乳液、溶液、悬浮液、糖浆或酊剂。
[0033]
在本发明的第二方面,提供了一种药物组合物或保健品或功能食品,包含:
[0034]
(l1)作为第一活性成分的式i化合物或其药学上可接受的盐、溶剂化物、光学纯异构体、立体异构体或它们的混合物;和/或
[0035]
(l2)作为第二活性成分的其他可治疗特发性肺纤维化的药物;
[0036]
(j)药学上可接受的载体或赋形剂;
[0037]
其中,式i化合物如上定义。
[0038]
在另一优选例中,所述式i化合物选自:式2化合物、式3化合物、或其组合;式2和或式3化合物如上定义。
[0039]
在另一优选例中,所述药物组合物或保健品或功能食品不包含栀子苷和京尼平。
[0040]
在另一优选例中,所述式i化合物为京尼平1-β-d龙胆双糖苷。
[0041]
在本发明的第三方面,提供了一种体外的非诊断性非治疗性的抑制胚肺成纤维细胞向肌成纤维细胞转分化的方法,包括步骤:将所述胚肺成纤维细胞与医学有效量的京尼平1-β-d龙胆双糖苷接触。
[0042]
在另一优选例中,所述细胞为哺乳动物的细胞。
[0043]
在另一优选例中,所述哺乳动物选自:人、小鼠、大鼠,狗或猴子;优选地为人。
[0044]
在本发明的第四方面,提供了一种预防和/或治疗特发性肺纤维化的方法,给有需要的患者施用医学有效量的式i化合物或其药学上可接受的盐、溶剂化物、光学纯异构体、立体异构体或它们的混合物,其中式i化合物如上定义。
[0045]
在另一优选例中,所述患者为特发性肺纤维化患者。
[0046]
在另一优选例中,所述患者为哺乳动物,优选地为人。
[0047]
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
[0048]
各组与模型组间的统计学差异根据one-way anova计算,*p《0.05,**p《0.01,***p《0.001,****p《0.0001。
[0049]
图1:吡非尼酮(pfd)和京尼平1-β-d-龙胆双糖苷各浓度对人胚肺成纤维细胞hfl1的抑制作用,两者各浓度下细胞存活率均大于90%。
[0050]
图2:京尼平1-β-d-龙胆双糖苷可显著降低hfl1细胞转分化模型中ⅰ型胶原col1a1、ⅲ型胶原col3a1、平滑肌肌动蛋白α-sma mrna水平的表达。
[0051]
图3:京尼平1-β-d-龙胆双糖苷可显著降低hfl1细胞转分化模型中肌成纤维细胞活化maekerα-sma、纤维粘连蛋白fibronectin的蛋白水平表达。
[0052]
图4:京尼平1-β-d-龙胆双糖苷可显著降低hfl1细胞转分化模型中炎症因子tnf-α、ifn-γ的mrna水平表达。
[0053]
图5:吡非尼酮(pfd)和京尼平1-β-d-龙胆双糖苷各浓度对人肺上皮细胞a549的抑制作用,前者400um时细胞存活率约80%,后者各浓度下细胞存活率均大于90%。
[0054]
图6:京尼平1-β-d-龙胆双糖苷可显著降低a549细胞emt模型中ⅰ型胶原col1a1、ⅲ型胶原col3a1、平滑肌肌动蛋白α-sma mrna水平的表达。
[0055]
图7:京尼平1-β-d-龙胆双糖苷可显著降低a549细胞emt模型中纤维粘连蛋白fibronectin的蛋白水平表达,该时间点模型组α-sma蛋白水平表达不充分。
[0056]
图8:京尼平1-β-d-龙胆双糖苷不可阻止htgfβ1诱导的a549发生的emt过程,无法改善模型组上皮标志e-cadherin下降和间质细胞标志n-cadherin的升高。
[0057]
图9:京尼平1-β-d-龙胆双糖苷对博来霉素诱导小鼠肺纤维化的体内药效学实验流程示意图。
[0058]
图10:京尼平1-β-d-龙胆双糖苷可缓解博来霉素诱导的肺纤维化小鼠的体重下降。
[0059]
图11:京尼平1-β-d-龙胆双糖苷可显著降低博来霉素诱导的肺纤维化小鼠的肺系数。
[0060]
图12:各组小鼠肺组织he、masson染色病理切片(10x)镜下观察。京尼平1-β-d-龙胆双糖苷可明显改善模型鼠肺组织损伤和肺泡结构破坏。
[0061]
图13:各组小鼠肺组织szapiel炎症评分、ashcroft纤维化评分结果。京尼平1-β-d-龙胆双糖苷可显著降低肺纤维化小鼠的炎症评分、可发挥优于阳性药pfd降低肺纤维化评分的疗效。
[0062]
图14:京尼平1-β-d-龙胆双糖苷双糖苷可显著降低肺纤维化小鼠体内col1a1和fibronectin纤维化指标的蛋白水平的表达。
具体实施方式
[0063]
本发明人经过广泛而深入的研究,意外地发现中药桅子的提取物京尼平-1-β-d-龙胆双糖苷,能延缓肺纤维化进程,在此基础上,完成了本发明。
[0064]
本发明研究发现京尼平1-β-d龙胆双糖苷能够改善特发性肺纤维化患病机体肺部纤维化程度;改善特发性肺纤维化患病机体肺部炎症水平;降低特发性肺纤维化患病机体肺脏胶原面积;降低特发性肺纤维化患病机体肌成纤维细胞活化蛋白α-sma水平;降低特发性肺纤维化患病机体纤维粘连蛋白fibronectin水平;明显改善特发性肺纤维化患病机体模型动物肺脏系数和活动状态;较好地维持模型鼠的肺泡结构,能够用于治疗特发性肺纤维化。并且京尼平1-β-d龙胆双糖苷提取自中药栀子,相比在研药而言,具有副作用少,药理活性范围广,多靶点调控的特点,因此能够用于制备治疗和/或缓解ipf的药物。
[0065]
术语如本文所用,“本发明的活性成分”、“本发明的活性化合物”、“本发明的化合物”可互换使用,均指的是提取自中药栀子的化合物京尼平1-β-d龙胆双糖苷。
[0066]
在本发明中,除非特别指出,所用术语具有本领域技术人员公知的一般含义。
[0067]
在本发明中,术语“c
1-c
4”是指具有1、2、3或4个碳原子。“3-8元”是指具有3-8个环原子,依此类推。
[0068]
在本发明中,术语“烷基”表示饱和的线性或支链烃部分,例如术语“c
1-c4烷基”是指具有1至4个碳原子的直链或支链烷基,非限制性地包括甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基。
[0069]
在本发明中,术语“烯基”表示包含至少一个双键的直链或支链烃基部分,例如术语“c
2-c4烯基”是指具有2至4个碳原子的含有一个双键的直链或支链烯基,非限制性地包括乙烯基、丙烯基、正丁烯基、异丁烯基。
[0070]
在本发明中,术语“炔基”是指含有一个三键的直链或支链炔基,非限制性地包括乙炔基、丙炔基、丁炔基、异丁炔基等。
[0071]
在本发明中,术语“芳基”表示包含一个或多个芳环的烃基部分。例如术语“c
6-c
10
芳基”是指在环上不含杂原子的具有6至10个碳原子的芳香族环基,如苯基、萘基等。
[0072]
除非另外说明,本文所述的烷基、烯基、炔基、杂芳基和芳基为取代的和未取代的基团,可能的取代基包括,但不限于:羟基、氨基、硝基、腈基、卤素、c1-c6烷基、c2-c10烯基、c2-c10炔基、c3-c20环烷基、c3-c20环烯基、c1-c20杂环烷基、c1-c20杂环烯基、c1-c6烷氧基、芳基、杂芳基、杂芳氧基、c1-c10烷基氨基、c1-c20二烷基氨基、芳基氨基、二芳基氨基、c1-c10烷基氨磺酰基、芳基氨磺酰基、c1-c10烷基亚氨基、c1-c10烷基磺基亚氨基、芳基磺基亚氨基、巯基、c1-c10烷硫基、c1-c10烷基磺酰基、芳基磺酰基、酰基氨基、氨酰基、氨基硫代酰基、胍基、脲基、氰基、酰基、硫代酰基、酰氧基、羧基和羧酸酯基。
[0073]
本发明中,所述取代为单取代或多取代,所述多取代为二取代、三取代、四取代、或五取代。所述二取代就是指具有两个取代基,依此类推。
[0074]
本发明所述药学上可接受的盐可以是阴离子与式i化合物上带正电荷的基团形成的盐。合适的阴离子为氯离子、溴离子、碘离子、硫酸根、硝酸根、磷酸根、柠檬酸根、甲基磺酸根、三氟乙酸根、乙酸根、苹果酸根、甲苯磺酸根、酒石酸根、富马酸根、谷氨酸根、葡糖醛酸根、乳酸根、戊二酸根或马来酸根。类似地,可以由阳离子与式i化合物上的带负电荷的基团形成盐。合适的阳离子包括钠离子、钾离子、镁离子、钙离子和铵离子,例如四甲基铵离子。
[0075]
在另一优选例中,“药学上可接受的盐”是指式i化合物同选自下组的酸形成的盐类:氢氟酸、盐酸、氢溴酸、磷酸、乙酸、草酸、硫酸、硝酸、甲磺酸、胺基磺酸、水杨酸、三氟甲磺酸、萘磺酸、马来酸、柠檬酸、醋酸、乳酸、酒石酸、琥珀酸、酢浆草酸、丙酮酸、苹果酸、谷氨酸、对甲苯磺酸、萘磺酸、乙磺酸、萘二磺酸、丙二酸、富马酸、丙酸、草酸、三氟乙酸、硬酯酸、扑酸、羟基马来酸、苯乙酸、苯甲酸、谷氨酸、抗坏血酸、对胺基苯磺酸、2-乙酰氧基苯甲酸和羟乙磺酸等;或者式i化合物与无机碱形成的钠盐、钾盐、钙盐、铝盐或铵盐;或者通式i化合物与有机碱形成的甲胺盐、乙胺盐或乙醇胺盐。
[0076]
特发性肺纤维化(idiopathic pulmonary fibrosis,ipf)
[0077]
形成过程中肺结构的渐进和不可逆破坏,导致瘢痕形成,进而阻止正常的生理肺功能(如呼吸),导致器官功能障碍,气体交换中断,最终机体由于呼吸衰竭而死亡。
[0078]
桅子(gardeniajasminoides)
[0079]
桅子(gardeniajasminoides)为茜草科植物桅子的干燥成熟果实,具有泻火、除烦、清热利尿、凉血解毒的功效。京尼平-1-β-d-龙胆双糖苷(genipin-1
‑‑
d-gentiobioside,gg)是栀子主要有效成分环烯醚萜苷类的主要成分之一。
[0080]
京尼平1-β-d-龙胆双糖苷(genipin-1-β-d-gentiobioside)
[0081]
京尼平1-β-d龙胆双糖苷是从从栀子(gardenia jasminoides ellis),美洲格尼帕树(genipaamericana)等植物中提取的一种环烯醚萜苷,也可采用人工合成或生物合成等,具有式4所示结构:
[0082][0083]
京尼平1-β-d-龙胆双糖苷双糖苷(genipin-1-β-d-gentiobioside),是中药栀子果实的主要化学成分。京尼平1-β-d-龙胆双糖苷双糖苷可以通过增加心肌收缩力、降低心脏的负荷来抗戊巴比妥钠诱导的心力衰竭(chen,l.;luo,z.;peng,g.;li,x.;liu,l.;sheng,x.;wang,z.,the cardiac systolic and diastol ic effects of genipin-1-beta-d-gentiobioside in the experimental heart failure.pharmacology and clinics of chinese materia medic,2013,29(2),39-41);减轻b16小鼠黑色素瘤细胞系的黑素合成(kihisa,t.;watanabe,k.;yamamoto,a.;zhang,j.;matsumoto,m.;fukatsu,m.,melanogenesis inhibitory activity of monoterpene glycosides from gardeniae fructus.chemistry&biodiversity 2012,9(8),1490-1499.);此外它被发现能通过增加脑内乙酰胆碱水平对记忆障碍小鼠模型发挥治疗效果(kwak,j.h.;lee,d.-u.,structure–antiamnesic activity relationship of iridoid glycosides from gardenia fruits.chemistry letters 2015,44(6),837-839.)。但是目前尚未有文献报道关于京尼平1-β-d-龙胆双糖苷有抗肺纤维化的作用。
[0084]
中国专利申请cn104510747a公布了京尼平1-β-d-龙胆双糖苷及其他成分配伍形成的组合物用于制备抗病毒、抗菌、退热、抗炎、抗氧化等新用途。临床上可用于治疗急性呼吸道感染、流感、肺炎、乙型病毒性感性、带状疱疹等病毒及细菌性感染疾病。
[0085]
中国专利申请cn102000102 a公布了京尼平龙胆双糖苷在制备和治疗心力衰竭疾病药物中的应用。中国专利申请cn106309462.a公布了京尼平1-β-d-龙胆双糖苷及组合物在体内外对脑缺血损伤模型均具有明显的治疗作用,且小鼠急性和大鼠长期毒性试验表明京尼平1-β-d-龙胆双糖苷具有较好的安全性。
[0086]
但是目前尚未有专利公布关于京尼平1-β-d-龙胆双糖苷对特发性肺纤维化的治疗作用。
[0087]
药物组合物
[0088]
本发明还提供一种药物组合物,用于制备预防或治疗特发性肺纤维化的药物或保
健品或功能食品,其包含的活性成分为京尼平1-β-d龙胆双糖苷。
[0089]
本发明还提供了一种药物组合物,它包含安全有效量范围内的活性成分京尼平1-β-d龙胆双糖苷,以及药学上可接受的载体,较佳地,本发明的药物组合物不包含栀子苷和京尼平。
[0090]“药学上可接受的载体”指的是:一种或多种相容性固体或液体填料或凝胶物质,它们适合于人使用,而且必须有足够的纯度和足够低的毒性。“相容性”在此指的是组合物中各组份能和本发明的活性成分以及它们之间相互掺和,而不明显降低活性成分的药效。药学上可以接受的载体部分例子有纤维素及其衍生物(如羧甲基纤维素钠、乙基纤维素钠、纤维素乙酸酯等)、明胶、滑石、固体润滑剂(如硬脂酸、硬脂酸镁)、硫酸钙、植物油(如豆油、芝麻油、花生油、橄榄油等)、多元醇(如丙二醇、甘油、甘露醇、山梨醇等)、乳化剂(如)、润湿剂(如十二烷基硫酸钠)、着色剂、调味剂、稳定剂、抗氧化剂、防腐剂、无热原水等。
[0091]
本发明的活性成分或药物组合物的施用方式没有特别限制,代表性的施用方式包括(但并不限于):口服、直肠、肠胃外(静脉内、肌肉内或皮下)等。
[0092]
用于口服给药的固体剂型包括胶囊剂、片剂、丸剂、散剂和颗粒剂。
[0093]
用于口服给药的液体剂型包括药学上可接受的乳液、溶液、悬浮液、糖浆或酊剂。除了活性成分外,液体剂型可包含本领域中常规采用的惰性稀释剂,如水或其它溶剂,增溶剂和乳化剂,例知,乙醇、异丙醇、碳酸乙酯、乙酸乙酯、丙二醇、1,3-丁二醇、二甲基甲酰胺以及油,特别是棉籽油、花生油、玉米胚油、橄榄油、蓖麻油和芝麻油或这些物质的混合物等。除了这些惰性稀释剂外,组合物也可包含助剂,如润湿剂、乳化剂和悬浮剂、甜味剂、矫味剂和香料。
[0094]
除了活性成分外,悬浮液可包含悬浮剂,例如,乙氧基化异十八烷醇、聚氧乙烯山梨醇和脱水山梨醇酯、微晶纤维素、甲醇铝和琼脂或这些物质的混合物等。
[0095]
用于肠胃外注射的组合物可包含生理上可接受的无菌含水或无水溶液、分散液、悬浮液或乳液,和用于重新溶解成无菌的可注射溶液或分散液的无菌粉末。适宜的含水和非水载体、稀释剂、溶剂或赋形剂包括水、乙醇、多元醇及其适宜的混合物。
[0096]
本发明的主要优点包括:
[0097]
(a)本发明的化合物提取自中药,具有广泛药理活性以及多靶点调控的优点,且毒副作用低,在治疗特发性肺纤维化方面具有极佳的临床推广价值。
[0098]
(b)本发明的实验表明,本发明的化合物治疗特发性成纤维化的效果强于吡非尼酮(已知药物),因此具有较好的治疗价值。
[0099]
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(new york:cold spring harbor laboratory press,1989)中所述的条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数是重量百分比和重量份数。
[0100]
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
[0101]
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0102]
本发明采用体外细胞模型和体内动物模型,以京尼平1-β-d龙胆双糖苷来作用于htgfβ1诱导的hfl1、a549细胞模型,检测其对于基质成分(ecm)沉积的改善情况;治疗动物,
观察其对于博来霉素诱导的肺纤维小鼠肺组织结构、炎症、纤维化改善情况。
[0103]
实施例1:体外细胞模型实验-hfl1肺成纤维细胞转分化(fmt)模型
[0104]
肺纤维化的确切病理过程至今还不清楚,但肌成纤维细胞活化是肺纤维化发生的核心环节,标志性的高表达有α-平滑肌肌动蛋白(α-sma)的肌成纤维细胞主要通过原位成纤维细胞的激活与转化和上皮-间质转化(emt)两种方式来源。在此选用htgfβ1诱导人胚肺成纤维细胞向肌成纤维细胞转分化(fmt)模型进行gg的体外药效及是否通过该机制发挥药效的评估。
[0105]
1)给药浓度确定:选用hfl1人胚肺成纤维细胞,以5000个/孔的浓度铺于96孔板,24h后以京尼平1-β-d龙胆双糖苷0、12.5、25、50、100、200、400、800um;阳性药吡非尼酮0、25、50、100、200、400、800um继续孵育48h,每孔加入10ul cck8试剂后于37℃培养箱继续培养1h,酶标仪测定450nm处吸光度,计算各给药浓度下细胞存活率,以确定合适给药浓度。
[0106]
2)fmt模型给药:以1
×
105个/ml的浓度铺于12孔板,贴壁12h后更换无血清培养基继续培养24h,以10ng/ml人重组tgfβ1刺激hfl1细胞48h诱导其向肌成纤维细胞分化的fmt模型,阳性药吡非尼酮400um、京尼平1-β-d龙胆双糖苷100um与造模同步给药,同时设置空白对照组(不加htgfβ1和供试品)和模型组(不加供试品)。药物干预结束后,收集细胞,提取细胞rna和蛋白,后期检测基质主要成分ⅰ型胶原col1a1、ⅲ型胶原col3a1、平滑肌肌动蛋白α-sma等含量变化。
[0107]
3)细胞rna提取:12孔板弃去培养上清,每孔加入200ul trizol溶液,反复吹打直至细胞全部裂解,收集于1.5ml ep管中,按试剂盒操作步骤完成rna的提取。利用scan drop 100超微量核酸蛋白测定仪检测所得rna的纯度及浓度,再利用primescript rt reagent kit,依据上一步测得的rna浓度,从中取1ug rna用于反转录获得cdna,进而rt-pcr进行上述基质成分的rna水平检测。
[0108]
4)细胞蛋白提取:12孔板弃去培养上清,每孔加入80ul ripa(内含1%pmsf),反复吹打,收集细胞于1.5ml ep管中,置于冰上裂解30分钟,离心取上清,即为蛋白样品。利用thermo的piercetm bca protein assay kit进行蛋白浓度的测定,后用1*sds工作液,将蛋白样品稀释为统一浓度(1.2mg/ml),95℃金属浴中煮10min,制样完成。western blotting进行上述基质成分的蛋白水平检测。
[0109]
5)结果分析:
[0110]
cck8检测结果发现吡非尼酮和京尼平1-β-d龙胆双糖苷各浓度对hfl1细胞均无明显的毒副作用(图1),存活率均高于90%,参考文献用量,最终选择阳性药400um,京尼平1-β-d龙胆双糖苷100um给药。
[0111]
对各组细胞col1a1、col3a1、α-sma等指标mrna水平的检测发现(图2):htgfβ1可显著诱导模型组分泌大量细胞外基质(ecm)成分胶原蛋白col1a1、col3a1、α-sma,而京尼平1-β-d龙胆双糖苷可显著降低上述指标的表达。此外,发现京尼平1-β-d龙胆双糖苷发挥了比阳性药更为显著的药效。
[0112]
对各组细胞肌成纤维细胞活化markerα-sma、基质非胶原成分纤连蛋白fibronectin等指标蛋白水平的检测发现(图3):htgfβ1可显著诱导模型组分泌肌成纤维细胞活化蛋白α-sma和非胶原成分fibronectin,而京尼平1-β-d-龙胆双糖苷可显著降低上述指标的表达。此外,发现京尼平1-β-d龙胆双糖苷发挥了比阳性药更为显著的药效。
[0113]
对各组细胞相关炎症因子tnf-α、ifn-γ的mrna水平检测发现(图4):京尼平1-β-d-龙胆双糖苷可显著降低hfl1细胞fmt模型中炎症因子的表达。
[0114]
综上,京尼平1-β-d-龙胆双糖苷可显著抑制htgfβ1诱导的人胚肺成纤维细胞向肌成纤维细胞的转分化这一重要的纤维化过程。
[0115]
实施例2:体外细胞模型实验-a549上皮间充质转换emt模型
[0116]
已有大量数据表明组织损伤时,emt参与并导致了组织纤维化(主要包括胶原成分、弹性蛋白及其他细胞外基质成分在间质的沉积)。上皮损伤是肺间质纤维化过程中的基础病变,肺泡上皮细胞的持续性损伤-修复过程,可能是肺纤维化病理机制的关键环节,且emt是肌成纤维细胞的重要来源,而tgf、egf等细胞因子的诱导作用则是肺纤维化过程中必不可少的促进因素。故同步选用htgfβ1诱导a549上皮间充质转换emt模型进行京尼平1-β-d-龙胆双糖苷的体外药效及可能的机制探讨。
[0117]
1)给药浓度确定:选用a549肺癌细胞系,以5000个/孔的浓度铺于96孔板,24h后以京尼平1-β-d龙胆双糖苷0、12.5、25、50、100、200、400、800um;阳性药吡非尼酮0、25、50、100、200、400、800um继续孵育24h,每孔加入10ul cck8试剂后于37℃培养箱继续培养1h,酶标仪测定450nm处吸光度,计算各给药浓度下细胞存活率,以确定合适给药浓度。
[0118]
2)emt模型给药:以2
×
105个/ml的浓度铺于12孔板,贴壁6h后更换无血清培养基继续培养24h,以10ng/ml人重组tgfβ1刺激a549细胞24h诱导emt模型,阳性药吡非尼酮400um、京尼平1-β-d龙胆双糖苷100um与造模同步给药,同时设置空白对照组(不加htgfβ1和供试品)和模型组(不加供试品)。药物干预结束后,收集细胞,提取细胞rna和蛋白,后期检测基质主要成分ⅰ型胶原col1a1、ⅲ型胶原col3a1、平滑肌肌动蛋白α-sma、上皮细胞标志e-cadherin、间质细胞标志n-cadherin等含量变化。
[0119]
3)细胞rna提取:同实施例1的3)。
[0120]
4)细胞蛋白提取:同实施例1的4)。
[0121]
5)结果分析:
[0122]
cck8检测结果发现(图5):吡非尼酮对a549细胞的增殖有一定影响,较高浓度存活率约80%;京尼平1-β-d龙胆双糖苷各浓度对a549细胞无明显的毒副作用,存活率均高于90%;参考文献用量,最终选择阳性药400um,京尼平1-β-d龙胆双糖苷100um给药。
[0123]
对各组细胞col1a1、col3a1、α-sma等指标mrna水平的检测发现(图6):htgfβ1可显著诱导模型组分泌大量细胞外基质(ecm)成分胶原蛋白col1a1、col3a1、α-sma,京尼平1-β-d龙胆双糖苷可显著降低上述指标的表达。而阳性药对此模型改善肺纤维化药效不如京尼平1-β-d龙胆双糖苷。
[0124]
对各组细胞基质非胶原成分纤连蛋白fibronectin指标蛋白水平的检测发现(图7):htgfβ1可显著诱导模型组分泌非胶原成分fibronectin,京尼平1-β-d龙胆双糖苷可显著降低fibronectin的表达,且京尼平1-β-d龙胆双糖苷发挥了比阳性药更为显著的药效。
[0125]
对各组细胞上皮细胞标志e-cadherin、间质细胞标志n-cadherin的mrna水平检测发现(图8):htgfβ1可显著诱导emt模型发生,各造模组e-cadherin显著下降,n-cadherin显著升高。而阳性药吡非尼酮和京尼平1-β-d-龙胆双糖苷均不可阻止该过程的发生,gg改善该模型纤维化指标很可能是通过抑制成纤维细胞的活化而实现的,实施例1中fmt的结果也可验证。
[0126]
综上,京尼平1-β-d-龙胆双糖苷不可阻止htgfβ1诱导的肺上皮细胞向间质细胞的转换过程,但可改善该模型最终表达的肺纤维化指标。
[0127]
实施例3:体内动物模型实验-博来霉素诱导的小鼠肺纤维化模型
[0128]
1)实验方案
[0129]
本发明采用c57bl/6小鼠气管单次注入博来霉素的方法建立肺纤维化动物模型,通过灌胃给予京尼平-1-β-d-龙胆双糖苷方式验证其疗效;
[0130]
具体过程:
[0131]
博莱霉素是最常用造肺纤维化模型的药物,可以通过气管内或经鼻途径直接给药,也可以通过皮下、腹腔或静脉注射系统给药。在这些途径中,使用单剂量经气管内给药的方法是最常用和参考的急性模型。选用6-8周龄c57雄性小鼠,经适应性喂养体重达25g左右时,随机纳入假手术(sham)组、模型(model)组、模型+阳性药吡非尼酮(pfd)组、模型+京尼平-1-β-d-龙胆双糖苷(gg)组,每组12只小鼠。小鼠腹腔注射麻醉后固定直立,用镊子拉出其舌头并在喉镜辅助下找到小鼠气管口,雾化吸入器注入生理盐水配制的硫酸博来霉素,剂量为1.8mg/kg。药液进入肺部后,左右摇晃使药液均匀分布,后放回笼中待其苏醒,造模完成。
[0132]
具体给药方式如图9所示:造模前一天过夜禁食不禁水。第0天,假手术组气管注入生理盐水(2ml/kg),模型组及给药组气管注入博来霉素构建肺纤维化模型(1.8mg/kg、2ml/kg)。第1天,各组小鼠持续灌胃给药相应药物13天,每天一次,阳性药pfd 300mg/kg,京尼平1-β-d-龙胆双糖苷240mg/kg。假手术组及模型组小鼠灌胃给药0.5%cmc-na溶液。
[0133]
动物处死取材:取材当日异氟烷吸入麻醉小鼠,待小鼠充分麻醉后,方可进行后续解剖。沿正中线剪开腹部皮肤、肌层、腹膜后,剪断下腔静脉放血,剪破胸膈膜,再沿两侧肋骨向上剪开至能将整个前胸揿开,剪取整个肺组织,于pbs清洗血污2遍后,左肺于10%福尔马林溶液中固定,病理诊断肺组织切片进行炎症和纤维化评分,右肺冻存进行相关纤维化因子的检测。
[0134]
动物常规指标的临床观察:造模后第一天起,每日称重、观察小鼠活动及反应性、查看小鼠毛发状态、倾听小鼠肺部湿啰音情况。解剖后称量湿肺重,并计算肺重/体重这一脏器系数,衡量病变肺的充血、水肿或增生肥大。
[0135]
肺部病理组织切片:取固定的肺组织,进行石蜡包埋切片后按照常规试剂盒的操作步骤苏木素伊红(hematoxylin and eosin,h&e)及masson染色。常规镜下观察并由专业的病理学专家为各组小鼠进行肺组织中炎症病变和纤维化的程度打分。
[0136]
病理结果评分:光学显微镜下观察he、masson染色病理切片,采取计算机图像分析软件k-viewer1.5.3.1采图系统采集图片,并根据szapiel评分标准,对纤维化肺组织进行炎症程度半定量分析。炎症程度分级0-3分:0分:无肺泡炎;1分:轻度肺泡炎,局部及近胸部可见单核细胞浸润,面积小于全肺20%,肺泡结构大致正常;2分:中度肺泡炎,病变面积占全肺的20%~50%;3分:重度肺泡炎和肺纤维化,病变面积大于全肺的50%,肺泡腔内偶有单核细胞和/或出血造成实变。同时根据ashcroft评分标准,对纤维化肺组织进行纤维化程度半定量分析。纤维化程度分级0-8级:0级(0分):正常肺组织;1级(1分):支气管肺泡壁轻度增厚,纤维化程度轻;2-3级(2-3分):纤维化程度加重,细支气管肺泡壁或肺泡壁中度增厚,但不伴有明显的肺泡结构紊乱;4-5级(4-5分):重度纤维化改变,支气管肺泡壁增厚明
显,有纤维条索或小范围纤维灶形成,结构明显破坏;6-7级(6-7分):大范围肺组织结构严重破坏,为纤维化极重度改变;8级(8分):胶原纤维占据整个视野。
[0137]
小鼠肺组织基质成分的蛋白水平的含量测定:取25mg左右肺组织,加入120ul ripa(内含1%pmsf),匀浆后冰上裂解30min,离心取上清获得蛋白样品,同细胞蛋白样品完成蛋白工作液的配制,进行col1a1、fibronectin基质代表成分的western blot含量测定。
[0138]
2)实验结果
[0139]
14天实验周期内小鼠体重曲线监测发现(图10):与假手术组的小鼠体重日趋增长相比,c57bl/6小鼠经气管灌注博来霉素后,体重持续下降。吡非尼酮阳性药和京尼平-1-β-d-龙胆双糖苷(gg)可略改善模型小鼠体重的降低但不显著。临床观察发现造模7天后模型小鼠逐渐活动减弱,部分出现湿啰音,pfd及京尼平1-β-d-龙胆双糖苷组活动状态好于模型组,但阳性药给药后半小时间小鼠出现明显不适感,趴卧不动,缓解后才可恢复。肺系数(图11)发现:模型小鼠肺系数显著增大,充血、水肿或增生肥大明显,pfd和京尼平1-β-d-龙胆双糖苷可显著降低该指标,减轻肺部病变。
[0140]
随后,对各组小鼠肺组织切片进行h&e染色和masson染色并对其炎性细胞浸润情况和纤维化程度进行评分,结果显示(图12、13):博来霉素造模处理后,小鼠炎症细胞浸润情况、胶原纤维沉积情况加重,支气管肺泡壁增厚明显,肺泡结构紊乱,炎症及纤维化评分显著增高。吡非尼酮用药时,可明显改善炎症浸润,但胶原纤维仅少许减少。京尼平-1-β-d-龙胆双糖苷用药时,可显著改善炎性细胞浸润程度,同时可明显抑制支气管肺泡壁增厚并维持肺泡结构的完整,纤维化程度明显改善,两项评分均明显下降。
[0141]
对各组小鼠基质胶原成分col1a1、基质非胶原成分纤连蛋白fibronectin纤维化指标蛋白水平的检测发现(图14):博来霉素可显著诱导模型组分泌ⅰ型胶原col1a1和非胶原成分fibronectin,而京尼平1-β-d-龙胆双糖苷可显著发挥与阳性药相当的降低上述指标的表达能力。
[0142]
综上,京尼平1-β-d-龙胆双糖苷可显著改善博来霉素诱导的小鼠肺组织损伤,肺泡结构破坏,减少肺组织炎症和肺纤维化,其对小鼠肺组织病理纤维化的改善优于阳性药吡非尼酮。
[0143]
讨论
[0144]
经研究发现,京尼平1-β-d龙胆双糖苷能够用于治疗特发性肺纤维化。京尼平1-β-d龙胆双糖苷能够改善特发性肺纤维化患病机体肺部纤维化程度;改善特发性肺纤维化患病机体肺部炎症水平;降低特发性肺纤维化患病机体肺脏胶原面积;降低特发性肺纤维化患病机体肌成纤维细胞活化蛋白α-sma水平;降低特发性肺纤维化患病机体纤维粘连蛋白fibronectin水平;明显改善特发性肺纤维化患病机体模型动物肺脏系数和活动状态;减轻肺组织损伤,较好地维持模型鼠的肺泡结构。
[0145]
具体地京尼平1-β-d龙胆双糖苷苷在htgfβ1诱导的a549肺泡上皮细胞和hfl1人胚肺成纤维细胞的模型上均可以改善纤维化水平,包括显著降低细胞内胶原(col1a1和col3a1)、肌成纤维细胞活化蛋白α-sma,纤维粘连蛋白fibronectin水平及炎症因子的表达;在博来霉素诱导的小鼠特发性肺纤维化模型上可明显改善模型动物肺脏系数、活动状态,降低模型动物col1a1等胶原含量和纤维粘连蛋白fibronectin水平,改善炎性细胞浸润和纤维化程度,较好地维持模型鼠的肺泡结构。京尼平1-β-d龙胆双糖苷改善肺纤维化是通
过抑制人胚肺成纤维细胞向肌成纤维细胞的转分化,而不是上皮细胞向间质细胞的转换过程实现的。
[0146]
目前已知专利申请了201911065621.7公布了京尼平苷对肺纤维化有治疗作用,京尼平苷(栀子苷)也是中药栀子中典型的环烯醚萜苷类化合物。但是正常大鼠在单词口服栀子苷0.574g/kg的时候就出现明显的肝毒性,其急毒ld50为1.4312g/kg(丁越,张彤,项乐源,浦益琼,陶建生。栀子苷致大鼠肝毒性时-量关系及其机理研究.中华中医药学会2009年药用植物化学与中药资源可持续发展学术研讨会)。
[0147]
对比该现有技术教导的药物而言,京尼平1-β-d-龙胆双糖苷在大鼠在给药剂量为3.25-g/kg/d-20g/kg/d连续给药一个月,均未发先明显的毒性(樊向德陈鸣珍.一种治疗脑缺血性疾病的药物及组合物:中国,cn106309462b,2020.01.21)。因此,认为京尼平1-β-d-龙胆双糖苷在治疗ipf方面,比京尼平苷具有更好的安全性及成药潜力。
[0148]
在本发明提及的所有文献都在本技术中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1