一种人源性血红蛋白类氧载体的制备方法及其产品和应用与流程
1.本发明涉及血红蛋白类氧载体技术领域,特别是涉及一种人源性血红蛋白类氧载体的制备方法及其产品和应用。
背景技术:
2.输血是临床重要的救助治疗措施,但同时存在着需进行交叉配型、存在各种病毒交叉感染的危险、血源紧张、贮存期较短等诸多限制。血红蛋白类氧载体(hemoglobin
‑
based oxygen carriers,hbocs)是一种新兴的具有携氧功能的血液代用品,具有可长时间保存、无需配型、便于运输、感染风险低等优点,其表现出良好治疗效果的同时也存在诸多问题,诸如在氧化应激、影响血管收缩、产生肾毒性损伤等毒副作用。polymerized hemoglobin
‑
superoxide dismutase
‑
catalase
‑
carbonic anhydrase(polyhb
‑
sod
‑
cat
‑
ca)是一种为解决上述问题进行优化的hbocs产品。
3.polyhb
‑
sod
‑
cat
‑
ca是一种血红蛋白与超氧化物歧化酶(sod)、过氧化氢酶(cat)和碳酸酐酶(ca)复合而成的血红蛋白类氧载体,其中,超氧化物歧化酶、过氧化氢酶和碳酸酐酶也来源于原料血中,从原料血中和血红蛋白一起被提取出来,并在体外进一步与血红蛋白交联、聚合;在体外的聚合过程中,酶会发生变性失活或是未交联被筛除,尤其是以人源性血红蛋白时,二聚体的产生使酶的交联更加困难,导致酶活的损失率较大。
技术实现要素:
4.本发明的目的在于提供一种人源性血红蛋白类氧载体的制备方法及其产品和应用。
5.本申请第一方面提供了一种人源性血红蛋白类氧载体的制备方法,其包括:
6.(1)将人源血液进行清洗、破膜、有机溶剂萃取,取水相,离心,取上清液,得到血红蛋白溶液;
7.(2)调节反应体系的ph为7
‑
9,向所述血红蛋白溶液中加入浓度为1.5
‑
2.5mol/l的赖氨酸,和终浓度为0.5
‑
2%(w/v)的酶活保护剂,搅拌并加入浓度为0.5
‑
1.5%(w/v)的戊二醛,其中,戊二醛与血红蛋白的摩尔比为(10
‑
20):1,赖氨酸与血红蛋白的摩尔比为(5
‑
10):1;
8.(3)2℃
‑
25℃的反应温度下进行聚合反应,反应时间2
‑
6小时;
9.(4)加入浓度为1.5
‑
2.5mol/l的赖氨酸终止反应,其中,赖氨酸与血红蛋白的物质的量之比为(180
‑
220):1;
10.(5)离心,取上清液,获得人源性血红蛋白类氧载体溶液。
11.本申请第二方面提供了采用本申请第一方面的方法制备的人源性血红蛋白类氧载体。
12.本申请第三方面提供了采用本申请第一方面的方法制备的人源性血红蛋白类氧载体作为血液代用品的用途。
13.采用本申请的方法制备人源性血红蛋白类氧载体,由于加入了特定的酶活保护剂,能够有效提高聚合过程中酶活的回收率,从而获得一种酶活性更高,进而具有更高的载氧能力的人源性血红蛋白类氧载体。
附图说明
14.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
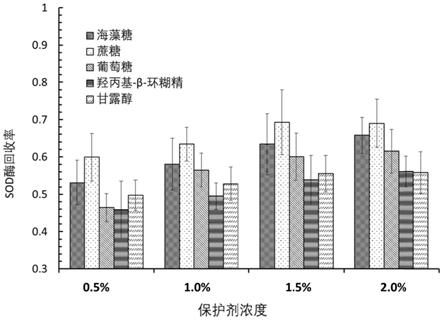
15.图1为实施例1
‑
20的人源性血红蛋白类氧载体中sod的酶活回收率结果;
16.图2为实施例1
‑
20的人源性血红蛋白类氧载体中cat的酶活回收率结果;
17.图3为实施例1
‑
20的人源性血红蛋白类氧载体中ca的酶活回收率结果。
具体实施方式
18.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
19.本申请第一方面提供了一种人源性血红蛋白类氧载体的制备方法,其包括:
20.(1)将人源血液进行清洗、破膜、有机溶剂萃取,取水相,离心,取上清液,得到血红蛋白溶液;
21.(2)调节反应体系的ph为7
‑
9,向所述血红蛋白溶液中加入浓度为1.5
‑
2.5mol/l的赖氨酸,和终浓度为0.5
‑
2%(w/v)的酶活保护剂,搅拌并加入浓度为0.5
‑
1.5%(w/v)的戊二醛,其中,戊二醛与血红蛋白的摩尔比为(10
‑
20):1,赖氨酸与血红蛋白的摩尔比为(5
‑
10):1;
22.(3)2℃
‑
25℃的反应温度下进行聚合反应,反应时间2
‑
6小时;
23.(4)加入浓度为1.5
‑
2.5mol/l的赖氨酸终止反应,其中,赖氨酸与血红蛋白的物质的量之比为(180
‑
220):1;
24.(5)离心,取上清液,获得人源性血红蛋白类氧载体溶液。
25.本申请对步骤(1)中提取血红蛋白溶液的条件(包括清洗、破膜、萃取剂离)不做限定,只要能够实现本发明本发明的目的即可,本领域技术人员可采用现有技术得到血红蛋白溶液,例如,采用生理盐水清洗,采用纯净水破膜,采用正己烷进行萃取等。
26.超氧化物歧化酶与过氧化氢酶在体内的半衰期极短,通过聚合将其交联在聚合血红蛋白上,能有效延长其作用周期,同时交联碳酸酐酶分解二氧化碳,起到天然红细胞中运输二氧化碳的功能;然而人源性血红蛋白在体外条件下容易降解成为二聚体状态,使酶的交联更加困难,在交联过程中,酶容易失活,发明人在研究中发现,当采用本申请的特定的反应条件,包括反应温度、反应时间、ph值以及戊二醛和赖氨酸的用量,配合特定浓度的酶活保护剂,可以使人源性血红蛋白与酶聚合成人源性血红蛋白类氧载体的过程中,有效的提高酶活回收率,从而使产物具有更高的酶活性和携氧能力。
27.在本申请第一方面的一些实施方式中,所述酶活保护剂选自海藻糖、葡萄糖、甘露醇、羟丙基
‑
β
‑
环糊精和蔗糖中的至少一种。发明人发现,当加入本申请的酶活保护剂后,sod、cat以及ca的酶活回收率明显提高。
28.发明人在研究在还发现,有些酶活保护剂会抑制人源性血红蛋白类氧载体的聚合反应,不利于二聚体形式的人源血红蛋白的聚合,发明人在研究中意外地发现,蔗糖与羟丙基
‑
β
‑
环糊精对聚合率的影响不大,海藻糖浓度的提高则会促进聚合;因此在本申请的一些优选的实施方式中,酶活保护剂的种类优选蔗糖、海藻糖和羟丙基
‑
β
‑
环糊精中的至少一种
29.发明人在研究中发现,戊二醛作为聚合反应的交联剂,不仅能交联血红蛋白,也能交联所需的酶,赖氨酸可以竞争性抑制戊二醛的交联作用,戊二醛用量过多或者赖氨酸用量过少,会导致超大分子的产生,造成粘度上升与免疫原性问题;而戊二醛用量过少或者赖氨酸用量过多,则会有大量二聚体形式存在。本申请发明人在研究中发现,当戊二醛与血红蛋白的摩尔比为(10
‑
20):1,赖氨酸与血红蛋白的摩尔比为(5
‑
10):1时,可以得到分子量适中的人源性血红蛋白类氧载体,二聚体的含量较低。进一步地,发明人还发现,戊二醛用量越高、赖氨酸用量越少,sod、cat、ca的酶活回收率越高,因此,在本申请第一方面的一些优选的实施方式中,步骤(2)中,赖氨酸、戊二醛与血红蛋白的摩尔比优选为(6.5
‑
7.5):(15
‑
20):1。
30.发明人在研究中还发现,反应时间控制在2
‑
4小时,sod回收率升高,4
‑
6小时,sod回收率下降;cat回收率随反应时间延长逐渐下降,ca回收率随时间变化不大,由此优选反应时间为2
‑
4小时。
31.在本申请第一方面的一些优选的实施方式中,反应温度为2
‑
6℃,发明人发现,低温可以减少高铁血红蛋白的产生,有利于提高人源性血红蛋白类氧载体携氧能力。
32.发明人在研究中还发现,ph对酶活回收率影响较大,sod、cat和ca的酶活回收率在ph 7
‑
7.5时,逐渐升高,而ph在7.5
‑
9时,酶活回收率逐渐降低;因此,在本申请第一方面的一些优选的实施方式中,反应体系的ph为7
‑
8。
33.在本申请第一方面的一些实施方式中,还包括所述人源性血红蛋白类氧载体的精制:
34.(6)将所述人源性血红蛋白类氧载体溶液经2
‑
6℃,2500
‑
3500rpm离心15
‑
30分钟;
35.(7)取上清液进行超滤离心,其中,超滤离心的条件包括:超滤离心管的截留分子量为50
‑
100kd,离心温度2
‑
6℃,转速2500
‑
3500rpm,离心时间15
‑
30分钟;
36.(8)重复超滤离心5
‑
7次;
37.(9)取上清液,于生理盐水中进行透析,透析温度2
‑
6℃,透析时间20
‑
30小时。
38.在本申请第一方面的一些实施方式中,所述人源血液选自脐带血或外周血中的至少一种。发明人在研究中发现,脐带血中的血红蛋白以hbf为主,对2,3
‑
二磷酸甘油酸亲和力较低,较之成人血具有更高的氧亲和力,且每年有大量新生儿出生,人脐带血通常被废弃,来源充足,因此可作为人源性血红蛋白类氧载体制备的原料血液来源。
39.在本申请第一方面的一些实施方式中,步骤(1)和步骤(5)的离心条件各自独立地包括:离心温度2
‑
6℃,转速6000
‑
10000rpm,离心时间30
‑
60分钟。
40.本申请第二方面提供了采用本申请第一方面的方法制备的人源性血红蛋白类氧载体。
41.本申请第三方面提供了采用本申请第一方面的方法制备的人源性血红蛋白类氧载体作为血液代用品的用途。
42.以下,基于实施例对本申请进行具体地说明,但本申请并不限于这些实施例。
43.人源性血红蛋白类氧载体聚合度测定:
44.以waters 2695型分析型高效液相色谱仪与zenix sec
‑
300色谱柱测定,以ph=7.0的150mmol/l pb作为流动相,流速0.5ml,检测波长280nm;以分子量为600kda、240kda、150kda、66kda、30kda的marker上样检测,以分子量大小作为横坐标,出峰时间作为纵坐标建立标准曲线。
45.将实施例1
‑
15的人源性血红蛋白类氧载体溶液稀释至1g/l后,经0.22um微孔过滤膜过滤,上样体积10ul,运行时间30min。得到分子量分布曲线,根据所述分子量分布曲线获得样品中分子量在600kda、240kda、150kda、66kda、30kda的分子所占面积的百分比,即为分子量分布中,各分子量分子百分比;根据标准曲线计算样品的平均分子量、有效转化率,有效转化率为去除了超大分子与未聚合小分子的部分所占比例,超大分子为分子量大于600kda的分子,未聚合小分子为分子量小于50kda的分子。
46.聚合率=(1
‑
未聚合小分子面积的百分比)
×
%100%;
47.平均分子量=σ分子量大小*该分子量所占面积百分比;
48.有效转化率=(1
‑
超大分子占面积百分比
‑
未聚合小分子占面积百分比)/1
×
100%。
49.酶活测定:
50.以sigma 19160 sod试剂盒测定超氧化物歧化酶活性(即酶活浓度)。
51.参考guo c等的《extraction of superoxide dismutase,catalase,and carbonic anhydrase from stroma
‑
free red blood cell hemolysate for the preparation of the nanobiotechnological complex of polyhemoglobin
–
superoxide dismutase
–
catalase
–
carbonic anhydrase》(artificial cells,nanomedicine,and biotechnology,2015,43(3),157
–
162)中的方法测定过氧化氢酶活性和碳酸酐酶活性。
52.酶回收率(或酶活回收率)=(反应前酶活浓度
×
反应前体积)/(反应后酶活浓度
×
反应后体积)。
53.实施例1
54.(1)将人脐带血等量分装至200ml血袋中,重量平衡后于2500rpm、4℃离心7分钟,弃上清液,加入预冷的生理盐水洗涤后并在2500rpm、4℃下离心7分钟后弃上清液,待上清液清澈且在全波长扫描下吸收峰等同于生理盐水。加入2倍体积的纯水静置30分钟使红细胞破膜,于8000rpm、4℃条件下离心45分钟后弃沉淀;
55.将0.5倍体积的正己烷作为萃取剂加入破膜液中,充分混匀后静置后于4℃下萃取2h。待离心管中的水相与有机相完全分层后收集水相,所得水相经真空旋蒸以去除其中的有机物残留后,于8000rpm、4℃条件下离心45分钟后弃沉淀,如此重复操作两次,得到血红蛋白溶液;
56.(2)调节反应体系的ph=8,向血红蛋白溶液中加入赖氨酸和终浓度为0.5%(w/v)的海藻糖,其中赖氨酸与血红蛋白摩尔比为7:1,在充分搅拌状态下分批逐滴加入戊二醛,戊二醛与血红蛋白摩尔比为15:1;
57.(3)在4℃的反应温度下搅拌反应,反应时间4小时;
58.(4)加入2mol/l赖氨酸终止反应,其中赖氨酸与血红蛋白摩尔比为200:1;
59.(5)8000rpm、4℃条件下离心45分钟后弃沉淀,得到人源性血红蛋白类氧载体溶液;
60.(6)将人源性血红蛋白类氧载体溶液在4℃下,3000rpm离心20分钟;
61.(7)取上清液进行超滤离心,其中,超滤离心的条件包括:超滤离心管的截留分子量为50kd,离心温度4℃,转速3000rpm,离心时间20分钟;
62.(8)重复超滤离心5次;
63.(9)取上清液,于生理盐水中,在4℃下透析20小时。
64.实施例2
‑465.除了将海藻糖的浓度调整为1.0%、1.5%、2.0%,其余与实施例1相同。
66.实施例5
67.除了将海藻糖替换为蔗糖,其余与实施例1相同。
68.实施例6
‑869.除了将蔗糖的浓度调整为1.0%、1.5%、2.0%,其余与实施例5相同。
70.实施例9
71.除了将海藻糖替换为葡萄糖,其余与实施例1相同。
72.实施例10
‑
12
73.除了将葡萄糖的浓度调整为1.0%、1.5%、2.0%,其余与实施例9相同。
74.实施例13
75.除了将海藻糖替换为羟丙基
‑
β
‑
环糊精,其余与实施例1相同。
76.实施例14
‑
16
77.除了将羟丙基
‑
β
‑
环糊精的浓度调整为1.0%、1.5%、2.0%,其余与实施例13相同。
78.实施例17
79.除了将海藻糖替换为甘露醇,其余与实施例1相同。
80.实施例18
‑
20
81.除了将甘露醇的浓度调整为1.0%、1.5%、2.0%,其余与实施例17相同。
82.对比例1
83.除了不添加海藻糖,其余与实施例1相同。
84.实施例3、4、6、12、15、20以及对比例1的人源性血红蛋白类氧载体的分子量分布、聚合率、平均分子量、有效转化率结果见表1。
[0085][0086]
从表1的结果中可以看出,不同酶活保护剂的加入对聚合结果的影响不同,甘露醇与葡萄糖会对聚合产生抑制效果,蔗糖与羟丙基
‑
β
‑
环糊精对聚合率的影响不大,海藻糖浓
度的提高则会促进聚合;因此,酶活保护剂的种类优选蔗糖、海藻糖和羟丙基
‑
β
‑
环糊精中的至少一种。
[0087]
实施例1
‑
20的人源性血红蛋白类氧载体中sod的酶活回收率结果如图1所示。
[0088]
实施例1
‑
20的人源性血红蛋白类氧载体中cat的酶活回收率结果如图2所示。
[0089]
实施例1
‑
20的人源性血红蛋白类氧载体中ca的酶活回收率结果如图3所示。
[0090]
如图1所示,不同浓度的酶活保护剂对酶活回收率的影响不同,其中,在浓度相同的情况下,各种类型的酶活保护剂中,蔗糖和海藻糖的效果最好,其中以蔗糖作为酶活保护剂,sod的酶活回收率最高(59.92
±
6.37%
‑
69.31
±
8.68%);对于不同酶活保护剂,当浓度在0.5%
‑
1.5%范围内,sod的回收率随着保护剂浓度的提升呈上升趋势,在浓度为1.5%后趋于平稳,之后无明显变化,蔗糖浓度为1.5%时sod酶回收率达到最高(69.31
±
8.68)。
[0091]
如图2所示,cat的回收率受酶活保护剂浓度影响较小,同一种酶活保护剂不同浓度间cat回收率差别在3%以下(海藻糖1.97%、蔗糖2.78%、葡萄糖2.77%、β
‑
环糊精2.63%、甘露醇0.88%)。在同浓度下蔗糖组的cat回收率最高(59.51
±
0.41%
‑
62.29
±
0.67%),其次是海藻糖组(57.00
±
0.41%
‑
58.97
±
0.51%)。在蔗糖浓度为2.0%时,cat回收率最高(62.29
±
0.67%)。
[0092]
如图3所示,蔗糖、葡萄糖、β
‑
环糊精浓度对ca的回收率影响较小,不同浓度下的ca回收率差别最大为3.51%(蔗糖:1.37%、葡萄糖:1.16%、β
‑
环糊精:3.51%);ca回收率随海藻糖浓度上升而上升。从海藻糖浓度0.5%时ca回收率71.89
±
1.16%上升至海藻糖浓度2.0时ca回收率76.95
±
1.56%;在甘露醇浓度为0.5%
‑
1.5%时,ca回收率随甘露醇浓度上升而下降,从甘露醇浓度分别为72.48
±
2.44%、68.57
±
1.32%、65.28
±
0.48%,甘露醇浓度在1.5%
‑
2.0%时,ca回收率变化幅度较小。
[0093]
同浓度下ca回收率最高的组时蔗糖组,其次是海藻糖组,在海藻糖浓度为2.0%,ca回收率最高,基本与加入2%的蔗糖相同(海藻糖组ca回收率76.95
±
1.56%,蔗糖组76.89
±
1.77%);此外加入浓度为1.5%与2.0%的蔗糖时,ca的酶活回收率也十分接近,分别为76.56
±
2.05%和76.89
±
1.77%。
[0094]
综合各酶活保护剂对不同酶的的影响,蔗糖和海藻糖对酶活回收率的包护作用明显高于其他酶活保护剂,蔗糖浓度为1.5%时sod酶回收率达到最高,浓度为2.0%时cat回收率最高;海藻糖浓度为2.0%,ca回收率最高,与加入1.5%与2.0%的蔗糖时,ca的酶活回收率十分接近,因此本申请更优选终浓度为1.5
‑
2%(w/v)的蔗糖或海藻糖作为酶活保护剂。
[0095]
通过上述实验可以看出,当采用本申请的酶活保护剂时,sod和cat的酶活回收率在45%以上,ca的酶活回收率在65%以上;优选地,当采用蔗糖或海藻糖作为酶活保护剂时,sod和cat回收率可达到55%以上,ca的酶活回收率在70%以上;更优选地,当采用终浓度为1.5
‑
2%(w/v)的蔗糖或海藻糖作为酶活保护剂时,sod回收率可达到65%
‑
70%,cat酶活回收率在60%左右,ca的酶活回收率在75%以上。可见,采用本申请的方法制备的人源性血红蛋白类氧载体酶活回收率高,酶活损失少,进而也具有更高的载氧能力。
[0096]
以上所述仅为本发明的较佳实施例而已,并非用于限定本发明的保护范围。凡在本发明的精神和原则之内所作的任何修改、等同替换、改进等,均包含在本发明的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1