通过合理设计增强的新型AAV病毒在视网膜中的高效转导和侧向扩散
通过合理设计增强的新型aav病毒在视网膜中的高效转导和侧向扩散
1.相关申请
2.本申请要求于2019年1月23日提交的美国临时申请no.62/795,695的申请日的权益,其全部内容通过引用并入本文。
3.联邦资助的研究
4.本发明是在美国国立卫生研究院授予的授权号r01 ey024280的政府支持下完成的。政府对本发明享有一定的权利。
技术领域
5.本发明一般性地涉及分子生物学和病毒学领域,特别地涉及用于治疗视网膜疾病的基因治疗载体和方法的开发。
背景技术:
6.通过使用病毒传递治疗性遗传物质,基因治疗领域已取得了重大进展。由于腺相关病毒的低免疫原性和对非分裂细胞进行有效转导的能力,作为用于基因治疗的高效病毒载体的腺相关病毒已吸引了相当多的关注。aav已显示可感染多种细胞和组织类型,并且在过去十年中取得了重大进展,使这种病毒系统适用于人基因治疗。
7.在aav的正常的“野生型”形式中,aav dna作为长度为约4600个核苷酸(nt)的单链分子被包装到病毒衣壳中。病毒感染细胞后,细胞的分子机制将单链dna转化为双链形式。只有这种双链dna形式才可能被细胞酶转录成rna,然后通过其他细胞途径将其翻译成多肽。
8.重组腺相关病毒(adeno
‑
associated virus,aav)载体已成功用于人疾病的多种临床前动物模型的体内基因转移,并已成功用于广泛多种治疗性基因的长期表达(daya and berns,2008;niemeyer et al.,2009;owen et al.,2002;keen
‑
rhinehart et al.,2005;scallan et al.,2003;song et al.,2004)。aav载体当靶向免疫特权位点时(例如,用于莱贝尔先天性黑蒙(leber’scongenial amaurosis)的眼部递送),也在人中产生了长期的临床益处(bainbridge et al.,2008;maguire et al.,2008;cideciyan et al.,2008)。这种载体的一个主要优点是其相对低的免疫谱,仅引起有限的炎症响应,并且在某些情况下,甚至指导对转基因产物的免疫耐受(loduca et al.,2009)。尽管如此,当靶向非免疫特权器官时,由于针对病毒衣壳的抗体和cd8+t细胞响应,治疗效率在人中被限制,而在动物模型中,也报道了对转基因产物的适应性响应(manno et al.,2006;mingozzi et al.,2007;muruve et al.,2008;vandenberghe and wilson,2007;mingozzi and high,2007)。
9.当视网膜色素上皮(retinal pigment epithelium,rpe)或光感受器(photoreceptor,pr)中需要转基因表达时,通常使用aav的视网膜下注射。视网膜下注射产生暂时的大泡性脱离,将光感受器外段与rpe层隔开。通常来说,对象中的视网膜下注射泡
(bleb)会在接下来的几天内消退。视网膜下注射可能对光感受器有一些有害影响,可想象,这样的影响在已经因疾病受损的视网膜中更为严重。特别地,已经提出在接受视网膜基因治疗治疗的rpe65
‑
lca患者中的中央凹(fovea)脱离可能是有害的(参见jacobson et al.,gene therapy for leber congenital amaurosis caused by rpe65 mutations:safety and efficacy in 15children and adults followed up to 3years,arch ophthalmol.2012;130(1):9
‑
24)。
10.仍然需要aav衣壳来提高视网膜转导效率并使视网膜下注射过程中中央凹的脱离最小化。
技术实现要素:
11.aav已成为将治疗性基因靶向视网膜的首选载体。天然存在的和合成的aav二者均已被鉴定为显示视网膜嗜性。最近,从取自正常恒河猴肾细胞培养物的猿猴腺病毒sv15的实验室储备中分离出一种新型aav衣壳血清型44.9。参考2016年11月17日公开的wo 2016/183297;2018年12月13日公开的美国专利公开no.2018/0355376;和novel adeno
‑
associated virus for gene therapy,fed.reg.80,149(2015年8月4日),其各自的全部内容整体并入本文。aav44.9有效转导多种细胞类型,包括唾液腺细胞、肝细胞和不同类型的神经元(例如,皮层细胞、嗅球细胞、脑干细胞和小脑purkinje细胞)。
12.aav44.9表现出与aav9相当的体内生物分布。这种衣壳的脑室内注射已显示出在皮层、嗅球、小脑、脉络丛和脑干中的转导水平与aav9观察到的那些相似。此外,抗体中和研究表明,与aav2相比,aav44.9中和抗体的频率较低。并且aav44.9的聚糖阵列研究已表明衣壳与末端含葡萄糖分子的结合。
13.aav44.9的衣壳蛋白vp1的氨基酸序列与报道最密切的分离株aavrh.8r的衣壳蛋白vp1的氨基酸序列在几个位置处不同(参见vandenberghe lh et al.,naturally occurring singleton residues in aav capsid impact vector performance and illustrate structural constraints,gene ther.16:1416
‑
1418(2009);vandenberghe lh,et al.,aav9 targets cone photoreceptors in the nonhuman primate retina,plos one 8(1):e53463(2013)),其中两个是可变结构域3中的丝氨酸残基。特别地,aav44.9的衣壳蛋白vp1的氨基酸序列相对于aavrh.8r的衣壳蛋白vp1的氨基酸序列在第179、473和483位不同。
14.aav44.9的衣壳蛋白vp1的氨基酸序列与密切报道的分离株aavrh.8的衣壳蛋白vp1的氨基酸序列(参见gao et al.,j.virol.78(12):6381
‑
6388(2004))在几个位置不同,其中两个是可变结构域3中的丝氨酸残基。特别地,aav44.9的衣壳蛋白vp1的氨基酸序列相对于aavrh.8的衣壳蛋白vp1的氨基酸序列在第179、473、483和531位不同。
15.衣壳蛋白中氨基酸的合理诱变研究已表明,某些突变对载体的基因转移活性具有抑制作用,特别是可变区中丝氨酸和苏氨酸残基的存在。报告表明,这些氨基酸增加了颗粒的表面电荷,并将它们作为靶标用于溶酶体中的降解,并且用其他不带电的氨基酸进行置换可提高转导活性。此外,与受体相互作用有关的残基突变也对视网膜转导和嗜性有很大影响。在视网膜的背景下,已经显示出含有表面暴露的酪氨酸到苯丙氨酸(y
‑
f)突变的aav2和aav8衣壳显示出相对于未经修饰衣壳的增强的视网膜转导。
16.鉴于在aav44.9的衣壳蛋白vp1的可变结构域3中相对于aavrh.8的衣壳蛋白vp1包含另外的丝氨酸残基,aav44.9在许多细胞类型中具有高基因转移活性。wo2016/183297中公开了aav44.9的衣壳蛋白vp1,其第470位的丝氨酸被天冬酰胺置换。当aav2衣壳中类似的丝氨酸残基发生改变时,它导致制成的载体的滴度大幅增加,尽管它不会改变转导效率(参见aslanidi et al.,high
‑
efficiency transduction of human monocyte
‑
derived dendritic cells by capsid
‑
modified recombinant aav2vectors,vaccine,30(26):3908
‑
3917(2012))。尽管如此,认为aav44.9中的s470r置换改变了aav44.9衣壳的转导和结合亲和力。
17.本公开内容的发明人使用合理设计方法通过将第531位残基处的谷氨酸诱变为天冬氨酸来设计新变体。这种新的血清型变体aav44.9(e531d)在视网膜下注射的小鼠和猕猴中进行了评价。已经假设在对应于aav2衣壳中e530位的位置(例如aavrh.8和aav44.9中的531位)处的氨基酸置换会改变转导效率。参见2018年8月30日公开的国际专利公开no.wo 2018/156654,其内容通过引用并入本文。
18.如本文所述,出乎意料地发现并入aav44.9(e531d)衣壳变体的raav颗粒能够在视网膜下注射之后高效转导视杆、视锥和视网膜色素上皮(“rpe”)。此外,aav44.9(e531d)表现出增强的侧向扩散,转导视网膜下注射泡外侧的光感受器和视网膜色素上皮。aav44.9(e531d)的增强的效力和侧向扩散使该变体成为靶向视网膜的基因治疗的有前途的载体。
19.在富含视锥的中央凹下进行视网膜下注射已显示会促进一些受治疗的患者中的中央视网膜厚度的损失以及视觉敏锐度的损失(rpe65
‑
lca2的i/ii期试验)。参见jacobson et al.,arch ophthalmol.2012;130(1):9
‑
24。然而,中央凹外视网膜的视网膜下注射耐受性良好。因此,在中央凹外视网膜下注射之后使用有效靶向中央凹视锥的载体可能是有利的,即中央凹在手术过程中不脱离。目前用于色盲和其他遗传性视网膜疾病的临床试验的载体不符合此标准。视网膜向注射位点的转导是新一代aav载体的一个理想特征,因为超出视网膜下泡的初始边界的转基因表达可能会在使有益的基因治疗效果最大化同时避免视网膜脱离的一些有害影响。例如,在人对象中,转导的侧向扩散可允许在中央凹旁(parafoveal)区域进行视网膜下注射,以产生对中央凹细胞的转导,同时避免诱发中央凹脱离的有害影响。最近,在正常狗中的视网膜下递送aav载体后,表达egfp的aav载体表现出转基因表达超出视网膜下注射位点的侧向扩散。参见breuwer et al.,evaluation of lateral spread of transgene expression following subretinal aav
‑
mediated gene delivery in dogs,plos one,2013;8(4):e60218。
20.中央凹旁区域是环绕中央凹的眼区域,距中央注视点约4度偏心率。中央凹旁具有最高密度的视杆,同时还含有大量视锥。它是视锥和视杆为主的视网膜之间的过渡区,在其中变性从外层进行到内层视网膜的疾病(例如视网膜色素变性(rp))的情况下是重要的。中央凹周围区域是环绕中央凹旁的区域,代表黄斑(macula)的最外带。像中央凹旁一样,中央凹周围在像rp的其中视网膜退化从周边开始并进展到中央视网膜的疾病的进展中具有重要作用。中央凹周围是在rp中黄斑经历变性的第一区域。
21.本公开内容的一些方面涉及用于治疗眼的包含经修饰的aav44.9衣壳的raav颗粒和载体。特别地,在一些实施方案中,本公开内容提供了用于治疗视网膜障碍的包含具有e531d突变的aav44.9衣壳的颗粒。在一些实施方案中,本公开内容提供了包含aav44.9
(e531d)衣壳的颗粒,所述衣壳在视网膜下注射至中央凹后表现出增强的侧向扩散,其中使中央凹的脱离最小化。在一些实施方案中,本公开内容提供了衣壳蛋白,例如,vp1、vp2或vp3衣壳蛋白,其分别包含seq id no:1、2或3中任一个的氨基酸序列。
22.在一些实施方案中,本公开内容提供了包含衣壳的raav颗粒,所述衣壳包含vp1、vp2和/或vp3蛋白,其中所述raav颗粒还包含含有异源核酸序列的多核苷酸。
23.在一些实施方案中,raav颗粒中的异源核酸序列编码诊断或治疗剂,例如多肽、肽、核酶、肽核酸、sirna、rnai、向导rna、反义寡核苷酸、反义多核苷酸、抗体、抗原结合片段或其任意组合。
24.在一些具体的实施方案中,治疗剂a)保护一个或更多个感光(pr)细胞或者一个或更多个视网膜色素上皮(“rpe”)细胞,b)恢复一个或更多个视杆和/或视锥介导的功能,c)全部或部分恢复一只或两只眼的视觉行为,或d)其任意组合。在一些实施方案中,在将所述raav颗粒初始施用至哺乳动物的一只或两只眼中之后,所述治疗剂的产生在一个或更多个感光细胞或者一个或更多个rpe细胞中基本上持续至少三个月的时间段。
25.在一些实施方案中,异源核酸序列包含与例如以下的疾病、障碍或病症相关的序列(例如,与目标编码序列具有至少80%同一性的序列):显性视锥营养不良;显性视锥
‑
视杆营养不良;莱贝尔先天性黑蒙;隐性视锥营养不良;隐性视锥
‑
视杆营养不良;黄斑营养不良;模式营养不良(pattern dystrophy);卵黄状营养不良;中心性脉络膜营养不良;眼底黄色斑点症(stargardt disease);常染色体显性、常染色体隐性和x连锁视网膜色素变性;与bardet
‑
biedl综合征相关的视网膜色素变性;x连锁青少年视网膜劈裂症;色盲;蓝视锥全色盲症(blue cone monochromacy);和i、ii和iii型usher综合征。在一些实施方案中,异源核酸序列(例如,与目标编码序列具有至少80%同一性的序列)包含与例如以下的疾病、障碍或病症相关的序列:迪谢内肌营养不良、肢带型肌营养不良、脊髓性肌萎缩症、糖原贮积症ⅱ型(pompe disease)、弗里德里希共济失调、黏多糖贮积症(mps)(所有形式)、溶酶体贮积症(lysosomal storage disease,lsd)(所有形式)、肌萎缩侧索硬化症(als)、帕金森病和阿尔茨海默病。
26.在一些实施方案中,异源核酸序列与目标编码序列具有至少80%的同一性。在一些实施方案中,异源核酸序列与目标编码序列具有至少95%的同一性。在一些实施方案中,异源核酸序列与目标编码序列具有至少98%或至少99%的同一性。在一些实施方案中,异源核酸序列与目标编码序列具有100%的同一性。在一些实施方案中,异源核酸序列包含gucy2d序列。
27.在一些实施方案中,异源核酸序列是替代编码序列(replacement coding sequence)。在一些具体的实施方案中,向对象施用替代编码序列以提供功能性蛋白质,例如gucy2d,以恢复例如对象(例如人)的完全或部分的光感受器功能。在一些实施方案中,通过将包含本文公开的异源核酸序列的raav颗粒施用至对象(例如,施用至患有显性视锥
‑
视杆营养不良的人)来沉默对象的目标编码序列的一个或两个等位基因。
28.示例性的目标编码序列包括:gucy2d和gucy2e,它们与显性视锥营养不良、显性视锥
‑
视杆营养不良和莱贝尔先天性黑蒙相关;spata7,与莱贝尔先天性黑蒙相关;prph2,与莱贝尔先天性黑蒙和常染色体显性视网膜疾病(例如,视网膜色素变性、模式营养不良、卵黄状营养不良、中心性脉络膜营养不良和黄斑营养不良)相关。gucy2d编码视网膜鸟苷酸环
化酶1(retgc1)酶,也称为鸟苷酸环化酶2d。该基因的突变导致莱贝尔先天性黑蒙和视锥
‑
视杆营养不良
‑
6障碍。gucy2e编码鸟苷酸环化酶2e(gucy2d的鼠同源物)。
29.其他的目标编码序列可包括aipl1、lca5、rpgrip1、crx、crb1、nmnat1、cep290、impdh1、rd3、rdh12、tulp1、kcnj13、gdf6和iqcb1(均与莱贝尔先天性黑蒙相关);bbs1、bbs2、arl6/bbs3、bbs4、bbs5、bbs7、ttc8/bbs8、bbs10、trim32/bbs11、bbs12、ccdcc28b、cep290、tmem67、mks1和mkks(均与bardet
‑
biedl综合征(bbs)相关);rho、prpf31、rp1、nrl和nr2e3(均与常染色体显性视网膜色素变性相关);rpgr和rp2(均与x连锁视网膜色素变性相关);pde6a、pde6b、pde6g、rp25、cnga1、cngb1和mak(均与常染色体隐性视网膜色素变性相关);rs1(与x连锁青少年视网膜劈裂症(xlrs)相关);cngb3、cnga3和gnat2(均与色盲相关);opn1lw和opn1mw(均与蓝视锥全色盲症(blue cone monochromacy,bcm)相关;crx、guca1a(gcap1)和guca1b(gcap2)(均与显性视锥营养不良和显性视锥
‑
视杆营养不良相关);abca4(与隐性视锥营养不良、隐性视锥
‑
视杆营养不良、黄斑营养不良和眼底黄色斑点症相关);prom1和elovl4(均与眼底黄色斑点症相关);myo7a、ush1c、cdh23、pcdh15和ush1g(均与i型usher综合征相关);ush2a和dfnb31(均与ii型usher综合征相关);和clrn1(与iii型usher综合征相关)。
30.在一些实施方案中,异源核酸序列包含与例如蓝视锥全色盲症的疾病、障碍或病症相关的目标基因组调节序列(例如,基因座控制区)。示例性目标调节序列是l/m视蛋白的基因座控制区,它与蓝视锥全色盲症相关。
31.在一些方面中,本公开内容提供了包含raav颗粒和可药用载体、赋形剂、稀释剂和/或缓冲剂的组合物。
32.在一些方面中,本公开内容提供了用于转导rpe和感光细胞以调节对象中异源核酸序列(或转基因)的表达的方法,该方法包括向对象(例如人对象)施用包含如本文所述的raav颗粒和可药用载体、赋形剂、稀释剂和/或缓冲剂的组合物。在一些方面中,本公开内容提供了用于治疗对象的视网膜疾病的方法,该方法包括向对象的眼施用组合物。
33.在一些方面中,本公开内容提供了用于治疗视网膜疾病的组合物和用于制备治疗视网膜疾病的药物的组合物。在一些方面中,本公开内容提供了包含如本文所述的raav颗粒的组合物,用于通过向哺乳动物的一只或两只眼经视网膜下或玻璃体内施用来治疗。
34.在一些方面中,本公开内容提供了用于在哺乳动物的一个或更多个感光细胞或rpe细胞中表达核酸区段的方法,所述方法包括:向所述哺乳动物的一只或两只眼经视网膜下或玻璃体内施用如本文所述的raav颗粒持续有效地在所述哺乳动物的一个或更多个pr细胞或rpe细胞中产生所述治疗剂的一段时间,其中所述raav颗粒包含多核苷酸,所述多核苷酸包含至少第一多核苷酸,所述第一多核苷酸包含与编码治疗剂的至少第一异源核酸序列有效地连接的pr
‑
或rpe
‑
细胞特异性启动子。
35.raav颗粒可包含多种(两种、三种、四种、五种、六种、七种、八种、九种或十种)异源核酸序列。在某些实施方案中,多种异源核酸序列包含在单个多核苷酸分子上。例如,可使用多种异源核酸序列来纠正或改善由多亚基蛋白引起的基因缺陷。在多个实施方案中,不同的异源核酸序列可用于编码蛋白质的每个亚基,或用于编码不同的肽或蛋白质。这在编码蛋白质亚基的核酸的尺寸大时,例如对于免疫球蛋白、血小板来源的生长因子或肌养蛋白是理想的。为了使细胞产生多亚基蛋白,细胞用含有不同亚基中的每一个的raav颗粒感
染。或者,蛋白质的不同亚基可由相同的核酸序列编码。在多个实施方案中,单个异源核酸序列包括编码每个亚基的核酸,其中针对每个亚基的核酸被内部核酶进入位点(internal ribozyme entry site,ires)隔开。当编码每个亚基的核酸的尺寸小时,例如,编码亚基的核酸和ires的总尺寸小于5千碱基时,这是理想的。
36.作为ires的一个替代方案,核酸可被编码2a肽的序列隔开,该肽在翻译后事件中自我切割。这种2a肽明显小于ires,使其非常适合在空间为限制因素的情况下使用。更常见的是,在异源核酸序列很大,由多亚基组成,或两个异源核酸序列被共同递送,或携带所需一种或更多种异源核酸序列或亚基的raav颗粒被共同施用以允许它们在体内多连体化(concatamerize)以形成单个载体基因组的情况下。在这样的实施方案中,第一raav颗粒可携带表达单一异源核酸序列的表达盒,并且第二raav颗粒可携带表达不同异源核酸序列的表达盒以在宿主细胞中共表达。然而,选定的异源核酸序列可编码任何生物活性产物或其他产物,例如对于研究理想的产物。
37.在一些实施方案中,raav颗粒内的多核苷酸包含调节序列,例如转录和翻译起始和终止密码子,其对待引入raav颗粒的宿主类型(例如,细菌、真菌、植物或动物)具有特异性。优选地,raav颗粒内的核酸分子包含对宿主的属具有特异性的调节序列。最优选地,该分子包含对宿主的种具有特异性的调节序列。
38.raav颗粒内的多核苷酸优选包含在宿主细胞中提供一种或更多种异源核酸序列表达的表达控制序列,例如启动子、增强子、多腺苷酸化信号、转录终止子、内部核糖体进入位点(ires)等。示例性表达控制序列是本领域已知的并且描述于例如goeddel,gene expression technology:methods in enzymology,vol.185,academic press,san diego,ca.(1990)中。
附图说明
39.以下附图构成本说明书的一部分,并被包括在内以说明本发明的某些方面。结合附图参考以下描述可更好地理解本发明,其中相似的附图标记表示相似的元件,并且其中:
40.图1示出了基于vp1的aav系统发育(aav44.9以粗体显示)和具有用于载体制备的aav构建体的详细信息的表格。
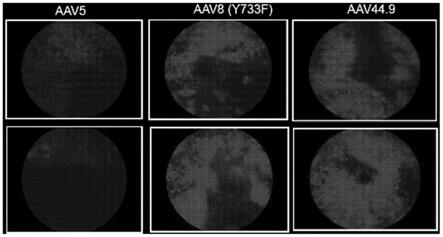
41.图2a、2b、2c、2d和2e示出了视网膜下注射4周时aav44.9、aav5和aav8(y733f)的定性和定量分析。图2a示出了曝光长25的眼底图像。图2b至2d示出了流式细胞术散点图,并且图2e示出了显示在视网膜下注射2
×
109载体基因组(vg)后,aav44.9比aav5和aav8(y733f)更有效地转导视杆的定量分析。
42.图3a、3b和3c示出了代表性视网膜横截面图像,显示了注射aav5(上图,图3a)、aav8(y733f)(上图,图3b)aav44.9(上图,图3c)的nrl
‑
gfp转基因小鼠视网膜中在视网膜下注射之后4周时光感受器和视网膜色素上皮(“rpe”)中的mcherry表达。图3a、3b和3c的下图示出了核dapi染色、视杆细胞中的内源性gfp表达和感光细胞中的mcherry表达的合并图像,如箭头所示。
43.图4a、4b和4c示出了aav44.9(y733f)和aav44.9(e531d)的定性和定量分析。图4a示出了曝光长25时的眼底图像,图4b示出了流式细胞术散点图,并且图4c示出了通过显示出在视网膜下注射2
×
109vg后aav44.9(e531d)比aav44.9和aav44.9(y733f)更有效地转导
视杆细胞的定量分析。
44.图5a和5b示出了代表性视网膜横截面图像,其示出了注射aav44.9(y733f)(上图,图5a)和aav44.9(e531d)(上图,图5b)的nrl
‑
gfp小鼠视网膜中在视网膜下注射之后4周时主要在光感受器和rpe中的mcherry表达。图5a和5b的下图示出了核dapi染色(蓝色)、视杆细胞中的内源性gfp(绿色)表达和感光细胞中的mcherry表达(红色)的合并图像。
45.图6a和6b示出了aav44.9和aav44.9(y733f)在眼细胞系中的转导效率。aav44.9(y733f)在小鼠视锥感光细胞系中显示出相对于aav44.9的提高的转导(图6a)。然而,aav44.9在人rpe细胞系中比aav9(y733f)更有效(图6b)。
46.图7a和7b示出了玻璃体内注射之后aav的定性分析。图7a示出了aav2、aav5、aav8(y733f)、aav44.9、aav44.9(y733f)和aav44.9(e531d)的眼底图像(以长25的积分(integration)),图7b示出了玻璃体内注射2
×
109vg 4周时的眼底图像(以长100的积分)变体。
47.图8a、8b和8c示出了含有视锥优先嵌合irbp增强子
‑
视锥转导蛋白启动子(irbp/gnat2)和gfp报道子的aav44.9,显示出图8a示出了sr注射之后4周视锥细胞中的gfp表达。图8b和8c示出了用视锥
‑
抑制蛋白抗体与gfp荧光共定位的共染色。
48.图9a示出了视网膜下注射aav44.9或aav44.9(e531d)之后4周采集的nrl
‑
gfp小鼠的代表性眼底图像(红色荧光滤光片)。载体以1ul中2v
×
109vg递送。曝光和增益设置在整个实验过程中一致。
49.图9b示出了在注射之后4周采集的每个细胞群的转导百分比和相应值。将nrl
‑
gfp小鼠(来自图9a)的视网膜用木瓜蛋白酶解离,并进行流式细胞术以量化经转导视杆(gfp+mcherry阳性)或非视杆细胞(mcherry阳性)的百分比,如之前在boye et al.,impact of heparan sulfate binding on transduction of retina by recombinant adeno
‑
associated virus vectors,j.virol.2016,90(8):4215
‑
4231中描述的,其全部内容通过引用并入本文。
50.图10a示出了视网膜下注射aavrh.8
‑
mcherry之后4周采集的nrl
‑
gfp小鼠的代表性眼底图像。载体以1ul中2
×
109vg递送。曝光和增益设置在整个实验过程中一致。
51.图10b示出了在注射之后4周取得的每个细胞群的转导百分比和相应值。将nrl
‑
gfp小鼠(来自图9a和10a)的视网膜用木瓜蛋白酶解离,并进行流式细胞术以量化经转导的视杆(gfp+mcherry阳性)或非视杆细胞(mcherry阳性)的百分比。
52.图11a示出了用较低滴度的自身互补aav44.9(“scaav44.9”)、scaav44.9(e531d)或scaavrh.8视网膜下注射之后4周采集的nrl
‑
gfp小鼠的代表性眼底图像。载体以1ul中2
×
108vg递送。曝光和增益设置在整个实验过程中一致。
53.图11b示出了在注射之后4周采集的每个细胞群的转导百分比和相应值。nrl
‑
gfp小鼠(来自图11a)的视网膜用木瓜蛋白酶解离并进行流式细胞术以量化经转导的视杆(gfp+mcherry阳性)或非视杆细胞(mcherry阳性)的百分比。
54.图12示出了在视网膜下注射之后6周,在视锥特异性irbpe
‑
gnat2嵌合启动子的情况下,aav44.9(e531d)和未经修饰的aav44.9的定性分析。示出了视网膜下注射2
×
10
12
vg后aav44.9(e531d)
‑
irbp/gnat2
‑
hgfp和aav44.9
‑
irbp/gnat2
‑
hgfp的眼底图像。
55.图13示出了视网膜下注射aav44.9(e531d)
‑
irbp/gnat2
‑
hgfp之后6周采集的wt小
鼠的代表性视网膜横截面。载体以1ul中2
×
10
12
vg递送。切片用抗gfp(绿色)和视锥抑制蛋白(红色)的抗体进行免疫染色。
56.图14示出了在视网膜下注射aav44.9
‑
irbp/gnat2
‑
hgfp之后6周采集的wt小鼠的代表性视网膜横截面。载体以1ul中2
×
10
12
vg递送。切片用抗gfp和视锥抑制蛋白的抗体进行免疫染色,如箭头所示。
57.图15示出了aav44.9
‑
hgrk1
‑
gfp和aav44.9(e531d)
‑
hgrk1
‑
gfp在视网膜下注射的猕猴中表现出增强的侧向扩散和效力。载体以1
×
10
12
vg vg/ml递送。给药当天泡的初始边界和产生的gfp表达的边界用白色虚线标出。相同的脉管系统以加粗的深色线突出显示以供参考。
58.图16示出了在猕猴中的中央凹外视网膜下注射aav44.9
‑
hgrk1
‑
gfp(1
×
10
12
vg/ml)后产生的三个视网膜下注射泡的光学相干断层成像(oct)扫描(参见左侧的负对比眼底图像)。
59.图17示出了中央凹外视网膜下注射aav44.9
‑
hgrk1
‑
gfp后猕猴视网膜的oct图像。slo图像(左上角)中的箭头指示在图的较下部分的扫描中显示的视网膜切片的位置。将切片针对视锥抑制蛋白和dapi进行染色。在每个区域中绘制表达gfp的视杆/视锥的百分比。onl,外核层;inl,内核层;gcl,神经节细胞层。
60.图18a和18b示出了视网膜下注射aav44.9(e531d)
‑
hgrk1
‑
gucy2e或aav8(y733f)
‑
hgrk1
‑
gucy2e后视网膜鸟苷酸环化酶1/2双敲除(gcdko)小鼠的erg记录。图18a示出了暗视(左)和明视(右)二者设置下的平均最大a波和b波振幅。图18b示出了用载体处理的眼或对侧未经处理(“无tx”)的眼的视锥的代表性erg轨迹。
61.图19示出了中央凹外视网膜下注射aav44.9(e531d)
‑
hgrk1
‑
gfp后猕猴视网膜的oct图像。slo图像(左上角)中的箭头指示在图的较下部分的扫描中显示的视网膜切片的位置。将切片针对视锥抑制蛋白和dapi染色。在每个区域中绘制表达gfp的视杆/视锥的百分比。
62.图20a、20b、20c和20d示出了中央凹外视网膜下注射aav44.9(e531d)
‑
hgrk1
‑
gfp和aav44.9
‑
hgrk1
‑
gfp后猕猴视网膜中央凹旁区域的代表性oct图像。比例尺的单位为a=40微米,b=20微米。
63.图21a和21b示出了在这些注射之后猕猴视网膜中央凹周围区域的代表性oct图像。
具体实施方式
64.本公开内容提供了aav44.9(e531d),衣壳血清型aav44.9的新变体,以及相对于基准载体密切相关的aavrh.8和未经修饰的aav44.9,在视网膜下注射的小鼠和猕猴中并入该质粒的载体和颗粒的性能评价。如本文所述,发现aav44.9(e531d)相对于未经修饰的aav44.9和aavrh.8介导更高的视网膜转导,并且两个种类的转导均显著高于基准衣壳(例如,基于aav5和aav8的载体)。
65.因此,本公开内容提供了包含aav44.9(e531d)的衣壳蛋白的raav颗粒及相关组合物和方法。在一些实施方案中,raav颗粒包含异源核酸序列,例如编码治疗剂或诊断剂的核酸序列。异源核酸序列可以是单链(ss)或自身互补(sc)aav核酸载体的形式,例如是单链或
自身互补重组病毒基因组的形式。
66.本公开内容还提供了包含aav44.9(y733f)的衣壳蛋白的raav颗粒及相关组合物和方法。这种aav44.9衣壳变体在第733位残基处具有y
‑
f突变。在一些实施方案中,raav颗粒包含异源核酸序列,例如编码治疗剂或诊断剂的核酸序列。异源核酸序列可以是单链(ss)或自身互补(sc)aav核酸载体的形式,例如是单链或自身互补重组病毒基因组的形式。
67.本公开内容的一些方面涉及包含aav44.9(e531d)衣壳的载体,该衣壳在视网膜下注射到中央凹后表现出增强的侧向扩散,其中使中央凹的脱离(例如,暂时性大泡性脱离)最小化。在一些实施方案中,本公开内容提供了衣壳蛋白,例如vp1、vp2或vp3衣壳蛋白,其包含seq id no:1、2或3的氨基酸序列。
68.在一些实施方案中,本公开内容提供了raav颗粒,其包含含有vp1、vp2和/或vp3蛋白的衣壳,其中所述raav颗粒还包含含有异源核酸序列的多核苷酸。在一些实施方案中,raav颗粒包含含有vp1、vp2和/或vp3蛋白的衣壳,其中vp1蛋白包含seq id no:1的氨基酸序列,vp2蛋白包含seq id no:2的氨基酸序列,和/或vp3蛋白包含seq id no:3的氨基酸序列,并且其中aav还包含含有异源核酸序列的多核苷酸。异源核酸序列的侧翼可以是一个或更多个末端反向重复(itr)序列。
69.在一些实施方案中,本公开内容提供了包含seq id no:1、2和/或3的氨基酸序列的衣壳蛋白。
70.在一些实施方案中,本公开内容提供了核酸,例如质粒或病毒载体,该核酸包含seq id no:4的核酸序列(其编码aav44.9(e531d)vp1)。在一些实施方案中,本公开内容提供了核酸,例如质粒或病毒载体,该核酸包含seq id no:5的核酸序列(其编码aav44.9(e531d)vp2)。在一些实施方案中,本公开内容提供了核酸,例如质粒或病毒载体,该核酸包含seq id no:6的核酸序列(其编码aav44.9(e531d)vp3)。在一些实施方案中,病毒载体是重组腺相关病毒(raav)载体。在一些实施方案中,raav载体是自身互补的。在一些实施方案中,核酸包含在细胞内,例如哺乳动物或昆虫细胞内。
71.seq id no:1至8的序列如下所提供。
72.seq id no:1
‑
aav44.9(e531d)vp1氨基酸序列
73.[0074][0075]
seq id no:2
‑
aav44.9(e531d)vp2氨基酸序列
[0076][0077]
seq id no:3
‑
aav44.9(e531d)vp3氨基酸序列
[0078][0079]
seq id no:4
‑
aav44.9(e531d)vp1氨基酸序列
[0080][0081]
seq id no:5
‑
aav44.9(e531d)vp2氨基酸序列
[0082][0083]
seq id no:6
‑
aav44.9(e531d)vp3氨基酸序列
[0084]
[0085][0086]
seq id no:7
‑
aav44.9野生型vp1氨基酸序列
[0087][0088]
seq id no:8
‑
aav44.9野生型vp1核苷酸序列
[0089][0090][0091]
产生和使用假型化raav载体的方法是本领域中已知的(参见,例如duan et al.,j.virol.,75:7662
‑
7671,2001;halbert et al.,j.virol.,74:1524
‑
1532,2000;
zolotukhin et al.,methods,28:158
‑
167,2002;以及auricchio et al.,hum.molec.genet.,10:3075
‑
3081,2001)。产生raav颗粒和异源核酸的方法也是本领域中已知的并且是市售的(参见,例如zolotukhin et al.production and purification of serotype 1,2,and 5recombinant adeno
‑
associated viral vectors.methods 28(2002)158
‑
167;以及美国专利公开号us 2007/0015238和us2012/0322861,其通过引用整体并入本文;以及可从atcc和cell biolabs,inc.获得的质粒和试剂盒)。例如,可将包含异源核酸序列的质粒与一种或更多种辅助质粒(例如包含rep基因(例如编码rep78、rep68、rep52和rep40)和cap基因(编码vp1、vp2和vp3,包括如本文所述的经修饰的vp3区域)组合并转染或永久整合到生产细胞系中,使得raav颗粒可包装并随后纯化。
[0092]
在一些实施方案中,一种或更多种辅助质粒包括包含rep基因和cap基因(例如,编码如本文所述的raav衣壳蛋白)的第一辅助质粒和包含e1a基因、e1b基因、e4基因、e2a基因和va基因的第二辅助质粒。在一些实施方案中,rep基因是源自aav2的rep基因,并且cap基因源自aav44.9且可包含对该基因的修饰以产生如本文所述的经修饰的衣壳蛋白。辅助质粒和制备这样的质粒的方法是本领域中已知的并且是市售的(参见,例如来自plasmidfactory,bielefeld,germany的pdm、pdg、pdp1rs、pdp2rs、pdp3rs、pdp4rs、pdp5rs、pdp6rs、pdg(r484e/r585e)和pdp8.ape质粒;其他产品和服务,其可获自vector biolabs,philadelphia,pa;cellbiolabs,san diego,ca;agilent technologies,santa clara,ca;和addgene,cambridge,ma;pxx6;grimm et al.(1998),novel tools for production and purification of recombinant adenoassociated virus vectors,human gene therapy,vol.9,2745
‑
2760;kern,a.et al.(2003),identification of a heparin
‑
binding motif on adeno
‑
associated virus type 2capsids,journal of virology,vol.77,11072
‑
11081.;grimm et al.(2003),helper virus
‑
free,optically controllable,and two
‑
plasmid
‑
based production of adeno
‑
associated virus vectors of serotypes 1to 6,molecular therapy,vol.7,839
‑
850;kronenberg et al.(2005),aconformational change in the adeno
‑
associated virus type 2capsid leads to the exposure of hidden vp1n termini,journal of virology,vol.79,5296
‑
5303;以及moullier,p.and snyder,r.o.(2008),international efforts for recombinant adeno
‑
associated viral vector reference standards,molecular therapy,vol.16,1185
‑
1188)。
[0093]
接下来描述一种示例性的非限制性raav颗粒产生方法。产生或获得一种或更多种辅助质粒,其包含期望aav血清型的rep和cap orf以及在其天然启动子的转录控制下的腺病毒va、e2a(dbp)和e4基因。cap orf还可包含一个或更多个修饰以产生如本文所述的经修饰的衣壳蛋白。利用辅助质粒和包含本文所述核酸载体的质粒,通过capo4介导的转染、脂质或聚合物分子如聚乙烯亚胺(pei)转染hek293细胞(可获自)。然后将hek293细胞孵育至少60小时以允许raav颗粒产生。作为替代地,在另一个实例中,用包含异源核酸序列的单一重组杆状病毒感染基于sf9的稳定生产细胞系。作为另一替代方案,在另一个实例中,用包含异源核酸序列的hsv和任选地包含如本文所述的rep和cap orf以及在其天然启动子的转录控制下的腺病毒va、e2a(dbp)和e4基因的一种或更多种辅助hsv感染hek293或bhk细胞系。然后将hek293、bhk或sf9细胞孵育至少60小时以允许raav颗粒产生。然后可使用本领域中已知或本文所述的任何方法、例如通过碘克沙醇逐步梯度、cscl梯度、色谱或聚
乙二醇(peg)沉淀来纯化raav颗粒。
[0094]
本公开内容还考虑了包含如本文所述的并入aav44.9(e531d)衣壳的颗粒、编码aav44.9(e531d)衣壳的核酸或raav颗粒的宿主细胞。这样的宿主细胞包括哺乳动物宿主细胞,其中人宿主细胞是优选的,并且可以是分离的,例如在细胞或组织培养物中。在一些实施方案中,宿主细胞是眼细胞。
[0095]
在一些实施方案中,提供了组合物,其包含如本文所述的raav颗粒(例如,包含aav44.9(e531d)衣壳),以及任选的可药用载体、赋形剂、稀释剂和/或缓冲剂。在一些实施方案中,可将本文所述的组合物施用至需要治疗的哺乳动物(或对象)。在一些实施方案中,对象患有或被怀疑患有一种或更多种视网膜障碍、视网膜疾病或视网膜营养不良。在一些实施方案中,对象患有或被怀疑患有本文公开的一种或更多种视网膜病症、疾病和障碍(例如,视锥
‑
视杆营养不良)。在一些实施方案中,对象具有一个或更多个内源突变等位基因(例如,与眼或视网膜的疾病、障碍或病症(例如视锥
‑
视杆营养不良)相关或者其造成该疾病、障碍或病症)。
[0096]
在一些实施方案中,提供了用于对哺乳动物感光细胞或视网膜色素上皮细胞进行转导的方法,所述方法包括向哺乳动物的一只或两只眼施用本文所述的raav颗粒。在一些具体的实施方案中,提供了用于在哺乳动物的一个或更多个感光细胞或rpe细胞中表达多核苷酸的方法,所述方法包括向所述哺乳动物的一只或两只眼经视网膜下或玻璃体内施用本文所述的raav颗粒或其组合物持续有效地在所述哺乳动物的一个或更多个pr细胞或rpe细胞中产生所述治疗剂的一段时间,其中所述raav颗粒包含多核苷酸,所述多核苷酸包含至少第一多核苷酸,所述第一多核苷酸包含与编码治疗剂的至少第一异源核酸序列有效地连接的pr或rpe细胞特异性启动子。
[0097]
在一些具体的实施方案中,本发明提供了与编码治疗剂的至少第一异源核酸序列有效地连接的pr或rpe细胞特异性启动子。示例性pr或rpe细胞特异性启动子可包含a)光感受器特异性启动子(在视杆细胞和视锥细胞中活化),例如irbp启动子(hirpb、irbp、irbp241)、视紫红质激酶启动子(hgrk1、grk1、grk、rk)和/或嵌合人retinoschisin
‑
irbp增强子(rs/irpb);视锥特异性启动子,例如红/绿视锥视蛋白启动子(其可包含2.1kb(pr2.1)形式或1.7kb(pr1.7)形式,参见美国专利公开no.2018/0112231,通过引用并入本文)、视锥抑制蛋白启动子(hcar、car)、嵌合irbp增强子
‑
视锥转导蛋白启动子(irbp/gnat2、irbpe
‑
gnat2);视杆特异性启动子,例如人视紫红质启动子(rho、rhop等)、人nrl启动子(nrl);或rpe特异性启动子,例如rpe65或bestrophin/vmd2(best1、best、vmd2)。
[0098]
在一些实施方案中,所公开的raav载体中任一种的启动子包含与seq id no:11中所示的hgrk1启动子序列具有至少95%、至少98%、至少99%或100%同一性的核苷酸序列:
[0099][0100]
因此,本公开内容中描述的示例性raav载体包括aav44.9(e531d)
‑
hgrk1
‑
gfp、
aav44.9(y733f)
‑
hgrk1
‑
gfp、aav44.9(e531d)
‑
irbp/gnat2
‑
hgfp、aav44.9(y733f)
‑
irbp/gnat2
‑
hgfp、aav44.9(e531d)
‑
hgrk1
‑
gucy2e和aav44.9(y733f)
‑
hgrk1
‑
gucy2e。
[0101]
在一些具体的实施方案中,本公开内容提供了与至少第一多核苷酸有效地连接的组成性启动子,其可包含cmv、cba、cb、smcba、cbh或ef1
‑
α。
[0102]
在一些实施方案中,提供了涉及为有此需要的哺乳动物提供治疗有效量的选定的治疗剂的方法,所述方法包括向所述哺乳动物的一只或两只眼施用本文所述的raav颗粒的量;并且持续有效地为所述哺乳动物提供治疗有效量的选定的治疗剂的一段时间。
[0103]
在某些实施方案中,所述哺乳动物被怀疑患有以下疾病、障碍或病症、处于发展以下疾病、障碍或病症之风险中或已被诊断患有以下疾病、障碍或病症:例如但不限于例如显性视锥营养不良;显性视锥
‑
视杆营养不良;莱贝尔先天性黑蒙;隐性视锥营养不良;隐性视锥
‑
视杆营养不良;黄斑营养不良;模式营养不良;卵黄状营养不良;中心性脉络膜营养不良;眼底黄色斑点症、常染色体显性、常染色体隐性和x连锁视网膜色素变性;与bardet
‑
biedl综合征相关的视网膜色素变性;x连锁青少年视网膜劈裂症;色盲;蓝视锥全色盲症;i、ii和iii型usher综合征;迪谢内肌营养不良;肢带型肌营养不良;脊髓性肌萎缩症;糖原贮积症ⅱ型;弗里德里希共济失调;黏多糖贮积症(mps)(所有形式);溶酶体贮积症(lsd)(所有形式);肌萎缩侧索硬化症(als);帕金森病;以及阿尔茨海默病的疾病、障碍或病症。在一些实施方案中,对象具有一个或更多个与眼或视网膜的疾病、障碍或病症相关或者引起该疾病、障碍或病症的内源性突变等位基因,例如基因gucy2d、gucy2e、spata7、prph2、abca4、aipl1、lca5、rpgrip1、crx、crb1、nmnat1、cep290、impdh1、rd3、rdh12、tulp1、kcnj13、gdf6、iqcb1、bbs1、bbs2、arl6/bbs3、bbs4、bbs5、bbs7、ttc8/bbs8、bbs10、trim32/bbs11、bbs12、ccdcc28b、cep290、tmem67、mks1 mkks、rho、prpf31、rp1、nrl、nr2e3、rpgr、rp2、pde6a、pde6b、pde6g、rp25、cnga1、cngb1、mak、rs1、cngb3、cnga3、gnat2、opn1lw、opn1mw、crx、guca1a(gcap1)、guca1b(gcap2)、abca4、prom1和elovl4、myo7a、ush1c、cdh23、pcdh15、ush1g、ush2a、dfnb31或clrn1中的等位基因。
[0104]
在一些具体的实施方案中,向对象施用替代编码序列以提供功能性蛋白质,例如gucy2d或gucy2e,以例如完全或部分地恢复对象(例如人)的光感受器功能。在一些实施方案中,通过将包含本文公开的异源核酸序列的raav颗粒施用至对象(例如,施用至患有显性视锥
‑
视杆营养不良的人)来沉默对象的目标编码序列的一个或两个等位基因。在一些具体的实施方案中,通过施用本文公开的raav颗粒来沉默或抑制一个或更多个目标编码序列的内源性突变等位基因。
[0105]
在一些实施方案中,本公开内容的任何raav核酸载体的异源核酸序列具有与选自seq id no:9或10的核苷酸序列具有至少95%同一性、至少98%同一性、至少99%同一性或100%同一性的序列。编码人gucy2d基因(seq id no:9)和小鼠gucy2e基因(seq id no:10)的核苷酸序列如下所示。
[0106]
gucy2d:
[0107]
[0108]
[0109][0110]
gucy2e:
[0111]
[0112]
[0113][0114]
在一些实施方案中,哺乳动物是人对象。在一些实施方案中,哺乳动物是非人灵长类对象。非人灵长类对象的非限制性实例包括猕猴(例如食蟹猴或恒河猴)、狨猴、绢毛猴、蜘蛛猴、枭猴、长尾黑颚猴(vervet monkey)、松鼠猴、狒狒、大猩猩、黑猩猩和猩猩。其他示例性对象包括家养动物,例如狗和猫;家畜,例如马、牛、猪、绵羊、山羊和鸡;以及其他动物,例如小鼠、大鼠、豚鼠和仓鼠。
[0115]
在某些实施方案中,提供了用于将本文所述的raav颗粒或其组合物视网膜下施用至哺乳动物的中央凹(例如,中央凹视锥细胞)的方法。在一些具体的实施方案中,在视网膜下施用期间和/或之后使中央凹的脱离最小化。在一些具体的实施方案中,在中央凹没有任何脱离的情况下进行raav颗粒的视网膜下施用。
[0116]
在一些实施方案中,向细胞或对象施用的raav颗粒的剂量可为约106至10
14
个颗粒/ml或103至10
15
个颗粒/ml,或在其任一范围之间的任何值,例如,约106、107、108、109、10
10
、10
11
、10
12
、10
13
或10
14
个颗粒/ml。在一个实施方案中,施用高于10
13
个颗粒/ml的raav颗粒。在一些实施方案中,向对象施用的raav颗粒的剂量可为约106至10
14
载体基因组(vg)/ml、或103至10
15
vg/ml,或在其任一范围之间的任何值,例如约106、107、108、109、10
10
、10
11
、10
12
、10
13
或10
14
vg/ml。在一个实施方案中,施用高于10
13
vg/ml的raav颗粒。根据实现所治疗的特定疾病、障碍或病症的治疗可需要的,raav颗粒可以单剂量施用或者分为两次或更多次施用。在一些实施方案中,将0.0001ml至10ml(例如0.0001ml、0.001ml、0.01ml、0.1ml、1ml、10ml)以一个剂量递送于对象。
[0117]
在一些实施方案中,raav颗粒滴度为1
×
10
10
至5
×
10
13
vg/ml。在一些实施方案中,raav颗粒滴度可为1
×
10
10
、2.5
×
10
10
、5
×
10
10
、1
×
10
11
、2.5
×
10
11
、5
×
10
11
、1
×
10
12
、2.5
×
10
12
、5
×
10
12
、1
×
10
13
、2.5
×
10
13
、或5
×
10
13
vg/ml。在一些实施方案中,颗粒滴度小于1
×
10
10
vg/ml。在一些实施方案中,raav颗粒滴度大于1
×
10
15
vg/ml。在一个实施方案中,raav
颗粒滴度大于5
×
10
13
vg/ml。在一些实施方案中,通过本文描述的方法(例如,视网膜下或玻璃体内)施用raav颗粒。
[0118]
根据实现所治疗的特定疾病、障碍或病症的治疗可需要的,raav颗粒可以单剂量施用或者分为两次或更多次施用。在一些实施方案中,将1至500微升的本申请中所述的组合物(例如,其包含raav颗粒)施用至对象的一只或两只眼。例如,在一些实施方案中,可向每只眼施用约1、约10、约50、约100、约200、约300、约400或约500微升。然而,应当理解,在一些实施方案中可施用更小或更大的体积。
[0119]
在一些实施方案中,本公开内容提供了本文公开的一种或更多种基于raav的组合物在可药用溶液中的制剂用于单独地或与一种或更多种其他治疗模式组合施用至细胞或动物,并且特别是用于人细胞、组织和影响人的疾病的治疗。
[0120]
如果需要,本文所述的raav颗粒也可与其他药剂例如蛋白质或多肽或多种药物活性剂组合施用,包括治疗性多肽、生物活性片段、或其变体的一个或更多个全身或局部施用。实际上,对于也可包含的其他组分几乎没有限制,只要该另外药剂在与靶细胞或宿主组织接触时不会引起明显的不利影响即可。因此,在特定情况下,raav颗粒可根据需要与多种其他药剂一起递送。这样的组合物可从宿主细胞或其他生物学来源中纯化,或作为替代,可如本文所述化学合成。
[0121]
可药用赋形剂和载体溶液的配制是本领域技术人员公知的,开发用于在多种治疗方案(包括例如视网膜下、玻璃体内、肠胃外、静脉内、鼻内、关节内和肌内施用和制剂)中使用本文所述的特定组合物的合适的给药和治疗方案也是本领域技术人员公知的。
[0122]
通常来说,这些制剂可包含至少约0.1%的治疗剂(例如raav颗粒)或更多,但是一种或更多种活性成分的百分比当然可变化并且可方便地为总制剂的重量或体积的约1%或2%至约70%或80%或更多。自然地,可以以在化合物的任何给定单位剂量中将获得合适剂量的方式来制备每种治疗上有用组合物中治疗剂(例如,raav颗粒)的量。制备这样的药物制剂领域的技术人员将考虑诸如溶解度、生物利用度、生物学半衰期、施用途径、产品保存期以及其他药理学考虑的因素,并且因此多种剂量和治疗方案可以是理想的。
[0123]
在某些情况下,视网膜下、眼内、玻璃体内、肠胃外、皮下、静脉内、脑室内、肌内、鞘内、经口、腹膜内、通过经口或鼻吸入、或通过经由直接注射而直接注射到一种或更多种细胞、组织或器官中来在本文中公开的适当配制的药物组合物中递送如本文所述的raav颗粒(例如包含aav44.9(e531d)衣壳)将是理想的。
[0124]
适用于注射用途(例如,包含如本文所述的raav颗粒)的组合物的药物形式包括无菌水溶液或分散体。在一些实施方案中,该形式是无菌的并且在存在容易可注射性的程度上是流体。在一些实施方案中,该形式在制造和储存条件下是稳定的,并且被保存以抵抗微生物(例如细菌和真菌)的污染作用。载体可以是溶剂或分散介质,其包含例如水、盐水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇等)、其合适的混合物、和/或植物油。可维持适当的流动性,例如通过使用包衣(例如卵磷脂)、通过在分散体的情况下维持所需的粒径以及通过使用表面活性剂来进行。
[0125]
术语“载体”是指与本文所述的raav颗粒一起施用的稀释剂、佐剂、赋形剂或载剂。这样的药用载体可以是无菌液体,例如水和油,包括以下那些:石油,例如矿物油;植物油,例如花生油、大豆油和芝麻油;动物油;或合成来源的油。盐水溶液以及葡萄糖和甘油水溶
液也可用作液体载体。
[0126]
本公开内容的组合物可通过多种途径递送至眼。其可以眼内、通过表面施用至眼或通过眼内注射到例如玻璃体(玻璃体内注射)或视网膜下(视网膜下注射)光感受器间空间来递送。在一些实施方案中,其被递送至视杆感光细胞。作为替代,其可通过插入或注射到眼周围的组织中而局部递送。其可通过经口途径或通过皮下、静脉内或肌内注射全身递送。作为替代,其可通过导管或通过植入物递送,其中这样的植入物由多孔、无孔或凝胶材料(包括膜,例如硅橡胶膜或纤维、可生物降解的聚合物或蛋白质性材料)制成。其可在病症发作之前施用以防止其发生,例如在对眼进行手术期间,或在病理病症发作之后立即或在急性或长期病症发生期间施用。
[0127]
对于可注射水溶液的施用,例如,如果需要的话,可将溶液适当地缓冲,并且首先用足够的盐水或葡萄糖使液体稀释剂等张。这些特定的水溶液特别适合于静脉内、肌内、玻璃体内、皮下和腹膜内施用。在这方面,根据本公开内容,本领域技术人员将知道可使用的无菌水性介质。例如,可将一个剂量溶解在1ml等张nacl溶液中,然后添加至1000ml皮下灌注流体中或注射在建议的输注部位(参见例如“remington's pharmaceutical sciences”第15版,第1035
‑
1038和1570
‑
1580页)。根据所治疗对象的状况,必然发生剂量的一些变化。在任何情况下,负责施用的人员决定用于个体对象的合适剂量。此外,对于人施用,制剂应符合例如fda生物学标准所所要求的无菌性、热原性以及一般安全性和纯度标准。
[0128]
无菌可注射溶液可通过将所需量的如本文所述的raav颗粒引入合适的溶剂(其根据需要具有上文列举的数种其他成分)中然后过滤灭菌来制备。通常来说,通过将多种经灭菌的活性成分引入无菌载剂中来制备分散体,所述无菌载剂包含基础分散介质和需要的来自以上列举的那些的其他成分。在用于制备无菌可注射溶液的无菌粉末的情况下,优选的制备方法是真空干燥和冷冻干燥技术,该技术由其经预先无菌过滤溶液产生活性成分加上任何另外期望成分的粉末。
[0129]
组合物(例如,包含如本文所述的raav颗粒)的量和施用这样的组合物的时间将在受益于本教导的技术人员的范围内。然而,很可能可通过单次施用实现治疗有效量的所公开组合物的施用,例如单次注射足够数量的raav颗粒以为接受这种治疗的患者提供治疗益处。作为替代,在一些情况下,在相对较短或相对延长的时间段内提供组合物的多次或连续施用可以是理想的,这可由监督这样的组合物的施用的医疗人员决定。
[0130]
在一些实施方案中,在施用本申请中所述的一种或更多种组合物之后,可保持或恢复(例如部分或全部地)视觉敏锐度。在一些实施方案中,在施用本申请中所述的一种或更多种组合物后,一个或更多个感光细胞或者一个或更多个rpe细胞可部分或全部保存,和/或者一种或更多种视杆和/或视锥介导的功能可部分或全部恢复。
[0131]“治疗”疾病如该术语在本文所用是指降低对象经历的疾病、障碍或病症(例如视杆
‑
视锥营养不良)的至少一种体征或症状的频率或严重程度。通常将上述组合物以有效量(即能够产生理想结果的量)施用至对象。理想结果将取决于所施用的活性剂。例如,raav颗粒的有效量可以是能够将异源核酸转移至宿主器官、组织或细胞的颗粒量。
[0132]
可通过标准药学方法使用培养物中的细胞或实验动物确定ld50(将该群体的50%致死的剂量)来确定本公开内容方法中使用的组合物的毒性和效力。毒性和效力之间的剂量比是治疗指数,并且其可表示为比例ld50/ed50。表现出大治疗指数的那些组合物是优选
的。虽然可使用表现出毒性副作用的那些,但应注意设计使这样的副作用的潜在损害最小化的递送系统。本文所述的组合物的剂量通常在包括ed50且具有很少或没有毒性的范围内。根据所采用的剂型和所使用的施用途径,剂量可在此范围内变化。
[0133]
实施例
[0134]
包括以下实施例以表明本发明的一些优选实施方案。本领域技术人员应当理解,在下文的实施例中公开的技术代表了发明人发现的在本发明的实践中很好地发挥作用的技术,并且因此可被认为构成其实践的优选模式。然而,根据本公开内容,本领域技术人员应当理解,在不脱离本发明的精神和范围的情况下,可在所公开的具体实施方案中进行许多改变,并且仍然获得类似或相似的结果。
[0135]
实施例1
‑
基于aav的视网膜基因治疗的治疗分子
[0136]
玻璃体内(ivt)或视网膜下(sr)注射之后评价aav44.9的视网膜转导和嗜性。通过利用gfp在全视杆光感受器中组成性表达的小鼠模型(nrl
‑
gfp
‑
smouse),对aav44.9和基准衣壳aav5和aav8(y733f)的光感受器转导效率进行了量化。
[0137]
寻求确定是否可通过在第733位残基处添加y
‑
f突变(y733f)和在第531位处单独将谷氨酸替换为天冬氨酸(e531d)来改善aav44.9的转导。由于视锥光感受器是许多视网膜基因治疗(例如色盲和视锥
‑
视杆营养不良)的靶点,因此评估了aav44.9在视锥光感受器中表达转基因的能力。
[0138]
实验方法
[0139]
aav衣壳系统发育树如图1所示。aav的vp1氨基酸序列使用clustalw(alignx
‑
vector nti)进行比对。然后使用embl
‑
ebi simple phylogeny程序(ebi.ac.uk/tools/phylogeny/simple_phylogeny/)通过邻接法使用该比对生成系统发育树。生成的树使用treeview程序可视化,aav5被指定为外类群。
[0140]
载体制备
[0141]
使用基于三重转染质粒的系统,在双层细胞工厂(1,272cm2细胞生长面积)中接种的贴壁hek293t中将含有驱动mcherry的截短的嵌合cmv
‑
鸡β肌动蛋白(smcba)启动子(sc
‑
smcba
‑
mcherry)的自身互补aav构建体包装到aav44.9、aav5和aav8(y733f)中。收获细胞并通过连续的冻融循环裂解细胞。裂解物中的病毒通过碘克沙醇密度梯度进行纯化,并进行缓冲液交换至补充有吐温20(0.014%)的alcon bss中。病毒通过qpcr相对于标准进行滴定并储存在
‑
80℃。y733f和e531d置换的添加通过aav2rep
‑
44.9cap质粒的定点诱变完成,并通过sanger测序确认。含有驱动绿色荧光蛋白(gfp)的视锥特异性irbpe
‑
gnat2嵌合启动子的另外的构建体包装在aav44.9中。
[0142]
体外转导测定
[0143]
arpe
‑
19(人视网膜色素上皮细胞系)和661w(小鼠视锥细胞系)细胞以1.0
×
104个细胞/孔的浓度接种于96孔板中。第二天,细胞以10,000p/细胞感染。感染之后三天,在固定曝光下进行荧光显微镜检查,分离细胞并使用流式细胞术通过荧光来定量报道蛋白表达(mcherry)。通过将平均mcherry荧光乘以阳性细胞数来计算mcherry表达。图表仅代表表达水平减去细胞水平。
[0144]
注射
[0145]
玻璃体内或视网膜下向4至5周龄的nrl
‑
gfp和c57bl/6j小鼠递送1ul中2
×
109vg
的含载体溶液。在每个实验中至少分析了6只接受成功注射的眼。
[0146]
眼底检查
[0147]
在注射之后4周,使用micron iii相机(phoenix research laboratories,pleasanton,ca)进行眼底检查。分别采集明场和红色荧光图像以使视网膜健康和mcherry表达可视化。实验之间的曝光设置是恒定的,并在附图说明中指出。
[0148]
通过流式细胞术测量视网膜转导
[0149]
收获每组群4至6个nrl
‑
gfp眼的神经视网膜(具有从视网膜手动剥离的rpe)并用木瓜蛋白酶解离。对经处理的解离的视网膜和未经处理的对照进行流式细胞术,以量化对gfp(视杆光感受器)、mcherry(由raav转导的非视杆视网膜神经元)或二者(由raav转导的视杆光感受器)呈阳性的细胞百分比。由每个载体转导的视杆和非视杆神经视网膜细胞的百分比分别进行平均。
[0150]
组织制备和免疫染色
[0151]
注射之后4周,将眼摘除,在4℃下在新鲜制备的磷酸盐缓冲盐水(pbs)中的4%多聚甲醛(pfa)中固定过夜。去除角膜和晶状体,将眼杯在30%蔗糖溶液中在4℃下孵育过夜。将眼包埋在低温恒温器化合物中并在
‑
80℃下冷冻。使用低温恒温器(leica microsystem,buffalo grove,il)切割切片(12μm厚)并转移到载玻片上。视网膜冷冻切片用1
×
磷酸盐缓冲盐水(pbs)冲洗,用0.5%triton
‑
x100和1%牛血清白蛋白(bsa)各封闭1小时,然后在4℃下用小鼠单克隆抗视锥抑制蛋白抗体(1:1000,由clay smith博士惠赠)孵育过夜。第二天用1
×
pbs冲洗载玻片,然后在室温下用alexa fluor驴抗小鼠二抗(1:500)在1
×
pbs中孵育1小时,并用dapi复染。使用共聚焦激光扫描显微镜(leica tcs sp8)和荧光显微镜(evos)获取图像。
[0152]
结果
[0153]
通过aav44.9的视杆转导高于通过基准载体aav5和aav8(y733f)的视杆转导
[0154]
图2a至2e示出了在视网膜下注射4周时aav44.9、aav5和aav8(y733f)的定性和定量分析。图2e中描绘的facs数据显示,在视网膜下注射2
×
109vg后,aav44.9比aav5和aav8(y733f)更有效地转导视杆。图3a至3c示出了视网膜下注射之后4周时显示出注射aav5、aav8(y733f)和aav44.9的nrl
‑
gfp小鼠视网膜中在光感受器和rpe中的mcherry表达的代表性视网膜横截面图像。
[0155]
aav44.9(y733f)和aav44.9(e531d)的定性和定量分析示出在图4a至4c中。图4c中描绘的facs数据显示,在视网膜下注射2
×
109vg后,aav44.9(e531d)比aav44.9和aav44.9(y733f)更有效地转导视杆细胞。图5a和图5b示出了视网膜下注射之后4周时注射aav44.9(y733f)和aav44.9(e531d)的nrl
‑
gfp小鼠视网膜中主要在光感受器和rpe中的mcherry表达的代表性视网膜横截面图像。
[0156]
未经修饰的aav44.9和aav44.9(y733f)在眼细胞系中的转导效率示出在图6a和图6b中。aav44.9(y733f)在小鼠视锥感光细胞系中显示出相对于aav44.9的增强的转导(图6a),而在人rpe细胞系中aav44.9比aav9(y733f)更有效(图6b)。
[0157]
玻璃体内注射之后aav衣壳的定性分析示出在图7a和图7b中。与aav5和aav8(y733f)类似,aav44.9及其衍生物在ivt注射之后不导致有效的视网膜转导。
[0158]
图8a中示出了在sr注射之后4周时,含有视锥优先irbp/gnat2启动子和gfp报道子
的aav44.9显示出在视锥细胞中的gfp表达。图8b和图8c还示出了用视锥抑制蛋白抗体共染色与gfp荧光共定位。
[0159]
以上讨论的结果表明,aav44.9对视杆的转导高于通过基准载体未经修饰的aav5和aav8(y733f)的该转导。将y733f突变添加至aav44.9并没有改善体内光感受器的转导。结果还显示,e531d突变大大增强了光感受器转导,而相比于未经修饰的aav44.9的61%的视杆转导,aav44.9(e531d)显示出82%的视杆转导。aav44.9有效地转导视锥细胞,如aav44.9
‑
irbpe/gnat2
‑
gfp的视网膜下递送所示。与aav5和aav8(y733f)类似,aav44.9及其衍生物在ivt递送后不能有效地转导视网膜。
[0160]
视网膜下注射之后,aav44.9(e531d)在小鼠视网膜中的表现优于未经修饰的aav44.9和aavrh.8
[0161]
在视网膜下注射aav44.9或aav44.9(e531d)之后4周采集nrl
‑
gfp小鼠的代表性眼底图像(红色荧光滤光片)(参见图9a)。载体以1ul中2
×
109vg递送。曝光和增益设置在整个实验过程中一致。实验重复两次以确认结果。注意用不同批次的病毒进行了“重复”实验。
[0162]
在注射之后4周,用木瓜蛋白酶解离nrl
‑
gfp小鼠(来自图9a中的实验的相同小鼠)的视网膜,并进行流式细胞术以量化转导的视杆(gfp+mcherry阳性)或非视杆细胞(mcherry阳性)的百分比,如boye et al.,impact of heparan sulfate binding on transduction of retina by recombinant adeno
‑
associated virus vectors,j.virol.2016,90(8):4215
‑
4231中所述。每个细胞群的转导百分比和相应值示出在图9b中。相对于未经修饰的aav44.9,aav44.9(e531d)转导了更高百分比的视杆光感受器。注意用不同批次的病毒进行了“重复”实验。
[0163]
在视网膜下注射aavrh.8
‑
mcherry之后4周采集nrl
‑
gfp小鼠的代表性眼底图像(参见图10a)。载体以1ul中2
×
109vg递送。gfp和mcherry过滤图像二者均包括在内。由于aavrh.8与aav44.9和aav44.9(e531d)二者的结构相似性,因此对其进行了评价。
[0164]
在注射之后4周,用木瓜蛋白酶解离nrl
‑
gfp小鼠(来自图9a和图10a中的实验的相同小鼠)的视网膜,并进行流式细胞术以量化转导的视杆(gfp+mcherry阳性)或非视杆细胞(mcherry阳性)的百分比。每个细胞群的转导百分比和相应值示出在图10b中。相对于未经修饰的aav44.9或aavrh.8,aav44.9(e531d)转导更高百分比的视杆光感受器。
[0165]
在视网膜下注射较低滴度的scaav44.9、scaav44.9(e531d)或scaavrh.8之后4周采集nrl
‑
gfp小鼠的代表性眼底图像(参见图11a)。载体以1ul中2
×
108vg递送。曝光和增益设置在整个实验过程中一致。
[0166]
在注射之后4周,用木瓜蛋白酶解离nrl
‑
gfp小鼠(来自图11a中的实验的相同小鼠)的视网膜,并进行流式细胞术以量化转导的视杆(gfp+mcherry阳性)或非视杆细胞(mcherry阳性)。每个细胞群的转导百分比和相应值示出在图11b中。相对于未经修饰的aav44.9或aavrh.8,aav44.9(e531d)转导更高百分比的视杆光感受器。
[0167]
视网膜下注射之后4周时aavrh.8、aav44.9和aav44.9(e531d)的定性和定量分析示出在图9a和9b中。图9b描绘了显示在视网膜下注射2
×
10
12
vg后aav44.9(e531d)比aav44.9更有效地转导视杆细胞的facs图。
[0168]
图11a和11b中示出了在视网膜下注射之后4周时较低滴度的aav44.9、aav44.9(e531d)和aavrh.8的定性和定量分析。图11b描绘了显示在视网膜下注射2
×
10
11
vg后
aav44.9(e531d)比aav44.9(e531d)和aavrh.8更有效地转导视杆细胞的facs图。图12示出了在视锥特异性irbpe
‑
gnat2嵌合启动子的情况下,在视网膜下注射之后6周时aav44.9(e531d)和aav44.9的定性分析。
[0169]
图13示出了视网膜下注射aav44.9(e531d)
‑
irbp/gnat2
‑
hgfp之后6周采集的wt小鼠的代表性视网膜横截面。irbp/gnat2启动子是视锥特异性启动子。载体以1ul中2
×
10
12
vg递送。切片用抗gfp(绿色)和视锥抑制蛋白(红色)的抗体进行免疫染色。aav介导的gfp表达与视锥抑制蛋白(视锥特异性标志物)共定位,证实该载体有效地转导视锥。图13中的代表性视网膜横截面图像显示出注射aav44.9(e531d)的nrl
‑
gfp小鼠视网膜中光感受器和rpe中的视锥抑制蛋白表达,并表明aav44.9(e531d)非常有效地转导视锥。
[0170]
在视网膜下注射aav44.9
‑
irbp/gnat2
‑
hgfp之后6周采集wt小鼠的代表性视网膜横截面(参见图14)。irbp/gnat2启动子是视锥特异性启动子。载体以1ul中2
×
10
12
vg递送。切片用抗gfp(绿色)和视锥抑制蛋白(红色)的抗体进行免疫染色。aav介导的gfp表达与视锥抑制蛋白(视锥特异性标志物)共定位,证实该载体有效地转导视锥。
[0171]
实施例2
‑
在猕猴中视网膜下施用aav44.9(e531d)
‑
hgrk1
‑
gfp后增强的侧向扩散和中央凹转导
[0172]
先前已确定人视紫红质激酶(hgrk1)启动子在非人灵长类视杆和视锥中具有专属活性。因此,评价了hgrk1启动子在改进的aav44.9(e531d)载体中驱动猕猴眼中gfp报道子表达的能力。还评价了从初始泡边界侧向扩散的程度。
[0173]
两种raav载体aav44.9
‑
hgrk1
‑
gfp和aav44.9(e531d)
‑
hgrk1
‑
gfp被视网膜下施用至猕猴眼。载体以1
×
10
12
vg/ml的浓度递送。还将对照载体aav5
‑
hgrk1
‑
gfp施用至眼。
[0174]
并入经修饰的和未经修饰的aav44.9载体二者的颗粒在视网膜下注射的猕猴对象中表现出增强的侧向扩散和效力(参见图15)。泡的初始边界和所产生的gfp表达的边界在图15中以白色虚线勾勒出轮廓。相同的脉管系统以加粗的深色线突出显示以供参考。aav44.9(e531d)介导的gfp表达在注射之后1周可见。aav44.9和aav44.9(e531d)二者在1
×
10
12
vg/ml剂量下在灵长类视网膜中均具有良好的耐受性。对照载体aav5介导仍然隔离在初始注射泡内的gfp限制。
[0175]
在猕猴对象中进行了aav44.9
‑
hgrk1
‑
gfp(浓度为1
×
10
12
vg/ml)的中央凹外视网膜下注射。oct扫描揭示在注射过程中中央凹没有脱离(图16)。即使中央凹没有脱离,这种中央凹外视网膜下注射也转导了甚至98%的中央凹视锥和100%的中央视杆(参见图17的右上方)。衣壳表现出增强的侧向扩散,因为泡的边界相对于初始边界扩大。
[0176]
还从注射了aav44.9(e531d)
‑
hgrk1
‑
gfp的猕猴眼中捕获了图像。单眼定性分析揭示约50%的中央凹视锥转导由aav44.9(e531d)介导。
[0177]
aav44.9(e531d)
‑
hgrk1
‑
gfp的3次视网膜下注射(每次30μl)在猕猴眼中央凹外的上部、颞侧和下部视网膜中进行。视网膜切片用抗视锥抑制蛋白的抗体染色,三个不知情观察者在穿过中央凹坑的单个平面上对5个视网膜区域中的gfp阳性视锥和视杆进行计数。该施用的结果示出在图19中。oct扫描揭示在注射期间中央凹没有脱离(参见图19的右图)。
[0178]
这些结果表明,aav44.9(e531d)
‑
hgrk1
‑
gfp在猕猴中的中央凹外视网膜下注射在没有中央凹脱离的情况下表现出显著的中央视锥和视杆细胞的转导。外围的视杆和视锥也被非常有效地转导。因此,中央凹外视网膜下注射导致整个中央凹区域上的高效转导。
[0179]
如图20a至20d所示,该注射之后对中央凹旁的检查揭示aav44.9(e531d)颗粒转导位于中央凹坑的鼻侧和颞侧二者的中央凹旁视锥。然而,值得注意的是,用未经修饰的aav44.9未实现中央凹旁视锥转导。这一发现是令人感兴趣的,至少因为i)中央凹旁视锥对通过多种aav衣壳变体的转导具有抵抗力,以及ii)由于老化和遗传性视网膜疾病引起的最早的结构和功能丧失通常发生在中央凹旁区域。尽管它们在该区域转导视锥的能力不同,但经修饰和未经修饰的aav44.9载体有效地将中央凹旁视杆转导到基本相同的程度。
[0180]
如图21a至21b所示,对中央凹周围的检查揭示了类似的模式:并入aav44.9(e531d)衣壳的颗粒转导中央凹周围视锥,但未经修饰的aav44.9不转导。在该区域中中央凹周围视杆被两个衣壳均有效地转导。中央凹周围包围中央凹旁。
[0181]
这些结果进一步证明,由改进的aav44.9(e531d)衣壳变体载体提供的增强的转导侧向扩散可允许在中央凹旁区域进行视网膜下注射以产生中央凹细胞的转导,同时避免在人对象中诱发中央凹脱离的有害影响。
[0182]
实施例3
‑
在小鼠中视网膜下施用aav44.9
‑
gucy2e
‑
gfp之后增强的侧向扩散
[0183]
前面的实施例展示了由改进的aav44.9(e531d)载体递送的报道基因的中央凹转导。接下来确定在施用编码感兴趣的治疗性肽的改进的aav44.9(e531d)载体之后侧向扩散的程度。选定的感兴趣的治疗性肽是gucy2e,它是人鸟苷酸环化酶2d gucy2d的鼠同源物。
[0184]
将两种载体aav44.9(e531d)
‑
hgrk1
‑
gucy2e和aav8(y733f)
‑
hgrk1
‑
gucy2e视网膜下施用至视网膜鸟苷酸环化酶1/2双基因敲除(gcdko)小鼠的眼。gcdko小鼠完全缺乏视网膜功能。由于这些光感受器中没有任何功能性视网膜鸟苷酸环化酶,因此视杆和视锥都不能对光作出响应。因此,在gcdko小鼠中进行的基因替代治疗可评价基因替代/补充是否同时在视杆细胞和视锥细胞中成功。载体以1
×
10
13
vg/ml的浓度递送。通过视网膜电图(erg)测量来评价经处理和未经处理的眼的响应功能。来自视网膜感光细胞的erg响应称为“a波”,并且来自视网膜双极细胞的电响应称为“b波”。
[0185]
如图18b所示,来自用aav载体处理的眼的视锥细胞的光响应功能相对于未经处理的眼的光响应功能得到改善。这些结果表明,这两类光感受器都被并入aav44.9(e531d)衣壳和aav44.9(y733f)衣壳的raav颗粒有效靶向。如图18a所示,在施用aav(y733f)载体后,最大a和b波振幅大于aav44.9(e531d)载体。
[0186]
该实验的另一个主要意义是,并入aav44.9(e531d)的表达设计用于治疗遗传性视网膜疾病的治疗性肽的临床候选raav载体(例如,用于递送人gucy2d转基因的载体)可能会在相应的小鼠疾病模型(例如,用于递送鼠gucy2e的载体)中发挥作用。这在制造的多个阶段或时期期间对多个批次的候选物进行临床前开发和评价的情况下是有利的。
[0187]
其他实施方案
[0188]
应当理解,本文中描述的实施例和实施方案仅用于举例说明目的,本领域技术人员可根据其提出多种修改或变化,并且这些修改或变化包括在本申请的精神和范围内和所附权利要求书的范围内。本文引用的所有参考文献,包括出版物、专利申请和专利,均通过引用并入于此,其程度就如同每篇参考文献被单独且具体地指示为通过引用并入并在本文中整体阐述一样。除非在本文中另有说明,否则本文对数值范围的引用仅旨在用作单独提及落入该范围内的每个单独值的速记方法,并且将每个单独值并入说明书中,就好像其在本文中单独引用一样。
[0189]
除非另有说明或与上下文明显矛盾,否则在本文中使用例如“包含”、“具有”、“包括”或“含有”的关于一个或更多个元素的术语对本发明的任何方面或实施方案的描述旨在为“由一个或更多个特定元素组成”、“基本上由一个或更多个特定元素组成”或“基本上包含一个或更多个特定元素”的本发明类似方面或实施方案提供支持(例如,本文描述为包含特定元素的组合物应理解为也描述了由该元素组成的组合物,除非另有说明或与上下文明显矛盾)。
[0190]
根据本公开内容,本文公开和要求保护的所有组合物和方法可在没有过度实验的情况下制备和实施。虽然本发明的组合物和方法已经根据一些优选实施方案进行了描述,但对于本领域技术人员来说明显的是,在不脱离本发明的概念、精神和范围的情况下,可对本文所述的组合物和方法以及方法的步骤或步骤顺序中进行变化。更具体地,明显的是,某些化学和/或生理学相关的药剂可替代本文所述的药剂,同时将获得相同或相似的结果。所有这些对本领域技术人员来说明显的类似替代和修改都被认为在所附权利要求书所限定的本发明的精神、范围和概念之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1