可切换嵌合抗原受体工程化的人自然杀伤细胞的制作方法
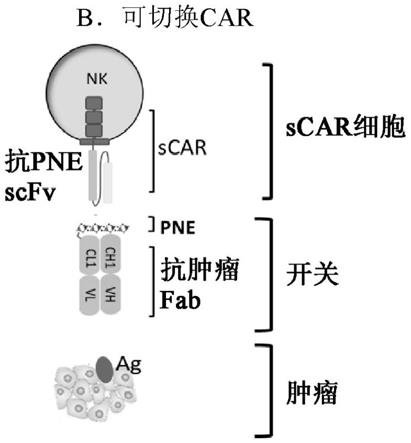
可切换嵌合抗原受体工程化的人自然杀伤细胞
1.相关申请的交叉引用
2.本技术要求于2019年3月22日提交的美国临时申请第62/822,389号的优先权权益,所述美国临时申请通过引用并入本文中。
技术领域
3.本发明涉及工程化的免疫疗法。
背景技术:
4.现有的基于car工程化的t细胞(car-t)的疗法代表了近年来开发的最成功的免疫疗法方法之一。大多数car-t细胞疗法已在临床上用于通过靶向b细胞特异性抗原cd19来治疗血液恶性肿瘤。然而,由于t细胞的一些内在特性,包含限制其严格用于自体患者的同种异体反应性以及由不受控制的增殖或不受控制的细胞因子释放引起的副作用,这种方法并非没有限制。另一方面,nk细胞起同种异体细胞毒性效应细胞的作用,所述同种异体细胞毒性效应细胞不必基于患者特异性应用,不需要事先致敏并且被证明毒性较小。由于这些原因,car工程化的nk(car-nk)细胞作为替代性car细胞疗法越来越引起关注。然而,还存在其它未解决的挑战。由于缺乏真正的肿瘤特异性抗原,针对实体瘤的靶向性基于car的疗法一直具有挑战性,因为大多数靶标由非恶性细胞所共享并且由于“在靶(on-target)、肿瘤外(off-tumor)”效应可能导致毒性。”可微调car疗法可用于更好地鉴定和靶向肿瘤,同时限制这种毒性。第二个挑战是难以扩大car细胞的制造速率以满足患者的需求。这是因为常规的car细胞是在针对一个靶标的一个car的基础上以刚性形式产生的。制备具有一种特异性的每个细胞批次需要时间、成本和复杂的制造设施,这通常使大多数患者无法接受治疗。最近开发的将效应细胞活化功能与抗原识别功能解偶的scar被设计成克服这些障碍。
5.过继细胞治疗的一个关键目标是精确控制治疗细胞群的抗肿瘤活性。目前策略,如fda批准的抗cd19 car-t细胞(tisageleclecuel(kymriah)和axicabtagene ciloleucel(yescarta))非常有效,但会导致使患者出现显著的免疫抑制和感染易感性
1,2
的长期(可能是永久性的)b细胞发育不全和低丙球蛋白血症。此外,如car介导的细胞因子释放综合征等毒性和神经毒性可能难以控制,并且在一些情况下会导致显著的发病率以及甚至死亡率
1-3
。car所靶向的许多肿瘤抗原可能导致“在靶、肿瘤外”毒性,如已经充分综述的
1,2
。例如,在患有结肠癌的患者中,通过car-t细胞靶向癌胚抗原由于正常结肠组织的抗原识别而导致严重结肠炎4。不幸的是,用抗her2 car-t细胞治疗患者会导致死亡,很可能是由于her2在肺细胞上的表达5。同样,针对aml抗原的car也是有问题的,因为大多数car也由正常造血干细胞共享,可能导致骨髓发育不全延长
6-8
。已经提出使用如自杀开关和基于rna的car表达等选项控制car-t细胞活性
1,9-11
。然而,杀伤开关不提供对t细胞活化和扩增的控制,并且导致潜在治疗性car-t细胞的不可逆消除。基于rna的系统仅导致短暂的car表达、较低的抗肿瘤活性并且不能捕获完全动态和可滴定的开/关活性
9,10
。
6.先前使用scar-t细胞的研究证明了免疫突触的选择性形成,其中scar-t细胞、开
关和靶细胞全部以结构明确和时间控制的方式相互作用。此scar-t细胞系统已显示出对cd19+细胞b细胞恶性肿瘤的强效杀伤作用,包含产生t中枢记忆(tcm)群体,所述群体能够有效地重新给药可溶性开关组分(仅施用单剂量的scar-t细胞)以治疗复发性疾病
12,13
。可溶性开关的使用也实现car接合的精确滴定。例如,可以首先用低剂量的开关治疗患者以使crs或神经毒性最小化,然后用更高的后续剂量治疗患者以增加抗肿瘤活性。此外,此系统能够轻易地使用多于一个开关组件,以使得能够双重靶向肿瘤细胞抗原,以便预防由于单个肿瘤抗原的丢失而导致的复发
12,13
。迄今为止,临床前研究表明,这些scar-t细胞不仅能靶向并杀伤cd19
+
b细胞恶性肿瘤,还能通过抗her2开关靶向并杀伤乳腺癌和胰腺癌
12-15
。
7.最后,已经提出了许多其它基于car的系统,如syn-notch系统、“条件car”、其它开关介导的car以及其它系统,以改善实体瘤的靶向性,同时维持对治疗的安全性和控制
2,16-18
。
技术实现要素:
8.本公开提供了一种用可切换嵌合抗原受体(scar)工程化的自然杀伤(nk)细胞、其制造方法和使用方法。
9.在实施例中,本发明提供了一种用可切换嵌合抗原受体(scar)工程化的自然杀伤(nk)细胞。在实施例中,所述scar包括对与肽新抗原表位(pne)结合具有特异性的抗体scfv区。在实施例中,所述scar进一步包括nkg2d跨膜结构域、2b4共刺激结构域和/或cd3ζ链(或其突变)。在实施例中,所述nk细胞进一步包括与所述scar结合的开关,其中所述开关包括与抗癌或抗病毒抗体fab区融合的肽新抗原表位(pne),所述抗癌或抗病毒抗体fab区对与癌症抗原或病毒抗原结合具有特异性。在实施例中,所述癌症抗原是cd19或卷曲蛋白7(frizzled 7)。在实施例中,本发明提供的是,所述癌症或病毒抗原可以是本文所公开的或本领域已知的那些癌症或病毒抗原中的任何癌症或病毒抗原。在实施例中,所述nk细胞源自人诱导的多能细胞。
10.在实施例中,本发明提供了一种治疗受试者的癌症或病毒的方法,所述方法包括向有需要的受试者施用有效量的自然杀伤(nk)细胞,所述nk细胞用针对所述癌症或所述病毒的抗原活化的可切换嵌合抗原受体(scar)工程化。
11.在实施例中,所述scar包括对与肽新抗原表位(pne)结合具有特异性的抗体scfv区。在实施例中,所述scar进一步包括nkg2d跨膜结构域、2b4共刺激结构域和cd3ζ链。
12.在实施例中,所述scar通过与开关结合而被进一步活化,其中所述开关包括分别与抗癌或抗病毒抗体fab区融合的pne,所述抗癌或抗病毒抗体fab区对与所述癌症抗原或所述病毒抗原结合具有特异性。在实施例中,所述癌症抗原是cd19或卷曲蛋白7。在实施例中,本发明提供的是,所述癌症或病毒抗原可以是本文所公开的或本领域已知的那些癌症或病毒抗原中的任何癌症或病毒抗原。
13.在实施例中,所述nk细胞是同种异体的。在实施例中,所述癌症是难治性的在实施例中,所述癌症是血液肿瘤或实体瘤。在实施例中,所述肿瘤是淋巴的或卵巢的。在实施例中,本发明提供的是,所述癌症可以是公开或已知的任何癌症。在实施例中,本发明提供的是,病毒可以是公开或已知的任何病毒。
14.在实施例中,本发明提供的是,所述方法可以进一步包括施用治疗量的针对所述
癌症或病毒的单克隆抗体疗法。
15.在实施例中,本发明提供了包括如本文所述的nk细胞的药物组合物。在实施例中,本发明提供了所述scar-nk细胞的细胞培养物。
16.在实施例中,本发明提供了一种制造自然杀伤(nk)细胞的方法,所述方法包括:对nk细胞进行工程化以展示包括可切换嵌合抗原受体(scar)的跨膜蛋白;以及储存工程化的nk细胞以随后活化所述scar。
17.在实施例中,本发明提供的是,所述scar包括对与肽新抗原表位(pne)结合具有特异性的抗体scfv区。在实施例中,所述scar进一步包括nkg2d跨膜结构域、2b4共刺激结构域和cd3ζ链。
18.在实施例中,本发明提供的是,所述制造方法进一步包括通过将所述scar与开关结合来活化所述scar,其中所述开关包括分别与抗癌或抗病毒抗体fab区融合的pne,所述抗癌或抗病毒抗体fab区对与癌症抗原或病毒区结合具有特异性。
附图说明
19.图1a-1c示出了常规car和scar的示意性比较。
20.图2a-2b示出了使用nk92效应细胞的scar介导的抗肿瘤活性。
21.图3a-3b示出了在表达scar的ipsc中的造血和nk细胞分化。
22.图4示出了在ipsc-nk细胞中的scar介导的抗肿瘤活性。
23.图5示出了incucyte杀伤测定。
24.图6示出了用人工混合细胞系进行的体外杀伤测定。
25.图7示出了始终使用的不同开关的配置。
26.图8示出了在存在增加浓度的抗cd19开关的情况下对nalm6的car4-nk92诱导的杀伤。
27.图9a-9c示出了靶细胞上的aml抗原的抗原表达和aml细胞系上的开关介导的杀伤测定。
28.图10a-10c是在具有自然混合细胞群的pbmc中的开关介导的杀伤的抗原特异性的证明。
29.图11是scar4与常规cd19-car4的比较。
30.图12示出了在用sb-scar4-p2a-gfp或sb-scar4-ires-gfp转染的nk92细胞上的gfp和scar4表达。
31.图13示出了在体外共培养杀伤测定中nk92-scar-ires与nk92-p2a-gfp的比较,其中在存在增加水平的抗fzd7或对照开关的情况下,将ma148细胞与用nk92-scar-ires或nk92-p2a-gfp转染的wt nk92或nk92共培养。
32.图14示出了gfp和scar4在经转染的ipsc的表面上的表达。
33.图15a-15b示出了表达scar4-p2a-gfp的ipsc源性nk细胞的再生。
具体实施方式
34.本发明涉及具有可切换嵌合抗原受体(scar)的自然杀伤(nk)细胞的工程化,所述scar被设计成产生被称为scar-nk细胞的靶向的、基于nk细胞的治疗模式,以更有效地治疗
难治性癌症——血液恶性肿瘤和实体瘤两者。具体而言,通过为nk细胞配备scar,使nk细胞能够以紧密滴定的方式靶向肿瘤并同时或依次靶向多种肿瘤抗原。因此,此系统介导经改进的抗肿瘤杀伤,防止作为肿瘤逃逸免疫介导的杀伤的一种手段的肿瘤抗原丢失的发展,并使对患者的毒性最小化。
35.在本发明中,以独特的方式组合不同的技术,以首先制备nk细胞特异性scar,并且然后用nk-scar对nk细胞进行基因工程化,以便产生独特的scar-nk细胞作为潜在的治疗性细胞产品。这种新型细胞整合了car-t细胞和nk细胞的最佳特性,以介导更好的功效、多功能性、剂量控制性和对正常细胞的最小毒性。在实施例中,使用nk92细胞(即在临床上使用的nk细胞系)以及源自人诱导的多能干细胞的nk细胞(ipsc-nk)来证明scar-nk细胞的原型。然而,本发明包含使用其它类型的nk细胞,包含由其它干细胞类型产生或由外周血或脐带血分离或产生的nk细胞。
36.本发明通过使用新颖的基于重组抗体的双功能开关系统改进nk细胞介导的免疫疗法的抗肿瘤活性和安全性,所述双功能开关系统由与肽新表位(pne)融合的肿瘤抗原特异性fab分子组成,所述pne被pne特异性可切换car(scar)唯一地识别。
37.另外的数据证明了抗fzd7开关(靶向实体瘤)和抗cll1开关(针对aml)的有效使用。因此,此系统对血液恶性肿瘤和实体瘤具有广泛的适用性。尽管本发明的重点是癌细胞的靶向和治疗,但也可以使用本发明用病毒抗原而不是癌抗原治疗病毒感染。
38.与表达scar的ipsc-nk细胞组合的本发明的可切换car系统是最可行且广泛适用的策略,以容易地转化为有效的患者疗法。
39.现有技术包含“常规”car-t细胞、表达scar的t细胞和car-nk细胞。通过用作不必与患者匹配的同种异体效应细胞(如常规car-t细胞和scar-t细胞的情况一样),scar-nk细胞改进了这些方法。另外,本发明通过允许靶向的最大灵活性来改进其它car-nk细胞。scar系统与ipsc源性car-nk细胞组合。这种组合提供了最大的灵活性,以利用与可溶性开关组合的一个标准化的同种异体效应细胞群来产生一种通用的细胞疗法方法——既因为nk细胞不需要源自个体患者,又因为可溶性开关可以用于基本上靶向任何肿瘤抗原(或多种肿瘤抗原),而无需对新的效应细胞群进行工程化。
40.另外,可以使用与针对2种(或更多种)肿瘤抗原的开关组合的scar-ipsc-nk细胞预防肿瘤抗原丢失逃逸变体。开关介导的靶向还可以与治疗性单克隆抗体(抗her2、抗egfr等)组合以更有效地靶向和杀伤肿瘤。
41.本发明允许使用相同的表达scar的ipsc源性nk细胞来治疗血液恶性肿瘤和实体瘤两者。以此方式,scar-ipsc-nk细胞再次为“现成的”细胞免疫疗法提供了一种通用策略,所述细胞免疫疗法可能在该领域中产生范式转换影响。
42.在实施例中,本发明提供了一种用可切换嵌合抗原受体(scar)工程化的自然杀伤(nk)细胞。在实施例中,所述scar包括对与肽新抗原表位(pne)结合具有特异性的抗体scfv区。在实施例中,所述scar进一步包括nkg2d跨膜结构域、2b4共刺激结构域和cd3ζ链。在实施例中,所述scar包括替代性信号传导结构域,包含但不限于:cd8a胞外结构域的胞外结构域,cd28、cd16、nkp44、nkp46的跨膜结构域;cd28、cd137、dap10和dap12的细胞质信号传导结构域。(19)
43.在实施例中,所述nk细胞进一步包括与所述scar结合的开关,其中所述开关包括
与抗癌或抗病毒抗体fab区融合的pne,所述抗癌或抗病毒抗体fab区对与癌症抗原或病毒抗原结合具有特异性。在实施例中,所述癌症抗原是cd19或卷曲蛋白7。在实施例中,本发明提供的是,所述癌症或病毒抗原可以是本文所公开的或本领域已知的那些癌症或病毒抗原中的任何癌症或病毒抗原。
44.在实施例中,所述nk细胞源自人诱导的多能细胞。在实施例中,本发明提供了所述scar-nk细胞的细胞培养物。
45.在实施例中,本发明提供了一种治疗受试者的癌症或病毒的方法,所述方法包括向有需要的受试者施用有效量的自然杀伤(nk)细胞,所述nk细胞用针对所述癌症或所述病毒的抗原活化的可切换嵌合抗原受体(scar)工程化。
46.在实施例中,所述scar包括对与肽新抗原表位(pne)结合具有特异性的抗体scfv区。在实施例中,所述scar进一步包括nkg2d跨膜结构域、2b4共刺激结构域和cd3ζ链。
47.在实施例中,所述scar-nk细胞通过与开关结合而被进一步活化,其中所述开关包括分别与抗癌或抗病毒抗体fab区融合的pne,所述抗癌或抗病毒抗体fab区对与所述癌症抗原或所述病毒抗原结合具有特异性。在实施例中,所述癌症抗原是cd19或卷曲蛋白7。在实施例中,本发明提供的是,所述癌症或病毒抗原可以是本文所公开的或本领域已知的那些癌症或病毒抗原中的任何癌症或病毒抗原。
48.在实施例中,所述开关可以使用除靶向癌症或病毒抗原的fab片段之外的结合分子。在实施例中,天然抗原相互作用蛋白结构域用于与特异性抗原结合。
(26)
在实施例中,蛋白质天然表达活化受体,所述活化受体在配体结合时活化免疫应答。在实施例中,nk细胞表达自然杀伤组2(即成员d(nkg2d),一种活化受体),所述自然杀伤组在配体结合时通过衔接分子dap10活化免疫细胞,由此触发细胞增殖、促炎性细胞因子产生和靶细胞消除。nkg2d配体(nkg2dl)包含主要组织相容性复合体(mhc)i类相关链a和b(分别为mica和micb)以及六种独特的长16结合蛋白(ulbp1-6)。在实施例中,可以使用其它nk细胞活化受体。其它nk细胞活化受体的实例包含:天然细胞毒性受体(ncr)、dnax辅助分子1(dnam1)和活化杀伤细胞免疫球蛋白样受体(kar)。
49.在实施例中,所述nk细胞是同种异体的。在实施例中,所述癌症是难治性的在实施例中,所述癌症是血液肿瘤或实体瘤。在实施例中,所述肿瘤是淋巴的或卵巢的。在实施例中,本发明提供的是,所述癌症可以是公开或已知的任何癌症。在实施例中,本发明提供的是,病毒可以是公开或已知的任何病毒。
50.在实施例中,本发明提供的是,所述方法可以进一步包括施用治疗量的针对所述癌症或病毒的单克隆抗体疗法。
51.在实施例中,本发明提供了包括如本文所述的nk细胞的药物组合物。在实施例中,本发明提供了所述scar-nk细胞的细胞培养物。
52.在实施例中,本发明提供了制造自然杀伤scar-nk细胞的方法,所述方法包括:对nk细胞进行工程化以展示包括可切换嵌合抗原受体(scar)的跨膜蛋白;以及储存工程化的nk细胞以随后活化所述scar。
53.在实施例中,本发明提供的是,所述scar包括对与肽新抗原表位(pne)结合具有特异性的抗体scfv区。在实施例中,所述scar进一步包括nkg2d跨膜结构域、2b4共刺激结构域和cd3ζ链。
54.在实施例中,本发明提供的是,所述制造方法进一步包括通过将所述scar与开关结合来活化所述scar,其中所述开关包括分别与抗癌或抗病毒抗体fab区融合的pne,所述抗癌或抗病毒抗体fab区对与癌症抗原或病毒区结合具有特异性。
55.采用了现有的scar模块,并将其工程化到nk细胞中,包含nk92和ips源性nk细胞(ips-nk)。如图1a-1c所示,与由通过铰链和跨膜结构域融合在一起的肿瘤抗原识别胞外域(svfc)和细胞内活化结构域构成的常规car(图1a)相比,scar(图1b)不同,因为其通常由类似的结构域展示构成,除了svfc的特异性不是针对肿瘤抗原,而是针对源自酵母gcn4蛋白的14aa的通用肽,即肽新抗原表位(pne)之外。pne连同其融合的单克隆抗体片段(fab)用作测定抗原特异性的“开关”分子。通过这种灵活的开关,scar系统允许car细胞的制备是通用的,并且独立于靶向的肿瘤抗原。此外,即使已经在患者体内施用scar细胞后,所述系统也允许重新定向抗原靶标。而且,开关依赖性允许更精确地控制car的活性,并且预测此控制将通过适当的给药减少car疗法的当前并发症。此外,如已经简要提及的,为了更好地促进nk细胞对肿瘤细胞的细胞毒性效应,在本发明中构建的scar含有pne特异性scfv,所述pne特异性scfv然后与nk细胞优化的car4信号传导基序组合,所述car4信号传导基序由nkg2d跨膜结构域、2b4共刺激结构域和cd3ζ链组成(称为car4,图1c)。将这些基序并入到scar系统中将进一步增强nk细胞功能。
56.已经使用nk92细胞和ipsc源性nk细胞来产生表达scar的nk细胞。使用ipsc源性nk细胞有若干个优点。这些细胞具有正常的nk细胞表型和基因表达谱(而nk92细胞是非整倍体,并且必须在施用于患者之前进行辐照)。现在可以在临床规模的cgmp条件下完成ipsc源性nk细胞的生产。因此,表达scar的ipsc源性nk细胞提供了可以基本上无限供应地生产的统一群体。由于nk细胞不必与特定患者相匹配(即,其起同种异体效应细胞的作用),因此可以使用与可溶性抗肿瘤开关组合的表达scar的ipsc源性nk细胞的一个标准化群体来由一个标准化“现成的”nk细胞产品靶向不同的肿瘤。这为所靶向的基于细胞的疗法提供了“通用”方法。此外,通过使用多个开关与相同的表达scar的nk细胞,可以靶向多于一种肿瘤抗原。
57.本发明可以在商业上应用为:(1)如本发明所述的癌症治疗模式;(2)感染性疾病的治疗模式(通过在hiv感染的细胞上靶向病毒感染的抗原,如gp120)。尽管概念证明研究中的描述和选择的抗原是基于癌症的,但是本发明的效用可以容易地转移到感染性疾病,特别是病毒感染,因为nk细胞杀伤癌细胞和病毒感染的细胞的机制是相似的;以及(3)用于抗原发现和验证研究的工具。基于car的癌症免疫疗法的未来成功在很大程度上取决于可靠的癌症特异性抗原的发现。目前在基因组学、表面蛋白质组学和生物信息学方面的进展使得以比以往更快的速度发现表面癌抗原成为可能。依靠常规的car疗法,将不可能适应日益增长的使用大规模抗原候选物验证car疗法的需求。本发明的scar-nk细胞为基于细胞的免疫疗法提供了一种真正通用的方法。
58.使用scar-nk系统的潜在靶标包含但不限于实体瘤、血液恶性肿瘤和病毒感染的靶标。
59.实体瘤的开关靶标的实例包含但不限于:achr(胎儿乙酰胆碱受体)、b7-h4、caix(碳酸酐酶ix)、cd133(prominin-1)、cd44v6、cd47(整合素相关蛋白或iap)、cd70-用于多种疾病类别、cea(癌胚抗原)、c-met(c-间充质-上皮转换因子)、dll3(δ样3)、egfr(表皮生长
因子受体)、egfrviii(iii型变异表皮生长因子受体、epcam(上皮细胞粘附分子)、epha2(产生促红细胞生成素的肝细胞癌a2)、erbb2、fap(成纤维细胞活化蛋白)、fra(叶酸受体α)、卷曲蛋白7(fzd7)、gd2(神经节苷脂gd2)、gpc3(磷脂酰肌醇蛋白聚糖-3)、gucy2c(鸟苷酰基环化酶c)、her1(人表皮生长因子受体1)、her2(erbb2,人表皮生长因子2)、icam-1(细胞间粘附分子1)、il11rα(白细胞介素11受体a)、il13rα2(白细胞介素13受体a2)、l1-cam(人l1细胞粘附分子,cd171),ley(lewis y抗原)、mage(黑素瘤相关抗原)、mcam(cd146)(黑素瘤细胞粘附分子)、间皮素、muc1(粘蛋白1)、muc16 ecto(粘蛋白16)、nkg2dl(自然杀伤组2成员d配体)、ny-eso-1(癌症/睾丸抗原1)、pd-l1(b7-h1)(cd274)、psca(前列腺干细胞抗原)、psma(前列腺特异性膜抗原)、ror1(受体酪氨酸激酶样孤儿受体)-用于多种疾病类别、tag72(肿瘤相关糖蛋白-72)和vegfr(血管内皮生长因子受体1)。
60.血液恶性肿瘤的开关靶标的实例包含但不限于:bcma(b细胞成熟抗原)、cd123、cd138(多配体聚糖-1)、cd19、cd20、cd22、cd24、cd30、cd33、cd37、cd38、cd4-用于多种疾病类别、cd7、cd70-用于多种疾病类别、cll1、cs1(连接区段1)、κ轻链和ror1(受体酪氨酸激酶样孤儿受体)-用于多种疾病类别。
61.病毒感染的开关靶标的实例包含但不限于:hiv(包膜糖蛋白gp120)、cd4-用于多种疾病类别、hbv(hbsag-乙型肝炎表面抗原)、ebv(lmp1-潜伏膜蛋白1)、cmv(gb-糖蛋白b)和hcv(糖蛋白e2)。
62.本说明书中所提及的所有公开、专利以及专利申请通过引用并入本文,其程度如同每个单独的公开、专利或专利申请被专门地且单独地指示通过引用并入。
63.除非另外定义,否则本文使用的所有技术和科学术语以及任何首字母缩写具有与本发明领域的普通技术人员通常理解的含义相同的含义。虽然可以在本发明的实践中使用与本文所描述的那些类似或等效的任何方法和材料,但是本文中描述了示例性方法、装置和材料。
64.除非另有指示,否则本发明的实践将采用在本领域技术范围内的常规分子生物学(包含重组技术)、微生物学、细胞生物学、生物化学和免疫学技术。此类技术在如以下文献中有充分解释:《分子克隆:实验室手册(molecular cloning:实验室手册(molecular cloning:a laboratory manual)》,第2版(sambrook等人,1989);《寡核苷酸合成(oligonucleotide synthesis)》(m.j.gait编辑,1984);《动物细胞培养(animal cell culture)》(r.i.freshney编辑,1987);《酶学方法(methods in enzymology)》(学术出版社有限公司(academic press,inc.));《当代分子生物学方案(current protocols in molecular biology)》(f.m.ausubel等人编辑,1987,并且定期更新);《pcr:聚合酶链反应(pcr:the polymerase chain reaction)》(mullis等人编辑,1994);《雷明顿:药学科学与实践(remington,the science and practice of pharmacy)》,第20版,利平科特
·
威廉斯和威尔金斯出版公司(lippincott,williams&wilkins),2003以及《雷明顿:药学科学与实践》,第22版,制药出版社(pharmaceutical press)和费城科学大学药学院(philadelphia college of pharmacy at the university of sciences),2012)。
65.如本文所使用的,术语“包括(comprises)”、“包括(comprising)”、“包含(includes)”、“包含(including)”、“具有(has)”、“具有(having)”“含有(contains)”、“含有(containing)”、“特征在于”或其任何其它变体旨在涵盖所列举的组件的非排他性包含,
经受以其它方式明确指出的任何限制。例如,融合蛋白、药物组合物和/或“包括”要素列表(例如,组分、特征或步骤)的方法不一定仅限于那些元件(或组分或步骤),而是可以包含融合蛋白未明确列出或固有的其它元件(或组分或步骤)、药物组成和/或方法。
66.如本文所使用的,过渡短语“由
……
组成(consists of)”和“由
……
组成(consisting of)”不包括未指定的任何要素、步骤或组分。例如,权利要求中使用的“由
……
组成(consists of)”或“由
……
组成(consisting of)”将权利要求限制到权利要求中具体列举的组分、材料或步骤,除了通常与其相关的杂质(即,给定组分内的杂质)之外。当短语“由
……
组成(consists of)”或“由
……
组成(consisting of)”出现在权利要求主体的条款中,而不是紧接在序言之后时,短语“由
……
组成(consists of)”或“由
……
组成(consisting of)”仅限制所述条款中阐述的要素(或组分或步骤);其它要素(或组分)作为整体未被排除在权利要求之外。
67.如本文所使用的,过渡短语“基本上由
……
组成(consists essentially of)”和“基本上由
……
组成(consisting essentially of)”用于定义融合蛋白、药物组合物和/或方法,除了那些字面上公开的之外,所述融合蛋白、药物组合物和/或方法包含材料、步骤、特征、组分或要素,条件是这些另外的材料、步骤、特征、组分或要素不会实质性地影响所要求保护的发明的基本和新颖的特性。术语“基本上由
……
组成”占据介于“包括”与“由
……
组成”之间的中间地带。
68.当介绍本发明或其优选的实施例的元件时,冠词“一个(a)”、“一种(an)”、“所述(the)”和“所述(said)”旨在表示存在元件中的一个或多个元件。术语“包括”、“包含”和“具有”旨在为包含性的并且意味着可以存在除所列元件之外的另外元件。
69.当用于两个或更多个项的列表中时,术语“和/或”意指所列项中的任何一项可以单独使用或与所列项中的任何一项或多项组合使用。例如,表达“a和/或b”旨在意指a和b中的一个或两者,即单独的a、单独的b或a和b的组合。表达“a、b和/或c”旨在意指单独的a、单独的b、单独的c、a和b的组合、a和c的组合、b和c的组合、或a、b和c的组合。
70.应理解,本文所述的本发明的方面和实施例包含“由方面和实施例组成”和/或“基本上由方面和实施例组成”。
71.应当理解的是,采用范围格式的描述仅为了方便和简洁起见,并且不应当解释为是对本发明的范围的硬性限制。因此,对范围的描述应当被认为已经明确地公开了所有可能的子范围以及所述范围内的单独数值。例如,对如从1到6-等范围的描述应当被认为是具有明确公开的子范围,如从1到3、从1到4、从1到5、从2到4、从2到6、从3到6等;以及所述范围内的单独数字,例如,1、2、3、4、5和6。无论范围的宽度为多少,这都适用。在本文中,值或范围可以表达为从“约”一个特定值和/或到“约”另一个特定值。当表达此类值或范围时,公开的其它实施例包含所列举的特定值、从一个特定值和/或到其它特定值。类似地,当通过使用先行词“约”将值表达为近似值时,应理解,特定值形成另一个实施例。应进一步理解的是,本文中公开了多个值,并且在本文中,每个值还被公开为除所述值本身之外的“约”所述特定值。在实施例中,“约”可以用于意指例如在所述值的10%内、在所述值的5%内或在所述值的2%内。
72.如本文所使用的,“患者”或“受试者”是指待治疗的人或动物。
73.如本文所使用的,术语“药物组合物”是指药学上可接受的组合物,其中所述组合
物包括药学活性剂,并且在一些实施例中进一步包括药学上可接受的载体。在一些实施例中,药物组合物可以是药物活性剂和载体的组合。
74.术语“组合”是指采用一种剂量单位形式的固定组合或用于组合施用的成套试剂盒,其中一种或多种活性化合物和组合配偶体(例如,如下所述的另一种药物,也称为“治疗剂”或“辅剂”)可以同时或单独地在时间间隔内独立施用。在一些情况下,组合配偶体示出协作性,例如协同效应。如本文所使用的,术语“共同施用”或“组合施用”等意指涵盖向有需要的单个受试者(例如,患者)施用所选组合配偶体,并且旨在包含其中不一定通过相同的施用途径或同时施用药剂的治疗方案。如本文所使用的,术语“药物组合物”意指由多于一种活性成分混合或组合而成的产物,并且包含活性成分的固定和非固定组合两者。术语“固定组合”意指活性成分,例如化合物和组合配偶体,都以单一实体或剂量的形式同时施用于患者。术语“非固定组合”意指活性成分,例如化合物和组合配偶体,都作为单独的实体同时、并发或顺序施用于患者,没有特定的时间限制,其中此类施用在患者体内提供了治疗有效水平的两种化合物。后者也适用于鸡尾酒疗法,例如施用三种或更多种活性成分。
75.如本文所使用的,术语“药学上可接受的”意指除可安全用于动物并且更具体地可用于人和/或非人哺乳动物的其它调配物之外由联邦或州政府的监管机构批准或列于美国药典、其它公认的药典中。
76.如本文所使用的,术语“药学上可接受的载体”是指与去甲基化化合物一起施用的赋形剂、稀释剂、防腐剂、增溶剂、乳化剂、佐剂和/或媒剂。此类载体可以是无菌液体,如水和油,包含石油、动物、植物或合成来源的那些油,如花生油、大豆油、矿物油、芝麻油等,聚乙二醇、甘油、丙二醇或其它合成溶剂。抗菌剂,如苯甲醇或对羟基苯甲酸甲酯;抗氧化剂,如抗坏血酸或亚硫酸氢钠;螯合剂,如乙二胺四乙酸;以及如氯化钠或右旋糖等用于调节张力的药剂,还可以是载体。本领域技术人员已知用于产生与载体组合的组合物的方法。在一些实施例中,语言“药学上可接受的载体”旨在包含与药物施用相容的任何和所有溶剂、分散介质、包衣、等渗剂以及吸收延迟剂等。将这种介质和药剂用于药物活性物质是本领域中熟知的。参见例如《雷明顿:药学科学与实践》,第20版,(利平科特
·
威廉斯和威尔金斯出版公司,2003)。除了任何常规介质或药剂与活性化合物不相容的情况之外,设想此类介质或药剂在组合物中的用途。
77.如本文所使用的,“治疗有效”是指足以治疗或改善、或以某种方式减轻与疾病和医学病状相关的症状的药物活性化合物的量。当参考方法使用时,所述方法足以有效治疗或改善、或以某种方式减轻与疾病或病状相关的症状。例如,关于疾病的有效量是足以阻断或预防发作的量;或者如果疾病病理已经开始,则缓解、改善、稳定、逆转或减缓疾病的进展、或以其它方式减少疾病的病理后果。在任何情况下,有效量可以单剂量或分开的剂量给定。
78.如本文所使用的,术语“治疗(treat)”,“治疗(treatment)”或“治疗(treating)”涵盖至少改善与患者疾病相关的症状,其中广义上使用改善是指至少减少参数的大小,例如与所治疗的疾病或病状相关的症状。如此,“治疗”还包含疾病、病症或病理病状或至少与其相关的症状被完全抑制(例如,防止发生)或停止(例如,终止)使得患者不再患有所述病状或至少表征所述病状的症状的情况。
79.如本文所使用的,除非另有说明,术语“预防(prevent)”,“预防(preventing)”和“预防(prevention)”是指预防疾病或病症或其一种或多种症状发作、复发或扩散。在某些实施例中,所述术语是指在症状发作之前,使用具有一种或多种其它另外的活性剂的本文所提供的化合物或剂型进行治疗或具体地向有风险患有本文所提供的疾病或病症的受试者施用所述化合物或剂型。这些术语涵盖抑制或减少特定疾病的症状。在某些实施例中,具有家族疾病史的受试者是预防方案的潜在候选者。在某些实施例中,具有复发症状史的受试者也是预防的潜在候选者。在这方面,术语“预防”可以与“预防性治疗”互换使用。
80.如本文所使用的,除非另有说明,否则化合物的“预防有效量”是足以预防疾病或病症或防止其复发的量。预防有效量的化合物是指在疾病预防中提供预防性益处的治疗剂单独或与一种或多种其它药剂组合的量。术语“有效量”可以涵盖改善总体预防或增强另一种预防剂的预防功效的量。如本文所使用的,除非另有说明,术语“受试者”在本文中被定义为包含动物,如哺乳动物,包含但不限于灵长类动物(例如,人)、牛、绵羊、山羊、马、狗、猫、兔、大鼠、小鼠等。在具体实施例中,受试者是人。术语“受试者”和“患者”在关于例如哺乳动物受试者,如人方面在本文中可互换地使用。
81.如本文所使用的,术语“抗体”是指免疫球蛋白分子和免疫球蛋白(ig)分子的免疫活性部分,即,含有与抗原免疫特异性结合的抗原结合位点的分子。抗体包含但不限于多克隆、单克隆、嵌合、dab(结构域抗体)、单链、f
ab
、f
ab'
和f
(ab')2
片段、单链fv片段(scfv)和f
ab
表达库。已知碱性抗体结构单元包括四聚体。每个四聚体由两对相同的多肽链构成,每对具有一个“轻”链(约25kda)和一个“重”链(约50-70kda)。每条链的氨基末端部分包含主要负责抗原识别的具有约100到110个或更多个氨基酸的可变区。每条链的羧基端部分限定了主要负责效应子功能的恒定区。通常,从人获得的抗体分子涉及igg、igm、iga、ige和igd类中的任何一种,它们因分子中存在的重链的性质而彼此不同。某些类也有亚类,如igg1、igg2等。此外,在人类中,轻链可以是κ链或λ链。
82.如本文所使用的,术语“抗体”涵盖单克隆抗体(包含全长单克隆抗体)、多克隆抗体、多特异性抗体(例如,双特异性抗体)和抗体片段,只要它们表现出与靶抗原位点以及其所关注同种型结合的所期望的生物活性。术语“抗体片段”包括全长抗体的一部分,通常是抗原结合或其可变区。抗体的fc、fv和fab区在本领域中是众所周知的。如本文所使用的,术语“抗体”涵盖源自任何物种和资源的任何抗体,包含但不限于人抗体、大鼠抗体、小鼠抗体、兔抗体等,并且可以合成制备或天然存在。
83.如本文所使用的,术语“单克隆抗体”是指从基本上均质抗体群体中获得的抗体,即包括所述群体的单独抗体是相同的,除了可以少量存在的可能天然存在的突变之外。单克隆抗体是高度特异性的,针对单个抗原位点。此外,与通常包含针对不同决定簇(表位)的不同抗体的常规(多克隆)抗体制剂相比,每种单克隆抗体针对抗原上的单一决定簇。还可以使用本领域已知的技术从噬菌体抗体库中分离“单克隆抗体”。
84.本文中的单克隆抗体包含“嵌合”抗体(免疫球蛋白),其中重链和/或轻链的一部分与源自特定物种或属于特定抗体类或亚类的抗体中的对应序列相同或同源,而链的其余部分与源自另一物种或属于另一抗体类或亚类的抗体以及此类抗体的片段中的对应序列相同或同源,只要它们表现出所期望的生物活性即可。如本文所使用的,“嵌合蛋白”或“融合蛋白”包括与第二多肽可操作地连接的第一多肽。嵌合蛋白可以任选地包括与第一多肽或第二多肽可操作地连接的第三多肽、第四多肽或第五多肽或其它多肽。嵌合蛋白可以包
括两种或更多种不同的多肽。嵌合蛋白可以包括相同多肽的多个拷贝。嵌合蛋白还可以包括一种或多种多肽中的一种或多种突变。用于制备嵌合蛋白的方法在本领域中是众所周知的。
85.为了避免单克隆抗体在人中的潜在免疫原性,具有所期望的功能的单克隆抗体优选地为人或人源化的。非人(例如,鼠类)抗体的“人源化”形式是嵌合抗体,所述嵌合抗体含有源自非人免疫球蛋白的最小序列。在大多数情况下,人源化抗体是人免疫球蛋白(受体抗体),其中受体的超可变区残基被来自非人物种(供体抗体)的超可变区残基替代,所述非人物种如具有所期望的特异性、亲和力和能力的小鼠、大鼠、兔或非人灵长类动物。此外,人源化抗体可以包括在受体抗体或供体抗体中未发现的残基。进行这些修饰以进一步改善抗体性能。
86.术语“抗原结合位点”或“结合部分”是指参与抗原结合的抗体分子部分。抗原结合位点由重链(“h”)和轻链(“l”)的n末端可变区(“v”)的氨基酸残基形成。重链和轻链的v区内的三个高度趋异的延伸段(被称为“高变区”)插置在更保守的侧翼延伸段(称为“框架区”或“fr”)之间。因此,术语“fr”是指天然存在于免疫球蛋白中的高变区之间并且邻近所述高变区的氨基酸序列。在抗体分子中,轻链的三个高变区和重链的三个高变区在三维空间中相对于彼此安置以形成抗原结合表面。抗原结合表面与所结合抗原的三维表面互补,并且重链和轻链中的每一个的三个高变区被称为“互补决定区”或“cdr”。对每个结构域的氨基酸的指配符合免疫学相关蛋白的卡巴特序列(kabat sequences of proteins of immunological interest)定义(美国国立卫生研究院(national institutes of health),贝塞斯达,马里兰州,(1987和1991))或chothia和lesk,《分子生物学杂志(j.mol.biol.)》196:901-917(1987);chothia等人,《自然(nature)》342:878-883(1989)。cdr鉴定指南可在http://www.bioinf.org.uk/abs/#cdrid处获得。
87.如本文所使用的,术语“表位”包含能够特异性结合抗体或t细胞受体的抗原的任何蛋白质决定簇。表位决定簇通常由如氨基酸或糖侧链等分子的化学活性表面基团组成,并且通常具有特异性三维结构特征以及特异性电荷特性。例如,可以产生针对多肽的n端或c端肽的抗体。当解离常数≤1μm时,认为抗体特异性结合抗原;优选地≤100nm,并且最优选地≤10nm。如本文所使用的,术语“肽新抗原表位(pne)”包含以前未被免疫系统识别的任何表位。pne可以用于靶向具有肿瘤特异性突变抗原(新抗原)的肿瘤细胞,从而实现个体化免疫疗法。
88.实例
89.表达scar的nk细胞:由于scar系统以前仅在t细胞中进行测试,因此对在nk92细胞中表达的抗cd19 scar进行了初始概念验证测试。nk92是一种以前曾用于测试新颖nk细胞-car构建体的nk细胞系
19
。在此,与在nk细胞中表达的car-t细胞构建体相比,对scar进行重新工程化,以包含上述介导nk细胞内信号传导通路活化并改进nk-car抗肿瘤活性的car4 nk细胞信号传导结构域
19
。证明了抗cd19开关和抗fzd7开关介导特异性杀伤cd19
+
raji b细胞成淋巴细胞白血病(血液恶性肿瘤模型)或fzd7
+
ma148卵巢癌细胞系(实体瘤模型)的功效(图2a-2b)。对于抗cd19开关,仅当使用cd19缺失的raji细胞和cd19阴性k562细胞呈递抗cd19开关时,才证明杀伤的特异性(图2a和数据未示出)。图2b示出了在存在不同fzd7开关的情况下,通过scar4-nk92细胞杀伤ma148细胞。
90.在ma-148模型中,再次使用crispr/cas9系统获得fzd7阴性(ma148ko细胞),以证明特异性fzd7接合。有趣的是,与nk92-scar4组合的6个fzd7开关中的5个开关能够介导对ma148细胞的抗原特异性杀伤,但未能介导对fdz7阴性ma148 ko细胞的抗原特异性杀伤。如所期望的,缺少pne的wt开关不与nk92细胞上的scar4结合,也不介导ma148细胞的杀伤。
91.表达scar的ipsc源性nk细胞的成功衍生和功能:在确认scar可以在nk92细胞中成功表达并发挥作用后,在人ipsc中表达scar构建体。在此,使用ucb源性ipsc系(uipsc)。用通过吉欧霉素选择的piggybac-scar4转染uipsc,并且通过gfp表达鉴定scar的稳定表达。接下来,如前所述,使用两阶段分化过程将uipsc分化为成熟nk细胞
19-22
。在阶段i,用所限定的细胞因子培养的scar转染的ipsc促进造血分化,如通过cd34
+
cd31
+
和cd34
+
cd43
+
造血祖细胞的发育所证明的。接下来,这些造血祖细胞分化为cd56
+
cd45
+
nk细胞,所述nk细胞表现出稳定的car表达(gfp
+
)(图3a-3b),并且具有正常表型,其中表达cd56、nkg2a、nkg2c、nkg2d、nkp44、nkp46、kir、fas和trail,如在之前的研究中一样
19
,20
,23
。
92.图3a-3b:在表达scar的ipsc中的造血和nk细胞分化。图3a示出了正常的造血-内皮细胞分化,其示出如在先前研究中所见的源自表达scar的ipsc的cd34+cd31+和cd34+cd43+细胞
19,20
。图3b示出了由表达scar的ipsc发育而来的正常nk细胞,其示出》95%cd45+cd56+nk细胞和》60%scar+cd56+nk细胞。如前所述,这些ipsc-nk细胞扩增为均匀的》95%cd56+nk细胞群。
19,20
93.表达scar的ipsc-nk细胞的抗肿瘤活性:与nk92-scar4细胞相似,ipsc-nk-scar4细胞能够在存在2种fdz7特异性开关(2108-ctbv和2106-lcct)的情况下介导肿瘤细胞系ma148的抗原特异性杀伤,但当敲除ma148细胞中的fdz7时则不能(图4)。
94.图4:在ipsc-nk细胞中的scar介导的抗肿瘤活性。在存在1nm的抗fzd7开关ctbv和lcct或wt阴性对照开关的情况下,将ipsc-nk-scar4细胞与靶细胞[亲本ma148细胞(左)或ma148-fdz7 ko细胞(右)]共培养(如在图1中一样)。这些研究证明了对fzd7+靶标(左)的有效scar+抗fzd7开关介导的杀伤,但对fzd7-靶标不进行所述杀伤(右)。
[0095]
可以在荧光显微镜下直接在35小时时间段内观察通过nk-scar-nk92细胞对肿瘤细胞的开关介导的杀伤。可以使用基于incucyte的测定定量地测量杀伤作用(图5)。具体地,图5示出了在存在fzd7特异性开关ctbv(2108)和对照开关(2102)的情况下通过scar4-nk细胞对ma148细胞的incucyte杀伤测定。
[0096]
最后,在混合不同抗原特异性的癌细胞的培养物中,证明了由开关的抗原特异性测定的选择性杀伤(图6)。具体而言,图6示出了在含有ma148和k562-cd19两者的混合共培养物中对靶细胞进行的开关介导的抗原特异性杀伤。两种开关以与在单独培养物(右)中的水平相当的水平在混合培养物(左)中诱导特异性杀伤。
[0097]
总之,这种scar-nk细胞策略使得能够密切控制car介导的活性。另外,此系统提供了针对肿瘤细胞上的多种抗原的灵活性,以潜在地防止可能导致复发性疾病的抗原丢失逃逸变体。
[0098]
用表达nk92的scar4测试抗cd19开关:关于b细胞白血病的car-nk研究已经从最初的一个开关(即lcnt)扩展到总共10个抗cd19开关,包含缺乏pne肽的对照开关(图7,rodgers等人,2016)。根据pne移植的位置命名的配置包含:wt(仅fab,不含pne)、hcnt(重链n末端(单价))、lcnt(轻链n末端(单价))、ntbv(n末端二价(两条链))、lcc1(轻链c1)、hcc1
(重链c1)、c1bv(c1二价(两条链))、hcct(重链c末端)、lcct(轻链c末端)和ctbv(c末端二价(两条链))。
[0099]
这些cd19开关已经在膜联蛋白v/7aad杀伤测定中用nk92-scar4进行测试。所有开关均以开关浓度依赖性方式通过nk92-scar4介导对nalm6细胞的杀伤,这与对照wt开关形成鲜明对比(图8,每组n=3或4+/-sem)。具体而言,图8示出了在存在增加浓度的抗cd19开关的情况下对nalm6的car4-nk92诱导的杀伤。每个开关的杀伤ec
50
按prizm计算,如表1所示。
[0100][0101][0102]
表1
[0103]
有趣的是,这些开关在nk92细胞介导的杀伤中示出的相对动力学与如之前由rodgers等人2016年所述的scar-t细胞诱导的细胞毒性中的相对动力学略有不同,这表明在t细胞中测定的开关的相对功效不能针对nk细胞直接转化。
[0104]
aml.本发明扩展到急性髓系白血病(aml)作为靶标的另外的血液恶性肿瘤。为此,开关被工程化为三种aml相关抗原,所述抗原由cd33、cd123和cll1组成。图9a-9c示出了这些抗原在aml细胞系molm14(图9a)、hl60(图9b)和molm13上的表面表达,以及在不同的scar4-nk92与molm14(图9a)或hl60比率(图9b)下、或在不同的开关浓度下(图9c)由这些开关介导的杀伤的相对水平。来自hl60(图9b)和molm13(图9c)的结果似乎表明杀伤敏感性与在靶细胞上表达的抗原水平之间的正相关。在此,将抗cd19和抗fzd7开关用作非特异性开关对照。
[0105]
过去,不同抗原特异性的细胞被人工混合,并且示出开关可以在这些环境中介导特异性杀伤。为了进一步说明更自然的环境中的开关依赖性抗原特异性,使用三个独立供体的商业pbmc(精准医疗(precision for medicine)),并在含有scar4-nk92细胞以及抗cd33或抗cd19开关或两者的共培养物中进行杀伤测定。仅当分别存在抗cd33或抗cd19开关时,才观察到巨噬细胞/单核细胞(表达cd33)或b细胞(表达cd19)的特异性杀伤(图10a-10c)。效应细胞和开关的存在不影响t细胞,因为cd33和cd19不在这些细胞上表达。当使用缺乏pne的wt cd19开关时,巨噬细胞/单核细胞或b细胞的杀伤最小。
[0106]
scar与常规car的比较:为了评估scar系统与常规car相比的功效,进行了两次头对头的体外杀伤测定(et=1:1;n=每组3+/-sd)。在一项测定中,共培养物含有raji或nalm6 b淋巴瘤细胞系、效应子scar4-nk92细胞和10pm抗cd19开关ctbv。在第二项测定中,将cd19-car4-nk92细胞直接与raji或nalm6细胞共培养。图11示出了平均细胞毒性水平。由
开关和scar4介导的对raji的细胞毒性略低于由常规car介导的细胞毒性,而nalm6的杀伤对于两种car系统是相当的。还将使用卵巢抗原fzd7和aml抗原作为靶标进行类似的比较。
[0107]
scar4-p2a-gfp构建体:为了使用gfp更好地监测scar的表达,使用其间的可切割肽p2a(未示出)将scar4与gfp使用相同读框融合的构建体被工程化为替代促进scar4和gfp的双顺反子表达的现有ires片段。用scar4-p2a-gfp转染的nk92细胞阐明了与含ires的构建体相似水平的体外细胞毒性。图12示出了gfp表达水平。具体而言,在用sb-scar4-p2a-gfp或sb-scar4-ires-gfp转染的nk92细胞上的gfp和scar4表达。与wt nk92进行比较。用fc-pne-af647测量scar4的表达。
[0108]
图13示出了在存在不同的抗fzd7开关的情况下,由表达scar4-p2agfp和scar4-ires-gfp的nk92细胞诱导的ma148细胞的体外杀伤的头对头比较。
[0109]
此构建体用于转染ipscs,旨在使成熟的nk细胞再生。在scar4-p2a-gfp转染的ipsc中的scar4的表达可以使用fc-npe-af647通过facs检测,尽管其水平低于nk92细胞上的水平(图14)。
[0110]
scar4-p2a-gfp转染的ipsc保留其多能性(图15a)并分化成造血祖细胞(图15b)。成熟的nk细胞在再生中,并将测试其杀伤肿瘤细胞的功效。
[0111]
本发明的结果令人惊讶且有利。在本发明之前,以前没有建议或试图知道所描述的可切换pne系统将如何使用nk细胞工作。尽管以前的系统已用于t细胞,但若干个因素使本发明的scar-nk细胞系统不同于任何scar-t细胞系统。
[0112]
在本发明之前,由于nk细胞与t细胞之间的显著差异,因此尚不清楚可切换pne系统是否将使用nk细胞工作。由于细胞表面上的密度或持续时间,nk细胞与t细胞之间的scar表达可能不同,这可能影响细胞如何接合开关和靶细胞。另外,nk细胞和t细胞使用不同组的表面受体进行活化、信号传导调节以及与靶细胞的相互作用。因此,在这些不同的受体和共受体相互作用的情况下,不可能基于其与t细胞的作用来预测开关将如何与nk细胞接合。具体而言,在scar4-nk92细胞介导的raji细胞杀伤中的不同cd19开关之间的杀伤动力学不同于t细胞接合的nalm6细胞杀伤的动力学(rodgers等人,2016)。如本发明所示,t细胞的最有效开关不一定是nk细胞的最有效开关,反之亦然。尚不清楚这种差异是否是由于nk细胞与t细胞之间的不同的表面受体拓扑或scar表达水平的影响造成的。
[0113]
在本发明中,还进行了用于在ipsc源性nk细胞中表达的scar遗传载体的优化。具体而言,表达质粒(piggybac)中需要包含绝缘子序列以防止scar基因沉默,而nk92细胞系中的scar表达不需要此类绝缘子。对于nk92细胞,通过使用小得多的载体(sleepingbeauty系统),很容易实现scar4在nk92细胞中的有效表达。此外,作为替代报道蛋白,当两种蛋白质以由scar4-ires-gfp构型中的ires片段介导的双顺反子方式表达时,gfp表达忠实地代表scar4在nk92细胞上的表达。相比之下,gfp表达不能正确指示具有相同构型的ipsc或ipsc-nk细胞上的scar4的表达。为了改善ipsc中的表达系统,新型构建体被工程化,其中ires片段被p2a切割位点替代。使用这种新型构建体,在工程化的ipsc中检测到gfp和scar4(图14)。
[0114]
最后,当面对靶细胞时,nk细胞接合的开关可能在结合携带抗原的细胞的强度方面表现不同于t细胞接合的开关,因此引发不同水平的功效。总之,通过将scar4工程化为ipsc源性nk细胞,制备了一种完全不同的具有自身独特特性的治疗性细胞产品。
res)》,2018;24(22):5502-5515。
[0125]
9.beatty gl、haas ar、maus mv等人,间皮素特异性嵌合抗原受体mrna工程化的t细胞在实体恶性肿瘤中诱导抗肿瘤活性(mesothelin-specific chimeric antigen receptor mrna-engineered t cells induce antitumor activity in solid malignancies),《癌症免疫学研究(cancer immunology research)》,2014;2(2):112-120。
[0126]
10.cummins kd、frey n、nelson am等人,用可生物降解的抗cd123 car修饰的t细胞治疗复发性/难治性(rr)aml(treating relapsed/refractory(rr)aml with biodegradable anti-cd123 car modified t cells),《血液学》,2017;130(增刊1):1359-1359。
[0127]
11.diaconu i、ballard b、zhang m等人,诱导型胱天蛋白酶-9选择性地调节cd19特异性嵌合抗原受体修饰的t细胞的毒性(inducible caspase-9selectively modulates the toxicities of cd19-specific chimeric antigen receptor-modified t cells),《分子疗法》,2017;25(3):580-592。
[0128]
12.rodgers dt、mazagova m、hampton en等人,用于b细胞恶性肿瘤的car-t细胞的开关介导的活化和再靶向(switch-mediated activation and retargeting of car-t cells for b-cell malignancies),《美国国家科学院院刊(proc natl acad sci usa)》,2016;113(4):e459-468。
[0129]
13.viaud s、ma jsy、hardy ir等人,对体内car t细胞扩增、b细胞耗竭和记忆诱导的可切换控制(switchable control over in vivo car t expansion,b cell depletion,and induction of memory),《美国国家科学院院刊》,2018;115(46):e10898-e10906。
[0130]
14.cao y、rodgers dt、du j等人,靶向乳腺癌的可切换嵌合抗原受体t细胞的设计(design of switchable chimeric antigen receptor t cells targeting breast cancer),《应用化学国际英文版(angew chem int ed engl)》,2016;55(26):7520-7524。
[0131]
15.raj d、yang mh、rodgers d等人,可切换car-t细胞介导转移性胰腺导管腺癌的缓解(switchable car-t cells mediate remission in metastatic pancreatic ductal adenocarcinoma),《肠道(gut)》,2018。
[0132]
16.morsut l、roybal kt、xiong x等人,使用合成notch受体对定制细胞感测和应答行为进行工程化(engineering customized cell sensing and response behaviors using synthetic notch receptors),《细胞(cell)》,2016;164(4):780-791。
[0133]
17.lim wa、june ch,对免疫细胞进行工程化以治疗癌症的原理(the principles of engineering immune cells to treat cancer),《细胞》,2017;168(4):724-740。
[0134]
18.cho jh、collins jj、wong ww,用于t细胞应答的多重和逻辑控制的通用嵌合抗原受体(universal chimeric antigen receptors for multiplexed and logical control of t cell responses),《细胞》,2018;173(6):1426-1438.e1411。
[0135]
19.y,hermanson dl、moriarity bs、kaufman ds,用嵌合抗原受体工程化的人ipsc源性自然杀伤细胞增强抗肿瘤活性(human ipsc-derived natural killer cells engineered with chimeric antigen receptors enhance anti-tumor activity),《细胞干细胞(cell stem cell)》,2018;23(2):181-192e185。
[0136]
20.knorr da、ni z、hermanson d等人,用于癌症疗法的从人多能干细胞临床规模推导自然杀伤细胞(clinical-scale derivation of natural killer cells from human pluripotent stem cells for cancer therapy),《干细胞转化医学(stem cells translational medicine)》,2013;2(4):274-283。
[0137]
21.bock am、knorr d、kaufman ds,从人胚胎干细胞(hesc)和诱导的多能干细胞(ipsc)开发、扩增和体内监测人nk细胞(development,expansion,and in vivo monitoring of human nk cells from human embryonic stem cells(hescs)and induced pluripotent stem cells(ipscs)),《可视实验杂志(j vis exp)》,2013(74):e50337。
[0138]
22.hermanson dl、bendzick l、pribyl l等人,用于治疗卵巢癌的诱导的多能干细胞源性自然杀伤细胞(induced pluripotent stem cell-derived natural killer cells for treatment of ovarian cancer),《干细胞(stem cells)》,2016;34(1):93-101。
[0139]
23.ni z、knorr da、bendzick l、allred j、kaufman ds,通过源自人多能干细胞的天然杀伤细胞表达嵌合受体cd4ζ改善体外活性,但不会增强对体内hiv感染的抑制(expression of chimeric receptor cd4ζby natural killer cells derived from human pluripotent stem cells improves in vitro activity but does not enhance suppression of hiv infection in vivo),《干细胞》,2014;32(4):1021-1031。
[0140]
24.june ch、sadelain m,嵌合抗原受体疗法(chimeric antigen receptor therapy),《新英格兰医学杂志(new england journal of medicine)》,2018;379(1):64-73。
[0141]
25.ps woll、ch martin、js miller、ds kaufman,人胚胎干细胞源性nk细胞获取功能性受体和溶细胞活性(human embryonic stem cell-derived nk cells acquire functional receptors and cytolytic activity),《免疫学期刊(j immunol.)》,175(2005),第5095-5103页。
[0142]
26.deng x,nkg2d car-t细胞对人结肠直肠癌细胞的体内和体外抗肿瘤活性(antitumor activity of nkg2d car-t cells against human colorectal cancer cells in vitro and in vivo),《美国癌症研究杂志(am j cancer res.)》,2019;9(5):945-958。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1