作为FGFR抑制剂的双环杂环的制作方法
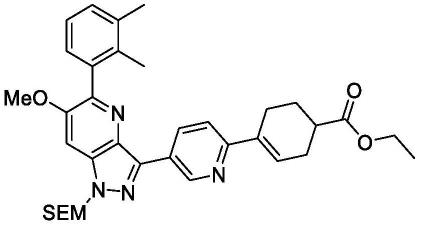
作为fgfr抑制剂的双环杂环
技术领域
1.本发明涉及作为酶fgfr的抑制剂并且可用于治疗诸如癌症的fgfr相关疾病的双环杂环,及其药物组合物。
背景技术:
2.成纤维细胞生长因子受体(fgfr)是结合至成纤维细胞生长因子(fgf)配体的受体酪氨酸激酶。四种fgfr蛋白(fgfr1-4)能够结合配体并且参与包括组织发育、血管生成、伤口愈合和代谢调控在内的多种生理学过程的调控。在配体结合时,所述受体经历二聚化和磷酸化,导致蛋白激酶活性的刺激和多种胞内对接蛋白的募集。这些相互作用促进包括ras-mapk、akt-pi3k和对于细胞生长、增殖和存活至关重要的磷脂酶c在内的胞内信号传导通路的阵列的激活(在eswarakumar等人cytokine&growth factor reviews,2005,16,139-149中综述)。通过fgf配体或fgfr的过表达或fgfr中的激活性突变引起的此通路的异常激活可导致肿瘤发育、进展和对常规癌症疗法的抗性。在人癌症中,已描述了导致配体非依赖性受体激活的基因改变,包括基因扩增、染色体易位和体细胞突变(在knights和cook,pharmacology&therapeutics,2010,125,105-117;turner和grose,nature reviews cancer,2010,10,116-129中综述)。数千个肿瘤样品的大规模dna测序已揭露,fgfr基因在多种癌症中发生改变(helsten等人clin cancer res.2016,22,259
–
267)。这些激活性突变中的一些与导致骨胳发育不良综合征的生殖系突变相同(gallo等人cytokine&growth factor reviews 2015,26,425
–
449)。人疾病中导致异常配体依赖性信号传导的机制包括fgf过表达和产生具有更混乱配体结合能力的受体的fgfr剪接变化。因此,靶向fgfr的抑制剂的开发可用于具有升高的fgf或fgfr活性的疾病的临床治疗。
3.其中涉及fgf/fgfr的癌症类型包括但不限于:癌(例如,膀胱、乳房、结肠直肠、子宫内膜、胃、头部和颈部、肾、肺、卵巢、前列腺);造血系统恶性肿瘤(例如,多发性骨髓瘤、急性骨髓性白血病和骨髓增生性赘生物);和其他赘生物(例如,胶质母细胞瘤和肉瘤)。除了在致癌性赘生物中的作用以外,fgfr激活还已涉及包括但不限于软骨发育不全和颅缝早闭综合征的骨胳和软骨细胞病症。
4.持续需要开发用于癌症治疗的新药物,并且本文所述的fgfr抑制剂帮助解决这种需要。
技术实现要素:
5.本公开涉及具有式(i)的化合物:
6.7.或其药学上可接受的盐,其中构成变量定义于本文中。
8.本公开进一步涉及包含式(i)化合物或其药学上可接受的盐和至少一种药学上可接受的载剂的药物组合物。
9.本公开进一步涉及抑制fgfr酶(例如fgfr3酶)的方法,其包括使所述酶与式(i)化合物或其药学上可接受的盐接触。
10.本公开进一步涉及一种治疗与fgfr酶(例如fgfr3酶)的异常活性或表达相关的疾病的方法,其包括向有需要的患者施用式(i)化合物或其药学上可接受的盐。
11.本公开进一步涉及用于治疗与fgfr酶(例如fgfr3酶)的异常活性或表达相关的疾病的式(i)化合物。
12.本公开进一步涉及一种用于治疗有需要的患者的由fgfr酶(例如fgfr3酶)或其突变体介导的病症的方法,其包括向所述患者施用式(i)化合物或其药学上可接受的组合物的步骤。
13.本公开进一步涉及一种用于治疗有需要的患者的由fgfr酶(例如fgfr3酶)或其突变体介导的病症的方法,其包括向所述患者施用与如本文所述的另一种疗法或治疗剂组合的式(i)化合物或其药学上可接受的盐或包含式(i)化合物或其药学上可接受的盐的组合物的步骤。
14.本文还提供一种治疗有需要的患者的癌症的方法,其包括向所述患者施用治疗有效量的式i,其中所述癌症的特征为fgfr2和/或fgfr3改变。
15.本公开进一步涉及式(i)化合物用于制备用于疗法中的药剂的用途。
具体实施方式
16.化合物
17.在一个方面,本公开提供式(i)化合物:
[0018][0019]
或其药学上可接受的盐,其中:
[0020]
cy1选自苯基和5-6元杂芳基;其中每个5-6元杂芳基具有至少一个成环碳原子和独立地选自n、o和s的1、2或3个成环杂原子;其中n和s任选地被氧化;其中5-6元杂芳基的成环碳原子任选地被氧代取代以形成羰基;并且其中所述苯基和5-6元杂芳基各自任选地被独立地选自r
10
的1、2、3或4个取代基取代;
[0021]
r1选自卤基、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-6
环烷基、4-5元杂环烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、c
1-3
烷氧基-c
1-3
烷基、c
1-3
烷氧基-c
1-3
烷氧基、ho-c
1-3
烷氧基、ho-c
1-3
烷基、氰基-c
1-3
烷基、h2n-c
1-3
烷基、c
1-6
烷基氨基、二(c
1-6
烷基)氨基、c
1-6
烷基硫基、c
1-6
烷基磺酰基、c
1-6
烷基羰基和c
1-6
烷氧基羰基;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c1-6
卤代烷基、c
3-6
环烷基、4-5元杂环烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、c
1-3
烷氧基-c
1-3
烷基、c
1-3
烷氧基-c
1-3
烷氧基、ho-c
1-3
烷氧基、ho-c
1-3
烷基、氰基-c
1-3
烷基、h2n-c
1-3
烷基、c
1-6
烷基氨基、二(c
1-6
烷基)氨基、c
1-6
烷基硫基、c
1-6
烷基磺酰基、c
1-6
烷基羰基和c
1-6
烷氧基羰基的一个或多个h原子任选地被一个或多个d原子替换;
[0022]
每个r2和r3独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-10元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基、5-10元杂芳基-c
1-3
亚烷基、卤基、cn、no2、or
a2
、sr
a2
、c(o)r
b2
、c(o)nr
c2rd2
、c(o)or
a2
、oc(o)r
b2
、oc(o)nr
c2rd2
、nr
c2rd2
、nr
c2
c(o)r
b2
、nr
c2
c(o)or
a2
、nr
c2
c(o)nr
c2rd2
、c(=nr
e2
)r
b2
、c(=nor
a2
)r
b2
、c(=nr
e2
)nr
c2rd2
、nr
c2
c(=nr
e2
)nr
c2rd2
、nr
c2
s(o)r
b2
、nr
c2
s(o)2r
b2
、nr
c2
s(o)2nr
c2rd2
、s(o)r
b2
、s(o)nr
c2rd2
、s(o)2r
b2
和s(o)2nr
c2rd2
;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-10元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基和5-10元杂芳基-c
1-3
亚烷基各自任选地被独立地选自r
21
的1、2、3或4个取代基取代;
[0023]
或苯环上的两个相邻r2取代基与其连接的原子一起形成稠合5元或6元环烷基环或稠合5元或6元杂环烷基环;其中每个稠合5元或6元杂环烷基环具有至少一个成环碳原子和独立地选自n、o和s的1或2个成环杂原子;其中每个稠合5元或6元杂环烷基环的成环碳原子任选地被氧代取代以形成羰基;并且其中所述稠合5元或6元环烷基环和所述稠合5元或6元杂环烷基环各自任选地被独立地选自r
21
的1、2、3或4个取代基取代;
[0024]
n选自0、1、2和3;
[0025]
每个r
10
独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-10
环烷基、4-12元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-12元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基、5-10元杂芳基-c
1-3
亚烷基、卤基、d、cn、no2、or
a1
、sr
a1
、c(o)r
b1
、c(o)nr
c1rd1
、c(o)or
a1
、oc(o)r
b1
、oc(o)nr
c1rd1
、nr
c1rd1
、nr
c1
c(o)r
b1
、nr
c1
c(o)or
a1
、nr
c1
c(o)nr
c1rd1
、c(=nr
e1
)r
b1
、c(=nor
a1
)r
b1
、c(=nr
e1
)nr
c1rd1
、nr
c1
c(=nr
e1
)nr
c1rd1
、nr
c1
s(o)r
b1
、nr
c1
s(o)2r
b1
、nr
c1
s(o)2nr
c1rd1
、s(o)r
b1
、s(o)nr
c1rd1
、s(o)2r
b1
和s(o)2nr
c1rd1
;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-10
环烷基、4-12元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-12元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基和5-10元杂芳基-c
1-3
亚烷基各自任选地被独立地选自r
11
的1、2、3或4个取代基取代;
[0026]
每个r
11
独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-10元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基、5-10元杂芳基-c
1-3
亚烷基、卤基、d、cn、or
a3
、sr
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3rd3
、nr
c3
c(o)r
b3
、nr
c3
c(o)or
a3
、nr
c3
s(o)r
b3
、nr
c3
s(o)2r
b3
、nr
c3
s(o)2nr
c3rd3
、s(o)r
b3
、s(o)nr
c3rd3
、s(o)2r
b3
和s(o)2nr
c3rd3
;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-10元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基和5-10元杂芳基-c
1-3
亚烷基各自任选地被独立地选自r
12
的1、2、3或4个取代基取代;
[0027]
每个r
12
独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-6
环烷基、c
6-10
芳基、5-10元杂芳基、4-7元杂环烷基、卤基、d、cn、or
a5
、sr
a5
、c(o)r
b5
、c(o)nr
c5rd5
、c(o)or
a5
、nr
c5rd5
、nr
c5
c(o)r
b5
、nr
c5
c(o)or
a5
、nr
c5
s(o)r
b5
、nr
c5
s(o)2r
b5
、nr
c5
s(o)2nr
c5rd5
、s(o)r
b5
、s(o)
nr
c5rd5
、s(o)2r
b5
和s(o)2nr
c5rd5
;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-6
环烷基、c
6-10
芳基、5-10元杂芳基和4-7元杂环烷基各自任选地被独立地选自rg的1、2、3或4个取代基取代;
[0028]
每个r
21
独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-10元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基、5-10元杂芳基-c
1-3
亚烷基、卤基、d、cn、or
a4
、sr
a4
、c(o)r
b4
、c(o)nr
c4rd4
、c(o)or
a4
、nr
c4rd4
、nr
c4
c(o)r
b4
、nr
c4
c(o)or
a4
、nr
c4
s(o)r
b4
、nr
c4
s(o)2r
b4
、nr
c4
s(o)2nr
c4rd4
、s(o)r
b4
、s(o)nr
c4rd4
、s(o)2r
b4
和s(o)2nr
c4rd4
;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-10元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基和5-10元杂芳基-c
1-3
亚烷基各自任选地被独立地选自r
22
的1、2、3或4个取代基取代;
[0029]
每个r
22
独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-6
环烷基、苯基、5-6元杂芳基、4-7元杂环烷基、卤基、d、cn、or
a6
、sr
a6
、c(o)r
b6
、c(o)nr
c6rd6
、c(o)or
a6
、nr
c6rd6
、nr
c6
c(o)r
b6
、nr
c6
c(o)or
a6
、nr
c6
s(o)r
b6
、nr
c6
s(o)2r
b6
、nr
c6
s(o)2nr
c6rd6
、s(o)r
b6
、s(o)nr
c6rd6
、s(o)2r
b6
和s(o)2nr
c6rd6
;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-6
环烷基、苯基、5-6元杂芳基和4-7元杂环烷基各自任选地被独立地选自rg的1、2、3或4个取代基取代;
[0030]
每个r
a1
、r
c1
和r
d1
独立地选自h、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基和5-10元杂芳基;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基和5-10元杂芳基各自任选地被独立地选自r
11
的1、2、3或4个取代基取代;
[0031]
或连接至同一个n原子的任何r
c1
和r
d1
与其连接的n原子一起形成任选地被独立地选自r
11
的1、2、3或4个取代基取代的4元、5元、6元或7元杂环烷基;
[0032]
每个r
b1
独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基和5-10元杂芳基;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基和5-10元杂芳基各自任选地被独立地选自r
11
的1、2、3或4个取代基取代;
[0033]
每个r
e1
独立地选自h、cn、c
1-6
烷基、c
1-6
卤代烷基、c
1-6
烷基硫基、c
1-6
烷基磺酰基、c
1-6
烷基羰基、c
1-6
烷基氨基磺酰基、氨甲酰基、c
1-6
烷基氨甲酰基、二(c
1-6
烷基)氨甲酰基、氨基磺酰基、c
1-6
烷基氨基磺酰基和二(c
1-6
烷基)氨基磺酰基;
[0034]
每个r
a2
、r
c2
和r
d2
独立地选自h、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基和5-10元杂芳基;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基和5-10元杂芳基各自任选地被独立地选自r
21
的1、2、3或4个取代基取代;
[0035]
或连接至同一个n原子的任何r
c2
和r
d2
与其连接的n原子一起形成任选地被独立地选自r
21
的1、2或3个取代基取代的4元、5元、6元或7元杂环烷基;
[0036]
每个r
b2
独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基和5-10元杂芳基;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基和5-10元杂芳基各自任选地被独立地选自r
21
的1、2、3或4个取代基取代;
[0037]
每个r
e2
独立地选自h、cn、c
1-6
烷基、c
1-6
卤代烷基、c
1-6
烷基硫基、c
1-6
烷基磺酰基、c1-6
烷基羰基、c
1-6
烷基氨基磺酰基、氨甲酰基、c
1-6
烷基氨甲酰基、二(c
1-6
烷基)氨甲酰基、氨基磺酰基、c
1-6
烷基氨基磺酰基和二(c
1-6
烷基)氨基磺酰基;
[0038]
每个r
a3
、r
c3
和r
d3
独立地选自h、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-6
环烷基、苯基、5-6元杂芳基和4-7元杂环烷基;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-6
环烷基、苯基、5-6元杂芳基和4-7元杂环烷基各自任选地被独立地选自r
12
的1、2、3或4个取代基取代;
[0039]
或连接至同一个n原子的任何r
c3
和r
d3
与其连接的n原子一起形成任选地被独立地选自r
12
的1、2或3个取代基取代的4元、5元、6元或7元杂环烷基;
[0040]
每个r
b3
独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-6
环烷基、苯基、5-6元杂芳基和4-7元杂环烷基;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-6
环烷基、苯基、5-6元杂芳基和4-7元杂环烷基各自任选地被独立地选自r
12
的1、2、3或4个取代基取代;
[0041]
每个r
a4
、r
c4
和r
d4
独立地选自h、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-6
环烷基、苯基、5-6元杂芳基和4-7元杂环烷基;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-6
环烷基、苯基、5-6元杂芳基和4-7元杂环烷基各自任选地被独立地选自r
22
的1、2、3或4个取代基取代;
[0042]
或连接至同一个n原子的任何r
c4
和r
d4
与其连接的n原子一起形成任选地被独立地选自r
22
的1、2或3个取代基取代的4元、5元、6元或7元杂环烷基;
[0043]
每个r
b4
独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-6
环烷基、苯基、5-6元杂芳基和4-7元杂环烷基;其中所述c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
3-6
环烷基、苯基、5-6元杂芳基和4-7元杂环烷基各自任选地被独立地选自r
22
的1、2、3或4个取代基取代;
[0044]
每个r
a5
、r
c5
和r
d5
独立地选自h、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基和c
1-6
卤代烷基;其中所述c
1-6
烷基、c
2-6
烯基和c
2-6
炔基各自任选地被独立地选自rg的1、2、3或4个取代基取代;
[0045]
每个r
b5
独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基和c
1-6
卤代烷基;其中所述c
1-6
烷基、c
2-6
烯基和c
2-6
炔基各自任选地被独立地选自rg的1、2、3或4个取代基取代;
[0046]
每个r
a6
、r
c6
和r
d6
独立地选自h、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基和c
1-6
卤代烷基;其中所述c
1-6
烷基、c
2-6
烯基和c
2-6
炔基各自任选地被独立地选自rg的1、2、3或4个取代基取代;
[0047]
每个r
b6
独立地选自c
1-6
烷基、c
2-6
烯基、c
2-6
炔基和c
1-6
卤代烷基;其中所述c
1-6
烷基、c
2-6
烯基和c
2-6
炔基各自任选地被独立地选自rg的1、2、3或4个取代基取代;并且
[0048]
每个rg独立地选自oh、no2、cn、卤基、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
卤代烷基、c
3-6
环烷基、c
3-6
环烷基-c
1-2
亚烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、c
1-3
烷氧基-c
1-3
烷基、c
1-3
烷氧基-c
1-3
烷氧基、ho-c
1-3
烷氧基、ho-c
1-3
烷基、氰基-c
1-3
烷基、h2n-c
1-3
烷基、氨基、c
1-6
烷基氨基、二(c
1-6
烷基)氨基、硫基、c
1-6
烷基硫基、c
1-6
烷基亚磺酰基、c
1-6
烷基磺酰基、氨甲酰基、c
1-6
烷基氨甲酰基、二(c
1-6
烷基)氨甲酰基、羧基、c
1-6
烷基羰基、c
1-6
烷氧基羰基、c
1-6
烷基羰基氨基、c
1-6
烷基磺酰基氨基、氨基磺酰基、c
1-6
烷基氨基磺酰基、二(c
1-6
烷基)氨基磺酰基、氨基磺酰基氨基、c
1-6
烷基氨基磺酰基氨基、二(c
1-6
烷基)氨基磺酰基氨基、氨基羰基氨基、c
1-6
烷基氨基羰基氨基和二(c
1-6
烷基)氨基羰基氨基。
[0049]
在一个方面,本公开提供式(i)化合物:
[0050][0051]
或其药学上可接受的盐,其中:
[0052]
cy1选自苯基、吡啶基和吡唑基;其中所述苯基吡啶基和吡唑基各自任选地被独立地选自r
10
的1、2、3或4个取代基取代;
[0053]
r1选自卤基、c
1-6
烷基、c
1-6
卤代烷基、c
3-5
环烷基、4-5元杂环烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、c
1-3
烷氧基-c
1-3
烷基、ho-c
1-3
烷基、c
1-6
烷基氨基和二(c
1-6
烷基)氨基;其中所述c
1-6
烷基、c
1-6
卤代烷基、c
3-5
环烷基、4-5元杂环烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、c
1-3
烷氧基-c
1-3
烷基、ho-c
1-3
烷基、c
1-6
烷基氨基和二(c
1-6
烷基)氨基的任何h原子均可被d原子替换;
[0054]
每个r2和r3独立地选自c
1-6
烷基、c
2-6
烯基、c
1-6
卤代烷基、c
3-6
环烷基、4-6元杂环烷基、卤基、cn、or
a2
、c(o)r
b2
、c(o)nr
c2rd2
、c(o)or
a2
、nr
c2rd2
和s(o)2r
b2
;其中所述c
1-6
烷基、c
2-6
烯基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
21
的1、2、3或4个取代基取代;
[0055]
或苯环上的两个相邻r2取代基与其连接的原子一起形成稠合5元或6元环烷基环或稠合5元或6元杂环烷基环;其中每个稠合5元或6元杂环烷基环具有至少一个成环碳原子和独立地选自o和n的1或2个成环杂原子;其中每个稠合5元或6元杂环烷基环的成环碳原子任选地被氧代取代以形成羰基;并且其中所述稠合5元或6元环烷基环和所述稠合5元或6元杂环烷基环各自任选地被独立地选自r
21
的1、2、3或4个取代基取代;
[0056]
n选自0和1;
[0057]
每个r
10
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-10
环烷基、4-12元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-12元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基、5-10元杂芳基-c
1-3
亚烷基、卤基、d、cn、or
a1
、c(o)r
b1
、c(o)nr
c1rd1
、c(o)or
a1
、nr
c1rd1
、nr
c1
c(o)r
b1
和s(o)2r
b1
;其中所述c
1-6
烷基、c
3-10
环烷基、4-12元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-12元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基和5-10元杂芳基-c
1-3
亚烷基各自任选地被独立地选自r
11
的1、2、3或4个取代基取代;
[0058]
每个r
11
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基、5-10元杂芳基、卤基、d、cn、or
a3
、sr
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3rd3
、nr
c3
c(o)r
b3
、nr
c3
c(o)or
a3
、nr
c3
s(o)2r
b3
、nr
c3
s(o)2nr
c3rd3
、s(o)2r
b3
和s(o)2nr
c3rd3
;其中所述c
1-6
烷基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基和5-10元杂芳基各自任选地被独立地选自r
12
的1、2、3或4个取代基取代;
[0059]
每个r
12
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基、4-7元杂环烷基、卤基、d、cn、or
a5
、sr
a5
、c(o)r
b5
、c(o)nr
c5rd5
、c(o)or
a5
、nr
c5rd5
、nr
c5
c(o)r
b5
、s(o)2r
b5
和s(o)2nr
c5rd5
;其中所述c
1-6
烷基、c
3-6
环烷基和4-7元杂环烷基各自任选地被独立地选自rg的1、2、3或4个取代基取代;
[0060]
每个r
21
独立地选自c
1-6
烷基、c
1-6
卤代烷基、卤基、d、cn、or
a4
、c(o)r
b4
、c(o)nr
c4rd4
、
c(o)or
a4
、nr
c4rd4
和s(o)2r
b4
;其中所述c
1-6
烷基任选地被独立地选自r
22
的1、2或3个取代基取代;
[0061]
每个r
22
独立地选自c
1-6
烷基、c
1-6
卤代烷基、卤基、d、cn、or
a6
和nr
c6rd6
;其中所述c
1-6
烷基任选地被独立地选自rg的1或2个取代基取代;
[0062]
每个r
a1
、r
c1
和r
d1
独立地选自h、c
1-6
烷基、c
1-6
卤代烷基、c
3-10
环烷基和4-10元杂环烷基;其中所述c
1-6
烷基、c
3-10
环烷基和4-10元杂环烷基各自任选地被独立地选自r
11
的1、2、3或4个取代基取代;
[0063]
或连接至同一个n原子的任何r
c1
和r
d1
与其连接的n原子一起形成任选地被独立地选自r
11
的1、2、3或4个取代基取代的4元、5元或6元杂环烷基;
[0064]
每个r
b1
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-10
环烷基和4-10元杂环烷基,其中所述c
1-6
烷基、c
3-10
环烷基和4-10元杂环烷基各自任选地被独立地选自r
11
的1、2、3或4个取代基取代;
[0065]
每个r
a2
、r
c2
和r
d2
独立地选自h、c
1-6
烷基、c
1-6
卤代烷基、c
3-10
环烷基和4-10元杂环烷基;其中所述c
1-6
烷基、c
3-10
环烷基和4-10元杂环烷基各自任选地被独立地选自r
21
的1、2、3或4个取代基取代;
[0066]
或连接至同一个n原子的任何r
c2
和r
d2
与其连接的n原子一起形成任选地被独立地选自r
21
的1、2或3个取代基取代的4元、5元或6元杂环烷基;
[0067]
每个r
b2
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-10
环烷基和4-10元杂环烷基;其中所述c
1-6
烷基、c
3-10
环烷基和4-10元杂环烷基各自任选地被独立地选自r
21
的1、2、3或4个取代基取代;
[0068]
每个r
a3
、r
c3
和r
d3
独立地选自h、c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基和4-7元杂环烷基;其中所述c
1-6
烷基、c
3-6
环烷基和4-7元杂环烷基各自任选地被独立地选自r
12
的1、2、3或4个取代基取代;
[0069]
或连接至同一个n原子的任何r
c3
和r
d3
与其连接的n原子一起形成任选地被独立地选自r
12
的1、2或3个取代基取代的4元、5元、6元或7元杂环烷基;
[0070]
每个r
b3
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基和4-7元杂环烷基;其中所述c
1-6
烷基、c
3-6
环烷基和4-7元杂环烷基各自任选地被独立地选自r
12
的1、2、3或4个取代基取代;
[0071]
每个r
a4
、r
c4
和r
d4
独立地选自h、c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自r
22
的1、2、3或4个取代基取代;
[0072]
每个r
b4
独立地选自c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自r
22
的1、2、3或4个取代基取代;
[0073]
每个r
a5
、r
c5
和r
d5
独立地选自h、c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自rg的1、2、3或4个取代基取代;
[0074]
每个r
b5
独立地选自c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自rg的1、2、3或4个取代基取代;
[0075]
每个r
a6
、r
c6
和r
d6
独立地选自h、c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自rg的1、2、3或4个取代基取代;
[0076]
每个r
b6
独立地选自c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选
自rg的1、2、3或4个取代基取代;并且
[0077]
每个rg独立地选自oh、cn、卤基、c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、c
1-3
烷氧基-c
1-3
烷基、ho-c
1-3
烷基、氰基-c
1-3
烷基、h2n-c
1-3
烷基、氨基、c
1-6
烷基氨基、二(c
1-6
烷基)氨基、c
1-6
烷基硫基、c
1-6
烷基磺酰基、羧基、c
1-6
烷基羰基、c
1-6
烷氧基羰基和c
1-6
烷基羰基氨基。
[0078]
在一个方面,本公开提供式(i)化合物:
[0079][0080]
或其药学上可接受的盐,其中:
[0081]
cy1选自苯基、吡啶-3-基和吡唑-4-基;其中cy1的苯基、吡啶-3-基和吡唑-4-基各自任选地被选自r
10
的1个取代基取代;
[0082]
r1选自cl、c
1-3
烷基、c
1-3
卤代烷基、环丙基、氮杂环丁基、羟基甲基、c
1-3
烷氧基、c
1-3
卤代烷氧基和c
1-3
烷基氨基;其中所述c
1-3
烷基、c
1-3
卤代烷基、环丙基、氮杂环丁基、羟基甲基、c
1-3
烷氧基、c
1-3
卤代烷氧基和c
1-3
烷基氨基各自任选地被1、2、3、4、5、6或7个氘取代;
[0083]
每个r2独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、f、cl、cn和or
a2
;其中所述c
1-3
烷基和c
3-6
环烷基各自任选地被独立地选自r
21
的1、2或3个取代基取代;
[0084]
或苯环上的r2取代基与其连接的原子一起形成稠合5元或6元环烷基环或稠合5元或6元杂环烷基环;其中每个稠合5元或6元杂环烷基环具有至少一个成环碳原子和1或2个成环o原子;并且其中所述稠合5元或6元环烷基环和所述稠合5元或6元杂环烷基环各自任选地被独立地选自r
21
的1或2个取代基取代;
[0085]
n是0;
[0086]
每个r
10
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-10元杂环烷基-c
1-2
亚烷基、5-6元杂芳基-c
1-2
亚烷基、f、cl、d、cn、or
a1
、c(o)nr
c1rd1
和nr
c1rd1
;其中所述c
1-3
烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-10元杂环烷基-c
1-2
亚烷基和5-6元杂芳基-c
1-2
亚烷基各自任选地被独立地选自r
11
的1或2个取代基取代;
[0087]
每个r
11
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、f、cl、d、cn、or
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3rd3
、nr
c3
c(o)r
b3
、nr
c3
s(o)2r
b3
、s(o)2r
b3
和s(o)2nr
c3rd3
;其中所述c
1-3
烷基、c
3-6
环烷基、4-10元杂环烷基和5-6元杂芳基各自任选地被独立地选自r
12
的1或2个取代基取代;
[0088]
每个r
12
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、4-7元杂环烷基、f、cl、d、cn、or
a5
、c(o)r
b5
、c(o)nr
c5rd5
和nr
c5rd5
;其中所述c
1-3
烷基、c
3-6
环烷基和4-7元杂环烷基各自任选地被独立地选自rg的1个取代基取代;
[0089]r21
独立地选自c
1-3
烷基、f、cl、d、cn和or
a4
;其中所述c
1-3
烷基任选地被独立地选自r
22
的1或2个取代基取代;
[0090]
每个r
22
独立地选自f、cl、d、cn和or
a6
;
[0091]
每个r
a1
、r
c1
和r
d1
独立地选自h、c
1-3
烷基、c
1-3
卤代烷基和4-6元杂环烷基;其中所述c
1-3
烷基和4-6元杂环烷基各自任选地被独立地选自r
11
的1个取代基取代;
[0092]
每个r
a2
独立地选自h、c
1-3
烷基和c
1-3
卤代烷基;
[0093]
每个r
a3
、r
c3
和r
d3
独立地选自h、c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基和4-6元杂环烷基;其中所述c
1-3
烷基c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
12
的1或2个取代基取代;
[0094]
或连接至同一个n原子的任何r
c3
和r
d3
与其连接的n原子一起形成任选地被独立地选自r
12
的1或2个取代基取代的4元、5元或6元杂环烷基;
[0095]
每个r
b3
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基和4-6元杂环烷基;其中所述c
1-3
烷基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
12
的1或2个取代基取代;
[0096]
每个r
a4
独立地选自h、c
1-3
烷基和c
1-3
卤代烷基;
[0097]
每个r
a5
、r
c5
和r
d5
独立地选自h、c
1-3
烷基和c
1-3
卤代烷基;其中所述c
1-3
烷基任选地被独立地选自rg的1个取代基取代;
[0098]
每个r
b5
独立地选自c
1-3
烷基和c
1-3
卤代烷基;其中所述c
1-3
烷基任选地被独立地选自rg的1个取代基取代;
[0099]
每个r
a6
独立地选自h和c
1-3
烷基;并且
[0100]
每个rg独立地选自oh、cn、f、cl、c
1-3
烷基和c
1-3
卤代烷基。
[0101]
在一些实施方案中,cy1选自苯基、吡啶基和吡唑基;其中所述苯基、吡啶基和吡唑基各自任选地被独立地选自r
10
的1、2、3或4个取代基取代。在一些实施方案中,cy1选自苯基、吡啶基和吡唑基;其中所述苯基、吡啶基和吡唑基各自任选地被独立地选自r
10
的1或2个取代基取代。在一些实施方案中,cy1选自苯基、吡啶基和吡唑基;其中所述苯基、吡啶基和吡唑基各自任选地被选自r
10
的1个取代基取代。在一些实施方案中,cy1选自苯基、吡啶基和吡唑基;其中所述苯基、吡啶基和吡唑基各自被选自r
10
的1个取代基取代。
[0102]
在一些实施方案中,cy1选自苯基、吡啶-3-基和吡唑-4-基;其中所述苯基、吡啶-3-基和吡唑-4-基各自任选地被选自r
10
的1个取代基取代。在一些实施方案中,cy1选自苯基、吡啶-3-基和吡唑-4-基;其中所述苯基、吡啶-3-基和吡唑-4-基各自被选自r
10
的1个取代基取代。
[0103]
在一些实施方案中,cy1是任选地被选自r
10
的1或2个取代基取代的5-6元杂芳基。在一些实施方案中,cy1选自吡啶-3-基和吡唑-4-基;其中所述吡啶-3-基和吡唑-4-基各自任选地被选自r
10
的1个取代基取代。
[0104]
在一些实施方案中,cy1是任选地被选自r
10
的1或2个取代基取代的吡唑-4-基。在一些实施方案中,cy1选自吡唑-4-基和吡啶-3-基;其中所述吡唑-4-基和吡啶-3-基各自任选地被选自r
10
的1或2个取代基取代。在一些实施方案中,cy1是任选地被选自r
10
的1或2个取代基取代的吡啶-3-基。在一些实施方案中,cy1是任选地被选自r
10
的1或2个取代基取代的苯基。
[0105]
在一些实施方案中,r1选自卤基、c
1-6
烷基、c
1-6
卤代烷基、c
3-5
环烷基、4-5元杂环烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、c
1-3
烷氧基-c
1-3
烷基、ho-c
1-3
烷基、c
1-6
烷基氨基和二(c
1-6
烷基)氨基;其中所述c
1-6
烷基、c
1-6
卤代烷基、c
3-5
环烷基、4-5元杂环烷基、c
1-6
烷氧基、c
1-6
卤代
烷氧基、c
1-3
烷氧基-c
1-3
烷基、ho-c
1-3
烷基、c
1-6
烷基氨基和二(c
1-6
烷基)氨基的一个或多个h原子任选地被一个或多个d原子替换。
[0106]
在一些实施方案中,r1选自cl、c
1-3
烷基、c
1-3
卤代烷基、环丙基、氮杂环丁基、羟基甲基、c
1-3
烷氧基、c
1-3
卤代烷氧基和c
1-3
烷基氨基;其中所述c
1-3
烷基、c
1-3
卤代烷基、环丙基、氮杂环丁基、羟基甲基、c
1-3
烷氧基、c
1-3
卤代烷氧基和c
1-3
烷基氨基的一个或多个h原子任选地被一个或多个d原子替换。
[0107]
在一些实施方案中,r1选自cl、c
1-2
烷基、c
1-2
卤代烷基、环丙基、羟基甲基、c
1-2
烷氧基、c
1-2
卤代烷氧基和c
1-2
烷基氨基;其中所述c
1-2
烷基、c
1-2
卤代烷基、环丙基、羟基甲基、c
1-2
烷氧基、c
1-2
卤代烷氧基和c
1-2
烷基氨基的一个或多个h原子任选地被d原子替换。
[0108]
在一些实施方案中,r1选自cl、c
1-2
烷基、c
1-2
卤代烷基、羟基甲基、c
1-2
烷氧基、c
1-2
卤代烷氧基和c
1-2
烷基氨基;其中所述c
1-2
烷基、c
1-2
卤代烷基、羟基甲基、c
1-2
烷氧基、c
1-2
卤代烷氧基和c
1-2
烷基氨基的一个或多个h原子任选地被一个或多个d原子替换。
[0109]
在一些实施方案中,r1选自cl、ch3、och3、ocd3、och2ch3、ochf2、nhch3、chf2和ch2oh。
[0110]
在一些实施方案中,r1是c
1-2
烷氧基。在一些实施方案中,r1是och3。在一些实施方案中,r1是ocd3。
[0111]
在一些实施方案中,每个r2和r3独立地选自c
1-6
烷基、c
2-6
烯基、c
1-6
卤代烷基、c
3-6
环烷基、4-6元杂环烷基、卤基、cn、or
a2
、c(o)r
b2
、c(o)nr
c2rd2
、c(o)or
a2
、nr
c2rd2
和s(o)2r
b2
;其中所述c
1-6
烷基、c
2-6
烯基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
21
的1、2、3或4个取代基取代。
[0112]
在一些实施方案中,每个r2独立地选自c
1-6
烷基、c
1-3
卤代烷基、c
3-6
环烷基、卤基、cn和or
a2
;其中所述c
1-6
烷基和c
3-6
环烷基各自任选地被独立地选自r
21
的1、2、3或4个取代基取代。
[0113]
在一些实施方案中,每个r2独立地选自c
1-6
烷基、c
3-6
环烷基、卤基和or
a2
;其中所述c
1-6
烷基和c
3-6
环烷基各自任选地被独立地选自r
21
的1、2、3或4个取代基取代。
[0114]
在一些实施方案中,苯环上的两个相邻r2取代基与其连接的原子一起形成稠合5元或6元环烷基环或稠合5元或6元杂环烷基环;其中每个稠合5元或6元杂环烷基环具有至少一个成环碳原子和独立地选自o和n的1或2个成环杂原子;其中每个稠合5元或6元杂环烷基环的成环碳原子任选地被氧代取代以形成羰基;并且其中所述稠合5元或6元环烷基环和所述稠合5元或6元杂环烷基环各自任选地被独立地选自r
21
的1、2、3或4个取代基取代。
[0115]
在一些实施方案中,苯环上的两个相邻r2取代基与其连接的原子一起形成稠合5元环烷基环或稠合5元或6元杂环烷基环;其中每个稠合5元或6元杂环烷基环具有至少一个成环碳原子和1或2个成环o原子;并且其中所述稠合5元环烷基环和所述稠合5元或6元杂环烷基环各自任选地被独立地选自r
21
的1或2个取代基取代。
[0116]
在一些实施方案中,每个r2独立地选自c
3-6
环烷基、c
1-2
烷基、c
1-2
卤代烷基、f、cl、cn和or
a2
;其中所述c
1-2
烷基任选地被选自r
21
的1个取代基取代。
[0117]
在一些实施方案中,每个r2独立地选自c
1-3
烷基、c
1-3
卤代烷基、f、cl、cn和or
a2
;其中所述c
1-6
烷基任选地被选自r
21
的1个取代基取代。
[0118]
在一些实施方案中,每个r2独立地选自c
1-2
烷基、c
1-2
卤代烷基、f、cl、cn和or
a2
;其中所述c
1-2
烷基任选地被选自r
21
的1个取代基取代。
[0119]
在一些实施方案中,每个r2独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、f、cl、cn和or
a2
;其中所述c
1-3
烷基和c
3-6
环烷基各自任选地被独立地选自r
21
的1、2或3个取代基取代。
[0120]
在一些实施方案中,每个r2独立地选自c
1-2
烷基和f;其中所述c
1-2
烷基任选地被选自r
21
的1个取代基取代。
[0121]
在一些实施方案中,每个r2独立地选自f、甲基、ch2cn和cd3。
[0122]
在一些实施方案中,每个r2独立地选自f、甲基、ch2cn、环丙基和cd3。
[0123]
在一些实施方案中,每个r2独立地选自f、甲基、ch2cn、cd3、oh、och3和环丙基。
[0124]
在一些实施方案中,每个r2是c
1-2
烷基。在一些实施方案中,每个r2是甲基。
[0125]
在一些实施方案中,苯环上的r2取代基与其连接的原子一起形成稠合5元环烷基环或稠合5-杂环烷基环;其中所述稠合5元杂环烷基环具有至少一个成环碳原子和1或2个成环o原子;并且其中所述稠合5元环烷基环和所述稠合5元杂环烷基环各自任选地被选自r
21
的1或2个取代基取代。
[0126]
在一些实施方案中,苯环上的r2取代基与其连接的原子一起形成稠合5元或6元环烷基环或稠合5元或6元杂环烷基环;其中每个稠合5元或6元杂环烷基环具有至少一个成环碳原子和1或2个成环o原子;并且其中所述稠合5元或6元环烷基环或该稠合5元或6元杂环烷基环各自任选地被选自r
21
的1个取代基取代
[0127]
在一些实施方案中,r2取代基与其连接的原子一起形成稠合环戊基或稠合四氢呋喃基,其中每一个任选地被选自r
21
的1或2个取代基取代。
[0128]
在一些实施方案中,r2取代基与其连接的原子一起形成稠合环戊基、稠合四氢呋喃基、稠合1,4-二噁烷基或稠合四氢吡喃基,其中每一个任选地被选自r
21
的1或2个取代基取代。
[0129]
在一些实施方案中,r2取代基与其连接的原子一起形成任选地被独立地选自oh、cn、ch2oh和f的1或2个取代基取代的稠合环戊基。
[0130]
在一些实施方案中,r2取代基与其连接的原子一起形成任选地被独立地选自d、oh、cn、ch2oh和f的1或2个取代基取代的稠合环戊基。
[0131]
在一些实施方案中,r2取代基与其连接的原子一起形成稠合环戊基或稠合环己基;其中所述稠合环戊基和所述稠合环己基具有至少一个成环碳原子并且各自任选地具有1或2个成环o原子;并且其中所述稠合环戊基和所述稠合环己基各自任选地被独立地选自d、oh、cn、ch2oh和f的1或2个取代基取代。
[0132]
在一些实施方案中,r2取代基与其连接的原子一起形成稠合环戊基。
[0133]
在一些实施方案中,n选自0和1。
[0134]
在一些实施方案中,n是0。在一些实施方案中,n是1。
[0135]
在一些实施方案中,每个r
10
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-10
环烷基、4-12元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-12元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基、5-10元杂芳基-c
1-3
亚烷基、卤基、d、cn、or
a1
、c(o)r
b1
、c(o)nr
c1rd1
、c(o)or
a1
、nr
c1rd1
、nr
c1
c(o)r
b1
和s(o)2r
b1
;其中所述c
1-6
烷基、c
3-10
环烷基、4-12元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-12元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基和5-10元杂芳基-c
1-3
亚烷基各自任选地被独立地选自r
11
的1、2、3或4个取代基取
代。
[0136]
在一些实施方案中,每个r
10
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基、4-6元杂环烷基、苯基、5-6元杂芳基、c
3-6
环烷基-c
1-3
亚烷基、4-6元杂环烷基-c
1-3
亚烷基、苯基-c
1-3
亚烷基、5-6元杂芳基-c
1-3
亚烷基、卤基、d、cn、or
a1
、c(o)r
b1
、c(o)nr
c1rd1
、c(o)or
a1
、nr
c1rd1
、nr
c1
c(o)r
b1
和s(o)2r
b1
;其中所述c
1-6
烷基、c
3-6
环烷基、4-6元杂环烷基、苯基、5-6元杂芳基、c
3-6
环烷基-c
1-3
亚烷基、4-6元杂环烷基-c
1-3
亚烷基、苯基-c
1-3
亚烷基和5-6元杂芳基-c
1-3
亚烷基各自任选地被独立地选自r
11
的1、2、3或4个取代基取代。
[0137]
在一些实施方案中,每个r
10
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基、4-6元杂环烷基、苯基、5-6元杂芳基、c
3-6
环烷基-c
1-3
亚烷基、4-6元杂环烷基-c
1-3
亚烷基、苯基-c
1-3
亚烷基、5-6元杂芳基-c
1-3
亚烷基、卤基、d、cn、or
a1
、c(o)r
b1
、c(o)nr
c1rd1
、c(o)or
a1
、nr
c1rd1
、nr
c1
c(o)r
b1
和s(o)2r
b1
;其中所述c
1-6
烷基、c
3-6
环烷基、4-6元杂环烷基、苯基、5-6元杂芳基、c
3-6
环烷基-c
1-3
亚烷基、4-6元杂环烷基-c
1-3
亚烷基、苯基-c
1-3
亚烷基和5-6元杂芳基-c
1-3
亚烷基各自任选地被独立地选自r
11
的1或2个取代基取代。
[0138]
在一些实施方案中,每个r
10
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基、5-6元杂芳基-c
1-2
亚烷基、卤基、d、cn、or
a1
、c(o)nr
c1rd1
和nr
c1rd1
;其中所述c
1-3
烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基和5-6元杂芳基-c
1-2
亚烷基各自任选地被独立地选自r
11
的1或2个取代基取代。
[0139]
在一些实施方案中,每个r
10
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基、5-6元杂芳基-c
1-2
亚烷基、卤基、d、cn、c(o)nr
c1rd1
和nr
c1rd1
;其中所述c
1-3
烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基和5-6元杂芳基-c
1-2
亚烷基各自任选地被独立地选自r
11
的1或2个取代基取代。
[0140]
在一些实施方案中,每个r
10
独立地选自c
1-3
烷基、c
1-3
卤代烷基、or
a1
、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基、5-6元杂芳基-c
1-2
亚烷基、卤基、d、cn、c(o)nr
c1rd1
和nr
c1rd1
;其中所述c
1-3
烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基和5-6元杂芳基-c
1-2
亚烷基各自任选地被独立地选自r
11
的1或2个取代基取代。
[0141]
在一些实施方案中,每个r
10
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基、5-6元杂芳基-c
1-2
亚烷基、卤基、d、cn、c(o)nr
c1rd1
和nr
c1rd1
;其中所述c
1-3
烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基和5-6元杂芳基-c
1-2
亚烷基各自任选地被选自r
11
的1个取代基取代,并且任选地被选自c
1-2
烷基的第二取代基取代。
[0142]
在一些实施方案中,每个r
10
独立地选自c
1-3
烷基、c
1-3
卤代烷基、or
a1
、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基、5-6元杂芳基-c
1-2
亚烷基、卤基、d、cn、c(o)nr
c1rd1
和nr
c1rd1
;其中所述c
1-3
烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基和5-6元杂芳基-c
1-2
亚烷基各自任选地被选自r
11
的1个取代基取代,并且任选地被选自c
1-2
烷基的第二取代基取代。
[0143]
在一些实施方案中,每个r
10
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、4-6元
杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基、5-6元杂芳基-c
1-2
亚烷基、卤基、d、cn、c(o)nr
c1rd1
和nr
c1rd1
;其中所述c
1-3
烷基、c
3-6
环烷基、4-6元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基和5-6元杂芳基-c
1-2
亚烷基各自任选地被独立地选自r
11
的1或2个取代基取代。
[0144]
在一些实施方案中,每个r
10
独立地选自c
1-3
烷基、c
1-3
卤代烷基、卤基、d、cn、c(o)nr
c1rd1
和nr
c1rd1
;其中所述c
1-3
烷基任选地被独立地选自r
11
的1或2个取代基取代。
[0145]
在一些实施方案中,每个r
10
独立地选自c
3-6
环烷基、4-6元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基和5-6元杂芳基-c
1-2
亚烷基;其中所述c
3-6
环烷基、4-6元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基和5-6元杂芳基-c
1-2
亚烷基各自任选地被独立地选自r
11
的1或2个取代基取代。
[0146]
在一些实施方案中,每个r
10
独立地选自c
1-2
烷基、c
1-2
卤代烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三唑基)甲基、1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮、f、cl、d、cn和nr
c1rd1
;其中所述c
1-2
烷基、c
3-6
环烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基和(吡啶基)甲基各自任选地被独立地选自r
11
的1或2个取代基取代。
[0147]
在一些实施方案中,每个r
10
独立地选自c
1-2
烷基、c
3-6
环烷基、卤基、d、cn、or
a1
、c(o)nr
c1rd1
、nr
c1rd1
、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三唑基)甲基、硫代吗啉基、1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮和六氢吡咯并[1,2-a]吡嗪-2(1h)-基;其中所述c
1-2
烷基、c
3-6
环烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三唑基)甲基、硫代吗啉基、1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮和六氢吡咯并[1,2-a]吡嗪-2(1h)-基各自任选地被独立地选自r
11
的1或2个取代基取代。
[0148]
在一些实施方案中,每个r
10
独立地选自c
1-2
烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三唑基)甲基、硫代吗啉基、1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮和六氢吡咯并[1,2-a]吡嗪-2(1h)-基,其中所述c
1-2
烷基、c
3-6
环烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三唑基)甲基、硫代吗啉基、1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮和六氢吡咯并[1,2-a]吡嗪-2(1h)-基各自任选地被独立地选自r
11
的1或2个取代基取代
[0149]
在一些实施方案中,当r
10
是4-10元杂环烷基时,所述杂环烷基环的杂原子在可接受的化合价内被r
11
取代。在一些实施方案中,当r
10
是4-6元杂环烷基时,所述杂环烷基环的杂原子在可接受的化合价内被r
11
取代。在一些实施方案中,所述杂环烷基环的s原子被nr取代。在一些实施方案中,所述杂环烷基环的s原子被nr和o取代。
[0150]
在一些实施方案中,每个r
10
独立地选自c
1-2
烷基、c
1-2
卤代烷基、f、cl、d、cn和nr
c1rd1
;其中所述c
1-2
烷基任选地被独立地选自r
11
的1或2个取代基取代。
[0151]
在一些实施方案中,每个r
10
独立地选自c
1-2
烷基、c
1-2
卤代烷基、f、cl、d、cn、or
a1
和nr
c1rd1
;其中所述c
1-2
烷基任选地被独立地选自r
11
的1或2个取代基取代。
[0152]
在一些实施方案中,每个r
10
独立地选自c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三嗪基)甲基和1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮;其中所述c
3-6
环烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基和(吡啶基)甲基各自任选地被独立地选自r
11
的1或2个取代基取代。
[0153]
在一些实施方案中,每个r
10
独立地选自c
1-2
烷基、c
1-2
卤代烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三嗪基)甲基、1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮、f、cl、d、cn、nr
c1rd1
;其中所述c
1-2
烷基、c
3-6
环烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基和(吡啶基)甲基各自任选地被选自r
11
的1个取代基取代,并且任选地被选自c
1-2
烷基的第二取代基取代。
[0154]
在一些实施方案中,每个r
10
独立地选自c
1-2
烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三唑基)甲基和1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮;其中所述c
1-2
烷基、c
3-6
环烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基和(三唑基)甲基各自任选地被独立地选自r
11
的1或2个取代基取代。
[0155]
在一些实施方案中,每个r
10
独立地选自c
1-2
烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三唑基)甲基和1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮;其中所述c
1-2
烷基、c
3-6
环烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基和(三唑基)甲基各自任选地被选自r
11
的1个取代基取代,并且任选地被选自c
1-2
烷基的第二取代基取代。
[0156]
在一些实施方案中,每个r
10
独立地选自甲基、(1-甲基-1h-1,2,4-三唑-5-基)甲基、吡咯烷-3-基、吡咯烷-1-基、1-乙基吡咯烷-3-基、1-甲基氮杂环丁-3-基、1-乙基氮杂环丁-3-基、4-乙酰基哌嗪-1-基、3-氰基环丁基、1-(二甲基氨甲酰基)哌啶-4-基、1-(甲氧基羰基)哌啶-4-基、1-(甲氧基羰基)氮杂环丁-3-基、1-乙酰基氮杂环丁-3-基、1-(甲基磺酰基)氮杂环丁-3-基、1-(二甲基氨甲酰基)氮杂环丁-3-基、1-(环丙烷羰基)氮杂环丁-3-基、吡啶-4-基甲基、2-吗啉代乙基、环丙基、2-氰基乙基、2-羟基乙基、吡啶-4-基、4-羟基环己基、4-甲基哌嗪-1-基、4-乙基哌嗪-1-基、吗啉代、4-甲基-3-氧代哌嗪-1-基、4-羟基哌啶-1-基、(r)-3,4-二甲基哌嗪-1-基、(1s,4s)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基、4-(二甲基氨甲酰基)哌啶-1-基、4-羧基-4-甲基哌啶-1-基、(1s,4s)-4-乙酰胺基环己基、2,4-二甲基哌嗪-1-基、4-(乙基氨甲酰基)哌嗪-1-基、4-氨甲酰基哌嗪-1-基、4-异丙基哌嗪-1-基、4-乙基哌嗪-1-基、2-氧代-1-氧杂-3,8-二氮杂螺[4.5]癸-8-基、吡啶-2-基甲基、1-乙酰基哌啶-4-基)和1-(甲氧基羰基)哌啶-4-基。
[0157]
在一些实施方案中,每个r
10
独立地选自甲基、(1-甲基-1h-1,2,4-三唑-5-基)甲基、吡咯烷-3-基、吡咯烷-1-基、1-乙基吡咯烷-3-基、1-甲基氮杂环丁-3-基、1-乙基氮杂环丁-3-基、4-乙酰基哌嗪-1-基、3-氰基环丁基、1-(二甲基氨甲酰基)哌啶-4-基、1-(甲氧基羰基)哌啶-4-基、1-(甲氧基羰基)氮杂环丁-3-基、1-乙酰基氮杂环丁-3-基、1-(甲基磺酰
基)氮杂环丁-3-基、1-(二甲基氨甲酰基)氮杂环丁-3-基、1-(环丙烷羰基)氮杂环丁-3-基、吡啶-4-基甲基、2-吗啉代乙基、环丙基、2-氰基乙基、2-羟基乙基、吡啶-4-基、4-羟基环己基、4-甲基哌嗪-1-基、4-乙基哌嗪-1-基、吗啉代、4-甲基-3-氧代哌嗪-1-基、4-羟基哌啶-1-基、(r)-3,4-二甲基哌嗪-1-基、(1s,4s)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基、4-(二甲基氨甲酰基)哌啶-1-基、4-羧基-4-甲基哌啶-1-基、(1s,4s)-4-乙酰胺基环己基、2,4-二甲基哌嗪-1-基、4-(乙基氨甲酰基)哌嗪-1-基、4-氨甲酰基哌嗪-1-基、4-异丙基哌嗪-1-基、4-乙基哌嗪-1-基、2-氧代-1-氧杂-3,8-二氮杂螺[4.5]癸-8-基、吡啶-2-基甲基、1-乙酰基哌啶-4-基)、1-(甲氧基羰基)哌啶-4-基、(四氢呋喃-3-基)氧基、1-甲基-5-氧代吡咯烷-3-基、1-(2-羟基丙酰基)哌啶-4-基、1-(2-羟基乙酰基)哌啶-4-基、4-羧基环己基、3-氨基-4-氟吡咯烷-1-基、(7r,8as)-7-羟基六氢吡咯并[1,2-a]吡嗪-2(1h)-基、(7r,8as)-7-羟基六氢吡咯并[1,2-a]吡嗪-2(1h)-基、4-亚氨基-4-氧代-4λ
6-哌嗪-1-基、(2-羟基-n-甲基乙酰胺基)吡咯烷-1-基、4-(2-羟基乙基)哌嗪-1-基、2-甲氧基乙氧基、(四氢-2h-吡喃-4-基)氧基、环丙基和3-(2-羟基-n-甲基乙酰胺基)氮杂环丁-1-基。
[0158]
在一些实施方案中,每个r
10
独立地选自1-(2-羟基乙酰基)吡咯烷-3-基、1-乙酰基哌啶-3-基、1-(3
’‑
吡咯烷-2
’‑
酮)吡咯烷-3-基、1-(1
’‑
甲基-(3
’‑
吡咯烷-2
’‑
酮))吡咯烷-3-基、1-(2-丙酰胺)吡咯烷-3-基、1-(甲基-l-脯氨酰基)哌啶-4-基、1-(4-甲基吗啉-3-基)吡咯烷-3-基、3-氰基环丁-1-基、1-(羟基甲基羰基)氮杂环丁-3-基、1-(2-(二甲基氨基)乙烷羰基)氮杂环丁-3-基、1-(二甲基氨基-甲基-乙酰基)氮杂环丁-3-基、1-((1-甲基氮杂环丁-2-基)羰基)氮杂环丁-3-基、1-(2-(4-甲基哌嗪-1-基)乙-1-酮)氮杂环丁-3-基、1-(2-(4-羟基哌嗪-1-基)乙-1-酮)氮杂环丁-3-基、1-((1-甲基氮杂环丁-2-基)羰基)氮杂环丁-3-基、1-(羟基-甲基-乙酰基)氮杂环丁-3-基、1-((反)-3-羟基环丁基羰基)氮杂环丁-3-基、1-((顺)-3-羟基环丁基羰基)氮杂环丁-3-基、1-((4-甲基吗啉-3-基)羰基)氮杂环丁-3-基、1-(羟基-乙酰基)吡咯烷-3-基、1-((四氢呋喃-2-基)羰基)氮杂环丁-3-基、1-((四氢呋喃-3-基)羰基)氮杂环丁-3-基、1-(羟基-甲基-乙酰基)吡咯烷-3-基、1-(3-羟基丁酰基)氮杂环丁-3-基、1-((-3-羟基-3-甲基环丁基)羰基)氮杂环丁-3-基、1-(4-甲基吗啉-3-基)羰基)吡咯烷-3-基、1-((羟基甲基)环丁基羰基)氮杂环丁-3-基、1-((1-乙基氮杂环丁-2-基)羰基)氮杂环丁-3-基、1-((1-(2-氟乙基)氮杂环丁-2-基)羰基)氮杂环丁-3-基、1-((1-异丙基氮杂环丁-2-基)羰基)氮杂环丁-3-基、1-((1-(2-氟乙基)氮杂环丁-2-基)羰基)吡咯烷-3-基、1-((反)-3-羟基环丁基羰基)吡咯烷-3-基、1-((顺)-3-羟基环丁基羰基)吡咯烷-3-基、1-((3-羟基-3-甲基环丁基)羰基)吡咯烷-3-基、1-(2-甲氧基乙-1-酮)氮杂环丁-3-基、1-(2-(二甲基氨基)-2-甲基丙-1-酮)氮杂环丁-3-基、1-((环丙烷-1-甲腈)羰基)氮杂环丁-3-基、1-((乙-1-醇)磺酰基)氮杂环丁-3-基、1-((n,n-二甲基乙-1-胺)磺酰基)氮杂环丁-3-基、1-((2-甲氧基乙基)羧酸酯)氮杂环丁-3-基、1-((3-甲氧基环丁基)羰基)氮杂环丁-3-基、3-(2-羟基-n-甲基乙酰胺)环戊基、3-(2-羟基丙酰胺)环戊基、3-(2-羟基乙酰胺)环戊基、3-(2-羟基乙基)-3-氮杂双环[3.1.0]己-1-基、(4-羟基哌啶-1-基)甲基、(2-氧杂-5-氮杂双环[2.2.1]庚-5-基)甲基、1-(吗啉-4-基)乙基、(5,6,7,8-四氢-[1,2,4]三唑并[1,5-a]吡嗪-7-基)甲基、1-(2-羟基乙基)哌啶-4-基-4-甲腈、1-(2-羟基乙酰基)哌啶-4-基-4-甲腈、2-甲氧基乙基哌嗪-1-基、1-(四氢-2h-吡喃-4-羰基)哌啶-4-基-4-d、1-(2-甲氧基乙酰基)吡咯烷-3-基、1-(四氢呋喃-2-羰基)吡咯烷-3-基、3-(2-羟基-n-甲基乙
酰胺)氮杂环丁-1-基、1-((四氢呋喃-2-基)羰基)氮杂环丁-3-基、1-((1-甲基哌啶-2-基)羰基)氮杂环丁-3-基、1-(2-(二甲基氨基)乙-1-酮)氮杂环丁-3-基、1-(3-羟基丙-1-酮)氮杂环丁-3-基、1-(2-羟基乙-1-酮)氮杂环丁-3-基、1-(2-羟基丙-1-酮)氮杂环丁-3-基、1-(2-羟基-n-甲基乙酰胺)环丁-3-基、1-(2-羟基乙-1-酮)-3-d-氮杂环丁-3-基、1-羧酸酯哌啶-4-基、1-(吗啉-4-羰基)哌啶-4-基、1-乙酰基吡咯烷-3-基、1-(吗啉-4-羰基)吡咯烷-3-基、氰基甲基、1-丙腈-氮杂环丁-3-基、1-(2-甲氧基-n-甲基乙酰胺)环丁-3-基、1-(3-羟基-n-甲基丙酰胺)环丁-3-基、1-(2-羟基-n-甲基丙酰胺)环丁-3-基、1-(2-羟基乙-1-酮)氮杂双环[3.1.0]己-3-基、1-((4-甲基吗啉-3-基)羰基)氮杂双环[3.1.0]己-3-基、1-(四氢-2h-吡喃-4-基)氮杂双环[3.1.0]己-3-基、1-(乙-1-醇)氮杂双环[3.1.0]己-3-基、1-(4-甲基吗啉-3-羰基)-3-甲腈-吡咯烷-3-基、1-(4-甲基吗啉-3-羰基)-4-甲腈-哌啶-4-基、1-(2-羟基乙酰基)-3-甲腈-吡咯烷-3-基、(1,3-二甲基哌嗪-4-基-2-酮)甲基和(2-氧杂-5-氮杂双环[2.2.1]庚-5-基)甲基。
[0159]
在一些实施方案中,每个r
10
独立地选自甲基、(1-甲基-1h-1,2,4-三唑-5-基)甲基、吡咯烷-3-基、吡咯烷-1-基、1-乙基吡咯烷-3-基、1-甲基氮杂环丁-3-基、1-乙基氮杂环丁-3-基、4-乙酰基哌嗪-1-基、3-氰基环丁基、1-(二甲基氨甲酰基)哌啶-4-基、1-(甲氧基羰基)哌啶-4-基、1-(甲氧基羰基)氮杂环丁-3-基、1-乙酰基氮杂环丁-3-基、1-(甲基磺酰基)氮杂环丁-3-基、1-(二甲基氨甲酰基)氮杂环丁-3-基、1-(环丙烷羰基)氮杂环丁-3-基、吡啶-4-基甲基、2-吗啉代乙基、环丙基、2-氰基乙基、2-羟基乙基、吡啶-4-基、4-羟基环己基、4-甲基哌嗪-1-基、4-乙基哌嗪-1-基、吗啉代、4-甲基-3-氧代哌嗪-1-基、4-羟基哌啶-1-基、(r)-3,4-二甲基哌嗪-1-基、(1s,4s)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基、4-(二甲基氨甲酰基)哌啶-1-基、4-羧基-4-甲基哌啶-1-基、(1s,4s)-4-乙酰胺基环己基、2,4-二甲基哌嗪-1-基、4-(乙基氨甲酰基)哌嗪-1-基、4-氨甲酰基哌嗪-1-基、4-异丙基哌嗪-1-基、4-乙基哌嗪-1-基、2-氧代-1-氧杂-3,8-二氮杂螺[4.5]癸-8-基、吡啶-2-基甲基、1-乙酰基哌啶-4-基)、1-(甲氧基羰基)哌啶-4-基、(四氢呋喃-3-基)氧基、1-甲基-5-氧代吡咯烷-3-基、1-(2-羟基丙酰基)哌啶-4-基、1-(2-羟基乙酰基)哌啶-4-基、4-羧基环己基、3-氨基-4-氟吡咯烷-1-基、(7r,8as)-7-羟基六氢吡咯并[1,2-a]吡嗪-2(1h)-基、(7r,8as)-7-羟基六氢吡咯并[1,2-a]吡嗪-2(1h)-基、4-亚氨基-4-氧代-4λ
6-哌嗪-1-基、(2-羟基-n-甲基乙酰胺基)吡咯烷-1-基、4-(2-羟基乙基)哌嗪-1-基、2-甲氧基乙氧基、(四氢-2h-吡喃-4-基)氧基、环丙基和3-(2-羟基-n-甲基乙酰胺基)氮杂环丁-1-基、1-(2-羟基乙酰基)吡咯烷-3-基、1-乙酰基哌啶-3-基、1-(3
’‑
吡咯烷-2
’‑
酮)吡咯烷-3-基、1-(1
’‑
甲基-(3
’‑
吡咯烷-2
’‑
酮))吡咯烷-3-基、1-(2-丙酰胺)吡咯烷-3-基、1-(甲基-l-脯氨酰基)哌啶-4-基、1-(4-甲基吗啉-3-基)吡咯烷-3-基、3-氰基环丁-1-基、1-(羟基甲基羰基)氮杂环丁-3-基、1-(2-(二甲基氨基)乙烷羰基)氮杂环丁-3-基、1-(二甲基氨基-甲基-乙酰基)氮杂环丁-3-基、1-((1-甲基氮杂环丁-2-基)羰基)氮杂环丁-3-基、1-(2-(4-甲基哌嗪-1-基)乙-1-酮)氮杂环丁-3-基、1-(2-(4-羟基哌嗪-1-基)乙-1-酮)氮杂环丁-3-基、1-((1-甲基氮杂环丁-2-基)羰基)氮杂环丁-3-基、1-(羟基-甲基-乙酰基)氮杂环丁-3-基、1-((反)-3-羟基环丁基羰基)氮杂环丁-3-基、1-((顺)-3-羟基环丁基羰基)氮杂环丁-3-基、1-((4-甲基吗啉-3-基)羰基)氮杂环丁-3-基、1-(羟基-乙酰基)吡咯烷-3-基、1-((四氢呋喃-2-基)羰基)氮杂环丁-3-基、1-((四氢呋喃-3-基)羰基)氮杂环丁-3-基、1-(羟基-甲基-乙酰基)吡咯
烷-3-基、1-(3-羟基丁酰基)氮杂环丁-3-基、1-((-3-羟基-3-甲基环丁基)羰基)氮杂环丁-3-基、1-(4-甲基吗啉-3-基)羰基)吡咯烷-3-基、1-((羟基甲基)环丁基羰基)氮杂环丁-3-基、1-((1-乙基氮杂环丁-2-基)羰基)氮杂环丁-3-基、1-((1-(2-氟乙基)氮杂环丁-2-基)羰基)氮杂环丁-3-基、1-((1-异丙基氮杂环丁-2-基)羰基)氮杂环丁-3-基、1-((1-(2-氟乙基)氮杂环丁-2-基)羰基)吡咯烷-3-基、1-((反)-3-羟基环丁基羰基)吡咯烷-3-基、1-((顺)-3-羟基环丁基羰基)吡咯烷-3-基、1-((3-羟基-3-甲基环丁基)羰基)吡咯烷-3-基、1-(2-甲氧基乙-1-酮)氮杂环丁-3-基、1-(2-(二甲基氨基)-2-甲基丙-1-酮)氮杂环丁-3-基、1-((环丙烷-1-甲腈)羰基)氮杂环丁-3-基、1-((乙-1-醇)磺酰基)氮杂环丁-3-基、1-((n,n-二甲基乙-1-胺)磺酰基)氮杂环丁-3-基、1-((2-甲氧基乙基)羧酸酯)氮杂环丁-3-基、1-((3-甲氧基环丁基)羰基)氮杂环丁-3-基、3-(2-羟基-n-甲基乙酰胺)环戊基、3-(2-羟基丙酰胺)环戊基、3-(2-羟基乙酰胺)环戊基、3-(2-羟基乙基)-3-氮杂双环[3.1.0]己-1-基、(4-羟基哌啶-1-基)甲基、(2-氧杂-5-氮杂双环[2.2.1]庚-5-基)甲基、1-(吗啉-4-基)乙基、(5,6,7,8-四氢-[1,2,4]三唑并[1,5-a]吡嗪-7-基)甲基、1-(2-羟基乙基)哌啶-4-基-4-甲腈、1-(2-羟基乙酰基)哌啶-4-基-4-甲腈、2-甲氧基乙基哌嗪-1-基、1-(四氢-2h-吡喃-4-羰基)哌啶-4-基-4-d、1-(2-甲氧基乙酰基)吡咯烷-3-基、1-(四氢呋喃-2-羰基)吡咯烷-3-基、3-(2-羟基-n-甲基乙酰胺)氮杂环丁-1-基、1-((四氢呋喃-2-基)羰基)氮杂环丁-3-基、1-((1-甲基哌啶-2-基)羰基)氮杂环丁-3-基、1-(2-(二甲基氨基)乙-1-酮)氮杂环丁-3-基、1-(3-羟基丙-1-酮)氮杂环丁-3-基、1-(2-羟基乙-1-酮)氮杂环丁-3-基、1-(2-羟基丙-1-酮)氮杂环丁-3-基、1-(2-羟基-n-甲基乙酰胺)环丁-3-基、1-(2-羟基乙-1-酮)-3-d-氮杂环丁-3-基、1-羧酸酯哌啶-4-基、1-(吗啉-4-羰基)哌啶-4-基、1-乙酰基吡咯烷-3-基、1-(吗啉-4-羰基)吡咯烷-3-基、氰基甲基、1-丙腈-氮杂环丁-3-基、1-(2-甲氧基-n-甲基乙酰胺)环丁-3-基、1-(3-羟基-n-甲基丙酰胺)环丁-3-基、1-(2-羟基-n-甲基丙酰胺)环丁-3-基、1-(2-羟基乙-1-酮)氮杂双环[3.1.0]己-3-基、1-((4-甲基吗啉-3-基)羰基)氮杂双环[3.1.0]己-3-基、1-(四氢-2h-吡喃-4-基)氮杂双环[3.1.0]己-3-基、1-(乙-1-醇)氮杂双环[3.1.0]己-3-基、1-(4-甲基吗啉-3-羰基)-3-甲腈-吡咯烷-3-基、1-(4-甲基吗啉-3-羰基)-4-甲腈-哌啶-4-基、1-(2-羟基乙酰基)-3-甲腈-吡咯烷-3-基、(1,3-二甲基哌嗪-4-基-2-酮)甲基和(2-氧杂-5-氮杂双环[2.2.1]庚-5-基)甲基。
[0160]
在一些实施方案中,每个r
11
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基、5-10元杂芳基、卤基、d、cn、or
a3
、sr
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3rd3
、nr
c3
c(o)r
b3
、nr
c3
c(o)or
a3
、nr
c3
s(o)2r
b3
、nr
c3
s(o)2nr
c3rd3
、s(o)2r
b3
和s(o)2nr
c3rd3
;其中所述c
1-6
烷基、c
3-10
环烷基、4-10元杂环烷基、c
6-10
芳基和5-10元杂芳基各自任选地被独立地选自r
12
的1、2、3或4个取代基取代。
[0161]
在一些实施方案中,每个r
11
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基、5-6元杂芳基、4-6元杂环烷基、卤基、d、cn、or
a3
、sr
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3rd3
、nr
c3
c(o)r
b3
、nr
c3
c(o)or
a3
、nr
c3
s(o)r
b3
、nr
c3
s(o)2r
b3
、nr
c3
s(o)2nr
c3rd3
、s(o)r
b3
、s(o)nr
c3rd3
、s(o)2r
b3
和s(o)2nr
c3rd3
;其中所述c
1-6
烷基、c
3-6
环烷基、5-6元杂芳基和4-6元杂环烷基各自任选地被独立地选自r
12
的1、2或3个取代基取代。
[0162]
在一些实施方案中,每个r
11
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-4
环烷基、5-6元杂芳基、4-6元杂环烷基、卤基、d、cn、or
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3rd3
、nr
c3
c(o)
(二甲基氨基)-2-甲基丙基-1-酮、(环丙烷-1-甲腈)甲基-1-酮、s(o)2ch2ch2oh、s(o)2ch2ch2n(ch3)2、2-甲氧基乙基-羧基、n-甲基甲烷磺酰胺基、2-羟基-n-甲基乙酰胺基、2-羟基丙酰氨基、四氢-2h-吡喃-4-甲基-1-酮、2-甲氧基乙酰基、2-羟基-n-甲基乙酰胺基、四氢呋喃-2-甲基-1-酮、(1-甲基哌啶-2-基)甲基-1-酮、2-(二甲基氨基)乙基-1-酮、3-羟基丙基-1-酮、甲氧基甲基-羧基、吗啉-4-羰基、丙腈、2-甲氧基-n-甲基乙酰胺基、3-羟基-n-甲基丙酰胺基、2-羟基-n-甲基丙酰胺基、四氢-2h-吡喃-4-基和1,3-二甲基哌嗪基-2-酮。
[0173]
在一些实施方案中,每个r
12
独立地选自c
1-6
烷基、c
1-6
卤代烷基、卤基、d、cn、or
a5
和nr
c5rd5
;其中所述c
1-6
烷基任选地被独立地选自rg的1、2、3或4个取代基取代。
[0174]
在一些实施方案中,每个r
12
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基、4-7元杂环烷基、卤基、d、cn、or
a5
、sr
a5
、c(o)r
b5
、c(o)nr
c5rd5
、c(o)or
a5
、nr
c5rd5
、nr
c5
c(o)r
b5
、s(o)2r
b5
和s(o)2nr
c5rd5
;其中所述c
1-6
烷基、c
3-6
环烷基和4-7元杂环烷基各自任选地被独立地选自rg的1、2、3或4个取代基取代。
[0175]
在一些实施方案中,每个r
12
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、4-7元杂环烷基、f、cl、d、cn、or
a5
、c(o)r
b5
、c(o)nr
c5rd5
和nr
c5rd5
;其中所述c
1-3
烷基、c
3-6
环烷基和4-7元杂环烷基各自任选地被独立地选自rg的1个取代基取代。
[0176]
在一些实施方案中,每个r
12
独立地选自c
1-3
烷基、卤基、d和or
a5
。
[0177]
在一些实施方案中,r
12
是甲基。
[0178]
在一些实施方案中,r
12
是oh。
[0179]
在一些实施方案中,每个r
21
独立地选自c
1-6
烷基、c
1-6
卤代烷基、卤基、d、cn、or
a4
、c(o)r
b4
、c(o)nr
c4rd4
、c(o)or
a4
、nr
c4rd4
和s(o)2r
b4
;其中所述c
1-6
烷基任选地被独立地选自r
22
的1、2或3个取代基取代。
[0180]
在一些实施方案中,每个r
21
独立地选自c
1-3
烷基、卤基、d、cn和or
a4
;其中所述c
1-3
烷基任选地被独立地选自r
22
的1或2个取代基取代。
[0181]
在一些实施方案中,每个r
21
独立地选自c
1-2
烷基、f、cl、d、cn和or
a4
;其中所述c
1-2
烷基任选地被选自r
22
的1个取代基取代。
[0182]
在一些实施方案中,每个r
21
独立地选自c
1-2
烷基、卤基、d、cn和or
a4
;其中所述c
1-3
烷基任选地被独立地选自r
22
的1或2个取代基取代。
[0183]
在一些实施方案中,每个r
21
独立地选自c
1-3
烷基、卤基、d、cn和or
a4
;其中所述c
1-3
烷基任选地被独立地选自r
22
的1或2个取代基取代。
[0184]
在一些实施方案中,每个r
21
独立地选自c
1-3
烷基、f、cl、d、cn和or
a4
;其中所述c
1-3
烷基任选地被独立地选自r
22
的1或2个取代基取代。在一些实施方案中,每个r
21
独立地选自c
1-2
烷基、f、d、cn和or
a4
;其中所述c
1-2
烷基任选地被选自r
22
的1个取代基取代。
[0185]
在一些实施方案中,每个r
21
独立地选自甲基、f、d、cn和oh;
[0186]
在一些实施方案中,每个r
22
独立地选自c
1-6
烷基、c
1-6
卤代烷基、卤基、d、cn、or
a6
和nr
c6rd6
;其中所述c
1-6
烷基任选地被独立地选自rg的1或2个取代基取代。
[0187]
在一些实施方案中,每个r
22
独立地选自f、cl、d、cn和or
a6
。
[0188]
在一些实施方案中,每个r
22
独立地选自卤基、d、cn和or
a6
。
[0189]
在一些实施方案中,每个r
22
独立地选自f、cl、cn和or
a6
。
[0190]
在一些实施方案中,r
22
是or
a6
。在一些实施方案中,r
22
是oh。在一些实施方案中,每
个r
22
独立地选自f和cl。在一些实施方案中,r
22
是cn。
[0191]
在一些实施方案中,每个r
a1
、r
c1
和r
d1
独立地选自h、c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基和4-6元杂环烷基;其中所述c
1-6
烷基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
11
的1、2或3个取代基取代。
[0192]
在一些实施方案中,每个r
a1
、r
c1
和r
d1
独立地选自h和c
1-6
烷基。
[0193]
在一些实施方案中,每个r
a1
、r
c1
和r
d1
独立地选自h、c
1-6
烷基和4-6元杂环烷基。
[0194]
在一些实施方案中,连接至同一个n原子的任何r
c1
和r
d1
与其连接的n原子一起形成任选地被独立地选自r
11
的1、2或3个取代基取代的4元、5元或6元杂环烷基。
[0195]
在一些实施方案中,每个r
c1
和r
d1
独立地选自h、c
1-3
烷基和c
1-3
卤代烷基。
[0196]
在一些实施方案中,r
c1
和r
d1
独立地选自h和c
1-2
烷基。
[0197]
在一些实施方案中,每个r
b1
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基和4-6元杂环烷基;其中所述c
1-6
烷基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
11
的1、2或3个取代基取代。在一些实施方案中,每个r
b1
独立地选自c
1-6
烷基。
[0198]
在一些实施方案中,每个r
a2
、r
c2
和r
d2
独立地选自h、c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基和4-6元杂环烷基;其中所述c
1-6
烷基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
21
的1、2或3个取代基取代。
[0199]
在一些实施方案中,每个r
a2
、r
c2
和r
d2
独立地选自h和c
1-6
烷基。
[0200]
在一些实施方案中,每个r
a2
独立地选自h和c
1-3
烷基。
[0201]
在一些实施方案中,每个r
a2
独立地选自h和c
1-2
烷基。
[0202]
在一些实施方案中,连接至同一个n原子的任何r
c2
和r
d2
与其连接的n原子一起形成任选地被独立地选自r
21
的1、2或3个取代基取代的4元、5元或6元杂环烷基。
[0203]
在一些实施方案中,每个r
b2
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基和4-6元杂环烷基;其中所述c
1-6
烷基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
21
的1、2或3个取代基取代。
[0204]
在一些实施方案中,每个r
b2
独立地选自c
1-6
烷基。
[0205]
在一些实施方案中,每个r
a3
、r
c3
和r
d3
独立地选自h、c
1-6
烷基、c
1-6
卤代烷基和c
3-6
环烷基;其中所述c
1-6
烷基和c
3-6
环烷基各自任选地被独立地选自r
12
的1或2个取代基取代。
[0206]
在一些实施方案中,每个r
a3
、r
c3
和r
d3
独立地选自h、c
1-3
烷基、c
1-3
卤代烷基和c
3-5
环烷基。
[0207]
在一些实施方案中,每个r
a3
、r
c3
和r
d3
独立地选自h和c
1-2
烷基。
[0208]
在一些实施方案中,连接至同一个n原子的任何r
c3
和r
d3
与其连接的n原子一起形成任选地被独立地选自r
12
的1或2个取代基取代的4元、5元或6元杂环烷基。
[0209]
在一些实施方案中,每个r
b3
独立地选自c
1-6
烷基、c
1-6
卤代烷基和c
3-6
环烷基;其中所述c
1-6
烷基和c
3-6
环烷基各自任选地被独立地选自r
12
的1或2个取代基取代。
[0210]
在一些实施方案中,每个r
b3
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基和4-6元杂环烷基;其中所述c
1-3
烷基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
12
的1或2个取代基取代。
[0211]
在一些实施方案中,每个r
b3
独立地选自c
1-3
烷基和c
3-5
环烷基。
[0212]
在一些实施方案中,每个r
b3
独立地选自c
1-2
烷基和环丙基。在一些实施方案中,每
个r
b3
独立地选自c
1-2
烷基。
[0213]
在一些实施方案中,每个r
a4
、r
c4
和r
d4
独立地选自h、c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自r
22
的1或2个取代基取代。
[0214]
在一些实施方案中,每个r
a4
、r
c4
和r
d4
独立地选自h、c
1-3
烷基和c
1-3
卤代烷基;其中所述c
1-3
烷基任选地被独立地选自r
22
的1或2个取代基取代。
[0215]
在一些实施方案中,每个r
a4
独立地选自h和c
1-3
烷基。
[0216]
在一些实施方案中,r
a4
独立地选自h和c
1-2
烷基。在一些实施方案中,r
a4
是h。
[0217]
在一些实施方案中,每个r
b4
独立地选自c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自r
22
的1或2个取代基取代。在一些实施方案中,每个r
b4
独立地选自c
1-6
烷基。
[0218]
在一些实施方案中,每个r
a5
、r
c5
和r
d5
独立地选自h、c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自rg的1或2个取代基取代。
[0219]
在一些实施方案中,r
a5
选自h和c
1-3
烷基。
[0220]
在一些实施方案中,每个r
b5
独立地选自c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自rg的1或2个取代基取代。
[0221]
在一些实施方案中,每个r
a6
、r
c6
和r
d6
独立地选自h、c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自rg的1或2个取代基取代。
[0222]
在一些实施方案中,每个r
a6
独立地选自h和c
1-3
烷基。
[0223]
在一些实施方案中,r
a6
独立地选自h和c
1-2
烷基。
[0224]
在一些实施方案中,每个r
b6
独立地选自c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自rg的1或2个取代基取代。在一些实施方案中,每个r
b6
独立地选自c
1-6
烷基。
[0225]
在一些实施方案中,每个rg独立地选自oh、cn、卤基、c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、c
1-3
烷氧基-c
1-3
烷基、ho-c
1-3
烷基、氰基-c
1-3
烷基、h2n-c
1-3
烷基、氨基、c
1-6
烷基氨基、二(c
1-6
烷基)氨基、c
1-6
烷基硫基、c
1-6
烷基磺酰基、羧基、c
1-6
烷基羰基、c
1-6
烷氧基羰基和c
1-6
烷基羰基氨基。
[0226]
在一些实施方案中,每个rg独立地选自卤基、c
1-6
烷基和c
1-6
卤代烷基。
[0227]
在一些实施方案中,每个rg独立地选自oh、cn、f、cl、c
1-3
烷基和c
1-3
卤代烷基。
[0228]
在一些实施方案中,式i化合物是式ia化合物:
[0229][0230]
或其药学上可接受的盐;其中cy1、r1和每个r2如本文所定义。
[0231]
在一些实施方案中,式i化合物是式iia化合物:
[0232][0233]
或其药学上可接受的盐;其中cy1、每个r2、r3和n如本文所定义。
[0234]
在一些实施方案中,式i化合物是式iib化合物:
[0235][0236]
或其药学上可接受的盐,其中cy1和每个r2如本文所定义。
[0237]
在一些实施方案中,式i化合物是式iiia化合物:
[0238][0239]
或其药学上可接受的盐,其中r1、每个r2和r
10
如本文所定义。
[0240]
在一些实施方案中,式i化合物是式iiib化合物:
[0241][0242]
或其药学上可接受的盐,其中r1、每个r2和r
10
如本文所定义。
[0243]
在一些实施方案中,式i化合物是式iiic化合物:
[0244][0245]
或其药学上可接受的盐,其中r1、每个r2和r
10
如本文所定义。
[0246]
在一些实施方案中,式i化合物是式iva化合物:
[0247][0248]
或其药学上可接受的盐,其中cy1和r1如本文所定义。
[0249]
在一些实施方案中,式i化合物是式ivb化合物:
[0250][0251]
或其药学上可接受的盐,其中cy1如本文所定义。
[0252]
在一些实施方案中,式i化合物是式va化合物:
[0253][0254]
或其药学上可接受的盐,其中m是0、1或2;并且其中cy1、r1和r
21
如本文所定义。在一些实施方案中,m是0。在一些实施方案中,m是1。在一些实施方案中,m是2。
[0255]
在一些实施方案中,式i化合物是式vb化合物:
[0256][0257]
或其药学上可接受的盐,其中cy1和r1如本文所定义。
[0258]
在一些实施方案中,式i化合物是式vc化合物:
[0259][0260]
或其药学上可接受的盐,其中cy1如本文所定义。
[0261]
在一些实施方案中,式i化合物是式vi化合物:
[0262][0263]
或其药学上可接受的盐,其中cy1和r1如本文所定义。
[0264]
在一些实施方案中,本文提供式(i)化合物或其药学上可接受的盐,其中:
[0265]
cy1选自苯基、吡啶基和吡唑基;其中所述苯基吡啶基和吡唑基各自任选地被独立地选自r
10
的1、2、3或4个取代基取代;
[0266]
r1选自卤基、c
1-6
烷基、c
1-6
卤代烷基、c
3-5
环烷基、4-5元杂环烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、c
1-3
烷氧基-c
1-3
烷基、ho-c
1-3
烷基、c
1-6
烷基氨基和二(c
1-6
烷基)氨基;其中所述c
1-6
烷基、c
1-6
卤代烷基、c
3-5
环烷基、4-5元杂环烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、c
1-3
烷氧基-c
1-3
烷基、ho-c
1-3
烷基、c
1-6
烷基氨基和二(c
1-6
烷基)氨基的一个或多个h原子任选地被一个或多个d原子替换;
[0267]
每个r2和r3独立地选自c
1-6
烷基、c
2-6
烯基、c
1-6
卤代烷基、c
3-6
环烷基、4-6元杂环烷基、卤基、cn、or
a2
、c(o)r
b2
、c(o)nr
c2rd2
、c(o)or
a2
、nr
c2rd2
和s(o)2r
b2
;其中所述c
1-6
烷基、c
2-6
烯基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
21
的1、2、3或4个取代基取代;
[0268]
或苯环上的两个相邻r2取代基与其连接的原子一起形成稠合5元或6元环烷基环
或稠合5元或6元杂环烷基环;其中每个稠合5元或6元杂环烷基环具有至少一个成环碳原子和独立地选自o和n的1或2个成环杂原子;其中每个稠合5元或6元杂环烷基环的成环碳原子任选地被氧代取代以形成羰基;并且其中所述稠合5元或6元环烷基环和所述稠合5元或6元杂环烷基环各自任选地被独立地选自r
21
的1、2、3或4个取代基取代;
[0269]
n选自0和1;
[0270]
每个r
10
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-10
环烷基、4-12元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-12元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基、5-10元杂芳基-c
1-3
亚烷基、卤基、d、cn、or
a1
、c(o)r
b1
、c(o)nr
c1rd1
、c(o)or
a1
、nr
c1rd1
、nr
c1
c(o)r
b1
和s(o)2r
b1
;其中所述c
1-6
烷基、c
3-10
环烷基、4-12元杂环烷基、c
6-10
芳基、5-10元杂芳基、c
3-10
环烷基-c
1-3
亚烷基、4-12元杂环烷基-c
1-3
亚烷基、c
6-10
芳基-c
1-3
亚烷基和5-10元杂芳基-c
1-3
亚烷基各自任选地被独立地选自r
11
的1、2、3或4个取代基取代;
[0271]
每个r
11
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基、5-6元杂芳基、4-6元杂环烷基、卤基、d、cn、or
a3
、sr
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3rd3
、nr
c3
c(o)r
b3
、nr
c3
c(o)or
a3
、nr
c3
s(o)r
b3
、nr
c3
s(o)2r
b3
、nr
c3
s(o)2nr
c3rd3
、s(o)r
b3
、s(o)nr
c3rd3
、s(o)2r
b3
和s(o)2nr
c3rd3
;其中所述c
1-6
烷基、c
3-6
环烷基、5-6元杂芳基和4-6元杂环烷基各自任选地被独立地选自r
12
的1、2或3个取代基取代;
[0272]
每个r
12
独立地选自c
1-6
烷基、c
1-6
卤代烷基、卤基、d、cn、or
a5
和nr
c5rd5
;其中所述c
1-6
烷基任选地被独立地选自rg的1、2、3或4个取代基取代;
[0273]
每个r
21
独立地选自c
1-6
烷基、c
1-6
卤代烷基、卤基、d、cn、or
a4
、c(o)r
b4
、c(o)nr
c4rd4
、c(o)or
a4
、nr
c4rd4
和s(o)2r
b4
;其中所述c
1-6
烷基任选地被独立地选自r
22
的1、2或3个取代基取代;
[0274]
每个r
22
独立地选自c
1-6
烷基、c
1-6
卤代烷基、卤基、d、cn、or
a6
和nr
c6rd6
;其中所述c
1-6
烷基任选地被独立地选自rg的1或2个取代基取代;
[0275]
每个r
a1
、r
c1
和r
d1
独立地选自h、c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基和4-6元杂环烷基;其中所述c
1-6
烷基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
11
的1、2或3个取代基取代;
[0276]
或连接至同一个n原子的任何r
c1
和r
d1
与其连接的n原子一起形成任选地被独立地选自r
11
的1、2或3个取代基取代的4元、5元或6元杂环烷基;
[0277]
每个r
b1
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基和4-6元杂环烷基,其中所述c
1-6
烷基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
11
的1、2或3个取代基取代;
[0278]
每个r
a2
、r
c2
和r
d2
独立地选自h、c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基和4-6元杂环烷基;其中所述c
1-6
烷基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
21
的1、2或3个取代基取代;
[0279]
或连接至同一个n原子的任何r
c2
和r
d2
与其连接的n原子一起形成任选地被独立地选自r
21
的1、2或3个取代基取代的4元、5元或6元杂环烷基;
[0280]
每个r
b2
独立地选自c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基和4-6元杂环烷基,其中所述c
1-6
烷基、c
3-6
环烷基和4-6元杂环烷基各自任选地被独立地选自r
21
的1、2或3个取代基取代;
[0281]
每个r
a3
、r
c3
和r
d3
独立地选自h、c
1-6
烷基、c
1-6
卤代烷基和c
3-6
环烷基;其中所述c
1-6
烷基和c
3-6
环烷基各自任选地被独立地选自r
12
的1或2个取代基取代;
[0282]
每个r
b3
独立地选自c
1-6
烷基、c
1-6
卤代烷基和c
3-6
环烷基;其中所述c
1-6
烷基和c
3-6
环烷基各自任选地被独立地选自r
12
的1或2个取代基取代;
[0283]
每个r
a4
、r
c4
和r
d4
独立地选自h、c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自r
22
的1或2个取代基取代;
[0284]
每个r
b4
独立地选自c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自r
22
的1或2个取代基取代;
[0285]
每个r
a5
、r
c5
和r
d5
独立地选自h、c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自rg的1或2个取代基取代;
[0286]
每个r
a6
、r
c6
和r
d6
独立地选自h、c
1-6
烷基和c
1-6
卤代烷基;其中所述c
1-6
烷基任选地被独立地选自rg的1或2个取代基取代;
[0287]
且
[0288]
每个rg独立地选自oh、cn、卤基、c
1-6
烷基、c
1-6
卤代烷基、c
3-6
环烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、c
1-3
烷氧基-c
1-3
烷基、ho-c
1-3
烷基、氰基-c
1-3
烷基、h2n-c
1-3
烷基、氨基、c
1-6
烷基氨基、二(c
1-6
烷基)氨基、c
1-6
烷基硫基、c
1-6
烷基磺酰基、羧基、c
1-6
烷基羰基、c
1-6
烷氧基羰基和c
1-6
烷基羰基氨基。
[0289]
在一些实施方案中,本文提供式(i)化合物或其药学上可接受的盐,其中:
[0290]
cy1选自苯基、吡啶-3-基和吡唑-4-基;其中cy1的苯基、吡啶-3-基和吡唑-4-基各自任选地被选自r
10
的1个取代基取代;
[0291]
r1选自cl、c
1-3
烷基、c
1-3
卤代烷基、环丙基、氮杂环丁基、羟基甲基、c
1-3
烷氧基、c
1-3
卤代烷氧基和c
1-3
烷基氨基;其中所述c
1-3
烷基、c
1-3
卤代烷基、环丙基、氮杂环丁基、羟基甲基、c
1-3
烷氧基、c
1-3
卤代烷氧基和c
1-3
烷基氨基的一个或多个h原子任选地被一个或多个d原子替换;
[0292]
每个r2独立地选自c
1-3
烷基、c
1-3
卤代烷基、f、cl、cn和or
a2
;其中所述c
1-6
烷基任选地被选自r
21
的1个取代基取代;
[0293]
或苯环上的r2取代基与其连接的原子一起形成稠合5元或6元环烷基环或稠合5元或6元杂环烷基环;其中每个稠合5元或6元杂环烷基环具有至少一个成环碳原子和1或2个成环o原子;并且其中所述稠合5元或6元环烷基环或该稠合5元或6元杂环烷基环各自任选地被选自r
21
的1个取代基取代;
[0294]
n是0;
[0295]r10
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基、5-6元杂芳基-c
1-2
亚烷基、卤基、d、cn、c(o)nr
c1rd1
和nr
c1rd1
;其中所述c
1-3
烷基、c
3-6
环烷基、4-10元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基和5-6元杂芳基-c
1-2
亚烷基各自任选地被独立地选自r
11
的1或2个取代基取代;
[0296]
每个r
11
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-4
环烷基、5-6元杂芳基、4-6元杂环烷基、卤基、d、cn、or
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3rd3
、nr
c3
c(o)r
b3
和s(o)2r
b3
;其中所述c
1-3
烷基、c
3-4
环烷基、5-6元杂芳基和4-6元杂环烷基各自任选地被选自r
12
的1个取代基取代;
[0297]
每个r
12
选自c
1-3
烷基、卤基、d和or
a5
;
[0298]
每个r
21
独立地选自c
1-3
烷基、卤基、d、cn和or
a4
;其中所述c
1-3
烷基任选地被独立地
选自r
22
的1或2个取代基取代;
[0299]
每个r
22
独立地选自卤基、d、cn和or
a6
;
[0300]rc1
和r
d1
独立地选自h、c
1-3
烷基和c
1-3
卤代烷基;
[0301]
每个r
a2
独立地选自h和c
1-3
烷基;
[0302]
每个r
a3
、r
c3
和r
d3
独立地选自h、c
1-3
烷基、c
1-3
卤代烷基和c
3-5
环烷基;
[0303]
每个r
b3
独立地选自c
1-3
烷基和c
3-5
环烷基;
[0304]
每个r
a4
独立地选自h和c
1-3
烷基;
[0305]
每个r
a5
选自h和c
1-3
烷基;并且
[0306]
每个r
a6
独立地选自h和c
1-3
烷基。
[0307]
在一些实施方案中,本文提供式(i)化合物或其药学上可接受的盐,其中:
[0308]
cy1选自苯基、吡啶-3-基和吡唑-4-基;其中cy1的苯基、吡啶-3-基和吡唑-4-基各自任选地被选自r
10
的1个取代基取代;
[0309]
r1选自cl、c
1-3
烷基、c
1-3
卤代烷基、环丙基、氮杂环丁基、羟基甲基、c
1-3
烷氧基、c
1-3
卤代烷氧基和c
1-3
烷基氨基;其中所述c
1-3
烷基、c
1-3
卤代烷基、环丙基、氮杂环丁基、羟基甲基、c
1-3
烷氧基、c
1-3
卤代烷氧基和c
1-3
烷基氨基的一个或多个h原子任选地被一个或多个d原子替换;
[0310]
每个r2独立地选自c
1-3
烷基、c
1-3
卤代烷基、f、cl、cn和or
a2
;其中所述c
1-6
烷基任选地被选自r
21
的1个取代基取代;
[0311]
或苯环上的r2取代基与其连接的原子一起形成稠合5元或6元环烷基环或稠合5元或6元杂环烷基环;其中每个稠合5元或6元杂环烷基环具有至少一个成环碳原子和1或2个成环o原子;并且其中所述稠合5元或6元环烷基环或该稠合5元或6元杂环烷基环各自任选地被选自r
21
的1个取代基取代;
[0312]
n是0;
[0313]r10
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-6
环烷基、4-6元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基、5-6元杂芳基-c
1-2
亚烷基、卤基、d、cn、c(o)nr
c1rd1
和nr
c1rd1
;其中所述c
1-3
烷基、c
3-6
环烷基、4-6元杂环烷基、5-6元杂芳基、4-6元杂环烷基-c
1-2
亚烷基和5-6元杂芳基-c
1-2
亚烷基各自任选地被独立地选自r
11
的1或2个取代基取代;
[0314]
每个r
11
独立地选自c
1-3
烷基、c
1-3
卤代烷基、c
3-4
环烷基、5-6元杂芳基、4-6元杂环烷基、卤基、d、cn、or
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3rd3
、nr
c3
c(o)r
b3
和s(o)2r
b3
;其中所述c
1-3
烷基、c
3-4
环烷基、5-6元杂芳基和4-6元杂环烷基各自任选地被选自r
12
的1个取代基取代;
[0315]
每个r
12
选自c
1-3
烷基、卤基、d和or
a5
;
[0316]
每个r
21
独立地选自c
1-3
烷基、卤基、d、cn和or
a4
;其中所述c
1-3
烷基任选地被独立地选自r
22
的1或2个取代基取代;
[0317]
每个r
22
独立地选自卤基、d、cn和or
a6
;
[0318]rc1
和r
d1
独立地选自h、c
1-3
烷基和c
1-3
卤代烷基;
[0319]
每个r
a2
独立地选自h和c
1-3
烷基;
[0320]
每个r
a3
、r
c3
和r
d3
独立地选自h、c
1-3
烷基、c
1-3
卤代烷基和c
3-5
环烷基;
[0321]
每个r
b3
独立地选自c
1-3
烷基和c
3-5
环烷基;
[0322]
每个r
a4
独立地选自h和c
1-3
烷基;
[0323]
每个r
a5
选自h和c
1-3
烷基;并且
[0324]
每个r
a6
独立地选自h和c
1-3
烷基。
[0325]
在一些实施方案中,本文提供式(i)化合物或其药学上可接受的盐,其中:
[0326]
cy1选自苯基、吡啶-3-基和吡唑-4-基;其中cy1的苯基、吡啶-3-基和吡唑-4-基各自任选地被选自r
10
的1个取代基取代;
[0327]
r1选自cl、c
1-2
烷基、c
1-2
卤代烷基、环丙基、羟基甲基、c
1-2
烷氧基、c
1-2
卤代烷氧基和c
1-2
烷基氨基;其中所述c
1-2
烷基、c
1-2
卤代烷基、环丙基、羟基甲基、c
1-2
烷氧基、c
1-2
卤代烷氧基和c
1-2
烷基氨基的一个或多个h原子任选地被一个或多个d原子替换;
[0328]
每个r2独立地选自c
1-2
烷基、c
1-2
卤代烷基、f、cl、cn和or
a2
;其中所述c
1-2
烷基任选地被选自r
21
的1个取代基取代;
[0329]
或苯环上的r2取代基与其连接的原子一起形成稠合5元或6元环烷基环或稠合5元或6元杂环烷基环;其中每个稠合5元或6元杂环烷基环具有至少一个成环碳原子和1或2个成环o原子;并且其中所述稠合5元或6元环烷基环或所述稠合5元或6元杂环烷基环各自任选地被选自r
21
的1个取代基取代;
[0330]
n是0;
[0331]r10
独立地选自c
1-2
烷基、c
1-2
卤代烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三唑基)甲基、1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮、f、cl、d、cn、nr
c1rd1
;其中所述c
1-2
烷基、c
3-6
环烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基和(三唑基)甲基各自任选地被独立地选自r
11
的1或2个取代基取代;
[0332]
每个r
11
独立地选自c
1-2
烷基、c
1-2
卤代烷基、f、cl、d、cn、or
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3rd3
、nr
c3
c(o)r
b3
和s(o)2r
b3
;
[0333]
每个r
21
独立地选自c
1-2
烷基、f、cl、d、cn和or
a4
;其中所述c
1-2
烷基任选地被选自r
22
的1个取代基取代;
[0334]
每个r
22
独立地选自f、cl、cn和or
a6
;
[0335]rc1
和r
d1
独立地选自h和c
1-2
烷基;
[0336]
每个r
a2
独立地选自h和c
1-2
烷基;
[0337]
每个r
a3
、r
c3
和r
d3
独立地选自h和c
1-2
烷基;
[0338]
每个r
b3
独立地选自c
1-2
烷基和环丙基;
[0339]
每个r
a4
独立地选自h和c
1-2
烷基;并且
[0340]
每个r
a6
独立地选自h和c
1-2
烷基。
[0341]
在一些实施方案中,本文提供式(i)化合物或其药学上可接受的盐,其中:
[0342]
cy1选自苯基、吡啶-3-基和吡唑-4-基;其中cy1的苯基、吡啶-3-基和吡唑-4-基各自被选自r
10
的1个取代基取代;
[0343]
r1选自cl、c
1-2
烷基、c
1-2
卤代烷基、羟基甲基、c
1-2
烷氧基、c
1-2
卤代烷氧基和c
1-2
烷基氨基;其中所述c
1-2
烷基、c
1-2
卤代烷基、羟基甲基、c
1-2
烷氧基、c
1-2
卤代烷氧基和c
1-2
烷基氨基的一个或多个h原子任选地被一个或多个d原子替换;
[0344]
每个r2独立地选自c
1-2
烷基和f;其中所述c
1-2
烷基各自任选地被选自r
21
的1个取代基取代;
[0345]
或苯环上的r2取代基与其连接的原子一起形成稠合5元环烷基环或稠合5元杂环烷基环;其中每个稠合5元杂环烷基环具有至少一个成环碳原子和1或2个成环o原子;并且其中所述稠合5元环烷基环和所述稠合5元杂环烷基环各自任选地被各自独立地选自r
21
的1或2个取代基取代;
[0346]
n是0;
[0347]r10
独立地选自c
1-2
烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三嗪基)甲基和1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮;其中所述c
1-2
烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基和(吡啶基)甲基各自任选地被独立地选自r
11
的1或2个取代基取代;
[0348]
每个r
11
独立地选自c
1-2
烷基、cn、or
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3
c(o)r
b3
和s(o)2r
b3
;
[0349]
每个r
21
独立地选自c
1-2
烷基、f、d、cn和or
a4
;其中所述c
1-2
烷基任选地被选自r
22
的1个取代基取代;
[0350]
每个r
22
是or
a6
;
[0351]
每个r
a3
、r
c3
和r
d3
独立地选自h和c
1-2
烷基;
[0352]
每个r
b3
独立地选自c
1-2
烷基和环丙基;并且
[0353]
每个r
a6
独立地选自h和c
1-2
烷基。
[0354]
在一些实施方案中,本文提供式(i)化合物或其药学上可接受的盐,其中:
[0355]
cy1选自苯基、吡啶-3-基和吡唑-4-基;其中cy1的苯基、吡啶-3-基和吡唑-4-基各自任选地被选自r
10
的1个取代基取代;
[0356]
r1选自cl、c
1-2
烷基、c
1-2
卤代烷基、环丙基、羟基甲基、c
1-2
烷氧基、c
1-2
卤代烷氧基和c
1-2
烷基氨基;其中所述c
1-2
烷基、c
1-2
卤代烷基、环丙基、羟基甲基、c
1-2
烷氧基、c
1-2
卤代烷氧基和c
1-2
烷基氨基的一个或多个h原子任选地被一个或多个d原子替换;
[0357]
每个r2独立地选自c
3-6
环烷基、c
1-2
烷基、c
1-2
卤代烷基、f、cl、cn和or
a2
;其中所述c
1-2
烷基任选地被选自r
21
的1个取代基取代;
[0358]
或苯环上的r2取代基与其连接的原子一起形成稠合5元或6元环烷基环或稠合5元或6元杂环烷基环;其中每个稠合5元或6元杂环烷基环具有至少一个成环碳原子和1或2个成环o原子;并且其中所述稠合5元或6元环烷基环或该稠合5元或6元杂环烷基环各自任选地被选自r
21
的1个取代基取代;
[0359]
n是0;
[0360]r10
独立地选自c
1-2
烷基、c
1-2
卤代烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三唑基)甲基、硫代吗啉基、1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮、六氢吡咯并[1,2-a]吡嗪-2(1h)-基、f、cl、d、cn、or
a1
和nr
c1rd1
,其中所述c
1-2
烷基、c
3-6
环烷基、c
3-6
环烷基、氮杂环丁基、吡咯烷基、哌啶基、吗啉基、哌嗪基、吡啶基、哌嗪酮基、二氮杂双环[2.2.1]庚基(吗啉基)乙基、(吡啶基)甲基、(三唑基)甲基、硫代吗啉基、1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮
和六氢吡咯并[1,2-a]吡嗪-2(1h)-基各自任选地被独立地选自r
11
的1或2个取代基取代;
[0361]
每个r
11
独立地选自c
1-2
烷基、c
1-2
卤代烷基、f、cl、d、cn、or
a3
、c(o)r
b3
、c(o)nr
c3rd3
、c(o)or
a3
、nr
c3rd3
、nr
c3
c(o)r
b3
和s(o)2r
b3
,其中所述c
1-2
烷基任选地被or
a5
取代;
[0362]
每个r
21
独立地选自c
1-2
烷基、f、cl、d、cn和or
a4
;其中所述c
1-2
烷基任选地被选自r
22
的1个取代基取代;
[0363]
每个r
22
独立地选自f、cl、cn和or
a6
;
[0364]
每个r
a1
、r
c1
和r
d1
独立地选自h、c
1-2
烷基和4-6元杂环烷基;
[0365]
每个r
a2
独立地选自h和c
1-2
烷基;
[0366]
每个r
a3
、r
c3
和r
d3
独立地选自h和c
1-2
烷基;
[0367]
每个r
b3
独立地选自c
1-2
烷基和环丙基;
[0368]
每个r
a4
独立地选自h和c
1-2
烷基;
[0369]
每个r
a5
独立地选自h和c
1-2
烷基;并且
[0370]
每个r
a6
独立地选自h和c
1-2
烷基。
[0371]
在一些实施方案中,本文提供选自以下的化合物:
[0372]
5-(2,3-二甲基苯基)-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0373]
5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0374]
5-(2,3-二甲基苯基)-6-甲氧基-3-(1-((1-甲基-1h-1,2,4-三唑-5-基)甲基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0375]
5-(2,3-二氢苯并呋喃-7-基)-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0376]
2-(3-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2-甲基苯基)乙腈;
[0377]
1-(4-(5-(6-(二氟甲氧基)-5-(2,3-二甲基苯基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌嗪-1-基)乙-1-酮;
[0378]
4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-酚;
[0379]
4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈;
[0380]
4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚;
[0381]
(4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-基)甲醇;
[0382]
2-氟-4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-酚;
[0383]
5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0384]
5-(2,3-二氢-1h-茚-4-基)-3-(1-(1-乙基吡咯烷-3-基)-1h-吡唑-4-基)-6-甲氧
基-1h-吡唑并[4,3-b]吡啶;
[0385]
3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)环丁烷甲腈;
[0386]
5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(1-甲基氮杂环丁-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0387]
5-(2,3-二氢-1h-茚-4-基)-3-(1-(1-乙基氮杂环丁-3-基)-1h-吡唑-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶;
[0388]
4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-n,n-二甲基哌啶-1-羧酰胺;
[0389]
4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)哌啶-1-羧酸甲酯;
[0390]
3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸甲酯;
[0391]
1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)乙-1-酮;
[0392]
5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(1-(甲基磺酰基)氮杂环丁-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0393]
3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-n,n-二甲基氮杂环丁烷-1-羧酰胺;
[0394]
环丙基(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)甲酮;
[0395]
5-(2,3-二氢-1h-茚-4-基)-6-乙氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0396]
5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡啶-4-基甲基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0397]
4-(2-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)乙基)吗啉;
[0398]
3-(1-环丙基-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶;
[0399]
3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)丙腈;
[0400]
2-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)乙-1-醇;
[0401]
5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡啶-4-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0402]
(反)-4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)环己-1-醇;
[0403]
5-(2,3-二甲基苯基)-n-甲基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-6-胺;
[0404]
6-(二氟甲基)-5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0405]
(5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-6-基)甲醇;
[0406]
5-(2,3-二氢-1h-茚-4-基)-n-甲基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-6-胺;
[0407]
(5-(2,3-二甲基苯基)-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-6-基)甲醇;
[0408]
4-(6-氯-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚;
[0409]
5-(2,3-二甲基苯基)-6-甲基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0410]
5-(2,3-二甲基苯基)-6-甲氧基-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶;
[0411]
5-(2,3-二甲基苯基)-3-(6-(4-乙基哌嗪-1-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶;
[0412]
1-(4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌嗪-1-基)乙-1-酮;
[0413]
4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吗啉;
[0414]
4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-甲基哌嗪-2-酮;
[0415]
1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-4-醇;
[0416]
(r)-5-(2,3-二甲基苯基)-3-(6-(3,4-二甲基哌嗪-1-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶;
[0417]
5-(2,3-二甲基苯基)-6-(甲氧基-d3)-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶;
[0418]
5-(2,3-二甲基苯基)-6-甲氧基-3-(6-((1s,4s)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶;
[0419]
1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n,n-二甲基哌啶-4-羧酰胺;
[0420]
1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-4-甲基哌啶-4-羧酸;
[0421]
3-(4-(5-(2-氟-3-甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-n,n-二甲基氮杂环丁烷-1-羧酰胺;
[0422]
n-((顺)-4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)环己基)乙酰胺;
[0423]
5-(2,3-二氢-1h-茚-4-基)-3-(6-(2,4-二甲基哌嗪-1-基)吡啶-3-基)-6-甲氧
基-1h-吡唑并[4,3-b]吡啶;
[0424]
2-(3-(3-(6-(4-乙酰基哌嗪-1-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2-甲基苯基)乙腈;
[0425]
2-(3-(6-甲氧基-3-(6-吗啉代吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2-甲基苯基)乙腈;
[0426]
5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(6-(吡咯烷-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶;
[0427]
4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吗啉;
[0428]
4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-乙基哌嗪-1-羧酰胺;
[0429]
4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌嗪-1-羧酰胺;
[0430]
1-(4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)苯基)哌嗪-1-基)乙-1-酮;
[0431]
5-(2,3-二氢-1h-茚-4-基)-3-(4-(4-异丙基哌嗪-1-基)苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶;
[0432]
5-(2,3-二氢-1h-茚-4-基)-3-(4-(4-乙基哌嗪-1-基)苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶;
[0433]
1-(4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌嗪-1-基)乙-1-酮;
[0434]
8-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮;
[0435]
5-(2,3-二甲基苯基)-6-甲氧基-3-(1-(吡啶-2-基甲基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶;
[0436]
3-(1-环丙基-1h-吡唑-4-基)-5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶;
[0437]
6-甲氧基-5-(2-甲基-3-(甲基-d3)苯基)-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶;
[0438]
1-(4-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)哌啶-1-基)乙-1-酮;
[0439]
4-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)哌啶-1-羧酸甲酯;
[0440]
3-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸甲酯;和
[0441]
3-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-n,n-二甲基氮杂环丁烷-1-羧酰胺;
[0442]
或前述任一种的药学上可接受的盐。
[0443]
在一些实施方案中,本文提供选自以下的化合物:
1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇;
[0464]
(7r,8as)-2-(5-(5-(2-环丙基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇;
[0465]
(7r,8as)-2-(5-(5-(色满-5-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇;
[0466]
(7r,8as)-2-(5-(5-(2-氟-3-甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇;
[0467]
4-(6-甲氧基-3-(6-(2-甲氧基乙氧基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚;
[0468]
4-(6-甲氧基-3-(6-((四氢-2h-吡喃-4-基)氧基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚;
[0469]
4-(3-(6-环丙基吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚;和
[0470]
n-(1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-3-基)-2-羟基-n-甲基乙酰胺;
[0471]
或前述任一种的药学上可接受的盐。
[0472]
在一些实施方案中,本文提供选自以下的化合物:
[0473]
1-(4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-基)乙-1-酮;
[0474]
1-(4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-基)-2-羟基乙-1-酮;
[0475]
1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)-2-羟基乙-1-酮(峰1);
[0476]
1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)-2-羟基乙-1-酮(峰2);
[0477]
1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)乙-1-酮(峰1);
[0478]
1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)乙-1-酮(峰2);
[0479]
3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-[1,3
’‑
联吡咯烷]-2
’‑
酮(峰1);
[0480]
3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1
’‑
甲基-[1,3
’‑
联吡咯烷]-2
’‑
酮(峰1);
[0481]
2-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)丙酰胺(峰1);
[0482]
5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(6-(1-(甲基-l-脯氨酰基)哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶;
[0483]
(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)((r)-4-甲基吗啉-3-基)甲酮(峰2);
基)-1h-吡唑-1-基)吡咯烷-1-基)-2-羟基乙-1-酮;
[0504]
(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(四氢呋喃-2-基)甲酮;
[0505]
(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(四氢呋喃-3-基)甲酮;
[0506]
(r)-1-((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)-2-羟基丙-1-酮;
[0507]
(s)-1-((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)-2-羟基丙-1-酮;
[0508]
(r)-1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-3-羟基丁-1-酮;
[0509]
(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)((1r,3r)-3-羟基-3-甲基环丁基)甲酮;
[0510]
(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)((1s,3s)-3-羟基-3-甲基环丁基)甲酮;
[0511]
((r)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)((s)-4-甲基吗啉-3-基)甲酮;
[0512]
((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)((r)-4-甲基吗啉-3-基)甲酮;
[0513]
(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(1-(羟基甲基)环丁基)甲酮;
[0514]
(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(1-乙基氮杂环丁-2-基)甲酮;
[0515]
(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(1-(2-氟乙基)氮杂环丁-2-基)甲酮;
[0516]
(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(1-异丙基氮杂环丁-2-基)甲酮;
[0517]
((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)((s)-1-(2-氟乙基)氮杂环丁-2-基)甲酮;
[0518]
((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)((反)-3-羟基环丁基)甲酮;
[0519]
((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)((顺)-3-羟基环丁基)甲酮;
[0520]
((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)((1s,3r)-3-羟基-3-甲基环丁基)甲酮;
[0521]
1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-2-甲氧基乙-1-酮;
[0522]
1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-2-(二甲基氨基)-2-甲基丙-1-酮;
1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈;
[0543]
4-(6-甲氧基-3-(1-((s)-1-((s)-四氢呋喃-2-羰基)吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈;
[0544]
(7r,8as)-2-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇;
[0545]
n-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-3-基)-2-羟基-n-甲基乙酰胺;
[0546]
(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)(四氢呋喃-2-基)甲酮;
[0547]
(s)-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)(1-甲基哌啶-2-基)甲酮;
[0548]
1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)-2-(二甲基氨基)乙-1-酮;
[0549]
1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)-3-羟基丙-1-酮;
[0550]
1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)-2-羟基乙-1-酮;
[0551]
(s)-1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)-2-羟基丙-1-酮;
[0552]
n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环丁基)-2-羟基-n-甲基乙酰胺;
[0553]
1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基-3-d)-2-羟基乙-1-酮;
[0554]
4-(5-(5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-羧酸甲酯;
[0555]
4-(6-甲氧基-3-(6-(1-(吗啉-4-羰基)哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈,峰2;
[0556]
4-(3-(6-(1-乙酰基哌啶-4-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈,峰2;
[0557]
4-(3-(6-(1-乙酰基吡咯烷-3-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈;
[0558]
4-(6-甲氧基-3-(6-(1-(吗啉-4-羰基)吡咯烷-3-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈;
[0559]
4-(3-(1-(氰基甲基)-1h-吡唑-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈;
[0560]
4-(6-甲氧基-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈;
[0561]
3-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)丙腈;
[0562]
n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环丁基)-2-甲氧基-n-甲基乙酰胺;
[0563]
n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环丁基)-3-羟基-n-甲基丙酰胺;
[0564]
(s)-n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环丁基)-2-羟基-n-甲基丙酰胺;
[0565]
1-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)-2-羟基乙-1-酮;
[0566]
(r)1-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)-2-羟基乙-1-酮,两种对映体;
[0567]
(s)1-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)-2-羟基乙-1-酮,两种对映体;
[0568]
(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基))((r)-4-甲基吗啉-3-基)甲酮;
[0569]
5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(6-(3-(四氢-2h-吡喃-4-基)-3-氮杂双环[3.1.0]己-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[0570]
2-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)乙-1-醇;
[0571]
(r)2-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)乙-1-醇,两种对映体;
[0572]
(s)2-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)乙-1-醇,两种对映体;
[0573]
3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-((r)-4-甲基吗啉-3-羰基)吡咯烷-3-甲腈;
[0574]
(r)-4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-(4-甲基吗啉-3-羰基)哌啶-4-甲腈;
[0575]
1-(1-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-3-氮杂双环[3.1.0]己-3-基)-2-羟基乙-1-酮;
[0576]
3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-(2-羟基乙酰基)吡咯烷-3-甲腈;
[0577]
(s)-4-((5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)甲基)-1,3-二甲基哌嗪-2-酮;和
[0578]
(1r,4r)-5-((5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)甲基)-2-氧杂-5-氮杂双环[2.2.1]庚烷;
[0579]
或前述任一种的药学上可接受的盐。
[0580]
应进一步理解,出于清晰目的在单独实施方案的情形下描述的本发明的某些特征也可组合提供于单一实施方案中。相反,出于简洁目的在单一实施方案的情形下描述的本发明的各种特征也可单独地或以任何合适的子组合提供。
[0581]
在本说明书中的不同地方,本发明化合物的取代基以分组或以范围形式公开。明
确意图本发明包括此类组和范围的成员的每一种个别子组合。例如,术语“c
1-6
烷基”明确意图个别地公开甲基、乙基、c3烷基、c4烷基、c5烷基和c6烷基。
[0582]
在本说明书中的不同地方,描述了各种芳基、杂芳基、环烷基和杂环烷基环。除非另外规定,否则这些环可在化合价允许的情况下在任何环成员处连接至所述分子的其余部分。例如,术语“吡啶环”或“吡啶基”可指吡啶-2-基、吡啶-3-基或吡啶-4-基环。
[0583]
术语“n元”(其中n是整数)通常描述部分中的成环原子的数目,其中成环原子的数目是n。例如,哌啶基是6元杂环烷基环的实例,吡唑基是5元杂芳基环的实例,吡啶基是6元杂芳基环的实例,并且1,2,3,4-四氢-萘是10元环烷基的实例。
[0584]
关于其中变量出现超过一次的本发明化合物,每个变量可以是独立地选自定义所述变量的组的不同部分。例如,在描述具有同时存在于同一化合物上的两个r基团的结构时,所述两个r基团可表示独立地选自针对r定义的组的不同部分。
[0585]
如本文所用,短语“任选地被取代”表示未被取代或被取代。
[0586]
术语“被取代”意指原子或原子团作为连接至另一个基团的“取代基”在形式上替换氢。除非另外指定,否则术语“被取代”是指其中允许此取代的任何取代水平,例如单取代、二取代、三取代、四取代或五取代。取代基是独立选择的,并且取代可在任何化学上可接近的位置处。应理解,在给定原子处的取代受到化合价限制。应理解,在给定原子处的取代产生化学稳定分子。单一二价取代基(例如氧代)可替换两个氢原子。
[0587]
如本文所用,与化学基团组合使用的术语“c
i-j”(其中i和j是整数)指明所述化学基团中的碳原子数目的范围,其中i-j定义所述范围。例如,c
1-6
烷基是指具有1、2、3、4、5或6个碳原子的烷基。
[0588]
如本文所用,单独或与其他术语组合使用的术语“烷基”是指饱和烃基,其可以是直链或支链。烷基在形式上对应于其中一个c-h键被烷基与化合物的剩余部分的连接点替换的烷烃。在一些实施方案中,烷基含有1至6个、1至4个或1至3个碳原子。烷基部分的实例包括但不限于诸如甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、2-甲基-1-丁基、3-戊基、正己基、1,2,2-三甲基丙基等的化学基团。在一些实施方案中,烷基是甲基、乙基或丙基。
[0589]
如本文所用,单独或与其他术语组合使用的术语“c
i-j
亚烷基”表示具有i至j个碳的饱和二价连接烃基团,其可以是直链或支链。在一些实施方案中,亚烷基含有1至4个碳原子、1至3个碳原子或1至2个碳原子。亚烷基部分的实例包括但不限于诸如亚甲基、亚乙基、1,1-亚乙基、1,2-亚乙基、1,3-亚丙基、1,2-亚丙基、1,1-亚丙基、异亚丙基等的化学基团。
[0590]
如本文所用,单独或与其他术语组合使用的“烯基”是指对应于具有一个或多个碳-碳双键的烷基的直链或支链烃基团。烯基在形式上对应于其中一个c-h键被烯基与化合物的剩余部分的连接点替换的烯烃。在一些实施方案中,烯基部分含有2至6个或2至4个碳原子。实例烯基包括但不限于乙烯基、正丙烯基、异丙烯基、正丁烯基、仲丁烯基等。
[0591]
如本文所用,单独或与其他术语组合使用的“炔基”是指对应于具有一个或多个碳-碳三键的烷基的直链或支链烃基团。炔基在形式上对应于其中一个c-h键被烷基与化合物的剩余部分的连接点替换的炔烃。在一些实施方案中,炔基部分含有2至6个或2至4个碳原子。实例炔基包括但不限于乙炔基、丙炔-1-基、丙炔-2-基等。
[0592]
如本文所用,单独或与其他术语组合使用的“卤基”或“卤素”包括氟基、氯基、溴基
和碘基。在一些实施方案中,卤基是f或cl。在一些实施方案中,卤基是f。
[0593]
如本文所用,单独或与其他术语组合使用的术语“卤代烷基”是指其中一个或多个氢原子已被卤素原子替换的烷基,具有至多卤素原子取代基的全价,所述取代基可以是相同或不同的。在一些实施方案中,卤素原子是氟原子。在一些实施方案中,烷基具有1至6个、1至4个或1至3个碳原子。实例卤代烷基包括cf3、c2f5、chf2、ccl3、chcl2、c2cl5等。
[0594]
如本文所用,单独或与其他术语组合使用的术语“烷氧基”是指式-o-烷基的基团。在一些实施方案中,烷基具有1至6个、1至4个或1至3个碳原子。实例烷氧基包括甲氧基、乙氧基、丙氧基(例如正丙氧基和异丙氧基)、叔丁氧基等。在一些实施方案中,烷氧基是甲氧基。
[0595]
如本文所用,单独或与其他术语组合使用的“卤代烷氧基”是指式-o-(卤代烷基)的基团。在一些实施方案中,烷基具有1至6个、1至4个或1至3个碳原子。实例卤代烷氧基是-ocf3。
[0596]
如本文所用,单独或与其他术语组合使用的“氨基”是指nh2。
[0597]
如本文所用,单独或与其他术语组合使用的术语“烷基氨基”是指式-nh(烷基)的基团。在一些实施方案中,烷基氨基具有1至6个或1至4个碳原子。实例烷基氨基包括甲基氨基、乙基氨基、丙基氨基(例如正丙基氨基和异丙基氨基)等。
[0598]
如本文所用,单独或与其他术语组合使用的术语“二烷基氨基”是指式-n(烷基)2的基团。实例二烷基氨基包括二甲基氨基、二乙基氨基、二丙基氨基(例如二(正丙基)氨基和二(异丙基)氨基)等。在一些实施方案中,每个烷基独立地具有1至6个或1至4个碳原子。
[0599]
如本文所用,单独或与其他术语组合使用的术语“烷基硫基”是指式-s-烷基的基团。在一些实施方案中,烷基具有1至6个或1至4个碳原子。
[0600]
如本文所用,单独或与其他术语组合使用的术语“环烷基”是指非芳族环烃,包括环状烷基和烯基。术语“c
n-m
环烷基”是指具有n至m个环成员碳原子的环烷基。环烷基可包括单环或多环(例如,具有2、3或4个稠合、桥联或螺环)环系。环烷基的定义中还包括具有稠合(即,共同具有一个键)至环烷基环的一个或多个芳环(例如芳基或杂芳基环)的部分,例如环戊烷、环己烯、环己烷等的苯并衍生物,或环戊烷或环己烷的吡啶并衍生物。含有稠合芳环的环烷基可通过任何成环原子(包括稠合芳环的成环原子)进行连接。环烷基的成环碳原子可任选地被氧代取代。环烷基还包括亚环烷基。术语“环烷基”还包括桥头环烷基(例如含有至少一个桥头碳的非芳族环烃部分,诸如金刚烷-1-基)和螺环烷基(例如含有在单一碳原子处稠合的至少两个环的非芳族烃部分,诸如螺[2.5]辛烷等)。在一些实施方案中,环烷基具有3至10个环成员或3至7个环成员或3至6个环成员。在一些实施方案中,环烷基是单环或双环。在一些实施方案中,环烷基是单环。在一些实施方案中,环烷基是c
3-7
单环环烷基。实例环烷基包括环丙基、环丁基、环戊基、环己基、环庚基、环戊烯基、环己烯基、环己二烯基、环庚三烯基、降冰片基、降蒎烷基(norpinyl)、降蒈烷基(norcarnyl)、四氢萘基、八氢萘基、茚满基等。在一些实施方案中,环烷基是环丙基、环丁基、环戊基或环己基。
[0601]
如本文所用,单独或与其他术语组合使用的术语“杂环烷基”是指非芳族环或环系,其可任选地含有一个或多个亚烯基或亚炔基作为环结构的部分,其具有独立地选自氮、硫、氧和磷的至少一个杂原子环成员,并且其具有4-14个环成员、4-10个环成员、4-7个环成员或4-6个环成员。术语“杂环烷基”内包括单环4元、5元、6元和7元杂环烷基。杂环烷基可包
噁二唑基、1,2,4-三唑基、1,2,4-噻二唑基、1,2,4-噁二唑基、1,3,4-三唑基、1,3,4-噻二唑基和1,3,4-噁二唑基。
[0606]
六元杂芳基环是具有六个环原子的杂芳基,其中一个或多个(例如,1、2或3个)环原子独立地选自n、o和s。示例性六元环杂芳基是吡啶基、吡嗪基、嘧啶基、三嗪基、异吲哚基和哒嗪基。
[0607]
术语“氧代”是指作为二价取代基的氧原子,当连接至碳时形成羰基,或连接至杂原子时形成亚砜或砜基团或n-氧化物基团。在一些实施方案中,杂环基可任选地被1或2个氧代(=o)取代基取代。
[0608]
关于成环n原子的术语“氧化的”是指成环n-氧化物。
[0609]
关于成环s原子的术语“氧化的”是指成环磺酰基或成环亚硫酰基。
[0610]
术语“芳族”是指具有一个或多个具有芳族性(即,具有(4n+2)个离域π(pi)电子,其中n是整数)的多不饱和环的碳环或杂环。
[0611]
在某些地方,所述定义或实施方案是指特定环(例如,氮杂环丁烷环、吡啶环等)。除非另外指定,否则这些环可连接至任何环成员,其条件在于不超过原子的化合价。例如,氮杂环丁烷环可在环的任何位置处进行连接,而氮杂环丁-3-基环是在3-位置处进行连接。
[0612]
本文所述的化合物可以是不对称的(例如,具有一个或多个立体中心)。除非另外指定,否则预期所有立体异构体,诸如对映体和非对映体。含有不对称取代的碳原子的本发明化合物可以光学活性或外消旋形式分离。本领域已知关于如何由光学无活性起始材料制备光学活性形式的方法,诸如通过外消旋混合物的拆分或通过立体选择性合成。烯烃、c=n双键等的多种几何异构体也可存在于本文所述的化合物中,并且所有此类稳定异构体均涵盖于本发明中。本发明化合物的顺式和反式几何异构体被描述并且可作为异构体的混合物或作为分离的异构体形式被分离。
[0613]
化合物的外消旋混合物的拆分可通过本领域已知的方法进行。实例方法包括使用对手性拆分酸的分级重结晶,所述手性拆分酸是光学活性、成盐有机酸。用于分级重结晶方法的合适拆分剂是例如光学活性酸,诸如酒石酸、二乙酰基酒石酸、二苯甲酰基酒石酸、扁桃酸、苹果酸、乳酸或各种光学活性樟脑磺酸的d和l形式。适用于分级结晶方法的其他拆分剂包括甲基苄胺(例如s和r形式,或非对映异构体纯形式)、2-苯基甘氨醇、去甲麻黄碱、麻黄碱、n-甲基麻黄碱、环己基乙胺、1,2-二氨基环己烷等的立体异构纯形式。
[0614]
外消旋混合物的拆分还可通过在用光学活性拆分剂(例如二硝基苯甲酰基苯基甘氨酸)填充的柱上洗脱来进行。合适的洗脱溶剂组成可由本领域技术人员测定。
[0615]
在一些实施方案中,本发明化合物具有(r)-构型。在其他实施方案中,化合物具有(s)-构型。在具有多于一个手性中心的化合物中,除非另外指定,否则化合物中的每个手性中心可独立地是(r)或(s)。
[0616]
本发明化合物还包括互变异构形式。互变异构形式由于用相邻双键交换单键以及质子的伴随迁移形成。互变异构形式包括质子移变互变异构体,其是具有相同实验式和总电荷的异构质子化状态。实例质子移变互变异构体包括酮-烯醇对、酰胺-亚胺酸对、内酰胺-内酰亚胺对、烯胺-亚胺对,及其中质子可占据杂环系的两个或更多个位置的环状形式(例如,1h-和3h-咪唑、1h-、2h-和4h-1,2,4-三唑、1h-和2h-异吲哚和1h-和2h-吡唑)。互变异构形式可处于平衡状态或通过适当取代在空间上锁定为一种形式。
[0617]
本发明化合物还包括存在于中间体或最终化合物中的原子的所有同位素。同位素包括具有相同原子序数但具有不同质量数的那些原子。例如,氢的同位素包括氚和氘。本发明化合物的一个或多个组成原子可被具有天然或非天然丰度的原子同位素替换或取代。在一些实施方案中,化合物包括至少一个氘原子。例如,本发明化合物中的一个或多个氢原子可被氘替换或取代。在一些实施方案中,化合物包括两个或更多个氘原子。在一些实施方案中,化合物包括1、2、3、4、5、6、7、8、9、10、11或12个氘原子。用于将同位素包括在有机化合物中的合成方法是本领域已知的(deuterium labeling in organic chemistry,alan f.thomas(new york,n.y.,appleton-century-crofts,1971;the renaissance of h/d exchange,jens atzrodt,volker derdau,thorsten fey和jochen zimmermann,angew.chem.int.ed.2007,7744-7765;the organic chemistry of isotopic labelling,james r.hanson,royal society of chemistry,2011)。同位素标记化合物可用于各种研究,诸如nmr光谱法、代谢实验和/或测定。
[0618]
用诸如氘的较重同位素取代可提供由较大代谢稳定性引起的某些治疗优势,例如增加的体内半衰期或降低的剂量需求,并且因此可在一些情况下是优选的。(a.kerekes等人j.med.chem.2011,54,201-210;r.xu等人j.label compd.radiopharm.2015,58,308-312)。
[0619]
如本文所用,术语“化合物”意在包括所描绘的结构的所有立体异构体、几何异构体、互变异构体和同位素。所述术语还意在指本发明化合物,无论其如何制备,例如以合成方式、通过生物过程(例如代谢或酶转化)或其组合。
[0620]
所有化合物及其药学上可接受的盐可与诸如水和溶剂的其他物质一起发现(例如,呈水合物和溶剂化物形式),或可被分离。当呈固态时,本文所述的化合物及其盐可以各种形式出现并且可例如采用溶剂化物的形式,包括水合物。化合物可呈任何固态形式,诸如多晶型物或溶剂化物,因此除非另外清楚地指定,否则本说明书中对于化合物及其盐的提及应理解为涵盖所述化合物的任何固态形式。
[0621]
在一些实施方案中,本发明化合物或其盐实质上被分离。“实质上被分离”表示化合物至少部分地或实质上从其中形成或检测到所述化合物的环境中分离。部分分离可包括例如本发明化合物富集的组合物。实质性分离可包括含有按重量计至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约97%或至少约99%本发明化合物或其盐的组合物。用于分离化合物及其盐的方法是本领域常规的。
[0622]
短语“药学上可接受的”在本文中用于指在合理医学判断的范围内适于与人和动物组织接触使用而无过量毒性、刺激、过敏反应或其他问题或并发症,与合理效益/风险比相称的那些化合物、材料、组合物和/或剂型。
[0623]
本发明还包括本文所述的化合物的药学上可接受的盐。如本文所用,“药学上可接受的盐”是指所公开的化合物的衍生物,其中亲本化合物通过将现有酸或碱部分转化为其盐形式来修饰。药学上可接受的盐的实例包括但不限于诸如胺的碱性残基的无机或有机酸盐;诸如羧酸的酸性残基的碱金属或有机盐;等。本发明的药学上可接受的盐包括例如由无毒无机或有机酸形成的母体化合物的无毒盐。本发明的药学上可接受的盐可通过常规化学方法由含有碱性或酸性部分的母体化合物合成。一般而言,此类盐可通过使这些化合物的游离酸或碱形式与化学计量的量的适当碱或酸在水中或在有机溶剂中或在两者的混合物
中反应来制备;一般而言,非水性介质是优选的,如醚、乙酸乙酯、醇(例如甲醇、乙醇、异丙醇或丁醇)或乙腈(acn)。合适盐的清单可在remington’s pharmaceutical sciences,第17版,mack publishing company,easton,pa.,1985,第1418页和journal of pharmaceutical science,66,2(1977)中找到,所述文献中每一个均以引用的方式整体并入本文。
[0624]
以下缩写可用于本文中:acoh(乙酸);ac2o(乙酸酐);aq.(水溶液);atm.(大气压);boc(叔丁氧基羰基);br(宽);cbz(羧基苄基);calc.(计算);d(双重峰);dd(双重峰的双重峰);dcm(二氯甲烷);dead(偶氮二羧酸二乙酯);diad(n,n
’‑
叠氮基二羧酸二异丙酯);dipea(n,n-二异丙基乙胺);dmf(n,n-二甲基甲酰胺);et(乙基);etoac(乙酸乙酯);g(克);h(小时);hatu(n,n,n’,n
’‑
四甲基-o-(7-氮杂苯并三唑-1-基)脲六氟磷酸盐);hcl(盐酸);hplc(高效液相色谱);hz(赫兹);j(耦合常数);lcms(液相色谱
–
质谱分析);m(多重峰);m(摩尔浓度);mcpba(3-氯过氧苯甲酸);mgso4(硫酸镁);ms(质谱分析);me(甲基);mecn(乙腈);meoh(甲醇);mg(毫克);min.(分钟);ml(毫升);mmol(毫摩尔);n(当量浓度);nahco3(碳酸氢钠);naoh(氢氧化钠);na2so4(硫酸钠);nh4cl(氯化铵);nh4oh(氢氧化铵);nis(n-碘代琥珀酰亚胺);nm(纳摩尔浓度);nmr(核磁共振光谱法);otf(三氟甲烷磺酸盐);pd(钯);ph(苯基);pm(皮摩尔浓度);pmb(对甲氧基苄基),pocl3(磷酰氯);rp-hplc(反相高效液相色谱);s(单峰);sem(2-三甲基甲硅烷基乙氧基甲基);t(三重峰或第三);tbs(叔丁基二甲基甲硅烷基);tert(第三);tt(三重峰的三重峰);t-bu(叔丁基);tfa(三氟乙酸);thf(四氢呋喃);μg(微克);μl(微升);μm(微摩尔浓度);wt%(重量百分比)。
[0625]
合成
[0626]
本发明化合物(包括其盐)可使用已知的有机合成技术并且根据各种可能合成途径来制备。
[0627]
用于制备本发明化合物的反应可在可容易地由有机合成领域的技术人员选择的合适溶剂中进行。合适溶剂可实质上不与起始材料(反应物)、中间体或产物在进行反应的温度,例如可介于溶剂的凝固温度至溶剂的沸腾温度范围内的温度下反应。给定反应可在一种溶剂或多于一种溶剂的混合物中进行。取决于特定反应步骤,用于特定反应步骤的合适溶剂可由本领域技术人员选择。
[0628]
本发明化合物的制备可涉及各种化学基团的保护和脱保护。对于保护和脱保护的需要和适当保护基的选择可容易地由本领域技术人员确定。保护基的化学性质可在例如t.w.greene和p.g.m.wuts,protective groups in organic synthesis,第3版,wiley&sons,inc.,new york(1999)中找到,所述文献以引用的方式整体并入本文。
[0629]
反应可根据本领域已知的任何合适方法进行监测。例如,产物形成可通过光谱手段,诸如核磁共振光谱法(例如1h或
13
c)、红外光谱法、分光光度法(例如uv-可见光)或质谱分析,或通过色谱,诸如高效液相色谱(hplc)或薄层色谱进行监测。
[0630]
如本文所用,表述“环境温度”、“室温”和“室温(室温)”是本领域所理解的,并且一般是指约为其中进行反应的房间的温度的温度,例如反应温度,例如约20℃至约30℃温度。
[0631]
在位置cy1处具有多种取代的式(i)化合物可使用如方案1中说明的过程制备。在方案1中描绘的过程中,式1-1化合物中的卤基取代基可经历交叉偶联反应,包括铃木(suzuki)(tetrahedron 2002,58,9633-9695)(例如,在诸如xphos pd g2的钯催化剂和诸
如磷酸钾的碱存在下)、negishi(acs catalysis 2016,6,1540-1552)或stille(acs catalysis 2015,5,3040-3053)(例如,在诸如四(三苯基膦)钯(0)的钯(0)催化剂存在下)等,以得到式1-2化合物。式1-2化合物中的保护基可在酸性条件(例如,在tfa或hcl存在下)去除以得到式1-3化合物。这些化合物可进一步用一种卤化剂(例如nis或碘)卤化,随后用合适保护基(例如boc)进行nh保护,以得到式1-4化合物。包括铃木(例如,在诸如xphos pd g2的钯催化剂和诸如磷酸钾的碱存在下)、negishi或stille(例如,在诸如四(三苯基膦)钯(0)的钯(0)催化剂存在下)在内的1-4的交叉偶联反应、随后保护基的脱保护会得到式(i)化合物。
[0632]
方案1
[0633][0634]
可选地,式(i)化合物可使用如方案2中说明的过程制备。式1-1化合物中的保护基可在酸性条件(例如,在tfa或hcl存在下)去除以得到式2-1化合物。这些化合物可用一种碘化剂(例如nis或碘)碘化,随后用合适保护基(例如boc)进行nh保护,以得到式2-2化合物。包括铃木(例如,在诸如pd(dppf)cl2的钯催化剂和诸如磷酸钾的碱存在下)在内的2-2的交叉偶联反应导致形成式2-3化合物。包括铃木(例如,在诸如xphos pd g2的钯催化剂和诸如磷酸钾的碱存在下)、negishi或stille(例如,在诸如四(三苯基膦)钯(0)的钯(0)催化剂存在下)在内的2-3的第二交叉偶联反应、随后保护基的脱保护会得到式(i)化合物。
[0635]
方案2
[0636][0637]
使用方法
[0638]
本发明化合物可抑制fgfr酶的活性。例如,本发明化合物可通过向需要fgfr酶的抑制的细胞、个体或患者施用抑制量的一种或多种本公开化合物而用于抑制细胞中或个体或患者中酶的活性。本发明化合物可通过向需要fgfr3酶的抑制的细胞、个体或患者施用抑制量的一种或多种本发明化合物而用于抑制细胞中或个体或患者中酶的活性。本发明化合物可通过向需要fgfr2酶的抑制的细胞、个体或患者施用抑制量的一种或多种本发明化合物而用于抑制细胞中或个体或患者中酶的活性。本发明化合物可通过向需要fgfr3和fgfr2酶的抑制的细胞、个体或患者施用抑制量的本发明化合物而用于抑制细胞中或个体或患者中酶的活性。
[0639]
在一些实施方案中,相对于fgfr1,本公开化合物对酶fgfr3具有选择性抑制活性。在一些实施方案中,相对于fgfr1,本公开化合物对fgfr3的选择性为10倍至25倍或25倍至50倍。在一些实施方案中,相对于fgfr4,本公开化合物对酶fgfr3具有选择性抑制活性。在一些实施方案中,相对于fgfr4,本公开化合物对fgfr3的选择性为10倍至25倍、25倍至50倍或50倍至100倍。在一些实施方案中,相对于fgfr2,本公开化合物对酶fgfr3具有选择性抑制活性。在一些实施方案中,相对于fgfr2,本公开化合物对fgfr3的选择性为1.5倍至2倍或2倍至3倍。
[0640]
在一些实施方案中,相对于us2018/0072718的化合物对fgfr3的抑制活性,实施例1至98的化合物对fgfr3的抑制活性为10倍或10倍以上,例如50倍、100倍、250倍、500倍、750倍、1000倍等。
[0641]
在一些实施方案中,相对于fgfr1,本公开化合物对酶fgfr3具有选择性抑制活性。不受特定理论约束,认为fgfr1与某些副作用,诸如fgfr1驱动性低磷酸盐血症相关。相对于非选择性fgfr抑制剂(例如,针对例如fgfr1和fgfr3两者具有类似抑制活性的化合物),本公开化合物可以是有利的,因为本公开化合物具有几乎无fgfr1驱动性低磷酸盐血症副作用的潜力,并且潜在地允许较高最大剂量,同时避免了与fgfr1相关的副作用。
[0642]
在一些实施方案中,相对于fgfr1,本公开化合物对酶fgfr2具有选择性抑制活性。在一些实施方案中,相对于fgfr1,本公开化合物对fgfr2的选择性为10倍至25倍或25倍至50倍。在一些实施方案中,相对于fgfr4,本公开化合物对酶fgfr2具有选择性抑制活性。在
一些实施方案中,相对于fgfr4,本公开化合物对fgfr2的选择性为10倍至25倍、25倍至50倍或50倍至100倍。
[0643]
作为fgfr抑制剂,本公开化合物可用于治疗与fgfr酶或fgfr配体的异常表达或活性相关的各种疾病。抑制fgfr的化合物将可用于提供一种预防肿瘤的生长或诱导细胞凋亡的手段,尤其通过抑制血管生成。因此,预期本公开化合物将证明可用于治疗或预防增生性病症,诸如癌症。具体地说,具有受体酪氨酸激酶的激活性突变体或受体酪氨酸激酶的上调的肿瘤可对所述抑制剂尤其敏感。
[0644]
在某些实施方案中,本发明提供一种用于治疗有需要的患者的fgfr介导的病症的方法,其包括向所述患者施用根据本发明的化合物或其药学上可接受的组合物的步骤。
[0645]
在一些实施方案中,可使用本公开化合物治疗的疾病和适应症包括但不限于血液学癌症、肉瘤、肺癌、胃肠癌、泌尿生殖道癌症、肝癌、骨癌、神经系统癌症、妇科癌症和皮肤癌。
[0646]
在一些实施方案中,可使用本公开化合物治疗的癌症选自腺癌、膀胱癌、乳腺癌、子宫颈癌、胆管癌、结肠直肠癌、子宫内膜癌、食道癌、胆囊癌、胃癌、神经胶质瘤、头颈部癌、肝细胞癌、肾癌、肝癌、肺癌、黑色素瘤、卵巢癌、胰腺癌、前列腺癌、横纹肌肉瘤、皮肤癌、甲状腺癌、白血病、多发性骨髓瘤、慢性淋巴细胞性淋巴瘤、成人t细胞白血病、b-细胞淋巴瘤、急性骨髓性白血病、霍奇金氏或非霍奇金氏淋巴瘤(hodgkin’s or non-hodgkin’s lymphoma)、华氏巨球蛋白血症(waldenstrom's macroglubulinemia)、毛细胞淋巴瘤和伯基特氏淋巴瘤(burkett's lymphoma)。
[0647]
在一些实施方案中,可使用本公开化合物治疗的癌症选自肝细胞癌、膀胱癌、乳腺癌、子宫颈癌、结肠直肠癌、子宫内膜癌、胃癌、头颈部癌、肾癌、肝癌、肺癌、卵巢癌、前列腺癌、食道癌、胆囊癌、胰腺癌、甲状腺癌、皮肤癌、白血病、多发性骨髓瘤、慢性淋巴细胞性淋巴瘤、成人t细胞白血病、b-细胞淋巴瘤、急性骨髓性白血病、霍奇金氏或非霍奇金氏淋巴瘤、华氏巨球蛋白血症、毛细胞淋巴瘤、伯基特氏淋巴瘤、胶质母细胞瘤、黑色素瘤和横纹肉瘤。
[0648]
在一些实施方案中,所述癌症选自腺癌、膀胱癌、乳腺癌、子宫颈癌、胆管癌、子宫内膜癌、胃癌、神经胶质瘤、头颈部癌、肺癌、卵巢癌、白血病和多发性骨髓瘤。
[0649]
在一些实施方案中,可使用本公开化合物治疗的癌症选自肝细胞癌、乳腺癌、膀胱癌、结肠直肠癌、黑色素瘤、间皮瘤、肺癌、前列腺癌、胰腺癌、睾丸癌、甲状腺癌、鳞状细胞癌、胶质母细胞瘤、神经母细胞瘤、子宫癌和横纹肉瘤。
[0650]
特征为fgfr2和/或fgfr3改变的癌症包括膀胱癌(fgfr3突变或融合)、胆管癌(fgfr2融合)和胃癌(fgfr2扩增)。
[0651]
本公开化合物可用于治疗具有fgfr2/3改变包括突变、融合、重排和扩增)的癌症患者。fgfr2/3改变发现于胆管癌、尿道上皮癌、多发性骨髓瘤、胃腺癌、神经胶质瘤、子宫内膜癌、卵巢癌、子宫颈癌、肺癌和乳腺癌的子集中。此外,本公开化合物可用于靶向归因于获得守门突变(fgfr3中的v555m/l/f/i、fgfr2中的v564m/l/f/i)而关于泛fgfr抑制剂治疗取得进展的患者。本公开化合物还可用于治疗其中fgfr2/3信号传导涉及对其他靶向疗法的抗性的癌症,例如其在er阳性乳腺癌中具有克服cdk4/6抑制剂抗性的潜力。
[0652]
示例性血液学癌症包括淋巴瘤和白血病,诸如急性淋巴母细胞性白血病(all)、急
性骨髓性白血病(aml)、急性早幼粒细胞性白血病(apl)、慢性淋巴细胞性白血病(cll)、慢性骨髓性白血病(cml)、弥漫性大b-细胞淋巴瘤(dlbcl)、套细胞淋巴瘤、非霍奇金淋巴瘤(包括复发性或难治性nhl和复发性滤泡性)、霍奇金淋巴瘤、骨髓增生性疾病(例如原发性骨髓纤维化(pmf)、真性红细胞增多症(pv)、原发性血小板增多症(et)、8p11骨髓增生性综合征)、骨髓发育不良综合征(mds)、t-细胞急性淋巴母细胞性淋巴瘤(t-all)、多发性骨髓瘤、皮肤t-细胞淋巴瘤、成人t-细胞白血病、华氏巨球蛋白血症、毛细胞淋巴瘤、边缘区淋巴瘤、慢性骨髓性淋巴瘤和伯基特氏淋巴瘤。
[0653]
示例性肉瘤包括软骨肉瘤、尤文氏肉瘤(ewing’s sarcoma)、骨肉瘤、横纹肌肉瘤、血管肉瘤、纤维肉瘤、脂肪肉瘤、粘液瘤、横纹肌瘤、横纹肉瘤、纤维瘤、脂肪瘤、错构瘤、淋巴肉瘤、平滑肌肉瘤和畸胎瘤。
[0654]
示例性肺癌包括非小细胞肺癌(nsclc)、小细胞肺癌、支气管源性癌瘤(鳞状细胞、未分化性小细胞、未分化性大细胞、腺癌)、肺泡(支气管)癌、支气管腺瘤、软骨瘤性错构瘤、间皮瘤、小细胞性和非小细胞性癌瘤、支气管腺瘤和胸膜肺母细胞瘤。
[0655]
示例性胃肠癌包括食道癌(鳞状细胞癌、腺癌、平滑肌肉瘤、淋巴瘤)、胃癌(癌瘤、淋巴瘤、平滑肌肉瘤)、胰腺癌(外分泌性胰腺癌、导管腺癌、胰岛素瘤、胰高血糖素瘤、促胃液素瘤、类癌瘤、血管活性肠肽瘤)、小肠癌(腺癌、淋巴瘤、类癌瘤、卡波西氏肉瘤(kaposi'ssarcoma)、平滑肌瘤、血管瘤、脂肪瘤、纤维神经瘤、纤维瘤)、大肠癌(腺癌、管状腺瘤、绒毛状腺瘤、错构瘤、平滑肌瘤)、结肠直肠癌、胆囊癌和肛门癌。
[0656]
示例性泌尿生殖道癌包括肾癌(腺癌、威尔姆氏肿瘤(wilm's tumor)[肾母细胞瘤]、肾细胞癌)、膀胱和尿道癌(鳞状细胞癌、移行细胞癌、腺癌)、前列腺癌(腺癌、肉瘤)、睾丸癌(精原细胞瘤、畸胎瘤、胚胎癌、畸胎癌、绒膜癌、肉瘤、间质细胞癌、纤维瘤、纤维腺瘤、腺瘤样肿瘤、脂肪瘤)和尿道上皮癌。
[0657]
示例性肝癌包括肝细胞瘤(肝细胞癌)、胆管癌、肝胚细胞瘤、血管肉瘤、肝细胞腺瘤和血管瘤。
[0658]
示例性骨癌包括例如骨源性肉瘤(骨肉瘤)、纤维肉瘤、恶性纤维性组织细胞瘤、软骨肉瘤、尤文氏肉瘤、恶性淋巴瘤(网状细胞肉瘤)、多发性骨髓瘤、恶性巨细胞肿瘤脊索瘤、骨软骨瘤(骨软骨性外生骨疣)、良性软骨瘤、软骨母细胞瘤、软骨粘液样纤维瘤、骨样骨瘤和巨细胞肿瘤
[0659]
示例性神经系统癌症包括颅骨癌(骨瘤、血管瘤、肉芽肿、黄瘤、畸形性骨炎)、脑膜癌(脑膜瘤、脑膜肉瘤、神经胶质瘤病)、脑癌(星形细胞瘤、髓母细胞瘤、神经胶质瘤、室鼓膜瘤、生殖细胞瘤(松果体瘤)、胶质母细胞瘤、多形性胶质母细胞瘤、少突神经胶质瘤、神经鞘瘤、视网膜母细胞瘤、先天性肿瘤、神经-外胚层肿瘤)和脊髓癌(纤维神经瘤、脑膜瘤、神经胶质瘤、肉瘤)、神经母细胞瘤、lhermitte-duclos疾病和松果体肿瘤。
[0660]
示例性妇科癌症包括乳腺癌(导管癌、小叶癌、乳房肉瘤、三阴性乳腺癌、her2阳性乳腺癌、发炎性乳腺癌、乳头状癌)、子宫癌(子宫内膜癌)、子宫颈癌(子宫颈癌、肿瘤前子宫颈发育不良)、卵巢癌(卵巢癌(浆液性囊腺癌、粘液性囊腺癌、未分类癌瘤)、颗粒-卵泡膜细胞肿瘤、sertoli-leydig细胞肿瘤、无性细胞瘤、恶性畸胎瘤)、外阴癌(鳞状细胞癌、上皮内癌、腺癌、纤维肉瘤、黑色素瘤)、阴道癌(透明细胞癌、鳞状细胞癌、葡萄状肉瘤(胚胎性横纹肌肉瘤)和输卵管(癌)。
[0661]
示例性皮肤癌包括黑色素瘤、基底细胞癌、鳞状细胞癌、卡波西氏肉瘤、梅克尔细胞皮肤癌(merkel cell skin cancer)、发育不良痣、脂肪瘤、血管瘤、皮肤纤维瘤和瘢痕疙瘩。
[0662]
示例性头颈部癌包括胶质母细胞瘤、黑色素瘤、横纹肉瘤、淋巴肉瘤、骨肉瘤、鳞状细胞癌、腺癌、口腔癌、喉癌、鼻咽癌、鼻和鼻旁癌、甲状腺和甲状旁腺癌、眼肿瘤、唇和口腔肿瘤和鳞状细胞头颈部癌。
[0663]
本公开化合物还可用于抑制肿瘤转移。
[0664]
除了致癌性赘生物以外,本发明化合物还可用于治疗骨胳和软骨细胞病症,包括但不限于软骨发育不全、软骨发育低下、侏儒症、致死性发育不良(td)(临床形式td i和td ii)、阿佩尔氏综合征(apert syndrome)、克鲁宗综合征(crouzon syndrome)、杰克逊-韦斯综合征(jackson-weiss syndrome)、贝尔-史蒂文森皮肤旋纹综合征(beare-stevenson cutis gyrate syndrome)、菲佛综合征(pfeiffer syndrome)和颅缝早闭综合征。在一些实施方案中,本发明提供一种用于治疗罹患骨胳和软骨细胞病症的患者的方法。
[0665]
在一些实施方案中,本文所述的化合物可用于治疗阿尔茨海默氏病、hiv或肺结核。
[0666]
如本文所用,术语“8p11骨髓增生性综合征”意在指与嗜酸性粒细胞增多和fgfr1异常相关的髓系/淋巴赘生物。
[0667]
如本文所用,术语“细胞”意在指体外、离体或体内细胞。在一些实施方案中,离体细胞可以是自诸如哺乳动物的生物体切除的组织样品的部分。在一些实施方案中,体外细胞可以是细胞培养物中的细胞。在一些实施方案中,体内细胞是在诸如哺乳动物的生物体中生活的细胞。
[0668]
如本文所用,术语“接触”是指在体外系统或体内系统中将所指示的部分放在一起。例如,使fgfr酶与本文所述的化合物“接触”包括向具有fgfr的个体或患者(诸如人)施用本文所述的化合物,以及例如将本文所述的化合物引入到含有含fgfr酶的细胞或纯化制剂的样品中。
[0669]
如本文所用,可互换使用的术语“个体”或“患者”是指任何动物,包括哺乳动物,优选地小鼠、大鼠、其他啮齿动物、兔、犬、猫、猪、牛、绵羊、马或灵长类动物,并且最优选地人类。
[0670]
如本文所用,短语“治疗有效量”是指在组织、系统、动物、个体或人中引起正由研究人员、兽医、医生或其他临床医师寻求的生物或医学反应的活性化合物或药剂的量,诸如如本文所公开的任何固体形式或其盐的量。任何个别情况下的适当“有效”量均可使用本领域技术人员已知的技术测定。
[0671]
短语“药学上可接受的”在本文中用于指在合理医学判断的范围内适于与人和动物组织接触使用而无过量毒性、刺激、过敏反应、免疫原性或其他问题或并发症,与合理效益/风险比相称的那些化合物、材料、组合物和/或剂型。
[0672]
如本文所用,短语“药学上可接受的载剂或赋形剂”是指药学上可接受的材料、组合物或媒介物,诸如液体或固体填充剂、稀释剂、溶剂或封装材料。赋形剂或载剂一般是安全、无毒的并且在生物学上或其他方面均合乎需要,并且包括兽医用途以及人药物用途可接受的赋形剂或载剂。在一个实施方案中,每种组分如本文所定义“药学上可接受的”。参见
例如remington:the science and practice of pharmacy,第21版;lippincott williams&wilkins:philadelphia,pa.,2005;handbook of pharmaceutical excipients,第6版;rowe等人编;the pharmaceutical press and the american pharmaceutical association:2009;handbook of pharmaceutical additives,第3版;ash和ash编;gower publishing company:2007;pharmaceutical preformulation and formulation,第2版;gibson编;crc press llc:boca raton,fla.,2009。
[0673]
如本文所用,术语“治疗(treating)”或“治疗(treatment)”是指抑制疾病;例如,抑制正在经历或展现出疾病、疾患或病症的病理学或症状学的个体的所述疾病、疾患或病症(即,遏制病理学和/或症状学的进一步发展)或改善疾病;例如,改善正在经历或展现出疾病、疾患或病症的病理学或症状学的个体的所述疾病、疾患或病症(即,逆转病理学和/或症状学),诸如减少疾病的严重程度。
[0674]
应理解,出于清晰目的在独立实施方案的情形下描述的本发明的某些特征也可组合提供于单一实施方案中(同时所述实施方案意图如同以多重附属形式书写一样组合)。相反,出于简洁目的在单一实施方案的情形下描述的本发明的各种特征也可独立地或以任何合适的子组合提供。
[0675]
组合疗法
[0676]
一种或多种额外药剂或治疗方法,诸如抗病毒剂、化学治疗剂或其他抗癌剂、免疫增强剂、免疫抑制剂、辐射、抗肿瘤和抗病毒疫苗、细胞因子疗法(例如il2、gm-csf等)和/或酪氨酸激酶抑制剂可与本文所述的化合物组合用于治疗fgfr相关疾病、病症或疾患,或如本文所述的疾病或疾患。所述剂可与本公开化合物组合成单一剂型,或所述剂可作为单独剂型同时或依序施用。
[0677]
本文所述的化合物可与一种或多种其他激酶抑制剂组合用于治疗受多种信号传导通路影响的疾病,诸如癌症。例如,组合可包括用于治疗癌症的以下激酶的一种或多种抑制剂:akt1、akt2、akt3、tgf-βr、pim、pka、pkg、pkc、cam-激酶、磷酸化酶激酶、mekk、erk、mapk、mtor、egfr、her2、her3、her4、ins-r、igf-1r、ir-r、pdgfαr、pdgfβr、csfir、kit、flk-ii、kdr/flk-1、flk-4、flt-1、fgfr1、fgfr2、fgfr3、fgfr4、c-met、ron、sea、trka、trkb、trkc、flt3、vegfr/flt2、flt4、epha1、epha2、epha3、ephb2、ephb4、tie2、src、fyn、lck、fgr、btk、fak、syk、frk、jak、abl、alk和b-raf。另外,如本文所述的fgfr抑制剂的固体形式可组合与pik3/akt/mtor信号传导通路相关的激酶,诸如pi3k、akt(包括akt1、akt2和akt3)和mtor激酶的抑制剂。
[0678]
在一些实施方案中,本文所述的化合物可与诸如hpk1、sblb、tut4、a2a/a2b、cd47、cdk2、sting、alk2、lin28、adar1、mat2a、riok1、hdac8、wdr5、smarca2和dclk1的酶或蛋白质受体的一种或多种抑制剂组合用于治疗疾病和病症。示例性疾病和病症包括癌症、感染、炎症和神经退行性病症。
[0679]
在一些实施方案中,本文所述的化合物可与靶向表观遗传学调控剂的治疗剂组合使用。表观遗传学调控剂的实例包括溴结构域抑制剂、组蛋白赖氨酸甲基转移酶、组蛋白精氨酸甲基转移酶、组蛋白去甲基化酶、组蛋白去乙酰酶、组蛋白乙酰化酶和dna甲基转移酶。组蛋白去乙酰酶抑制剂包括例如伏立诺他(vorinostat)。
[0680]
对于治疗癌症和其他增生性疾病,本文所述的化合物可与包括以下的靶向疗法组
合使用:jak激酶抑制剂(芦可替尼(ruxolitinib),额外jak1/2和jak1选择性,巴瑞替尼(baricitinib)或incb39110)、pim激酶抑制剂(例如lgh447、incb053914和sgi-1776)、pi3激酶抑制剂(包括pi3k-δ选择性和广谱pi3k抑制剂(例如incb50465和incb54707)、pi3k-γ抑制剂(诸如pi3k-γ选择性抑制剂))、mek抑制剂、csf1r抑制剂(例如plx3397和ly3022855)、tam受体酪氨酸激酶抑制剂(tyro-3、axl和mer;例如incb81776)、血管生成抑制剂、白介素受体抑制剂、细胞周期素依赖性激酶抑制剂、braf抑制剂、mtor抑制剂、蛋白酶体抑制剂(硼替佐米(bortezomib)、卡非佐米(carfilzomib))、hdac-抑制剂(帕比司他(panobinostat)、伏立诺他(vorinostat))、dna甲基转移酶抑制剂、地塞米松、溴和额外末端家族成员抑制剂(例如溴结构域抑制剂或bet抑制剂,诸如otx015、cpi-0610、incb54329或incb57643)、lsd1抑制剂(例如gsk2979552、incb59872和incb60003)、精氨酸酶抑制剂(例如incb1158)、吲哚胺2,3-双加氧酶抑制剂(例如艾卡哚司他(epacadostat)、nlg919或bms-986205)、parp抑制剂(例如奥拉帕尼(olaparib)或瑞卡帕布(rucaparib))、btk抑制剂(诸如依鲁替尼(ibrutinib))、c-met抑制剂(例如卡帕替尼(capmatinib))、alk2抑制剂(例如incb00928);或其组合。
[0681]
对于治疗癌症和其他增生性疾病,本文所述的化合物可与化学治疗剂、核受体的激动剂或拮抗剂或其他抗增生剂组合使用。本文所述的化合物还可与医学疗法,诸如外科手术或放射疗法,例如γ-放射、中子束放射疗法、电子束放射疗法、质子疗法、近距离疗法和全身性放射性同位素组合使用。
[0682]
合适化学治疗剂的实例包括以下中的任一种:阿巴瑞克、阿比特龙、阿法替尼、阿柏西普、阿地白介素、阿仑单抗、阿利维a酸、别嘌呤醇、六甲蜜胺、阿米多克斯(amidox)、安吖啶、阿那曲唑、艾弗迪隆(aphidicolon)、三氧化二砷、天冬酰胺酶、阿西替尼、阿扎胞苷、贝伐珠单抗、贝沙罗汀、巴瑞替尼、苯达莫司汀、比卡鲁胺、博莱霉素、硼替佐比(bortezombi)、硼替佐米(bortezomib)、布立尼布、布帕利司(buparlisib)、静脉注射白消安、口服白消安、卡鲁睾酮、伊立替康、卡培他滨、卡铂、卡莫司汀、西地尼布、西妥昔单抗、苯丁酸氮芥、顺铂、克拉屈滨、氯法拉滨、克唑替尼、环磷酰胺、阿糖胞苷、达卡巴嗪、达克替尼、放线菌素d、达肝素钠、达沙替尼、放线菌素d、道诺霉素、地西他滨、地加瑞克、地尼白介素、地尼白介素白喉毒素连接物、去氧助间型霉素、右雷佐生、迪多克斯、多西他赛、多柔比星、屈洛昔芬、丙酸屈他雄酮、依库珠单抗、恩杂鲁胺、表鬼臼毒素、表柔比星、埃博霉素、厄洛替尼、雌莫司汀、磷酸依托泊苷、依托泊苷、依西美坦、柠檬酸芬太尼、非格司亭、脱氧氟脲苷、氟达拉滨、氟尿嘧啶、氟他胺、氟维司琼、吉非替尼、吉西他滨、吉妥珠单抗(gemtuzumab ozogamicin)、乙酸戈舍瑞林、乙酸组胺瑞林、替伊莫单抗、伊达比星、艾代拉利司(idelalisib)、异环磷酰胺、甲磺酸伊马替尼、干扰素α2a、伊立替康、二甲苯磺酸拉帕替尼、来那度胺、来曲唑、甲酰四氢叶酸、乙酸亮丙瑞林、左旋咪唑、洛那法尼(lonafarnib)、洛莫司汀、氮芥(meclorethamine)、乙酸甲地孕酮、美法仑、巯基嘌呤、甲氨喋呤、甲氧沙林、光神霉素、丝裂霉素c、米托坦、米托蒽醌、苯丙酸诺龙、诺维本、耐昔妥珠单抗、纳拉滨、来那替尼、尼洛替尼、尼鲁米特、尼拉帕利、诺非单抗、戈舍瑞林(oserelin)、奥沙利铂、太平洋紫杉醇、帕米膦酸盐、帕尼单抗、帕比司他、帕唑帕尼、培加帕酶、培非格司亭、培美曲塞二钠、喷司他丁、皮拉利司(pilaralisib)、哌泊溴烷、普卡霉素、普纳替尼、卟吩姆钠、泼尼松、丙卡巴肼、奎纳克林、雷珠单抗、拉布立酶、瑞格菲尼、雷罗沙芬(reloxafine)、雷利米得、利妥昔
单抗、瑞卡帕布、芦可替尼、索拉非尼、链脲佐菌素、舒尼替尼、马来酸舒尼替尼、他莫昔芬、替加氟、替莫唑胺、替尼泊苷、睾内酯、替扎他滨(tezacitabine)、沙利度胺、硫鸟嘌呤、噻替派、替吡法尼、拓扑替康、托瑞米芬、托西莫单抗、曲妥珠单抗、维甲酸、曲阿平、曲美多、曲普瑞林、尿嘧啶氮芥、戊柔比星、凡德他尼、长春花碱、长春新碱、长春地辛、长春瑞滨、伏立诺他、维利帕尼、他拉唑帕尼和唑来膦酸盐。
[0683]
癌细胞生长和存活可受多种信号传导通路的功能障碍影响。因此,组合在由其调节活性的标靶中表现出不同偏好的不同酶/蛋白质/受体抑制剂,以治疗所述疾患是有用的。靶向多于一种信号传导通路(或涉及给定信号传导通路的多于一种生物分子)可降低在细胞群体中产生药物抗性的可能性,和/或降低治疗毒性。
[0684]
一种或多种额外药剂(诸如化学治疗剂、消炎剂、类固醇、免疫抑制剂、免疫-肿瘤剂、代谢酶抑制剂、趋化因子受体抑制剂和磷酸酯酶抑制剂)以及靶向疗法(诸如bcr-abl、flt-3、egfr、her2、jak、c-met、vegfr、pdgfr、c-kit、igf-1r、raf、fak、cdk2和cdk4/6激酶抑制剂,诸如wo 2006/056399中描述的那些)可与本发明的治疗方法和方案组合用于治疗癌症和实性肿瘤。诸如治疗抗体的其他剂可与本发明的治疗方法和方案组合用于治疗癌症和实性肿瘤。所述一种或多种额外药剂可同时或依序施用于患者。
[0685]
如本文所公开的治疗方法可与一种或多种其他酶/蛋白质/受体抑制剂疗法组合用于治疗疾病,诸如癌症和本文所述的其他疾病或病症。例如,本发明的治疗方法和方案可与以下激酶的一种或多种抑制剂组合用于治疗癌症:akt1、akt2、akt3、bcl2、cdk2、cdk4/6、tgf-βr、pka、pkg、pkc、cam-激酶、磷酸化酶激酶、mekk、erk、mapk、mtor、egfr、her2、her3、her4、ins-r、idh2、igf-1r、ir-r、pdgfαr、pdgfβr、pi3k(α、β、γ、δ和多重或选择性)、csf1r、kit、flk-ii、kdr/flk-1、flk-4、flt-1、fgfr1、fgfr2、fgfr3、fgfr4、c-met、parp、ron、sea、trka、trkb、trkc、tam激酶(axl、mer、tyro3)、flt3、vegfr/flt2、flt4、epha1、epha2、epha3、ephb2、ephb4、tie2、src、fyn、lck、fgr、btk、fak、syk、frk、jak、abl、alk和b-raf。可与本发明的治疗方法和方案组合用于治疗癌症的抑制剂的非限制性实例包括fgfr抑制剂(fgfr1、fgfr2、fgfr3或fgfr4,例如培米替尼(incb54828)、incb62079)、egfr抑制剂(也称作erb-1或her-1;例如厄洛替尼、吉非替尼、凡德他尼或奥希替尼、西妥昔单抗、耐昔妥珠单抗或帕尼单抗)、vegfr抑制剂或通路阻断剂(例如贝伐珠单抗、帕唑帕尼、舒尼替尼、索拉非尼、阿西替尼、瑞格非尼、普纳替尼、卡博替尼、凡德他尼、雷莫芦单抗、乐伐替尼、阿柏西普(ziv-aflibercept))、parp抑制剂(例如奥拉帕尼、瑞卡帕布、维利帕尼或尼拉帕利)、jak抑制剂(jak1和/或jak2,例如芦可替尼、巴瑞替尼、伊他替尼(incb39110)、lsd1抑制剂(例如incb59872和incb60003)、tdo抑制剂、pi3k-δ抑制剂(例如incb50465和incb50797)、pi3k-γ抑制剂(诸如pi3k-γ选择性抑制剂)、pim抑制剂(例如incb53914)、csf1r抑制剂、tam受体酪氨酸激酶(tyro-3、axl和mer)、腺苷受体拮抗剂(例如a2a/a2b受体拮抗剂)、hpk1抑制剂、趋化因子受体抑制剂(例如ccr2或ccr5抑制剂)、shp1/2磷酸酯酶抑制剂、组蛋白去乙酰酶抑制剂(hdac)(诸如hdac8抑制剂)、血管生成抑制剂、白介素受体抑制剂、溴和额外末端家族成员抑制剂(例如溴结构域抑制剂或bet抑制剂,诸如incb54329和incb57643)、c-met抑制剂(例如卡帕替尼)、抗cd19抗体(例如塔法西他单抗(tafasitamab))、alk2抑制剂(例如incb00928);或其组合。
[0686]
在一些实施方案中,本文所述的治疗方法与pi3kδ抑制剂的施用组合。在一些实施
方案中,本文所述的治疗方法与jak抑制剂的施用组合。在一些实施方案中,本文所述的治疗方法与jak1或jak2抑制剂(例如巴瑞替尼或芦可替尼)的施用组合。在一些实施方案中,本文所述的治疗方法与jak1抑制剂的施用组合。在一些实施方案中,本文所述的治疗方法与选择性超过jak2的jak1抑制剂的施用组合。
[0687]
可以组合疗法施用的实例抗体包括但不限于曲妥珠单抗(例如抗her2)、雷珠单抗(例如抗vegf-a)、贝伐珠单抗(avastin
tm
,例如抗vegf)、帕尼单抗(例如抗egfr)、西妥昔单抗(例如抗egfr)、美罗华(例如抗cd20)和针对c-met的抗体。
[0688]
一种或多种以下剂可与本发明的治疗方法组合施用于患者并且作为非限制性清单呈现:细胞抑制剂、顺铂、多柔比星、泰索帝、紫杉醇、依托泊苷、伊立替康、坎姆思达(camptostar)、拓扑替康、太平洋紫杉醇、多西他赛、埃博霉素、他莫昔芬、5-氟脲苷、甲氨喋呤、替莫唑胺、环磷酰胺、sch 66336、r115777、l778,123、bms 214662、iressa
tm
(吉非替尼)、tarceva
tm
(厄洛替尼)、egfr抗体、内含子、ara-c、阿霉素、癌得星、吉西他滨、尿嘧啶氮芥、恩比兴、异环磷酰胺、美法仑、苯丁酸氮芥、哌泊溴烷、三亚乙基三聚氰胺、三亚乙基硫代磷酰胺、白消安、卡莫司汀、洛莫司汀、链脲佐菌素、达卡巴嗪、脱氧氟脲苷、阿糖胞苷、6-巯基嘌呤、6-硫鸟嘌呤、磷酸氟达拉滨、奥沙利铂、甲酰四氢叶酸、eloxatin
tm
(奥沙利铂)、喷司他汀、长春花碱、长春新碱、长春地辛、博来霉素、放线菌素d、道诺霉素、多柔比星、表柔比星、伊达比星、光神霉素、去氧助间型霉素、丝裂霉素-c、l-天冬酰胺酶、替尼泊苷17.α.-乙炔基雌二醇、己烯雌酚、睾酮、泼尼松、氟甲睾酮、丙酸屈他雄酮、睾内酯、乙酸甲地孕酮、甲泼尼龙、甲基睾酮、泼尼松龙、曲安奈德、氯烯雌醚、羟孕酮、胺鲁米特、雌莫司汀、乙酸甲羟孕酮、亮丙瑞林、氟他胺、托瑞米芬、戈舍瑞林、卡铂、羟基脲、安吖啶、丙卡巴肼、米托坦、米托蒽醌、左旋咪唑、诺维本、阿那曲唑、来曲唑、卡培他滨、雷罗色分、屈洛昔芬、六甲三聚氰胺、阿瓦斯汀、herceptin
tm
(曲妥珠单抗)、bexxar
tm
(托西莫单抗)、velcade
tm
(硼替佐米)、zevalin
tm
(替伊莫单抗)、trisenox
tm
(三氧化二砷)、xeloda
tm
(卡培他滨)、长春瑞滨、卟吩姆钠、erbitux
tm
(西妥昔单抗)、噻替派、六甲蜜胺、美法仑、曲妥珠单抗、来曲唑、氟维司琼、依西美坦、异环磷酰胺、利妥昔单抗、c225(西妥昔单抗)、campath(阿仑单抗)、氯法拉滨、克拉屈滨、艾弗迪隆、美罗华、舒尼替尼、达沙替尼、替扎他滨、sml1、氟达拉滨、喷司他汀、曲阿平、迪多克斯、曲美多、阿米多克斯、3-ap和mdl-101,731。
[0689]
本发明的治疗方法和方案可进一步与例如通过化学疗法、辐射疗法、肿瘤靶向疗法、佐剂疗法、免疫疗法或外科手术治疗癌症的其他方法组合使用。免疫疗法的实例包括细胞因子治疗(例如干扰素、gm-csf、g-csf、il-2)、crs-207免疫疗法、癌症疫苗、单克隆抗体、双特异性或多特异性抗体、抗体药物缀合物、过继性t细胞转移、toll受体激动剂、rig-i激动剂、溶瘤病毒疗法和免疫调节小分子(包括沙利度胺或jak1/2抑制剂、pi3kδ抑制剂等)。化合物可与一种或多种抗癌药物,诸如化学治疗剂组合施用。化学治疗剂的实例包括以下中的任一种:阿巴瑞克、阿地白介素、阿仑单抗、阿利维a酸、别嘌呤醇、六甲蜜胺、阿那曲唑、三氧化二砷、天冬酰胺酶、阿扎胞苷、贝伐珠单抗、贝沙罗汀、巴瑞替尼、博莱霉素、硼替佐米、静脉注射白消安、口服白消安、卡鲁睾酮、卡培他滨、卡铂、卡莫司汀、西妥昔单抗、苯丁酸氮芥、顺铂、克拉屈滨、氯法拉滨、环磷酰胺、阿糖胞苷、达卡巴嗪、放线菌素d、达肝素钠、达沙替尼、道诺霉素、地西他滨、地尼白介素、地尼白介素白喉毒素连接物、右雷佐生、多西他赛、多柔比星、丙酸屈他雄酮、依库珠单抗、艾卡哚司他、表柔比星、厄洛替尼、雌莫司汀、
磷酸依托泊苷、依托泊苷、依西美坦、柠檬酸芬太尼、非格司亭、脱氧氟脲苷、氟达拉滨、氟尿嘧啶、氟维司琼、吉非替尼、吉西他滨、吉妥珠单抗、乙酸戈舍瑞林、乙酸组胺瑞林、替伊莫单抗、伊达比星、异环磷酰胺、甲磺酸伊马替尼、干扰素α2a、伊立替康、二甲苯磺酸拉帕替尼、来那度胺、来曲唑、甲酰四氢叶酸、乙酸亮丙瑞林、左旋咪唑、洛莫司汀、氮芥(meclorethamine)、乙酸甲地孕酮、美法仑、巯基嘌呤、甲氨喋呤、甲氧沙林、丝裂霉素c、米托坦、米托蒽醌、苯丙酸诺龙、纳拉滨、诺非单抗、奥沙利铂、太平洋紫杉醇、帕米膦酸盐、帕尼单抗、培加帕酶、培非格司亭、培美曲塞二钠、喷司他丁、哌泊溴烷、普卡霉素、丙卡巴肼、奎纳克林、拉布立酶、利妥昔单抗、芦可替尼、索拉非尼、链脲佐菌素、舒尼替尼、马来酸舒尼替尼、他莫昔芬、替莫唑胺、替尼泊苷、睾内酯、沙利度胺、硫鸟嘌呤、噻替派、拓扑替康、托瑞米芬、托西莫单抗、曲妥珠单抗、维甲酸、尿嘧啶氮芥、戊柔比星、长春花碱、长春新碱、长春瑞滨、伏立诺他和唑来膦酸盐。
[0690]
化学治疗剂的额外实例包括蛋白酶体抑制剂(例如硼替佐米)、沙利度胺、雷利米得和dna损伤剂(诸如美法仑、多柔比星、环磷酰胺、长春新碱、依托泊苷、卡莫司汀等)。
[0691]
实例类固醇包括皮质类固醇,诸如地塞米松或泼尼松。
[0692]
实例bcr-abl抑制剂包括甲磺酸伊马替尼(gleevac
tm
)、尼洛替尼、达沙替尼、博舒替尼和普纳替尼以及药学上可接受的盐。合适bcr-abl抑制剂的其他实例包括美国专利号5,521,184、wo 04/005281和u.s.号60/578,491中所公开的属和种的化合物及其药学上可接受的盐。
[0693]
合适flt-3抑制剂的实例包括米哚妥林、来他替尼、利尼伐尼、舒尼替尼、马来酸舒尼替尼、索拉非尼、奎扎替尼、克莱拉尼、帕瑞替尼、坦度替尼、plx3397和asp2215及其药学上可接受的盐。合适flt-3抑制剂的其他实例包括如wo 03/037347、wo 03/099771和wo 04/046120中所公开的化合物及其药学上可接受的盐。
[0694]
合适raf抑制剂的实例包括达拉非尼、索拉非尼和维罗非尼以及其药学上可接受的盐。合适raf抑制剂的其他实例包括如wo 00/09495和wo 05/028444中所公开的化合物及其药学上可接受的盐。
[0695]
合适fak抑制剂的实例包括vs-4718、vs-5095、vs-6062、vs-6063、bi853520和gsk2256098以及其药学上可接受的盐。合适fak抑制剂的其他实例包括如wo 04/080980、wo 04/056786、wo 03/024967、wo 01/064655、wo 00/053595和wo 01/014402中所公开的化合物及其药学上可接受的盐。
[0696]
合适cdk4/6抑制剂的实例包括帕博西尼、瑞博西尼、曲拉西尼、乐若西尼(lerociclib)和玻玛西尼以及其药学上可接受的盐。合适cdk4/6抑制剂的其他实例包括如wo 09/085185、wo 12/129344、wo 11/101409、wo 03/062236、wo 10/075074和wo 12/061156中所公开的化合物及其药学上可接受的盐。
[0697]
在一些实施方案中,本公开化合物可与包括伊马替尼在内的一种或多种其他激酶抑制剂组合使用,尤其用于治疗抵抗伊马替尼或其他激酶抑制剂的患者。
[0698]
在一些实施方案中,本发明的治疗方法可与化学治疗剂组合用于治疗癌症,并且与对单独化学治疗剂的反应相比,可改善治疗反应,而不会加剧其毒性作用。在一些实施方案中,本发明的治疗方法可与本文所提供的化学治疗剂组合使用。例如,用于治疗多发性骨髓瘤的额外药剂可包括但不限于美法仑、美法仑加泼尼松[mp]、多柔比星、地塞米松和
velcade(硼替佐米)。用于治疗多发性骨髓瘤的其他额外剂包括bcr-abl、flt-3、raf和fak激酶抑制剂。在一些实施方案中,所述剂是烷基化剂、蛋白酶体抑制剂、皮质类固醇或免疫调节剂。烷基化剂的实例包括环磷酰胺(cy)、美法仑(mel)和苯达莫司汀。在一些实施方案中,蛋白酶体抑制剂是卡非佐米。在一些实施方案中,皮质类固醇是地塞米松(dex)。在一些实施方案中,免疫调节剂是来那度胺(len)或泊马度胺(pom)。加性或协同效应是组合本发明的治疗方法与额外剂的期望结果。
[0699]
所述剂可与本发明治疗方法的化合物1和/或结合至人pd-1或人pd-l1的抗体或其抗原结合片段组合成单一或连续剂型,或所述剂可作为单独剂型同时或依序施用。
[0700]
在一些实施方案中,诸如地塞米松的皮质类固醇与本公开的治疗方法组合施用于患者,其中地塞米松间歇地施用,而非连续地。
[0701]
本文所述的治疗方法可与另一种免疫原性剂,诸如癌细胞、纯化肿瘤抗原(包括重组蛋白、肽和碳水化合物分子)、细胞和经编码免疫刺激细胞因子的基因转染的细胞组合。可使用的肿瘤疫苗的非限制性实例包括黑色素瘤抗原的肽,诸如gp100、mage抗原、trp-2、marti和/或酪氨酸酶的肽,或经转染以表达细胞因子gm-csf的肿瘤分子。
[0702]
本文所述的治疗方法可与用于治疗癌症的疫苗接种方案组合使用。在一些实施方案中,肿瘤细胞经转导以表达gm-csf。在一些实施方案中,肿瘤疫苗包括来自与人癌症有关的病毒,诸如人乳头状瘤病毒(hpv)、肝炎病毒(hbv和hcv)和卡波西氏疱疹肉瘤病毒(khsv)的蛋白质。在一些实施方案中,本公开的治疗方法和方案可与肿瘤特异性抗原,诸如从肿瘤组织自身分离出来的热休克蛋白组合使用。在一些实施方案中,本文所述的治疗方法可与免疫化以激活有效抗肿瘤反应的树突状细胞组合。
[0703]
本公开的治疗方法和方案可与使表达feα或feγ受体的效应子细胞靶向肿瘤细胞的双特异性巨环肽组合使用。本公开的治疗方法和方案还可与激活宿主免疫反应性的巨环肽组合。
[0704]
在一些其他实施方案中,本公开的治疗方法与在骨髓移植或干细胞移植之前、期间和/或之后将其他治疗剂施用于患者组合。本公开的治疗方法和方案可与骨髓移植组合用于治疗造血系统起源的多种肿瘤。
[0705]
当多于一种药剂施用于患者时,如以上实施方案中的任一项所讨论,其可同时、单独地、依序或组合施用(例如,针对超过两种剂)。
[0706]
本领域技术人员已知用于大多数这些化学治疗剂的安全且有效施用的方法。另外,其施用描述于标准文献中。例如,多种化学治疗剂的施用描述于“physicians’desk reference”(pdr,例如1996版,medical economics company,montvale,nj)中,所述文献的公开内容以引用的方式并入本文,就如同整体陈述一样。
[0707]
在一些实施方案中,本文所述的化合物可与免疫检查点抑制剂组合使用。示例性免疫检查点抑制剂包括针对诸如以下的免疫检查点分子的抑制剂:cd27、cd28、cd40、cd122、cd96、cd73、cd47、ox40、gitr、csf1r、jak、pi3kδ、pi3kγ、tam、精氨酸酶、cd137(也称作4-1bb)、icos、a2ar、b7-h3、b7-h4、btla、ctla-4、lag3(例如incagn2385)、tim3(例如incb2390)、vista、pd-1、pd-l1和pd-l2。在一些实施方案中,免疫检查点分子是选自cd27、cd28、cd40、icos、ox40(例如incagn1949)、gitr(例如incagn1876)和cd137的刺激性检查点分子。在一些实施方案中,免疫检查点分子是选自a2ar、b7-h3、b7-h4、btla、ctla-4、ido、
kir、lag3、pd-1、tim3和vista的抑制性检查点分子。在一些实施方案中,本文所提供的化合物可与选自kir抑制剂、tigit抑制剂、lair1抑制剂、cd160抑制剂、2b4抑制剂和tgfrβ抑制剂的一种或多种剂组合使用。
[0708]
在一些实施方案中,免疫检查点分子的抑制剂是小分子pd-l1抑制剂。在一些实施方案中,小分子pd-l1抑制剂在描述于美国专利公布号us 20170107216、us 20170145025、us 20170174671、us20170174679、us 20170320875、us 20170342060、us 20170362253和us 20180016260中的pd-l1测定中具有小于1μm、小于100nm、小于10nm或小于1nm的ic50,所述专利中的每一个出于所有目的以引用的方式整体并入。
[0709]
在一些实施方案中,免疫检查点分子的抑制剂是pd-1抑制剂,例如抗pd-1单克隆抗体。在一些实施方案中,抗pd-1单克隆抗体是mga012、纳武单抗、派姆单抗(也称作mk-3475)、匹地利珠单抗、shr-1210、pdr001、伊匹木单抗或amp-224。在一些实施方案中,抗pd-1单克隆抗体是纳武单抗或派姆单抗。在一些实施方案中,抗pd1抗体是派姆单抗。在一些实施方案中,抗pd1抗体是纳武单抗。在一些实施方案中,抗pd-1单克隆抗体是mga012(瑞弗利单抗)。在一些实施方案中,抗pd1抗体是shr-1210。其他抗癌剂包括抗体治疗剂,诸如4-1bb(例如乌瑞芦单抗、乌托鲁单抗)。
[0710]
在一些实施方案中,本公开化合物可与incb086550组合使用。
[0711]
在一些实施方案中,免疫检查点分子的抑制剂是pd-l1抑制剂,例如抗pd-l1单克隆抗体。在一些实施方案中,抗pd-l1单克隆抗体是bms-935559、medi4736、mpdl3280a(也称作rg7446)或msb0010718c。在一些实施方案中,抗pd-l1单克隆抗体是mpdl3280a或medi4736。
[0712]
在一些实施方案中,免疫检查点分子的抑制剂是ctla-4抑制剂,例如抗ctla-4抗体。在一些实施方案中,抗ctla-4抗体是伊匹单抗、替西木单抗、agen1884或cp-675,206。
[0713]
在一些实施方案中,免疫检查点分子的抑制剂是lag3抑制剂,例如抗lag3抗体。在一些实施方案中,抗lag3抗体是bms-986016、lag525或incagn2385。
[0714]
在一些实施方案中,免疫检查点分子的抑制剂是tim3抑制剂,例如抗tim3抗体。在一些实施方案中,抗tim3抗体是incagn2390、mbg453或tsr-022。
[0715]
在一些实施方案中,免疫检查点分子的抑制剂是gitr抑制剂,例如抗gitr抗体。在一些实施方案中,抗gitr抗体是trx518、mk-4166、incagn1876、mk-1248、amg228、bms-986156、gwn323或medi1873。
[0716]
在一些实施方案中,免疫检查点分子的抑制剂是ox40激动剂,例如ox40激动剂抗体或ox40l融合蛋白。在一些实施方案中,抗ox40抗体是medi0562、moxr-0916、pf-04518600、gsk3174998或bms-986178。在一些实施方案中,ox40l融合蛋白是medi6383。
[0717]
在一些实施方案中,免疫检查点分子的抑制剂是cd20抑制剂,例如抗cd20抗体。在一些实施方案中,抗cd20抗体是奥比妥珠单抗或利妥昔单抗。
[0718]
在一些实施方案中,免疫检查点分子的抑制剂是cd19抑制剂,例如抗cd19抗体。在一些实施方案中,抗cd19抗体是塔法西他单抗。
[0719]
本公开化合物可与双特异性抗体组合使用。在一些实施方案中,双特异性抗体的一个结构域靶向pd-1、pd-l1、ctla-4、gitr、ox40、tim3、lag3、cd137、icos、cd3或tgfβ受体。
[0720]
在一些实施方案中,本公开化合物可与一种或多种代谢酶抑制剂组合使用。在一
些实施方案中,代谢酶抑制剂是ido1、tdo或精氨酸酶的抑制剂。ido1抑制剂的实例包括艾卡哚司他、nlg919、bms-986205、pf-06840003、iom2983、rg-70099和ly338196。
[0721]
本公开化合物可与一种或多种免疫检查点抑制剂组合用于治疗疾病,诸如癌症或感染。示例性免疫检查点抑制剂包括针对诸如以下的免疫检查点分子的抑制剂:cbl-b、cd20、cd28、cd40、cd70、cd122、cd96、cd73、cd47、cdk2、gitr、csf1r、jak、pi3kδ、pi3kγ、tam、精氨酸酶、hpk1、cd137(也称作4-1bb)、icos、a2ar、b7-h3、b7-h4、btla、ctla-4、lag3、tim3、tlr(tlr7/8)、tigit、cd112r、vista、pd-1、pd-l1和pd-l2。在一些实施方案中,免疫检查点分子选自cd27、cd28、cd40、icos、ox40、gitr和cd137的刺激性检查点分子。在一些实施方案中,免疫检查点分子选自a2ar、b7-h3、b7-h4、btla、ctla-4、ido、kir、lag3、pd-1、tim3、tigit和vista的抑制性检查点分子。在一些实施方案中,本文所提供的化合物可与选自kir抑制剂、tigit抑制剂、lair1抑制剂、cd160抑制剂、2b4抑制剂和tgfrβ抑制剂的一种或多种剂组合使用。
[0722]
在一些实施方案中,本文所提供的化合物可与免疫检查点分子,例如ox40、cd27、gitr和cd137(也称作4-1bb)的一种或多种激动剂组合使用。
[0723]
在一些实施方案中,免疫检查点分子的抑制剂是抗pd1抗体、抗pd-l1抗体或抗ctla-4抗体。
[0724]
在一些实施方案中,免疫检查点分子的抑制剂是pd-1或pd-l1抑制剂,例如抗pd-1或抗pd-l1单克隆抗体。在一些实施方案中,抗pd-1或抗pd-l1抗体是纳武单抗、派姆单抗、阿特珠单抗、度伐鲁单抗、阿维鲁单抗、西米普利单抗、阿特珠单抗、阿维鲁单抗、替雷利珠单抗、斯巴达珠单抗(pdr001)、赛曲利单抗(jnj-63723283)、特瑞普利单抗(js001)、卡瑞利珠单抗(shr-1210)、信迪利单抗(ibi308)、ab122(gls-010)、amp-224、amp-514/medi-0680、bms936559、jtx-4014、bgb-108、shr-1210、medi4736、faz053、bcd-100、kn035、cs1001、bat1306、lzm009、ak105、hlx10、shr-1316、cbt-502(tqb2450)、a167(kl-a167)、sti-a101(zkab001)、ck-301、bgb-a333、msb-2311、hlx20、tsr-042或ly3300054。在一些实施方案中,pd-1或pd-l1抑制剂是公开于美国专利号7,488,802、7,943,743、8,008,449、8,168,757、8,217,149或10,308,644;美国公布号2017/0145025、2017/0174671、2017/0174679、2017/0320875、2017/0342060、2017/0362253、2018/0016260、2018/0057486、2018/0177784、2018/0177870、2018/0179179、2018/0179201、2018/0179202、2018/0273519、2019/0040082、2019/0062345、2019/0071439、2019/0127467、2019/0144439、2019/0202824、2019/0225601、2019/0300524或2019/0345170;或pct公布号wo 03042402、wo 2008156712、wo 2010089411、wo 2010036959、wo 2011066342、wo 2011159877、wo 2011082400或wo 2011161699中的抑制剂,所述专利各自以引用的方式整体并入本文。在一些实施方案中,pd-l1抑制剂是incb086550。
[0725]
在一些实施方案中,抗体是抗pd-1抗体,例如抗pd-1单克隆抗体。在一些实施方案中,抗pd-1抗体是纳武单抗、派姆单抗、西米普利单抗、斯巴达珠单抗、卡瑞利珠单抗、赛曲利单抗、特瑞普利单抗、信迪利单抗、ab122、amp-224、jtx-4014、bgb-108、bcd-100、bat1306、lzm009、ak105、hlx10或tsr-042。在一些实施方案中,抗pd-1抗体是纳武单抗、派姆单抗、西米普利单抗、斯巴达珠单抗、卡瑞利珠单抗、赛曲利单抗、特瑞普利单抗或信迪利单抗。在一些实施方案中,抗pd-1抗体是派姆单抗。在一些实施方案中,抗pd-1抗体是纳武
单抗。在一些实施方案中,抗pd-1抗体是西米普利单抗。在一些实施方案中,抗pd-1抗体是斯巴达珠单抗。在一些实施方案中,抗pd-1抗体是卡瑞利珠单抗。在一些实施方案中,抗pd-1抗体是赛曲利单抗。在一些实施方案中,抗pd-1抗体是特瑞普利单抗。在一些实施方案中,抗pd-1抗体是信迪利单抗。在一些实施方案中,抗pd-1抗体是ab122。在一些实施方案中,抗pd-1抗体是amp-224。在一些实施方案中,抗pd-1抗体是jtx-4014。在一些实施方案中,抗pd-1抗体是bgb-108。在一些实施方案中,抗pd-1抗体是bcd-100。在一些实施方案中,抗pd-1抗体是bat1306。在一些实施方案中,抗pd-1抗体是lzm009。在一些实施方案中,抗pd-1抗体是ak105。在一些实施方案中,抗pd-1抗体是hlx10。在一些实施方案中,抗pd-1抗体是tsr-042。在一些实施方案中,抗pd-1单克隆抗体是纳武单抗或派姆单抗。在一些实施方案中,抗pd1抗体是shr-1210。其他抗癌剂包括抗体治疗剂,诸如4-1bb(例如乌瑞芦单抗、乌托鲁单抗)。在一些实施方案中,免疫检查点分子的抑制剂是pd-l1抑制剂,例如抗pd-l1单克隆抗体。在一些实施方案中,抗pd-l1单克隆抗体是阿特珠单抗、阿维鲁单抗、度伐鲁单抗、替雷利珠单抗、bms-935559、medi4736、阿特珠单抗(mpdl3280a;也称作rg7446)、阿维鲁单抗(msb0010718c)、faz053、kn035、cs1001、shr-1316、cbt-502、a167、sti-a101、ck-301、bgb-a333、msb-2311、hlx20或ly3300054。在一些实施方案中,抗pd-l1抗体是阿特珠单抗、阿维鲁单抗、度伐鲁单抗或替雷利珠单抗。在一些实施方案中,抗pd-l1抗体是阿特珠单抗。在一些实施方案中,抗pd-l1抗体是阿维鲁单抗。在一些实施方案中,抗pd-l1抗体是度伐鲁单抗。在一些实施方案中,抗pd-l1抗体是替雷利珠单抗。在一些实施方案中,抗pd-l1抗体是bms-935559。在一些实施方案中,抗pd-l1抗体是medi4736。在一些实施方案中,抗pd-l1抗体是faz053。在一些实施方案中,抗pd-l1抗体是kn035。在一些实施方案中,抗pd-l1抗体是cs1001。在一些实施方案中,抗pd-l1抗体是shr-1316。在一些实施方案中,抗pd-l1抗体是cbt-502。在一些实施方案中,抗pd-l1抗体是a167。在一些实施方案中,抗pd-l1抗体是sti-a101。在一些实施方案中,抗pd-l1抗体是ck-301。在一些实施方案中,抗pd-l1抗体是bgb-a333。在一些实施方案中,抗pd-l1抗体是msb-2311。在一些实施方案中,抗pd-l1抗体是hlx20。在一些实施方案中,抗pd-l1抗体是ly3300054。
[0726]
在一些实施方案中,免疫检查点分子的抑制剂是结合至pd-l1的小分子,或其药学上可接受的盐。在一些实施方案中,免疫检查点分子的抑制剂是结合至且内化pd-l1的小分子,或其药学上可接受的盐。在一些实施方案中,免疫检查点分子的抑制剂是选自us 2018/0179201、us 2018/0179197、us 2018/0179179、us 2018/0179202、us 2018/0177784、us 2018/0177870、us序列号16/369,654(2019年3月29日申请)和us序列号62/688,164中的那些的化合物,或其药学上可接受的盐,所述专利中的每一个都以引用的方式整体并入本文。
[0727]
在一些实施方案中,免疫检查点分子的抑制剂是kir、tigit、lair1、cd160、2b4和tgfrβ抑制剂。
[0728]
在一些实施方案中,抑制剂是mcla-145。
[0729]
在一些实施方案中,免疫检查点分子的抑制剂是ctla-4抑制剂,例如抗ctla-4抗体。在一些实施方案中,抗ctla-4抗体是伊匹单抗、替西木单抗、agen1884或cp-675,206。
[0730]
在一些实施方案中,免疫检查点分子的抑制剂是lag3抑制剂,例如抗lag3抗体。在一些实施方案中,抗lag3抗体是bms-986016、lag525、incagn2385或eftilagimodα(imp321)。
[0731]
在一些实施方案中,免疫检查点分子的抑制剂是cd73抑制剂。在一些实施方案中,cd73抑制剂是奥来鲁单抗(oleclumab)。
[0732]
在一些实施方案中,免疫检查点分子的抑制剂是tigit抑制剂。在一些实施方案中,tigit抑制剂是omp-31m32。
[0733]
在一些实施方案中,免疫检查点分子的抑制剂是vista抑制剂。在一些实施方案中,vista抑制剂是jnj-61610588或ca-170。
[0734]
在一些实施方案中,免疫检查点分子的抑制剂是b7-h3抑制剂。在一些实施方案中,b7-h3抑制剂是依诺妥珠单抗(enoblituzumab)、mgd009或8h9。
[0735]
在一些实施方案中,免疫检查点分子的抑制剂是kir抑制剂。在一些实施方案中,kir抑制剂是利瑞鲁单抗或iph4102。
[0736]
在一些实施方案中,免疫检查点分子的抑制剂是a2ar抑制剂。在一些实施方案中,a2ar抑制剂是cpi-444。
[0737]
在一些实施方案中,免疫检查点分子的抑制剂是tgf-β抑制剂。在一些实施方案中,tgf-β抑制剂是曲贝德生、加鲁色替尼(galusertinib)或m7824。
[0738]
在一些实施方案中,免疫检查点分子的抑制剂是pi3k-γ抑制剂。在一些实施方案中,pi3k-γ抑制剂是ipi-549。
[0739]
在一些实施方案中,免疫检查点分子的抑制剂是cd47抑制剂。在一些实施方案中,cd47抑制剂是hu5f9-g4或tti-621。
[0740]
在一些实施方案中,免疫检查点分子的抑制剂是cd73抑制剂。在一些实施方案中,cd73抑制剂是medi9447。
[0741]
在一些实施方案中,免疫检查点分子的抑制剂是cd70抑制剂。在一些实施方案中,cd70抑制剂是库萨珠单抗(cusatuzumab)或bms-936561。
[0742]
在一些实施方案中,免疫检查点分子的抑制剂是tim3抑制剂,例如抗tim3抗体。在一些实施方案中,抗tim3抗体是incagn2390、mbg453或tsr-022。
[0743]
在一些实施方案中,免疫检查点分子的抑制剂是cd20抑制剂,例如抗cd20抗体。在一些实施方案中,抗cd20抗体是奥比妥珠单抗或利妥昔单抗。
[0744]
在一些实施方案中,免疫检查点分子的抑制剂是ox40、cd27、cd28、gitr、icos、cd40、tlr7/8和cd137(也称作4-1bb)的激动剂。
[0745]
在一些实施方案中,cd137激动剂是乌瑞芦单抗。在一些实施方案中,cd137激动剂是乌托鲁单抗。
[0746]
在一些实施方案中,免疫检查点分子的激动剂是gitr抑制剂。在一些实施方案中,gitr激动剂是trx518、mk-4166、incagn1876、mk-1248、amg228、bms-986156、gwn323、medi1873或medi6469。在一些实施方案中,免疫检查点分子的激动剂是ox40激动剂,例如ox40激动剂抗体或ox40l融合蛋白。在一些实施方案中,抗ox40抗体是incagn01949、medi0562(他利昔珠单抗)、moxr-0916、pf-04518600、gsk3174998、bms-986178或9b12。在一些实施方案中,ox40l融合蛋白是medi6383。
[0747]
在一些实施方案中,免疫检查点分子的激动剂是cd40激动剂。在一些实施方案中,cd40激动剂是cp-870893、adc-1013、cdx-1140、sea-cd40、ro7009789、jnj-64457107、apx-005m或chi lob 7/4。
[0748]
在一些实施方案中,免疫检查点分子的激动剂是icos激动剂。在一些实施方案中,icos激动剂是gsk-3359609、jtx-2011或medi-570。
[0749]
在一些实施方案中,免疫检查点分子的激动剂是cd28激动剂。在一些实施方案中,cd28激动剂是替拉珠单抗(theralizumab)。
[0750]
在一些实施方案中,免疫检查点分子的激动剂是cd27激动剂。在一些实施方案中,cd27激动剂是伐立鲁单抗(varlilumab)。
[0751]
在一些实施方案中,免疫检查点分子的激动剂是tlr7/8激动剂。在一些实施方案中,tlr7/8激动剂是medi9197。
[0752]
本公开化合物可与双特异性抗体组合使用。在一些实施方案中,双特异性抗体的一个结构域靶向pd-1、pd-l1、ctla-4、gitr、ox40、tim3、lag3、cd137、icos、cd3或tgfβ受体。在一些实施方案中,双特异性抗体结合至pd-1和pd-l1。在一些实施方案中,结合至pd-1和pd-l1的双特异性抗体是mcla-136。在一些实施方案中,双特异性抗体结合至pd-l1和ctla-4。在一些实施方案中,结合至pd-l1和ctla-4的双特异性抗体是ak104。
[0753]
在一些实施方案中,本公开化合物可与一种或多种代谢酶抑制剂组合使用。在一些实施方案中,代谢酶抑制剂是ido1、tdo或精氨酸酶的抑制剂。ido1抑制剂的实例包括艾卡哚司他、nlg919、bms-986205、pf-06840003、iom2983、rg-70099和ly338196。精氨酸酶抑制剂的抑制剂包括incb1158。
[0754]
如本文所提供,额外化合物、抑制剂、剂等可与本公开化合物组合成单一或连续剂型,或其可作为单独剂型同时或依序施用。
[0755]
在一些实施方案中,本文所述的化合物可与一种或多种剂组合用于治疗疾病,诸如癌症。在一些实施方案中,所述剂是烷基化剂、蛋白酶体抑制剂、皮质类固醇或免疫调节剂。烷基化剂的实例包括环磷酰胺(cy)、美法仑(mel)和苯达莫司汀。在一些实施方案中,蛋白酶体抑制剂是卡非佐米。在一些实施方案中,皮质类固醇是地塞米松(dex)。在一些实施方案中,免疫调节剂是来那度胺(len)或泊马度胺(pom)。
[0756]
预期与本公开化合物组合使用的合适抗病毒剂可包含核苷和核苷酸逆转录酶抑制剂(nrti)、非核苷逆转录酶抑制剂(nnrti)、蛋白酶抑制剂和其他抗病毒药物。
[0757]
合适nrti的实例包括齐多夫定(azt);去羟肌苷(ddl);扎西他滨(ddc);司他夫定(d4t);拉米夫定(3tc);阿巴卡韦(1592u89);阿德福韦酯[双(pom)-pmea];洛布卡韦(bms-180194);bch-10652;恩曲他滨[(-)-ftc];β-l-fd4(也称作β-l-d4c并命名为β-l-2’,3
’‑
双脱氧-5-氟-胞苷);dapd,((-)-β-d-2,6,-二氨基-嘌呤二氧戊环);和洛德腺苷(fdda)。典型合适nnrti包括纳韦拉平(bi-rg-587);地拉韦啶(bhap,u-90152);依法韦仑(dmp-266);pnu-142721;ag-1549;mkc-442(1-(乙氧基-甲基)-5-(1-甲基乙基)-6-(苯基甲基)-(2,4(1h,3h)-嘧啶二酮);和(+)-胡桐素a(nsc-675451)和b。典型合适蛋白酶抑制剂包括沙奎那韦(ro 31-8959);瑞托那韦(abt-538);印地那韦(mk-639);纳非那韦(ag-1343);安瑞那韦(141w94);拉西那韦(bms-234475);dmp-450;bms-2322623;abt-378;和ag-1 549。其他抗病毒剂包括羟基脲、利巴韦林、il-2、il-12、喷他夫西和伊萨姆项目号11607。
[0758]
与本文所述的化合物组合用于治疗癌症的合适剂包括化学治疗剂、靶向癌症疗法、免疫疗法或放射疗法。本文所述的化合物可与抗激素剂组合有效用于治疗乳腺癌和其他肿瘤。合适实例是抗雌激素剂(包括但不限于他莫昔芬和托瑞米芬)、芳香酶抑制剂(包括
但不限于来曲唑、阿那曲唑和依西美坦)、肾上腺皮质类固醇(例如泼尼松)、黄体素(例如乙酸甲地孕酮)和雌激素受体拮抗剂(例如氟维司群)。用于治疗前列腺和其他癌症的合适抗激素剂也可与本文所述的化合物组合。这些包括抗雄激素(包括但不限于氟他胺、比卡鲁胺和尼鲁米特)、黄体激素释放激素(lhrh)类似物(包括亮丙瑞林、戈舍瑞林、曲普瑞林和组胺瑞林)、lhrh拮抗剂(例如地加瑞克)、雄激素受体阻断剂(例如恩杂鲁胺)和抑制雄激素产生的剂(例如阿比特龙)。
[0759]
本文所述的化合物可与针对膜受体激酶的其他剂组合或依序使用,尤其用于已发展对靶向疗法的原发性或获得性抗性的患者。这些治疗剂包括针对egfr、her2、vegfr、c-met、ret、igfr1或flt-3和针对诸如bcr-abl和eml4-alk的癌症相关融合蛋白激酶的抑制剂或抗体。针对egfr的抑制剂包括吉非替尼和厄洛替尼,并且针对egfr/her2的抑制剂包括但不限于达克替尼、阿法替尼、拉帕替尼和来那替尼。针对egfr的抗体包括但不限于西妥昔单抗、帕尼单抗和耐昔妥珠单抗。c-met的抑制剂可与fgfr抑制剂组合使用。这些包括奥纳珠单抗、替伐替尼和inc-280。针对abl(或bcr-abl)的剂包括伊马替尼、达沙替尼、尼洛替尼和普纳替尼并且针对alk(或eml4-alk)的那些包括克唑替尼。
[0760]
血管生成抑制剂与fgfr抑制剂组合可在一些肿瘤中有效。这些包括针对vegf或vegfr的抗体或vegfr的激酶抑制剂。针对vegf的抗体或其他治疗蛋白包括贝伐珠单抗和阿帕西普。vegfr激酶抑制剂和其他抗血管生成抑制剂包括但不限于舒尼替尼、索拉非尼、阿昔替尼、西地尼布、帕唑帕尼、瑞格非尼、布立尼布和凡德他尼
[0761]
胞内信号传导通路的激活在癌症中频繁发生,并且靶向这些通路的组分的剂已与受体靶向剂组合以增强功效并降低抗性。可与本文所述的化合物组合的剂的实例包括pi3k-akt-mtor通路抑制剂、raf-mapk通路抑制剂、jak-stat通路抑制剂以及蛋白伴侣蛋白和细胞周期进展的抑制剂。
[0762]
针对pi3激酶的剂包括但不限于托普拉利司(topilaralisib)、艾代拉利司(idelalisib)、布帕利司(buparlisib)。诸如雷帕霉素、西罗莫司、坦西莫司和依维莫司的mtor抑制剂可与fgfr抑制剂组合。其他合适实例包括但不限于维罗非尼和达拉非尼(raf抑制剂)和曲美替尼、司美替尼和gdc-0973(mek抑制剂)。一种或多种jak(例如芦可替尼、巴瑞替尼、托法替尼)、hsp90(例如坦螺旋霉素)、细胞周期素依赖性激酶(例如帕博西尼)、hdac(例如帕比司他)、parp(例如奥拉帕尼)和蛋白酶体(例如硼替佐米、卡非佐米)抑制剂也可与本文所述的化合物组合。在一些实施方案中,jak抑制剂对jak1的选择性超过jak2和jak3。
[0763]
与本文所述的化合物组合使用的其他合适剂包括化学疗法组合,诸如用于肺癌和其他实性肿瘤的基于铂的双药(顺铂或卡铂加吉西他滨;顺铂或卡铂加多西他赛;顺铂或卡铂加太平洋紫杉醇;顺铂或卡铂加培美曲塞)或吉西他滨加太平洋紫杉醇结合粒子
[0764]
合适化学治疗剂或其他抗癌剂包括例如烷基化剂(包括但不限于氮芥、乙烯亚胺衍生物、烷基磺酸盐、亚硝基脲和三氮烯),诸如尿嘧啶氮芥、恩比兴、环磷酰胺(cytoxan
tm
)、异环磷酰胺、美法仑、苯丁酸氮芥、哌泊溴烷、三亚乙基-三聚氰胺、三亚乙基硫代磷酰胺、白消安、卡莫司汀、洛莫司汀、链脲佐菌素、达卡巴嗪和替莫唑胺。
[0765]
与本文所述的化合物组合使用的其他合适剂包括类固醇,包括17α-乙炔基雌二
醇、己烯雌酚、睾酮、泼尼松、氟甲睾酮、甲泼尼龙、甲基睾酮、泼尼松龙、曲安奈德、氯烯雌醚、羟孕酮、胺鲁米特和乙酸甲羟孕酮。
[0766]
与本文所述的化合物组合使用的其他合适剂包括:达卡巴嗪(dtic),任选地连同其他化学疗法药物,诸如卡莫司汀(bcnu)和顺铂;“dartmouth方案”,其由dtic、bcnu、顺铂和他莫昔芬组成;顺铂、长春花碱和dtic的组合;或替莫唑胺。本文所述的化合物亦可与免疫疗法药物,包括细胞因子,诸如干扰素α、白介素2和肿瘤坏死因子(tnf)组合。
[0767]
合适化学治疗剂或其他抗癌剂包括例如抗代谢物(包括但不限于叶酸拮抗剂、嘧啶类似物、嘌呤类似物和腺苷去胺酶抑制剂),诸如甲氨喋呤、5-氟脲苷、脱氧氟脲苷、阿糖胞苷、6-巯基嘌呤、6-硫鸟嘌呤、磷酸氟达拉滨、喷司他汀和吉西他滨。
[0768]
合适化学治疗剂或其他抗癌剂进一步包括例如某些天然产物及其衍生物(例如长春花生物碱、抗肿瘤抗生素、酶、淋巴因子和表鬼臼毒素),诸如长春花碱、长春新碱、长春地辛、博来霉素、放线菌素d、道诺霉素、多柔比星、表柔比星、伊达比星、ara-c、太平洋紫杉醇(taxol
tm
)、光神霉素、去氧助间型霉素、丝裂霉素-c、l-天冬酰胺酶、干扰素(尤其ifn-a)、依托泊苷和替尼泊苷。
[0769]
其他细胞毒性剂包括诺维本、cpt-11、阿那曲唑、来曲唑、卡培他滨、雷洛昔芬、环磷酰胺、异环磷酰胺和卓洛昔芬。
[0770]
细胞毒性剂,诸如表鬼臼毒素;抗肿瘤酶;拓扑异构酶抑制剂;丙卡巴肼;米托蒽醌;铂配位复合物,诸如顺铂和卡铂;生物反应调节剂;生长抑制剂;抗激素治疗剂;甲酰四氢叶酸;替加氟;和造血生长因子也是合适的。
[0771]
其他抗癌剂包括抗体治疗剂,诸如曲妥珠单抗(herceptin)、共刺激分子抗体(诸如ctla-4、4-1bb、pd-l1和pd-1抗体)或细胞因子(il-10、tgf-β等)抗体。
[0772]
其他抗癌剂还包括阻断免疫分子迁移的那些,诸如趋化因子受体(包括ccr2和ccr4)的拮抗剂。
[0773]
其他抗癌剂还包括增加免疫系统的那些,诸如佐剂或过继性t细胞转移。
[0774]
抗癌疫苗包括树突状细胞、合成肽、dna疫苗和重组病毒。在一些实施方案中,肿瘤疫苗包括来自涉及人癌症的病毒,诸如人乳头状瘤病毒(hpv)、肝炎病毒(hbv和hcv)和卡波西氏疱疹肉瘤病毒(khsv)的蛋白质。可使用的肿瘤疫苗的非限制性实例包括黑色素瘤抗原的肽,诸如gp100、mage抗原、trp-2、marti和/或酪氨酸酶的肽,或经转染以表达细胞因子gm-csf的肿瘤分子。
[0775]
本公开化合物可与骨髓移植组合用于治疗造血系统起源的多种肿瘤。
[0776]
本领域技术人员已知用于大多数这些化学治疗剂的安全且有效施用的方法。另外,其施用描述于标准文献中。例如,多种化学治疗剂的施用描述于“physicians’desk reference”(pdr,例如1996版,medical economics company,montvale,nj)中,所述文献的公开内容以引用的方式并入本文,就如同整体陈述一样。
[0777]
如本文所提供,额外化合物、抑制剂、剂等可与本公开化合物组合成单一或连续剂型,或其可作为单独剂型同时或依序施用。
[0778]
药物制剂和剂型
[0779]
当作为药物采用时,本文所述的化合物可以药物组合物形式施用,所述形式是指一种或多种本文所述的化合物和至少一种药学上可接受的载剂或赋形剂的组合。这些组合
物可以制药领域众所周知的方式制备,并且可通过多种途径施用,这取决于是否需要局部或全身性治疗以及取决于要治疗的区域。施用可以是局部(包括眼科和至粘膜,包括鼻内、阴道和直肠递送)、肺(例如通过粉剂或气雾剂的吸入或吹入,包括通过喷雾器;气管内、鼻内、表皮和经皮)、眼睛、口服或胃肠外施用。用于眼睛递送的方法可包括局部施用(滴眼剂)、通过以外科手术方式置于结膜囊中的气囊导管或眼科插入物进行的结膜下、眼周或玻璃体内注射或引入。胃肠外施用包括静脉内、动脉内、皮下、腹膜内或肌肉内注射或输注;或颅内(例如鞘内或室内)施用。胃肠外施用可呈单一推注剂量的形式,或可例如通过连续灌注泵。用于局部施用的药物组合物和制剂可包括经皮贴剂、软膏、洗剂、乳膏、凝胶、滴剂、栓剂、喷雾剂、液体和粉剂。常规药物载剂、水性、粉末或油性基质、增稠剂等可以是必需或所期望的。
[0780]
本公开还包括含有与一种或多种药学上可接受的载剂或赋形剂组合的作为活性成分的一种或多种本文所述的化合物的药物组合物。在制备本文所述的组合物时,活性成分典型地与赋形剂混合,通过赋形剂稀释或以例如胶囊、药包、纸或其他容器的形式封入这样的载剂内。当赋形剂充当稀释剂时,其可以是固体、半固体或液体材料,所述材料充当用于活性成分的媒介物、载剂或介质。因此,所述组合物可呈片剂、丸剂、粉剂、锭剂、药包、扁囊剂、酏剂、混悬液、乳液、溶液、糖浆、气雾剂(作为固体或在液体介质中)、含有例如按重量计多至10%活性化合物的软膏、软和硬明胶胶囊、栓剂、无菌可注射溶液和无菌包装粉剂的形式。在一些实施方案中,组合物适用于局部施用。
[0781]
在制备制剂时,在与其他成分组合之前,可研磨活性化合物以提供适当粒径。如果活性化合物实质上是不溶性的,则可将其研磨至小于200目的粒径。如果活性化合物实质上是水溶性的,则粒径可通过研磨来调整以提供制剂中的实质上均一分布,例如约40目。
[0782]
本发明化合物可使用诸如湿磨的已知研磨程序进行研磨以获得适用于片剂形成并且适用于其他制剂类型的粒径。本发明化合物的精细分散(纳米颗粒)制剂可通过本领域已知的方法来制备,参见例如wo 2002/000196。
[0783]
合适赋形剂的一些实例包括乳糖、右旋糖、蔗糖、山梨糖醇、甘露糖醇、淀粉、阿拉伯胶、磷酸钙、藻酸盐、黄蓍胶、明胶、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮、纤维素、水、糖浆和甲基纤维素。所述制剂可另外包括:润滑剂,诸如滑石、硬脂酸镁和矿物油;润湿剂;乳化和助悬剂;防腐剂,诸如甲基-和丙基羟基-苯甲酸酯;甜味剂;和调味剂。可配制本文所述的组合物以便在通过使用本领域已知的程序施用于患者之后提供活性成分的快速、持续或延迟释放。
[0784]
在一些实施方案中,药物组合物包含硅化微晶纤维素(smcc)和至少一种本文所述的化合物,或其药学上可接受的盐。在一些实施方案中,硅化微晶纤维素包含约98%微晶纤维素和约2%二氧化硅w/w。
[0785]
在一些实施方案中,组合物是包含至少一种本文所述的化合物或其药学上可接受的盐,和至少一种药学上可接受的载剂或赋形剂的持续释放组合物。在一些实施方案中,组合物包含至少一种本文所述的化合物或其药学上可接受的盐,和选自微晶纤维素、乳糖一水合物、羟基丙基甲基纤维素和聚环氧乙烷的至少一种组分。在一些实施方案中,组合物包含至少一种本文所述的化合物或其药学上可接受的盐,和微晶纤维素、乳糖一水合物和羟基丙基甲基纤维素。在一些实施方案中,组合物包含至少一种本文所述的化合物或其药学
上可接受的盐,和微晶纤维素、乳糖一水合物和聚环氧乙烷。在一些实施方案中,组合物还包含硬脂酸镁或二氧化硅。在一些实施方案中,微晶纤维素是avicel ph102
tm
。在一些实施方案中,乳糖一水合物是fast-flo 316
tm
。在一些实施方案中,羟基丙基甲基纤维素是羟基丙基甲基纤维2208k4m(例如methocel k4 m premier
tm
)和/或羟基丙基甲基纤维素2208k100lv(例如methocel k00lv
tm
)。在一些实施方案中,聚环氧乙烷是聚环氧乙烷wsr 1105(例如polyox wsr 1105
tm
)。
[0786]
在一些实施方案中,使用湿式造粒工艺来产生组合物。在一些实施方案中,使用干式造粒工艺来产生组合物。
[0787]
组合物可以单位剂型进行调配,每个剂量含有例如约5mg至约1000mg、约5mg至约100mg、约100mg至约500mg或约10至约30mg活性成分。在一些实施方案中,每个剂量含有约10mg活性成分。在一些实施方案中,每个剂量含有约50mg活性成分。在一些实施方案中,每个剂量含有约25mg活性成分。术语“单位剂型”是指适合作为单位剂量用于人受试者和其他哺乳动物的物理离散单位,每个单位含有预定量的活性材料,所述预定量经计算以产生与合适药物赋形剂相关的所需治疗效果。
[0788]
用于配制药物组合物的组分具有高纯度并且实质上不含潜在有害的污染物(例如至少国家食品级,一般地至少分析级,并且更典型地至少药品级)。尤其对于人类消耗,组合物优选地在如美国食品和药物管理局(u.s.food and drug administration)的适用法规所定义的良好制造规范标准下制造或配制。例如,合适制剂可以是无菌的和/或实质上等渗的和/或完全遵守美国食品和药物管理局的所有良好制造规范法规。
[0789]
活性化合物可在宽剂量范围内有效并且一般地以药学有效量施用。然而,应理解实际上施用的化合物的量通常将由医师根据相关情况,包括要治疗的疾患、所选施用途径、施用的实际化合物、个别患者的年龄、体重和反应、患者症状的严重程度等来确定。
[0790]
本发明化合物的治疗剂量可根据例如进行治疗所针对的特定用途、化合物的施用方式、患者的健康和疾患以及处方医师的判断而变化。本发明化合物在药物组合物中的比例或浓度可根据多种因素,包括剂量、化学特征(例如疏水性)和施用途径而变化。例如,本公开化合物可在含有约0.1至约10%w/v所述化合物的水性生理缓冲溶液中提供以供胃肠外施用。一些典型剂量范围为约1μg/kg至约1g/kg体重/天。在一些实施方案中,剂量范围为约0.01mg/kg至约100mg/kg体重/天。剂量有可能取决于诸如疾病或病症的类型和进展程度、特定患者的总体健康状况、所选化合物的相对生物功效、赋形剂的配制及其施用途径的变量。有效剂量可从来源于体外或动物模型测试系统的剂量-反应曲线推断。
[0791]
关于制备诸如片剂的固体组合物,主要活性成分与药物赋形剂混合以形成含有一种或多种本文所述的化合物的均质混合物的预配制组合物。当将这些预配制组合物称为均质时,活性成分典型地均匀分散在整个组合物中,使得组合物可容易地细分成同样有效的单位剂型,诸如片剂、丸剂和胶囊。这种固体预制剂然后细分成上述类型的单位剂型,含有例如0.1至约500mg本公开的活性成分。
[0792]
本公开的片剂或丸剂可被包衣或以其他方式混配以提供具有延长作用的优势的剂型。例如,片剂或丸剂可包含内部剂量和外部剂量组分,后者呈前者上方的包膜形式。两种组分可通过肠溶层分离,所述肠溶层用于抵抗胃中的崩解并且允许内部组分完整传递至十二指肠中或延迟释放。多种材料可用于此类肠溶层或包衣,此类材料包括多种聚合物酸
和聚合物酸与诸如虫胶、鲸蜡醇和乙酸纤维素的材料的混合物。
[0793]
其中可掺入如本文所述的化合物或组合物以供口服或通过注射施用的液体形式包括水溶液、适当调味的糖浆、水性或油性混悬液和用诸如棉籽油、芝麻油、椰子油或花生油的食用油调味的乳液,以及酏剂和类似药物媒介物。
[0794]
用于吸入或吹入的组合物包括药学上可接受的水性或有机溶剂或其混合物中的溶液和混悬液,以及粉末。液体或固体组合物可含有如上文所述的合适的药学上可接受的赋形剂。在一些实施方案中,组合物通过口服或鼻呼吸途径施用以实现局部或全身性作用。可通过使用惰性气体将其中的组合物雾化。雾化溶液可直接地从雾化装置呼吸,或雾化装置可连接至面罩或间歇正压呼吸机。溶液、混悬液或粉末组合物可口服或经鼻从以适当方式递送所述制剂的装置施用。
[0795]
局部制剂可含有一种或多种常规载剂。在一些实施方案中,软膏可含有水,和选自例如液体石蜡、聚氧乙烯烷基醚、丙二醇、白凡士林等的一种或多种疏水性载剂。乳膏的载剂组合物可基于水与甘油和一种或多种其他组分(例如单硬脂酸甘油酯、peg-单硬脂酸甘油酯和鲸蜡硬脂醇)的组合。凝胶可使用适当地与诸如甘油、羟基乙基纤维素等的其他组分组合的异丙醇和水进行配制。在一些实施方案中,局部制剂含有至少约0.1、至少约0.25、至少约0.5、至少约1、至少约2或至少约5wt%的本发明化合物。局部制剂可适当地包装在例如100g管中,所述管附有任选地与关于所选适应症(例如牛皮癣或其他皮肤疾患)的治疗的说明书。
[0796]
施用于患者的化合物或组合物的量将根据正在施用的内容、施用目的(诸如预防或治疗)、患者状态、施用方式等而变化。在治疗应用中,组合物可以足以治愈或至少部分地遏制疾病及其并发症的症状的量施用于已经罹患所述疾病的患者。有效剂量将取决于正在治疗的疾病状况,以及临床医师根据诸如疾病的严重程度、患者的年龄、体重和一般状况等的因素做出的判断。
[0797]
施用于患者的组合物可呈上文所述的药物组合物形式。这些组合物可通过常规灭菌技术灭菌,或可以无菌过滤。水溶液可包装以供原样使用,或被冻干,冻干制剂在施用之前与无菌水性载剂组合。化合物制剂的ph将典型地在3与11之间,更优选地为5至9并且最优选地为7至8。应理解,某些前述赋形剂、载剂或稳定剂的使用将导致形成药用盐。
[0798]
本公开化合物的治疗剂量可根据例如进行治疗所针对的特定用途、化合物的施用方式、患者的健康和疾患以及处方医师的判断而变化。化合物在药物组合物中的比例或浓度可根据多种因素,包括剂量、化学特征(例如疏水性)和施用途径而变化。例如,本公开化合物可在含有约0.1至约10%w/v化合物的水性生理缓冲溶液中提供以供胃肠外施用。一些典型剂量范围为约1μg/kg至约1g/kg体重/天。在一些实施方案中,剂量范围为约0.01mg/kg至约100mg/kg体重/天。剂量有可能取决于诸如疾病或病症的类型和进展程度、特定患者的总体健康状况、所选化合物的相对生物功效、赋形剂的配制及其施用途径的变量。有效剂量可从来源于体外或动物模型测试系统的剂量-反应曲线推断。
[0799]
本文所述的化合物还可与一种或多种额外活性成分组合配制,所述额外活性成分可包括任何药剂,诸如抗病毒剂、疫苗、抗体、免疫增强剂、免疫抑制剂、消炎剂等。
[0800]
标记化合物和测定方法
[0801]
本发明的另一个方面系关于本公开的标记化合物(放射性标记、荧光标记等),所
述化合物将不仅可用于成像技术,而且可用于体外和体内测定,以供定位和量化组织样品(包括人)中的fgfr3蛋白,以及供通过标记化合物的抑制结合来鉴定fgfr3配体。本公开化合物的一个或多个原子的取代也可用于产生区分的adme(吸附、分布、代谢和排泄)。因此,本发明包括含有此类标记或取代化合物的fgfr结合测定。
[0802]
本公开还包括同位素标记的本公开化合物。“同位素标记”或“放射性标记”化合物是本公开化合物,其中一个或多个原子被原子质量或质量数不同于典型地在自然界中发现(即,天然存在)的原子质量或质量数的原子替换或取代。可掺入本公开化合物中的合适放射性核素包括但不限于2h(对于氘也写为d)、3h(对于氚也写为t)、
11
c、
13
c、
14
c、
13
n、
15
n、
15
o、
17
o、
18
o、
18
f、
35
s、
36
cl、
82
br、
75
br、
76
br、
77
br、
123
i、
124
i、
125
i和
131
i。例如,本公开化合物中的一个或多个氢原子可被氘原子替换(例如,式(i)的c
1-6
烷基的一个或多个氢原子可任选地被氘原子取代,诸如
–
cd3取代
–
ch3)。在一些实施方案中,式(i)中的烷基可被全氘化。
[0803]
本文所呈现的化合物的一个或多个组成原子可被具有天然或非天然丰度的原子同位素替换或取代。在一些实施方案中,化合物包括至少一个氘原子。在一些实施方案中,该合物包括两个或更多个氘原子。在一些实施方案中,化合物包括1-2、1-3、1-4、1-5或1-6个氘原子。在一些实施方案中,化合物中的所有氢原子均可被氘原子替换或取代。
[0804]
本领域已知用于将同位素包括在有机化合物中的合成方法(deuterium labeling in organic chemistry,alan f.thomas(new york,n.y.,appleton-century-crofts,1971;the renaissance of h/d exchange,jens atzrodt,volker derdau,thorsten fey和jochen zimmermann,angew.chem.int.ed.2007,7744-7765;the organic chemistry of isotopic labelling,james r.hanson,royal society of chemistry,2011)。同位素标记化合物可用于各种研究,诸如nmr光谱法、代谢实验和/或测定。
[0805]
用诸如氘的较重同位素取代可提供由较大代谢稳定性引起的某些治疗优势,例如增加的体内半衰期或降低的剂量需求,并且因此可在一些情况下是优选的。(参见例如a.kerekes等人j.med.chem.2011,54,201-210;r.xu等人j.label compd.radiopharm.2015,58,308-312)。具体地说,一个或多个代谢位点处的取代可提供一种或多种治疗优势。
[0806]
掺入本发明放射性标记化合物中的放射性核素将取决于所述放射性标记化合物的具体应用。例如,在体外腺苷受体标记和竞争测定中,掺入3h、
14
c、
82
br、
125
i、
131
i或
35
s的化合物可以是有用的。对于放射性成像应用,
11
c、
18
f、
125
i、
123
i、
124
i、
131
i、
75
br、
76
br或
77
br可以是有用的。
[0807]
应理解,“放射性标记”或“标记化合物”是已掺入至少一种放射性核素的化合物。在一些实施方案中,放射性核素选自由3h、
14
c、
125
i、
35
s和
82
br组成的组。
[0808]
本公开还可包括用于将放射性同位素掺入本公开化合物中的合成方法。用于将放射性同位素掺入有机化合物中的合成方法是本领域众所周知的,并且本领域普通技术人员将容易地识别可用于本公开化合物的方法。
[0809]
本公开的标记化合物可用于筛选测定以鉴定和/或评估化合物。例如,标记的新合成或鉴定化合物(即,测试化合物)可通过追踪标记监测当与fgfr3蛋白接触时的其浓度变化来评估其结合fgfr3的能力。例如,可评估测试化合物(标记的)降低已知结合至fgfr3蛋白(即,标准化合物)的另一种化合物的结合的能力。因此,测试化合物与标准化合物竞争结
合至fgfr3蛋白的能力直接地与其结合亲和力相关。相反,在一些其他筛选测定中,标准化合物被标记而测试化合物未被标记。因此,监测标记标准化合物的浓度以便评估标准化合物与测试化合物之间的竞争,并且因此确定测试化合物的相对结合亲和力。
[0810]
药盒
[0811]
本公开还包括可用于例如治疗或预防fgfr相关疾病或病症,诸如癌症和本文中所提及的其他疾病的药盒,其包括含有包含治疗有效量的本公开化合物的药物组合物的一个或多个容器。如需要,此类药盒还可包括各种常规药盒组分中的一种或多种,诸如具有一种或多种药学上可接受的载剂的容器、额外容器等,如本领域技术人员将显而易见。作为插页或作为标签的说明书也可包括在药盒中,指示要施用的组分的量、关于施用的指南和/或关于混合所述组分的指南。
[0812]
本公开将通过具体实施例更详细地加以描述。以下实施例出于说明性目的提供,并且不意图以任何方式限制本发明。本领域技术人员将容易地识别多种非关键参数,所述参数可发生变化或修改以产生基本上相同结果。如下文所述,发现实施例的化合物是fgfr3抑制剂。
[0813]
实施例
[0814]
关于本发明化合物的实验程序提供于下文中。在waters质量导向分级分离系统上进行所制备的一些化合物的制备型lc-ms纯化。关于这些系统的操作的基础设备设置、方案和控制软件已详细地描述于文献中。参见例如“two-pump at column dilution configuration for preparative lc-ms”,k.blom,j.combi.chem.,4,295(2002);“optimizing preparative lc-ms configurations and methods for parallel synthesis purification”,k.blom,r.sparks,j.doughty,g.everlof,t.haque,a.combs,j.combi.chem.,5,670(2003);和“preparative lc-ms purification:improved compound specific method optimization”,k.blom,b.glass,r.sparks,a.combs,j.combi.chem.,6,874-883(2004)。所分离的化合物典型地在以下条件下经历分析型液相色谱质谱分析(lcms)以供纯度分析:仪器;agilent 1100系列,lc/msd,柱:waters sunfire
tm c
18 5μm,2.1
×
50mm,缓冲液:流动相a:含0.025%tfa的水和流动相b:乙腈;梯度2%-80%b,3分钟,流动速率2.0ml/分钟。
[0815]
所制备的一些化合物还通过使用ms检测器的反相高效液相色谱(rp-hplc)或快速色谱(硅胶)以制备规模被分离,如实施例中所指定。典型制备型反相高效液相色谱(rp-hplc)柱条件如下:
[0816]
ph=2纯化:waters sunfire
tm c
18 5μm,19
×
100mm柱,用流动相a:含0.1%tfa(三氟乙酸)的水和流动相b:乙腈洗脱;流动速率为30ml/分钟,分离梯度使用如文献中所描述的化合物特异性方法优化方案(compound specific method optimization protocol)针对每种化合物进行优化[参见“preparative lcms purification:improved compound specific method optimization”,k.blom,b.glass,r.sparks,a.combs,j.comb.chem.,6,874-883(2004)]。典型地,与30
×
100mm柱一起使用的流动速率为60ml/分钟。
[0817]
ph=10纯化:waters xbridge c
18 5μm,19
×
100mm柱,用流动相a:含0.15%nh4oh的水和流动相b:乙腈洗脱;流动速率为30ml/分钟,分离梯度使用如文献中所述的化合物特异性方法优化方案针对每种化合物优化[参见“preparative lcms purification:
羧酸叔丁酯
[0839][0840]
将5-氯-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(8.73g,21.31mmol)、1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑(5.32g,25.6mmol)、pdcl2(dppf)-ch2cl2加合物(3.48g,4.26mmol)和磷酸钾(6.79g,32.0mmol)置于烧瓶中并且将烧瓶抽真空并用n2回填三次。然后添加1,4-二噁烷(150ml)和水(15ml)并且将反应在80℃下搅拌1h。在冷却至室温之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过biotage isolera纯化。对于c
16h19
cln5o3(m+h)
+
,lcms计算值:m/z=364.1;实验值:364.0。
[0841]
步骤8. 5-(2,3-二甲基苯基)-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[0842]
将5-氯-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(8mg,0.022mmol)、(2,3-二甲基苯基)硼酸(4.95mg,0.033mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(1.7mg,2.2μmol)和磷酸钾(9.34mg,0.044mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(1ml)和水(100μl)之后,将反应混合物在100℃下搅拌1h。然后过滤反应,并且在真空中蒸发溶剂。添加dcm(1ml)和tfa(0.5ml)并且将反应混合物在室温下搅拌30min。其然后用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
19h20
n5o(m+h)
+
,lcms计算值:m/z=334.2;实验值:334.2。1h nmr(500mhz,dmso-d6)δ8.27(s,1h),8.00(s,1h),7.45(s,1h),7.25
–
7.20(m,1h),7.19
–
7.14(t,j=7.5hz,1h),7.12
–
7.09(m,1h),3.89(s,3h),3.82(s,3h),2.31(s,3h),1.96(s,3h)ppm。
[0843]
实施例2. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[0844][0845]
此化合物根据实施例1中所描述的程序,使用2-(2,3-二氢-1h-茚-4-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环替代(2,3-二甲基苯基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
20h20
n5o(m+h)
+
,lcms计算值:m/z=346.2;实验值:346.2。1h nmr(500mhz,dmso-d6)δ8.34
–
8.29(s,1h),8.09
–
8.01(s,1h),7.51
–
7.44(s,1h),7.30
–
7.25(m,2h),7.25
–
7.19(m,1h),3.94
–
3.90(s,3h),3.90
–
3.84(s,3h),2.99
–
2.91(t,j=7.4hz,2h),2.85
–
2.75(t,j=7.4hz,2h),2.02
–
1.91(p,j=7.4hz,2h)ppm。
[0846]
实施例3. 5-(2,3-二甲基苯基)-6-甲氧基-3-(1-((1-甲基-1h-1,2,4-三唑-5-基)甲基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[0847][0848]
步骤1. 5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-3-(1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[0849][0850]
向5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(实施例69,100mg,0.2mmol)于1,4-二噁烷(3ml)和水(0.3ml)中的溶液中添加4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑(118mg,0.4mmol)、磷酸钾(128mg,0.6mmol)和[1,1
’‑
双(二苯基膦基)二茂铁]-二氯化钯(ii)(1:1)(16mg,0.02mmol)。将反应用n2吹扫并在80℃下搅拌2h。此后,将其冷却至室温并用etoac稀释。然后依序用水、饱和nacl溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以提供所需产物。对于c
26h26
n5o2(m+h)+,lc-ms计算值:m/z=440.2;实验值440.2。
[0851]
步骤2. 5-(2,3-二甲基苯基)-6-甲氧基-3-(1-((1-甲基-1h-1,2,4-三唑-5-基)甲基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[0852]
向5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-3-(1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶(90mg,0.2mmol)于乙腈(3ml)中的溶液中添加5-(氯甲基)-1-甲基-1h-1,2,4-三唑(70mg,0.53mmol)和碳酸铯(400mg,1.23mmol)。将反应在80℃下搅拌12h。此后,将其冷却至室温并用etoac稀释。然后依序用水、饱和nacl溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物溶解于tfa(1ml)中并加热至80℃持续1h。然后将反应混合物用meoh稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
22h23
n8o(m+h)
+
,lc-ms计算值:m/z=415.2;实验值415.2。1h nmr(600mhz,dmso-d6)δ8.55
–
8.45(s,1h),8.14
–
8.03(s,1h),7.93
–
7.82(s,1h),7.52
–
7.42(s,1h),7.25
–
7.21(d,j=7.5hz,1h),7.19
–
7.14(t,j=7.5hz,1h),7.13
–
7.08(d,j=7.5hz,1h),5.75
–
5.60(s,2h),3.91
–
3.86(s,2h),3.86
–
3.76(s,3h),2.34
–
2.27(s,3h),2.01
–
1.90(s,3h)ppm。
[0853]
实施例4. 5-(2,3-二氢苯并呋喃-7-基)-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[0854][0855]
此化合物根据实施例1中所描述的程序,使用(2,3-二氢苯并呋喃-7-基)硼酸替代(2,3-二甲基苯基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
19h18
n5o2(m+h)
+
,lcms计算值:m/z=348.1;实验值:348.1。1h nmr(500mhz,dmso-d6)δ8.33
–
8.29(s,1h),8.06
–
8.02(s,1h),7.45
–
7.40(s,1h),7.31
–
7.25(d,j=5.8hz,1h),7.21
–
7.16(d,j=6.3hz,1h),6.96
–
6.86(t,j=7.5hz,1h),4.54
–
4.44(t,j=8.7hz,2h),3.94
–
3.90(s,3h),3.87
–
3.82(s,3h),3.29
–
3.20(t,j=8.7hz,2h)ppm。
[0856]
中间体1. 2-(2-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)苯基)乙腈
[0857][0858]
在氮气下向4,4,5,5,4’,4’,5’,5
’‑
八甲基-[2,2’]双[[1,3,2]二氧硼戊环基](1.28g,5.1mmol)、乙酸钾(0.57g,5.83mmol)和[1,1
’‑
双(二苯基膦基)二茂铁]二氯化钯(ii)与二氯甲烷的复合物(1:1)(0.318g,0.389mmol)的混合物中添加2-(3-碘-2-甲基苯基)乙腈(1g,3.89mmol)于1,4-二噁烷(30ml)中的溶液。将反应混合物在氮气下在100℃下搅拌3天。在冷却至室温之后,将混合物用dcm稀释并过滤。在真空中浓缩滤液并且将所得残余物通过biotage isolera纯化以得到所需产物。
[0859]
实施例5. 2-(3-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2-甲基苯基)乙腈
[0860][0861]
此化合物根据实施例1中所描述的程序,使用2-(2-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)苯基)乙腈(中间体1)替代(2,3-二甲基苯基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
20h19
n6o(m+h)
+
,lcms计算值:m/z=359.2;实验值:359.2。1h nmr(500mhz,dmso-d6)δ8.33
–
8.22(s,1h),8.05
–
7.95(s,1h),7.53
–
7.48(s,1h),7.47
–
7.41(d,j=6.8hz,1h),7.36
–
7.30(t,j=7.6hz,1h),7.30
–
7.25(d,j=6.2hz,1h),4.13
–
4.05(s,2h),3.92
–
3.87(s,3h),3.85
–
3.80(s,3h),2.08
–
2.01(s,3h)ppm。
[0862]
中间体2. 4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-1-酚
[0863][0864]
在氮气下向4,4,5,5,4’,4’,5’,5
’‑
八甲基-[2,2’]双[[1,3,2]二氧硼戊环基](626mg,2.46mmol)、乙酸钾(322mg,3.29mmol)和[1,1
’‑
双(二苯基膦基)二茂铁]二氯化钯(ii)与二氯甲烷的复合物(1:1)(201mg,0.246mmol)的混合物中添加4-溴-2,3-二氢-1h-茚-1-酚(350mg,1.643mmol)于1,4-二噁烷(15ml)中的溶液。将反应混合物在氮气下在100℃下搅拌过夜。在冷却至室温之后,将混合物用dcm稀释并过滤。在真空中浓缩滤液并且将所得残余物通过biotage isolera纯化以得到所需产物。
[0865]
实施例6. 1-(4-(5-(6-(二氟甲氧基)-5-(2,3-二甲基苯基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌嗪-1-基)乙-1-酮
[0866][0867]
步骤1. 1-三苯甲基-1h-吡唑并[4,3-b]吡啶-6-醇
[0868][0869]
将6-溴-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(实施例1,步骤1;20g,45.4mmol)、koh(12.74g,227mmol)和
t
buxphos pd g3(0.727g,0.908mmol)于1,4-二噁烷(100ml)水(100ml)中的混合物在100℃下加热3h。此后,将其冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤,经na2so4干燥,过滤并浓缩至干。粗材料不经进一步纯化即用于下一步骤中。对于c
25h20
n3o(m+h)
+
,lcms计算值:m/z=378.2;实验值:378.1。
[0870]
步骤2. 6-(二氟甲氧基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[0871][0872]
在0℃下向1-三苯甲基-1h-吡唑并[4,3-b]吡啶-6-醇(17g,45mmol)和koh(12.62g,225mmol)于乙腈(100ml)和水(10ml)中的混合物中添加(溴二氟甲基)-膦酸二乙酯(16.02ml,90mmol)。在添加之后,将反应在室温下搅拌过夜。然后添加水并且将产物用etoac萃取。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过
biotage isolera纯化。对于c
26h20
f2n3o(m+h)
+
,lcms计算值:m/z=428.2;实验值:428.2。
[0873]
步骤3. 5-氯-6-(二氟甲氧基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[0874][0875]
将3-氯过氧苯甲酸(7.64g,33.2mmol)在0℃下缓慢地添加至6-(二氟甲氧基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(7.1g,16.61mmol)于dcm(100ml)中的溶液中。在室温下搅拌过夜之后,将反应用na2s2o3溶液和1m naoh溶液处理。在室温下搅拌30min之后,分离有机相并用1m naoh溶液洗涤3次并用盐水溶液洗涤2次。有机相经硫酸钠干燥,过滤并在真空中去除溶剂。
[0876]
将所得产物溶解于dcm(100ml)中。在0℃下依序向此溶液中添加diea(7.25ml,41.5mmol)和草酰氯(2.91ml,33.2mmol)。使反应混合物升温至室温并在此温度下搅拌过夜。将反应混合物用dcm稀释并小心地用水处理。分离有机相,用水洗涤3次,用饱和nahco3溶液洗涤2次,用盐水洗涤2次并经硫酸钠干燥。在真空中去除溶剂之后,将粗材料通过biotage isolera纯化。对于c
26h19
clf2n3o(m+h)
+
,lcms计算值:m/z=462.1;实验值:462.1。
[0877]
步骤4. 6-(二氟甲氧基)-5-(2,3-二甲基苯基)-1h-吡唑并[4,3-b]吡啶
[0878][0879]
将5-氯-6-(二氟甲氧基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(2.2g,4.76mmol)、(2,3-二甲基苯基)硼酸(1.072g,7.14mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(0.38g,0.47mmol)和k3po4(2.1g,9.53mmol)置于烧瓶中并且将烧瓶抽真空并用n2回填三次。在添加1,4-二噁烷(20ml)和水(2ml)之后,将反应混合物在100℃下搅拌1h。在冷却至室温之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。
[0880]
将粗材料溶解于tfa(2ml)、dcm(10ml)和水(2ml)中。在室温下搅拌30min之后,添加ch3cn和水并在真空中蒸发dcm。滤出沉淀的固体。将反应混合物进一步用水稀释并用etoac/己烷1:1混合物洗涤3次。分离水相并在真空中去除所有溶剂。将残余物溶解于dcm中并用nahco3溶液中和。将有机相用nahco3溶液洗涤2次,用盐水洗涤1次,经硫酸钠干燥并在真空中浓缩。所得粗产物不经进一步纯化即用于下一步骤中。对于c
15h14
f2n3o(m+h)
+
,lc-ms计算值:m/z=290.1;实验值:290.1。
[0881]
步骤5. 6-(二氟甲氧基)-5-(2,3-二甲基苯基)-3-碘-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[0882][0883]
将1-碘吡咯烷-2,5-二酮(1.5g,6.57mmol)添加至6-(二氟甲氧基)-5-(2,3-二甲基苯基)-1h-吡唑并[4,3-b]吡啶(1.9g,6.57mmol)于dmf(25ml)中的溶液中。在80℃下搅拌1h之后,将反应混合物冷却至室温,并且添加cs2co3(5.35g,16.42mmol)和1-(氯甲基)-4-甲氧基苯(1.714ml,13.14mmol)。在80℃下再搅拌1h之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过biotage isolera纯化。对于c
23h21
f2in3o2(m+h)
+
,lcms计算值:m/z=536.1;实验值:536.1。
[0884]
步骤6. 1-(4-(5-(6-(二氟甲氧基)-5-(2,3-二甲基苯基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌嗪-1-基)乙-1-酮
[0885]
将6-(二氟甲氧基)-5-(2,3-二甲基苯基)-3-碘-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(27mg,0.050mmol)、1-(4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪-1-基)乙-1-酮(56mg,0.17mmol)、xphos pd g2(4mg,5μmol)、磷酸钾(44mg,0.21mmol)于水(0.100ml)和二噁烷(1ml)中的溶液加热至80℃持续2h。此后,将其冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。将残余物溶解于三氟甲磺酸(0.5ml)中。将混合物在室温下搅拌1h,用ch3cn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
26h27
f2n6o2(m+h)+,lcms计算值:m/z=493.2;实验值493.3。1h nmr(500mhz,dmso-d6)δ13.47(s,1h),9.16(d,j=2.2hz,1h),8.50(dd,j=9.0,2.4hz,1h),7.91(s,1h),7.46-7.01(m,5h),3.66
–
3.58(m,8h),2.35(s,3h),2.05(s,3h),2.02(s,3h)ppm。
[0886]
实施例7和实施例8.4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-酚,两种对映体
[0887][0888]
将5-氯-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(35mg,0.096mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-1-酚(32mg,0.12mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(15mg,0.02mmol)和磷酸钾(30mg,0.14mmol)置于小瓶中并且将小瓶
抽真空并用n2回填三次。在添加1,4-二噁烷(2ml)和水(200μl)之后,将反应混合物在100℃下搅拌1h。在冷却至室温之后,将混合物用dcm稀释并过滤。在真空中浓缩滤液并且将所得残余物通过biotage isolera纯化。
[0889]
将纯化的材料再溶解于1,4-二噁烷(2ml)和水(2ml)中。在添加碳酸铯(31.3mg,0.096mmol)和吗啉(0.3ml)之后,将反应混合物在100℃下加热2h。在冷却至室温之后,将混合物用dcm稀释,用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。
[0890]
然后,将两种对映体用手性制备型hplc(phenomenex lux 5um amylose-1,21.2
×
250mm,用25%etoh/己烷洗脱,流动速率20ml/min,t
r,峰1
=15.4min,t
r,峰2
=17.6min)分离。在真空中蒸发溶剂之后,将两种对映体通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。
[0891]
实施例7.峰1:对于c
20h20
n5o2(m+h)
+
,lcms计算值:m/z=362.2;实验值:362.2。1h nmr(500mhz,dmso-d6)δ8.32
–
8.25(s,1h),8.07
–
8.00(s,1h),7.49
–
7.44(s,1h),7.41
–
7.38(d,j=7.3hz,1h),7.38
–
7.35(d,j=7.5hz,1h),7.33
–
7.28(m,1h),5.18
–
5.09(t,j=6.7hz,1h),3.95
–
3.88(s,3h),3.88
–
3.82(s,3h),2.87
–
2.75(m,1h),2.75
–
2.65(m,1h),2.35
–
2.28(m,1h),1.83
–
1.68(m,1h)ppm。
[0892]
实施例8.峰2:对于c
20h20
n5o2(m+h)
+
,lcms计算值:m/z=362.2;实验值:362.2。1h nmr(500mhz,dmso-d6)δ8.33
–
8.28(s,1h),8.06
–
8.02(s,1h),7.49
–
7.45(s,1h),7.42
–
7.38(d,j=7.2hz,1h),7.38
–
7.35(m,1h),7.33
–
7.28(m,1h),5.19
–
5.07(t,j=6.7hz,1h),3.93
–
3.89(s,3h),3.89
–
3.85(s,3h),2.86
–
2.75(m,1h),2.75
–
2.66(m,1h),2.36
–
2.22(m,1h),1.82
–
1.67(m,1h)ppm。
[0893]
实施例9. 4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[0894][0895]
将甲烷磺酰氯(5mg,0.04mmol)添加至三乙胺(6.04μl,0.043mmol)和5-(1-羟基-2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(实施例8的中间体,10mg,0.022mmol)于dcm(1ml)中的溶液中。在室温下搅拌30min之后,将反应混合物通过硅胶垫过滤,用dcm和甲醇洗涤滤液,合并有机级分并在真空中蒸发溶剂。将所得残余物溶解于dmf(1ml)中,并且添加氰化钾(2.82mg,0.043mmol)和18-冠-6(11mg,0.043mmol)。将反应混合物在80℃下搅拌2h,之后添加水并用dcm萃取所需产物。用盐水洗涤有机相并在真空中蒸发溶剂。将所得材料溶解于dcm(1ml)和tfa(0.5ml)中,并且将反应混合物在室温下搅拌30min。其然后用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
21h19
n6o(m+h)
+
,lcms计算值:m/z=371.2;实验值:371.2。
[0896]
中间体3. 4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-2-酚
[0897][0898]
此化合物根据中间体2中所描述的程序,使用4-溴-2,3-二氢-1h-茚-2-酚替代4-溴-2,3-二氢-1h-茚-1-酚作为起始材料来制备。
[0899]
实施例10. 4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚
[0900][0901]
将5-氯-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(35mg,0.096mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-2-酚(32mg,0.12mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(15mg,0.02mmol)和磷酸钾(30mg,0.14mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(2ml)和水(200μl)之后,将反应混合物在100℃下搅拌1h。在冷却至室温之后,将混合物用dcm稀释并过滤。在真空中浓缩滤液并且将所得残余物通过biotage isolera纯化。
[0902]
将两种对映体用手性制备型hplc(phenomenex lux cellulose-1 5um 21.2
×
250mm,用20%ipa(含有2mm nh3)/己烷洗脱,流动速率65ml/min,t
r,峰1
=6.5min,t
r,峰2
=7.5min)分离。收集峰2并且在真空中蒸发溶剂。将所得材料再溶解于1,4-二噁烷(2ml)和水(2ml)中。在添加碳酸铯(31.3mg,0.096mmol)和吗啉(0.3ml)之后,将反应混合物在100℃下加热2h。在冷却至室温之后,将混合物用ch3cn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
20h20
n5o2(m+h)
+
,lcms计算值:m/z=362.2;实验值:362.2。1h nmr(500mhz,dmso-d6)δ8.35
–
8.29(s,1h),8.08
–
8.03(s,1h),7.48
–
7.45(s,1h),7.34
–
7.28(d,j=7.2hz,1h),7.29
–
7.25(m,1h),7.25
–
7.20(m,1h),4.52
–
4.45(m,1h),3.94
–
3.90(s,3h),3.89
–
3.84(s,3h),3.21
–
3.11(dd,j=16.0,6.0hz,1h),3.09
–
3.00(dd,j=16.4,5.9hz,1h),2.88
–
2.78(dd,j=16.0,3.6hz,1h),2.71
–
2.64(dd,j=16.4,3.6hz,1h)ppm。
[0903]
中间体4.(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-1-基)甲醇
[0904][0905]
步骤1.(4-溴-2,3-二氢-1h-茚-1-基)甲醇
[0906][0907]
将lihmds(29.6ml,29.6mmol)的1m thf溶液在0℃下缓慢地添加至(甲氧基甲基)三苯基氯化鏻(10.15g,29.6mmol)于thf(150ml)中的悬浮液中。将此溶液在0℃下搅拌1h之后,缓慢地添加4-溴-2,3-二氢-1h-茚-1-酮(5.0g,23.7mmol)于thf(20ml)中的溶液并且将反应混合物在室温下搅拌2h。将反应然后用水淬灭并用etoac萃取产物。将合并的有机相用盐水洗涤,经无水na2so4干燥并浓缩。将粗产物通过biotage isolera纯化。
[0908]
将bbr3(21.2ml,21.2mmol)的1m dcm溶液在-78℃下添加至上述纯化材料于dcm(50ml)中的溶液中。在所述温度下搅拌1h之后,将反应用水淬灭并用dcm萃取产物。将有机相经硫酸钠干燥并在真空中蒸发溶剂。将粗产物通过biotage isolera纯化。
[0909]
将nabh4(0.630g,16.7mmol)添加至所得上述材料于thf(15ml)和meoh(15ml)的混合物中的溶液中。将反应混合物在室温下搅拌1h之后,添加水。用etoac萃取所需产物,将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。所得粗产物不经进一步纯化即用于下一步骤中。
[0910]
步骤2.(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-1-基)甲醇
[0911]
此化合物根据中间体2中所描述的程序,使用(4-溴-2,3-二氢-1h-茚-1-基)甲醇替代4-溴-2,3-二氢-1h-茚-1-酚作为起始材料来制备。
[0912]
实施例11和实施例12.(4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-基)甲醇,两种对映体
[0913][0914]
这些化合物根据实施例7中所描述的程序,使用(4-(4,4,5,5-四甲基-1,3,2-二氧
1-酚
[0925]
此化合物根据中间体2中所描述的程序,使用4-溴-2-氟-2,3-二氢-1h-茚-1-酚替代4-溴-2,3-二氢-1h-茚-1-酚作为起始材料来制备。中间体5作为顺式异构体被分离,仅具有痕量反式异构体。
[0926]
实施例13. 2-氟-4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-酚
[0927][0928]
此化合物根据实施例7中所描述的程序,使用2-氟-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-1-酚(中间体5)替代4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-1-酚作为起始材料来制备。
[0929]
将两种对映体用手性制备型hplc(phenomenex lux 5um amylose-1,21.2
×
250mm,用35%etoh/己烷洗脱,流动速率20ml/min,t
r,峰1
=7.8min,t
r,峰2
=9.8min)分离。收集峰2。在真空中蒸发溶剂之后,产物通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
20h19
fn5o2(m+h)
+
,lcms计算值:m/z=380.2;实验值:380.2。1h nmr(500mhz,dmso-d6)δ8.35
–
8.31(s,1h),8.07
–
8.04(s,1h),7.51
–
7.47(s,1h),7.48
–
7.44(m,1h),7.43
–
7.34(m,2h),5.28
–
5.13(m,1h),5.13
–
5.07(m,1h),3.94
–
3.89(s,3h),3.89
–
3.86(s,3h),3.24
–
3.06(ddd,j=35.5,17.3,4.1hz,1h),2.97
–
2.86(dd,j=22.2,17.0hz,1h)ppm。对作为顺式异构体的中间体5进行单晶x射线,并且测定其绝对立体化学,从而确认标题化合物的绝对立体化学。
[0930]
在本实施例中用作起始材料的5-氯-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯的制备描述于下文中:
[0931][0932]
步骤1. 6-溴-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[0933][0934]
将nah(在矿物油中60%,2.46g,61.6mmol)在0℃下缓慢地添加至6-溴-1h-吡唑并
[4,3-b]吡啶(10.16g,51.3mmol)于dmf(70ml)中的溶液中。在室温下搅拌20min之后,缓慢地添加(氯甲烷三基)三苯(15.73g,56.4mmol)并且将反应混合物在室温下搅拌1h。然后添加水并且将沉淀的产物通过过滤进行收集,用水洗涤并空气干燥。其不经进一步纯化即用于下一步骤。对于c
25h19
brn3(m+h)
+
,lc-ms计算值:m/z=440.1和442.1;实验值440.0和442.0。
[0935]
步骤2. 6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[0936][0937]
将6-溴-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(25.0g,56.8mmol)、碳酸铯(25.9g,79mmol)、甲醇(6.89ml,170mmol)和
t
buxphos pd g3(1.52g,1.7mmol)于甲苯(150ml)中的混合物在80℃下加热1h。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过biotage isolera纯化。对于c
26h22
n3o(m+h)
+
,lcms计算值:m/z=392.2;实验值:392.1。
[0938]
步骤3. 6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶4-氧化物
[0939][0940]
将m-cpba(14.5g,64.6mmol)在0℃下缓慢地添加至6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(16.8g,43.0mmol)于dcm(150ml)中的溶液中。在室温下搅拌过夜之后,将反应用na2s2o3溶液和1m naoh溶液淬灭。在室温下搅拌30min之后,分离有机相并用1m naoh溶液洗涤3次并用盐水溶液洗涤2次。然后,将有机相经硫酸钠干燥,过滤并在真空中去除溶剂。所得产物不经进一步纯化即用于下一步骤中。对于c
26h22
n3o2(m+h)
+
,lc-ms计算值:m/z=408.2;实验值408.2。
[0941]
步骤4. 5-氯-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[0942][0943]
将草酰氯(5.36ml,61.3mmol)于dcm中的溶液在0℃下缓慢地添加至6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶4-氧化物(16.65g,40.9mmol)和dipea(14.27ml,82mmol)于dcm(100ml)中的溶液中。在0℃下搅拌1h之后,将反应用dcm稀释并小心地用水淬灭。分离有机相,用水洗涤3次,用饱和nahco3溶液洗涤2次,用盐水洗涤2次并经硫酸钠干燥。在真空中去除溶剂之后,所得产物不经进一步纯化即用于下一步骤中。对于c
26h21
cln3o(m+h)
+
,lc-ms计算值:m/z=426.1;实验值426.2。
[0944]
步骤5. 5-氯-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[0945][0946]
将tfa(29ml,376mmol)和水(1.35ml,75mmol)添加至5-氯-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(16g,37.6mmol)于dcm(75ml)中的溶液中。在室温下搅拌30min之后,添加ch3cn和水并在真空中蒸发dcm。滤出沉淀的固体。将反应混合物进一步用水稀释并用etoac/己烷1:1混合物洗涤3次。分离水相并在真空中去除所有溶剂。将残余物再溶解于dcm中并用nahco3溶液中和。将有机相进一步用nahco3溶液、盐水洗涤2次,然后经硫酸钠干燥。在真空中蒸发溶剂。所得粗产物不经进一步纯化即用于下一步骤中。对于c7h7cln3o(m+h)
+
,lc-ms计算值:m/z=184.0;实验值184.1。
[0947]
步骤6. 5-氯-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[0948][0949]
将nis(6.87g,30.6mmol)添加至5-氯-6-甲氧基-1h-吡唑并[4,3-b]吡啶(5.5g,30.0mmol)于dmf(60ml)中的溶液中。在60℃下搅拌2h之后,将反应混合物冷却至室温,并且添加三乙胺(6.26ml,44.9mmol)和boc-酸酐(8.17g,37.4mmol)。在室温下再搅拌1h之后,添加水并通过过滤收集沉淀的产物。将固体产物风干并且不经进一步纯化即用于下一步骤中。对于c
12h14
clin3o3(m+h)
+
,lc-ms计算值:m/z=410.0;实验值410.1。
[0950]
步骤7. 5-氯-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[0951][0952]
将5-氯-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(8.73g,21.31mmol)、1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑(5.32g,25.6mmol)、pdcl2(dppf)-ch2cl2加合物(3.48g,4.26mmol)和磷酸钾(6.79g,32.0mmol)置于烧瓶中并且将烧瓶抽真空并用n2回填三次。然后添加1,4-二噁烷(150ml)和水(15ml)并且将反应在80℃下搅拌1h。在冷却至室温之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过biotage isolera纯化。对于c
16h19
cln5o3(m+h)
+
,lcms计算值:m/z=364.1;实验值:364.0。
[0953]
实施例14. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[0954][0955]
步骤1. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[0956][0957]
将5-氯-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(实施例1,步骤4,0.50g,1.174mmol)、2-(2,3-二氢-1h-茚-4-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环(0.32g,1.31mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(102mg,0.13mmol)和磷酸钾(274mg,1.3mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(10ml)和水(1ml)之后,将反应混合物在80℃下搅拌2h。在冷却至室温之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过biotage isolera纯化以得到白色固体(0.59g,99%)。对于c
35h30
n3o(m+h)
+
,lcms计算值:m/z=508.2;实验值508.1。
[0958]
步骤2. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[0959][0960]
将dcm(10ml)和tfa(4ml)的混合物中的5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(0.58g,1.143mmol)在室温下搅拌1h。将反应然后在真空中浓缩,溶解于dcm中并用nahco3溶液中和。分离有机相,经硫酸钠干燥并在真空中浓缩。将粗材料通过biotage isolera纯化以得到白色固体(0.2g,66%)。对于c
16h16
n3o(m+h)
+
,lcms计算值:m/z=266.1;实验值266.1。
[0961]
步骤3. 5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[0962][0963]
将nis(0.220g,0.978mmol)添加至5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(0.20g,0.754mmol)于dmf(10ml)中的溶液中。在80℃下搅拌2h之后,将反应混合物冷却至室温,并且添加三乙胺(0.3ml,2.2mmol)和boc-酸酐(0.411g,1.885mmol)。在室温下再搅拌1h之后,添加水并通过过滤收集沉淀的产物并风干。将粗材料通过biotage isolera纯化以得到白色固体(0.29g,78%)。对于c
21h23
in3o3(m+h)
+
,lcms计算值:m/z=492.1;实验值492.1。
[0964]
步骤4. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[0965]
将5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(0.10g,0.204mmol)、(1-(1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)硼酸(0.114g,0.407mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(17mg,22μmol)和磷酸钾(40mg,0.18mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(3ml)和水(300μl)之后,将反应混合物在80℃下搅拌2h。然后过滤反应,并且在真空中蒸发溶剂。将hcl于二噁烷(2ml)中的4n溶液添加至所得残余物中并且将反应混合物在室温下搅拌1h。然后将混合物用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
23h25
n6o(m+h)
+
,lcms计算值:m/z=401.1;实验值:401.1。
[0966]
实施例15. 5-(2,3-二氢-1h-茚-4-基)-3-(1-(1-乙基吡咯烷-3-基)-1h-吡唑-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[0967][0968]
将乙醛(11mg,0.24mmol)和三乙酰氧基硼氢化钠(25mg,0.12mmol)添加至5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶(25mg,0.062mmol)和一滴乙酸于dce(1ml)中的溶液中。在室温下搅拌过夜之后,然后将反应用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
25h29
n6o(m+h)
+
,lcms计算值:m/z=429.1;实验值:429.1。
[0969]
实施例16. 3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)环丁烷甲腈
[0970][0971]
此化合物根据实施例14中所描述的程序,使用3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)环丁烷-1-甲腈替代(1-(1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
24h23
n6o(m+h)
+
,lcms计算值:m/z=411.2;实验值:411.2。1h nmr(500mhz,dmso-d6)δ8.44
–
8.37(s,1h),8.20
–
8.15(s,1h),7.50
–
7.44(s,1h),7.32
–
7.27(m,2h),7.25
–
7.20(t,j=7.4hz,1h),5.39
–
5.27(p,j=8.0hz,1h),3.92
–
3.82(s,3h),3.02
–
2.88(m,4h),2.85
–
2.73(m,4h),2.06
–
1.91(p,j=7.4hz,3h)ppm。
[0972]
实施例17. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(1-甲基氮杂环丁-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[0973][0974]
步骤1. 3-(1-(1-(叔丁氧基羰基)氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[0975][0976]
此化合物根据实施例14中所描述的程序,使用3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸叔丁酯替代(1-(1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)硼酸作为起始材料来制备。对于c
32h39
n6o5(m+h)
+
,lcms计算值:m/z=587.3;实验值:587.3。
[0977]
步骤2. 3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[0978][0979]
将3-(1-(1-(叔丁氧基羰基)氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(0.14g,0.239mmol)于dcm(2ml)和tfa(2ml)的混合物中的溶液在室温下搅拌2h。然后在真空中蒸发溶剂并且粗产物不经进一步纯化直接用于下一步骤中。对于c
22h23
n6o(m+h)
+
,lcms计算值:m/z=387.2;实验值:387.2。
[0980]
步骤3. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(1-甲基氮杂环丁-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[0981]
将甲醛溶液(0.02ml)和三乙酰氧基硼氢化钠(25mg,0.12mmol)添加至3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(24mg,0.062mmol)和一滴乙酸于dce(1ml)中的溶液中。在室温下搅拌过夜之后,然后将反应用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
23h25
n6o(m+h)
+
,lcms计算值:m/z=401.2;实验值:401.2。1h nmr(500mhz,dmso-d6)δ12.97
–
12.91(s,1h),8.50
–
8.39(s,1h),8.16
–
8.10(s,1h),7.51
–
7.45(s,1h),7.33
–
7.27(m,2h),7.26
–
7.18(m,1h),5.16
–
5.00(dt,j=13.6,6.7hz,1h),3.90
–
3.83(s,3h),3.75
–
3.65(t,j=7.5hz,2h),3.45
–
3.36(m,2h),3.01
–
2.89(t,j=7.3hz,2h),2.88
–
2.77(t,j=7.4hz,2h),2.36
–
2.29(s,3h),2.03
–
1.90(dt,j=14.8,7.4hz,2h)ppm。
[0982]
实施例18. 5-(2,3-二氢-1h-茚-4-基)-3-(1-(1-乙基氮杂环丁-3-基)-1h-吡唑-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[0983][0984]
此化合物根据实施例17中所描述的程序,使用乙醛替代甲醛作为起始材料来制备。产物作为tfa盐被分离。对于c
24h27
n6o(m+h)
+
,lcms计算值:m/z=415.2;实验值:415.2。
[0985]
实施例19. 4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-n,n-二甲基哌啶-1-羧酰胺
[0986][0987]
步骤1.5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[0988][0989]
将1-(氯甲基)-4-甲氧基苯(0.149g,0.951mmol)添加至5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶(实施例14,步骤3,0.31g,0.792mmol)和碳酸铯(500mg,1.54mmol)于dmf(5ml)中的混合物中。在80℃下搅拌1h之后,将反应用dcm稀释并用水和盐水洗涤。将有机相经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过biotage isolera纯化(0.40,99%)。对于c
24h23
in3o2(m+h)
+
,lcms计算值:m/z=512.1;实验值512.1。
[0990]
步骤2. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(1-(哌啶-4-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[0991][0992]
将5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(0.200g,0.391mmol)、4-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)哌啶-1-羧酸叔丁酯(0.177g,0.469mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(17mg,22μmol)和磷酸钾(100mg,0.44mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(3ml)和水(300μl)之后,将反应混合物在100℃下搅拌1h。然后过滤反应,并且在真空中蒸发溶剂。在通过biotage isolera纯化之后,将dcm(1ml)和tfa(1ml)添加至纯化材料中并且将反应混合物在室温下搅拌1h。然后将反应混合物用dcm稀释并用nahco3溶液中和。用dcm萃取产物,并且将有机相经硫酸钠干燥并在真空中浓缩。所得产物不经进一步纯化即用于下一步骤中。对于c
32h35
n6o2(m+h)
+
,lcms计算值:m/z=535.2;实验值:535.2。
[0993]
步骤3. 4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-n,n-二甲基哌啶-1-羧酰胺
[0994][0995]
向5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(1-(哌啶-4-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶(10mg,0.019mmol)于1,4-二噁烷(0.5ml)和et3n(0.02ml)中的溶液中添加二甲基氨基甲酰氯(10mg,0.094mmol)。在室温下搅拌1h之后,将反应在真空中浓缩。将tfa(1ml)添加至粗材料中并且将所得溶液在100℃下加热2h。将反应然后用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h32
n7o2(m+h)
+
,lcms计算值:m/z=486.2;实验值:486.2。
[0996]
实施例20. 4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)哌啶-1-羧酸甲酯
[0997][0998]
此化合物根据实施例19中所描述的程序,使用氯甲酸甲酯替代二甲基氨基甲酰氯来制备。产物作为tfa盐被分离。对于c
26h29
n6o3(m+h)
+
,lc-ms计算值:m/z=473.2;实验值:473.2。
[0999]
实施例21. 3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸甲酯
[1000][1001]
步骤1. 3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1002]
[1003]
此化合物根据实施例19中所描述的程序,使用3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸叔丁酯替代4-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)哌啶-1-羧酸叔丁酯来制备。对于c
30h31
n6o2(m+h)
+
,lc-ms计算值:m/z=507.2;实验值:507.2。
[1004]
步骤2. 3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸甲酯
[1005]
此化合物根据实施例19中所描述的程序,使用3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶替代5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(1-(哌啶-4-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶,并且使用氯甲酸甲酯替代二甲基氨基甲酰氯来制备。产物作为tfa盐被分离。对于c
24h25
n6o3(m+h)
+
,lc-ms计算值:m/z=445.1;实验值:445.1。
[1006]
实施例22. 1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)乙-1-酮
[1007][1008]
此化合物根据实施例21中所描述的程序,使用乙酰氯替代氯甲酸甲酯来制备。产物作为tfa盐被分离。对于c
24h25
n6o2(m+h)
+
,lc-ms计算值:m/z=429.1;实验值:429.1。
[1009]
实施例23. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(1-(甲基磺酰基)氮杂环丁-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1010][1011]
此化合物根据实施例21中所描述的程序,使用甲烷磺酰氯替代氯甲酸甲酯来制备。产物作为tfa盐被分离。对于c
23h25
n6o3s(m+h)
+
,lc-ms计算值:m/z=465.1;实验值:465.1。
[1012]
实施例24. 3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-n,n-二甲基氮杂环丁烷-1-羧酰胺
[1013]
[1014]
此化合物根据实施例21中所描述的程序,使用二甲基氨基甲酰氯替代氯甲酸甲酯来制备。产物作为tfa盐被分离。对于c
25h28
n7o2(m+h)
+
,lc-ms计算值:m/z=458.1;实验值:458.1。
[1015]
实施例25.环丙基(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)甲酮
[1016][1017]
此化合物根据实施例21中所描述的程序,使用环丙烷甲酰氯替代氯甲酸甲酯来制备。产物作为tfa盐被分离。对于c
26h27
n6o2(m+h)
+
,lc-ms计算值:m/z=455.1;实验值:455.1。1h nmr(500mhz,dmso-d6)δ8.52
–
8.44(s,1h),8.26
–
8.16(s,1h),7.51
–
7.43(s,1h),7.31
–
7.25(m,2h),7.25
–
7.18(t,j=7.4hz,1h),5.52
–
5.41(m,1h),4.75
–
4.69(m,1h),4.60
–
4.52(m,1h),4.36
–
4.26(t,j=9.1hz,1h),4.21
–
4.11(dd,j=10.1,5.1hz,1h),3.90
–
3.84(s,3h),3.01
–
2.93(t,j=7.4hz,2h),2.85
–
2.77(t,j=7.4hz,2h),2.03
–
1.90(p,j=7.4hz,2h),1.66
–
1.53(m,1h),0.82
–
0.70(m,4h)ppm。
[1018]
实施例26. 5-(2,3-二氢-1h-茚-4-基)-6-乙氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1019][1020]
步骤1. 6-乙氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1021][1022]
将6-溴-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(2.5g,5.7mmol)、碳酸铯(2.6g,8mmol)、乙醇(0.7ml,12mmol)和
t
buxphos pd g3(0.15g,0.17mmol)于甲苯(30ml)中的混合物在80℃下加热1h。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过biotage isolera纯化。对于c
27h24
n3o(m+h)
+
,lc-ms计算值:m/z=406.1;实验值406.1。
[1023]
步骤2. 6-乙氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶4-氧化物
[1024][1025]
在0℃下向6-乙氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(1.08g,2.66mmol)于10ml dcm中的溶液中添加3-氯过氧苯甲酸(1.5g,6.52mmol)。将反应在室温下搅拌2小时。将反应混合物用dcm稀释并且将有机相用na2s2o3溶液、随后nahco3溶液洗涤。在真空中浓缩溶剂之后,将粗材料通过biotage isolera纯化以得到白色固体(0.80g,71%)。对于c
27h24
n3o2(m+h)
+
,lc-ms计算值:m/z=422.1;实验值422.1。
[1026]
步骤3. 5-氯-6-乙氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1027][1028]
向6-乙氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶4-氧化物(0.80g,1.9mmol)于20ml dcm中的溶液中添加1.0ml et3n。将混合物在冰浴中冷却至0℃,并且缓慢地添加草酰氯(0.60g,4.7mmol)。将反应混合物在0℃下搅拌1小时,然后用nahco3溶液中和。分离有机相,经硫酸钠干燥并在真空中浓缩。将粗材料通过biotage isolera纯化以得到白色固体(0.26g,31%)。对于c
27h23
cln3o(m+h)
+
,lc-ms计算值:m/z=440.2;实验值440.2。
[1029]
步骤4. 5-(2,3-二氢-1h-茚-4-基)-6-乙氧基-1h-吡唑并[4,3-b]吡啶
[1030][1031]
此化合物根据实施例14中所描述的程序,使用5-氯-6-乙氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶替代5-氯-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶来制备。对于c
17h18
n3o(m+h)
+
,lc-ms计算值:m/z=280.1;实验值280.1。
[1032]
步骤5. 5-(2,3-二氢-1h-茚-4-基)-6-乙氧基-3-碘-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1033][1034]
此化合物根据实施例21步骤2中所描述的程序,使用5-(2,3-二氢-1h-茚-4-基)-6-乙氧基-1h-吡唑并[4,3-b]吡啶替代5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶来制备。对于c
22h25
in3o3(m+h)
+
,lc-ms计算值:m/z=506.1;实验值506.1。
[1035]
步骤6. 5-(2,3-二氢-1h-茚-4-基)-6-乙氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1036]
将1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑(20mg,0.096mmol)、5-(2,3-二氢-1h-茚-4-基)-6-乙氧基-3-碘-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(7mg,0.014mmol)、x-phos pd g2(4mg,0.001mmol)和k3po4(10mg,0.05mmol)的混合物与二噁烷(1ml)和水(0.1ml)合并并且将反应混合物在80℃下加热2小时。在冷却至室温之后,过滤反应并且添加2ml含4n hcl的二噁烷。将反应混合物在室温下再搅拌1小时,然后在真空中浓缩。然后将残余物溶解于ch3cn和水的混合物中,并且将产物用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
21h22
n5o(m+h)
+
,lc-ms计算值:m/z=360.1;实验值:360.1。
[1037]
实施例27. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡啶-4-基甲基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1038][1039]
此化合物根据实施例14中所描述的程序,使用4-((4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)甲基)吡啶替代(1-(1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)硼酸作为起始材料来制备。
[1040]
产物作为tfa盐被分离。对于c
25h23
n6o(m+h)
+
,lc-ms计算值:m/z=423.1;实验值:423.1。
[1041]
实施例28. 4-(2-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)乙基)吗啉
[1042][1043]
此化合物根据实施例14中所描述的程序,使用4-(2-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)乙基)吗啉替代(1-(1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
25h29
n6o2(m+h)
+
,lc-ms计算值:m/z=445.1;实验值:445.1。
[1044]
实施例29. 3-(1-环丙基-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1045][1046]
此化合物根据实施例14中所描述的程序,使用1-环丙基-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑替代(1-(1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
22h22
n5o(m+h)
+
,lc-ms计算值:m/z=372.1;实验值:372.1。
[1047]
实施例30. 3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)丙腈
[1048][1049]
此化合物根据实施例14中所描述的程序,使用3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)丙腈替代(1-(1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
22h21
n6o(m+h)
+
,lc-ms计算值:m/z=385.1;实验值:385.1。
[1050]
实施例31. 2-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)乙-1-醇
[1051][1052]
此化合物根据实施例14中所描述的程序,使用2-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)乙-1-醇替代(1-(1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
21h22
n5o2(m+h)
+
,lc-ms计算值:m/z=376.1;实验值:376.1。1h nmr(500mhz,dmso-d6)δ8.38
–
8.30(s,1h),8.11
–
8.04(s,1h),7.50
–
7.42(s,1h),7.33
–
7.26(m,2h),7.25
–
7.17(m,1h),4.29
–
4.17(t,j=5.5hz,2h),3.92
–
3.83(s,3h),3.79
–
3.73(t,j=5.5hz,2h),3.00
–
2.91(t,j=7.3hz,2h),2.84
–
2.78(t,j=7.4hz,2h),2.07
–
1.92(p,j=7.5hz,2h)ppm。
[1053]
实施例32. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡啶-4-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1054][1055]
此化合物根据实施例14中所描述的程序,使用4-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)吡啶替代(1-(1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
24h21
n6o(m+h)
+
,lc-ms计算值:m/z=409.1;实验值:409.1。
[1056]
实施例33.(反)-4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)环己-1-醇
[1057][1058]
此化合物根据实施例14中所描述的程序,使用((反)-4-((叔丁基二甲基甲硅烷基)氧基)环己基)-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑替代(1-(1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
25h28
n5o2(m+h)
+
,lc-ms计算值:m/z=430.1;实验值:430.1。
[1059]
实施例34.5-(2,3-二甲基苯基)-n-甲基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-6-胺
[1060][1061]
步骤1. 6-溴-3-碘-1h-吡唑并[4,3-b]吡啶
[1062][1063]
向6-溴-1h-吡唑并[4,3-b]吡啶(8.0g,40.4mmol)于60ml dmf中的溶液中添加1-碘吡咯烷-2,5-二酮(7.69g,44.4mmol),并且将反应混合物在室温下搅拌2h。将混合物倒入水(300ml)中并且再搅拌10min。所得固体通过过滤进行收集并且用水洗涤。将其风干并且不经进一步纯化即用于下一步骤中。对于c6h4brin3(m+h)
+
,lc-ms计算值:m/z=323.9;实验值323.9。
[1064]
步骤2. 6-溴-3-碘-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1065][1066]
在0℃下向nah(1.63g,40.8mmol)于dmf(100ml)中的悬浮液中逐滴添加6-溴-3-碘-1h-吡唑并[4,3-b]吡啶(12.0g,37.0mmol)于20ml dmf中的溶液。在添加完成之后,将反应混合物升温至室温并且在所述温度下搅拌30min。然后将混合物冷却回0℃并用(氯甲烷三基)三苯(11.4g,40.8mmol)于20ml dmf中的溶液处理。将反应混合物在室温下搅拌2h。然后添加水并用dcm萃取产物。将有机相在真空中浓缩。所得固体通过过滤进行收集并风干。对于c
25h18
brin3(m+h)
+
,lc-ms计算值:m/z=566.0;实验值566.0。
[1067]
步骤3. 6-溴-3-(1-甲基-1h-吡唑-4-基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1068][1069]
将6-溴-3-碘-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(5.0g,8.83mmol)、1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑(1.837g,8.83mmol)、pdcl2(dppf)-ch2cl2加合物(0.7g,0.883mmol)和磷酸钾(2.81g,13.25mmol)置于圆底烧瓶中并且将烧瓶抽真空并用n2回填三次。然后添加1,4-二噁烷(100ml)和水(10ml)并且将反应在70℃下搅拌1h。然后添加水并且将产物用etoac萃取。将溶液用盐水洗涤,干燥并浓缩。将残余物通过biotage isolera纯化以得到所需产物。对于c
29h23
brn5(m+h)
+
,lc-ms计算值:m/z=520.2;
实验值:520.2。
[1070]
步骤4. n-甲基-3-(1-甲基-1h-吡唑-4-基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶-6-胺
[1071][1072]
将含有6-溴-3-(1-甲基-1h-吡唑-4-基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(0.460g,0.884mmol)、氯(2-二环己基膦基-2’,6
’‑
二-异丙氧基-1,1
’‑
联苯基)(2
’‑
氨基-1,1
’‑
联苯-2-基)钯(ii)(0.069g,0.088mmol)和碳酸铯(0.576g,1.768mmol)的微波小瓶密封并抽真空并用氮气回填三次。添加1,4-二噁烷(12ml)和甲胺溶液(1.105ml,2.210mmol)。将反应混合物加热至100℃持续2h。然后添加水并且将产物用etoac萃取。将合并的有机相用盐水洗涤,干燥并浓缩。将残余物通过biotage isolera纯化以得到所需产物。对于c
30h27
n6(m+h)
+
,lc-ms计算值:m/z=471.2;实验值471.2。
[1073]
步骤5.5-溴-n-甲基-3-(1-甲基-1h-吡唑-4-基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶-6-胺
[1074][1075]
向n-甲基-3-(1-甲基-1h-吡唑-4-基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶-6-胺(300mg,0.638mmol)于dmf(5ml)中的溶液中添加nbs(125mg,0.701mmol)。将反应混合物在室温下搅拌2h,然后用水处理。用dcm萃取产物。将有机相用水和盐水洗涤,经na2so4干燥,并浓缩。将残余物通过biotage isolera纯化以得到所需产物。对于c
30h26
brn6(m+h)
+
,lc-ms计算值:m/z=549.2;实验值549.2。
[1076]
步骤6. 5-(2,3-二甲基苯基)-n-甲基-3-(1-甲基-1h-吡唑-4-基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶-6-胺
[1077][1078]
将5-溴-n-甲基-3-(1-甲基-1h-吡唑-4-基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶-6-胺(100mg,0.182mmol)、(2,3-二甲基苯基)硼酸(0.030g,0.200mmol)、cs2co3(0.089g,
0.273mmol)、xphos pdg2(3.46mg,9.10μmol)置于小瓶中并且将小瓶抽真空并用氮气回填三次。添加1,4-二噁烷(5ml)和水(1.25ml)并且将反应混合物在70℃下搅拌1小时。将反应混合物用水淬灭并用乙酸乙酯萃取产物。将有机相用水和盐水洗涤,经硫酸钠干燥并浓缩。将残余物通过biotage isolera纯化以得到所需产物。对于c
38h35
n6(m+h)
+
,lc-ms计算值:m/z=575.2;实验值:575.2。
[1079]
步骤7. 5-(2,3-二甲基苯基)-n-甲基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-6-胺
[1080]
5-(2,3-二甲基苯基)-n-甲基-3-(1-甲基-1h-吡唑-4-基)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶-6-胺(0.060g,0.100mmol)溶解于2ml二氯甲烷中并添加2ml tfa。将反应混合物在室温下搅拌1小时。在真空中去除大部分溶剂并且将残余物用水处理。将产物用乙酸乙酯萃取,并且用饱和nahco3溶液中和至ph~7。分离有机相,用水和盐水洗涤,经硫酸钠干燥并浓缩。将残余物通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
19h21
n6(m+h)
+
,lc-ms计算值:m/z=333.2;实验值:333.2。1h nmr(500mhz,dmso-d6)δ8.25
–
8.19(s,1h),7.98
–
7.94(s,1h),7.31
–
7.26(d,j=7.4hz,1h),7.25
–
7.20(t,j=7.5hz,1h),7.12
–
7.05(d,j=6.1hz,1h),6.80
–
6.73(s,1h),3.91
–
3.86(s,3h),2.75
–
2.68(s,3h),2.36
–
2.31(s,3h),1.99
–
1.88(s,3h)ppm。
[1081]
实施例35. 6-(二氟甲基)-5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1082][1083]
步骤1. 6-溴-5-氯-2-甲基吡啶-3-胺
[1084][1085]
将nbs(6.51g,36.6mmol)添加至5-氯-2-甲基吡啶-3-胺(4.97g,34.9mmol)于dmf(349ml)中的溶液中。在室温下搅拌30min之后,添加水并通过过滤收集沉淀的产物并在空气中干燥过夜。粗产物不经进一步纯化即用于下一步骤中。对于c6h7n2brcl(m+h)
+
,lcms计算值:m/z=221.0;实验值221.0。
[1086]
步骤2.n-(6-溴-5-氯-2-甲基吡啶-3-基)乙酰胺
[1087][1088]
向6-溴-5-氯-2-甲基吡啶-3-胺(7.0g,31.6mmol)于乙酸(79ml)中的溶液中添加乙酸酐(3.73ml,39.5mmol)。将反应在50℃下搅拌1h,然后添加水并通过过滤收集沉淀的产物。其不经进一步纯化即用于下一步骤。对于c8h9n2brclo(m+h)
+
,lcms计算值:m/z=263.0;实验值263.0。
[1089]
步骤3. 1-(5-溴-6-氯-1h-吡唑并[4,3-b]吡啶-1-基)乙-1-酮
[1090][1091]
向n-(6-溴-5-氯-2-甲基吡啶-3-基)乙酰胺(7.2g,27.3mmol)于甲苯(137ml)中的悬浮液中添加乙酸酐(7.73ml,82mmol)、乙酸钾(3.22g,32.8mmol)和亚硝酸异戊酯(5.87ml,43.7mmol)。将反应混合物在100℃下加热2h,然后用etoac稀释。将混合物用饱和nahco3和盐水洗涤,经na2so4干燥。在真空下去除溶剂以提供作为粗产物的棕色固体,其不经纯化直接用于下一步骤中。对于c8h6n3brclo(m+h)
+
,lcms计算值:m/z=274.0;实验值274.0。
[1092]
步骤4. 5-溴-6-氯-1h-吡唑并[4,3-b]吡啶
[1093][1094]
向1-(5-溴-6-氯-1h-吡唑并[4,3-b]吡啶-1-基)乙-1-酮(7g,25.5mmol)于thf(31.9ml)和甲醇(31.9ml)中的溶液中添加1m氢氧化钠溶液(38.3ml,38.3mmol)。将混合物在50℃下搅拌1h。完成之后,大部分溶剂蒸发,然后添加1n hcl(40ml),随后添加200ml水。在反应的搅拌期间,缓慢地形成棕色固体。将粗产物通过过滤进行收集并且不经进一步纯化即用于下一步骤中。对于c6h4n3brcl(m+h)
+
,lcms计算值:m/z=232.0;实验值232.0。
[1095]
步骤5. 5-溴-6-氯-3-碘-1h-吡唑并[4,3-b]吡啶
[1096][1097]
向5-溴-6-氯-1h-吡唑并[4,3-b]吡啶(4.0g,17.2mmol)于30ml dmf中的溶液中添加1-碘吡咯烷-2,5-二酮(4.3g,19.0mmol),并且将反应混合物在室温下搅拌2h。将混合物
倒入水(200ml)中并且再搅拌10min。过滤所得固体并风干。所得材料不经进一步纯化即用于下一步骤中。对于c6h3brclin3(m+h)
+
,lc-ms计算值:m/z=358.0;实验值358.0。
[1098]
步骤6. 5-溴-6-氯-3-碘-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶
[1099][1100]
在0℃下向5-溴-6-氯-3-碘-1h-吡唑并[4,3-b]吡啶(5.0g,14.0mmol)于dmf(40ml)中的悬浮液中添加60%nah(0.72g,18.0mmol)。在添加完成之后,将反应升温至室温并在室温下搅拌30min。当添加(2-(氯甲氧基)乙基)三甲基硅烷(3.0g,18.0mmol)于10ml dmf中的溶液时,将混合物冷却回0℃。将反应在室温下搅拌2h。将水添加至反应混合物中并用dcm萃取产物。分离有机相,经硫酸钠干燥并在真空中蒸发溶剂。将残余物通过biotage isolera纯化以得到所需产物。对于c
12h17
brclin3osi(m+h)
+
,lc-ms计算值:m/z=488.2;实验值:488.2。
[1101]
步骤7. 5-溴-6-氯-3-(1-甲基-1h-吡唑-4-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶
[1102][1103]
将5-溴-6-氯-3-碘-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶(1.50g,3.07mmol)、1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑(0.652g,3.13mmol)、pdcl2(dppf)-ch2cl2加合物(0.251g,0.307mmol)和磷酸钾(912mg,4.30mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。添加1,4-二噁烷(10ml)和水(2.0ml)并且将反应在65℃下搅拌1h。然后添加水并且将产物用etoac萃取。将溶液用盐水洗涤,干燥并浓缩。将残余物通过biotage isolera纯化以得到所需产物。对于c
16h22
brcln5osi(m+h)
+
,lc-ms计算值:m/z=442.2;实验值:442.2。
[1104]
步骤8. 6-氯-5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶
[1105][1106]
将5-溴-6-氯-3-(1-甲基-1h-吡唑-4-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲
基)-1h-吡唑并[4,3-b]吡啶(700mg,1.58mmol)、2-(2,3-二氢-1h-茚-4-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环(463mg,1.9mmol)、
t
buxphos pd g3(175mg,0.22mmol)和磷酸钾(0.356ml,4.30mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。添加1,4-二噁烷(10ml)和水(2.0ml)并且将反应在80℃下搅拌1h。然后添加水并且将产物用etoac萃取。将有机相用盐水洗涤,干燥并浓缩。将残余物通过biotage isolera纯化以得到所需产物。对于c
25h31
cln5osi(m+h)
+
,lc-ms计算值:m/z=480.2;实验值:480.2。
[1107]
步骤9. 5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-6-乙烯基-1h-吡唑并[4,3-b]吡啶
[1108][1109]
将6-氯-5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶(200mg,0.42mmol)、4,4,5,5-四甲基-2-乙烯基-1,3,2-二氧硼戊环(83mg,0.542mmol)、cs2co3(271mg,0.833mmol)和xphos pd g2(31.7mg,0.083mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。添加1,4-二噁烷(5ml)和水(1ml)并且将反应在75℃下搅拌1h。然后添加水并且将产物用etoac萃取。将有机相用盐水洗涤,经硫酸钠干燥并浓缩。将残余物通过biotage isolera纯化以得到所需产物。对于c
27h34
n5osi(m+h)
+
,lc-ms计算值:m/z=472.2;实验值:472.2。
[1110]
步骤10. 5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-6-甲醛
[1111][1112]
向5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-6-乙烯基-1h-吡唑并[4,3-b]吡啶(0.250g,0.530mmol)和高碘酸钠(0.57g,2.65mmol)于四氢呋喃(5ml)和水(1.5ml)中的混合物中添加含4%四氧化锇(viii)的水(0.337g,0.053mmol)。将反应混合物在室温下搅拌1小时。将其用饱和硫代硫酸钠溶液淬灭。将产物用dcm萃取(3次)。将合并的萃取物用水、盐水洗涤,经硫酸钠干燥并浓缩。粗材料不经进一步纯化即用于下一步骤中。对于c
26h32
n5o2si(m+h)
+
,lc-ms计算值:m/z=474.2;实验值:474.2。
[1113]
步骤11. 6-(二氟甲基)-5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1114]
向5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-6-甲醛(20mg,0.042mmol)于二氯甲烷(2ml)中的溶液中添加二乙基氨基三氟化硫(11.22μl,0.084mmol)。在室温下搅拌过夜之后,添加nahco3溶液并且将产物用dcm萃取,将有机相用盐水洗涤,经na2so4干燥并浓缩。
[1115]
将所得残余物再溶解于含50%tfa的ch2cl2中。在室温下搅拌30min之后,蒸发溶剂并添加氨水。在室温下再搅拌30min之后,将反应用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
20h18
f2n5(m+h)
+
,lc-ms计算值:m/z=366.2;实验值:366.2。
[1116]
实施例36.(5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-6-基)甲醇
[1117][1118]
在0℃下向5-(2,3-二氢-1h-茚-4-基)-3-(1-甲基-1h-吡唑-4-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-6-甲醛(实施例35,步骤10)(20mg,0.042mmol)于thf(2.0ml)和meoh(1.0ml)中的溶液中添加硼氢化钠(8mg,0.21mmol)。在室温下搅拌1h之后,添加nahco3溶液并用etoac萃取产物。将有机相用盐水洗涤,经na2so4干燥并在真空中浓缩。将所得残余物溶解于含50%tfa的ch2cl2中。在室温下搅拌30min之后,蒸发溶剂并添加氨水。在室温下再搅拌30min之后,将反应用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
20h20
n5o(m+h)
+
,lc-ms计算值:m/z=346.2;实验值:346.2。
[1119]
实施例37. 5-(2,3-二氢-1h-茚-4-基)-n-甲基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-6-胺
[1120][1121]
此化合物根据实施例34中所描述的程序,使用2-(2,3-二氢-1h-茚-4-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环替代(2,3-二甲基苯基)硼酸来制备。产物作为tfa盐被分离。对于c
20h21
n6(m+h)
+
,lc-ms计算值:m/z=345.2;实验值345.2。
[1122]
实施例38.(5-(2,3-二甲基苯基)-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-6-基)甲醇
[1123][1124]
此化合物根据实施例35和36中所描述的程序,使用(2,3-二甲基苯基)硼酸替代2-(2,3-二氢-1h-茚-4-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环来制备。产物作为tfa盐被分离。对于c
19h20
n5o(m+h)
+
,lc-ms计算值:m/z=334.2;实验值334.2。1h nmr(500mhz,dmso-d6)δ8.34
–
8.26(s,1h),8.08
–
8.05(s,1h),8.05
–
8.01(s,1h),7.29
–
7.23(d,j=7.4hz,1h),7.23
–
7.16(t,j=7.5hz,1h),7.08
–
7.00(d,j=6.1hz,1h),4.36
–
4.17(m,2h),3.95
–
3.87(s,3h),2.38
–
2.28(s,3h),1.92
–
1.81(s,3h)ppm。
[1125]
实施例39. 4-(6-氯-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚
[1126][1127]
步骤1. 6-溴-5-氯-2-甲基吡啶-3-胺
[1128][1129]
将nbs(10.4g,58.4mmol)添加至5-氯-2-甲基吡啶-3-胺(7.9g,55.6mmol)于dmf(100ml)中的溶液中。在室温下搅拌10min之后,添加水并通过过滤收集沉淀的产物。将所得产物用水洗涤并风干。其不经进一步纯化即用于下一步骤。对于c6h7brcln2(m+h)
+
,lc-ms计算值:m/z=221.0和223.0;实验值221.0和223.0。
[1130]
步骤2.n-(6-溴-5-氯-2-甲基吡啶-3-基)乙酰胺
[1131][1132]
将乙酸酐(6.3ml,66.3mmol)添加至6-溴-5-氯-2-甲基吡啶-3-胺(11.75g,53.1mmol)于乙酸(130ml)中的溶液中。在50℃下搅拌1h之后,添加水并通过过滤收集沉淀的产物。所得产物用水洗涤并且风干。其不经进一步纯化即用于下一步骤。对于c8h9brcln2o(m+h)
+
,lc-ms计算值:m/z=263.0和265.0;实验值263.0和265.0。
[1133]
步骤3. 1-(5-溴-6-氯-1h-吡唑并[4,3-b]吡啶-1-基)乙-1-酮
[1134][1135]
向n-(6-溴-5-氯-2-甲基吡啶-3-基)乙酰胺(12.7g,48.2mmol)于甲苯(120ml)中的悬浮液中添加乙酸酐(13.6ml,145mmol)、乙酸钾(5.7g,57.8mmol)和亚硝酸异戊酯(10.4ml,77mmol)。在110℃下加热2h之后,将反应混合物冷却至室温且添加etoac。然后,将有机相用nahco3溶液洗涤,经硫酸钠干燥,过滤,并且在真空中去除溶剂。所得粗产物通过biotage isolera纯化以得到所需化合物。
[1136]
步骤4. 5-溴-6-氯-1h-吡唑并[4,3-b]吡啶
[1137][1138]
将碳酸钾(7.40g,53.6mmol)添加至1-(5-溴-6-氯-1h-吡唑并[4,3-b]吡啶-1-基)乙-1-酮(13.37g,48.7mmol)于甲醇(100ml)中的溶液中。在60℃下搅拌1h之后,添加水并通过过滤收集沉淀的产物。将所得产物用水洗涤并风干。其不经进一步纯化即用于下一步骤。对于c6h4brcln3(m+h)
+
,lc-ms计算值:m/z=232.0和234.0;实验值232.0和234.0。
[1139]
步骤5. 5-溴-6-氯-3-碘-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1140][1141]
将nis(4.95g,22mmol)添加至5-溴-6-氯-1h-吡唑并[4,3-b]吡啶(5g,21.55mmol)于dmf(50ml)中的溶液中。在60℃下搅拌2h之后,将反应混合物冷却至室温,并且添加三乙胺(6.26ml,44.9mmol)和boc-酸酐(8.17g,37.4mmol)。在室温下再搅拌1h之后,添加水并通过过滤收集沉淀的固体并风干。所得产物不经进一步纯化即用于下一步骤中。对于c
11h11
brclin3o2(m+h)
+
,lc-ms计算值:m/z=457.9和459.9;实验值457.9和459.9。
[1142]
步骤6. 5-溴-6-氯-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1143][1144]
将5-溴-6-氯-3-碘-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(5.36g,11.69mmol)、
1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑(2.48g,11.92mmol)、pdcl2(dppf)-ch2cl2加合物(0.96g,1.17mmol)和磷酸钾(3.47g,16.37mmol)置于烧瓶中并且将烧瓶抽真空并用n2回填三次。然后添加1,4-二噁烷(100ml)和水(10ml)并且将反应在80℃下搅拌1h。在冷却至室温之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中去除溶剂。将粗材料通过biotage isolera纯化。对于c
15h16
brcln5o2(m+h)
+
,lc-ms计算值:m/z=412.0和414.0;实验值412.0和414.0。
[1145]
步骤7. 4-(6-氯-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚
[1146][1147]
将5-溴-6-氯-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(265mg,0.642mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-2-酚(175mg,0.674mmol)、氯[(三-叔丁基膦)-2-(2-氨基联苯基)]钯(ii)(33.0mg,0.064mmol)和磷酸钾(204mg,0.963mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(4ml)和水(400μl)之后,将反应混合物在80℃下搅拌1h。将混合物冷却至室温,用dcm稀释并过滤。在真空中浓缩滤液并且将所得残余物通过biotage isolera纯化。
[1148]
将所得纯化材料溶解于1,4-二噁烷(6ml)和水(6ml)中。在添加碳酸铯(313mg,0.96mmol)和吗啉(1ml)之后,将反应混合物在100℃下加热2h。将混合物冷却至室温,用dcm稀释,用盐水洗涤,经硫酸钠干燥,并且在真空中去除溶剂。
[1149]
将产物的两种对映体用手性sfc-pr-2(phenomenex lux i-cellulose-5 5um 21.2
×
250mm,用30%ipa/co2洗脱,流动速率60ml/min,t
r,峰1
=8.2min,t
r,峰2
=9.9min)分离。在真空中蒸发溶剂之后,将峰2通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
19h17
cln5o(m+h)
+
,lc-ms计算值:m/z=366.1;实验值366.1。
[1150]
实施例40. 5-(2,3-二甲基苯基)-6-甲基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1151][1152]
向小瓶中添加6-氯-5-(2,3-二甲基苯基)-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并
[4,3-b]吡啶-1-羧酸叔丁酯(20mg,0.046mmol,以与实施例35步骤1-8类似的方式制备)、2,4,6-三甲基-1,3,5,2,4,6-三氧杂三硼烷(11mg,0.09mmol)、cs2co3(30mg,0.091mmol)、xphos pdg2(4mg,0.009mmol)。将小瓶密封,然后抽真空并用n2回填三次。在添加甲苯(1.0ml)和水(0.2ml)之后,将反应混合物在75℃下加热1h。然后添加水并且将产物用etoac萃取。将有机相用盐水洗涤,经硫酸钠干燥并浓缩。将所得残余物溶解于含50%tfa的ch2cl2中。在室温下搅拌30min之后,将反应用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
19h20
n5(m+h)
+
,lc-ms计算值:m/z=318.2;实验值:318.2。
[1153]
实施例41. 5-(2,3-二甲基苯基)-6-甲氧基-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1154][1155]
将5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(实施例66,25mg,0.052mmol)、1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪(47.4mg,0.156mmol)、xphos pd g2(4.10mg,5.22μmol)、磷酸钾(44.3mg,0.209mmol)于水(0.100ml)和二噁烷(1ml)中的溶液加热至80℃持续20小时。此后,将其冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物溶解于dcm(1ml)中并添加tfa(1ml)。将混合物在室温下搅拌1h且通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
25h29
n6o(m+h)
+
,lcms计算值:m/z=429.2;实验值429.0。1h nmr(500mhz,dmso-d6)δ10.02(s,1h),9.21(d,j=2.3hz,1h),8.50(dd,j=9.0,2.3hz,1h),7.52(s,1h),7.23(d,j=7.1hz,1h),7.17(t,j=7.5hz,1h),7.13
–
7.05(m,2h),4.46(d,j=13.2hz,2h),3.84(s,3h),3.57
–
3.46(m,2h),3.25
–
3.02(m,4h),2.85(s,3h),2.32(s,3h),1.98(s,3h)ppm。
[1156]
5-(2,3-二甲基苯基)-6-甲氧基-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶的替代合成:
[1157]
步骤1. 6-溴-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1158][1159]
将nah(在矿物油中60%,2.46g,61.6mmol)在0℃下缓慢地添加至6-溴-1h-吡唑并[4,3-b]吡啶(10.16g,51.3mmol)于dmf(70ml)中的溶液中。在室温下搅拌20min之后,缓慢地添加(氯甲烷三基)三苯(15.73g,56.4mmol)并且将反应混合物在室温下搅拌1h。然后添加水并且将沉淀的产物通过过滤进行收集,用水洗涤并空气干燥。其不经进一步纯化即用于下一步骤。对于c
25h19
brn3(m+h)
+
的lc-ms计算值:m/z=440.1和442.1;实验值440.0和
442.0。
[1160]
步骤2. 6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1161][1162]
将6-溴-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(25.0g,56.8mmol)、碳酸铯(25.9g,79mmol)、甲醇(6.89ml,170mmol)和
t
buxphospd g3(1.52g,1.7mmol)于甲苯(150ml)中的混合物在80℃下加热1h。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过biotage isolera纯化。对于c
26h22
n3o(m+h)
+
,lcms计算值:m/z=392.2;实验值:392.1。
[1163]
步骤3. 6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶4-氧化物
[1164][1165]
将m-cpba(14.5g,64.6mmol)在0℃下缓慢地添加至6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(16.8g,43.0mmol)于dcm(150ml)中的溶液中。在室温下搅拌过夜之后,将反应用na2s2o3溶液和1mnaoh溶液处理。在室温下搅拌30min之后,分离有机相并用1mnaoh溶液洗涤3次并用盐水溶液洗涤2次。然后,将有机相经硫酸钠干燥,过滤并在真空中去除溶剂。所得产物不经进一步纯化即用于下一步骤中。对于c
26h22
n3o2(m+h)
+
,lc-ms计算值:m/z=408.2;实验值408.2。
[1166]
步骤4. 5-氯-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1167][1168]
将草酰氯(5.36ml,61.3mmol)于dcm中的溶液在0℃下缓慢地添加至6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶4-氧化物(16.65g,40.9mmol)和dipea(14.27ml,82mmol)于dcm(100ml)中的溶液中。在0℃下搅拌1h之后,将反应用dcm稀释并小心地用水处理。分离有机相,用水洗涤3次,用饱和nahco3溶液洗涤2次,用盐水洗涤2次并经硫酸钠干燥。在真空中去除溶剂之后,所得产物不经进一步纯化即用于下一步骤中。对于c
26h21
cln3o(m+h)
+
,lc-ms计算值:m/z=426.1;实验值426.2。
[1169]
步骤5. 5-(2,3-二甲基苯基)-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1170][1171]
将5-氯-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(11.29g,26.5mmol)、(2,3-二甲基苯基)硼酸(11.93g,80mmol)、xphospd g2(4.17g,5.30mmol)和磷酸钾(22.51g,106mmol)于二噁烷(100ml)和水(10ml)中的混合物加热至85℃持续2小时。此后,将溶液冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤,经na2so4干燥,过滤,并浓缩至干。所获得的粗物质直接用于下一步骤中。对于c
34h30
n3o(m+h)
+
,lcms计算值:m/z=496.2;实验值496.4。
[1172]
步骤6. 5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1173][1174]
向5-(2,3-二甲基苯基)-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(13g,26.2mmol)于100ml ch2cl2中的溶液中添加tfa(40ml)和水(2ml)并且将所得溶液在室温下搅拌。1.5小时之后,添加250ml mecn:h2o(1:1)溶液。将混合物再搅拌10min并且在真空中去除有机溶剂。滤出沉淀的固体并且将滤液用200ml etoac/己烷(1:1)洗涤3次。分离水相并浓缩。然后将所获得的粗物质溶解于100ml ch2cl2和100ml h2o中。将混合物用nh4oh水溶液中和。分离有机相并用水洗涤2次。然后将所获得的有机相经na2so4干燥,过滤并浓缩以获得所需产物。对于c
15h16
n3o(m+h)
+
,lcms计算值:m/z=254.1;实验值254.2。
[1175]
步骤7. 5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1176][1177]
将n-碘代琥珀酰亚胺(20.38g,91mmol)添加至5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(15.3g,60.4mmol)于dmf(100ml)中的溶液中。在60℃下搅拌4小时之后,将反应混合物冷却至室温,并且添加n,n-二异丙基乙胺(31.6ml,181mmol)和二碳酸二叔丁酯(39.5g,181mmol)。然后将所得反应混合物在室温下搅拌1.5小时。然后将反应混合物用水处理,用etoac萃取,用盐水洗涤。将合并的有机相用水洗涤3次并浓缩。将粗物质
溶解于meoh(约150ml)中并且通过过滤收集沉淀的固体并干燥以获得所需产物。对于c
20h23
in3o3(m+h)
+
,lcms计算值:m/z=480.1;实验值480.2。
[1178]
步骤8. 5-(2,3-二甲基苯基)-6-甲氧基-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1179]
将5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(25mg,0.052mmol)、1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪(47.4mg,0.156mmol)、xphospd g2(4.10mg,5.22μmol)、磷酸钾(44.3mg,0.209mmol)于水(0.1ml)和二噁烷(1ml)中的溶液加热至80℃持续20小时。此后,将其冷却至室温,用水稀释并用etoac萃取产物。将合并的有机相用饱和nacl水溶液洗涤,经na2so4干燥,过滤,并浓缩至干。然后将残余物溶解于dcm(1ml)中并添加tfa(1ml)。将混合物在室温下搅拌1h并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。标题化合物作为tfa盐被分离。对于c
25h29
n6o(m+h)
+
,lcms计算值:m/z=429.2;实验值429.0。1h nmr(500mhz,dmso-d6)δ10.02(s,1h),9.21(d,j=2.3hz,1h),8.50(dd,j=9.0,2.3hz,1h),7.52(s,1h),7.23(d,j=7.1hz,1h),7.17(t,j=7.5hz,1h),7.13
–
7.05(m,2h),4.46(d,j=13.2hz,2h),3.84(s,3h),3.57
–
3.46(m,2h),3.25
–
3.02(m,4h),2.85(s,3h),2.32(s,3h),1.98(s,3h)ppm。
[1180]
实施例42. 5-(2,3-二甲基苯基)-3-(6-(4-乙基哌嗪-1-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1181][1182]
此化合物根据实施例41中所描述的程序,使用1-乙基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪替代1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪来制备。产物作为tfa盐被分离。对于c
26h31
n6o(m+h)
+
,lc-ms计算值:m/z=443.3;实验值443.4。
[1183]
实施例43. 1-(4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌嗪-1-基)乙-1-酮
[1184][1185]
此化合物根据实施例41中所描述的程序,使用1-(4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪-1-基)乙-1-酮替代1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪来制备。产物作为tfa盐被分离。对于c
26h29
n6o2(m+h)
+
,lc-ms计算值:m/z=457.2;实验值457.1。
[1186]
实施例44. 4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吗啉
[1187][1188]
此化合物根据实施例41中所描述的程序,使用4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)吗啉替代1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪来制备。产物作为tfa盐被分离。对于c
24h26
n5o2(m+h)
+
,lc-ms计算值:m/z=416.2;实验值416.1。
[1189]
实施例45. 4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-甲基哌嗪-2-酮
[1190][1191]
步骤1. 5-(2,3-二甲基苯基)-3-(6-氟吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1192][1193]
将5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(150mg,0.313mmol)、(6-氟吡啶-3-基)硼酸(132mg,0.939mmol)、xphos pd g2(24.62mg,0.031mmol)和磷酸钾(266mg,1.25mmol)于二噁烷(5ml)和水(0.500ml)中的溶液加热至80℃持续12小时。此后,将其冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤,经na2so4干燥,然后过滤并浓缩至干。然后将残余物溶解于dcm(2ml)中并添加tfa(2ml)。将混合物在室温下搅拌1h并通过硅胶色谱纯化以得到所需产物。对于c
20h18
fn4o(m+h)
+
,lcms计算值:m/z=349.1;实验值349.1。
[1194]
步骤2. 4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-甲基哌嗪-2-酮
[1195]
将5-(2,3-二甲基苯基)-3-(6-氟吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(20mg,0.057mmol)、1-甲基哌嗪-2-酮盐酸盐(25.9mg,0.172mmol)和n,n-二异丙基乙胺(100μl,0.574mmol)于dmso(0.5ml)中的溶液加热至120℃持续20小时。将混合物冷却至室
温并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
25h27
n6o2(m+h)
+
,lcms计算值:m/z=443.2;实验值443.2。
[1196]
实施例46. 1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-4-醇
[1197][1198]
此化合物根据实施例45中所描述的程序,使用哌啶-4-醇替代1-甲基哌嗪-2-酮盐酸盐来制备。产物作为tfa盐被分离。对于c
25h28
n5o2(m+h)
+
,lc-ms计算值:m/z=430.2;实验值430.2。
[1199]
实施例47.(r)-5-(2,3-二甲基苯基)-3-(6-(3,4-二甲基哌嗪-1-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1200][1201]
此化合物根据实施例45中所描述的程序,使用(r)-1,2-二甲基哌嗪二盐酸盐替代1-甲基哌嗪-2-酮盐酸盐来制备。产物作为tfa盐被分离。对于c
26h31
n6o(m+h)
+
,lc-ms计算值:m/z=443.3;实验值443.4。
[1202]
实施例48. 5-(2,3-二甲基苯基)-6-(甲氧基-d3)-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1203][1204]
步骤1. 6-(甲氧基-d3)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1205][1206]
将6-溴-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(实施例1,步骤1;10.0g,22.7mmol)、碳酸铯(11.10g,34.1mmol)、甲醇-d4(6.89ml)和
t
buxphos pd g3(0.18g,0.22mmol)于甲苯
(70ml)中的混合物在80℃下加热1h。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过biotage isolera纯化。对于c
26h19
d3n3o(m+h)
+
,lcms计算值:m/z=395.2;实验值:395.2。
[1207]
步骤2. 6-(甲氧基-d3)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶4-氧化物
[1208][1209]
将3-氯过氧苯甲酸(9.33g,40.6mmol)在0℃下缓慢地添加至6-(甲氧基-d3)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(8g,20.28mmol)于dcm(100ml)中的溶液中。在室温下搅拌过夜之后,将反应用na2s2o3溶液和1m naoh溶液处理。在室温下搅拌30min之后,分离有机相并用1m naoh溶液洗涤3次并用盐水溶液洗涤2次。将有机相经硫酸钠干燥,过滤并在真空中去除溶剂。所得产物不经进一步纯化即用于下一步骤中。对于c
26h19
d3n3o2(m+h)
+
,lc-ms计算值:m/z=411.2;实验值411.2。
[1210]
步骤3. 5-氯-6-(甲氧基-d3)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1211][1212]
将草酰氯(2.65ml,30.3mmol)于dcm中的溶液在0℃下缓慢地添加至6-(甲氧基-d3)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶4-氧化物(8.3g,20.22mmol)和diea(10.59ml,60.7mmol)于dcm(100ml)中的溶液中。在0℃下搅拌1h之后,将反应用dcm稀释并小心地用水处理。分离有机相,用水洗涤3次,用饱和nahco3溶液洗涤2次,用盐水洗涤2次并经硫酸钠干燥。在真空中去除溶剂之后,所得产物不经进一步纯化即用于下一步骤中。对于c
26h18
d3cln3o(m+h)
+
,lc-ms计算值:m/z=429.1;实验值429.2。
[1213]
步骤4. 5-(2,3-二甲基苯基)-6-(甲氧基-d3)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1214][1215]
将5-氯-6-(甲氧基-d3)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(1.1g,2.56mmol)、(2,3-二甲基苯基)硼酸(0.577g,3.85mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(0.205g,0.256mmol)和k3po4(1.1g,5.13mmol)置于烧瓶中并且将烧瓶抽真空并用n2回填三次。在添加1,4-二噁烷(10ml)和水(1ml)之后,
将反应混合物在100℃下搅拌1h。在冷却至室温之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过biotage isolera纯化。对于c
34h27
d3n3o(m+h)
+
,lcms计算值:m/z=499.3;实验值:499.2。
[1216]
步骤5. 5-(2,3-二甲基苯基)-6-(甲氧基-d3)-1h-吡唑并[4,3-b]吡啶
[1217][1218]
将tfa(10ml)和水(1ml)添加至5-(2,3-二甲基苯基)-6-(甲氧基-d3)-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(1.0g,2.0mmol)于dcm(10ml)中的溶液中。在室温下搅拌30min之后,添加ch3cn和水并在真空中蒸发dcm。滤出沉淀的固体。将反应混合物进一步用水稀释并用etoac/己烷1:1混合物洗涤3次。分离水相并在真空中去除所有溶剂。将残余物溶解于dcm中并用nahco3溶液中和。将有机相进一步用nahco3溶液、盐水洗涤2次,然后经硫酸钠干燥。在真空中蒸发溶剂。所得粗产物不经进一步纯化即用于下一步骤中。对于c
15h13
d3n3o(m+h)
+
,lc-ms计算值:m/z=257.1;实验值257.1。
[1219]
步骤6. 5-(2,3-二甲基苯基)-3-碘-6-(甲氧基-d3)-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1220][1221]
将1-碘吡咯烷-2,5-二酮(614mg,2.73mmol)添加至5-(2,3-二甲基苯基)-6-(甲氧基-d3)-1h-吡唑并[4,3-b]吡啶(700mg,2.73mmol)于dmf(5ml)中的溶液中。在80℃下搅拌1h之后,将反应混合物冷却至室温,并且添加cs2co3(1.7g,5.46mmol)和1-(氯甲基)-4-甲氧基苯(535μl,4.10mmol)。在80℃下再搅拌1h之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过biotage isolera纯化。对于c
23h20
d3in3o2(m+h)
+
,lcms计算值:m/z=503.1;实验值:503.1。
[1222]
步骤7. 5-(2,3-二甲基苯基)-6-(甲氧基-d3)-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1223]
将5-(2,3-二甲基苯基)-3-碘-6-(甲氧基-d3)-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(25mg,0.050mmol)、1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪(47.4mg,0.156mmol)、xphos pd g2(4.10mg,5.22μmol)、磷酸钾(44.3mg,0.209mmol)于水(0.100ml)和1,4-二噁烷(1ml)中的溶液加热至80℃持续2h。然后将反应混合物冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤,经na2so4干燥,过滤,并浓缩至干。然后将残余物溶解于三氟甲磺酸(0.5ml)中。将混合物在室
温下搅拌1h,用ch3cn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
25h26
d3n6o(m+h)+,lcms计算值:m/z=432.2;实验值432.3。
[1224]
实施例49. 5-(2,3-二甲基苯基)-6-甲氧基-3-(6-((1s,4s)-5-甲基-2,5-二氮杂双环[2.2.1]庚-2-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1225][1226]
此化合物根据实施例45中所描述的程序,使用(1s,4s)-2-甲基-2,5-二氮杂双环[2.2.1]庚烷二氢溴酸盐替代1-甲基哌嗪-2-酮盐酸盐来制备。产物作为tfa盐被分离。对于c
26h29
n6o(m+h)
+
,lc-ms计算值:m/z=441.2;实验值441.3。
[1227]
实施例50. 1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n,n-二甲基哌啶-4-羧酰胺
[1228][1229]
此化合物根据实施例45中所描述的程序,使用n,n-二甲基哌啶-4-羧酰胺替代1-甲基哌嗪-2-酮盐酸盐来制备。产物作为tfa盐被分离。对于c
28h33
n6o2(m+h)
+
,lc-ms计算值:m/z=485.3;实验值485.3。
[1230]
实施例51. 1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-4-甲基哌啶-4-羧酸
[1231][1232]
步骤1. 1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-4-甲基哌啶-4-羧酸叔丁酯
[1233][1234]
此化合物根据实施例45中所描述的程序,使用4-甲基哌啶-4-羧酸叔丁酯盐酸盐替代1-甲基哌嗪-2-酮盐酸盐来制备。对于c
31h38
n5o3(m+h)
+
,lcms计算值:m/z=528.3;实验值528.5。
[1235]
步骤2. 1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-4-甲基哌啶-4-羧酸
[1236]
此化合物通过用含tfa的dcm处理1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-4-甲基哌啶-4-羧酸叔丁酯,随后通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化来制备。产物作为tfa盐被分离。对于c
27h30
n5o3(m+h)
+
,lc-ms计算值:m/z=472.2;实验值472.4。
[1237]
实施例52. 3-(4-(5-(2-氟-3-甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-n,n-二甲基氮杂环丁烷-1-羧酰胺
[1238][1239]
步骤1. 5-(2-氟-3-甲基苯基)-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1240][1241]
将5-氯-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(实施例14,步骤4;0.50g,1.174mmol)、(2-氟-3-甲基苯基)硼酸(0.217g,1.41mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(0.094g,0.117mmol)和磷酸钾(0.498g,2.348mmol)置于烧瓶中并且将烧瓶抽真空并用n2回填三次。在添加1,4-二噁烷(5ml)和水(500μl)之后,将反应混合物在100℃下搅拌1h。此后,将其冷却至室温,用水稀释并用etoac萃取三次。将合并的有机相用饱和nacl洗涤,经na2so4干燥,过滤并浓缩至干。将残余物通过硅胶色谱纯化以得到所需产物。对于c
33h27
fn3o(m+h)
+
,lc-ms计算值:m/z=500.2;实验值500.2。
四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸叔丁酯(266mg,0.763mmol)、磷酸钾(270mg,1.272mmol)和[二氯[1,1
’‑
双(二苯基膦基)二茂铁]钯(ii)二氯甲烷加合物(51.9mg,0.064mmol)。将反应用n2脱气并在80℃下搅拌2h。此后,将其冷却至室温,用etoac稀释,依序用水、饱和nacl洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
33h36
fn6o4(m+h)
+
,lc-ms计算值:m/z=599.3;实验值599.3。
[1251]
步骤5. 3-(4-(5-(2-氟-3-甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-n,n-二甲基氮杂环丁烷-1-羧酰胺
[1252]
向3-(4-(5-(2-氟-3-甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸叔丁酯(20mg,0.033mmol)于dcm(1ml)中的溶液中添加0.5ml tfa。将反应搅拌1h,然后浓缩至干。将粗材料溶解于dcm(1ml)中,然后向其中添加tea(9.31μl,0.067mmol)和二甲基氨基甲酰氯(3.95mg,0.037mmol)。将反应混合物在室温下搅拌1h,随后添加0.5ml三氟甲磺酸。在室温下再搅拌2h之后,将反应用水和meoh稀释,然后通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
23h25
fn7o2(m+h)
+
,lcms计算值:m/z=450.2;实验值450.2。
[1253]
实施例53.n-((顺)-4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)环己基)乙酰胺
[1254][1255]
步骤1. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶
[1256][1257]
将5-氯-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(实施例14,步骤4;0.50g,1.174mmol)、2-(2,3-二氢-1h-茚-4-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环(0.344g,1.409mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(0.094g,0.117mmol)和磷酸钾(0.498g,2.348mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(5ml)和水(500μl)之后,将反应混合物在100℃下搅拌1h。此后,将其冷却至室温,用水稀释并用etoac萃取三次。将合并的有机相用饱和nacl
洗涤,经na2so4干燥,过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
35h30
n3o(m+h)
+
,lc-ms计算值:m/z=508.2;实验值508.2。
[1258]
步骤2. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1259][1260]
将tfa(1.23ml,16mmol)和水(0.028ml,1.6mmol)添加至5-(2-氟-3-甲基苯基)-6-甲氧基-1-三苯甲基-1h-吡唑并[4,3-b]吡啶(400mg,0.80mmol)于dcm(2ml)中的溶液中。在室温下搅拌30min之后,添加ch3cn和水并在真空中蒸发dcm。滤出沉淀的固体。将反应混合物进一步用水稀释并用etoac/己烷1:1混合物洗涤3次。分离水相并在真空中去除所有溶剂。将残余物溶解于dcm中并用nahco3溶液中和。将有机相进一步用nahco3溶液、盐水洗涤2次,然后干燥并在真空中蒸发溶剂。所得粗产物不经进一步纯化即用于下一步骤中。对于c
16h16
n3o(m+h)
+
,lc-ms计算值:m/z=266.1;实验值266.1。
[1261]
步骤3. 5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1262][1263]
向5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(190mg,0.74mmol)于dmf(2ml)中的溶液中添加1-碘吡咯烷-2,5-二酮(180mg,0.81mmol)。将反应温至80℃并在所述温度下搅拌1h。此后,将反应混合物冷却至室温并添加1-(氯甲基)-4-甲氧基苯(131mg,0.90mmol)和cs2co3(380mg,1.166mmol)。将反应混合物在90℃下搅拌1h。此后,将其冷却至室温,用水稀释并用etoac萃取三次。将合并的有机相用饱和nacl洗涤,经na2so4干燥,过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
24h23
in3o2(m+h)
+
,lc-ms计算值:m/z=512.1;实验值512.0。
[1264]
步骤4. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1265]
[1266]
向5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(300mg,0.587mmol)于1,4-二噁烷(2ml)和水(0.4ml)中的溶液中添加4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-羧酸叔丁酯(207mg,0.704mmol)、磷酸钾(249mg,1.173mmol)和[二氯[1,1
’‑
双(二苯基膦基)二茂铁]钯(ii)二氯甲烷加合物(47.9mg,0.059mmol)。将反应用n2脱气并在80℃下搅拌2h。此后,将其冷却至室温,并且添加2ml tfa。将反应再搅拌30min,然后用etoac稀释。将有机溶液依序用水、饱和nacl洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
27h26
n5o2(m+h)
+
,lc-ms计算值:m/z=452.2;实验值452.2。
[1267]
步骤5.n-((顺)-4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)环己基)乙酰胺
[1268]
在小瓶中,将n-((反)-4-羟基环己基)乙酰胺(13.93mg,0.089mmol)和tea(12.4μl,0.089mmol)溶解于dcm(1ml)中。将甲烷磺酰氯(6.90μl,0.089mmol)在0℃下经5min逐滴添加至反应混合物中。在室温下搅拌30min之后,将饱和nahco3溶液添加至反应混合物中,随后用二氯甲烷萃取。将合并的有机相经na2so4干燥,过滤并浓缩。将5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶(20mg,0.044mmol)和cs2co3(28.9mg,0.089mmol)的乙腈(1ml)溶液添加至所得材料中。将反应混合物加热至100℃。5h之后,将三氟甲磺酸(0.5ml)在室温下添加至反应混合物中。10min之后,将反应混合物用meoh稀释,然后通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h31
n6o2(m+h)+,lc-ms计算值:m/z=471.2;实验值471.2。
[1269]
实施例54. 5-(2,3-二氢-1h-茚-4-基)-3-(6-(2,4-二甲基哌嗪-1-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1270][1271]
步骤1. 3-(6-氯吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1272][1273]
向5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(实施例53,步骤3;500mg,0.98mmol)于1,4-二噁烷(4ml)和水(1ml)中的溶液中添加(6-氯吡啶-3-基)硼酸(185mg,1.173mmol)、磷酸钾(415mg,1.956mmol)和[二氯[1,1
’‑
双
(二苯基膦基)二茂铁]钯(ii)二氯甲烷加合物(80mg,0.098mmol)。将反应用n2脱气并在80℃下搅拌8h。此后,将其冷却至室温,然后用etoac稀释。所得溶液依序用水、饱和nacl洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过硅胶色谱纯化以得到所需产物。对于c
29h26
cln4o2(m+h)
+
,lc-ms计算值:m/z=497.2;实验值497.2。
[1274]
步骤2. 5-(2,3-二氢-1h-茚-4-基)-3-(6-(2,4-二甲基哌嗪-1-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1275]
向3-(6-氯吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(20mg,0.040mmol)于1,4-二噁烷(0.5ml)中的溶液中添加1,3-二甲基哌嗪(4.6mg,0.04mmol)、叔丁醇钠(7.7mg,0.080mmol)和氯(2-二环己基膦基-2’,6
’‑
二异丙氧基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(ii)(3.29mg,4.02μmol)。将反应用n2脱气并在100℃下搅拌。1h之后,将三氟甲磺酸(0.5ml)在室温下添加至反应混合物中。10min之后,将反应混合物用meoh稀释,然后通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h31
n6o(m+h)+,lc-ms计算值:m/z=455.3;实验值455.3。
[1276]
实施例55. 2-(3-(3-(6-(4-乙酰基哌嗪-1-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2-甲基苯基)乙腈
[1277][1278]
步骤1. 5-(3-(氰基甲基)-2-甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1279][1280]
此化合物根据实施例14中所描述的程序,使用2-(2-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)苯基)乙腈(中间体1)替代2-(2,3-二氢-1h-茚-4-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环作为起始材料来制备。对于c
21h22
in4o3(m+h)
+
,lc-ms计算值:m/z=505.1;实验值505.0。
[1281]
步骤2. 2-(3-(3-(6-(4-乙酰基哌嗪-1-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2-甲基苯基)乙腈
[1282]
向5-(3-(氰基甲基)-2-甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(20mg,0.040mmol)于1,4-二噁烷(0.5ml)和水(0.1ml)中的溶液中添加1-(4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪-1-基)乙-1-酮(16mg,
0.048mmol)、磷酸钾(16mg,0.079mmol)和[二氯[1,1
’‑
双(二苯基膦基)二茂铁]钯(ii)二氯甲烷加合物(3mg,4μmol)。将反应用n2脱气并在80℃下搅拌2h。此后,将其冷却至室温,并且添加1ml tfa。将反应再搅拌30min,然后用meoh稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h28
n7o2(m+h)+,lc-ms计算值:m/z=482.2;实验值482.3。
[1283]
实施例56. 2-(3-(6-甲氧基-3-(6-吗啉代吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2-甲基苯基)乙腈
[1284][1285]
此化合物根据实施例55中所描述的程序,使用4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)吗啉替代1-(4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪-1-基)乙-1-酮来制备。产物作为tfa盐被分离。对于c
25h25
n6o2(m+h)
+
,lc-ms计算值:m/z=441.2;实验值441.2。
[1286]
实施例57. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(6-(吡咯烷-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1287][1288]
向5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(实施例53,步骤3;20mg,0.04mmol)于1,4-二噁烷(0.5ml)和水(0.1ml)中的溶液中添加2-(吡咯烷-1-基)-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶(13mg,0.047mmol)、磷酸钾(17mg,0.078mmol)和[二氯[1,1
’‑
双(二苯基膦基)二茂铁]钯(ii)二氯甲烷加合物(3mg,4μmol)。将反应用n2脱气并在80℃下搅拌。2h之后,将三氟甲磺酸(0.5ml)在室温下添加至反应混合物中。10min之后,将反应混合物用meoh稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
25h26
n5o(m+h)+,lc-ms计算值:m/z=412.2;实验值412.2。
[1289]
实施例58. 4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吗啉
[1290][1291]
此化合物根据实施例57中所描述的程序,使用4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)吗啉替代2-(吡咯烷-1-基)-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶来制备。产物作为tfa盐被分离。对于c
25h26
n5o2(m+h)
+
,lc-ms计算值:m/z=428.2;实验值428.2。1h nmr(600mhz,dmso-d6)δ13.20(s,1h),9.18(d,j=2.2hz,1h),8.55(dd,j=9.1,2.4hz,1h),7.53(s,1h),7.33
–
7.20(m,3h),7.14(s,1h),4.49(bs,3h),3.85(s,3h),3.75(t,j=4.9hz,4h),2.93(t,j=7.4hz,2h),2.79(t,j=7.3hz,2h),2.48(s,1h),1.98(m,2h)ppm。
[1292]
实施例59. 4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-乙基哌嗪-1-羧酰胺
[1293][1294]
步骤1. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1295][1296]
向5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(实施例53,步骤3;200mg,0.4mmol)于1,4-二噁烷(5ml)和水(1ml)中的溶液中添加4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪-1-羧酸叔丁酯(183mg,0.469mmol)、磷酸钾(166mg,0.78mmol)和[二氯[1,1
’‑
双(二苯基膦基)二茂铁]钯(ii)二氯甲烷加合物(32mg,0.039mmol)。将反应用n2脱气并在80℃下搅拌8h。此后,将其冷却至室温,并且添加2ml tfa。将反应再搅拌30min,然后用etoac稀释。将溶液依序用水、饱和nacl洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
33h35
n6o2(m+h)
+
,lc-ms计算值:m/z=547.3;实验值547.3。
[1297]
步骤2. 4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-乙基哌嗪-1-羧酰胺
[1298]
向5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌嗪-1-基)
吡啶-3-基)-1h-吡唑并[4,3-b]吡啶(20mg,0.037mmol)于dcm(1ml)中的溶液中添加tea(10μl,0.073mmol)和异氰酸根合乙烷(3mg,0.040mmol)。将反应在室温下搅拌1h,然后浓缩至干。将三氟甲磺酸(0.5ml)添加至粗材料中并且将反应在室温下搅拌10min。然后将反应用水和meoh稀释,然后通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
28h32
n7o2(m+h)
+
,lcms计算值:m/z=498.2;实验值498.3。
[1299]
实施例60. 4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌嗪-1-羧酰胺
[1300][1301]
此化合物根据实施例59中所描述的程序,使用异氰酸根合三甲基癸烷替代异氰酸根合乙烷来制备。产物作为tfa盐被分离。对于c
26h28
n7o2(m+h)
+
,lc-ms计算值:m/z=470.2;实验值470.2。
[1302]
实施例61. 1-(4-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)苯基)哌嗪-1-基)乙-1-酮
[1303][1304]
此化合物根据实施例57中所描述的程序,使用1-(4-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)苯基)哌嗪-1-基)乙-1-酮替代2-(吡咯烷-1-基)-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶来制备。产物作为tfa盐被分离。对于c
28h30
n5o2(m+h)
+
,lc-ms计算值:m/z=468.2;实验值468.2。
[1305]
实施例62. 5-(2,3-二氢-1h-茚-4-基)-3-(4-(4-异丙基哌嗪-1-基)苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1306][1307]
此化合物根据实施例57中所描述的程序,使用1-异丙基-4-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)苯基)哌嗪替代2-(吡咯烷-1-基)-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶来制备。产物作为tfa盐被分离。对于c
29h34
n5o(m+h)
+
,lc-ms计算值:m/
z=468.3;实验值468.3。
[1308]
实施例63. 5-(2,3-二氢-1h-茚-4-基)-3-(4-(4-乙基哌嗪-1-基)苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1309][1310]
此化合物根据实施例57中所描述的程序,使用1-乙基-4-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)苯基)哌嗪替代2-(吡咯烷-1-基)-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶来制备。产物作为tfa盐被分离。对于c
28h32
n5o(m+h)
+
,lc-ms计算值:m/z=454.3;实验值454.3。
[1311]
实施例64. 1-(4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌嗪-1-基)乙-1-酮
[1312][1313]
此化合物根据实施例57中所描述的程序,使用1-(4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪-1-基)乙-1-酮替代2-(吡咯烷-1-基)-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶来制备。产物作为tfa盐被分离。对于c
27h29
n6o2(m+h)
+
,lc-ms计算值:m/z=469.2;实验值469.2。
[1314]
实施例65. 8-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮
[1315][1316]
此化合物根据实施例45中所描述的程序,使用1-氧杂-3,8-二氮杂螺[4.5]癸-2-酮盐酸盐替代1-甲基哌嗪-2-酮盐酸盐来制备。产物作为tfa盐被分离。对于c
27h29
n6o3(m+h)
+
,lc-ms计算值:m/z=485.2;实验值485.2。
[1317]
实施例66. 5-(2,3-二甲基苯基)-6-甲氧基-3-(1-(吡啶-2-基甲基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1318][1319]
步骤1. 6-溴-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1320][1321]
将6-溴-1h-吡唑并[4,3-b]吡啶(10g,50.5mmol)、1-(氯甲基)-4-甲氧基苯(8.7g,55.5mmol)、碳酸钾(7.68g,55.5mmol)置于圆底烧瓶中。在添加dmf(168ml)之后,将反应混合物在80℃下搅拌4h。此后,将其冷却至室温,用水稀释并用etoac萃取3次。将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤并浓缩至干。将残余物通过硅胶色谱纯化以得到所需产物。对于c
14h13
brn3o(m+h)
+
,lc-ms计算值:m/z=318.2;实验值318.2。
[1322]
步骤2. 6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1323][1324]
向250ml圆底烧瓶中添加cs2co3(4.67g,14.3mmol)、叔丁基xphos pd g3(0.47g,0.6mmol)、meoh(10ml)、甲苯(50ml)和6-溴-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(3.8g,11.9mmol)。将混合物抽真空并用n2回填三次并加热至100℃持续4h。将所得混合物过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
15h16
n3o2(m+h)
+
,lc-ms计算值:m/z=270.1;实验值270.1。
[1325]
步骤3. 6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶4-氧化物
[1326][1327]
向水浴中冷却的6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(13.3g,49.3mmol)于dcm(100ml)中的溶液中添加3-氯过氧苯甲酸(16.6g,74mmol)。将反应在室温下搅拌2h。将混合物用na2s2o3饱和溶液洗涤,随后用nahco3饱和溶液洗涤。将合并的有机相用饱和nacl洗涤,经na2so4干燥,过滤并浓缩至干。将残余物通过硅胶色谱纯化以得到所需产物。对于c
15h16
n3o3(m+h)
+
,lc-ms计算值:m/z=286.2;实验值286.2。
[1328]
步骤4. 5-氯-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1329][1330]
向6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶4-氧化物(12g,42.1mmol)于dcm(90ml)中的溶液中添加n,n-二异丙基乙胺(10.9g,84mmol)。将混合物在冰浴中冷却并添加草酰氯(8.01g,63.1mmol)。将所得混合物在0℃下搅拌1h,然后用饱和nahco3溶液淬灭。将产物用dcm萃取,合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
15h15
cln3o2(m+h)
+
,lc-ms计算值:m/z=304.1;实验值304.1。
[1331]
步骤5. 5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1332][1333]
将5-氯-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(3.5g,11.52mmol)、(2,3-二甲基苯基)硼酸(2.07g,13.83mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(0.90g,1.15mmol)和碳酸铯(7.51g,23.05mmol)置于圆底烧瓶中并且将烧瓶抽真空并用n2回填三次。在添加1,4-二噁烷(32ml)和水(6.4ml)之后,将反应混合物在100℃下搅拌1h。此后,将其冷却至室温,用水稀释并用etoac萃取3次。将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
23h24
n3o2(m+h)
+
,lc-ms计算值:m/z=374.2;实验值374.2。
[1334]
步骤6. 5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1335][1336]
将5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(3.87g,10.36mmol)溶解于tfa(12ml)中。将混合物加热至100℃持续1h,然后其冷却至0℃并用4n naoh水溶液中和。将产物用dcm(50ml
×
3)萃取并且将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤并浓缩至干。向残余物中添加nis(2.56g,11.4mmol)和dmf(20ml)。将所得混合物加热至80℃持续2h。此后,将其冷却至室温,用水稀释并用etoac萃取3次。将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤并浓缩至干。残余物不经纯
化直接用于下一步骤中。对于c
15h15
in3o(m+h)
+
,lc-ms计算值:m/z=380.2;实验值380.2。
[1337]
步骤7. 5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1338][1339]
向5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶(1.9g,5.01mmol)于dmf(10ml)中的溶液中添加二碳酸二叔丁酯(2.19g,10.02mmol)、三乙胺(1.27g,12.53mmol)和4-二甲基氨基吡啶(6mg,0.05mmol)。将所得混合物在室温下搅拌2h。此后,将其用水稀释并用etoac萃取3次。将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
20h23
in3o3(m+h)
+
,lc-ms计算值:m/z=480.2;实验值480.2。
[1340]
步骤8. 5-(2,3-二甲基苯基)-6-甲氧基-3-(1-(吡啶-2-基甲基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1341]
向5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(15mg,0.031mmol)于1,4-二噁烷(0.5ml)和水(0.05ml)中的溶液中添加2-((4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)甲基)吡啶(18mg,0.063mmol)、磷酸钾(19.9mg,0.094mmol)和氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(2.5mg,0.003mmol)。将反应用n2脱气并在80℃下搅拌3h。此后,将其冷却至室温,用etoac稀释,依序用水、饱和nacl洗涤并且经na2so4干燥。合并有机相,过滤并浓缩至干。将残余物溶解于含4n hcl的二噁烷(1ml)中并且将所得混合物在室温下搅拌。10min之后,将反应混合物用meoh稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
24h23
n6o(m+h)+,lc-ms计算值:m/z=411.2;实验值411.2。
[1342]
实施例67. 3-(1-环丙基-1h-吡唑-4-基)-5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1343][1344]
此化合物根据实施例66中所描述的程序,使用1-环丙基-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑替代2-((4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)甲基)吡啶作为起始材料来制备。产物作为tfa盐被分离。对于c
21h22
n5o(m+h)
+
,lc-ms计算值:m/z=360.2;实验值360.2。
[1345]
实施例68. 6-甲氧基-5-(2-甲基-3-(甲基-d3)苯基)-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1346][1347]
步骤1. 1-溴-2-甲基-3-(甲基-d3)苯
[1348][1349]
在-20℃下向1-溴-3-碘-2-甲基苯(300mg,1mmol)于thf(3ml)中的溶液中缓慢地添加thf中的2.0m异丙基氯化镁溶液(0.76ml,1.5mmol)。将反应混合物在0℃下搅拌1h,然后添加碘甲烷-d3。将混合物在室温下搅拌过夜并且然后用etoac稀释。将混合物依序用水和饱和nacl溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。
[1350]
步骤2. 4,4,5,5-四甲基-2-(2-甲基-3-(甲基-d3)苯基)-1,3,2-二氧硼戊环
[1351][1352]
向1-溴-2-甲基-3-(甲基-d3)苯(112mg,0.6mmol)于1,4-二噁烷(4ml)中的溶液中添加双(频哪醇合)二硼(302mg,1.19mmol)、乙酸钾(175mg,1.79mmol)和[1,1
’‑
双(二苯基膦基)二茂铁]二氯化钯(ii)(1:1)(49mg,0.06mmol)。将反应用n2吹扫并在90℃下搅拌12h。此后,将其冷却至室温并用etoac稀释。然后依序用水、饱和nacl溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
14h19
d3bo2(m+h)+,lc-ms计算值:m/z=236.2;实验值236.2。
[1353]
步骤3. 6-甲氧基-1-(4-甲氧基苄基)-5-(2-甲基-3-(甲基-d3)苯基)-1h-吡唑并[4,3-b]吡啶
[1354]
[1355]
将5-氯-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(155mg,0.51mmol)、4,4,5,5-四甲基-2-(2-甲基-3-(甲基-d3)苯基)-1,3,2-二氧硼戊环(100mg,0.43mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(33mg,0.043mmol)和碳酸铯(277mg,0.85mmol)置于圆底烧瓶中并且将烧瓶抽真空并用n2回填三次。在添加1,4-二噁烷(2.5ml)和水(0.5ml)之后,将反应混合物在100℃下搅拌1h。将反应混合物冷却至室温,用水稀释并用etoac萃取3次。将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
23h21
d3n3o2(m+h)
+
,lc-ms计算值:m/z=377.2;实验值377.2。
[1356]
步骤4. 3-碘-6-甲氧基-5-(2-甲基-3-(甲基-d3)苯基)-1h-吡唑并[4,3-b]吡啶
[1357][1358]
将6-甲氧基-1-(4-甲氧基苄基)-5-(2-甲基-3-(甲基-d3)苯基)-1h-吡唑并[4,3-b]吡啶(0.3g,0.8mmol)溶解于tfa(1ml)中。将混合物加热至100℃持续1h,然后冷却至0℃并用4n naoh水溶液中和。将产物用dcm(5ml
×
3)萃取并且将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤并浓缩至干。
[1359]
向残余物中添加nis(0.18g,0.8mmol)和dmf(4ml)。将所得混合物加热至80℃持续2h。此后,将其冷却至室温,用水稀释并用etoac萃取3次。将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤并浓缩至干。残余物不经纯化直接用于下一步骤中。对于c
15h12
d3in3o(m+h)
+
,lc-ms计算值:m/z=383.2;实验值383.2。
[1360]
步骤5. 3-碘-6-甲氧基-5-(2-甲基-3-(甲基-d3)苯基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶
[1361][1362]
向3-碘-6-甲氧基-5-(2-甲基-3-(甲基-d3)苯基)-1h-吡唑并[4,3-b]吡啶(306mg,0.8mmol)于dmf(4ml)中的溶液中添加2-(三甲基甲硅烷基)乙氧基甲基氯化物(0.2g,1.2mmol)和碳酸铯(0.52g,1.6mmol)。所得混合物在80℃下搅拌1h。此后,将混合物用水稀释并用etoac萃取3次。将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤并浓缩至干。残余物不经纯化直接用于下一步骤中。对于c
21h26
d3in3o2si(m+h)
+
,lc-ms计算值:m/z=513.2;实验值513.2。
[1363]
步骤6. 6-甲氧基-5-(2-甲基-3-(甲基-d3)苯基)-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1364]
向3-碘-6-甲氧基-5-(2-甲基-3-(甲基-d3)苯基)-1-((2-(三甲基甲硅烷基)-乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶(60mg,0.12mmol)于1,4-二噁烷(1ml)和水(0.1ml)中的溶液中添加1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪(71mg,0.23mmol)、磷酸钾(75mg,0.35mmol)和[1,1
’‑
双(二苯基膦基)二茂铁]-二氯化钯(ii)(1:1)(10mg,0.012mmol)。将反应用n2吹扫并在80℃下搅拌2h。将混合物冷却至室温并用etoac稀释。然后依序用水、饱和nacl溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物溶解于tfa(0.5ml)中并在室温下搅拌1h。浓缩混合物并添加氢氧化铵溶液(0.5ml)。将反应混合物在室温下搅拌1h然后浓缩。将残余物溶解于meoh中并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
25h26
d3n6o(m+h)
+
,lc-ms计算值:m/z=432.2;实验值432.2。1h nmr(400mhz,dmso-d6)δ9.23
–
9.18(d,j=2.3hz,1h),8.53
–
8.46(dd,j=8.9,2.4hz,1h),7.54
–
7.49(s,1h),7.26
–
7.21(d,j=1.6hz,1h),7.20
–
7.14(t,j=7.5hz,1h),7.12
–
7.06(m,2h),4.50
–
4.42(d,j=13.2hz,2h),3.87
–
3.82(s,3h),3.22
–
3.05(dt,j=24.7,12.1hz,4h),2.88
–
2.82(d,j=3.7hz,3h),2.00
–
1.95(s,3h)ppm。
[1365]
实施例69. 1-(4-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)哌啶-1-基)乙-1-酮
[1366][1367]
步骤1. 5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1368][1369]
向5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶(实施例66,1.9g,5.01mmol)于dmf(10ml)中的溶液中添加1-(氯甲基)-4-甲氧基苯(1.02g,6.51mmol)和碳酸钾(1.04g,7.52mmol)。所得混合物在80℃下搅拌1h。此后,将其用水稀释并且将产物用etoac萃取3次。将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤并浓缩至干。残余物不经纯化直接用于下一步骤中。对于c
23h23
in3o2(m+h)
+
,lc-ms计算值:m/z=500.2;实验值500.2。
[1370]
步骤2. 4-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)哌啶-1-羧酸叔丁酯
[1371][1372]
向5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(150mg,0.3mmol)于1,4-二噁烷(3ml)和水(0.3ml)中的溶液中添加4-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)哌啶-1-羧酸叔丁酯(227mg,0.6mmol)、磷酸钾(191mg,0.9mmol)和氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(24mg,0.03mmol)。将反应用n2脱气并在80℃下搅拌3h。此后,将其冷却至室温并用etoac稀释。所得溶液依序用水、饱和nacl溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
36h43
n6o4(m+h)+,lc-ms计算值:m/z=623.2;实验值623.2。
[1373]
步骤3. 5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-3-(1-(哌啶-4-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1374][1375]
将4-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)哌啶-1-羧酸叔丁酯(156mg,0.3mmol)溶解于含4n hcl的二噁烷(3ml)中并且将所得混合物在室温下搅拌。10min之后,将反应混合物浓缩至干并且粗物质直接用于下一步骤。对于c
31h35
n6o2(m+h)
+
,lc-ms计算值:m/z=523.2;实验值523.2。
[1376]
步骤4. 1-(4-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)哌啶-1-基)乙-1-酮
[1377]
向5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-3-(1-(哌啶-4-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶(10mg,0.019mmol)于dcm(0.5ml)中的溶液中添加n,n-二异丙基乙胺(24mg,0.19mmol)和乙酰氯(7.5mg,0.096mmol)。将反应混合物在室温下搅拌1h。此后,将其用etoac稀释,依序用水、饱和nacl溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物溶解于dcm(0.5ml)和三氟甲磺酸(0.5ml)中。30min之后,将反应混合物用meoh稀释,然后通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
25h29
n6o2(m+h)+,lc-ms计算值:m/z=445.2;实验值445.2。
[1378]
实施例70. 4-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)哌啶-1-羧酸甲酯
[1379][1380]
此化合物根据实施例69中所描述的程序,使用氯甲酸甲酯替代乙酰氯作为起始材料来制备。产物作为tfa盐被分离。对于c
25h29
n6o3(m+h)
+
,lc-ms计算值:m/z=461.2;实验值461.2。
[1381]
实施例71. 3-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸甲酯
[1382][1383]
步骤1. 3-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸叔丁酯
[1384][1385]
向5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(实施例69,150mg,0.3mmol)于1,4-二噁烷(3ml)和水(0.3ml)中的溶液中添加3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸叔丁酯(210mg,0.6mmol)、磷酸钾(191mg,0.9mmol)和氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(24mg,0.03mmol)。将反应用n2脱气并在80℃下搅拌3h。此后,将其冷却至室温,然后用etoac稀释。然后依序用水、饱和nacl溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
34h39
n6o4(m+h)+,lc-ms计算值:m/z=595.2;实验值595.2。
[1386]
步骤2. 3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1387][1388]
将3-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸叔丁酯(178mg,0.3mmol)溶解于含4n hcl的二噁烷(3ml)中并且将所得混合物在室温下搅拌。10min之后,将反应混合物浓缩至干并且粗物质直接用于下一步骤中。对于c
29h31
n6o2(m+h)
+
,lc-ms计算值:m/z=495.2;实验值495.2。
[1389]
步骤3. 3-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸甲酯
[1390]
向3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(10mg,0.02mmol)于dcm(0.5ml)中的溶液中添加n,n-二异丙基乙胺(24mg,0.19mmol)和氯甲酸甲酯(9mg,0.096mmol)。将混合物在室温下搅拌1h。此后,将其用etoac稀释,依序用水、饱和nacl溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物溶解于dcm(0.5ml)和三氟甲磺酸(0.5ml)中。30min之后,将反应混合物用meoh稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
23h25
n6o3(m+h)
+
,lc-ms计算值:m/z=433.2;实验值433.2。
[1391]
实施例72. 3-(4-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-n,n-二甲基氮杂环丁烷-1-羧酰胺
[1392][1393]
向3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(实施例71,10mg,0.02mmol)于dcm(0.5ml)中的溶液中添加n,n-二异丙基乙胺(24mg,0.19mmol)和二甲基氨基甲酰氯(11mg,0.1mmol)。将混合物在室温下搅拌1h。此后,将其用etoac稀释,依序用水、饱和nacl溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物溶解于dcm(0.5ml)和三氟甲磺酸(0.5ml)中。30min之后,将反应混合物用meoh稀释,然后通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
24h28
n7o2(m+h)
+
,lc-ms计算值:m/z=446.2;实验值446.2。1h nmr(500mhz,dmso-d6)δ8.53
–
8.31(s,1h),8.26
–
8.10(s,1h),7.55
–
7.40(s,1h),7.24
–
7.19(d,j=8.1hz,1h),7.19
–
7.13(t,j=7.5hz,1h),7.11
–
7.07(dd,j=7.4,1.7hz,1h),5.47
–
5.24(m,1h),4.32
–
4.26(t,j=8.4hz,
2h),4.26
–
4.20(dd,j=8.7,5.9hz,2h),3.91
–
3.70(s,3h),2.82
–
2.76(s,6h),2.36
–
2.27(s,3h),2.01
–
1.92(s,3h)ppm。
[1394]
实施例73. 4-(6-甲氧基-3-(6-((四氢呋喃-3-基)氧基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚
[1395][1396]
步骤1. 5-(2-羟基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1397][1398]
5-氯-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(2.00g,7.05mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-2-酚(2.2g,8.46mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(120mg,0.15mmol)和磷酸钾(4.6g,14.1mmol)置于烧瓶中并且将烧瓶抽真空并用n2回填三次。在添加1,4-二噁烷(20ml)和水(4ml)之后,将反应混合物在80℃下搅拌2h。在冷却至室温之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过biotage isolera纯化以得到白色固体(2.40g,89%)。对于c
21h24
n3o4(m+h)
+
,lcms计算值:m/z=382.2;实验值382.2。
[1399]
步骤2. 4-(6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚
[1400][1401]
将dcm(20ml)和tfa(10ml)的混合物中的5-(2-羟基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(2.40g,6.29mmol)在室温下搅拌1h。然后将反应混合物在真空中浓缩,溶解于dcm中并用nahco3溶液中和。分离有机相,经硫酸钠干燥并在真空中浓缩。粗材料不经进一步纯化即用于下一步骤中。对于c
16h16
n3o2(m+h)
+
,lcms计算值:m/z=282.1;实验值282.1。
[1402]
步骤3. 5-(2-羟基-2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]
nh3)/co2洗脱,流动速率65ml/min,t
r,峰1
=11.1min,t
r,峰2
=12.4min)分离。收集峰2并且在真空中蒸发溶剂。
[1411]
将所得材料溶解于1,4-二噁烷(2ml)和水(2ml)中。在添加碳酸铯(31.3mg,0.096mmol)之后,将反应混合物在100℃下加热2小时。在冷却至室温之后,将混合物用ch3cn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
25h25
n4o4(m+h)
+
,lcms计算值:m/z=445.2;实验值:445.2。
[1412]
实施例74. 4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)2,3-二氢-1h-茚-2-d-2-酚
[1413][1414]
步骤1. 4-溴-2,3-二氢-1h-茚-2-d-2-酚
[1415][1416]
将硼氘化钠(0.397g,9.48mmol)添加至4-溴-1,3-二氢-2h-茚-2-酮(1.00g,4.74mmol)于thf(5ml)和meoh(5ml)中的溶液中。将反应混合物在室温下搅拌1h之后,添加水。用etoac萃取所需产物,将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。所得粗产物不经进一步纯化即用于下一步骤中。
[1417]
步骤2. 4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-2-d-2-酚
[1418][1419]
此化合物根据中间体2中所描述的程序,使用4-溴-2,3-二氢-1h-茚-2-d-2-酚替代4-溴-2,3-二氢-1h-茚-1-酚作为起始材料来制备。
[1420]
步骤3. 4-(6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)2,3-二氢-1h-茚-2-d-2-酚
[1421]
将5-氯-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(1.05g,2.89mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-2-d-2-酚(0.904g,3.46mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(150mg,0.20mmol)和磷酸钾(150mg,7.00mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(10.0ml)和水(2.0ml)之后,将反应混
合物在100℃下搅拌1h。在冷却至室温之后,将混合物用dcm稀释并过滤。在真空中浓缩滤液并且将所得残余物通过biotage isolera纯化。
[1422]
将两种对映体用手性制备型hplc(phenomenex lux cellulose-1 5um 21.2
×
250mm,用10%etoh/co2洗脱,流动速率65ml/min,t
r,峰1
=19.5min,t
r,峰2
=21.8min)分离。收集峰2并且在真空中蒸发溶剂。
[1423]
将所得材料溶解于1,4-二噁烷(2ml)和水(2ml)中。在添加碳酸铯(31.3mg,0.096mmol)之后,将反应混合物在100℃下加热2h。在冷却至室温之后,将混合物用ch3cn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
20
dh
19
n5o2(m+h)
+
,lcms计算值:m/z=363.2;实验值:363.2。1h nmr(500mhz,dmso-d6)δ8.35(s,1h),8.08(s,1h),7.50(s,1h),7.34
–
7.28(d,j=7.2hz,1h),7.29
–
7.20(m,2h),3.90(s,3h),3.84(s,3h),3.16-3.11(d,j=16.0,1h),3.08
–
3.00(d,j=16.0,1h),2.88
–
2.80(d,j=16.0,1h),2.70
–
2.64(d,j=16.0,1h)ppm。
[1424]
实施例75. 4-(6-甲氧基-3-(6-(1-甲基-5-氧代吡咯烷-3-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1425][1426]
步骤1. 4-(5-溴吡啶-2-基)-2-氧代吡咯烷-1-羧酸叔丁酯
[1427][1428]
向配备有搅拌棒的30-ml带螺旋盖的小瓶中装入2,6-二甲基-1,4-二氢吡啶-3,5-二羧酸二乙酯(413mg,1.629mmol)、5-溴-2-碘吡啶(300mg,1.057mmol)、[ir{df(cf3)ppy}2(dtbbpy)]pf6(28.1mg,0.025mmol)和2-氧代-2,5-二氢-1h-吡咯-1-羧酸叔丁酯(689mg,3.76mmol)。将小瓶密封并通过施加真空并用n2回填来交换气氛。在n2气氛下,经由注射器向管装入脱气溶剂(3:1dmso:h2o,15ml)。将所得悬浮液在用蓝色led辐照下搅拌18小时。然后将反应混合物用饱和碳酸氢钠溶液(60ml)处理并用乙酸乙酯(3
×
40ml)萃取。合并有机相,经硫酸镁干燥,过滤,并在真空下浓缩。将残余物通过快速柱色谱纯化以得到所需产物。对于c
14h18
brn2o3(m+h)
+
,lc-ms计算值:m/z=341.0;实验值341.0。
[1429]
步骤2. 4-(5-溴吡啶-2-基)-1-甲基吡咯烷-2-酮
[1430][1431]
将4-(5-溴吡啶-2-基)-2-氧代吡咯烷-1-羧酸叔丁酯(294mg,0.865mmol)溶解于
1ml tfa中并且将所得混合物在室温下搅拌。10min之后,将反应混合物浓缩至干。将所得残余物溶解于2ml dmf中并用冰浴冷却至0℃。添加氢化钠(41.5mg,1.73mmol)并且将所得溶液在0℃下搅拌30min。然后添加mei(108μl,1.73mmol),并且将所得混合物升温至室温并搅拌2小时。将反应用饱和nh4cl溶液处理并用dcm萃取。合并有机相,经硫酸镁干燥,过滤,并且在真空下浓缩。将残余物通过快速柱色谱纯化以得到所需产物。对于c
10h12
brn2o(m+h)+,lc-ms计算值:m/z=255.0;实验值255.0。
[1432]
将两种对映体用手性制备型hplc(phenomenex lux amylose-1 5um 21.2
×
250mm,用35%meoh/co2洗脱,流动速率65ml/min,t
r,峰1
=3.6min,t
r,峰2
=4.7min)分离。
[1433]
步骤3. 1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)吡咯烷-2-酮
[1434][1435]
将4-(5-溴吡啶-2-基)-1-甲基吡咯烷-2-酮(60mg,0.235mmol)的两种对映体单独地添加至双(频哪醇合)二硼(65.7mg,0.259mmol)、乙酸钾(69.2mg,0.706mmol)和pdcl2(dppf)-ch2cl2加合物(19.21mg,0.024mmol)于1,4-二噁烷(1ml)中的混合物中。将混合物加热至100℃持续8h。此后,将其冷却至室温。粗产物溶液不经进一步纯化直接用于下一步骤中。对于c
16h24
bn2o3(m+h)
+
,lcms计算值:m/z=303.2;实验值303.2。
[1436]
步骤4. 4-溴-2,3-二氢-1h-茚-1-甲腈
[1437][1438]
在0℃下向4-溴-2,3-二氢-1h-茚-1-酮(10g,47.4mmol)于dme(250ml)和
t
buoh(40ml)中的溶液中添加叔丁醇钾(10.63g,95mmol)和对甲基磺酰甲基异腈(11.10g,56.9mmol)。将混合物搅拌过夜,然后用水和1n hcl处理。将混合物用etoac萃取,合并有机相,经硫酸镁干燥,过滤,并在真空下浓缩。将残余物通过快速柱色谱纯化以得到所需产物。对于c
10
h9brn(m+h)
+
,lc-ms计算值:m/z=222.0;实验值222.2。
[1439]
步骤5. 4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,3-二氢-1h-茚-1-甲腈
[1440][1441]
将4-溴-2,3-二氢-1h-茚-1-甲腈(5.8g,26.5mmol)、乙酸钾(7.81g,80mmol)、双(频哪醇合)二硼(8.09g,31.8mmol)、pdcl2(dppf)-ch2cl2加合物(1.083g,1.327mmol)于1,4-二噁烷(100ml)中的混合物加热至100℃持续8h。此后,将其冷却至室温。粗产物溶液不经
1-羧酸叔丁酯(50mg,0.097mmol)、1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)吡咯烷-2-酮(来自步骤5的峰1,35.1mg,0.116mmol)、pdcl2(dppf)-ch2cl2加合物(7.91mg,9.68μmol)和k3po4(41.1mg,0.194mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(1ml)和水(100μl)之后,将反应混合物在80℃下搅拌1h。然后过滤反应,并且在真空中蒸发溶剂。添加dcm(1ml)和tfa(0.5ml)并且将反应混合物在室温下搅拌30min。然后将混合物用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。
[1450]
产物用饱和nahco3洗涤并且进一步用手性制备型hplc(phenomenex lux 5um cellulose-2,21.2
×
250mm,用80%etoh/己烷洗脱,流动速率20ml/min,t
r,峰1
=13min,t
r,峰2
=16min)分离。峰1是所需产物。对于c
27h25
n6o2(m+h)
+
,lcms计算值:m/z=465.2;实验值:465.2。1h nmr(500mhz,dmso-d6)δ13.46(s,1h),9.55(d,j=2.1hz,1h),8.68(dd,j=8.2,2.2hz,1h),7.61(s,1h),7.56
–
7.46(m,3h),7.41(t,j=7.5hz,1h),4.58(t,j=8.1hz,1h),3.91(s,3h),3.86
–
3.71(m,2h),3.52(dd,j=9.2,6.4hz,1h),3.02
–
2.84(m,2h),2.77(s,3h),2.68
–
2.53(m,3h),2.21(dq,j=12.5,8.3hz,1h)ppm。
[1451]
实施例76. 4-(6-甲氧基-3-(6-(1-甲基-5-氧代吡咯烷-3-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1452][1453]
此化合物根据实施例75中所描述的程序,使用1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)吡咯烷-2-酮对映体峰2替代来自步骤3的峰1来制备。产物作为tfa盐被分离。
[1454]
将两种对映体用手性制备型hplc(phenomenex lux amylose-1 5um 21.2
×
250mm,用45%etoh/己烷洗脱,流动速率20ml/min,t
r,峰1
=9.7min,t
r,峰2
=12.7min)分离,其中峰2是所需产物。对于c
27h25
n6o2(m+h)
+
,lcms计算值:m/z=465.2;实验值:465.2。
[1455]
实施例77.(s)-1-(4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-基)-2-羟基丙-1-酮
[1456][1457]
步骤1. 5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶
[1458][1459]
在0℃下向5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶(1.5g,3.90mmol)的dmf(10ml)溶液中添加diea(1.363ml,7.80mmol)和sem-cl(1.04ml,5.85mmol)。在搅拌过夜之后,将反应用水处理并用etoac萃取产物。将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤,浓缩至干并通过快速柱色谱纯化以得到所需产物。对于c
21h29
in3o2si(m+h)
+
,lc-ms计算值:m/z=510.1;实验值510.1。
[1460]
步骤2. 3-(6-氯吡啶-3-基)-5-(2,3-二甲基苯基)-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶
[1461][1462]
向5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶(761mg,1.493mmol)于1,4-二噁烷(5ml)和水(1ml)中的溶液中添加(6-氯吡啶-3-基)硼酸(282mg,1.792mmol)、k3po4(633mg,2.99mmol)和pdcl2(dppf)-ch2cl2加合物(119mg,0.149mmol)。将反应用n2脱气并在80℃下搅拌3h。此后,将其冷却至室温,用etoac稀释,依序用水、饱和nacl洗涤并且经na2so4干燥。合并有机相,过滤,浓缩至干并通过快速柱色谱纯化以得到所需产物。对于c
26h32
cln4o2si(m+h)
+
,lc-ms计算值:m/z=495.2;实验值495.2。
[1463]
步骤3. 5-(5-(2,3-二甲基苯基)-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-3-基)-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯
[1464][1465]
向3-(6-氯吡啶-3-基)-5-(2,3-二甲基苯基)-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶(99mg,0.201mmol)于1,4-二噁烷(2ml)和水(0.4ml)中的溶液中添加4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-3,6-二氢吡啶-1(2h)-羧酸叔丁酯(124mg,0.402mmol)、k3po4(85mg,0.402mmol)和氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(16mg,0.02mmol)。将反应
用n2脱气并在100℃下搅拌3h。此后,将其冷却至室温,用etoac稀释,依序用水、饱和nacl洗涤并且经na2so4干燥。合并有机相,过滤,浓缩至干并通过快速柱色谱纯化以得到所需产物。对于c
36h48
n5o4si(m+h)
+
,lc-ms计算值:m/z=642.3;实验值642.2。
[1466]
步骤4. 5-(2,3-二甲基苯基)-6-甲氧基-3-(6-(哌啶-4-基)吡啶-3-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶
[1467][1468]
向5-(5-(2,3-二甲基苯基)-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-3-基)-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯(100mg,0.156mmol)的meoh(5ml)溶液中添加pd/c(16.58mg,0.016mmol)。将反应用h2吹扫并在室温下搅拌,连接至填充有氢气的气球持续4小时。完成之后,将反应通过短硅藻土移液管过滤并浓缩反应。将粗产物溶解于dcm(2ml)中并在室温下用tfa(0.5ml)处理。然后将混合物浓缩至干并且无需纯化即用于下一反应中。对于c
31h42
n5o2si(m+h)
+
,lc-ms计算值:m/z=544.3;实验值544.2。
[1469]
步骤5.(s)-1-(4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-基)-2-羟基丙-1-酮
[1470]
向5-(2,3-二甲基苯基)-6-甲氧基-3-(6-(哌啶-4-基)吡啶-3-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶(20mg,0.037mmol)的thf(1ml)溶液中添加(s)-2-羟基丙酸(3.31mg,0.037mmol)、diea(6.42μl,0.037mmol)和hatu(13.98mg,0.037mmol)。在搅拌过夜之后,将1ml 4n hcl添加至反应中,然后将所述反应加热至50℃持续30min。添加meoh并且将反应通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
28h32
n5o3(m+h)
+
,lc-ms计算值:m/z=486.2;实验值486.2。1h nmr(400mhz,dmso-d6)δ13.41(s,1h),9.49(s,1h),8.67(d,j=8.0hz,1h),7.57(s,1h),7.49(d,j=8.2hz,1h),7.17(m,3h),4.47(m,2h),4.11(d,j=13.4hz,1h),3.86(s,3h),3.14(m,1h),3.08
–
3.00(m,1h),2.72(m,1h),2.32(s,3h),1.98(s,3h),1.91(d,j=12.5hz,2h),1.80
–
1.54(m,2h),1.20m,3h)ppm。
[1471]
实施例78. 1-(4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-基)-2-羟基乙-1-酮
[1472][1473]
此化合物根据实施例77中所描述的程序,使用2-羟基乙酸替代(s)-2-羟基丙酸来
制备。产物作为tfa盐被分离。对于c
27h30
n5o3(m+h)
+
,lc-ms计算值:m/z=472.2;实验值472.2。1h nmr(600mhz,dmso-d6)δ13.77(s,1h),9.67(d,j=2.1hz,1h),9.07
–
8.97(m,1h),7.84(d,j=8.4hz,1h),7.73(s,1h),7.41
–
7.21(m,3h),4.64(d,j=12.8hz,1h),4.28(m,1h),3.99(s,3h),3.98
–
3.92(m,2h),3.29
–
3.20(m,2h),2.87(m,1h),2.44(s,3h),2.10(s,3h),2.06(d,j=13.1hz,2h),1.82(m,2h)ppm。
[1474]
实施例79. 4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环己烷-1-甲酸
[1475][1476]
步骤1. 5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶
[1477][1478]
将n-碘代琥珀酰亚胺(0.586g,2.61mmol)添加至5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶(0.82g,2.17mmol)于dmf(6ml)中的溶液中并且将反应在60℃下搅拌1小时。在用冰浴冷却之后,将混合物相继用dipea(0.455ml,2.61mmol)、sem-cl(0.385ml,2.17mmol)处理。将反应混合物在室温下搅拌2小时,然后用水处理并用etoac萃取产物。将有机相用饱和na2s2o3、盐水洗涤,经na2so4干燥,过滤并浓缩。将残余物通过biotage isolera纯化以得到所需产物。对于c
21h29
in3o2si(m+h)
+
,lc-ms计算值:m/z=510.1;实验值510.0。
[1479]
步骤2. 3-(6-氯吡啶-3-基)-5-(2,3-二甲基苯基)-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶
[1480][1481]
将5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶(0.500g,0.981mmol)、(6-氯吡啶-3-基)硼酸(0.232g,
ms计算值:m/z=587.3;实验值587.4。
[1488]
步骤5. 4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环己烷-1-甲酸
[1489]
将tfa(0.5ml,2.60mmol)添加至4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环己烷-1-羧酸(20mg,0.034mmol)于dcm(0.5ml)中的溶液中并且将反应混合物在室温下搅拌1h。在真空中浓缩之后,将残余物用水(28%)(0.5ml)和meoh(1ml)中的氢氧化铵溶液处理。将反应混合物在室温下搅拌1h。然后将反应用水和meoh稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h29
n4o3(m+h)
+
,lcms计算值:m/z=457.2;实验值457.2。
[1490]
实施例80.(3s,4r)-1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-4-氟吡咯烷-3-胺
[1491][1492]
步骤1. 5-(2,3-二甲基苯基)-3-(6-氟吡啶-3-基)-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶
[1493][1494]
将5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶(0.830g,1.629mmol)、(6-氟吡啶-3-基)硼酸(0.344g,2.444mmol)、二环己基(2’,4’,6
’‑
三异丙基联苯-2-基)膦-(2
’‑
氨基联苯-2-基)(氯)钯(0.128g,0.163mmol)和k3po4(0.69g,3.26mmol)置于具有隔膜的小瓶中。将小瓶抽真空并用n2回填三次,添加1,4-二噁烷(10ml)和水(2ml),并且将反应混合物在60℃下搅拌1h。过滤混合物。将滤液分配于水与etoac之间。分离有机相,用盐水洗涤,经na2so4干燥,过滤并浓缩。将残余物通过biotage isolera纯化以得到所需产物。对于c
26h32
fn4o2si(m+h)
+
,lc-ms计算值:m/z=479.2;实验值479.1。
[1495]
步骤2.(3s,4r)-1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-4-氟吡咯烷-3-胺
[1496]
将5-(2,3-二甲基苯基)-3-(6-氟吡啶-3-基)-6-甲氧基-1-((2-(三甲基甲硅烷基)-乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶(20mg,0.042mmol)、((3s,4r)-4-氟吡咯烷-3-基)氨基羧酸叔丁酯(8.53mg,0.042mmol)和dipea(21.89μl,0.125mmol)于dmso(0.2ml)中
的混合物在110℃下搅拌过夜。在冷却至室温之后,将混合物分配于水与etoac之间。分离有机相,用盐水洗涤,干燥并浓缩。将残余物溶解于dcm(0.5ml)中,用tfa(0.5ml,2.60mmol)处理并在室温下搅拌1h。在真空中浓缩之后,将残余物用水(28%)(0.5ml)和meoh(1ml)中的氢氧化铵溶液处理。将反应混合物在室温下搅拌1h。然后将反应用水和meoh稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
24h26
fn6o(m+h)
+
,lcms计算值:m/z=433.2;实验值433.2。1h nmr(600mhz,dmso-d6)δ9.18(s,1h),8.66(s,2h),8.53(dd,j=8.9,2.3hz,1h),7.53(s,1h),7.25
–
7.21(m,1h),7.17(t,j=7.5hz,1h),7.12(d,j=9.0hz,1h),6.80(d,j=9.0hz,1h),5.50(dt,j=53.9,3.5hz,1h),4.25
–
4.08(m,1h),4.05
–
3.98(m,1h),3.95
–
3.86(m,1h),3.85(s,3h),3.78(dd,j=13.2,3.5hz,1h),3.48(t,j=9.7hz,1h),2.32(s,3h),1.98(s,3h)ppm。
[1497]
实施例81.(2s)-1-(4-(5-(5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-基)-2-羟基丙-1-酮
[1498][1499]
步骤1. 4-溴-2,3-二氢-1h-茚-2-酚的手性分离
[1500][1501]
将可商购获得的4-溴-2,3-二氢-1h-茚-2-酚的两种对映体通过手性制备型sfc(chiraltech ig 5um 21
×
250mm,用15%etoh(含有2mm氨)洗脱,流动速率70ml/min,t
r,峰1
=3.2min,t
r,峰2
=3.9min)分离。收集峰2并且在真空中蒸发溶剂。
[1502]
步骤2. 4-溴-2-氟-2,3-二氢-1h-茚
[1503][1504]
将4-溴-2,3-二氢-1h-茚-2-酚(0.50g,2.3mmol)(来自步骤1中的手性分离的峰2)于dcm(5ml)中的溶液在干冰/丙酮浴中冷却,然后缓慢地添加dast(0.4ml,3.03mmol)。30min之后,使混合物升温至室温。将反应用冰处理并用dcm萃取产物。分离有机相,用盐水洗涤,经硫酸钠干燥并在真空中去除溶剂。将所获得的粗材料通过biotage isolera纯化。
[1505]
步骤3. 2-(2-氟-2,3-二氢-1h-茚-4-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环
[1506][1507]
将4-溴-2-氟-2,3-二氢-1h-茚(0.20g,0.930mmol)、4,4,4’,4’,5,5,5’,5
’‑
八甲基-2,2
’‑
联(1,3,2-二氧硼戊环)(0.472g,1.9mmol)、[1,1
’‑
双(二苯基膦基)-二茂铁]-二氯化钯(ii)(25mg,0.03mmol)和乙酸钾(0.5g)于二噁烷(5ml)中的混合物在80℃下搅拌过夜。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过biotage isolera纯化。
[1508]
步骤4. 5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1509][1510]
将2-(2-氟-2,3-二氢-1h-茚-4-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环(0.25g,0.95mmol)、5-氯-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(0.27g,0.954mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(25mg,33mmol)和k3po4(300mg)于二噁烷(4ml)和水(0.4ml)中的混合物在80℃下在氮气下搅拌过夜。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过biotage isolera纯化。
[1511]
将含4n hcl的二噁烷(2ml)然后添加至所需产物中并且将反应混合物在室温下搅拌2小时。将其用乙酸乙酯萃取并用nahco3溶液中和。分离有机相,用盐水洗涤,经硫酸钠干燥,过滤并在真空中去除溶剂。对于c
16h15
fn3o(m+h)
+
,lc-ms计算值:m/z=284.1;实验值284.2。
[1512]
步骤5. 5-(2-氟-2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1513][1514]
将nis(0.206g,0.918mmol)添加至5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(0.26g,0.918mmol)于dmf(5ml)中的溶液中。在60℃下搅拌2h之后,将反应混合物冷却至室温,并添加三乙胺(0.23ml,1.64mmol)和boc-酸酐(0.30g,1.37mmol)。在室温下再搅拌1h之后,添加水并通过过滤收集沉淀的产物,风干并且不经进
一步纯化即用于下一步骤中。对于c
21h22
fin3o3(m+h)
+
,lc-ms计算值:m/z=510.1;实验值510.1。
[1515]
步骤6. 5-溴-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯
[1516][1517]
将4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-3,6-二氢吡啶-1(2h)-羧酸叔丁酯(1.85g,5.98mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(250mg,0.330mmol)、k3po4(1.0g)于二噁烷(10ml)和水(2ml)中的混合物在80℃下搅拌过夜。然后将反应混合物冷却至室温,过滤,并且在真空中蒸发溶剂。将所获得的粗材料通过biotage isolera纯化两次以得到0.23g白色固体。对于c
11h11
brn2o2(m-tbu+h)
+
,lc-ms计算值:m/z=282.1,284.1;实验值282.1,284.1
[1518]
步骤7. 5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯
[1519][1520]
将4,4,4’,4’,5,5,5’,5
’‑
八甲基-2,2
’‑
联(1,3,2-二氧硼戊环)(0.275g,1.085mmol)、5-溴-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯(0.23g,0.678mmol)、乙酸钾(0.2g)和[1,1
’‑
双(二苯基膦基)二茂铁]-二氯化钯(ii)(50mg,0.06mmol)于二噁烷(3ml)中的混合物在80℃下搅拌过夜。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过biotage isolera纯化。对于c
21h32
bn2o4(m+h)
+
,lc-ms计算值:m/z=387.2;实验值387.2。
[1521]
步骤8. 3-(1
’‑
(叔丁氧基羰基)-1’,2’,3’,6
’‑
四氢-[2,4
’‑
联吡啶]-5-基)-5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1522][1523]
将5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯(0.050g,0.130mmol)、5-(2-氟-2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(0.066g,0.130mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(8mg,11μmol)和k3po4(0.050g)于二噁烷(3ml)和水(0.3ml)中的混合物在80℃下搅拌过夜。在冷却至室温之后,过滤反应混合物并在真空中蒸发溶剂。将粗材料溶解于甲醇中并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
36h41
fn5o5(m+h)
+
,lc-ms计算值:m/z=642.3,实验值642.3。
[1524]
步骤9. 5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(6-(哌嗪-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1525][1526]
将3-(1
’‑
(叔丁氧基羰基)-1’,2’,3’,6
’‑
四氢-[2,4
’‑
联吡啶]-5-基)-5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(0.010g,0.016mmol)和钯/碳(5mg,10%)于甲醇(5ml)中的混合物连接至填充有氢气的气球并且将反应混合物在室温下搅拌3小时。然后过滤反应混合物并在真空中浓缩。然后添加二噁烷中的4n hcl溶液并且将反应在室温下搅拌30min。然后将其用甲醇稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
26h27
fn5o(m+h)
+
,lc-ms计算值:m/z=444.1;实验值444.1。
[1527]
步骤10.(2s)-1-(4-(5-(5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-基)-2-羟基丙-1-酮
[1528]
将hatu(35mg,0.09mmol)添加至(s)-2-羟基丙酸(32mg,0.355mmol)、5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶(5mg,10.15μmol)和dipea(0.05ml)于dmf(1ml)中的溶液中。在室温下搅拌1h之后,将反应混合物用甲醇稀释,过滤并+用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
29h31
fn5o3(m+h)
+
,lc-ms计算值:m/z=516.3;实验值516.3。
[1529]
实施例82. 1-(4-(5-(5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-基)-2-羟基乙-1-酮
[1530][1531]
此化合物根据实施例81中所描述的程序,使用2-羟基乙酸替代(s)-2-羟基丙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h29
fn5o3(m+h)
+
,lc-ms计算值:m/z=502.2;实验值502.2。
[1532]
实施例83.(7r,8as)-2-(5-(5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1533][1534]
步骤1.(7r,8as)-2-(5-溴吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1535][1536]
将(7r,8as)-八氢吡咯并[1,2-a]吡嗪-7-醇(0.045g,0.316mmol)、5-溴-2-氟吡啶(0.056g,0.316mmol)和cs2co3(120mg,0.369mmol)于dmf(1ml)中的混合物在80℃下搅拌4h。然后在真空中蒸发溶剂并且将残余物通过biotage isolera纯化。对于c
12h17
brn3o(m+h)
+
,lc-ms计算值:m/z=298.1,300.1;实验值297.9,299.9。
[1537]
步骤2.(7r,8as)-2-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1538][1539]
将4,4,4’,4’,5,5,5’,5
’‑
八甲基-2,2
’‑
联(1,3,2-二氧硼戊环)(0.061g,0.241mmol)、(7r,8as)-2-(5-溴吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇(0.045g,0.151mmol)、乙酸钾(0.050g)和[1,1
’‑
双(二苯基膦基)二茂铁]-二氯化钯(ii)(16mg,0.02mmol)于二噁烷(2ml)中的混合物在80℃下搅拌过夜。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
18h29
bn3o3(m+h)
+
,lc-ms计算值:m/z=346.2;实验值346.2。
[1540]
步骤3.(7r,8as)-2-(5-(5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1541]
将(7r,8as)-2-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇(0.027g,0.079mmol)、5-(2-氟-2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(0.020g,0.039mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯基)[2-(2
’‑
氨基-1,1
’‑
联苯基)]钯(8mg,10μmol)和k3po4(10mg)于二噁烷(1ml)和水(0.1ml)中的混合物在80℃下搅拌过夜。在真空中浓缩混合物。在添加甲醇(1ml)和含4n hcl的二噁烷(1ml)之后,将所获得的反应混合物在室温下搅拌1h。然后将其用甲醇稀释,过滤并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
28h30
fn6o2(m+h)
+
,lc-ms计算值:m/z=501.3;实验值501.2。1h nmr(500mhz,dmso-d6)δ9.30
–
9.19(m,1h),8.52(dd,j=8.8,2.3hz,1h),7.55(s,1h),7.43
–
7.35(m,2h),7.32(t,j=7.5hz,1h),6.91(d,j=8.9hz,1h),5.49(dt,j=53.5,4.8hz,1h),4.71(dd,j=102.1,13.9hz,1h),4.47(d,j=
4.0hz,1h),4.30(dd,j=14.5,4.5hz,1h),4.18
–
4.04(m,1h),3.90(s,3h),3.85
–
3.75(m,1h),3.73
–
3.59(m,2h),3.56
–
3.11(m,6h),2.96(dd,j=25.8,17.8hz,1h),2.15
–
1.94(m,2h)ppm。
[1542]
实施例84. 5-(2-氟-2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-甲基-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1543][1544]
此化合物根据实施例83中所描述的程序,使用1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑替代(7r,8as)-2-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇作为起始材料来制备。产物作为tfa盐被分离。对于c
20h19
fn5o(m+h)
+
,lc-ms计算值:m/z=364.1;实验值364.1。1h nmr(600mhz,dmso-d6)δ8.29(s,1h),8.06(s,1h),7.49(s,1h),7.40(d,j=7.6hz,1h),7.38
–
7.34(m,1h),7.33
–
7.29(m,1h),5.62
–
5.36(m,1h),3.91(s,3h),3.89(s,3h),3.45
–
3.13(m,3h),3.01(dd,j=25.9,17.8hz,1h)ppm。
[1545]
实施例85.(7s,8ar)-2-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1546][1547]
步骤1. 5-(2,3-二甲基苯基)-3-(6-氟吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1548][1549]
将5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(200mg,0.417mmol)、2-氟-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶(186mg,0.835mmol)、xphospd g2(32.8mg,0.042mmol)和磷酸钾(354mg,1.669mmol)于二噁烷(5ml)和水(0.5ml)中的混合物加热至80℃持续2小时。此后,将溶液冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
25h26
fn4o3(m+h)
+
,lcms计算
值:m/z=449.2;实验值449.2。
[1550]
步骤2.(7s,8ar)-2-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1551]
将5-(2,3-二甲基苯基)-3-(6-氟吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(20mg,0.045mmol)、(7s,8ar)-八氢吡咯并[1,2-a]吡嗪-7-醇二盐酸盐(28.8mg,0.134mmol)和n,n-二异丙基乙胺(78μl,0.45mmol)于dmso(1ml)中的溶液在100℃下加热20小时。此后,将溶液冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物溶解于dcm(1ml)中并添加tfa(1ml)。将混合物在室温下搅拌1小时并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h31
n6o2(m+h)
+
,lcms计算值:m/z=471.2;实验值471.5。
[1552]
实施例86. 4-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-亚氨基-1λ
6-硫代吗啉1-氧化物
[1553][1554]
此化合物根据实施例85中所描述的程序,使用1-亚氨基-1λ
6-硫代吗啉1-氧化物盐酸盐替代(7s,8ar)-八氢吡咯并[1,2-a]吡嗪-7-醇二盐酸盐作为起始材料来制备。产物作为tfa盐被分离。对于c
24h27
n6o2s(m+h)
+
,lc-ms计算值:m/z=463.2;实验值463.2。1h nmr(500mhz,dmso-d6)δ9.23(d,j=2.3hz,1h),8.52(dd,j=8.9,2.3hz,1h),7.52(s,1h),7.25
–
7.14(m,3h),7.11(dd,j=7.6,1.5hz,1h),4.59(dt,j=15.1,4.1hz,2h),3.85(s,3h),3.81
–
3.72(m,2h),3.72
–
3.64(m,2h),3.60
–
3.52(m,2h),2.32(s,3h),1.98(s,3h)ppm。
[1555]
实施例87.(7r,8as)-2-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1556][1557]
步骤1. 5-(2,3-二甲基苯基)-3-(6-氟吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1558][1559]
将5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(200mg,0.417mmol)(实施例41,步骤7)、2-氟-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶(186mg,0.835mmol)、xphospd g2(32.8mg,0.042mmol)和磷酸钾(354mg,1.669mmol)于二噁烷(5ml)和水(0.5ml)中的混合物加热至80℃持续2小时。此后,将溶液冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。残余物然后通过硅胶色谱纯化以得到所需产物。对于c
25h26
fn4o3(m+h)
+
,lcms计算值:m/z=449.2;实验值449.2。
[1560]
步骤2.(7r,8as)-2-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1561]
将5-(2,3-二甲基苯基)-3-(6-氟吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(20mg,0.045mmol)、(7r,8as)-八氢吡咯并[1,2-a]吡嗪-7-醇(19.0mg,0.134mmol)和n,n-二异丙基乙胺(38.9μl,0.223mmol)于dmso(1ml)中的溶液在100℃下加热20小时。此后,将溶液冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物溶解于dcm(1ml)中并添加tfa(1ml)。将混合物在室温下搅拌1小时并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h31
n6o2(m+h)
+
,lcms计算值:m/z=471.2;实验值471.5。1h nmr(500mhz,dmso-d6,针对游离碱形式)δ9.15(d,j=2.3hz,1h),8.41(dd,j=9.1,2.4hz,1h),7.54(s,1h),7.22(d,j=7.4hz,1h),7.16(t,j=7.5hz,1h),7.11(d,j=7.5hz,1h),6.94(d,j=9.0hz,1h),4.46
–
4.35(m,1h),4.29
–
4.20(m,2h),3.83(s,3h),3.45
–
3.18(m,2h),3.00
–
2.92(m,1h),2.84(td,j=12.2,3.4hz,1h),2.47(t,j=11.1hz,1h),2.32(s,3h),2.30
–
2.14(m,2h),1.99
–
1.94(m,4h),1.69
–
1.58(m,2h)。
[1562]
实施例88.(s)-n-(1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-3-基)-2-羟基-n-甲基乙酰胺
[1563][1564]
步骤1.(s)-甲基(1-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)吡咯烷-3-基)氨基甲酸叔丁酯
[1565][1566]
此化合物根据实施例83步骤1-2中所描述的程序,使用(s)-甲基(吡咯烷-3-基)氨基甲酸叔丁酯替代(7r,8as)-八氢吡咯并[1,2-a]吡嗪-7-醇作为起始材料来制备。对于c
21h35
bn3o4(m+h)
+
,lc-ms计算值:m/z=404.3;实验值404.2。
[1567]
步骤2.(s)-1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基吡咯烷-3-胺
[1568][1569]
将5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(0.20g,0.42mmol)、(s)-甲基(1-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)吡咯烷-3-基)氨基甲酸叔丁酯(0.26g,0.81mmol)、xphospd g2(20mg,25μmol)和k3po4(0.050g,0.24mmol)于二噁烷(5ml)水(0.5ml)中的混合物在80℃下加热过夜。在冷却至室温之后,过滤反应,在真空中蒸发溶剂并且将残余物通过biotage isolera纯化。合并含有所需产物的级分并在真空中浓缩。将含4n hcl的二噁烷(2ml)添加至所获得的材料中并且将反应混合物在室温下搅拌1小时。然后将其在真空中浓缩并且不经进一步纯化直接用于下一步骤中。对于c
25h29
n6o(m+h)
+
,lc-ms计算值:m/z=429.2,实验值429.1
[1570]
步骤3.(s)-n-(1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-3-基)-2-羟基-n-甲基乙酰胺
[1571]
将hatu(100mg,0.263mmol)添加至(s)-1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基吡咯烷-3-胺(0.078g,0.18mmol)、2-羟基乙酸(0.100g,1.32mmol)和dipea(0.05ml,0.29mmol)于dmf(2ml)中的溶液中。在室温下搅拌1小时之后,将反应混合物用甲醇稀释,过滤并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h31
n6o3(m+h)
+
,lc-ms计算值:m/z=487.3,实验值487.2
[1572]
实施例89. 2-(3-(3-(6-(4-(2-羟基乙基)哌嗪-1-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2-甲基苯基)乙腈
[1573][1574]
步骤1. 2-(4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪-1-基)乙-1-醇
四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇(实施例83,步骤1-2)替代1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑作为起始材料来制备。对于c
24h30
cln6o4(m+h)
+
,lcms计算值:m/z=501.2,实验值:501.2。
[1584]
步骤2.(7r,8as)-2-(5-(6-甲氧基-5-(3-甲氧基-2-甲基苯基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1585]
将5-氯-3-(6-((7r,8as)-7-羟基六氢吡咯并[1,2-a]吡嗪-2(1h)-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(8mg,0.02mmol)、(3-甲氧基-2-甲基苯基)硼酸(5.30mg,0.032mmol)、xphospd g2(1.9mg,2.4μmol)和磷酸钾(5.1mg,0.024mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(1ml)和水(100μl)之后,将反应混合物在100℃下搅拌1小时。然后过滤反应,并且在真空中蒸发溶剂。添加dcm(1ml)和tfa(0.5ml)并且将反应混合物在室温下搅拌30min。然后将其用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h31
n6o3(m+h)
+
,lcms计算值:m/z=487.3,实验值:487.3。1h nmr(500mhz,dmso-d6)δ9.23
–
9.16(m,1h),8.51(dd,j=8.9,2.3hz,1h),7.52(s,1h),7.25(t,j=7.9hz,1h),7.03(dd,j=8.4,1.2hz,1h),6.94(d,j=9.0hz,1h),6.90(dd,j=7.6,1.1hz,1h),4.52
–
4.43(m,1h),4.35
–
4.23(m,1h),4.16
–
4.00(m,1h),3.89
–
3.83(m,6h),3.82
–
3.75(m,1h),3.73
–
3.60(m,3h),3.56
–
3.47(m,1h),3.47
–
3.40(m,2h),2.19
–
1.95(m,2h),1.92(s,3h)ppm。
[1586]
实施例91.(7r,8as)-2-(5-(5-(2,3-二氢苯并[b][1,4]二氧杂环己二烯-5-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1587][1588]
此化合物根据实施例90中所描述的程序,使用2-(2,3-二氢苯并[b][1,4]二氧杂环己二烯-5-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环替代(3-甲氧基-2-甲基苯基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
27h29
n6o4(m+h)
+
,lcms计算值:m/z=501.2;实验值:501.2。
[1589]
实施例92.(7r,8as)-2-(5-(5-(2-环丙基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1590][1591]
此化合物根据实施例90中所描述的程序,使用(2-环丙基苯基)硼酸替代(3-甲氧基-2-甲基苯基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h31
n6o2(m+h)
+
,
lcms计算值:m/z=483.2;实验值:483.3。
[1592]
实施例93.(7r,8as)-2-(5-(5-(色满-5-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1593][1594]
此化合物根据实施例90中所描述的程序,使用2-(色满-5-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环替代(3-甲氧基-2-甲基苯基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h31
n6o3(m+h)
+
,lcms计算值:m/z=499.3;实验值:499.2。
[1595]
实施例94.(7r,8as)-2-(5-(5-(2-氟-3-甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[1596][1597]
此化合物根据实施例90中所描述的程序,使用(2-氟-3-甲基苯基)硼酸替代(3-甲氧基-2-甲基苯基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
26h28
fn6o2(m+h)
+
,lcms计算值:m/z=475.2;实验值:475.2。1h nmr(500mhz,dmso-d6)δ9.25
–
9.18(m,1h),8.50(dd,j=8.9,2.3hz,1h),7.55(s,1h),7.37(t,j=7.4hz,1h),7.35
–
7.31(m,1h),7.21(t,j=7.5hz,1h),6.94(d,j=9.0hz,1h),4.47(s,1h),4.30(dd,j=14.0,4.3hz,1h),4.16
–
4.06(m,1h),3.88(s,3h),3.84
–
3.76(m,1h),3.73
–
3.60(m,3h),3.58
–
3.46(m,1h),3.46
–
3.39(m,2h),2.31(s,3h),2.17
–
1.91(m,2h)ppm。
[1598]
实施例95. 4-(6-甲氧基-3-(6-(2-甲氧基乙氧基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚
[1599][1600]
步骤1. 2-(2-甲氧基乙氧基)-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶
[1601][1602]
将5-溴-2-(2-甲氧基乙氧基)吡啶(250mg,1.08mmol)、4,4,4’,4’,5,5,5’,5
’‑
八甲基-2,2
’‑
联(1,3,2-二氧硼戊环)(356mg,1.4mmol)、[1,1
’‑
双(二苯基膦基)-二茂铁]-二氯化钯(ii)(88mg,0.11mmol)和乙酸钾(159mg,1.62mmol)于二噁烷(5ml)中的混合物在80℃下搅拌过夜。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过biotage isolera纯化。对于c
14h23
bno4(m+h)
+
,lcms计算值:m/z=280.2;实验值:280.2。
[1603]
步骤2. 4-(6-甲氧基-3-(6-(2-甲氧基乙氧基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚
[1604]
此化合物根据实施例73中所描述的程序,使用2-(2-甲氧基乙氧基)-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶替代2-((四氢呋喃-3-基)氧基)-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶作为起始材料来制备。产物作为tfa盐被分离。对于c
24h25
n4o4(m+h)
+
,lcms计算值:m/z=433.2;实验值:433.2。1h nmr(600mhz,dmso-d6)δ9.23(d,j=2.3hz,1h),8.62(dd,j=8.6,2.3hz,1h),7.55(s,1h),7.32(d,j=7.3hz,1h),7.28(d,j=6.1hz,1h),7.25(t,j=7.4hz,1h),6.97(d,j=8.7hz,1h),4.52
–
4.45(m,1h),4.45
–
4.41(m,2h),3.89(s,3h),3.71
–
3.64(m,2h),3.31(s,3h),3.16(dd,j=16.0,6.0hz,1h),3.03(dd,j=16.4,6.0hz,1h),2.84(dd,j=15.9,3.8hz,1h),2.65(dd,j=16.4,3.9hz,1h)ppm。
[1605]
实施例96. 4-(6-甲氧基-3-(6-((四氢-2h-吡喃-4-基)氧基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚
[1606][1607]
此化合物根据实施例95中所描述的程序,使用5-溴-2-((四氢-2h-吡喃-4-基)氧基)吡啶替代5-溴-2-(2-甲氧基乙氧基)吡啶作为起始材料来制备。产物作为tfa盐被分离。对于c
26h27
n4o4(m+h)
+
,lcms计算值:m/z=459.2;实验值:459.2。1h nmr(600mhz,dmso-d6)δ9.22(d,j=2.4hz,1h),8.61(dd,j=8.6,2.3hz,1h),7.55(s,1h),7.32(d,j=5.9hz,1h),7.28(d,j=6.1hz,1h),7.25(t,j=7.4hz,1h),6.94(d,j=8.6hz,1h),5.24(tt,j=8.9,4.2hz,1h),4.53
–
4.43(m,1h),3.89(s,3h),3.88
–
3.83(m,2h),3.57
–
3.45(m,2h),3.16(dd,j=16.0,6.1hz,1h),3.01(dd,j=16.4,6.0hz,1h),2.84(dd,j=15.9,3.8hz,1h),2.64(dd,j=16.4,3.8hz,1h),2.09
–
2.01(m,2h),1.75
–
1.60(m,2h)ppm。
[1608]
实施例97. 4-(3-(6-环丙基吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-2-酚
[1609][1610]
此化合物根据实施例73中所描述的程序,使用(6-环丙基吡啶-3-基)硼酸替代2-((四氢呋喃-3-基)氧基)-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶作为起始材料来制备。产物作为tfa盐被分离。对于c
24h23
n4o2(m+h)
+
,lcms计算值:m/z=399.2;实验值:399.2。1h nmr(500mhz,dmso-d6)δ9.47(d,j=2.2hz,1h),8.74(d,j=8.3hz,1h),7.59(s,1h),7.52(d,j=8.4hz,1h),7.36
–
7.31(m,1h),7.29(d,j=7.1hz,1h),7.25(t,j=7.4hz,1h),4.55
–
4.44(m,1h),3.90(s,3h),3.16(dd,j=16.0,6.0hz,1h),3.04(dd,j=16.4,5.9hz,1h),2.84(dd,j=16.1,3.8hz,1h),2.64(dd,j=16.3,3.8hz,1h),2.29
–
2.17(m,1h),1.15
–
0.94(m,4h)ppm。
[1611]
实施例98.n-(1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-3-基)-2-羟基-n-甲基乙酰胺
[1612][1613]
步骤1. 5-(2,3-二甲基苯基)-3-(6-氟吡啶-3-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1614][1615]
向5-(2,3-二甲基苯基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(实施例69,步骤1,255mg,0.511mmol)于1,4-二噁烷(5ml)和水(0.5ml)中的溶液中添加2-氟-5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶(219mg,0.940mmol)、磷酸钾(312mg,1.47mmol)和[1,1
’‑
双(二苯基膦基)二茂铁]-二氯化钯(ii)(40mg,0.049mmol)。将反应用n2脱气并在80℃下搅拌3小时。此后,将其冷却至室温并用etoac稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
28h26
fn4o2(m+h)
+
,lc-ms计算值:m/z=469.2;实验值469.2。
[1616]
步骤2.(1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-3-基)(甲基)氨基甲酸叔丁酯
[1617][1618]
向5-(2,3-二甲基苯基)-3-(6-氟吡啶-3-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(120mg,0.256mmol)于dmso(2.5ml)中的溶液中添加氮杂环丁-3-基(甲基)氨基甲酸叔丁酯(114mg,0.512mmol)和碳酸铯(417mg,1.22mmol)。将反应用n2脱气并在100℃下搅拌5小时。此后,将其冷却至室温并用etoac稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
37h43
n6o4(m+h)
+
,lc-ms计算值:m/z=635.2;实验值635.2。
[1619]
步骤3. 1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基氮杂环丁-3-胺
[1620][1621]
向(1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-3-基)(甲基)氨基甲酸叔丁酯(163mg,0.256mmol)于二氯甲烷(0.5ml)中的溶液中添加三氟乙酸(0.5ml)。将反应在室温下搅拌1小时。此后,将其用二氯甲烷稀释。所得溶液依序用水、饱和nacl水溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。残余物不经纯化直接用于下一步骤中。对于c
32h35
n6o2(m+h)
+
,lc-ms计算值:m/z=535.3;实验值535.2。
[1622]
步骤4.n-(1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-3-基)-2-羟基-n-甲基乙酰胺
[1623]
向1-(5-(5-(2,3-二甲基苯基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基氮杂环丁-3-胺(10mg,0.019mmol)于二氯甲烷(0.5ml)中的溶液中添加2-羟基乙酸(7mg,0.09mmol)、三甲胺(22mg,0.17mmol)和hatu(11mg,0.028mmol)。将反应在室温下搅拌1小时。此后,将其用二氯甲烷稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物溶解于二氯甲烷(0.5ml)和三氟甲烷磺酸(0.2ml)中。将反应在室温下搅拌。30min之后,将反应混合物用meoh稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
26h29
n6o3(m+h)
+
,lc-ms计算值:m/z=473.2;实验值473.2。1h nmr(600mhz,dmso-d6)δ13.41(s,1h),9.07(d,j=2.0hz,1h),8.66(d,j=9.2hz,1h),7.57(s,1h),7.24(dd,j=7.6,1.4hz,1h),7.18(t,j=7.5hz,1h),7.12(dd,j=7.6,1.5hz,1h),6.98(t,j=9.9hz,1h),5.30(td,j=8.1,3.8hz,1h),4.44(t,j=
9.0hz,2h),4.35
–
4.29(m,2h),4.17(s,1h),4.12(s,1h),3.86(s,3h),2.99(s,3h),2.32(s,3h),1.98(s,3h)ppm。
[1624]
实施例99. 1-(4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-基)乙-1-酮
[1625][1626]
步骤1. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1627][1628]
将5-氯-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(6.4g,22.5mmol)、2-(2,3-二氢-1h-茚-4-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环(6.0g,24.7mmol)、氯(2-二环己基膦基-2’,4’,6
’‑
三-异丙基-1,1
’‑
联苯基)(2
’‑
氨基-1,1
’‑
联苯-2-基)钯(ii)(0.89g,1.124mmol)和cs2co3(14.65g,45.0mmol)置于250ml圆底烧瓶中并且将烧瓶抽真空并用n2回填三次。将二噁烷(80ml)和水(20ml)添加至混合物中并且将反应混合物在70℃下搅拌过夜。在冷却至室温之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过biotage isolera纯化以得到白色固体(7.20g,88%)。对于c
21h24
n3o3(m+h)
+
,lcms计算值:m/z=366.2;实验值366.2。
[1629]
步骤2. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1630][1631]
将dcm(30ml)和tfa(15.0ml)的混合物中的5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(7.20g,19.7mmol)在室温下搅拌1h。然后将反应在真空中浓缩,将残余物溶解于dcm中并用nahco3溶液中和。分离有机相,经硫酸钠干燥并在真空中浓缩。所获得的粗材料不经进一步纯化即用于下一步骤。对于c
16h16
n3o(m+h)
+
,lcms计算值:m/z=266.1;实验值266.1。
[1632]
步骤3. 5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑
并[4,3-b]吡啶
[1633][1634]
将1-碘吡咯烷-2,5-二酮(6.11g,27.1mmol)添加至5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(6.00g,22.61mmol)于dmf(60ml)中的溶液中。在60℃下搅拌1h之后,将混合物冷却至室温,随后添加碳酸铯(14.74g,45.2mmol)和1-(氯甲基)-4-甲氧基苯(3.66ml,27.1mmol)。将反应混合物在80℃下搅拌1h。将反应混合物冷却至室温,添加水,并用etoac萃取产物。分离有机相,用盐水洗涤,经na2so4干燥并在真空中浓缩。将残余物通过biotage isolera纯化以得到黄色固体。对于c
24h23
in3o2(m+h)
+
,lcms计算值:m/z 512.2;实验值512.2。
[1635]
步骤4. 3-(6-氯吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1636][1637]
将5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(6.0g,11.73mmol)、(6-氯吡啶-3-基)硼酸(2.2g,14.08mmol)、pdcl2(dppf)-ch2cl2加合物(0.96g,1.173mmol)和磷酸钾(3.24g,15.25mmol)置于250ml圆底烧瓶中并且将烧瓶抽真空并用n2回填三次。将二噁烷(80ml)和水(20ml)转移至烧瓶中,并且将反应混合物在70℃下搅拌2h。在冷却至室温之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过biotage isolera纯化以得到黄色固体(5.0g,86%)。对于c
29h26
cln4o2(m+h)
+
,lcms计算值:m/z=497.2,实验值497.2。
[1638]
步骤5. 5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯
[1639][1640]
将3-(6-氯吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄
基)-1h-吡唑并[4,3-b]吡啶(3.75g,7.55mmol)、xphos pd g2(0.6g,0.76mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-3,6-二氢吡啶-1(2h)-羧酸叔丁酯(3.03g,9.81mmol)和cs2co3(4.92g,15.09mmol)置于具有隔膜的250ml圆底烧瓶中。在将烧瓶抽真空并用n2回填三次之后,将二噁烷(80ml)和水(20ml)转移至烧瓶中。将反应混合物在70℃下搅拌2h。在冷却至室温之后,添加水并用etoac萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中蒸发溶剂。将粗材料通过biotage isolera纯化以得到油状物(4.0g,82%)。对于c
39h42
n5o4(m+h)
+
,lcms计算值:m/z=644.2;实验值644.2。
[1641]
步骤6. 4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-羧酸叔丁酯
[1642][1643]
将5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯(0.80g,1.2mmol)和pd-c(0.132g,0.124mmol)于meoh(10ml)和乙酸乙酯(10ml)中的混合物在帕尔震荡器(parr-shaker)中在30psi h2下搅拌过夜。然后过滤反应混合物,并且在真空中浓缩滤液以得到呈无色油状的所需产物(0.80g,99%)。对于c
39h44
n5o4(m+h)
+
,lcms计算值:m/z=646.2;实验值646.2。
[1644]
步骤7. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1645][1646]
将hcl于二噁烷(10ml)中的4n溶液添加至4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-羧酸叔丁酯(0.80g,1.24mmol)于etoac(5ml)和甲醇(5ml)的混合物中的溶液中。将反应混合物在室温下搅拌1小时,然后在真空中浓缩至干以得到作为hcl盐的产物(0.80g,》98%)。对于c
34h36
n5o2(m+h)
+
,lcms计算值:m/z=546.2;实验值546.2。
[1647]
步骤8. 1-(4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-基)乙-1-酮
[1648]
将5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶(0.80g,1.466mmol)和三乙胺(0.511ml,3.67mmol)于
dcm(5ml)中的溶液冷却至0℃并通过注射器逐滴添加乙酰氯(2.2ml,2.2mmol)。将反应混合物在室温下搅拌1h,然后用水淬灭。用dcm萃取所需产物。将有机相用盐水洗涤,经na2so4干燥并在真空中去除溶剂。
[1649]
将残余物溶解于dcm(2ml)中,并添加三氟甲烷磺酸(0.66g,4.4mmol)。将反应混合物在室温下搅拌1h。然后,将混合物用饱和nahco3溶液中和并用dcm萃取产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中浓缩。将混合物用ch3cn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
28h30
n5o2(m+h)
+
,lcms计算值:m/z=468.2;实验值:468.2。1h nmr(500mhz,dmso-d6)δ13.49(s,1h),9.56(d,j=2.1hz,1h),8.80(d,j=8.3hz,1h),7.65(d,j=8.3hz,1h),7.59(s,1h),7.30(t,j=7.3hz,2h),7.24(t,j=7.4hz,1h),4.55(d,j=13.2hz,1h),4.53(d,j=13.2hz,1h),3.89(s,3h),3.17(td,j=13.1,2.7hz,1h),3.12(m,1h),2.96(t,j=7.4hz,2h),2.80(t,j=7.4hz,2h),2.65(td,j=12.8,2.8hz,1h),2.04(s,3h),2.02
–
1.86(m,4h),1.74(qd,j=12.6,4.2hz,1h),1.59(qd,j=12.6,4.3hz,1h)ppm。
[1650]
实施例100. 1-(4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-基)-2-羟基乙-1-酮
[1651][1652]
将5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶(1.0g,1.83mmol)(来自实施例99,步骤7)、2-羟基乙酸(0.14g,1.8mmol)、hatu(1.22g,2.75mmol)和dipea(0.960ml,5.50mmol)于dmf(10ml)中的溶液在室温下搅拌2h。然后添加水并用dcm萃取产物。将有机相用盐水洗涤并且经na2so4干燥。在真空中浓缩溶液。
[1653]
将残余物溶解于dcm(2ml)中,并且添加三氟甲烷磺酸(0.660g,4.40mmol)。将反应混合物在室温下搅拌1h。然后,将混合物用饱和nahco3溶液中和,并且用dcm萃取所需产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中浓缩。将残余物再溶解于ch3cn中并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
28h30
n5o3(m+h)
+
,lcms计算值:m/z=484.2;实验值:484.2。1h nmr(500mhz,dmso-d6)δ13.49(s,1h),9.56(d,j=2.1hz,1h),8.82(dd,j=8.1,2.1hz,1h),7.63(d,j=8.3hz,1h),7.59(s,1h),7.30(t,j=7.3hz,2h),7.24(t,j=7.4hz,1h),4.51(d,j=13.1hz,1h),4.14(t,j=7.4hz,2h),4.05(s,3h),3.90(t,j=7.4hz,1h),3.15
–
2.80(m,4h),2.96(t,j=7.4hz,1h),2.83
–
2.71(m,3h),2.03
–
1.90(m,4h),1.80
–
1.69(m,1h),1.69
–
1.58(m,1h)ppm。
[1654]
实施例101. 1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)-2-羟基乙-1-酮(峰1)
[1655][1656]
步骤1. 3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-2,5-二氢-1h-吡咯-1-羧酸叔丁酯
[1657][1658]
此化合物根据实施例99步骤5中所描述的程序,使用3-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,5-二氢-1h-吡咯-1-羧酸叔丁酯替代4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-3,6-二氢吡啶-1(2h)-羧酸叔丁酯来制备。对于c
38h40
n5o4(m+h)
+
,lc-ms计算值:m/z=630.3;实验值630.2。
[1659]
步骤2. 3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-羧酸叔丁酯(峰1和峰2)
[1660][1661]
此化合物的外消旋混合物根据实施例99步骤6中所描述的程序,使用3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-2,5-二氢-1h-吡咯-1-羧酸叔丁酯替代5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯作为起始材料来制备。对于c
38h42
n5o4(m+h)
+
,lc-ms计算值:m/z=632.3;实验值632.2。
[1662]
将两种对映体用手性制备型sfc(phenomenex cellulose-5 5um 21.2
×
250mm,用15%meoh/co2洗脱,流动速率90ml/min,t
r,峰1
=4.9min,t
r,峰2
=5.6min)分离。收集峰1和峰2并且在真空中蒸发溶剂。对于c
38h42
n5o4(m+h)
+
,lcms计算值:m/z=632.3;实验值:632.2。
[1663]
步骤3. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(吡咯
烷-3-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶(峰1和峰2)
[1664][1665]
这些化合物根据实施例99步骤7中所描述的程序,使用3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-羧酸叔丁酯替代4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-羧酸叔丁酯来制备。对于c
33h34
n5o2(m+h)
+
,lc-ms计算值:m/z=532.3;实验值532.2。
[1666]
步骤4. 1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)-2-羟基乙-1-酮(峰1)
[1667]
此化合物根据实施例100中所描述的程序,使用5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(吡咯烷-3-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶(峰1)替代5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶作为起始材料来制备。对于c
27h28
n5o3(m+h)
+
,lc-ms计算值:m/z=470.2;实验值470.2。1h nmr(500mhz,dmso-d6)δ13.43(s,1h),9.56(d,j=2.1hz,1h),8.73(td,j=8.1,7.5,2.2hz,1h),7.57(d,j=15.1hz,2h),7.30(t,j=7.0hz,2h),7.24(t,j=7.4hz,1h),4.10
–
3.98(m,2h),3.90(s,3h),3.90
–
3.81(m,1h),3.73
–
3.60(m,3h),3.51
–
3.36(m,1h),2.96(t,j=7.4hz,2h),2.80(t,j=7.4hz,2h),2.40
–
2.13(m,2h),1.98(p,j=7.4hz,2h)ppm。
[1668]
实施例102. 1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)-2-羟基乙-1-酮(峰2)
[1669][1670]
此化合物根据实施例100中所描述的程序,使用5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(吡咯烷-3-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶(峰2)替代5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶来制备。对于c
27h28
n5o3(m+h)
+
,lc-ms计算值:m/z=470.2;实验值470.2。
[1671]
实施例103. 1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]
吡啶-3-基)吡啶-2-基)吡咯烷-1-基)乙-1-酮(峰1)
[1672][1673]
此化合物根据实施例99步骤8中所描述的程序,使用5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(吡咯烷-3-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶(峰1)替代5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶来制备。对于c
27h28
n5o2(m+h)
+
,lc-ms计算值:m/z=454.2;实验值454.2。
[1674]
实施例104. 1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)乙-1-酮(峰2)
[1675][1676]
此化合物根据实施例99步骤8中所描述的程序,使用5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(吡咯烷-3-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶(峰2)替代5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶来制备。对于c
27h28
n5o2(m+h)
+
,lc-ms计算值:m/z=454.2;实验值454.2。1h nmr(500mhz,dmso-d6)δ13.45(s,1h),9.57(t,j=2.1hz,1h),8.76(ddd,j=10.2,8.1,2.2hz,1h),7.62
–
7.56(m,2h),7.30(t,j=7.1hz,2h),7.24(t,j=7.4hz,1h),3.95
–
3.83(m,4h),3.74
–
3.50(m,3h),3.46(dd,j=11.5,8.3hz,1h),3.34(ddd,j=11.6,9.3,7.0hz,1h),2.96(d,j=14.7hz,2h),2.80(t,j=7.3hz,2h),2.38
–
2.15(m,2h),2.14
–
1.94(m,4h)ppm。
[1677]
实施例105. 3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-[1,3
’‑
联吡咯烷]-2
’‑
酮(峰1)
[1678][1679]
将5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-3-(6-(吡咯烷-3-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶(峰1)(15mg,0.028mmol)、3-溴吡咯烷-2-酮(7mg,0.042mmol)和碳酸铯(18mg,0.056mmol)于1,4-二噁烷(1ml)和dmf(0.2ml)中的混合物在70℃下搅拌2h。将混合物冷却至室温,用nahco3溶液淬灭,并且用dcm萃取产物。将有机相用盐水洗涤并且经na2so4干燥。在真空中浓缩该溶液。
[1680]
将残余物溶解于dcm(0.5ml)中,并且添加三氟甲烷磺酸(00.16g,1.0mmol)。将反应混合物在室温下搅拌1h。然后将混合物用饱和nahco3溶液中和并用dcm萃取产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中浓缩。将混合物用ch3cn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
29h31
n6o2(m+h)
+
,lcms计算值:m/z=495.2;实验值:495.2。
[1681]
实施例106. 3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1
’‑
甲基-[1,3
’‑
联吡咯烷]-2
’‑
酮(峰1)
[1682][1683]
此化合物根据实施例105中所描述的程序,使用3-溴-1-甲基吡咯烷-2-酮替代3-溴吡咯烷-2-酮来制备。对于c
30h33
n6o2(m+h)
+
,lc-ms计算值:m/z=509.3;实验值509.2。
[1684]
实施例107. 2-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)丙酰胺(峰1)
[1685][1686]
此化合物根据实施例105中所描述的程序,使用2-溴-丙酰胺替代3-溴吡咯烷-2-酮来制备。对于c
28h31
n6o2(m+h)
+
,lc-ms计算值:m/z=483.2;实验值483.2。
[1687]
实施例108. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(6-(1-(甲基-l-脯氨酰基)哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[1688][1689]
此化合物根据实施例100中所描述的程序,使用甲基-l-脯氨酸替代2-羟基乙酸来制备。对于c
32h37
n6o2(m+h)
+
,lc-ms计算值:m/z=537.3;实验值537.3。
[1690]
实施例109.(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)吡咯烷-1-基)((r)-4-甲基吗啉-3-基)甲酮(峰2)
[1691][1692]
此化合物根据实施例102中所描述的程序,使用(r)-4-甲基吗啉-3-甲酸替代2-羟基乙酸来制备。对于c
31h35
n6o3(m+h)
+
,lc-ms计算值:m/z=539.3;实验值539.3。
[1693]
实施例110. 4-(6-甲氧基-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1694][1695]
步骤1. 4-(3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1696]
[1697]
将nis(2.01g,8.96mmol)添加至4-(6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(2.6g,8.96mmol)于dmf(60ml)中的溶液中。在60℃下搅拌2h之后,将反应混合物冷却至室温,并且添加diea(3.13ml,17.91mmol)和sem-cl(2.4ml,13.43mmol)。在室温下再搅拌12h之后,添加水并用etoac萃取产物。将合并的有机相用饱和nacl溶液洗涤,经na2so4干燥,过滤,浓缩至干并通过快速柱色谱纯化以得到所需产物。对于c
23h28
in4o2si(m+h)
+
,lc-ms计算值:m/z=547.1;实验值547.1。
[1698]
步骤2. 4-(6-甲氧基-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1699]
将4-(3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(50mg,0.091mmol)、1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪(42mg,0.137mmol)、pdcl2(dppf)-ch2cl2加合物(8mg,9.68μmol)和na2co3(20mg,0.183mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(1ml)和水(100μl)之后,将反应混合物在80℃下搅拌1h。然后过滤反应,并且在真空中蒸发溶剂。添加dcm(1ml)和tfa(0.5ml)并且将反应混合物在室温下搅拌30min。然后浓缩反应并且添加1ml meoh和氢氧化铵溶液,将混合物搅拌10min并且然后用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h28
n7o(m+h)
+
,lc-ms计算值:m/z=466.2;实验值466.2。
[1700]
实施例111. 4-(3-(1-(3-氰基环丁基)-1h-吡唑-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1701][1702]
此化合物根据实施例110中所描述的程序,使用3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)环丁烷-1-甲腈替代步骤2中的1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪来制备。产物作为tfa盐被分离。对于c
25h22
n7o(m+h)
+
,lcms计算值:m/z=436.2;实验值:436.2。
[1703]
实施例112. 4-(3-(1-(1-乙酰基哌啶-4-基)-1h-吡唑-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1704]
1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(50mg,0.094mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)环己-3-烯-1-醇(32mg,0.141mmol)、xphos-pdg2(8mg,9.40μmol)和k3po4(40mg,0.188mmol)置于具有隔膜的小瓶中。将小瓶抽真空并用n2回填三次,添加1,4-二噁烷(1ml)和水(0.2ml),并且将反应混合物在100℃下搅拌1h。过滤混合物。将滤液分配于水与etoac之间。分离有机相,用盐水洗涤,经na2so4干燥,过滤并浓缩。将残余物通过biotage isolera纯化以得到所需产物。对于c
34h40
n5o3si(m+h)
+
,lc-ms计算值:m/z=594.3;实验值594.3。
[1714]
步骤3. 4-(3-(6-(4-羟基环己基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1715]
将4-(3-(6-(4-羟基环己-1-烯-1-基)吡啶-3-基)-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(35mg,0.059mmol)和钯/碳(6mg,10%)于甲醇(5ml)中的混合物连接至填充有氢气的气球并且将反应混合物在室温下搅拌3小时。然后过滤反应混合物并在真空中浓缩。然后添加二噁烷中的4n hcl溶液并且将反应在室温下搅拌30min。然后将其用甲醇稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
28h28
n5o2(m+h)
+
,lc-ms计算值:m/z=466.2,实验值466.2。
[1716]
实施例114. 4-(3-(6-(4-(2-羟基乙基)哌嗪-1-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1717][1718]
此化合物根据实施例110中所描述的程序,使用2-(4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪-1-基)乙-1-醇替代步骤2中的1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪来制备。产物作为tfa盐被分离。对于c
28h30
n7o2(m+h)
+
,lcms计算值:m/z=496.2;实验值:496.2。1h nmr(500mhz,dmso-d6)δ13.2(1h,s),9.22(d,j=1.6hz,1h),8.52(dd,j=8.9,1.9hz,1h),7.56(s,1h),7.49(d,j=7.6hz,2h),7.41(t,j=7.5hz,1h),7.11(d,j=8.9hz,1h),4.57(t,j=8.0hz,1h),4.44(d,j=13.6hz,2h),3.90(s,3h),3.81
–
3.75(m,2h),3.60(d,j=11.6hz,2h),3.31(m,4h),3.17
–
3.12(m,2h),2.90(m,2h),2.56(m,1h),2.21(m,1h)ppm。
[1719]
实施例115. 4-(3-(6-(1-(2-羟基乙酰基)哌啶-4-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1720][1721]
步骤1. 5-(5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-3-基)-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯
[1722][1723]
将4-(3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(600mg,1.098mmol)、5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯(467mg,1.208mmol)、pdcl2(dppf)-ch2cl2加合物(90mg,0.110mmol)和k3po4(466mg,2.2mmol)于1,4-二噁烷(6ml)和水(0.6ml)中的混合物在80℃下搅拌过夜。在冷却至室温之后,过滤反应混合物并在真空中蒸发溶剂。将粗材料溶解于甲醇中并通过biotage isolera纯化以得到所需产物。对于c
38h47
n6o4si(m+h)
+
,lc-ms计算值:m/z=679.3;实验值679.3。
[1724]
步骤2. 4-(6-甲氧基-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1725][1726]
将5-(5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-3-基)-3’,6
’‑
二氢-[2,4
’‑
联吡啶]-1’(2’h)-羧酸叔丁酯(150mg,0.221mmol)和钯/碳(23mg,10%)于甲醇(5ml)中的混合物连接至填充有氢气的气球并且将反应混合物在室温下搅拌3小时。然后过滤反应混合物并在真空中浓缩。然后添加二噁烷中的4n hcl溶液并且将反应在室温下搅拌30min。然后将其用甲醇稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
27h27
n6o(m+h)
+
,lc-ms计算值:m/z=451.2,实验值451.2。
[1727]
步骤3. 4-(3-(6-(1-(2-羟基乙酰基)哌啶-4-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1728]
将hatu(63mg,0.166mmol)添加至2-羟基乙酸(13mg,0.166mmol)、4-(6-甲氧基-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(50mg,0.111mmol)和diea(39μl,0.222mmol)于dmf(1ml)中的溶液中。在室温下搅拌1h之后,将反应混合物用甲醇稀释,过滤并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
29h29
n6o3(m+h)
+
,lc-ms计算值:m/z=509.2,实验值509.3。1h nmr(500mhz,dmso-d6)δ13.5(s,1h),9.53(s,1h),8.76(d,j=7.9hz,1h),7.62(s,1h),7.57(d,j=8.0hz,1h),7.50(d,j=7.6hz,2h),7.41(t,j=7.5hz,1h),4.57(t,j=8.0hz,1h),4.51(d,j=11.9hz,1h),4.13(q,j=14.8hz,2h),3.91(s,3h),3.82(d,j=12.6hz,1h),3.13
–
3.03(m,2h),2.93(m,2h),2.75(t,j=12.4hz,1h),2.56(m,1h),2.22(dd,j=12.5,8.2hz,1h),1.93(d,j=12.3hz,2h),1.62(m,2h)ppm。
[1729]
实施例116. 1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-2-羟基乙-1-酮
[1730][1731]
步骤1. 3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[1732][1733]
此化合物根据实施例129中所描述的程序,使用3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸叔丁酯替代(s)-3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)吡咯烷-1-羧酸叔丁酯作为起始材料来制备。对于c
22h23
n6o(m+h)
+
,lc-ms计算值:m/z=387.2;实验值387.2。
[1734]
步骤2. 1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-2-羟基乙-1-酮
[1735]
将3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(10mg,0.026mmol)、2-羟基乙酸(2mg,0.026mmol)、bop试剂(17mg,0.04mmol)和dipea(14μl,0.078mmol)于dmf(0.4ml)中的溶液在室温下搅拌1小时。然后向混合物中添加0.1ml 1n naoh溶液。将反应混合物在40℃下搅拌1h。然后将反应混合物用meoh稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,
流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
24h25
n6o3(m+h)
+
,lc-ms计算值:m/z=445.2;实验值445.1。1h nmr(500mhz,dmso-d6)δ8.47(d,j=1.8hz,1h),8.22(d,j=1.8hz,1h),7.48(d,j=1.9hz,1h),7.28(t,j=7.7hz,2h),7.25
–
7.19(m,1h),5.44(ddd,j=12.7,7.7,4.9hz,1h),4.65(t,j=8.8hz,1h),4.51(dd,j=9.7,5.3hz,1h),4.36(t,j=9.2hz,1h),4.20(dd,j=10.3,5.3hz,1h),3.97(d,j=1.8hz,2h),3.87(d,j=1.8hz,3h),2.95(t,j=7.5hz,2h),2.80(t,j=7.4hz,2h),1.98(p,j=7.3hz,2h)ppm。
[1736]
实施例117. 1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-3-(二甲基氨基)丙-1-酮
[1737][1738]
此化合物根据实施例116中所描述的程序,使用3-(二甲基氨基)丙酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
27h32
n7o2(m+h)
+
,lc-ms计算值:m/z=486.2;实验值486.3。
[1739]
实施例118.(s)-1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-2-(二甲基氨基)丙-1-酮
[1740][1741]
此化合物根据实施例116中所描述的程序,使用二甲基-l-丙胺酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
27h32
n7o2(m+h)
+
,lc-ms计算值:m/z=486.2;实验值486.3。1h nmr(500mhz,dmso-d6)δ9.81(s,1h),8.52(dd,j=8.3,1.8hz,1h),8.25(d,j=1.8hz,1h),7.49(d,j=1.9hz,1h),7.28(dd,j=12.5,7.4hz,2h),7.22(t,j=7.4hz,1h),5.48(m,1h),4.80(t,j=8.9hz,1h),4.74
–
4.63(m,1h),4.58
–
4.41(m,1h),4.29(m,1h),4.13(q,j=6.8hz,1h),3.87(d,j=1.7hz,3h),2.95(t,j=7.4hz,2h),2.80(d,j=4.0hz,6h),1.98(p,j=7.4hz,2h),1.44(dd,j=7.0,1.8hz,3h)ppm。
[1742]
实施例119.(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(1-甲基氮杂环丁-2-基)甲酮
[1743]
[1744]
此化合物根据实施例116中所描述的程序,使用(s)-1-甲基氮杂环丁烷-2-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
27h30
n7o2(m+h)
+
,lc-ms计算值:m/z=484.2;实验值484.2。
[1745]
实施例120. 1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-2-(4-甲基哌嗪-1-基)乙-1-酮
[1746][1747]
此化合物根据实施例116中所描述的程序,使用2-(4-甲基哌嗪-1-基)乙酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
29h35
n8o2(m+h)
+
,lc-ms计算值:m/z=527.3;实验值527.3。
[1748]
实施例121. 1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-2-(4-羟基哌啶-1-基)乙-1-酮
[1749][1750]
此化合物根据实施例116中所描述的程序,使用2-(4-羟基哌嗪-1-基)乙酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
27h34
n7o3(m+h)
+
,lc-ms计算值:m/z=528.3;实验值528.2。
[1751]
实施例122.(r)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(1-甲基氮杂环丁-2-基)甲酮
[1752][1753]
此化合物根据实施例116中所描述的程序,使用(r)-1-甲基氮杂环丁烷-2-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
27h30
n7o2(m+h)
+
,lc-ms计算值:m/z=484.2;实验值484.2。
[1754]
实施例123.(r)-1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,
3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-2-羟基丙-1-酮
[1755][1756]
此化合物根据实施例116中所描述的程序,使用(r)-2-羟基丙酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
25h27
n6o3(m+h)
+
,lc-ms计算值:m/z=459.2;实验值459.2 1
h nmr(500mhz,dmso-d6)δ8.47(s,1h),8.22(d,j=1.6hz,1h),7.48(d,j=1.7hz,1h),7.28(t,j=7.9hz,2h),7.22(t,j=7.1hz,1h),5.43(m,1h),4.72(m,1h),4.62
–
4.53(m,1h),4.33(dt,j=17.0,9.2hz,1h),4.23
–
4.12(m,2h),3.87(d,j=1.7hz,3h),2.95(t,j=7.4hz,2h),2.80(t,j=7.4hz,2h),1.98(p,j=7.3hz,2h),1.21(dd,j=6.7,1.7hz,3h)。
[1757]
实施例124.(s)-1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-2-羟基丙-1-酮
[1758][1759]
此化合物根据实施例116中所描述的程序,使用(s)-2-羟基丙酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
25h27
n6o3(m+h)
+
,lc-ms计算值:m/z=459.2;实验值459.2
[1760]
实施例125.(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)((反)-3-羟基环丁基)甲酮
[1761][1762]
此化合物根据实施例116中所描述的程序,使用(反)-3-羟基环丁烷-1-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
27h28
n6o3(m+h)
+
,lc-ms计算值:m/z=485.2;实验值485.2
[1763]
实施例126.(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)((顺)-3-羟基环丁基)甲酮
[1764][1765]
此化合物根据实施例116中所描述的程序,使用(顺)-3-羟基环丁烷-1-羧酸替代2-羟基乙酸作为起始材料来制备。对于c
27h29
n6o3(m+h)
+
,lc-ms计算值:m/z=485.2;实验值485.2。1h nmr(600mhz,dmso-d6)δ8.47(s,1h),8.21(s,1h),7.48(s,1h),7.28(t,j=8.2hz,2h),7.22(t,j=7.4hz,1h),5.41(m,1h),4.52(t,j=8.5hz,1h),4.38(dd,j=9.1,5.3hz,1h),4.29(dd,j=9.9,8.2hz,1h),4.14(dd,j=10.1,5.3hz,1h),3.95(m,1h),3.87(s,3h),2.95(t,j=7.4hz,2h),2.80(t,j=7.4hz,2h),2.56
–
2.46(m,1h),2.31(m,2h),2.02
–
1.90(m,4h)。
[1766]
实施例127.(r)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(4-甲基吗啉-3-基)甲酮
[1767][1768]
此化合物根据实施例116中所描述的程序,使用(r)-4-甲基吗啉-3-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h32
n7o3(m+h)
+
,lc-ms计算值:m/z=514.2;实验值514.2
[1769]
实施例128.(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(4-甲基吗啉-3-基)甲酮
[1770][1771]
此化合物根据实施例116中所描述的程序,使用(s)-4-甲基吗啉-3-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h32
n7o3(m+h)
+
,lc-ms计算值:m/z=514.2;实验值514.2
[1772]
实施例129.(s)-1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)-2-羟基乙-1-酮
[1773][1774]
步骤1.5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶
[1775][1776]
向5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(2.20g,8.29mmol)于dmf(26ml)中的溶液中添加n-碘代琥珀酰亚胺(2.80g,12.44mmol),并且将反应混合物在60℃下搅拌1h。在用冰浴冷却之后,向反应混合物中相继添加dipea(1.7ml,9.95mmol)、sem-cl(1.62ml,9.12mmol)。将反应混合物在室温下搅拌2h。然后将其用水淬灭,并用etoac萃取所需产物。将有机相用饱和na2s2o3溶液洗涤,经na2so4干燥,在真空中浓缩,并且将残余物通过biotage isolera纯化。纯化得到呈油状物的所需产物。对于c
22h29
in3o2si(m+h)
+
,lc-ms计算值:m/z=522.1;实验值522.1。
[1777]
步骤2.(s)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1778][1779]
将5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶(440mg,0.844mmol)、(s)-3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)吡咯烷-1-羧酸叔丁酯(400mg,1.1mmol)、二环己基(2’,4’,6
’‑
三异丙基联苯-2-基)膦-(2
’‑
氨基联苯-2-基)(氯)钯(1:1)(66mg,0.084mmol)和k3po4(358mg,1.688mmol)置于具有隔膜的小瓶中。在3次真空/n2之后,添加1,4-二噁烷(6ml)和水(1ml),并且将反应混合物在60℃下搅拌1h。然后将其冷却至室温并用etoac/水稀释。将有机相用盐水洗涤,经na2so4干燥,在真空中浓缩,并且将残余物通过biotage isolera纯化。
[1780]
将tfa(5ml)和dcm(5ml)添加至所获得的材料中并且将反应在室温下搅拌1h。然后将其在真空中浓缩并再溶解于meoh(5ml)中。添加浓氨水溶液(1ml)并且将反应在室温下搅
拌1h。然后添加水,并且用dcm萃取产物。将有机相用盐水洗涤,经na2so4干燥并浓缩以得到所需产物。对于c
23h25
n6o(m+h)
+
,lc-ms计算值:m/z=401.2;实验值401.2。
[1781]
步骤3.(s)-1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)-2-羟基乙-1-酮
[1782]
此化合物根据实施例116中所描述的程序,使用(s)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶替代3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶作为起始材料来制备。产物作为tfa被分离。对于c
25h27
n6o3(m+h)
+
,lc-ms计算值:m/z=459.2;实验值459.2。1h nmr(500mhz,dmso-d6)δ8.41(m,1h),8.14(m,1h),7.48(d,j=1.9hz,1h),7.29(d,j=7.4hz,2h),7.26
–
7.19(m,1h),5.18-5.12(m,1h),4.04(s,1h),4.00(s,1h),3.90(t,j=5.6hz,2h),3.87(s,3h),3.78-3.61(m,2h),3.57
–
3.52(m,1h),3.52
–
3.46(m,1h),2.95(t,j=7.4hz,2h),2.81(t,j=7.4hz,2h),2.46
–
2.24(m,2h),1.98(p,j=7.4hz,2h)。
[1783]
实施例130.(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(四氢呋喃-2-基)甲酮
[1784][1785]
此化合物根据实施例116中所描述的程序,使用(s)-四氢呋喃-2-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
27h29
n6o3(m+h)
+
,lc-ms计算值:m/z=485.2;实验值485.4
[1786]
实施例131.(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(四氢呋喃-3-基)甲酮
[1787][1788]
此化合物根据实施例116中所描述的程序,使用(s)-四氢呋喃-3-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
27h29
n6o3(m+h)
+
,lc-ms计算值:m/z=485.2;实验值485.4
[1789]
实施例132.(r)-1-((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)-2-羟基丙-1-酮
[1790][1791]
此化合物根据实施例129中所描述的程序,使用(r)-2-羟基丙酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
26h29
n6o3(m+h)
+
,lc-ms计算值:m/z=473.2;实验值473.2
[1792]
实施例133.(s)-1-((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)-2-羟基丙-1-酮
[1793][1794]
此化合物根据实施例129中所描述的程序,使用(s)-2-羟基丙酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
26h29
n6o3(m+h)
+
,lc-ms计算值:m/z=473.2;实验值473.2
[1795]
实施例134.(r)-1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-3-羟基丁-1-酮
[1796][1797]
此化合物根据实施例116中所描述的程序,使用(r)-3-羟基丁酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
26h29
n6o3(m+h)
+
,lc-ms计算值:m/z=473.2;实验值473.2
[1798]
实施例135.(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)((1r,3r)-3-羟基-3-甲基环丁基)甲酮
[1799]
[1800]
此化合物根据实施例116中所描述的程序,使用(1r,3r)-3-羟基-3-甲基环丁烷-1-羧酸作为起始材料来制备。对于c
28h31
n6o3(m+h)
+
,lc-ms计算值:m/z=499.2;实验值499.2
[1801]
实施例136.(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)((1s,3s)-3-羟基-3-甲基环丁基)甲酮
[1802][1803]
此化合物根据实施例116中所描述的程序,使用(1s,3s)-3-羟基-3-甲基环丁烷-1-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h31
n6o3(m+h)
+
,lc-ms计算值:m/z=499.2;实验值499.2。1h nmr(600mhz,dmso-d6)δ8.47(s,1h),8.22(s,1h),7.48(s,1h),7.28(t,j=7.5hz,2h),7.22(t,j=7.4hz,1h),5.41(m,1h),4.52(t,j=8.6hz,1h),4.39(dd,j=9.1,5.2hz,1h),4.30(dd,j=10.0,8.1hz,1h),4.14(dd,j=10.1,5.3hz,1h),3.87(s,3h),2.95(t,j=7.4hz,2h),2.80(t,j=7.3hz,2h),2.67
–
2.58(m,1h),2.15(m,2h),2.04(m,2h),1.98(p,j=7.4hz,2h),1.25(s,3h)。
[1804]
实施例137.((r)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)((s)-4-甲基吗啉-3-基)甲酮
[1805][1806]
步骤1.(r)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶
[1807][1808]
此化合物根据实施例129(步骤2)中所描述的程序,使用(r)-3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)吡咯烷-1-羧酸酯替代(s)-3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)吡咯烷-1-羧酸酯作为起始材料来制备。对于c
23h25
n6o(m+h)
+
,lc-ms计算值:m/z=401.2;实验值401.2
[1809]
步骤2.((r)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡
啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)((s)-4-甲基吗啉-3-基)甲酮
[1810]
此化合物根据实施例116中所描述的程序,使用(r)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(1-(吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶替代3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶并使用(s)-4-甲基吗啉-3-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa被分离。对于c
29h34
n7o3(m+h)
+
,lc-ms计算值:m/z=528.3;实验值528.3
[1811]
实施例138.((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)((r)-4-甲基吗啉-3-基)甲酮
[1812][1813]
此化合物根据实施例129中所描述的程序,使用(r)-4-甲基吗啉-3-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
29h34
n7o3(m+h)
+
,lc-ms计算值:m/z=528.3;实验值528.3
[1814]
实施例139.(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(1-(羟基甲基)环丁基)甲酮
[1815][1816]
此化合物根据实施例116中所描述的程序,使用1-(羟基甲基)环丁烷-1-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h31
n6o3(m+h)
+
,lc-ms计算值:m/z=499.2;实验值499.3
[1817]
实施例140.(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(1-乙基氮杂环丁-2-基)甲酮
[1818][1819]
此化合物根据实施例116中所描述的程序,使用(s)-1-乙基氮杂环丁烷-2-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h32
n7o2(m+h)
+
,lc-ms计算值:m/z=498.2;实验值498.2
[1820]
实施例141.(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(1-(2-氟乙基)氮杂环丁-2-基)甲酮
[1821][1822]
此化合物根据实施例116中所描述的程序,使用(s)-1-(2-氟乙基)氮杂环丁烷-2-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h31
fn7o2(m+h)
+
,lc-ms计算值:m/z=516.2;实验值516.2
[1823]
实施例142.(s)-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)(1-异丙基氮杂环丁-2-基)甲酮
[1824][1825]
此化合物根据实施例116中所描述的程序,使用(s)-1-异丙基氮杂环丁烷-2-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
29h34
n7o2(m+h)
+
,lc-ms计算值:m/z=512.3;实验值512.3
[1826]
实施例143.((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)((s)-1-(2-氟乙基)氮杂环丁-2-基)甲酮
[1827][1828]
此化合物根据实施例129中所描述的程序,使用(s)-1-(2-氟乙基)氮杂环丁烷-2-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
29h33
fn7o2(m+h)
+
,lc-ms计算值:m/z=530.3;实验值530.3
[1829]
实施例144.((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)((反)-3-羟基环丁基)甲酮
[1830][1831]
此化合物根据实施例129中所描述的程序,使用(反)-3-羟基环丁烷-1-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h31
n6o3(m+h)
+
,lc-ms计算值:m/z=499.2;实验值499.3
[1832]
实施例145.((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)吡咯烷-1-基)((顺)-3-羟基环丁基)甲酮
[1833][1834]
此化合物根据实施例129中所描述的程序,使用(顺)-3-羟基环丁烷-1-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h31
n6o3(m+h)
+
,lc-ms计算值:m/z=499.2;实验值499.2
[1835]
实施例146.((s)-3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)((1s,3r)-3-羟基-3-甲基环丁基)甲酮
[1836][1837]
此化合物根据实施例129中所描述的程序,使用(1s,3s)-3-羟基-3-甲基环丁烷-1-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
29h33
n6o3(m+h)
+
,lc-ms计算值:m/z=513.2;实验值513.2
[1838]
实施例147. 1-(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)-2-甲氧基乙-1-酮
甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1850][1851]
将5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(0.8g,1.56mmol)、3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸叔丁酯(0.71g,2.03mmol)、二环己基(2’,4’,6
’‑
三异丙基联苯-2-基)膦-(2
’‑
氨基联苯-2-基)(氯)钯(1:1)(0.12g,0.156mmol)和碳酸铯(0.66g,2.03mmol)置于具有隔膜的小瓶中。在3次真空/n2之后,添加1,4-二噁烷(10ml)和水(2ml),并且将反应混合物在60℃下搅拌1h。然后将其冷却至室温并用etoac/水稀释。分离有机相,用盐水洗涤,经na2so4干燥,在真空中浓缩,并且残余物通过biotage isolera纯化。
[1852]
将tfa(5ml)和dcm(5ml)添加至所获得的中间体中,并且将反应混合物在室温下搅拌1h。然后将其在真空中浓缩,并且将反应用饱和nahco3溶液中和。用dcm萃取产物。将有机相用盐水洗涤,经na2so4干燥并浓缩以得到所需产物。对于c
30h31
n6o2(m+h)
+
,lc-ms计算值:m/z=507.2;实验值507.2
[1853]
步骤2. 2-((3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)磺酰基)乙-1-醇
[1854]
在0℃下向3-(1-(氮杂环丁-3-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(10mg,0.020mmol)和tea(6μl,0.04mmol)于dcm(1ml)中的溶液中添加2-羟基乙烷-1-磺酰氯(3mg,0.020mmol)。将反应混合物在室温下搅拌1h。然后将其用盐水淬灭,并且用dcm萃取产物。将有机相经硫酸钠干燥并在真空中浓缩。
[1855]
将残余物溶解于dcm(0.5ml)中,并且添加三氟甲烷磺酸(0.2ml)。将反应混合物在室温下搅拌1h。然后将混合物用饱和nahco3溶液中和并用dcm萃取产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中浓缩。将混合物用ch3cn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
24h27
n6o4s(m+h)
+
,lc-ms计算值:m/z=495.2;实验值495.1
[1856]
实施例151. 2-((3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)磺酰基)-n,n-二甲基乙-1-胺
[1857][1858]
此化合物根据实施例150中所描述的程序,使用2-(二甲基氨基)乙烷-1-磺酰氯替
代2-羟基乙烷-1-磺酰氯作为起始材料来制备。产物作为tfa盐被分离。对于c
26h32
n7o3s(m+h)
+
,lc-ms计算值:m/z=522.2;实验值522.2
[1859]
实施例152. 3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁烷-1-羧酸2-甲氧基乙酯
[1860][1861]
此化合物根据实施例150中所描述的程序,使用氯甲酸2-甲氧基乙酯替代2-羟基乙烷-1-磺酰氯作为起始材料来制备。产物作为tfa盐被分离。对于c
26h29
n6o4(m+h)
+
,lc-ms计算值:m/z=489.2;实验值489.2
[1862]
实施例153.(3-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)氮杂环丁-1-基)((1s,3s)-3-甲氧基环丁基)甲酮
[1863][1864]
此化合物根据实施例116中所描述的程序,使用(1s,3s)-3-甲氧基环丁烷-1-羧酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h31
n6o3(m+h)
+
,lc-ms计算值:m/z=499.2;实验值499.2
[1865]
实施例154.n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)-n-甲基甲烷磺酰胺
[1866][1867]
步骤1. 3-(6-溴吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[1868]
[1869]
将5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(3.5g,6.84mmol)、(6-溴吡啶-3-基)硼酸(2.5g,12.32mmol)、pd(dppf)2cl2(1.5g)和cs2co3(3.5g)在二噁烷(35ml)和水(8ml)中混合在一起。将反应混合物用氮气吹扫并在70℃下加热4小时。过滤所得溶液,并且用dcm洗涤固体。合并滤液级分,在真空中浓缩,并且将产物通过biotage isolera纯化。对于c
29h26
brn4o2(m+h)
+
,lcms计算值:m/z=541.3;实验值:541.3
[1870]
步骤2.(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊-3-烯-1-基)氨基甲酸叔丁酯
[1871][1872]
将3-(6-溴吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(1.06g,2.0mmol)、(3-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)环戊-3-烯-1-基)氨基甲酸叔丁酯(0.73g,2.35mmol)、cs2co3(1.0g)和x-phos pd g2(250mg)在1,4-二噁烷(20ml)和水(2ml)中混合在一起并用氮气冲洗。将混合物密封并在80℃下加热3小时。过滤反应并且在真空中浓缩滤液。将粗材料用biotage isolera纯化以得到所需产物。对于c
39h42
n5o4(m+h)
+
,lcms计算值:m/z=644.3;实验值:644.4。
[1873]
步骤3.(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)氨基甲酸叔丁酯
[1874][1875]
将(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊-3-烯-1-基)氨基甲酸叔丁酯(1.2g,1.86mmol)和pd/c(0.30g)于甲醇(20ml)和1,4-二噁烷(20ml)的溶液中的混合物在50psi氢气下搅拌过夜。然后将其过滤并在真空中浓缩。将粗材料用biotage isolera纯化以得到所需产物。对于c
39h44
n5o4(m+h)
+
,lcms计算值:m/z=646.3;实验值:646.4。
[1876]
步骤4. 3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基环戊-1-胺
[1877][1878]
将lah于thf(2ml)中的2m溶液缓慢地添加至在干冰-己烷浴中冷却的(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)氨基甲酸叔丁酯(0.70g,1.084mmol)于thf(5ml)中的溶液中。使反应混合物升温至室温并搅拌过夜。将反应小心地用冰淬灭。向其中添加20ml 1n naoh溶液。用dcm 2
×
20ml萃取产物。分离有机相,通过硅藻土过滤,经na2so4干燥并在真空中浓缩。所得材料不经进一步纯化即用于下一步骤。对于c
35h38
n5o2(m+h)
+
,lcms计算值:m/z=560.3;实验值:560.4。
[1879]
步骤5.n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)-n-甲基甲烷磺酰胺
[1880]
将甲烷磺酰氯(8mg,0.071mmol)添加至3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基环戊-1-胺(4mg,7.2μmol)和dipea(50mg)于thf(0.5ml)中的溶液中,并且将反应混合物在室温下搅拌1h。向此溶液中添加0.5ml三氟甲磺酸/dcm(1:1)混合物并且将反应再在室温下搅拌1h。然后将混合物用饱和nahco3溶液中和并用dcm萃取产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中浓缩。将混合物用ch3cn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
28h32
n5o3s(m+h)
+
,lcms计算值:m/z=518.2;实验值:518.3。
[1881]
实施例155.n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)-2-羟基-n-甲基乙酰胺(峰1)
[1882][1883]
步骤1.(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)(甲基)氨基甲酸叔丁酯
[1884]
[1885]
将boc-酸酐(0.20g)添加至3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基环戊-1-胺(0.10g,0.18mmol)和三乙胺(0.5ml)于二氯甲烷(5ml)中的溶液中,并且将反应混合物在室温下搅拌过夜。将水添加至反应混合物中,并且用dcm萃取所需产物。合并有机相,经硫酸钠干燥,在真空中浓缩,并通过biotage isolera纯化。对于c
40h46
n5o4(m+h)
+
,lcms计算值:m/z=660.3;实验值:660.4。
[1886]
将两种对映体在具有手性柱phenomenex lux 5um i-amylose-1(21.2
×
250mm),用25%甲醇/co2洗脱(65ml/min)的手性制备型sfc上分离。
[1887]
步骤2.3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基环戊-1-胺(峰1)
[1888][1889]
将2ml于二噁烷中的4n hcl溶液添加至(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)(甲基)氨基甲酸叔丁酯(10mg,0.015mmol)(来自手性分离的峰1)于0.5ml甲醇中的溶液中。在将反应混合物在室温下搅拌过夜之后,在真空中去除溶剂,并且所获得的所需产物的hcl盐不经进一步纯化即用于下一步骤中。对于c
35h38
n5o2(m+h)
+
,lcms计算值:m/z=560.3;实验值:560.4。
[1890]
步骤3.n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)-2-羟基-n-甲基乙酰胺(峰1)
[1891]
将hatu(10mg)添加至3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基环戊-1-胺(5mg,8.93μmol,峰1)、2-羟基乙酸(7mg,0.089mmol)和dipea(50mg)于dmf(0.5ml)中的溶液中。将反应混合物在室温下搅拌1h,然后添加水,并用dcm萃取所需产物。合并有机级分,经硫酸钠干燥并在真空中浓缩。
[1892]
将残余物溶解于dcm(2ml)中,并且添加三氟甲烷磺酸(0.66g,4.4mmol)。将反应混合物在室温下搅拌1h。然后,将混合物用饱和nahco3溶液中和并用dcm萃取产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中浓缩。将混合物用ch3cn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
29h32
n5o3(m+h)
+
,lcms计算值:m/z=498.2;实验值:498.3。
[1893]
实施例156.(2s)-n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)-2-羟基丙酰胺
[1894][1895]
步骤1. 3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊-1-胺
[1896][1897]
将(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)氨基甲酸叔丁酯(0.10g,0.155mmol)溶解于dcm(2ml)中,并且添加三氟甲烷磺酸(0.66g,4.4mmol)。将反应混合物在室温下搅拌1h。然后,将混合物用饱和nahco3溶液中和并用dcm萃取产物。将有机相用盐水洗涤,经硫酸钠干燥并在真空中浓缩。对于c
26h28
n5o(m+h)
+
,lcms计算值:m/z=426.3;实验值:426.4。
[1898]
步骤2.(2s)-n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)-2-羟基丙酰胺
[1899]
将hatu(10mg)添加至3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊-1-胺(0.005g,11.7μmol)、(s)-2-羟基丙酸(8.25mg,0.092mmol)和dipea(50mg)于dmf(0.5ml)中的溶液中,并且将反应混合物在室温下搅拌1h。然后将反应混合物用4.5ml甲醇稀释,过滤并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
29h32
n5o3(m+h)
+
,lcms计算值:m/z=498.2;实验值:498.3。
[1900]
实施例157.n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊基)-2-羟基乙酰胺
[1901][1902]
将hatu(10mg)添加至3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环戊-1-胺(5mg,11.7μmol)、2-羟基乙酸(7mg,0.092mmol)和dipea(50mg)于dmf(0.5ml)中的溶液中,并且将反应混合物在室温下搅拌1h。然后将反应混合物用4.5ml甲醇稀释,过滤并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
28h30
n5o3(m+h)
+
,lcms计算值:m/z=484.2;
pd g2(10mg,0.012mmol)和磷酸钾(39mg,0.183mmol)于二噁烷(1ml)和水(0.1ml)中的混合物加热至80℃持续20小时。此后,将溶液冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物溶解于dcm(1ml)中并添加tfa(1ml)。将混合物在室温下搅拌1h并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
29h31
n4o2(m+h)
+
,lcms计算值:m/z=467.2;实验值467.3。
[1913]
实施例159. 4-(3-(4-((1r,5s)-3-(2-羟基乙基)-3-氮杂双环[3.1.0]己-1-基)苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1914][1915]
步骤1.(1r,5s)-3-(2-((叔丁基二甲基甲硅烷基)氧基)乙基)-1-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)苯基)-3-氮杂双环[3.1.0]己烷
[1916][1917]
此化合物根据实施例158中所描述的程序,使用(1r,5s)-1-(4-溴苯基)-3-氮杂双环[3.1.0]己烷替代1-(4-溴苯基)-3-氮杂双环[3.1.0]己烷来制备。对于c
25h43
bno3si(m+h)
+
,lcms计算值:m/z=444.3;实验值:444.5。
[1918]
步骤2. 4-(3-(4-((1r,5s)-3-(2-羟基乙基)-3-氮杂双环[3.1.0]己-1-基)苯基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1919]
此化合物根据实施例158中所描述的程序,使用4-(3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈和(1r,5s)-3-(2-((叔丁基二甲基甲硅烷基)氧基)乙基)-1-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)苯基)-3-氮杂双环[3.1.0]己烷替代5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯和3-(2-((叔丁基二甲基甲硅烷基)氧基)乙基)-1-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)苯基)-3-氮杂双环[3.1.0]己烷作为起始材料来制备。对于c
30h30
n5o2(m+h)
+
,lcms计算值:m/z=492.2;实验值:492.4。
[1920]
实施例160. 1-((5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)甲基)哌啶-4-醇
[1921][1922]
步骤1. 5-(2,3-二氢-1h-茚-4-基)-3-(6-(羟基甲基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1923][1924]
将5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(1.5g,3.05mmol)、(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)甲醇(1.8g,7.63mmol)、xphos pd g2(0.48g,0.61mmol)和磷酸钾(2.59g,12.21mmol)于二噁烷(20ml)和水(2.0ml)中的混合物加热至80℃持续20小时。此后,将溶液冷却至室温,用水稀释并用etoac萃取产物。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物通过硅胶色谱纯化以得到所需产物。对于c
27h29
n4o4(m+h)
+
,lcms计算值:m/z=473.2;实验值:473.1。
[1925]
步骤2. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(6-(((甲基磺酰基)氧基)甲基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1926][1927]
向5-(2,3-二氢-1h-茚-4-基)-3-(6-(羟基甲基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(400mg,0.846mmol)和n,n-二异丙基乙胺(591μl,3.39mmol)于dcm(10ml)中的溶液中添加甲烷磺酰氯(200μl,2.54mmol)。将所得溶液在室温下搅拌1.5小时。然后将反应用饱和nahco3水溶液淬灭,用dcm萃取,经na2so4干燥并浓缩。粗产物直接用于下一步骤中。对于c
28h31
n4o6s(m+h)
+
,lcms计算值:m/z=551.2;实验值:551.0。
[1928]
步骤3. 1-((5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)甲基)哌啶-4-醇
[1929]
将5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(6-(((甲基磺酰基)氧基)甲基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(30mg,0.054mmol)、哌啶-4-醇(11mg,
(m+h)
+
,lcms计算值:m/z=485.2;实验值:485.0。
[1938]
步骤2. 4-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)乙基)吗啉
[1939]
将3-(6-乙酰基吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(30mg,0.062mmol)、吗啉(11mg,0.124mmol)和三乙酰氧基硼氢化钠(26mg,0.124mmol)于dcm(1ml)中的混合物在室温下搅拌20小时。此后,将溶液用水稀释并用dcm萃取。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物溶解于dcm(1ml)中,并且添加tfa(1ml)。将混合物在室温下搅拌1h并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
27h30
n5o2(m+h)
+
,lcms计算值:m/z=456.2;实验值456.2。
[1940]
实施例163. 7-((5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)甲基)-5,6,7,8-四氢-[1,2,4]三唑并[1,5-a]吡嗪
[1941][1942]
此化合物根据实施例160中所描述的程序,使用5,6,7,8-四氢-[1,2,4]三唑并[1,5-a]吡嗪替代哌啶-4-醇来制备。对于c
27h27
n8o(m+h)
+
,lc-ms计算值:m/z=479.2;实验值479.0。
[1943]
实施例164. 4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-(2-羟基乙基)哌啶-4-甲腈
[1944][1945]
步骤1. 4-(5-溴吡啶-2-基)-4-氰基哌啶-1-羧酸叔丁酯
[1946][1947]
在0℃下向4-氰基哌啶-1-羧酸叔丁酯(2.0g,9.51mmol)于thf(48ml)中的溶液中逐滴添加双(三甲基甲硅烷基)胺化钠于thf中的溶液(1.0m,12.4ml,12.4mmol)。将所得溶液在室温下搅拌。1小时之后,逐滴添加5-溴-2-氟吡啶(2.5g,14.27mmol)并且将所得溶液在室温下搅拌20小时。此后,将溶液用水淬灭并用dcm萃取。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物通过硅胶色谱纯化以得到所需产物。对于c
12h13
brn3o2(m-c4h7)
+
,lcms计算值:m/z=310.0;实验值:309.9。
[1948]
步骤2. 4-氰基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌啶-1-羧酸叔丁酯
[1949][1950]
将4-(5-溴吡啶-2-基)-4-氰基哌啶-1-羧酸叔丁酯(2.50g,6.83mmol)、4,4,4’,4’,5,5,5’,5
’‑
八甲基-2,2
’‑
联(1,3,2-二氧硼戊环)(2.4g,9.6mmol)、pdcl2dppf.dcm(0.836g,1.02mmol)和乙酸钾(2.01g,20.5mmol)于二噁烷(50ml)中的混合物在85℃下加热20小时。然后将反应混合物通过硅藻土过滤,用etoac洗涤,并浓缩。然后将残余物通过硅胶色谱纯化以得到所需产物。对于c
18h25
bn3o4(m-c4h7)
+
,lcms计算值:m/z=358.2;实验值:358.1。
[1951]
步骤3. 4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-4-甲腈
[1952][1953]
将5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(265mg,0.539mmol)、4-氰基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌啶-1-羧酸叔丁酯(446mg,1.08mmol)、sphos pd g3(84mg,0.108mmol)和碳酸铯(527mg,1.618mmol)于二噁烷(3ml)和水(0.3ml)中的混合物加热至80℃持续20小时。此后,将溶液冷却至室温,用水稀释并用etoac萃取。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物溶解于dcm(3ml)中,并且添加tfa(2ml)。将溶液在室温下搅拌1h。然后去除溶剂并且将残余物通过硅胶色谱纯化以得到所需产物。对于c
27h27
n6o(m+h)
+
,lcms计算值:m/z=451.2;实验值:451.2。
[1954]
步骤4. 4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-(2-羟基乙基)哌啶-4-甲腈
[1955]
将4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-4-甲腈(30mg,0.067mmol)、2-((叔丁基二甲基甲硅烷基)氧基)乙醛(35mg,0.200mmol)和三乙酰氧基硼氢化钠(28mg,0.133mmol)于dcm(1ml)中的混合物在室温下搅拌20小时。此后,将溶液用水稀释并用dcm萃取。将合并的有机相用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物溶解于dcm(1ml)中,并添加tfa(1ml)。将混合物在室温下搅拌1h并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
29h31
n6o2(m+h)
+
,lcms计算值:m/z=495.2;实验值495.0。
[1956]
实施例165. 4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡
啶-3-基)吡啶-2-基)-1-(2-羟基乙酰基)哌啶-4-甲腈
[1957][1958]
将4-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-4-甲腈(30mg,0.067mmol)、2-羟基乙酸(5mg,0.067mmol)、hatu(38mg,0.10mmol)和n,n-二异丙基乙胺(23μl,0.133mmol)于dmf(0.5ml)中的混合物在室温下搅拌1小时。然后将混合物用mecn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
29h29
n6o3(m+h)
+
,lcms计算值:m/z=509.2;实验值509.0。
[1959]
实施例166. 2-(3-(6-甲氧基-3-(6-(4-(2-甲氧基乙基)哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2-甲基苯基)乙腈
[1960][1961]
步骤1. 1-(2-甲氧基乙基)-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪
[1962][1963]
此化合物根据实施例89步骤1中所描述的程序,使用1-溴-2-甲氧基乙烷替代2-溴乙-1-醇作为起始材料来制备。产物作为tfa盐被分离。对于c
12h21
bn3o3(硼酸,m+h)
+
,lcms计算值:m/z=266.2,实验值:266.3。
[1964]
步骤2. 2-(3-(6-甲氧基-3-(6-(4-(2-甲氧基乙基)哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2-甲基苯基)乙腈
[1965]
此化合物根据实施例89步骤2中所描述的程序,使用1-(2-甲氧基乙基)-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪替代2-(4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌嗪-1-基)乙-1-醇作为起始材料来制备。将混合物通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
28h32
n7o2(m+h)
+
,lc-ms计算值:m/z=498.3,实验值498.4。1h nmr(500mhz,dmso-d6)δ13.40
–
12.90(s,1h),9.89
–
9.71(s,1h),8.48(d,j=9.0hz,1h),7.54(s,1h),7.45(d,j=7.5hz,1h),7.35
–
7.30(m,1h),7.28(d,j=7.6hz,1h),7.08(d,j=8.9hz,1h),4.42(d,j=14.0hz,2h),4.09(s,2h),3.84(s,3h),3.69(t,j=
4.9hz,2h),3.57(d,j=12.1hz,2h),3.39
–
3.32(m,5h),3.25(t,j=13.0hz,2h),3.17
–
3.07(m,2h),2.05(s,3h)ppm。
[1966]
实施例167. 4-(6-甲氧基-3-(1-(1-(四氢-2h-吡喃-4-羰基)哌啶-4-基-4-d)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1967][1968]
步骤1. 4-羟基哌啶-1-羧酸叔丁酯-4-d
[1969][1970]
在0℃下向4-氧代哌啶-1-羧酸叔丁酯(2.0g,10mmol)于甲醇(20ml)中的溶液中逐份添加硼氘化钠(0.84g,20mmol)。在添加完成之后,将反应混合物在氮气下在0℃下搅拌2小时
·
。然后使反应混合物升温至室温持续45分钟,然后用盐水淬灭。将水溶液用乙酸乙酯萃取3次。将汇集的有机萃取物经硫酸钠干燥,过滤,并且在真空中去除溶剂。所得产物不经进一步纯化即用于下一步骤中。对于c6h
11
dno3(m-tbu+h)
+
,lcms计算值:m/z=147.1,实验值:147.1。
[1971]
步骤2. 4-((甲基磺酰基)氧基)哌啶-1-羧酸叔丁酯-4-d
[1972][1973]
在0℃下通过注射器向4-羟基哌啶-1-羧酸叔丁酯-4-d(2.1g,10mmol)于无水二氯甲烷(103ml)中的溶液中添加三乙胺(2.2g,15mmol)。通过注射器逐滴向搅拌的反应混合物中添加甲烷磺酰氯(0.97ml,12mmol)。使反应升温至室温持续1小时,然后在真空中去除溶剂。将所得残余物溶解于100ml乙醚中。将乙醚溶液依序用15ml 1m盐酸水溶液、15ml水和15ml饱和碳酸氢钠水溶液洗涤。然后将有机相经硫酸钠干燥,过滤,并且在真空中去除溶剂。所得产物不经进一步纯化即用于下一步骤中。对于c7h
13
dno5s(m-tbu+h)
+
,lcms计算值:m/z=225.1,实验值:225.0。
[1974]
步骤3. 4-(4-碘-1h-吡唑-1-基)哌啶-1-羧酸叔丁酯-4-d
[1975][1976]
在0℃下向4-碘-1h-吡唑(1.46g,7.54mmol)于dmf(26ml)中的溶液中分批添加氢
化钠(0.362g,60wt%,9.04mmol)。在添加完成之后,将反应混合物在氮气下在0℃下搅拌1小时。然后,向此溶液中添加含4-((甲基磺酰基)氧基)哌啶-1-羧酸叔丁酯-4-d(2.32g,8.29mmol)的dmf(3ml)。然后将反应混合物加热至100℃持续3小时,之后将其冷却回室温并用50ml水淬灭。将水溶液用50ml乙酸乙酯萃取4次。然后将汇集的有机相经硫酸钠干燥,过滤,并且在真空中去除溶剂。将残余物通过硅胶色谱纯化以得到所需产物。对于c9h
12
din3o2(m-tbu+h)
+
,lcms计算值:m/z=323.0,实验值:323.0。
[1977]
步骤4. 4-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)哌啶-1-羧酸叔丁酯-4-d
[1978][1979]
向4-(4-碘-1h-吡唑-1-基)哌啶-1-羧酸叔丁酯-4-d(1.95g,5.15mmol)于dmso(22ml)中的溶液中添加双(频哪醇合)二硼(1.83g,7.21mmol)、乙酸钾(2.02g,20.6mmol)和四(三苯基膦)钯(0)(595mg,0.515mmol)。将反应用n2吹扫并在80℃下搅拌2小时。此后,将其冷却至室温并通过硅藻土垫过滤,用乙酸乙酯冲洗。然后将有机溶液用盐水洗涤两次,经硫酸钠干燥,过滤,并在真空中浓缩。将残余物通过硅胶色谱纯化以得到所需产物。对于c
19h32
dbn3o4(m+h)
+
,lcms计算值:m/z=379.3,实验值:379.3。
[1980]
步骤5. 3-(1-(1-(叔丁氧基羰基)哌啶-4-基-4-d)-1h-吡唑-4-基)-5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1981][1982]
向5-(1-氰基-2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(实施例75,步骤7;287mg,0.555mmol)于1,4-二噁烷(4.6ml)和水(0.93ml)中的溶液中添加4-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)哌啶-1-羧酸叔丁酯-4-d(252mg,0.666mmol)、磷酸钾(236mg,1.11mmol)和xphospd g2(44mg,0.055mmol)。将反应用n2脱气并在60℃下搅拌2小时。此后,将其冷却至室温并通过硅藻土垫过滤,用乙酸乙酯冲洗。将残余物通过硅胶色谱纯化以得到所需产物。对于c
35h41
dn7o5(m+h)
+
,lcms计算值:m/z=641.3,实验值:641.4。
[1983]
步骤6. 4-(6-甲氧基-3-(1-(哌啶-4-基-4-d)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1984][1985]
在室温下向3-(1-(1-(叔丁氧基羰基)哌啶-4-基-4-d)-1h-吡唑-4-基)-5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(15mg,0.023mmol)于二氯甲烷(82μl)中的溶液中添加tfa(82μl,1.1mmol)。将反应混合物搅拌30min,然后在真空中浓缩。将残余物通过添加饱和碳酸氢钠水溶液调节至ph 7,然后用10%甲醇/二氯甲烷萃取两次。将汇集的有机萃取物经硫酸钠干燥,过滤,并在真空中浓缩。所得产物不经进一步纯化即用于下一步骤中。对于c
25h25
dn7o(m+h)
+
,lcms计算值:m/z=441.2,实验值:441.2。
[1986]
步骤7. 4-(6-甲氧基-3-(1-(1-(四氢-2h-吡喃-4-羰基)哌啶-4-基-4-d)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1987]
在室温下在搅拌下向4-(6-甲氧基-3-(1-(哌啶-4-基-4-d)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(10mg,0.023mmol)、四氢-2h-吡喃-4-羧酸(3.0mg,0.023mmol)和bop(15mg,0.035mmol)于dmf(0.36ml)中的溶液中添加二异丙基乙胺(10μl,0.058mmol)。将反应混合物继续搅拌80min,然后将其用meoh稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
31h33
dn7o3(m+h)
+
,lc-ms计算值:m/z=553.3,实验值553.3。
[1988]
实施例168. 4-(6-甲氧基-3-(1-((s)-1-(2-甲氧基乙酰基)吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1989][1990]
步骤1. 3-(1-((s)-1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)-5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[1991]
[1992]
此化合物根据实施例167步骤5中所描述的程序,使用(s)-3-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)吡咯烷-1-羧酸叔丁酯替代4-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)哌啶-1-羧酸叔丁酯-4-d作为起始材料来制备。将残余物通过硅胶色谱纯化以得到所需产物。非对映体的分离通过手性制备型sfc(chiralpak ih 5um 21.2
×
250mm,用15%etoh(含有2mm氨)洗脱,40℃,流动速率70ml/min,t
r,峰1
=4.6min,t
r,峰2
=5.8min)来实现。收集峰2并且在真空中蒸发溶剂。对于c
30h32
n7o5(m-tbu+h)
+
,lcms计算值:m/z=570.3,实验值:570.3。
[1993]
步骤2. 4-(6-甲氧基-3-(1-((s)-吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1994][1995]
此化合物根据实施例167步骤6中所描述的程序,使用3-(1-((s)-1-(叔丁氧基羰基)吡咯烷-3-基)-1h-吡唑-4-基)-5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯替代3-(1-(1-(叔丁氧基羰基)哌啶-4-基-4-d)-1h-吡唑-4-基)-5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯作为起始材料来制备。对于c
24h24
n7o(m+h)
+
,lcms计算值:m/z=426.2,实验值:426.2。
[1996]
步骤3. 4-(6-甲氧基-3-(1-((s)-1-(2-甲氧基乙酰基)吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1997]
此化合物根据实施例167步骤7中所描述的程序,使用4-(6-甲氧基-3-(1-((s)-吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈替代4-(6-甲氧基-3-(1-(哌啶-4-基-4-d)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈且使用2-甲氧基乙酸替代四氢-2h-吡喃-4-羧酸作为起始材料来制备。对于c
27h28
n7o3(m+h)
+
,lcms计算值:m/z=498.2,实验值:498.2。
[1998]
实施例169. 4-(6-甲氧基-3-(1-((s)-1-((s)-四氢呋喃-2-羰基)吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[1999][2000]
此化合物根据实施例167步骤7中所描述的程序,使用4-(6-甲氧基-3-(1-((s)-吡咯烷-3-基)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈替代4-(6-甲氧基-3-(1-(哌啶-4-基-4-d)-1h-吡唑-4-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,
3-二氢-1h-茚-1-甲腈并且使用(s)-四氢呋喃-2-羧酸替代四氢-2h-吡喃-4-羧酸作为起始材料来制备。对于c
29h30
n7o3(m+h)
+
,lcms计算值:m/z=524.2,实验值:524.2。
[2001]
实施例170.(7r,8as)-2-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)八氢吡咯并[1,2-a]吡嗪-7-醇
[2002][2003]
此化合物根据实施例90中所描述的程序,使用2-(2,3-二氢-1h-茚-4-基)-4,4,5,5-四甲基-1,3,2-二氧硼戊环替代(3-甲氧基-2-甲基苯基)硼酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h31
n6o2(m+h)
+
,lcms计算值:m/z=483.3;实验值:483.3。
[2004]
实施例171.n-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-3-基)-2-羟基-n-甲基乙酰胺
[2005][2006]
步骤1.(1-(5-溴吡啶-2-基)氮杂环丁-3-基)(甲基)氨基甲酸叔丁酯
[2007][2008]
向5-溴-2-氟吡啶(2g,11.36mmol)于dmso(10ml)中的溶液中添加氮杂环丁-3-基(甲基)氨基甲酸叔丁酯(2.18g,11.36mmol)和碳酸铯(7.4g,22.73mmol)。将反应用n2脱气并在100℃下搅拌2小时。此后,将其冷却至室温并用etoac稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
14h21
brn3o2(m+h)
+
,lc-ms计算值:m/z=342.1;实验值342.1。
[2009]
步骤2.甲基(1-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)氮杂环丁-3-基)氨基甲酸叔丁酯
[2010][2011]
将(1-(5-溴吡啶-2-基)氮杂环丁-3-基)(甲基)氨基甲酸叔丁酯(2.96g,8.65mmol)、4,4,4’,4’,5,5,5’,5
’‑
八甲基-2,2
’‑
联(1,3,2-二氧硼戊环)(3.3g,12.97mmol)、[1,1
’‑
双(二苯基膦基)-二茂铁]-二氯化钯(ii)(706mg,0.865mmol)和乙酸钾(1.66g,17.3mmol)于二噁烷(20ml)中的混合物在100℃下搅拌90分钟。在冷却至室温之后,
过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过biotage isolera纯化。对于c
20h33
bn3o4(m+h)
+
,lcms计算值:m/z=390.2;实验值:390.2。
[2012]
步骤3.(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-3-基)(甲基)氨基甲酸叔丁酯
[2013][2014]
向5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(实施例53,步骤3;1g,1.96mmol)于1,4-二噁烷(6ml)和水(1.2ml)中的溶液中添加甲基(1-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)氮杂环丁-3-基)氨基甲酸叔丁酯(1.14g,2.93mmol)、磷酸钾(1.25g,5.87mmol)和[1,1
’‑
双(二苯基膦基)二茂铁]-二氯化钯(ii)(160mg,0.196mmol)。将反应用n2脱气并在80℃下搅拌2小时。此后,将其冷却至室温并用etoac稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
38h43
n6o4(m+h)
+
,lc-ms计算值:m/z=647.3;实验值647.3。
[2015]
步骤4. 1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基氮杂环丁-3-胺
[2016][2017]
向(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-3-基)(甲基)氨基甲酸叔丁酯(1.01g,1.56mmol)于二氯甲烷(3ml)中的溶液中添加三氟乙酸(4ml)。将反应在室温下搅拌1小时。此后,将其用二氯甲烷稀释。所得溶液依序用水、饱和nacl水溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。残余物不经纯化直接用于下一步骤中。对于c
33h35
n6o2(m+h)
+
,lc-ms计算值:m/z=547.3;实验值547.3。
[2018]
步骤5.n-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-3-基)-2-羟基-n-甲基乙酰胺
[2019]
向1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基氮杂环丁-3-胺(200mg,0.37mmol)于二氯甲烷(4ml)中的溶液中添加2-羟基乙酸(42mg,0.55mmol)、三甲胺(95mg,0.73mmol)和hatu(181mg,0.48mmol)。将反应在室温下搅拌1小时。此后,将其用二氯甲烷稀释。所得溶液依序
用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物溶解于二氯甲烷(3ml)和三氟甲烷磺酸(1.5ml)中。将反应在室温下搅拌。30min之后,将反应混合物用4n naoh水溶液淬灭并用二氯甲烷稀释。所得混合物依序用水、饱和nacl水溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。残余物用meoh稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h29
n6o3(m+h)
+
,lc-ms计算值:m/z=485.2;实验值485.2。
[2020]
实施例172.(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)(四氢呋喃-2-基)甲酮
[2021][2022]
步骤1. 3-(5-溴吡啶-2-基)氮杂环丁烷-1-羧酸叔丁酯
[2023][2024]
向锌粉(1.73g,26.5mmol)于thf(30ml)中的溶液中添加1,2-二溴乙烷(332mg,1.77mmol)和氯三甲基硅烷(192mg,1.77mmol)。将反应用n2脱气并在60℃下搅拌15分钟,然后添加含3-碘氮杂环丁烷-1-羧酸叔丁酯(5g,17.7mmol)的dma(30ml)。将混合物加热至60℃并搅拌15分钟,然后冷却至室温。向冷却的混合物中添加2,5-二溴吡啶(4.6g,19.4mmol)、[1,1
’‑
双(二苯基膦基)二茂铁]-二氯化钯(ii)(1:1)(721mg,0.88mmol)和碘化亚铜(168mg,0.88mmol)。将混合物加热至80℃持续2小时。此后,将其冷却至室温并用etoac稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
13h18
brn2o2(m+h)
+
,lc-ms计算值:m/z=313.0;实验值313.0。
[2025]
步骤2.甲基(1-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)氮杂环丁-3-基)氨基甲酸叔丁酯
[2026][2027]
将(1-(5-溴吡啶-2-基)氮杂环丁-3-基)(甲基)氨基甲酸叔丁酯(2.96g,8.65mmol)、4,4,4’,4’,5,5,5’,5
’‑
八甲基-2,2
’‑
联(1,3,2-二氧硼戊环)(3.3g,12.97mmol)、[1,1
’‑
双(二苯基膦基)-二茂铁]-二氯化钯(ii)(706mg,0.865mmol)和乙酸钾(1.66g,17.3mmol)于二噁烷(20ml)中的混合物在100℃下搅拌90分钟。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过biotage isolera纯化。对于c
20h33
bn3o4(m+h)
+
,lcms计算值:m/z=390.2;实验值:390.2。
[2028]
步骤3. 3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡
唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁烷-1-羧酸叔丁酯
[2029][2030]
向5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(实施例53,步骤3;545mg,1.07mmol)于1,4-二噁烷(5ml)和水(1ml)中的溶液中添加3-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)氮杂环丁烷-1-羧酸叔丁酯(499mg,1.39mmol)、磷酸钾(521mg,1.60mmol)和甲烷磺酸(2-二环己基膦基-2
′
,6
′‑
二甲氧基联苯)[2-(2
′‑
氨基-1,1
′‑
联苯基)]钯(ii)(83mg,0.11mmol)。将反应用n2脱气并在80℃下搅拌2小时。此后,将其冷却至室温并用etoac稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
37h40
n5o4(m+h)
+
,lc-ms计算值:m/z=618.3;实验值618.3。
[2031]
步骤4. 3-(6-(氮杂环丁-3-基)吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶
[2032][2033]
向3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁烷-1-羧酸叔丁酯(527mg,0.85mmol)于二氯甲烷(2ml)中的溶液中添加三氟乙酸(2ml)。将反应在室温下搅拌1小时。此后,将其用二氯甲烷稀释。所得溶液依序用水、饱和nacl水溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。残余物不经纯化直接用于下一步骤中。对于c
32h32
n5o2(m+h)
+
,lc-ms计算值:m/z=518.2;实验值518.2。
[2034]
步骤5.(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)(四氢呋喃-2-基)甲酮
[2035]
向3-(6-(氮杂环丁-3-基)吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(20mg,0.039mmol)于二氯甲烷(0.5ml)中的溶液中添加四氢呋喃-2-羧酸(9mg,0.077mmol)、三乙胺(10mg,0.077mmol)和hatu(22mg,0.058mmol)。将反应在室温下搅拌1小时。此后,将其用二氯甲烷稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物溶解于二氯甲烷(0.5ml)和三氟甲烷磺酸(0.1ml)中。将反应在室温下搅拌。30min之后,将反应混合物用4n naoh水溶液淬灭并用二氯甲烷稀释。所得混合物依序用水、饱和nacl水溶液洗涤并且
经na2so4干燥。将有机相过滤并浓缩至干。将残余物用meoh稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
29h30
n5o3(m+h)
+
,lc-ms计算值:m/z=496.2;实验值496.2。
[2036]
实施例173.(s)-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)(1-甲基哌啶-2-基)甲酮
[2037][2038]
此化合物根据实施例172步骤5中所描述的程序,使用(s)-1-甲基哌啶-2-羧酸替代四氢呋喃-2-羧酸作为起始材料来制备。产物作为tfa盐被分离。对于c
31h35
n6o2(m+h)
+
,lcms计算值:m/z=523.3;实验值:523.3。
[2039]
实施例174. 1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)-2-(二甲基氨基)乙-1-酮
[2040][2041]
此化合物根据实施例172步骤5中所描述的程序,使用二甲基甘氨酸替代四氢呋喃-2-羧酸作为起始材料来制备。产物作为tfa盐被分离。对于c
28h31
n6o2(m+h)
+
,lcms计算值:m/z=483.2;实验值:483.2。
[2042]
实施例175. 1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)-3-羟基丙-1-酮
[2043][2044]
此化合物根据实施例172步骤5中所描述的程序,使用3-羟基丙酸替代四氢呋喃-2-羧酸作为起始材料来制备。产物作为tfa盐被分离。对于c
27h28
n5o3(m+h)
+
,lcms计算值:m/z=470.2;实验值:470.2。
[2045]
实施例176. 1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)-2-羟基乙-1-酮
[2046][2047]
此化合物根据实施例172步骤5中所描述的程序,使用2-羟基乙酸替代四氢呋喃-2-羧酸作为起始材料来制备。产物作为tfa盐被分离。对于c
26h26
n5o3(m+h)
+
,lcms计算值:m/z=456.2;实验值:456.2。
[2048]
实施例177.(s)-1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)-2-羟基丙-1-酮
[2049][2050]
此化合物根据实施例172步骤5中所描述的程序,使用(s)-2-羟基丙酸替代四氢呋喃-2-羧酸作为起始材料来制备。产物作为tfa盐被分离。对于c
27h28
n5o3(m+h)
+
,lcms计算值:m/z=470.2;实验值:470.2。
[2051]
实施例178.n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环丁基)-2-羟基-n-甲基乙酰胺
[2052][2053]
步骤1.(3-(5-溴吡啶-2-基)环丁基)(甲基)氨基甲酸叔丁酯
[2054][2055]
向锌粉(892mg,13.64mmol)于thf(20ml)中的溶液中添加1,2-二溴乙烷(171mg,0.91mmol)和氯三甲基硅烷(99mg,0.91mmol)。将反应用n2脱气并在60℃下搅拌15分钟,然后添加含(3-碘环丁基)(甲基)氨基甲酸叔丁酯(2.83g,9.09mmol)的dma(20ml)。将混合物加热至60℃且搅拌15分钟,然后冷却至室温。向冷却的混合物中添加2,5-二溴吡啶(2.37g,10mmol)、[1,1
’‑
双(二苯基膦基)二茂铁]-二氯化钯(ii)(1:1)(371mg,0.46mmol)和碘化亚铜(87mg,0.049mmol)。将混合物加热至80℃持续2小时。此后,将其冷却至室温并用etoac稀
释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
15h22
brn2o2(m+h)
+
,lc-ms计算值:m/z=341.1;实验值341.1。
[2056]
步骤2.甲基(3-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)环丁基)氨基甲酸叔丁酯
[2057][2058]
将(3-(5-溴吡啶-2-基)环丁基)(甲基)氨基甲酸叔丁酯(1.34g,3.93mmol)、4,4,4’,4’,5,5,5’,5
’‑
八甲基-2,2
’‑
联(1,3,2-二氧硼戊环)(1.5g,5.89mmol)、[1,1
’‑
双(二苯基膦基)-二茂铁]-二氯化钯(ii)(320mg,0.393mmol)和乙酸钾(754mg,7.85mmol)于二噁烷(14ml)中的混合物在80℃下搅拌2小时。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂,并且将粗材料通过biotage isolera纯化。对于c
21h34
bn2o4(m+h)
+
,lcms计算值:m/z=389.3;实验值:389.3。
[2059]
步骤3.(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环丁基)(甲基)氨基甲酸叔丁酯
[2060][2061]
向5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(实施例53,步骤3;456mg,0.89mmol)于1,4-二噁烷(5ml)和水(1ml)中的溶液中添加甲基(3-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)环丁基)氨基甲酸叔丁酯(450mg,1.16mmol)、碳酸铯(436mg,1.34mmol)和甲烷磺酸(2-二环己基膦基-2
′
,6
′‑
二甲氧基联苯)[2-(2
′‑
氨基-1,1
′‑
联苯基)]钯(ii)(70mg,0.089mmol)。将反应用n2脱气并在80℃下搅拌2小时。此后,将其冷却至室温并用etoac稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
39h44
n5o4(m+h)
+
,lc-ms计算值:m/z=646.3;实验值646.3。
[2062]
步骤4. 3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基环丁-1-胺
[2063][2064]
向(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环丁基)(甲基)氨基甲酸叔丁酯(461mg,0.71mmol)于二氯甲烷(2ml)中的溶液中添加三氟乙酸(2ml)。将反应在室温下搅拌1小时。此后,将其用二氯甲烷稀释。所得溶液依序用水、饱和nacl水溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。残余物不经纯化直接用于下一步骤中。对于c
34h36
n5o2(m+h)
+
,lc-ms计算值:m/z=546.3;实验值546.3。
[2065]
步骤5.n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环丁基)-2-羟基-n-甲基乙酰胺
[2066]
向3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-n-甲基环丁-1-胺(20mg,0.037mmol)于二氯甲烷(0.5ml)中的溶液中添加2-羟基乙酸(6mg,0.073mmol)、三甲胺(9mg,0.073mmol)和hatu(21mg,0.055mmol)。将反应在室温下搅拌1小时。此后,将其用二氯甲烷稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物溶解于二氯甲烷(0.5ml)和三氟甲烷磺酸(0.1ml)中。将反应在室温下搅拌。30min之后,将反应混合物用4n naoh水溶液淬灭并用二氯甲烷稀释。所得混合物依序用水、饱和nacl水溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物用meoh稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
28h30
n5o3(m+h)
+
,lc-ms计算值:m/z=484.2;实验值484.2。
[2067]
实施例179. 1-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基-3-d)-2-羟基乙-1-酮
[2068][2069]
步骤1. 3-羟基氮杂环丁烷-1-羧酸叔丁酯-3-d
[2070][2071]
在0℃下向3-氧代氮杂环丁烷-1-羧酸叔丁酯(420mg,2.45mmol)于meoh(5ml)中的溶液中分批添加硼氘化钠(124mg,2.94mmol)。将混合物升温至室温并搅拌30分钟。此后,将
所得溶液浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c8h
15
dno3(m+h)
+
,lc-ms计算值:m/z=175.1;实验值175.1。
[2072]
步骤2. 3-碘氮杂环丁烷-1-羧酸叔丁酯-3-d
[2073][2074]
向3-羟基氮杂环丁烷-1-羧酸叔丁酯-3-d(180mg,1.03mmol)于thf(4ml)中的溶液中添加咪唑(141mg,2.07mmol)、三苯基膦(677mg,2.58mmol)和碘(394mg,1.55mmol)。将混合物加热至50℃并搅拌过夜。此后,将所得溶液浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c8h
14
dino2(m+h)
+
,lc-ms计算值:m/z=285.0;实验值285.0。
[2075]
步骤3. 3-(5-溴吡啶-2-基)氮杂环丁烷-1-羧酸叔丁酯-3-d
[2076][2077]
向锌粉(97mg,1.48mmol)于thf(3ml)中的溶液中添加1,2-二溴乙烷(19mg,0.1mmol)和氯三甲基硅烷(11mg,0.1mmol)。将反应用n2脱气并在60℃下搅拌15分钟,然后添加含3-碘氮杂环丁烷-1-羧酸叔丁酯-3-d(280mg,0.99mmol)的dma(3ml)。将混合物加热至60℃且搅拌15分钟,然后冷却至室温。向冷却的混合物中添加2,5-二溴吡啶(257mg,1.08mmol)、[1,1
’‑
双(二苯基膦基)二茂铁]二氯化钯(ii)(1:1)(40mg,0.049mmol)和碘化亚铜(9mg,0.049mmol)。将混合物加热至80℃持续2小时。此后,将其冷却至室温并用etoac稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
13h17
dbrn2o2(m+h)
+
,lc-ms计算值:m/z=314.1;实验值314.1。
[2078]
步骤4. 3-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)氮杂环丁烷-1-羧酸叔丁酯-3-d
[2079][2080]
将3-(5-溴吡啶-2-基)氮杂环丁烷-1-羧酸叔丁酯-3-d(206mg,0.66mmol)、4,4,4’,4’,5,5,5’,5
’‑
八甲基-2,2
’‑
联(1,3,2-二氧硼戊环)(250mg,0.98mmol)、[1,1
’‑
双(二苯基膦基)-二茂铁]-二氯化钯(ii)(54mg,0.066mmol)和乙酸钾(126mg,1.31mmol)于二噁烷(3ml)中的混合物在80℃下搅拌2小时。在冷却至室温之后,过滤反应混合物,在真空中蒸发溶剂并且将粗材料通过biotage isolera纯化。对于c
19h29
dbn2o4(m+h)
+
,lcms计算值:m/z=362.2;实验值:362.2。
[2081]
步骤5. 5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)-甲基)-1h-吡唑并[4,3-b]吡啶
[2082][2083]
向5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(实施例53,步骤2;2.5g,6.39mmol)于dmf(5ml)中的溶液中添加n-碘代琥珀酰亚胺(2.87g,12.78mmol)。所得混合物在60℃下搅拌1h。将混合物冷却至室温,并且添加2-(三甲基甲硅烷基)乙氧基甲基氯化物(1.39g,8.31mmol)和cs2co3(3.12g,9.59mmol)。将反应混合物在80℃下搅拌1h。此后,将其冷却至室温,用水稀释并用etoac萃取三次。将合并的有机相用饱和nacl洗涤,经na2so4干燥,过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
22h29
in3o2si(m+h)+,lc-ms计算值:m/z=522.1;实验值522.1。
[2084]
步骤6. 3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)甲基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁烷-1-羧酸叔丁酯-3-d
[2085][2086]
向5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1-((2-(三甲基甲硅烷基)乙氧基)-甲基)-1h-吡唑并[4,3-b]吡啶(70mg,0.13mmol)于1,4-二噁烷(1ml)和水(0.2ml)中的溶液中添加3-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)氮杂环丁烷-1-羧酸叔丁酯-3-d(63mg,0.17mmol)、碳酸铯(66mg,0.20mmol)和甲烷磺酸(2-二环己基膦基-2
′
,6
′‑
二甲氧基联苯)[2-(2
′‑
氨基-1,1
′‑
联苯基)]钯(ii)(10mg,0.013mmol)。将反应用n2脱气并在80℃下搅拌1小时。此后,将其冷却至室温并用etoac稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物通过biotage isolera纯化以得到所需产物。对于c
35h45
dn5o4si(m+h)
+
,lc-ms计算值:m/z=629.3;实验值629.3。
[2087]
步骤7. 3-(6-(氮杂环丁-3-基-3-d)吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[2088]
+h)
+
,lc-ms计算值:m/z=241.1;实验值241.2。
[2100]
步骤3. 4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌啶-1-羧酸叔丁酯
[2101][2102]
向4-(5-氯吡啶-2-基)哌啶-1-羧酸叔丁酯(0.75g,2.53mmol)、4,4,4’,4’,5,5,5’,5
’‑
八甲基-2,2
’‑
联(1,3,2-二氧硼戊环)(0.96g,3.79mmol)、乙酸钾(0.74g,7.58mmol)、xphos(0.18g,0.379mmol)和乙酸钯(ii)(0.085g,0.379mmol)于1,4-二噁烷(8ml)中的混合物喷射n2并加热至80℃持续1h。在冷却至室温之后,使用etoac/meoh过滤反应混合物并在真空中蒸发溶剂。粗材料不经进一步纯化即用于下一反应中。关于相应硼酸c
15h24
bn2o4(m-c6h
10
+h)
+
,lc-ms计算值:m/z=307.2;实验值307.2。
[2103]
步骤4. 4-(3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[2104][2105]
此化合物根据实施例53步骤3中所描述的程序,使用4-(6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(实施例75,步骤6)替代5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶作为起始材料来制备。对于c
25h22
in4o2(m+h)
+
,lc-ms计算值:m/z=537.1;实验值537.1。
[2106]
步骤5. 4-(5-(5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-羧酸叔丁酯
[2107][2108]
向4-(3-碘-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(1.2g,2.237mmol)、4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)哌啶-1-羧酸叔丁酯(0.96g,2.46mmol)、[1,1
’‑
双(二苯基膦基)二茂铁]-二氯化钯(ii)(0.183g,0.224mmol)和k3po4(1.43g,6.71mmol)于1,4-二噁烷(10ml)和水(2ml)中的混合物喷射n2并加热至80℃持续2h。将反应混合物用etoac/meoh稀释,通过硅藻土过滤并
且将残余物通过isco nextgen纯化。对于c
40h43
n6o4(m+h)
+
,lc-ms计算值:m/z=671.3;实验值671.3。
[2109]
步骤6. 4-(6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[2110][2111]
向4-(5-(5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-羧酸叔丁酯(69mg,0.103mmol)中添加dcm(0.5ml)和tfa(1ml)并且将混合物在室温下搅拌30min。在真空中蒸发过量tfa,将残余物用dcm稀释并且然后使用饱和nahco3溶液中和。将有机相经硫酸钠干燥,过滤,并且在真空中蒸发溶剂。粗材料不经进一步纯化即用于下一反应中。对于c
35h35
n6o2(m+h)
+
,lc-ms计算值:m/z=571.3;实验值571.3。
[2112]
步骤7. 4-(5-(5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-羧酸甲酯
[2113]
向4-(6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(12mg,0.021mmol)和三乙胺(18μl,0.126mmol)于二噁烷(1ml)中的溶液中添加氯甲酸甲酯(8μl,0.105mmol)。将混合物在室温下搅拌1h。将反应用水淬灭,用dcm萃取。将有机相经na2so4干燥,过滤并浓缩。将残余物溶解于dcm(1ml)中并添加三氟甲磺酸(0.1ml)。将混合物在室温下搅拌30min,然后用meoh淬灭并且在真空中蒸发过量dcm。将残余物用ch3cn稀释并通过siliprep thiol滤筒过滤并通过制备型lcms(waters sunfire c18柱,5um粒径,30
×
100mm)用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
29h29
n6o3(m+h)+,lcms计算值:m/z=509.2;实验值509.2。
[2114]
实施例181. 4-(6-甲氧基-3-(6-(1-(吗啉-4-羰基)哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈,峰2
[2115][2116]
步骤1. 4-(5-(5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-羧酸叔丁酯(峰1和峰2)
[2117][2118]
外消旋混合物根据实施例180步骤5中所描述的程序来制备。对于c
40h43
n6o4(m+h)
+
,lc-ms计算值:m/z=671.3;实验值671.3。然后,将两种对映体用制备型fsc(chrialpak ih,21
×
250mm,用30%meoh/co2洗脱,流动速率65ml/min,tr,峰1=3.7min,t
r,峰2
=4.1min)分离。收集峰2并且在真空中蒸发溶剂并且残余物不经进一步纯化直接用于下一步骤中。
[2119]
步骤2. 4-(6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(峰2)
[2120][2121]
此化合物根据实施例180步骤6中所描述的程序,使用4-(5-(5-(1-氰基-2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)哌啶-1-羧酸叔丁酯峰2作为起始材料替代外消旋材料(实施例180,步骤5)来制备。对于c
35h35
n6o2(m+h)
+
,lc-ms计算值:m/z=571.3;实验值571.3。
[2122]
步骤3. 4-(6-甲氧基-3-(6-(1-(吗啉-4-羰基)哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(峰2)
[2123]
此化合物根据实施例180步骤7中所描述的程序,使用4-(6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈峰2和吗啉-4-碳酰氯作为起始材料来制备。产物作为tfa盐被分离。对于c
32h34
n7o3(m+h)
+
,lc-ms计算值:m/z=564.3;实验值564.2。
[2124]
实施例182. 4-(3-(6-(1-乙酰基哌啶-4-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈,峰2
[2125]
[2126]
此化合物根据实施例180和181步骤7中所描述的程序,使用4-(6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈(实施例181,步骤2,峰2)和乙酰氯作为起始材料来制备。产物作为tfa盐被分离。对于c
29h29
n6o2(m+h)
+
,lc-ms计算值:m/z=493.2;实验值493.2。
[2127]
实施例183:4-(3-(6-(1-乙酰基吡咯烷-3-基)吡啶-3-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[2128][2129]
步骤1. 3-(5-氯吡啶-2-基)-2,5-二氢-1h-吡咯-1-羧酸叔丁酯
[2130][2131]
此化合物根据实施例180步骤1中所描述的程序,使用3-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-2,5-二氢-1h-吡咯-1-羧酸叔丁酯替代4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-3,6-二氢吡啶-1(2h)-羧酸叔丁酯作为起始材料来制备。对于c
10h10
cln2o2(m-c4h9+h)
+
,lc-ms计算值:m/z=225.0;实验值225.0。
[2132]
步骤2. 3-(5-氯吡啶-2-基)吡咯烷-1-羧酸叔丁酯,峰1和峰2
[2133][2134]
将5%rh/c(0.58g,5.64mmol)添加至3-(5-氯吡啶-2-基)-2,5-二氢-1h-吡咯-1-羧酸叔丁酯(1.9g,6.77mmol)于thf(10ml)、etoh(10ml)和etoac(20.00ml)中的溶液中。将反应用h2吹扫并在室温下搅拌,连接至填充有氢气的气球持续20小时。在完成之后,将反应通过硅藻土使用etoac过滤。然后将滤液浓缩至干以提供外消旋混合物。对于c
10h12
cln2o2(m-c4h9+h)
+
,lc-ms计算值:m/z=227.1;实验值227.1。
[2135]
将两种对映体用制备型fsc(phenomenex lux 5um amylose-1,21.2
×
250mm,用20%meoh/co2洗脱,流动速率70ml/min,tr,峰1=2.9min,t
r,峰2
=3.4min)分离。收集峰2并且在真空中蒸发溶剂并且残余物不经进一步纯化直接用于下一步骤。
[2136]
步骤3. 3-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)吡咯烷-1-羧酸叔丁酯,峰2
[2137][2138]
此化合物根据实施例180步骤3中所描述的程序,使用3-(5-氯吡啶-2-基)吡咯烷-1-羧酸叔丁酯峰2替代4-(5-氯吡啶-2-基)哌啶-1-羧酸叔丁酯作为起始材料来制备。对于
1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[2148][2149]
此化合物根据实施例180步骤7中所描述的程序,使用4-(6-甲氧基-1-(4-甲氧基苄基)-3-(6-(哌啶-4-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈峰a和吗啉-4-碳酰氯作为起始材料来制备。产物作为tfa盐被分离。对于c
31h32
n7o3(m+h)
+
,lc-ms计算值:m/z=550.3;实验值550.2。
[2150]
实施例185. 4-(3-(1-(氰基甲基)-1h-吡唑-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[2151][2152]
步骤1. 5-(1-氰基-2,3-二氢-1h-茚-4-基)-3-(1-(氰基甲基)-1h-吡唑-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[2153][2154]
向5-(1-氰基-2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(实施例75,步骤7;150mg,0.291mmol)于1,4-二噁烷(1.2ml)和水(0.24ml)中的溶液中添加2-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)乙腈(81mg,0.35mmol)、磷酸钾(123mg,0.581mmol)和xphospd g2(23mg,0.029mmol)。将反应用n2脱气并在60℃下搅拌1小时。此后,将其冷却至室温并通过硅藻土垫过滤,用乙酸乙酯冲洗。将残余物通过硅胶色谱纯化以得到所需产物。对映体的分离通过手性制备型sfc(chiralpak ib-n 5um 20
×
250mm,用20%meoh洗脱,40℃,流动速率70ml/min,t
r,峰1
=7.1min,t
r,峰2
=7.7min)来实现。收集峰1并且在真空中蒸发溶剂。对于c
27h26
n7o3(m+h)
+
,lcms计算值:m/z=496.2,实验值:496.2。
[2155]
步骤2. 4-(3-(1-(氰基甲基)-1h-吡唑-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡
啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[2156]
在室温下向5-(1-氰基-2,3-二氢-1h-茚-4-基)-3-(1-(氰基甲基)-1h-吡唑-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(36mg,0.073mmol)于二氯甲烷(50μl)中的溶液中添加tfa(50μl,6.5mmol)。将反应混合物搅拌30min,然后在真空中浓缩。将残余物用meoh稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
22h18
n7o(m+h)
+
,lc-ms计算值:m/z=396.2,实验值396.2。
[2157]
实施例186. 4-(6-甲氧基-3-(6-(4-甲基哌嗪-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶-5-基)-2,3-二氢-1h-茚-1-甲腈
[2158][2159]
将5-(1-氰基-2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(峰1,50mg,0.097mmol)(单一对映体通过在手性制备型hplc phenomenex lux 5um amylose-1,21.2
×
250mm上进行手性分离而获得,用15%etoh/己烷洗脱,流动速率20ml/min,t
r,峰1
=17.5min,t
r,峰2
=23.3min,50mg,0.097mmol)、(6-(4-甲基哌嗪-1-基)吡啶-3-基)硼酸(25.1mg,0.116mmol)、xphos-pdg2(7.6mg,9.68μmol)和nahco3(16mg,0.194mmol)置于小瓶中并且将小瓶抽真空并用n2回填三次。在添加1,4-二噁烷(1ml)和水(100μl)之后,将反应混合物在70℃下搅拌1h。然后过滤反应,并且在真空中蒸发溶剂。添加dcm(1ml)和tfa(0.5ml)并且将反应混合物在室温下搅拌30min。然后将混合物用ch3cn和水稀释并用制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h28
n7o(m+h)
+
,lc-ms计算值:m/z=466.2;实验值466.2
[2160]
实施例187. 3-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)氮杂环丁-1-基)丙腈
[2161][2162]
向3-(6-(氮杂环丁-3-基)吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1-(4-甲氧基苄基)-1h-吡唑并[4,3-b]吡啶(20mg,0.039mmol,实施例172)于mecn(1ml)中的溶液中添加3-溴丙腈(15mg,0.12mmol)和碳酸铯(63mg,0.19mmol)。将反应在50℃下加热2小时。此后,将其用二氯甲烷稀释。所得溶液依序用水、饱和nacl水溶液洗涤,并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物溶解于二氯甲烷(0.5ml)和三氟甲烷磺酸
(0.1ml)中。将反应在室温下搅拌。30min之后,将反应混合物用4n naoh水溶液淬灭并用二氯甲烷稀释。所得混合物依序用水、饱和nacl水溶液洗涤并且经na2so4干燥。将有机相过滤并浓缩至干。将残余物用tfa和meoh酸化并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。产物作为tfa盐被分离。对于c
27h27
n6o(m+h)
+
,lc-ms计算值:m/z=451.2;实验值451.2。
[2163]
实施例188.n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环丁基)-2-甲氧基-n-甲基乙酰胺
[2164][2165]
此化合物根据实施例178中所描述的程序,使用2-甲氧基乙酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
29h32
n5o3(m+h)
+
,lcms计算值:m/z=498.2;实验值:498.2。
[2166]
实施例189.n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环丁基)-3-羟基-n-甲基丙酰胺
[2167][2168]
此化合物根据实施例178中所描述的程序,使用3-羟基丙酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
29h32
n5o3(m+h)
+
,lcms计算值:m/z=498.2;实验值:498.2。
[2169]
实施例190.(s)-n-(3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)环丁基)-2-羟基-n-甲基丙酰胺
[2170][2171]
此化合物根据实施例178中所描述的程序,使用(s)-2-羟基丙酸替代2-羟基乙酸作为起始材料来制备。产物作为tfa盐被分离。对于c
29h32
n5o3(m+h)
+
,lcms计算值:m/z=498.2;实验值:498.2。
[2172]
实施例191a.1-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]
吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)-2-羟基乙-1-酮
[2173][2174]
步骤1. 5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯
[2175][2176]
将nis(0.220g,0.978mmol)添加至5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(0.20g,0.754mmol)于dmf(10ml)中的溶液中。在80℃下搅拌2h之后,将反应混合物冷却至室温,并添加三乙胺(0.3ml,2.2mmol)和boc-酸酐(0.411g,1.89mmol)。在室温下再搅拌1h之后,添加水并通过过滤收集沉淀的产物并风干。将粗材料通过biotage isolera纯化以得到白色固体(0.29g,78%)。对于c
21h23
in3o3(m+h)
+
,lcms计算值:m/z=492.1;实验值492.1。
[2177]
步骤2. 1-(5-溴吡啶-2-基)-3-氮杂双环[3.1.0]己烷-3-羧酸叔丁酯
[2178][2179]
将2,5-二溴吡啶(0.49g,2.075mmol)、1-(三氟-l4-硼烷基)-3-氮杂双环[3.1.0]己烷-3-羧酸叔丁酯,钾盐(0.30g,1.04mmol)、碳酸铯(1.01g,3.11mmol)和a pd g3(0.076g,0.104mmol)于甲苯(20ml)和水(2ml)中的混合物加热至80℃持续40小时。此后,将溶液用水稀释并用etoac萃取产物。将合并的有机层用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物通过硅胶色谱纯化以得到所需产物。对于c
11h12
brn2o2(m-c4h7)
+
,lcms计算值:m/z=283.0;实验值:283.1。
[2180]
步骤3. 1-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)-3-氮杂双环[3.1.0]己烷-3-羧酸叔丁酯
[2181]
[2182]
将1-(5-溴吡啶-2-基)-3-氮杂双环[3.1.0]己烷-3-羧酸叔丁酯(85mg,0.25mmol)、4,4,4’,4’,5,5,5’,5
’‑
八甲基-2,2
’‑
联(1,3,2-二氧硼戊环)(89mg,0.35mmol)、pdcl2dppf.dcm(31mg,0.038mmol)和乙酸钾(74mg,0.75mmol)于二噁烷(2.5ml)中的混合物在85℃下加热20小时。然后将反应混合物冷却至室温并通过硅藻土过滤,用etoac洗涤,并浓缩。然后将残余物通过硅胶色谱纯化以得到所需产物。对于c
15h22
bn2o4(m-c6h9)
+
,lcms计算值:m/z=305.2;实验值:305.1。
[2183]
步骤4. 3-(6-(3-氮杂双环[3.1.0]己-1-基)吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[2184][2185]
将5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(450mg,0.916mmol)、1-(5-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)吡啶-2-基)-3-氮杂双环[3.1.0]己烷-3-羧酸叔丁酯(531mg,1.374mmol)、sphos pd g3(107mg,0.137mmol)和碳酸铯(895mg,2.75mmol)于二噁烷(5ml)和水(0.5ml)中的混合物加热至80℃持续20小时。此后,将溶液冷却至室温,用水稀释,并用etoac萃取产物。将合并的有机层用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物溶解于dcm(3ml)中,并且添加tfa(2ml)。将溶液在室温下搅拌1h。然后在真空中去除溶剂,并且残余物通过硅胶色谱纯化以得到所需产物。对于c
26h26
n5o(m+h)
+
,lcms计算值:m/z=424.2;实验值:424.4。
[2186]
步骤5. 1-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)-2-羟基乙-1-酮
[2187]
将3-(6-(3-氮杂双环[3.1.0]己-1-基)吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(20mg,0.047mmol)、2-羟基乙酸(4mg,0.052mmol)、hatu(20mg,0.052mmol)和n,n-二异丙基乙胺(25μl,0.142mmol)于dmf(0.5ml)中的混合物在室温下搅拌2小时。然后将混合物用mecn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
28h28
n5o3(m+h)
+
,lcms计算值:m/z=482.2;实验值482.4。
[2188]
实施例191b和实施例191c.1-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)-2-羟基乙-1-酮,将两种对映体
[2189][2190]
1-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)-2-羟基乙-1-酮的两种对映体用手性sfc(phenomenex cellulose-3,2
×
250mm,用40%meoh/co2洗脱,流动速率65ml/min)分离。实施例191b:峰1,tr=3.4min。实施例191c:峰2,tr=4.1min。对于c
28h28
n5o3(m+h)
+
,lcms计算值:m/z=482.2;实验值482.4。
[2191]
实施例192.(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基))((r)-4-甲基吗啉-3-基)甲酮
[2192][2193]
此化合物根据实施例191中所描述的程序,使用(r)-4-甲基吗啉-3-羧酸盐酸盐替代2-羟基乙酸来制备。对于c
32h35
n6o3(m+h)
+
,lc-ms计算值:m/z=551.3;实验值551.3。
[2194]
实施例193. 5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-3-(6-(3-(四氢-2h-吡喃-4-基)-3-氮杂双环[3.1.0]己-1-基)吡啶-3-基)-1h-吡唑并[4,3-b]吡啶
[2195][2196]
将3-(6-(3-氮杂双环[3.1.0]己-1-基)吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(20mg,0.047mmol)、四氢-4h-吡喃-4-酮(14mg,0.142mmol)和三乙酰氧基硼氢化钠(20mg,0.094mmol)于dcm(1ml)中的混合物在室温下搅拌20小时。此后,将溶液用tfa(0.5ml)淬灭。将混合物用mecn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
31h34
n5o2(m+h)
+
,lcms计算值:m/z=508.3;实验值508.4。
[2197]
实施例194a.2-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)乙-1-醇
[2198][2199]
将3-(6-(3-氮杂双环[3.1.0]己-1-基)吡啶-3-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(30mg,0.071mmol)、2-((叔丁基二甲基甲硅烷基)氧基)乙醛(37mg,0.213mmol)和三乙酰氧基硼氢化钠(30mg,0.142mmol)于dcm(1ml)中的混合物在室温下搅拌20小时。此后,将溶液用水稀释,并且用dcm萃取产物。将合并的有机层用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物溶解于dcm(1ml)中并添加tfa(1ml)。将混合物在室温下搅拌1h并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
28h30
n5o2(m+h)
+
,lcms计算值:m/z=468.2;实验值468.4。
[2200]
实施例194b和实施例194c.2-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)乙-1-醇,两种对映体
[2201][2202]
2-(1-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-3-氮杂双环[3.1.0]己-3-基)乙-1-醇的两种对映体用手性制备型hplc(phenomenex lux 5um cellulose-2,21.2
×
250mm,用30%etoh/己烷洗脱,流动速率20ml/min)分离。实施例194b:峰1,tr=14.4min。实施例194c:峰2,tr=16.1min。对于c
28h30
n5o2(m+h)
+
,lcms计算值:m/z=468.2;实验值468.4。
[2203]
实施例195. 3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-((r)-4-甲基吗啉-3-羰基)吡咯烷-3-甲腈
[2204][2205]
步骤1. 3-(5-溴吡啶-2-基)-3-氰基吡咯烷-1-羧酸叔丁酯
茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶
[2225][2226]
将5-(2,3-二氢-1h-茚-4-基)-3-碘-6-甲氧基-1h-吡唑并[4,3-b]吡啶-1-羧酸叔丁酯(150mg,0.305mmol)、1-(4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环-2-基)-1h-吡唑-1-基)-3-氮杂双环[3.1.0]己烷-3-羧酸叔丁酯(172mg,0.458mmol)、sphos pd g3(48mg,0.061mmol)和碳酸铯(298mg,0.916mmol)于二噁烷(2ml)和水(0.200ml)中的混合物在80℃下加热2小时。此后,将溶液冷却至室温,用水稀释,并用etoac萃取产物。将合并的有机层用饱和nacl水溶液洗涤并且经na2so4干燥,然后过滤并浓缩至干。然后将残余物溶解于dcm(3ml)中并添加tfa(2ml)。将溶液在室温下搅拌1h。然后去除溶剂并且将残余物通过硅胶色谱纯化以得到所需产物。对于c
24h25
n6o(m+h)
+
,lcms计算值:m/z=413.2;实验值:413.4
[2227]
步骤3. 1-(1-(4-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)-1h-吡唑-1-基)-3-氮杂双环[3.1.0]己-3-基)-2-羟基乙-1-酮
[2228]
将3-(1-(3-氮杂双环[3.1.0]己-1-基)-1h-吡唑-4-基)-5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶(10mg,0.024mmol)、2-羟基乙酸(2mg,0.024mmol)、hatu(14mg,0.036mmol)和n,n-二异丙基乙胺(9μl,0.048mmol)于dmf(0.5ml)中的混合物在室温下搅拌1小时。然后将混合物用mecn稀释并通过制备型lcms(xbridge c18柱,用乙腈/含有0.1%tfa的水的梯度洗脱,流动速率60ml/min)纯化。对于c
26h27
n6o3(m+h)
+
,lcms计算值:m/z=471.2;实验值471.2。
[2229]
实施例198. 3-(5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)-1-(2-羟基乙酰基)吡咯烷-3-甲腈
[2230][2231]
此化合物根据实施例195中所描述的程序,使用2-羟基乙酸替代(r)-4-甲基吗啉-3-羧酸盐酸盐来制备。对于c
28h27
n6o3(m+h)
+
,lc-ms计算值:m/z=495.2;实验值495.1。
[2232]
实施例199.(s)-4-((5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)甲基)-1,3-二甲基哌嗪-2-酮
[2233][2234]
此化合物根据实施例160中所描述的程序,使用(s)-1,3-二甲基哌嗪-2-酮替代哌啶-4-醇来制备。对于c
28h31
n6o2(m+h)
+
,lc-ms计算值:m/z=483.2;实验值483.2。
[2235]
实施例200.(1r,4r)-5-((5-(5-(2,3-二氢-1h-茚-4-基)-6-甲氧基-1h-吡唑并[4,3-b]吡啶-3-基)吡啶-2-基)甲基)-2-氧杂-5-氮杂双环[2.2.1]庚烷
[2236][2237]
此化合物根据实施例160中所描述的程序,使用(1r,4r)-2-氧杂-5-氮杂双环[2.2.1]庚烷替代哌啶-4-醇来制备。对于c
27h28
n5o2(m+h)
+
,lc-ms计算值:m/z=454.2;实验值454.4。
[2238]
实施例a
[2239]
fgfr酶法测定
[2240]
在使用fret测量值来测量肽磷酸化以检测产物形成的酶不连续测定中测定所例示化合物的抑制剂效能。抑制剂连续稀释于dmso中并将0.2μl体积转移至384孔板的孔中。将5μl/孔体积的稀释于测定缓冲液(50mm hepes、10mm mgcl2、1mm egta、0.01%tween-20、5mm dtt,ph 7.5)中的fgfr酶同工型(-1、-2、-3野生型和突变体同工型-4,包括磷酸化和未磷酸化蛋白)添加至板中并在环境温度下与抑制剂预孵育5至15分钟。适当的对照(酶空白和不具有抑制剂的酶)包括于板上。反应通过添加5μl/孔体积的含有生物素化eqedepegdyfewle肽底物(seq id no.1)和atp两者的测定缓冲液来启动。肽底物的10μl/孔反应浓度为500nm,而atp浓度保持在接近或低于atp km。atp km值在一系列单独实验中预测定。将反应板在25℃下孵育1小时并且反应通过添加5μl/孔的淬灭溶液(50mm tris、150mm nacl、0.5mg/ml bsa,ph 7.8;45mm edta、600nm星形孢菌素、3.75nm eu-抗体py20和180nm apc-链霉亲和素的perkin elmer lance试剂)来终止。使板在环境温度下平衡约10分钟,然后在pherastar读板器(bmg labtech)仪器上进行扫描。
[2241]
使用graphpad prism或xlfit来分析数据。通过使数据拟合至四参数逻辑方程,从而产生具有可变希尔系数的s型剂量-反应曲线来导出ic
50
值。prism方程:y=底部+(顶部-底部)/(1+10^((logic
50-x)*希尔斜率));xlfit方程:y=(a+((b-a)/(1+((x/c)^d)))),其中x是抑制剂浓度的对数并且y是反应。具有1μm或更小的ic
50
的化合物被认为是有活性的。
[2242]
使用graphpad prism3来分析数据。通过使数据拟合至针对具有可变斜率的s型剂量-反应的方程来导出ic
50
值。y=底部+(顶部-底部)/(1+10^((logic
50-x)*希尔斜率)),其
中x是浓度的对数并且y是反应。具有1μm或更小的ic
50
的化合物被认为是有活性的。
[2243]
表1提供了稀释于测定缓冲液中、添加至板并预孵育4小时之后在fgfr酶法测定中测定的本发明化合物的ic
50
数据。符号:“+”指示小于6nm的ic
50
;“++”指示大于或等于6nm但小于40nm的ic
50
;“+++”指示大于或等于40nm但小于100nm的ic
50
;并且“++++”指示大于或等于100nm的ic
50
。
[2244]
表1中的数据是在野生型未磷酸化fgfr1、fgfr2、fgfr3和fgfr4蛋白中量测的。
[2245]
表1
[2246]
[2247]
[2248]
[2249]
[2250][2251]
*空白条目未进行测试。
[2252]
还根据上文所述的方案评估了公开于us 2018/0072718中的化合物的fgfr3抑制活性。相应地,表2提供了针对us 2018/0072718的化合物的ic
50
数据。符号:“+”指示小于6nm的ic
50
;“++”指示大于或等于6nm但小于60nm的ic
50
;“+++”指示大于或等于60nm但小于200nm的ic
50
;并且“++++”指示大于或等于200nm的ic
50
。
[2253]
表2
[2254]
[2255][2256]
实施例b:发光活力测定
[2257]
从atcc(manassas,va)购买rt112细胞(细胞系和基因谱进一步详述于表3中)并维持在rpmi,10%fbs(gibco/life technologies)中。为了测量测试化合物对细胞活力的作用,将细胞在存在或不存在下50ul某一浓度范围的测试化合物的情况下用rpmi 10%fbs(5
×
103个细胞/孔/50μl)涂铺于黑色96孔greiner聚苯乙烯板中。3天后,添加100ul celltiter-glo试剂(promega)。用topcount(perkinelmer)读取发光。通过使用graphpad prism 5.0软件拟合百分比抑制对抑制剂浓度log的曲线来进行ic
50
测定。
[2258]
表3
[2259][2260]
*rt112 v555m:v555m突变是使用crispr介导的基因组编辑工程化的。
[2261]
**fgfr2-bicc1融合代表胆管癌中最流行的fgfr2改变
[2262]
实施例c:pfgfr2和pfgfr1,3功能性细胞htrf测定
[2263]
为了测量磷酸化成纤维细胞生长因子受体2(fgfr2),从atcc购买katoiii细胞(human gastric carcinoma)并维持在含有20%fbs的iscove氏培养基(gibco/life technologies)中。对于pfgfr2测定,katoiii细胞在5%fbs和iscove氏培养基中以5
×
104个细胞/孔涂铺在corning 96孔平底组织培养物处理板中过夜。第二天早上,将50μl含有0.5%fbs的新鲜培养基在37℃、5%co2下在存在或不存在另外50ul某一浓度范围的测试化合物的情况下孵育1小时。细胞用pbs洗涤,在室温下用含有标准蛋白酶抑制剂的cell signaling裂解缓冲液裂解45min。将总共4μl cis bio anti phospho-yap d2和cis bio anti phospho-yap cryptate一起添加至裂解物中并充分混合(按照试剂盒的说明)。然后将16μl转移至384孔greiner白板并在暗处在4℃下储存过夜。板在pherastar读板器上在665nm和620nm波长下读数。通过使用graphpad prism 5.0软件拟合抑制剂百分比抑制对抑制剂浓度log的曲线来进行ic
50
测定。
[2264]
为了测量磷酸化成纤维细胞生长因子受体3(fgfr3),将内部稳定细胞系baf3-tel-fgfr1或baf3-tel-fgfr3维持在含有10%fbs和1ug/ml嘌呤霉素的rpmi(gibco/life technologies)中。对于所述测定,将无血清和无嘌呤霉素rpmi培养基中的12nl baf3-tel-fgfr1或baf3-tel-fgfr3细胞以1
×
106个细胞/ml添加至已经含有20nl在某一浓度范围下的化合物点的384greiner白板。所述板在室温下轻柔地震荡(100rpm)持续2分钟以充分混合并在37℃、5%co2下在单层中孵育2小时。将4μl/孔的裂解缓冲液#3(cis bio)的1/25稀释液与标准蛋白酶抑制剂一起添加并在室温下以200rpm震荡持续20分钟。将总共4μl cis bio tb-pfgfr ab(10ng)和d2-fgfr3(1ng)添加至裂解物中并充分混合。将板密封并在室温
下在暗处孵育过夜。所述板在pherastar读板器上在665nm和620nm波长下读数。通过使用graphpad prism 5.0软件拟合抑制剂百分比抑制对抑制剂浓度log的曲线来进行ic
50
测定。
[2265]
实施例d:pfgfr3功能性全血htrf测定
[2266]
为了在全血测定中测量磷酸化成纤维细胞生长因子受体3(fgfr3),将内部稳定细胞系baf3-tel-fgfr3维持在含有10%fbs和1μg/ml嘌呤霉素的rpmi(gibco/life technologies)中。对于所述测定,将10%fbs和无嘌呤霉素rpmi培养基中的100ul baf3-tel-fgfr3细胞在37℃、5%co2下以5
×
104个细胞/孔添加至纤连蛋白包被的96孔组织培养板中(5ug/ml)过夜。第二天,通过低速旋转(1200rpm)从血液的顶部分离血清,并且通过在56℃下孵育15分钟进行热灭活。将30μl冷却的血清添加至预先点样有在某一浓度范围下的70nm化合物点的96孔板中。细胞板用培养基轻柔地洗涤,将所有血液/化合物混合物添加至板中,并将板在37℃、5%co2下孵育2小时。通过添加培养基至孔的侧面,然后倾倒板中的培养基,并且使板短暂地放置于纸巾上进行排干,来将板中的血液轻柔地洗涤两次。将70μl/孔的1x裂解缓冲液#1(cis bio)与标准蛋白酶抑制剂一起添加,并且在室温下以400rpm震荡30分钟。在裂解之后,将板离心5分钟并且将16ul裂解物转移至384孔小体积板中。将总共4μlcis bio tb-pfgfr ab(10ng)和d2-fgfr3(1ng)添加至裂解物中并充分混合。将板经密封并在室温下在暗处孵育过夜。板在pherastar读板器上在665nm和620nm波长下读数。通过使用graphpad prism 5.0软件拟合抑制剂百分比抑制对抑制剂浓度log的曲线来进行ic
50
测定。
[2267]
实施例e:katoiii全血pfgfr2αelisa测定
[2268]
为了在kato iii加标全血测定中测量酪氨酸磷酸化成纤维细胞生长因子受体2α(fgfr2α),从atcc购买kato iii细胞并维持在含有20%fbs的iscove氏培养基(gibco/life technologies)中。为了测量测试化合物的fgfr2α活性的抑制,将细胞以5
×
106个细胞/ml重悬于iscove氏,0.2%fbs中。然后将50μl细胞在存在或不存在某一浓度范围的测试化合物和300ul人肝素化全血(biological specialty corp,colmar pa)的情况下加标至96-深孔2ml聚丙烯测定块(costar)中。在37℃下4小时孵育之后,使用qiagen el缓冲液裂解红细胞并将细胞裂解物重悬于含有标准蛋白酶抑制剂混合物(calbiochem/emd)和pmsf(sigma)的裂解缓冲液(cell signaling)中在冰上持续30分钟。将裂解物转移至标准v型底丙烯组织培养板并在-80℃下冷冻过夜。在r&d systems duoset ic human phospho-fgf r2αelisa中测试样品并且使用设定至450nm并且波长校正为540的spectramax m5微孔板测量所述板。通过使用graphpad prism 5.0软件拟合抑制剂百分比抑制对抑制剂浓度log的曲线来进行ic
50
测定。
[2269]
实施例f:fgfr通路的抑制
[2270]
通过测量具有fgfr2/3改变的细胞系中的fgfr或fgfr下游效应子成纤维细胞生长因子受体底物2(frs2)和胞外-信号-调控激酶(erk)的磷酸化来测定化合物的细胞效能。
[2271]
为了测量磷酸化成纤维细胞生长因子受体、成纤维细胞生长因子受体底物2(frs2)和细胞外-信号-调控激酶(erk),将细胞(关于细胞系和所产生的数据的类型的详情进一步详述于表4中)于10%fbs和rpmi培养基中以5-7.5
×
105个细胞/孔进入corning 6孔组织培养物处理板中接种于6孔板中过夜。第二天早上,将2ml含有10%fbs的新鲜培养基在37℃、5%co2下在存在或不存在某一浓度范围的测试化合物的情况下孵育4小时。细胞用
pbs洗涤并用含有标准蛋白酶抑制剂的cell signaling裂解缓冲液裂解。使用以下抗体将20-40μg总蛋白裂解物应用于蛋白质印迹分析:来自r&d systems(minneapolis,mn))的磷酸化frs2 tyr436(af5126)、来自cell signaling technologies(danvers,ma))的磷酸化fgfr-tyr653/654(#2476s)、磷酸化erk1/2-thr202/tyr204(#9101l)和总erk1/2(#9102l)。
[2272]
表4
[2273][2274]
实施例g:具有fgfr2/3改变的体内肿瘤模型上的活性
[2275]
通过测量fgfr2/3改变模型中当用不同剂量的化合物处理时的肿瘤生长来测定化合物的体内活性。
[2276]
rt112/84肿瘤细胞(85061106,ecacc,uk)按照来源的建议进行维持(肿瘤模型进一步详述于表5中)。在实验的第0天,将2.0
×
106个rt112/84细胞用1:1pbs:matrigel(354263,corning)皮下接种至雌性nsg小鼠(jackson)的右后侧腹中。在肿瘤接种之后第7天,当肿瘤平均为约200mm3时,开始使用0(媒介物)、100mg/kg、30mg/kg或10mg/kg化合物的po qd治疗,并且继续直至研究结束。在实验的过程中,监测小鼠的肿瘤生长和明显耐受性。使用式(l
×
w2)/2计算肿瘤体积,其中l和w分别是指长度和宽度尺寸。使用式(1-(v
t
/vc))*100计算肿瘤生长抑制(tgi),其中v
t
是在治疗的最后一天治疗组的肿瘤体积,并且vc是在治疗的最后一天对照组的肿瘤体积。使用单因素anova来测定研究结束时在治疗组之间的统计学差异。
[2277]
表5
[2278][2279]
除了本文所述的那些以外,本领域技术人员还将由前述描述显而易见本发明的各种修改。此类修改也意图落入在所附加权利要求的范围内。本技术中所引用的每个参考文献,包括所有专利、专利申请和公布,均以引用的方式整体并入本文。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1