治疗实体瘤的方法和药剂与流程
治疗实体瘤的方法和药剂
1.相关事项
2.本技术要求2019年12月26日提交的美国临时专利申请第62/953,792号的优先权。这些申请的全部内容通过引用并入本文。
技术领域
3.本公开涉及用于治疗癌症的方法和药剂,更具体地,涉及使用减毒的鼠伤寒沙门氏菌治疗实体瘤癌症的方法和药剂。
背景技术:
4.尽管肿瘤治疗取得了很大进展,但癌症仍然是全球第二大常见死因。癌症治疗的主要支柱是化疗,其目的是使用具有可耐受副作用的最高剂量药剂来治愈或控制癌症。用于减少副作用的策略包括,例如,改变抗肿瘤剂的组合、节拍给药和将化学治疗剂直接递送至受影响的器官。在过去的几年中,癌症治疗的免疫疗法取得了进展,许多免疫药剂已在该领域显示出前景。然而,显着的毒性和肿瘤耐药性限制了这种治疗策略。
5.由于其固有的免疫刺激和癌症靶向特性,基于微生物的实体是癌症的潜在治疗方法。然而,迄今为止,许多动物研究和有限的人体试验的结果好坏参半。大多数研究都是在转移性疾病发生后很长一段时间内通过静脉注射进行细菌治疗,并且与显著的毒性有关,或者所给细菌不含任何免疫调节蛋白。
6.因此,希望提供一种用于癌症治疗的含有这种免疫调节蛋白的基于微生物的实体。还希望提供这样一种既无毒又能有效治疗癌症的治疗方法。
技术实现要素:
7.本公开涉及通过向受试者施用基本上由减毒鼠伤寒沙门氏菌组成的组合物和伴随的护理标准化疗来治疗受试者中的实体瘤癌症的方法和药剂。
8.在一个实施方式中,本公开提供了一种治疗实体瘤癌症的方法。该方法包括向有需要的受试者施用组合。该组合可包含单一化疗剂或两种或更多种化疗剂的组合,以及一定剂量的基本上由减毒的鼠伤寒沙门氏菌组成的组合物。
9.在另一个实施方式,本公开提供了一种治疗胰腺癌的方法。该方法包括向有需要的受试者施用组合。该组合可包含单一化疗剂或两种或多种化疗剂的组合,以及一定剂量的组合物,该组合物基本上由减毒鼠伤寒沙门氏菌组成,该减毒的鼠伤寒沙门氏菌含有携带编码截短的人白介素-2的编码序列的质粒。截短的人白介素-2由seq id no:2所示的氨基酸序列组成。在一些情况下,两种或更多种化疗剂的组合包括吉西他滨和卡培他滨。在其他情况下,两种或更多种化疗剂的组合包括亚叶酸、5-氟尿嘧啶、伊立替康和奥沙利铂。
10.在又一个实施方式中,本公开提供了一种治疗实体瘤癌症的方法。该方法包括向有需要的受试者施用组合。该组合可包含单一化疗剂或两种或多种化疗剂的组合,以及一定剂量的组合物,该组合物基本上由减毒鼠伤寒沙门氏菌组成,该减毒的鼠伤寒沙门氏菌
含有携带编码截短的人白介素-2的编码序列的质粒。截短的人白介素-2由seq id no:2所示的氨基酸序列组成。
11.在另一个实施方式中,本公开提供了一种用于治疗癌症的方法中的抗肿瘤剂。抗肿瘤剂包括可包含单一化疗剂或两种或更多种化疗剂的组合的组合,以及一定剂量的基本上由减毒鼠伤寒沙门氏菌组成的组合物,用于治疗实体瘤癌症。该方法包括向有需要的受试者施用该组合。
12.在又一个实施方式中,本公开提供了用于治疗癌症的方法中的抗肿瘤剂。抗肿瘤剂包括可包含单一化疗剂或两种或更多种化疗剂的组合的组合,以及一定剂量的组合物,该组合物基本上由减毒的鼠伤寒沙门氏菌组成,该减毒沙门氏菌含有携带编码截短的人白介素的编码序列的质粒-2。截短的人白介素-2由seq id no:2所示的氨基酸序列组成。该方法包括向有需要的受试者施用该组合。
附图说明
13.图1显示了含有编码人白介素-2蛋白的编码序列的pil2质粒,用于构建具有il-2基因的减毒鼠伤寒沙门氏菌(本文也称为“salpil2”)。
14.图2是根据各种实施方式的用减毒鼠伤寒沙门氏菌和至少两种化疗剂的组合治疗癌症的方法的流程图。
15.图3是显示口服施用salpil2五周后salpil2对血液淋巴细胞群的影响的条形图。
16.图4是显示患者1的ca 19-9水平与治疗周数的线形图。
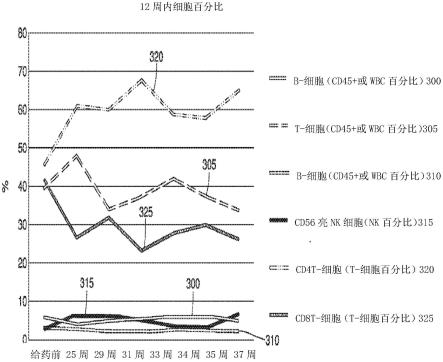
17.图5是显示不同细胞百分比对患者1治疗周数的线形图。
18.图6是显示cd56 bright nk细胞百分比与患者1治疗周数的线形图。
19.图7是显示患者1中ca 19-9水平从0到15个月的又一线形图(基于从最初诊断为转移性胰腺癌的时间)。
具体实施方式
20.以下详细描述在本质上是示例性的,且不希望以任何方式限制本公开的范围、适用性或配置。除非另有定义,本文使用的所有技术和科学术语与本发明所属领域的普通技术人员通常理解的含义相同。尽管在本发明或测试中可以使用与本文描述的那些相似或等效的方法和材料,但本文描述了合适的方法和材料。材料、方法和实施例仅是说明性的,而不是限制性的。本领域技术人员将认识到许多所述实施例具有各种合适的替代方案。本文所述的与分析化学、合成有机化学以及医药化学结合使用的命名法以及实验室程序和技术是本领域众所周知的和常用的。标准技术可用于化学合成、化学分析、药物制剂、配方和递送以及患者的治疗。
21.如在本文的描述和随后的权利要求中使用的,“一个(a)”、“一个(an)”和“该(the)”的含义包括复数引用,除非上下文另有明确规定。
22.如本文所用,“减毒”是指选择或改变细菌以大大降低其引起疾病的能力,但仍能够保持其定殖于肠道相关淋巴组织的能力。
23.如本文所用,“编码序列”和“编码区”可互换使用,是指编码蛋白质的多核苷酸,并且当置于适当调节序列的控制下时,表达编码的蛋白质。编码区的边界通常由其5'端的翻
译起始密码子和其3'端的翻译终止密码子确定。
24.如本文所用,“il-2”是指蛋白质人白介素-2。
25.如本文所用,“nk”或“nk细胞”是指自然杀伤细胞。
26.由于其固有的免疫刺激和癌症靶向特性,基于微生物的实体是癌症的潜在治疗方法。重要的是,其中一些基于微生物的选择的副作用似乎远远优于细胞毒性化疗和免疫疗法。然而,迄今为止,动物研究和有限的人体试验的结果参差不齐,尽管大多数研究都是在转移性疾病发生很久之后,通过静脉注射进行细菌治疗,并且与显著的毒性有关,或者给药的细菌不含任何免疫调节蛋白。
27.减毒的鼠伤寒沙门氏菌已被开发为将治疗药剂递送至肿瘤的载体。鼠伤寒沙门氏菌的潜力主要是由于据报道其在肿瘤中积累的浓度比健康组织高1000倍以上。此外,鼠伤寒沙门氏菌的基因可操作性允许外源重组蛋白的表达,使这些细菌成为一种有效的递送系统,用于输送全身给药时可能有毒的蛋白质。
28.鼠伤寒沙门氏菌(s.typhimurium)已显示优先定殖于实体瘤。特别是,它感染和定殖实体瘤,并在细胞内感染细胞后刺激细胞免疫反应。因此,它被认为是一种将免疫调节蛋白直接递送至肿瘤微环境的极其有效的方法。例如,已经证明鼠伤寒沙门氏菌在实体瘤中的积累比例(1000:1到10000:1)远高于感染期间沙门氏菌定植的“天然”目标生物,即肝脏和脾。
29.白细胞介素-2(il-2)是人体自然产生的一种蛋白质,可促进淋巴细胞增殖,增强t细胞和自然杀伤(nk)细胞的溶细胞功能。因此,它能够刺激免疫系统产生破坏癌症的白细胞。在某些类型的癌症中,基于il-2的免疫疗法已经研究了多年,但成果有限。由seq id no:4编码的正常人il-2蛋白(编码正常人il-2的dna序列)的氨基酸序列(seq id no:3)在美国专利申请序列号第13/524,503号的图3上示出,其作为美国专利第8,647,618号公布,其为2009年4月17日提交的美国专利申请序列号第12/425,927号的延续,其作为美国专利第8,221,739号公布,其为美2004年4月29日提交的美国专利序列号第10/834,587号的部分延续并要求其优先权,现已放弃,每个申请的内容均通过引用整体并入本文。
30.虽然il-2是由人体自然产生的,但要使其发挥最大效力,需要更高的浓度和更特异的递送载体至疾病位点。然而,发现高剂量的il-2在许多患者中会导致严重的毒性。解决这个问题的方法是使用一种活的鼠伤寒沙门氏菌菌株,这种菌株被减毒以大大降低其引起疾病的能力。使用鼠伤寒沙门氏菌是因为它具有定殖肠道相关淋巴组织(galt)、肝脏和脾脏的天然能力。减毒的鼠伤寒沙门氏菌对肝脏的定植进一步引发了针对细菌的普遍细胞反应,或者可以作为携带者状态持续存在。本公开中使用的鼠伤寒沙门氏菌的χ4550菌株含有通过用tn10进行转座子诱变然后选择呋喃甲酸抗性而构建的基因缺失。这种遗传改变方法导致tn10和相邻dna序列的缺失,从而产生天冬氨酸半醛脱氢酶(asd)的缺失。这种突变需要二氨基庚二酸。这些细菌中缺乏asd酶导致无法构建稳定的细胞壁,从而导致鼠伤寒沙门氏菌的致死性裂解。因此,为确保所需蛋白质的稳定表达,构建了携带asd基因的质粒(pya292)。
31.图1显示了含有编码人白细胞介素2蛋白的编码序列的pil2质粒,用于构建具有il-2基因的减毒鼠伤寒沙门氏菌salpil2。为了确保鼠伤寒沙门氏菌菌株的无毒力,采用小鼠毒性鼠伤寒沙门氏菌sr-11菌株χ3306的标准p22噬菌体转导构建缺乏合成腺苷酸环化酶
和camp受体蛋白(crp)能力的χ4550菌株。环状amp和camp受体蛋白对于许多与分解代谢物的运输和分解有关的基因和操纵子的转录是必需的。尽管在哺乳动物组织中发现了camp,理论上细菌可以利用camp来增加毒力的潜力,但camp受体蛋白的缺乏应该消除这些突变细菌摄取camp可能产生的任何益处。
32.使用众所周知的方法将编码截短的人il-2蛋白、优化用于在大肠杆菌中表达的合成cdna(seq id no:5)插入质粒pya292中。截短的cdna(seq id no:1)是合成il-2核苷酸序列(seq id no:5)的一部分。该序列比旨在编码全长成熟人il-2蛋白的序列少一个核苷酸。如本文所用,“成熟”是指缺乏起始(n-末端)20个氨基酸信号序列的蛋白质,当该分子从人体细胞分泌时该信号序列被切割掉。发生的突变是272位的“a”和273位的“g”之间的“t”核苷酸缺失。这导致在274位截断所得il-2蛋白的框内taa终止密码子。得到的dna核苷酸序列是seq id no:1,表达的蛋白质是seq id no:2。
33.用限制性内切酶ecori(威斯康星州麦迪逊普洛麦格公司)和hindiii(马萨诸塞州贝利弗新英格兰生物实验室)完全消化天冬氨酸半醛脱氢酶(asd+)载体和合成的截短的人il-2cdna。pya292的约3.4kb线性化载体片段和il-2基因的ecori-hindiii片段在琼脂糖凝胶电泳后使用prepagene试剂盒(加利福尼亚州大力神伯乐公司)分离。使用t4 dna连接酶(威斯康星州麦迪逊普洛麦格公司)将il-2基因片段连接到pya292载体中,插入物摩尔过量为3:1,并在16℃下孵育4小时。然后将连接混合物电穿孔到减毒鼠伤寒沙门氏菌的χ4550菌株中。鼠伤寒沙门氏菌,δcya-1δcrp-1δasda1菌株χ4550在含有50mg/ml二氨基庚二酸(dap)的lb培养基(密苏里州圣路易斯西格玛)中生长。
34.培养物在od
600
(大约108菌落形成单位(cfu)/ml的肉汤)下生长至吸光度为0.200,并准备细胞用于电穿孔。使用具有0.2cm一次性比色皿的电穿孔装置(伯乐公司)将质粒载体pya292和连接混合物电穿孔到χ4550中。细胞在2.5kv和25μf下使用200ohms的脉冲控制器进行脉冲处理。随后将细胞置于不含dap的luria琼脂上,并使用magic mini-prep dna纯化系统(普洛麦格公司)鉴定重组克隆,并用ecori和hindiii进行限制性内切酶消化,并用1.2琼脂糖进行凝胶电泳。限制性内切酶图谱显示,pya292中插入il-2片段的质粒与预期的质粒相对应,该质粒更名为pil2。新的转化子被重命名为χ4550(pil2),在本文中也称为“salpil2”35.用质粒(pil2)转化asd缺失的菌株可以稳定表达il-2。如上所述,由于此处使用的特定鼠伤寒沙门氏菌菌株(χ4550)缺乏天冬氨酸半醛脱氢酶(asd),因此该载体的稳定性得以维持,而含有il-2基因(pil2)的质粒则含有该酶。缺乏asd的细菌不能制造二氨基庚二酸(dap),它是细菌细胞壁的重要成分,因此不会长期存活。因此,如果减毒的鼠伤寒沙门氏菌试图恢复其野生型菌株并失去质粒,它将死于“无dap”的死亡。因为含有il-2的质粒的丢失也会导致编码asd的质粒的丢失,所以实现了il-2基因的稳定表达。
36.图2是方法200的流程图。方法200涉及根据各种实施方式用减毒的鼠伤寒沙门氏菌和单一化疗剂的组合或两种或更多种化疗剂的组合治疗癌症的方法。在方法200中治疗的癌症可以是任何实体瘤癌症,包括但不限于肝癌、肺癌、胰腺癌、乳腺癌、前列腺癌、皮肤癌、肾癌、骨癌、胃肠癌、癌症软组织(例如,肌肉癌)、肾上腺癌、结肠癌和膀胱癌。在某些示例性实施方式中,所治疗的癌症是胰腺癌。在本公开的任何实施方式中,所治疗的癌症可以是转移性或非转移性癌症并且可以任选地是难治性癌症。
37.方法200包括向有需要的受试者施用组合治疗。组合治疗可以包括向受试者施用第一剂量的减毒鼠伤寒沙门氏菌和第一剂量的单一化疗剂(或两种或更多种化疗剂的组合)的步骤201。在一些实施方式中,受试者是哺乳动物。在本公开的任何实施方式中,哺乳动物可以是人。
38.方法200可以包括向受试者施用单剂量的组合(即,仅向受试者施用第一剂量的减毒鼠伤寒沙门氏菌和第一剂量的单一化疗剂,或两种或更多种化疗剂的组合)。或者,方法200可涉及在特定时间段内(例如,在数周的时间段内,例如每两周、每三周、每四周等)向同一受试者施用多个剂量。例如,方法200可以包括以下步骤中的任何一个或多个:施用第二剂量的减毒鼠伤寒沙门氏菌(202);施用第二剂量单一化疗剂或两种或多种化疗剂的组合(203);施用第三剂量减毒的鼠伤寒沙门氏菌(204);以及施用第三剂量单一化疗剂或两种或更多种化疗剂的组合(205)。施用第二剂量的减毒鼠伤寒沙门氏菌(202)和施用第二剂量的单一化疗剂或两种或更多种化疗剂的组合(203)的步骤可以在同一天发生,或者这种治疗可以错开(这样这些步骤发生在不同的日子)。类似地,施用第三剂量的减毒鼠伤寒沙门氏菌(204)和施用第三剂量的单一化疗剂或两种或更多种化疗剂的组合(205)的步骤可以在同一天发生,或者这样的治疗可以错开(这样这些步骤发生在不同的日子)。
39.如上所述,方法200不需要包括图2所示的所有步骤。例如,在一些实施方式中,方法200可以排除施用第二剂减毒鼠伤寒沙门氏菌(202)和施用第三剂减毒鼠伤寒沙门氏菌(204)的步骤。此外,方法200可以包括额外的步骤,诸如施用第四剂减毒的鼠伤寒沙门氏菌和/或施用第四剂量的单一化疗剂或两种或更多种化疗剂的组合。另外或替代地,方法200可以排除施用第二剂量的单一化疗剂或两种或更多种化疗剂的组合的步骤(203);并且可以排除施用第三剂量的单一化疗剂或两种或更多种化疗剂的组合的步骤(205)。
40.方法200中减毒的鼠伤寒沙门氏菌和单一化疗剂(或两种或更多种化疗剂的组合)的剂量数量可以根据特定患者、所治疗癌症的类型和患者对先前剂量的反应而变化。
41.每剂量的鼠伤寒沙门氏菌都可以是基本上由减毒的鼠伤寒沙门氏菌组成的组合物的一部分。在一些这样的情况下,减毒的鼠伤寒沙门氏菌的剂量含有携带编码截短的人白细胞介素2的编码序列的质粒,其中截短的人白细胞介素2由seq id no:2中所示的氨基酸序列组成。因此,在这种情况下,鼠伤寒沙门氏菌减毒菌株已被工程化为携带人类il-2基因,从而在肿瘤微环境中赋予免疫介导的肿瘤细胞杀伤。
42.在一些实施方式中,施用的减毒鼠伤寒沙门氏菌的剂量(在方法200的步骤期间)可以是103至10
12
菌落形成单位(例如,106至10
11
菌落形成单位,或105至10
10
菌落形成单位)。然而,并非所有实施方式都需要这样的剂量,并且还考虑了可替代的鼠伤寒沙门氏菌剂量。
43.在某些实施方式中,施用每一剂量减毒的鼠伤寒沙门氏菌可以包括口服施用减毒的鼠伤寒沙门氏菌。通过口服沙门氏菌-il2,可以避免与革兰氏阴性菌本身相关的全身毒性。在一个实施方式中,施用一剂减毒的鼠伤寒沙门氏菌包括施用105至10
10
菌落形成单位的口服剂量的salpil2。
44.在某些实施方式中,单一化疗剂或两种或更多种化疗剂的组合通过静脉内或口服给药。然而,本领域技术人员将理解任何合适的给药途径可用于给药方法200的化疗剂。
45.在一些实施方式中,施用一剂单一化疗剂或两种或更多种化疗剂的组合包括施用吉西他滨和卡培他滨。在其他实施方式中,施用一剂单一化疗剂或两种或更多种化疗剂的
组合包括施用亚叶酸、5-氟尿嘧啶、伊立替康和奥沙利铂中的两种或更多种(在一些情况下,每种)。亚叶酸、5-氟尿嘧啶、伊立替康和奥沙利铂各自的组合通常称为“folfirinox”。在其他实施方式中,至少两种化疗剂可以包括两种或更多种本文未具体列举的化疗剂。
46.方法200是有利的,因为该组合允许使用较低且毒性较小的化疗剂剂量。这提供了有效的治疗,同时最大限度地减少了由化疗剂的毒性引起的副作用。
47.本公开的某些实施方式提供了用于治疗癌症的方法中的抗肿瘤剂。在一些情况下,抗肿瘤剂可用于上述方法200。
48.实施例
49.安全性研究
50.这项研究是一项剂量递增研究,以确定施用salpil2的安全性。组织学证实实体瘤转移至肝脏且无有效治疗方法的患者被纳入该研究。
51.给药前,给每位患者立即口服30ml的美乐事或胃能达中和胃酸。然后,口服给药单剂量的salpil2。通过在30ml盐水中稀释解冻的甘油原液来制备剂量。在施用salpil2的所述剂量后,立即给每位患者口服200ml生理盐水,然后至少一小时内不口服任何东西。
52.计划的剂量递增从105菌落形成单位的细菌开始,增加一个数量级,直到最大剂量为10
10
菌落形成单位,同时监测剂量限制毒性(dlt)。不良事件报告的描述和分级量表采用了修订后的美国国家癌症研究所通用毒性标准(ctc)3.0版指南。dlt被定义为脓毒症综合征、4级呕吐或腹泻或其他3级毒性。计划在给药后11周进行密切随访,每月入组一至两名患者。
53.使用实体瘤临床疗效评价标准(recist)委员会标准评估患有可测量疾病的患者的反应和进展。除了不良事件监测外,还对外周血样本进行流式细胞术以观察免疫细胞亚群以确定研究生物药剂的免疫效应。
54.结果和结论
55.总共入组了22名患者并被施用了salpil2。8名患者未完成试验,如下表1所示。没有不良事件被判断为可能或肯定是由于研究入组。研究生物体的所有血液和粪便培养物均呈阴性。
56.表1:入组和研究完成
[0057][0058]
总体而言,与给药后5周相比,研究前访视时检测的血清化学和全血细胞计数之间没有统计学上的显着差异(n=14)。比较低剂量(105)与高剂量(10
10
)队列,研究前和给药后
5周之间血小板计数的平均变化略有不同(+58,500+/-86,720与-40,667+/-356,978/ml,p=0.046),但在测试的实验室值中没有其他统计学上的显着差异。
[0059]
图3是条形图,显示了对所有给药剂量在给药前采集的样品与在口服给药后5周采集的样品进行比较。如图3所示,给药后样本显示外周血nk细胞百分比(平均值=12.1vs 14.6%,p=0.02)和nk t细胞(平均值=3.4vs 5.6%,p=0.02)有统计学意义的增加,但没有统计学意义测量的其他细胞群的显着差异。每个剂量组的给药后5周样本的患者数量为6(105cfu)、2(106cfu)、2(107cfu)、1(108cfu)、1(109cfu)、和2(10
10
cfu)。
[0060]
在这项i期研究中证明单次口服沙门氏菌-il2没有毒性和免疫反应之后,加拿大卫生部批准了一项=1试验,用于沙门氏菌-il2的多剂量试验和辅助化疗患有转移性胰腺癌4期的患者(在整个本公开内容中被称为“患者1”)。salpil2每两周通过标准护理化疗施用于患者1。现在,在诊断后11个月,患者1对salpil2没有任何毒性并继续她的治疗,她的碳水化合物抗原(ca)19-9值已正常化,通过荧光激活细胞分选(facs)分析显示出强烈的nk反应,并证明了转移性肿瘤负荷的放射学消退。
[0061]
这项i期剂量递增研究的结果表明,含有人il-2基因(salpil2)的口服减毒鼠伤寒沙门氏菌表现出免疫反应,并且在高达10
10
cfu的剂量下没有引起明显的毒性。以前使用减毒沙门氏菌或其他细菌的研究没有这项研究那么有希望。一项对转移性黑色素瘤患者使用vnp20009的试验未证明生存效率,并显示静脉注射细菌的毒性。同样,最近一份关于随机接受化疗或李斯特菌疫苗的转移性胰腺癌患者的iib期研究报告并未显示生存差异。
[0062]
案例分析
[0063]
一位患有转移性胰腺癌的患者(以下简称“患者1”)单独寻求在她的标准护理化疗之外接受salpil2的可能性。
[0064]
患者1是一名70岁的女性,既往有高胆固醇血症病史,并有数周的腹痛和腹胀病史。患者1的检查最终发现胰腺尾部有一个3.9x5.7厘米的肿块,侵入了脾门和左肾上腺。此外,患者1的肺部和肝脏中存在多个转移性结节。随后的细针抽吸和活检证实了4期胰腺导管腺癌的诊断。患者1立即开始接受亚叶酸、5-氟尿嘧啶、伊立替康和奥沙利铂的folfirinox方案,每两周给药一次。患者1很清楚她的中位生存期为11.1个月的预后,因此寻求在她的治疗方案中添加salpil2的可能性。因此,在开始化疗方案五个月后,在收到加拿大卫生部对n=1的研究性新药申请的批准以及犹太总医院研究伦理委员会(reb)加拿大魁北克省蒙特利尔麦吉尔大学医学研究院的批准后,患者1开始每两周同时口服salpil2六剂。如果注意到反应,治疗肿瘤学家可以选择无限期地每两周继续给药salpil2。为了评估患者1的反应并监测潜在毒性,与她的肿瘤医生安排的就诊包括以下内容:ca19-9评估、全血计数、综合代谢小组、胸部和腹部定期mri,以及为流式细胞术分析抽取的血液,发送至明尼苏达州奥克代尔市医学博士。
[0065]
确诊后,患者1的ca19-9水平显着升高,并且在5个月内对folfirinox有阳性反应,ca19-9水平稳定在75-100ku/l一个月(见图4和7)。此外,到第6个月,患者1开始遭受奥沙利铂的严重神经毒性,表现为她的手脚都没有感觉。因此,停止向患者1施用奥沙利铂。在第5个月,salpil2被添加到患者1的治疗方案中,到第6个月,她的ca19-9水平正常化并在过去11个月内保持在正常范围内。此外,定期磁共振成像显示原发性胰腺肿块的大小从5.4x3.4 cm整体减小到4.9x2.2 cm。此外,肝转移瘤的大小从平均最大直径1.7cm减少到1.1cm。mri
还显示肝脏或其他任何地方没有新的转移性病变,这些转移性沉积物的信号强度明显低于患者最初出现时的信号强度。最后,在全身化疗给药前每两周进行的外周血流式细胞术分析表明,与基线相比,cd56
明亮
nk细胞(315)显着增加(图5和6)。cd4 t细胞(320)也显示出显着增加。然而,也如图5所示,尽管进行了细胞毒性化疗,但患者1的其他主要细胞群没有减少,包括b细胞(300)、t细胞(305)、nkt细胞310和cd8 t细胞(325)。此外,虽然在诊断时没有获得pet扫描,但在第14个月获得的扫描并未显示转移性肿瘤沉积物中的任何代谢活动(即,通过pet扫描显示完全没有肿瘤活动)。
[0066]
患者1未报告salpil2的任何不良反应。也就是说,患者没有任何发烧、腹泻、恶心或呕吐。迄今为止,每两周对患者进行的所有粪便培养都对沙门氏菌呈阴性,包括大约在第48周腹泻发作后获得的粪便培养物。
[0067]
通常情况下,使用folfirinox治疗转移性胰腺癌表现出大约6到8个月的治疗反应,然后大多数患者的疾病出现显着进展,中位生存期为11.1个月。在这种情况下,尽管由于神经毒性副作用而消除了奥沙利铂(oxaloplatin),但现在到第15个月,患者仍然感觉良好,并且积极参与日常生活活动。此外,鉴于在她的ca19-9水平和放射学反应中看到的这种反应,决定无限期地继续使用salpil2。
[0068]
结果与讨论
[0069]
i期剂量递增研究的结果表明,单次口服salpil2剂量高达10
10
菌落形成单位的剂量时没有引起明显的毒性。最常见的不良事件包括腹部或侧面疼痛、虚弱和稀便。部分患者出现自限性腹泻。然而,在任何患者的粪便中都没有培养出沙门氏菌。外周血化学和具有白细胞差异的cbc显示给药前和给药后时间段之间没有显着差异。低剂量组和高剂量组之间血小板计数变化略有差异的原因并不明显。尽管在研究期间没有患者出现临床反应,但所有患者在入组前已经患有明显的转移性疾病。
[0070]
外周血的流式细胞仪分析显示,在研究前与给药后5周相比,循环nk细胞和nk t细胞的百分比显着增加。这些发现不是剂量依赖性的,并且与先前的临床前研究一致,这些研究显示口服salpil2后全身nk细胞活化增加,这可能解释了该疗法在降低狗肺转移性骨肉瘤比率方面的效果(该器官通常与鼠伤寒沙门氏菌浸润无关)。
[0071]
此外,与该案例研究相关的本公开部分概述salpil2在患有转移性胰腺癌的患者(患者1)中的多次给药策略中的首次使用。临床前研究证明了salpil2和阿霉素之间的协同作用,并且已经提出了这种协同作用的各种机制。患者1表现出cd56
亮
nk细胞显着增加,这些细胞已被证明是浸润某些癌症的主要亚群之一,并且在细胞因子刺激该细胞系后,可以显着分化为高细胞毒性nk细胞。
[0072]
尽管不得不停止化疗策略的一个组成部分,即奥沙利铂(oxaloplatin),但患者1在临床和放射学上表现出重大反应。此外,流式细胞术显示,尽管进行了细胞毒性化疗,免疫细胞群仍得以维持。有了这些令人鼓舞的结果,将启动一项针对多达60名转移性胰腺癌患者的沙门氏菌-il2扩大的多剂量ii期试验。
[0073]
当在体外研究各种癌细胞系时,发现与肝癌、神经母细胞瘤、腺癌和骨肉瘤相比,沙门氏菌-il2最容易侵入肝细胞。然而,在检查分裂效率(即一旦发生定植后在肿瘤中分裂的能力)时,骨肉瘤和神经母细胞瘤的分裂效率最高。
[0074]
此外,体内实验表明,口服沙门氏菌-il2可以稳定地定植多种肿瘤类型。因为沙门
氏菌可以定殖实体瘤,申请人认为沙门氏菌-il2可以通过侵入和局部释放il-2到肿瘤微环境中来充当“智能炸弹”,同时避免来自il-2的任何全身毒性。
[0075]
尽管已经描述了本公开的一些优选实施方式,但是应当理解,在不脱离本发明的精神和所附权利要求的范围的情况下,可以在其中进行各种改变、调整和修改。
[0076]
序列
[0077]
截短的白细胞介素-2(智人)的dna序列(seq id no:1)
[0078][0079]
截短的白细胞介素-2(智人)的蛋白质序列(seq id no:2)
[0080]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1