用于减少局部脂肪的气体发泡型胶束的制作方法
1.本发明涉及用于减少局部脂肪的气体发泡型胶束。
背景技术:
2.存在于皮肤的表皮和真皮下方的皮下脂肪的减少为美容处理的最重要的领域中之一,为了这种美容处理的目的,使用多种手术方法。
3.用于减少皮下脂肪的手术有将插管(cannula)插入于皮下脂肪来吸入脂肪的吸脂术、将冷却垫附着于皮肤表面来使皮下脂肪冷却坏死的冷冻手术、向皮下脂肪组织照射高频或超声波,通过加热去除皮下脂肪的加热手术、利用注射针头向皮下脂肪慢慢注入二氧化碳(co2)来促进脂肪组织的血液循环及淋巴循环,以去除脂肪的羧基疗法(carboxytherapy)手术、向皮下脂肪注入肥胖治疗用药物的美塑疗法(mesotherapy)手术等。
4.被熟知手术中效果最高的吸脂术在手术时伴随的痛苦及往后管理方面存在缺点。代表性地,吸脂时会出血,手术时伴随疼痛。手术之后,也引起疼痛,根据各人还产生需要服用镇痛剂的情况。与此同时,吸入手术之后,需要穿弹力衣一周以上,手术之后需要管理一个月左右。
5.并且,冷冻手术虽然手术简便,但存在手术效果低的缺点。在韩国公开专利第10-2011-0119640号中使用使制冷剂循环到内部,将冷却的探针插入于皮下脂肪的侵袭性手术。但是,当使用侵袭性冷却手术时,手术时间相比于非侵袭性冷却手术缩短,但存在需要相当长的手术时间,以防止冷却引起的皮下脂肪的坏死的缺点。
6.另一方面,羧基疗法为集中治疗脂肪过度堆积的部位的手术,在韩国授权专利第10-0772961中均执行美塑疗法手术和羧基疗法手术,以提高脂肪去除效率。但是,上述专利中对各个手术使用单独的注射器针头,存在内部结构复杂,各个针头导致产生单独的切口的缺点。
7.当前,获得食品医药品安全厅的批准的局部脂肪分解补充剂的用途非常受限,当前,市场上频繁施行标签外手术。这种标签外手术对安全性及有效性的根据不足,是非受医疗保险区,因而处于安全使用管理的盲区,制度管理不足。
8.作为脂肪分解补充剂获得批准的药物有通过破坏局部脂肪细胞的细胞膜,使脂肪细胞凋亡的倍克脂。但是,倍克脂存在只可有限地利用于双下巴手术的缺点。并且,据报告,这种药物非特异性地破坏细胞膜,因而对包括脂肪细胞在内的周边细胞的影响大,有可能对周边组织产生副作用,因而当前乳腺癌或大肠癌的危险性增加。
技术实现要素:
9.技术问题
10.本发明提供可制作成可注射的制剂,分解局部脂肪的局部脂肪分解补充剂或减肥美容产品,以解决上述的问题。
11.解决问题的方案
12.本发明提供用于减少脂肪的气体发泡型胶束,上述用于减少脂肪的气体发泡型胶束包含由以下化学式1表示的化合物,利用通过上述化合物的水解产生的二氧化碳破坏脂肪细胞。
13.化学式1
[0014][0015]
在上述化学式1中,
[0016]
p为12至227的整数,
[0017]
q为2至14的整数,
[0018]
n为0至5的整数,
[0019]
l为脂肪细胞靶序列(ats)肽或r9(精氨酸(arginine))肽。
[0020]
本发明还提供用于减少脂肪的气体发泡型胶束的制备方法,上述用于减少脂肪的气体发泡型胶束包含由以下化学式1表示的化合物,上述用于减少脂肪的气体发泡型胶束的制备方法包括:
[0021]
混合聚乙二醇(polyethylene glycol)及氯甲酸烷基酯(alkyl chl oroformate)来合成作为由化学式4表示的化合物的聚乙二醇衍生物的步骤;
[0022]
在上述聚乙二醇衍生物中结合选自由脂肪细胞靶序列(ats)肽及r9(精氨酸)肽组成的组中的一种以上的肽来合成结合有肽的聚乙二醇衍生物的步骤;以及
[0023]
使上述聚乙二醇衍生物及结合有上述肽的聚乙二醇衍生物溶解于选自乙腈、二氯甲烷、氯仿及甲醇中的一种或两种以上的混合溶剂之后,使溶剂蒸发来合成胶束的步骤。
[0024]
化学式4
[0025][0026]
化学式1
[0027][0028]
在上述化学式1或4中,
[0029]
r1为氢、c1至5的烷基、胺基、c1至5的烷基胺基、羧基或c1至5的烷基羧基,
[0030]
p为12至227的整数,
[0031]
q为2至14的整数,
[0032]
n为0至3的整数,
[0033]
l为脂肪细胞靶序列(ats)肽或r9(精氨酸)肽。
[0034]
本发明还提供包含上述的用于减少脂肪的气体发泡型胶束的用于减少脂肪的组
合物。
[0035]
发明的效果
[0036]
本发明的用于减少脂肪的气体发泡型胶束可局部给药,浸渍于脂肪细胞部位来产生二氧化碳,以可通过脂肪细胞的凋亡分解脂肪。尤其,在本发明中,可使用配体(肽)靶向脂肪细胞,因而可将对周边组织及细胞的影响最小化,由此可将对药物的副作用最小化,可开发可实现更安全的手术的产品。上述胶束通常可适用于手术频率高的下巴、大腿、手臂、腹部等部位。
[0037]
并且,本发明的用于减少脂肪的气体发泡型胶束可制作成可注射的制剂,适用于减肥美容领域及肥胖治疗剂领域,可用作通过局部脂肪的凋亡分解局部脂肪的局部脂肪分解补充剂、体型矫正剂或减肥美容产品等。
附图说明
[0038]
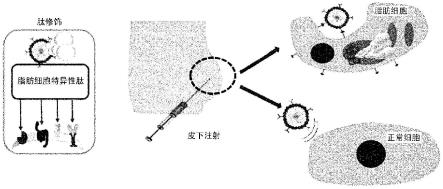
图1为表示本发明一例的气体发泡型胶束在脂肪细胞中的堆积及通过气体发泡的脂肪减少的示意图。
[0039]
图2为表示聚乙二醇碳酸烷基酯和肽的结合的示意图。
[0040]
图3为表示本发明一例的气体发泡型胶束的制备工序的示意图。
[0041]
图4为根据本发明的一例制备的胶束中产生的气泡(气体)的照片。
[0042]
图5为利用傅里叶变换红外(ft-ir)分析根据本发明的一例制备的聚乙二醇碳酸烷基酯的曲线图。
[0043]
图6为利用ft-ir分析根据本发明的一例制备的导入有肽的聚乙二醇碳酸烷基酯的曲线图。
[0044]
图7为表示通过核磁共振(nmr)确认根据本发明的一例制备的导入有肽的聚乙二醇碳酸烷基酯的气体的产生的结果的曲线图。
[0045]
图8为表示根据本发明的一例制备的聚乙二醇碳酸烷基酯的气体产生速度的测定结果的照片。
[0046]
图9为测定从根据本发明的一例制备的聚乙二醇碳酸烷基酯的气体产生的光学显微镜图像。
[0047]
图10为表示根据本发明的一例制备的聚乙二醇碳酸烷基酯的细胞毒性评价结果的图表。
[0048]
图11为表示根据肽导入量的根据本发明的一例制备的气体发泡型胶束的脂肪细胞凋亡效果评价结果的图表。
[0049]
图12为表示根据胶束浓度及肽组合的脂肪细胞凋亡效果评价结果的图表。
[0050]
图13为表示除了根据本发明的一例制备的气体发泡型胶束的脂肪细胞之外的细胞凋亡效果评价结果的图表。
具体实施方式
[0051]
实施本发明的最佳方式
[0052]
本发明涉及用于减少脂肪的气体发泡型胶束,上述用于减少脂肪的气体发泡型胶束包含由以下化学式1表示的化合物,利用通过上述化合物的水解产生的二氧化碳破坏脂
肪细胞。
[0053]
化学式1
[0054][0055]
在本发明中,利用生物亲和性高的材料形成胶束,并且通过向胶束的表面导入肽,即,细胞靶配体,可将向除了脂肪细胞之外的周边细胞及组织的传递最小化,将向脂肪细胞内的传递最大化。由此,可利用为将现有产品的副作用最小化的脂肪分解补充剂。并且,利用对人体无害的气体(如二氧化碳)诱导细胞打击,因而相比于其他化学药品材料,可改善安全性。
[0056]
以下,更详细说明本发明的用于减少脂肪的气体发泡型胶束。
[0057]
本发明的用于减少脂肪的气体发泡型胶束(以下,由气体发泡型胶束或胶束表示)包含由以下化学式1表示的化合物(以下,由化学式1的化合物表示)。
[0058]
化学式1
[0059][0060]
在上述化学式1中,
[0061]
p可以为12至227的整数,
[0062]
q可以为2至14的整数,
[0063]
n可以为0至5的整数,
[0064]
l可以为脂肪细胞靶序列(ats)肽或r9(精氨酸)肽。
[0065]
在一具体例中,q可以为4至10的整数、4至8的整数、6至10的整数或8至10的整数,n可以为1至3的整数。
[0066]
在一具体例中,上述化学式1的化合物的分子量可以为550至10000da(g/mol)、1000至10000da、2000至6000da、1500至3000da、2000至2500da、4500至6000da或5000至5500da。
[0067]
在一具体例中,上述胶束的直径可以为150至500nm或200至400nm。当直径小时,无法得到所需的脂肪细胞凋亡效果,当直径过大时,不适合适用于体内注入,因而优选地,将直径调节在上述范围内。
[0068]
在本发明中,术语“胶束(micelle)”通常意味着同时具有两亲性,例如亲水基团和疏水基团的低分子量的物质所形成的球形结构的化合物。上述胶束具有热力学上稳定的特性。当在具有上述胶束结构的化合物中溶解非水溶性(疏水性)药物来投入时,上述药物存在于胶束内部。
[0069]
本发明的胶束包含氯甲酸烷基酯与聚乙二醇的羟基形成共轭来形成碳酸酯基的化合物。在本发明中,可将以下上述化合物表示为衍生物。
[0070]
具体地,上述胶束具有存在于疏水性核(core)的氯甲酸烷基酯与位于表面(或壳,shell)的亲水性聚乙二醇之间的碳酸酯键。因此,在衍生物中,具有氯甲酸烷基酯部分位于
胶束的内部,聚乙二醇部分位于表面的形态。
[0071]
并且,本发明的胶束具有上述胶束的表面结合有肽的结构。上述肽作为靶向配体可以为选自脂肪细胞靶序列(ats)肽及r9(精氨酸)肽中的一种以上的肽。上述肽可与存在于胶束表面的聚乙二醇的末端部位相结合来形成强键,在一具体例中,肽的羧基可与聚乙二醇的末端的胺基形成结合。根据肽的特性,本发明的胶束可具有靶向性。在本发明中,术语“配体(ligand)”意味着与配体结合蛋白质相结合来引起结构上的变化的分子。上述配体可以为选自脂肪细胞靶序列(ats)肽及r9(精氨酸)肽中的一种以上。可通过上述脂肪细胞靶序列(ats)肽提高对脂肪细胞,尤其,白色脂肪的靶向率,可通过r9(精氨酸)肽提高细胞渗透率。
[0072]
在一具体例中,包含在本发明的胶束的化学式1的化合物可以为由以下化学式2表示的化合物(以下,由化学式2的化合物表示)。并且,化学式1的化合物可以为由以下化学式3表示的化合物(以下,由化学式3的化合物表示)。上述化学式2的化合物为结合有脂肪细胞靶序列(ats)肽的化合物,化学式3的化合物为结合有r9(精氨酸)肽的化合物。
[0073]
化学式2
[0074][0075]
化学式3
[0076][0077]
在上述化学式2至3中,p及q可与化学式1的p及q相同。
[0078]
在一具体例中,胶束除了由化学式1表示的化合物之外,还可包含由化学式4表示的化合物(以下,化学式4的化合物)。
[0079]
化学式4
[0080][0081]
在上述化学式4中,r1可以为氢、c1至5的烷基、胺基、c1至5的烷基胺基、羧基或c1至5的烷基羧基,p及q可与化学式1的p及q相同。
[0082]
并且,本发明涉及上述的用于减少脂肪的气体发泡型胶束的制备方法。
[0083]
本发明的用于减少脂肪的气体发泡型胶束可通过如下步骤制备,其包括:
[0084]
混合聚乙二醇(polyethylene glycol)及氯甲酸烷基酯(alkyl chloroformate)
来合成作为由化学式4表示的化合物的聚乙二醇衍生物的步骤;
[0085]
在上述聚乙二醇衍生物中结合选自由脂肪细胞靶序列(ats)肽及r9(精氨酸)肽组成的组中的一种以上的肽来合成结合有肽的聚乙二醇衍生物的步骤;以及
[0086]
使上述聚乙二醇衍生物及结合有上述肽的聚乙二醇衍生物溶解于选自乙腈、二氯甲烷、氯仿及甲醇中的一种或两种以上的混合溶剂之后,使溶剂蒸发来合成胶束的步骤。
[0087]
化学式4
[0088][0089]
化学式1
[0090][0091]
在上述化学式1或4中,
[0092]
r1为氢、c1至5的烷基、胺基、c1至5的烷基胺基、羧基或c1至5的烷基羧基,
[0093]
p为12至227的整数,
[0094]
q为2至14的整数,
[0095]
n为0至5的整数,
[0096]
l为脂肪细胞靶序列(ats)肽或r9(精氨酸)肽。
[0097]
在一具体例中,上述化合物的q可以为4至10的整数、4至8的整数、6至10的整数或8至10的整数,n可以为1至3的整数。
[0098]
以下,详细察看本发明的气体发泡型胶束制备方法(图2及图3)。
[0099]
1.聚乙二醇衍生物的合成
[0100]
制备胶束之前,先制备用于形成胶束的聚乙二醇衍生物。
[0101]
首先,使聚乙二醇和氯甲酸烷基酯分别溶解于乙腈来准备聚乙二醇溶液及氯甲酸烷基酯溶液。在准备的聚乙二醇溶液中添加氯甲酸烷基酯溶液之后,进行搅拌。在上述搅拌结束的混合物中添加吡啶之后,进行反应来制备聚乙二醇-碳酸烷基酯。
[0102]
在一具体例中,聚乙二醇不局限于此,但分子量可以为550至10000da(g/mol)、1000至10000da、2000至6000da、1500至3000da、2000至2500da、4500至6000da或5000至5500da。
[0103]
在一具体例中,氯甲酸烷基酯可以为脂肪族化合物,可以为具有碳原子数为4至10、碳原子数为4至8、碳原子数为6至10或碳原子数为8至10的烷基的氯甲酸酯。例如,作为氯甲酸烷基酯,可使用氯甲酸丁酯、氯甲酸辛酯或氯甲酸十二烷基酯,但不局限于此。
[0104]
在一具体例中,聚乙二醇溶液可使聚乙二醇0.2至0.8mmol溶解于乙腈2至6ml来准备,氯甲酸烷基酯溶液可使氯甲酸烷基酯1至3mmol溶解于乙腈3至7ml来准备。
[0105]
在一具体例中,可在聚乙二醇溶液中添加氯甲酸烷基酯溶液之后,搅拌2至10分钟、3至8分钟、4至6分钟或5分钟。
[0106]
在一具体例中,当进行上述搅拌时,可分次给予氮气。反应物弱于大气中的水分,
因而在本发明中,通过分次给予反应性低的氮气,能够以可稳定进行反应的方式进行诱导。
[0107]
在一具体例中,可在上述搅拌结束的混合物中添加吡啶1.5至3.5mmol之后,在0至5℃中反应20至40分钟,之后,在常温下反应24小时,以制备聚乙二醇衍生物。
[0108]
这种聚乙二醇衍生物为聚乙二醇-碳酸烷基酯。
[0109]
可通过ft-ir光谱法及nmr分析确认聚乙二醇衍生物的合成。
[0110]
2.导入有肽的聚乙二醇衍生物的合成
[0111]
可向在上述1.中制备的聚乙二醇衍生物导入肽来提高向脂肪细胞的靶向性。
[0112]
使具有氨基的化合物和肽进行edc/nhs反应,以制备结合有肽的聚乙二醇。
[0113]
在一具体例中,具有氨基的化合物可以为氨基乙二醇(aminopolyethylene glycol),肽可以为选自由脂肪细胞靶序列(ats)肽及r9(精氨酸)肽组成的组中的一种以上。
[0114]
在一具体例中,具有氨基的化合物和肽的摩尔比可以为1:0.1至1:10或1:0.5至1:3,可通过edc/nhs反应制备结合有肽的聚乙二醇衍生物。
[0115]
在一具体例中,可制备结合有肽的聚乙二醇之后,进行透析,通过过滤器去除杂质及未反应物质。
[0116]
可通过ft-ir光谱法及nmr分析确认结合有肽的聚乙二醇衍生物的合成。
[0117]
3.利用溶剂蒸发法的胶束粒子的制备
[0118]
在上述1.中制备的聚乙二醇衍生物及在上述2.中制备的导入有肽的聚乙二醇衍生物可通过溶剂蒸发法制备成胶束。
[0119]
具体地,可将聚乙二醇衍生物及导入有肽的聚乙二醇衍生物溶解于有机溶剂,执行使溶剂挥发的溶剂蒸发法之后,再次分散于亲水性溶液,以制备胶束。
[0120]
在一具体例中,在上述步骤中,可使用选自由作为化学式2的化合物的导入有脂肪细胞靶序列(ats)肽的聚乙二醇衍生物及作为化学式3的化合物的导入有r9(精氨酸)肽的聚乙二醇衍生物组成的组中的一种以上的衍生物和作为化学式4的化合物的聚乙二醇衍生物形成胶束。
[0121]
在一具体例中,当使用化学式2的化合物及化学式4的化合物制备胶束时,化学式2的化合物及化学式4的化合物的摩尔比可以为99.5:0.5至95.0:5.0、99.5:0.5至96.0:4.0、99.0:1.0至97.0:3.0或99.0:1.0至98.0:2.0。
[0122]
在一具体例中,当使用化学式3的化合物及化学式4的化合物制备胶束时,化学式3的化合物及化学式4的化合物的摩尔比可以为99.5:0.5至95.0:5.0、99.5:0.5至96.0:4.0、99.0:1.0至97.0:3.0或99.0:1.0至98.0:2.0。
[0123]
并且,在一具体例中,当使用化学式2的化合物、化学式3的化合物及化学式4的化合物制备胶束时,化学式2的化合物、化学式3的化合物及化学式4的化合物的摩尔比可以为99:0.5:0.5至90.0:5.0:5.0、99:0.5:0.5至97.0:1.5:1.5或99.0:0.5:0.5至98.0:1.0:1.0。
[0124]
在一具体例中,可将聚乙二醇衍生物及导入有肽的聚乙二醇衍生物5至15mg溶解于有机溶剂。上述有机溶剂可以为通常使用的有机溶剂,例如,可以为乙腈、二氯甲烷、氯仿及甲醇。
[0125]
并且,有机溶剂可以为二氯甲烷及乙腈的混合溶剂、二氯甲烷及氯仿的混合溶剂、
二氯甲烷及甲醇的混合溶剂。
[0126]
本发明中使用的混合溶剂中二氯甲烷和另一溶剂的比例可以为3至1:1至3。
[0127]
在一具体例中,可将聚乙二醇衍生物及导入有肽的聚乙二醇衍生物溶解于有机溶剂之后,利用浓缩机在真空中以100至300rpm、150至200rpm或180rpm在25至45℃、30至40℃或37℃中对玻璃壁面涂敷约5至10分钟。在本发明中,可利用浓缩机进行涂敷,从而以对玻璃壁面均匀地涂敷的方式诱导。在利用氮的溶剂蒸发法中,通过手工使溶剂蒸发,因而需要用于规定地调节旋转速度及旋转角度的追加努力,但在本发明中,利用浓缩机执行涂敷,具有可继续且均匀地涂敷的优点。
[0128]
并且,在一具体例中,亲水性溶液可包含磷酸盐缓冲液(pbs)及蒸馏水。
[0129]
并且,本发明涉及包含上述的用于减少脂肪的气体发泡型胶束的用于减少脂肪的组合物。
[0130]
本发明的用于减少脂肪的气体发泡型胶束在其结构内包含碳酸酯基,在水溶性条件下,上述胶束的碳酸酯基因水解而断开,并引起生成二氧化碳气体的反应。因此,本发明的用于减少脂肪的气体发泡型胶束以纳米粒子的形态局部给药,浸渍于脂肪细胞而产生气体。通过所产生的上述二氧化碳引起的细胞打击,引起脂肪细胞的坏死,由此可减少脂肪(图1)。
[0131]
上述细胞打击可调节气体发泡型胶束的结构,调节生成的二氧化碳的产生量和产生时间,可使上述胶束移入细胞内之后产生。
[0132]
本发明的用于减少脂肪的组合物可包含上述化学式1的化合物。
[0133]
并且,本发明的用于减少脂肪的组合物可包含含有选自由以下化学式2的化合物及以下化学式3的化合物组成的组中的一种以上的化合物及以下化学式4的化合物的气体发泡型胶束。
[0134]
化学式2
[0135][0136]
化学式3
[0137][0138]
化学式4
[0139][0140]
在上述化学式2至4中,
[0141]
r1为氢、c1至3的烷基、胺基、c1至3的烷基胺基、羧基或c1至3的烷基羧基。
[0142]
p及q可与化学式1的化合物中的p及q相同。
[0143]
在一具体例中,当用于减少脂肪的组合物包含含有化学式2的化合物及化学式4的化合物的气体发泡型胶束时,化学式2的化合物及化学式4的化合物的摩尔比可以为99.5:0.5至95.0:5.0、99.5:0.5至96.0:4.0、99.0:1.0至97.0:3.0或99.0:1.0至98.0:2.0。
[0144]
在一具体例中,当用于减少脂肪的组合物包含含有化学式3的化合物及化学式4的化合物的气体发泡型胶束时,化学式3的化合物及化学式4的化合物的摩尔比可以为99.5:0.5至95.0:5.0、99.5:0.5至96.0:4.0、99.0:1.0至97.0:3.0或99.0:1.0至98.0:2.0。
[0145]
并且,在一具体例中,当用于减少脂肪的组合物包含含有化学式2的化合物、化学式3的化合物及化学式4的化合物的气体发泡型胶束时,化学式2的化合物、化学式3的化合物及化学式4的化合物的摩尔比可以为99:0.5:0.5至90.0:5.0:5.0、99:0.5:0.5至97.0:1.5:1.5或99.0:0.5:0.5至98.0:1.0:1.0。
[0146]
在一具体例中,在用于减少脂肪的组合物中,气体发泡型胶束的含量可根据适用部位等不同,例如,在组合物总重量中,可以为0.01至1.0重量份或0.1至0.5重量份。
[0147]
在一具体例中,本发明的用于减少脂肪的组合物可用于局部或静脉注射,通常可适用于手术频率高的下巴、大腿、手臂、腹部等部位。
[0148]
在一具体例中,本发明的用于减少脂肪的组合物可用作局部脂肪分解补充剂、体型矫正剂或减肥美容产品等。
[0149]
以下,通过实施例更详细说明本发明。这些实施例仅用于更具体说明本发明,根据本发明的要旨,本发明的范围不局限于这些实施例,这对于本发明所属技术领域的普通技术人员来说是显而易见的。
[0150]
实施本发明的方式
[0151]
实施例
[0152]
《参考》实验材料
[0153]
聚乙二醇从西格玛奥德里奇(sigma aldrich)购买并使用。可使用的聚乙二醇的数均分子量(mn)为550至20000,其中,数均分子量为5000的聚乙二醇优选地用于制备气体发泡型胶束,将其用于本实验中。
[0154]
作为氯甲酸烷基酯,使用链状脂肪族化合物,即,氯甲酸辛酯(西格玛奥德里奇)。
[0155]
实施例1.气体发泡型胶束的制备
[0156]
(1)聚乙二醇衍生物的合成
[0157]
使聚乙二醇和氯甲酸烷基酯分别溶解于乙腈。具体地,使聚乙二醇0.5mmol溶解于乙腈4ml,以准备聚乙二醇溶液,将氯甲酸烷基酯2mmol添加到乙腈5ml,以准备氯甲酸烷基酯溶液。
[0158]
在准备的聚乙二醇溶液中添加氯甲酸烷基酯溶液之后,搅拌5分钟。当进行上述搅
拌时,分次给予反应性低的氮气。在上述搅拌结束的混合物中添加吡啶2.5mmol之后,在0℃中反应30分钟。反应结束之后,在常温中搅拌24小时,以结束合成。
[0159]
使上述合成结束的溶液沉淀于二乙醚之后,通过过滤器过滤,之后,在真空干燥机中干燥3至7天,获取作为合成高分子的聚乙二醇衍生物,即,聚乙二醇-碳酸烷基酯。
[0160]
根据聚乙二醇的数均分子量及氯甲酸烷基酯的烷基的种类,可制备另一种类的聚乙二醇衍生物,即,聚乙二醇-碳酸烷基酯。例如,聚乙二醇的数均分子量为5000,当使用氯甲酸辛酯时,制备聚乙二醇5000-碳酸辛酯,其可表示为peg
5000-octylcarbonate。
[0161]
图4表示利用显微镜从peg
5000-octylcarbonate确认气体发泡的结果。如上述图4所示,可确认当将衍生物粉末放入蒸馏水(dw)时,观察到气泡。
[0162]
(2)聚乙二醇衍生物中肽(配体)的导入
[0163]
聚乙二醇衍生物中肽的导入执行如下。
[0164]
首先,以1:1的摩尔比使具有氨基的氨基聚乙二醇衍生物和肽进行edc/nhs反应来制备结合有肽的聚乙二醇衍生物。之后,透析4天,通过过滤器去除杂质及未反应物质之后,执行冷冻干燥。
[0165]
在本发明中,当根据肽的种类,使用脂肪细胞靶序列(ats)肽时,可表示为ats-peg
5000-octylcarbonate。上述衍生物中聚乙二醇的数均分子量为5000,使用氯甲酸辛酯。
[0166]
(3)利用溶剂蒸发法的胶束粒子的制备
[0167]
胶束通过利用以2:1的比例包含二氯甲烷及乙腈的混合溶剂的溶剂蒸发法制备。
[0168]
将在上述的(1)中制备的聚乙二醇衍生物和/或在(2)中制备的导入有肽的聚乙二醇衍生物溶解于混合溶剂之后,利用浓缩机(n-1300)在真空中以180rpm在37℃中对玻璃壁面涂敷约5至10分钟,对玻璃表面涂敷衍生物粒子(溶剂蒸发)。
[0169]
溶剂蒸发之后,放入亲水性溶液(包含pbs及蒸馏水),以执行自组装,制备胶束。
[0170]
在本发明中,根据使用的衍生物的结构,制备四个种类的胶束粒子。
[0171]-胶束a(non):由在(1)中制备的聚乙二醇衍生物制备的胶束
[0172]-胶束b(9r):由导入有9r肽的聚乙二醇衍生物2重量百分比及聚乙二醇衍生物98重量百分比制备的胶束
[0173]-胶束c(ats):由导入有ats肽的聚乙二醇衍生物2重量百分比及聚乙二醇衍生物98重量百分比制备的胶束
[0174]-胶束d(ats/9r):由导入有9r肽的聚乙二醇衍生物1重量百分比、导入有ats肽的聚乙二醇衍生物1重量百分比及聚乙二醇衍生物98重量百分比制备的胶束
[0175]
实验例1.聚乙二醇衍生物的合成的确认
[0176]
确认在实施例1的(1)中制备的聚乙二醇衍生物是否合成,其利用ft-ir光谱仪(nicholetis50,thermo)确认。
[0177]
根据利用ft-ir光谱法分析是否导入聚乙二醇-碳酸烷基酯的碳酸酯键的结果,在波数(wave number)1742cm-1
和1653cm-1
中确认碳酸酯连接基(c=o),确认到聚乙二醇-碳酸烷基酯中导入有碳酸酯键(图5)。
[0178]
实验例2.聚乙二醇衍生物中肽导入的确认
[0179]
确认在实施例1的(2)中制备的结合有肽的聚乙二醇衍生物是否导入肽,其利用ft-ir光谱仪(nicholetis50,thermo)确认。
[0180]
根据利用ft-ir光谱法分析是否导入上述肽的结果,可确认当导入肽时,在1650~1580cm-1
中观察到伯胺(nh2)峰,在1680cm-1
及1760cm-1
中观察到仲酰胺(c=o)峰(图6)。
[0181]
实验例3.利用聚乙二醇衍生物的胶束性质的分析
[0182]
分析在实施例1的(3)中制备的胶束a至d的性质。
[0183]
将其结果示于下列表1中。
[0184]
表1
[0185][0186]
如上述表1中所示,可确认导入有肽的情况相比于未导入肽的胶束(胶束a.non),纳米粒子的大小变大。并且,可确认通过导入肽,表面电荷上升。
[0187]
实验例4.聚乙二醇衍生物的气体产生的确认
[0188]
确认在实施例1的(1)中制备的聚乙二醇衍生物中的气体产生,其通过nmr分析进行确认。具体地,测定mpeg
5000
及聚乙二醇衍生物的nmr,将上述衍生物保存于水溶性溶液24小时之后,再次测定nmr。
[0189]
根据利用nmr分析上述气体产生的结果,可确认mpeg
5000
的羟基的信号(-oh score)在衍生物合成之后消失,可确认保存于(4.56ppm)水溶性溶液之后,当再次测定时,羟基的信号在4.56ppm附近重新恢复。由此可确认衍生物中的气体产生(图7)。
[0190]
实验例5.聚乙二醇衍生物的气体产生速度的确认
[0191]
确认在实施例1的(1)中制备的聚乙二醇衍生物中的气体产生速度,其通过超声波设备(sonon300l)进行确认。具体地,确认mpeg
2000-碳酸丁酯(butylcarbonate)、mpeg
2000-碳酸辛酯(octylcarbonate)、mpeg
5000-butylcarbonate及mpeg
5000-octylcarbonate这四个种类的聚乙二醇衍生物的n气体产生速度。
[0192]
根据利用超声波设备分析上述气体产生速度的结果,可确认根据构成胶束的衍生物的种类,气体产生速度不同,由mpeg
5000-octylcarbonate构成的胶束呈现最高的稳定性(图8)。
[0193]
并且,利用荧光显微镜确认由呈现高的稳定性的mpeg
5000-octylcarbonate构成的胶束的气体产生。
[0194]
根据利用荧光显微镜确认的结果,可确认气体从胶束中稳定地释放(图9)。
[0195]
实验例6.聚乙二醇衍生物的细胞毒性的分析
[0196]
分析聚乙二醇衍生物的细胞毒性,其根据mts assay方式执行。
[0197]
使3t3-l1细胞以2
×
103细胞/板(cell/plate)培养或分化在96-孔板中,以0.5mg/ml~5mg/ml处理胶束的浓度。之后,在37℃、5%co2中培养24小时。利用pbs将培养的细胞清
洗1次,将mts溶液处理1小时之后,通过紫外-可见光吸收(uv/vis)光谱仪在490nm中分析吸光度,以确认细胞毒性。
[0198]
将其结果示于图10中。
[0199]
如上述图10所示,可确认脂肪细胞分化前后将在本发明的实施例1的(1)中制备的聚乙二醇-碳酸烷基酯(mpeg
5000-octylcarbonate)处理于细胞的结果呈现几乎无毒性。
[0200]
实验例7.导入有肽的胶束的脂肪细胞凋亡能力的分析
[0201]
针对使用导入有肽(r9肽或ats肽)的聚乙二醇衍生物制备的胶束,分析根据肽的浓度的脂肪细胞凋亡能力。此时,在衍生物总重量(重量)中,肽的导入量为0%至4%。
[0202]
上述凋亡能力根据mts assay方式执行。
[0203]
以2
×
103细胞/板将3t3-l1细胞分注到96-孔板之后,分化2至3周。之后,将衍生物的浓度设定为0.2wt%处理,24小时之后利用pbs清洗1次。利用mts溶液处理1小时之后,分析吸光度(以与实验例6相同的方式分析)。
[0204]
将其结果示于图11中。
[0205]
如图11所示,可确认根据肽的导入量,呈现具有倾向性的细胞凋亡效果。只是,呈现r9肽在导入量为4%时,抑制细胞凋亡效果。
[0206]
由此,可确认在用于脂肪细胞凋亡的胶束的制备中,相比于基础衍生物的重量,滴定肽导入衍生物的浓度为1%至3%。
[0207]
实验例8.根据肽组合及胶束浓度的脂肪细胞凋亡能力
[0208]
针对在实施例1的(3)中制备的胶束a至d,以0.1至0.3wt%浓度处理上述胶束来评价细胞凋亡能力。
[0209]
此时,ats用于脂肪细胞靶,利用为用于9r细胞内渗透的肽。
[0210]
将其结果示于图12中。在上述图12中,peg
5000-碳酸辛酯胶束(octylcarbonatemicells)表示胶束a,r9-peg
5000-octylcarbonatemicells表示胶束b,ats-peg
5000-octylcarbonatemicells表示胶束c,ats-r9-peg
5000-octylcarbonatemicells表示胶束d。
[0211]
如图12所示,未导入有肽的胶束a呈现90%以上的细胞存活率。
[0212]
相反,可确认导入有肽的胶束随着浓度变高,细胞凋亡效果增加。尤其,可确认胶束d中当0.3wt%时呈现最高的凋亡结果。
[0213]
实验例9.肽功效的确认
[0214]
针对在实施例1的(3)中制备的胶束a至d,评价多种细胞(成纤维细胞(fibroblast)、成肌细胞(myoblast)、脂肪细胞(adipocyte))中上述胶束的靶向功效。
[0215]
将其结果示于图13中。在上述图13中,对照组(control)表示胶束a,r9表示胶束b,ats表示胶束c,ats/r9表示胶束d。
[0216]
如图13所示,可确认r9肽与细胞的种类无关地,细胞凋亡率呈现相似的倾向,ats肽中脂肪细胞具有高于其他细胞的凋亡率。可确认ats/r9中脂肪细胞具有高于其他细胞的凋亡率,脂肪细胞具有比单独使用ats及r9时更优秀的细胞凋亡率。
[0217]
工业实用性
[0218]
本发明的用于减少脂肪的气体发泡型胶束可制作成可注射的制剂,适用于减肥美容领域及肥胖治疗剂领域,可用作通过局部脂肪的凋亡分解局部脂肪的局部脂肪分解补充
剂、体型矫正剂或减肥美容产品等。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1