蛋白微粒及其制备方法和用途
1.本发明涉及生物技术领域,具体涉及一种具有良好稳定性的蛋白微粒及其制备方法和用途。
背景技术:
2.谷物醇溶蛋白是一种不溶于水的植物微颗粒,一般占胚乳中蛋白质的50%以上。根据结构与溶解性,可被分为α
‑
,β
‑
,γ
‑
和δ
‑
醇溶蛋白。因其独特的自组装特性,良好的生物相容性以及可降解性,醇溶蛋白可作为可食用颗粒,并可作为药物载体。此外,醇溶蛋白还可作为营养素载体,运载如姜黄素、β
‑
胡萝卜素、多肽、脂溶性和水溶性维生素、铁、锌等营养素。
3.谷物醇溶蛋白颗粒分散到水中时,若分散液中含有盐离子,或者ph在4
‑
7之间,非常容易沉淀。现有技术路线制成的颗粒虽然可以在较宽的ph范围内保持稳定,但极易受盐溶液影响,即使在低浓度的盐溶液中也会聚沉,不利于实际应用。
4.cn110051006a公开了一种玉米醇溶蛋白/阿拉伯胶复合纳米颗粒及其制备方法,通过将玉米醇溶蛋白和阿拉伯胶的乙醇水溶液共混,通过调节ph、混合比例等实验参数即可形成均一、稳定、单分散分布的复合纳米颗粒分散液,无需反溶剂过程。但是,该制备方法并没有解决颗粒在不同ph、不同浓度的盐溶液下不稳定的问题。
5.因此,增强谷物醇溶蛋白颗粒在分散体系中的稳定性,在宽范围的盐浓度和ph值条件下保持稳定,不沉淀、絮凝是非常有必要的。
技术实现要素:
6.本发明的目的是为了克服现有技术存在的问题,提供一种蛋白微粒及其制备方法和用途。
7.本发明第一方面提供了一种蛋白微粒,该微粒以谷物醇溶蛋白为核、阿拉伯胶为壳,且可食用多酚存在于核与壳之间并与谷物醇溶蛋白和阿拉伯胶分别结合。
8.本发明第二方面提供了如上所述蛋白微粒的制备方法,该方法包括:将可食用多酚溶液与含谷物醇溶蛋白和阿拉伯胶的分散系混合。
9.本发明第三方面提供了一种由上述方法制得的蛋白微粒。
10.本发明第四方面提供了一种所述蛋白微粒作为药物载体或营养素载体的用途。
11.通过本发明的制备方法制备的蛋白微粒在ph4
‑
8.5的具有不同盐浓度(0.2
‑
3mol/l)的盐溶液中均具有良好的稳定性,不发生沉淀或絮凝。因此,本发明所述的蛋白微粒在作为药物载体或营养素载体方面具有重要应用潜力。具体地:
12.1、本发明利用阿拉伯胶分子通过静电作用和/或疏水作用吸附于谷物醇溶蛋白表面,形成了以谷物醇溶蛋白为核心,以阿拉伯胶为外壳的“核
‑
壳”结构;可食用多酚如单宁酸等含有大量羟基,能够与蛋白质上的羰基反应,该反应会产生稳定的氢键,从而促进谷物醇溶蛋白与阿拉伯胶上蛋白质基团间的交联反应。所形成的“核
‑
壳”分子因在表面引入大
量亲水多糖基团,因而能够在高浓度盐溶液中保持稳定从而增强谷物醇溶蛋白颗粒的稳定性,使其更具实用性。
13.2、本发明所述方法包含将可食用多酚溶液与谷物醇溶蛋白和阿拉伯胶的分散系混合,操作简单,实用性强,效果显著。其中,在优选的情况下,本发明通过将加入可食用多酚溶液加至含有谷物醇溶蛋白和阿拉伯胶的分散系中,以此加入顺序制备得到的蛋白微粒在不同盐浓度及ph值溶液中都具有更好的稳定性。
14.3、本发明方法制备得到的蛋白微粒的稳定性较好,可以作为药物载体或营养素载体应用可以增加药物或营养素的吸收利用率。
附图说明
15.图1a
‑
f为实施例1及各对比例的分散液在不同ph和nacl浓度条件下的背散射光强度变化图。图1a为实施例1中的玉米醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒分散液,图1b为玉米醇溶蛋白颗粒
‑
阿拉伯胶分散液,图1c为玉米醇溶蛋白颗粒
‑
单宁酸分散液,图1d为玉米醇溶蛋白颗粒分散液,图1e为阿拉伯胶
‑
单宁酸分散液,图1f为阿拉伯胶分散液。
16.图2为实施例1及对比例1
‑
5各组分散液经离心后的状态图。a为实施例1中的玉米醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒分散液,b为玉米醇溶蛋白颗粒
‑
阿拉伯胶分散液,c为玉米醇溶蛋白颗粒
‑
单宁酸分散液,d为玉米醇溶蛋白颗粒分散液,e为阿拉伯胶
‑
单宁酸分散液,f为阿拉伯胶分散液。
17.图3显示的是ph值对实施例1中玉米醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒分散液的zeta
‑
电位值的影响结果图。
具体实施方式
18.在本文中所披露的范围的端点和任何值都不限于该精确的范围或值,这些范围或值应当理解为包含接近这些范围或值的值。对于数值范围来说,各个范围的端点值之间、各个范围的端点值和单独的点值之间,以及单独的点值之间可以彼此组合而得到一个或多个新的数值范围,这些数值范围应被视为在本文中具体公开。
19.一方面,本发明提供了一种蛋白微粒,该微粒以谷物醇溶蛋白为核、阿拉伯胶为壳,且可食用多酚存在于核与壳之间并与谷物醇溶蛋白和阿拉伯胶分别结合。
20.本发明对谷物醇溶蛋白的种类没有特别限定,可为本领域常见的谷物醇溶蛋白。优选的情况下,所述醇溶蛋白包括α
‑
醇溶蛋白、β
‑
醇溶蛋白、γ
‑
醇溶蛋白和δ
‑
醇溶蛋白的一种或多种。
21.更优选的,所述谷物醇溶蛋白选自玉米醇溶蛋白、小麦醇溶蛋白、大麦醇溶蛋白。进一步优选的情况下,所述醇溶蛋白为玉米醇溶蛋白。
22.在本发明中,所述可食用多酚可以是本领域常见的食品添加用多酚,所述可食用多酚包括但不限于单宁酸、表没食子儿茶素没食子酸酯、绿原酸、茶多酚、槲皮素和白藜芦醇中的至少一种。优选的情况下,所述可食用多酚为单宁酸。
23.优选的情况下,所述谷物醇溶蛋白与阿拉伯胶的质量比为1:0.25
‑
4,更优选为1:1
‑
3.5。
24.优选的情况下,所述谷物醇溶蛋白与可食用多酚的质量比为1:0.05
‑
1,更优选为
1:0.06
‑
0.85。
25.在本发明优选的实施方式中,所述蛋白微粒的直径为150
‑
300nm,优选为180
‑
270nm,多分散指数为0.01
‑
0.4,优选为0.05
‑
0.32。蛋白微粒的直径通过动态光散射测试结果计算得到,多分散指数动通过动态光散射方法得到。
26.根据本发明的优选实施方式,所述蛋白微粒为玉米醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒。
27.另一方面,本发明还提供了一种用于制备上述蛋白微粒的方法,其特征在于,该方法包括:将可食用多酚溶液与含谷物醇溶蛋白和阿拉伯胶的分散系混合。在本发明优选的实施方式中,所述混合方式为将可食用多酚溶液加至谷物醇溶蛋白
‑
阿拉伯胶分散系中。对加入速度没有特别的要求,但为了进一步改善蛋白微粒的稳定性,相对于每100ml的含谷物醇溶蛋白和阿拉伯胶的分散系,所述可食用多酚溶液的加入速度为0.1
‑
20ml/min,优选为1
‑
10ml/min。
28.优选的情况下,所述可食用多酚溶液的质量浓度为0.01%
‑
6%,更优选为1
‑
6%。可食用多酚溶液中的溶剂通常为水,优选为超纯水。
29.优选的,所述谷物醇溶蛋白与可食用多酚的质量比为1:0.07
‑
1.5,优选为1:0.1
‑
1。
30.根据本发明,为了更好的增强蛋白微粒的稳定性,所述含谷物醇溶蛋白和阿拉伯胶的分散系可以通过以下步骤而制得:将ph值为7
‑
9.5阿拉伯胶分散系与谷物醇溶蛋白分散系混合,持续搅拌。在本发明优选的实施方式中,所述混合方法为将阿拉伯胶分散系加至谷物醇溶蛋白分散系中。对加入速度没有特别的要求,但为了进一步改善蛋白微粒的稳定性,相对于每100ml的含谷物醇溶蛋白的分散系,所述阿拉伯胶分散系的加入速度为0.01
‑
50ml/min,优选为5
‑
50ml/min。优选的,所述谷物醇溶蛋白与阿拉伯胶的质量比为1:0.3
‑
7,更优选的情况下,所述谷物醇溶蛋白与阿拉伯胶的质量比为1:0.3
‑
6。
31.优选的,所述阿拉伯胶分散系中阿拉伯胶的质量浓度为0.01
‑
6%,更优选为1
‑
6%。所述阿拉伯胶分散系中的溶剂通常为水,优选为超纯水。
32.根据本发明,为了更好地增强蛋白微粒的稳定性,所述谷物醇溶蛋白分散系可以通过以下步骤制得:将ph值为7
‑
9.5谷物醇溶蛋白溶液分散于水中。所述分散方式可为本领域常规方法,例如反溶剂沉淀法、蒸发法等。在本发明优选的实施方式中,所述分散方法为将谷物醇溶蛋白溶液加至水中。对加入速度没有特别的要求,但为了进一步改善蛋白微粒的稳定性,相对于每100ml的水,谷物醇溶蛋白溶液的加入速度为0.02
‑
10ml/min,优选为1
‑
10ml/min。更优选的,所述谷物醇溶蛋白溶液与水的体积比为1:0.1
‑
80,优选为1:1
‑
10。优选的情况下,所述谷物醇溶蛋白分散系的ph值为7
‑
9.5。
33.为了更好地增强蛋白微粒的稳定性,所述谷物醇溶蛋白溶液、阿拉伯胶分散系、谷物醇溶蛋白分散系的ph值保持一致。
34.在本发明中,所述谷物醇溶蛋白溶液可以通过本领域常规的方法制备。优选的,所述谷物醇溶蛋白溶液可以通过将谷物醇溶蛋白溶于乙醇水溶液、丙酮水溶液、异丙醇水溶液、ph大于11.5的水溶液中制备。其中,所述ph大于11.5的水溶液由碱金属氢氧化物(如氢氧化钠)调节ph制成。在优选的情况下,通过将谷物醇溶蛋白溶于50
‑
90%(v/v)的乙醇水溶液制备谷物醇溶蛋白溶液。
35.优选的,所述谷物醇溶蛋白溶液的质量浓度为0.005
‑
15%,优选为1
‑
10%。
36.在本发明中,所述阿拉伯胶分散系可以通过本领域常规的制备方法制得。优选的,阿拉伯胶分散系通过以下步骤而制得:将阿拉伯胶溶于水中,于温水(温度为40
‑
60℃的水)中搅拌、溶解,待溶液温度降至室温后调节其ph值为7
‑
9.5。在本发明中,所述可食用多酚和谷物醇溶蛋白的种类在第一方面已经进行了详细的阐述,在此不再赘述。
37.根据本发明的优选实施方式,所述方法包括如下步骤:
38.(1)将玉米醇溶蛋白溶于溶剂中,使其完全分散得到质量浓度玉米醇溶蛋白溶液,并将溶液的ph值调节至7
‑
9.5;
39.(2)将阿拉伯胶于温水中搅拌、溶解,而后待溶液温度降至室温后将其ph值调至7
‑
9.5,得到阿拉伯胶分散系;
40.(3)将步骤(1)制备得到的玉米醇溶蛋白溶液加至水中,相对于每100ml的水,玉米醇溶蛋白溶液的加入速度为1
‑
10ml/min,制备得到玉米醇溶蛋白分散系,其中,使用0.1mol/l naoh溶液将ph值调至7
‑
9.5;
41.(4)将步骤(2)制备得到的阿拉伯胶分散系加至步骤(3)制备得到的玉米醇溶蛋白分散系中,相对于每100ml的含玉米醇溶蛋白的分散系,所述阿拉伯胶分散系的加入速度为5
‑
50ml/min,持续搅拌,得到含玉米醇溶蛋白和阿拉伯胶的分散系;
42.(5)将单宁酸溶液加至步骤(4)制备得到的玉米醇溶蛋白和阿拉伯胶的分散系中,相对于每100ml的含玉米醇溶蛋白和阿拉伯胶的分散系,所述可食用多酚溶液的加入速度为1
‑
10ml/min,得到稳定的玉米醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒。根据该优选实施方式制得的蛋白微粒的稳定性更强。
43.本发明还提供了由上述方法制得的蛋白微粒。
44.上述蛋白微粒在不同ph、不同盐浓度的溶液中均具有良好的稳定性,不易沉淀或聚沉。因此,另一方面,本发明提供了一种所述蛋白微粒作为药物载体或营养素载体的用途。所述营养素可以为姜黄素、β
‑
胡萝卜素、多肽、脂溶性和水溶性维生素、铁、锌,所述蛋白微粒以非共价结合方式搭载营养素,从而能够增加营养素的吸收利用率。
45.以下将通过实施例对本发明进行详细描述。
46.下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中所用的原料、试剂等,如无特殊说明,均可以从商业途径得到。室温指“25℃”。
47.下述实施例中,如无特殊说明,玉米醇溶蛋白、小麦醇溶蛋白、大麦醇溶蛋白、阿拉伯胶、单宁酸、茶多酚、没食子儿茶素没食子酸酯购自美国sigma试剂公司,乙醇购自天津永大试剂公司,naoh购自天津永大试剂公司。
48.下述实施例中,如无特殊说明,搅拌器为wh220
‑
ht数字式加热磁力搅拌器,购自德国wiggens公司。
49.喷雾冻干的条件:样品于lgj
‑
12型冻干机(北京松源华兴生物技术有限公司)中干燥至恒重。
50.体积排阻色谱条件:两支tsk
‑
gel g2000 swxl(300mm*7.8mm,tosho公司),串联;流动相含8mol l
‑
1尿素和0.05mol l
‑
1tris水溶液(ph8.0)。取0.05g冻干后的粉末加到3.5ml 8mol l
‑
1尿素水溶液中(ph8.0),样品进样量20微升。
51.实施例1
52.(1)将5克玉米醇溶蛋白溶于100ml的80%(v/v)的乙醇水溶液中,于室温600rpm搅拌1h,得到玉米醇溶蛋白溶液,再使用0.1mol/l naoh溶液将玉米醇溶蛋白溶液的ph值调为9;
53.(2)将10克阿拉伯胶于50℃240毫升超纯水中600rpm连续搅拌1h,得到阿拉伯胶分散系,随后,降至室温并使用0.1mol/l naoh溶液将ph值调至9;
54.(3)将步骤(1)中的玉米醇溶蛋白溶液的20ml以相对于每100ml的超纯水5ml/min的加入速度加至5倍体积的超纯水中制备玉米醇溶蛋白分散系,其中,使用0.1mol/l naoh溶液将ph值调至9,600rpm持续搅拌1h;
55.(4)以玉米醇溶蛋白与阿拉伯胶为1:2的质量比将步骤(2)中的阿拉伯胶分散系以相对于每100ml的玉米醇溶蛋白分散系10ml/min的加入速度加至步骤(3)中的玉米醇溶蛋白分散系,600rpm持续搅拌1h,得到含玉米醇溶蛋白和阿拉伯胶的分散系;
56.(5)将5ml浓度为0.04g/ml的单宁酸溶液以相对于每100ml的含玉米醇溶蛋白和阿拉伯胶的分散系10ml/min的加入速度加至步骤(4)中的含玉米醇溶蛋白和阿拉伯胶的分散系中,600rpm持续搅拌30min,从而形成稳定的玉米醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒分散液(zein
‑
ga
‑
ta)。向该分散液中加入500ml去离子水后,于超滤装置中过滤(膜孔径100kda,德国sartorius vivaflow 50回旋流/切向流超滤器),弃去透过液后,收集截留液。
57.(6)将步骤(5)获得的截留液喷雾冻干后,得到玉米醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒a1。采用体积排阻色谱测定该颗粒中阿拉伯胶、玉米醇溶蛋白的含量,得出玉米醇溶蛋白与阿拉伯胶的质量比为1:1;采用《单宁酸分析试验方法(ly/t 1642
‑
2005)》分析颗粒中单宁酸的含量,得出玉米醇溶蛋白与单宁酸的质量比为7:1。
58.实施例2
59.按照实施例1的方法制备蛋白微粒,不同的是,步骤(1)、步骤(2)和步骤(3)中玉米醇溶蛋白溶液、阿拉伯胶分散系和玉米醇溶蛋白分散系的ph值分别调至7,且更改步骤(4)中玉米醇溶蛋白和阿拉伯胶的质量比为1:6,更改步骤(5)中单宁酸溶液的加入量为2.5ml,最终得到玉米醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒a2。
60.采用体积排阻色谱测定该颗粒中阿拉伯胶、玉米醇溶蛋白的含量,得出玉米醇溶蛋白与阿拉伯胶的质量比为1:3.5;采用《单宁酸分析试验方法(ly/t1642
‑
2005)》分析颗粒中单宁酸的含量,得出玉米醇溶蛋白与单宁酸的质量比为15.2:1。
61.实施例3
62.按照实施例1的方法制备蛋白微粒,不同的是,步骤(1)、步骤(2)和步骤(3)中玉米醇溶蛋白溶液、阿拉伯胶分散系和玉米醇溶蛋白分散系的ph值分别调至9.5,且更改步骤(4)中玉米醇溶蛋白和阿拉伯胶的质量比为1:1,更改步骤(5)中单宁酸溶液的加入量为25ml,最终得到玉米醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒a3。
63.采用体积排阻色谱测定该颗粒中阿拉伯胶、玉米醇溶蛋白的含量,得出玉米醇溶蛋白与阿拉伯胶的质量比为1:1.03;采用《单宁酸分析试验方法(ly/t 1642
‑
2005)》分析颗粒中单宁酸的含量,得出玉米醇溶蛋白与单宁酸的质量比为2:1.7。
64.实施例4
65.按照实施例1的方法制备蛋白微粒,不同的是,使用了小麦醇溶蛋白替代玉米醇溶蛋白,最终得到小麦醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒a4。
66.实施例5
67.按照实施例1的方法制备蛋白微粒,不同的是,使用了大麦醇溶蛋白替代玉米醇溶蛋白,最终得到大麦醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒a5。
68.实施例6
69.按照实施例1的方法制备蛋白微粒,不同的是,使用了茶多酚替代单宁酸,最终得到玉米醇溶蛋白
‑
茶多酚
‑
阿拉伯胶微粒a6。
70.实施例7
71.按照实施例1的方法制备蛋白微粒,不同的是,使用了表没食子儿茶素没食子酸酯替代单宁酸,最终得到玉米醇溶蛋白
‑
表没食子儿茶素没食子酸酯
‑
阿拉伯胶微粒a7。
72.对比例1
73.将5克玉米醇溶蛋白粉加入80%(v/v)乙醇/水中(100ml),室温连续搅拌1h,用0.1mol/l naoh溶液调节ph至9。将10克阿拉伯胶粉末加到240ml的超纯水(50℃)中,以600rpm的转速搅拌1h使阿拉伯胶充分水合,得到阿拉伯胶分散系。将玉米醇溶蛋白的乙醇溶液(20ml)以5ml/min的加入速度加到超纯水(100ml)中,制备玉米醇溶蛋白颗粒分散液。以玉米醇溶蛋白与阿拉伯胶为1:2的质量比将阿拉伯胶分散系以相对于每100ml的玉米醇溶蛋白分散系10ml/min的加入速度加至玉米蛋白颗粒分散系中,获得玉米醇溶蛋白颗粒
‑
阿拉伯胶分散液(zein
‑
ga),将所述分散液喷雾冻干后,得到玉米醇溶蛋白颗粒
‑
阿拉伯胶b。
74.对比例2
75.将5克玉米醇溶蛋白粉加入80%(v/v)乙醇/水中(100ml),室温连续搅拌1h,用0.1mol/l naoh溶液调节ph至9。将玉米醇溶蛋白的乙醇溶液(20ml)以相对于每100ml的超纯水5ml/min的加入速度加至超纯水(100ml)中,制备玉米醇溶蛋白颗粒分散系。将5ml质量浓度为4%的单宁酸溶液以相对于每100ml的含玉米醇溶蛋白和阿拉伯胶的分散系1ml/min的加入速度加至玉米醇溶蛋白颗粒分散系中,获得玉米醇溶蛋白颗粒
‑
单宁酸分散液(zein
‑
ta),将所述分散液喷雾冻干后,得到玉米醇溶蛋白颗粒
‑
单宁酸c。
76.对比例3
77.将玉米醇溶蛋白粉加入80%(v/v)乙醇/水中(100ml),室温连续搅拌1h,用0.1mol/l naoh溶液调节ph至9。将玉米醇溶蛋白的乙醇溶液(20ml)相对于每100ml的超纯水5ml/min的加入速度加至超纯水(100ml)中,制备玉米醇溶蛋白颗粒分散系(zp),将所述分散系喷雾冻干后室温贮藏,得到玉米醇溶蛋白颗粒d。
78.对比例4
79.将阿拉伯胶粉末加到240ml的超纯水(50℃)中,以600rpm的转速搅拌1h使阿拉伯胶充分水合。加5ml浓度为0.04g/ml的单宁酸溶液,获得阿拉伯胶
‑
单宁酸分散液(ga+ta),喷雾冻干后室温贮藏,得到阿拉伯胶
‑
单宁酸e。
80.对比例5
81.将阿拉伯胶粉(10g)加入240ml超纯水(50℃)中,600rpm搅拌1h,用0.1mol/l naoh溶液调节体系的ph至9,将分散液冷却至室温,得到阿拉伯胶分散液(ga),将所述分散液喷雾冻干后室温贮藏,得到阿拉伯胶f。
82.测试例1
83.针对上述实施例以及对比例制备得到的各分散液或颗粒进行颗粒稳定性检测。所用方法为:
84.(1)turbiscan仪器稳定性测试法。该仪器含有880nm波长的脉冲近红外光源,以及2个同步检测器用来测试体系的透射光强度和被反射的光强度。turbiscan稳定性分析仪应用多重光散射的原理,检测器所得到透射光和背散射光强度是直接由分散相的浓度(体积百分数)和平均直径(或是粒子/微滴/气泡的平均直径)决定的。通过测量透射光和背散射强度的变化,就可以知道样品在某一截面浓度或颗粒粒径的变化。仪器的工作原理为:测量探头收集透射光和背散射光的数据,在55mm长度上每40微米扫描一次。得到的图形在浓度上和粒子直径上表征了样品的均匀性,编辑其测量次数,然后沿着样品不断重复扫描,从而得到一张表征产品稳定性或不稳定特征的指纹图谱。
85.将实施例1及各对比例得到的分散液分为五组,分别添加氯化钠使其浓度为0.25、0.5、1、2和3mol/l,其中每组分别调节ph为4、7、8.5得到体系样品。取约20ml体系样品与圆柱形透明玻璃瓶中扫描24h。在本发明中,由于样品不透光,因此选择样品经过不同的放置时间后,被反射光强信号的变化情况来反应样品是否发生聚并、聚集、上浮或者沉淀。根据仪器自带的软件计算出体系的不稳定性指数,其计算公式为:
[0086][0087]
其中x
i
为在某一高度处单次测量所获得的体系的背散射光强值,x
bs
为体系自上而下扫描后所测得的xi的平均值,n为扫描的总次数。分别测定实施例1及各对比例组的分散液在不同ph和nacl浓度条件下的背散射光强变化,结果如图1a
‑
f所示。当ph为7或者4,nacl浓度为0.25、0.5、1、2和3mol/l时,在含有玉米醇溶蛋白
‑
阿拉伯胶b(图1b)、玉米醇溶蛋白
‑
单宁酸c(图1c)或玉米醇溶蛋白d(图1d)中的背散射光强变化程度显著高于实施例1制备的组别,证明本发明的方法能有效提高玉米醇溶蛋白质颗粒对盐的稳定性,按照本发明的方法制备得到的蛋白微粒对盐具有较高的稳定性。
[0088]
(2)粒径法。将冻干后的各实施例或对比例所述颗粒分散到100ml超纯水中,使样品分散液的计数率介于300~700counting rate/s,4℃条件下磁力搅拌12h,室温下放置2h后进行测试。取100μl样品分散于10ml超纯水中,向其中添加不同质量的氯化钠,使其浓度分别为0、0.25、0.5、1、2、3mol/l,并将ph值分别调至4、7和8.5。进行动态光散射测试,获得颗粒的布朗运动的自相关函数,通过拟合,仪器可自动计算其z
‑
平均直径。使用的仪器为nano zetasizer(英国malvern公司),检测所用的条件为:检测温度25℃,溶剂的折光指数为1.333,粘度为1.002mpa
·
s。
[0089]
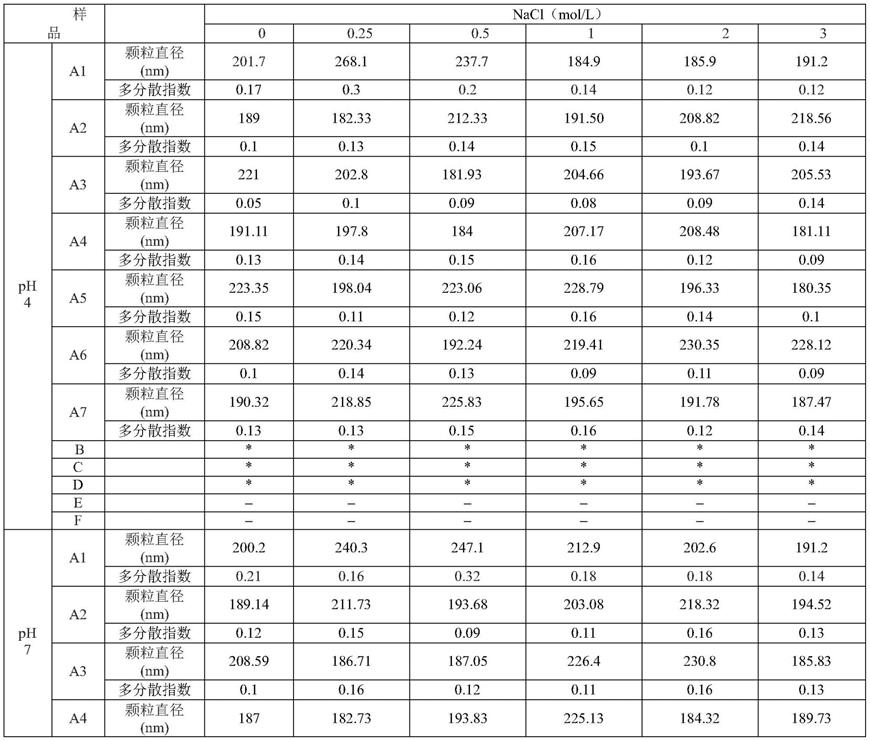
各实施例和对比例在不同ph和nacl浓度条件下的颗粒直径和多分散指数见表1。实施例1
‑
7制备得到的醇溶蛋白微粒a1
‑
a7的直径虽然随ph和nacl浓度发生变化,但是均在300nm范围内;而经过其他处理方式获得的玉米醇溶蛋白颗粒虽然在ph8.5,nacl浓度为0的情况下直径较小,但在其他条件下时由于发生聚集无法测试。
[0090]
将实施例1及各对比例得到的分散液分为五组,分别添加氯化钠使其浓度为0.25、0.5、1、2和3mol/l,其中每组分别调节ph为4、7、8.5。将上述分散液分别取12ml至15ml离心管中,室温下4500
×
g离心20min,离心后的状态如图2所示。当ph为8.5时,在没有nacl的情
况下,所有分散液中均没有观察到沉淀。nacl浓度为0.25、0.5、1、2和3mol/l时,在含有玉米醇溶蛋白
‑
阿拉伯胶b、玉米醇溶蛋白
‑
单宁酸c或玉米醇溶蛋白d的分散液中观察到明显的沉降。然而经过单宁酸处理后的玉米醇溶蛋白
‑
阿拉伯胶微粒a1分散液中没有观察沉淀,证明本发明所述方法制备得到的微粒能有效提高玉米醇溶蛋白质颗粒对盐的稳定性。当ph为7或者4时,除了实施例1制备得到的微粒组外,其它组别均出现不同程度的絮凝或者沉淀。上述结果说明使用本发明所述方法制备的微粒在不同ph条件下均具备抵抗盐离子的能力。
[0091]
表1
[0092]
[0093][0094]
(1)“*”为样品沉淀。
[0095]
(2)
“–”
表示没有准确数据。
[0096]
使用nano zetasizer对实施例1中玉米醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒分散液进行zeta
‑
电位值测定,分散液被超纯水稀释了200倍。ph值对实施例1中玉米醇溶蛋白
‑
单宁酸
‑
阿拉伯胶微粒分散液的zeta
‑
电位值的影响如图3所示,可发现所述微粒的zeta
‑
电位在ph3
‑
9的范围内均为负值,且在ph值为4、7、8.5时均稳定。
[0097]
通过上述结果可以看出,本发明的制备方法得到的蛋白颗粒在不同的ph值和不同nacl浓度下具有更好的稳定性。
[0098]
以上详细描述了本发明的优选实施方式,但是,本发明并不限于此。在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,包括各个技术特征以任何其它的合适方式进行组合,这些简单变型和组合同样应当视为本发明所公开的内容,均属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1