一种基于皮肤源脱细胞基质衍生支架及其构建方法
1.本发明属于组织工程学、材料学及生物学领域,提供一种由皮肤源脱细胞基质、明胶和壳聚糖三种材料复合的组织工程支架及其构建方法。
背景技术:
2.皮肤作为人体最大的器官,具有维持体内环境稳定和阻止微生物入侵的屏障作用,并发挥着体温调节、体液平衡、维生素d合成、废物排泄等重要功能。由于外界损伤或疾病等原因造成的皮肤缺损,往往会导致体液流失、病菌感染,对患者造成二次伤害,甚至威胁患者生命。皮肤组织工程作为一种新型的皮肤修复技术,具有高效、材料来源广泛、无免疫排斥、成本低等特点,弥补了传统的自体及异体移植技术的不足,从而近年来受到了广泛关注。
3.皮肤组织工程修复技术的首要步骤,是制备生物相容性好、无毒可降解、无免疫原性、有适宜机械强度,特别的具有一定抗菌性能的组织工程支架。然而单一材料难以同时满足以上所有要求,因此需要将不同性质与功能的材料进行复合,协同发挥多种材料的优点,以满足皮肤修复与愈合的需要。
4.脱细胞细胞外基质(decellularized extracellular matrix,decm)(以下简称为“脱细胞基质”或“decm”)是一种由动物组织经脱细胞技术将细胞及dna等抗原成分脱除得到的细胞外基质(extracellular matrix,ecm)。脱细胞基质最大限度地保留了组织的细胞外基质成分,如胶原、糖胺聚糖、透明质酸、弹力蛋白等,用其构建的支架可最真实的模拟细胞生长的内环境,有利于细胞的黏附、生长与分化,因此,近年来脱细胞基质在组织工程领域中受到广泛的关注。然而单独使用消化后的脱细胞基质构建细胞支架,其机械强度弱,在组织完全修复之前难以维持细胞生长的空间结构。随着组织工程技术的发展,越来越多的生物材料引起了学者们的关注,将其应用于皮肤组织工程中,如壳聚糖、明胶、海藻酸钠、纳米纤维等。其中,明胶(gelatin,gel)是一种由胶原蛋白部分水解的产物,含有类似arg
‑
gly
‑
asp(rgd)的序列,可促进细胞的黏附与迁移,具有良好的生物相容性,无免疫原性。明胶来源于胶原,但与胶原相比具有更高的机械强度。壳聚糖(chitosan,cs)是由天然几丁质去乙酰化制得,是一种含有丰富
‑
nh2和
‑
oh活性基团的线型多糖,易与其他聚合物通过化学键或氢键结合。壳聚糖同样是一种天然的生物材料,具有生物相容性、无免疫原性、可降解等优良性能,除此之外,壳聚糖具有一般生物材料不具备的广谱抗菌活性,因此,在组织工程及医学领域中具有广泛的应用。
5.明胶和壳聚糖在组织工程中领域已得到充分的认可和广泛的应用,但目前基于脱细胞基质的皮肤组织工程复合支架还未见报道。本发明通过脱细胞技术,将猪皮依次用胰酶法、triton
‑
x
‑
100法和dnase法进行脱细胞处理,用胃蛋白酶消化冻干的脱细胞基质后,与明胶、壳聚糖以一定的比例进行配比混合,冷冻干燥得到多孔的三维脱细胞基质衍生支架(decm/gel/cs)。通过检测,该脱细胞基质衍生支架表现出良好的机械强度、降解性和生物相容性,此外还表现出一定的广谱抗菌性能,在组织修复中具有潜在的应用价值。
技术实现要素:
6.本发明的内容旨在建立一种基于皮肤源的脱细胞基质衍生支架的构建方法及其在组织工程中的应用,该方法制备出的脱细胞基质衍生支架具有良好的机械强度、生物相容性及一定的广谱抗菌性能。
7.为了达到上述目的,本发明的技术方案如下:
8.一种基于皮肤源脱细胞基质衍生支架的构建方法,所述构建方法包括皮肤组织脱细胞处理、脱细胞基质溶液的制备和脱细胞基质/明胶/壳聚糖复合支架的构建三部分,具体步骤如下:
9.第一步,皮肤组织脱细胞处理,包括以下步骤:
10.(1)从市场购买新鲜的猪皮,将其洗净后剪成0.2~2.0cm2的小块,置于含有0.1wt%~1.0wt%的胰蛋白酶和1~5mm乙二胺四乙酸(edta)的pbs溶液中,10~50℃水浴条件下搅拌2~10h进行脱细胞,其搅拌速度为50~500rpm;
11.(2)将由步骤(1)得到的基质置于含有0.5~5.0wt%triton
‑
x
‑
100和5~50mm edta的pbs溶液中,室温条件下搅拌12~60h进行脱细胞,其搅拌速度为50~500rpm;
12.(3)将由步骤(2)得到的基质置于含有体积分数5~40%的异丙醇溶液中,常温条件下搅拌12~60h洗脱多余的脂肪,其搅拌速度为50~500rpm;
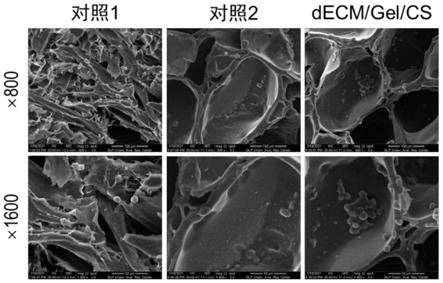
13.(4)将由步骤(3)得到的基质用pbs溶液在室温条件下清洗3~4次,每次间隔1h,用含有5~40mm mgcl2和10~80u/ml dnase的pbs溶液中,10~50℃水浴条件下搅拌12~60h进行完全脱细胞,其搅拌速度为50~500rpm;
14.(5)将由步骤(4)得到的基质分别用pbs溶液和蒸馏水在室温条件下清洗12~60h和0.1~1.0h,其搅拌速度为50~500rpm,再用含有0.1~1.0%过氧乙酸和2~10%乙醇的水溶液室温条件下搅拌1~5h进行灭菌,其搅拌速度为50~500rpm;
15.(6)将由步骤(5)得到的基质分别用pbs溶液和蒸馏水室温条件下搅拌2~3次,每间隔15min换液,其搅拌速度为50~500rpm。进而冷冻干燥12~60h得到脱细胞基质。
16.第二步,脱细胞基质溶解,包括以下步骤:
17.(7)将由步骤(6)得到的脱细胞基质,按5~40mg/100mg decm的比例称取胃蛋白酶,用0.5mol/l的醋酸溶液在4~40℃条件下搅拌溶解0.5~4wt%decm,其搅拌速度为50~500rpm;
18.第三步,脱细胞基质衍生支架的构建,包括以下步骤:
19.(8)在50℃加热条件下,称取1~5g的明胶(gel)和壳聚糖(cs)依次溶于0.5mol/l醋酸溶液中,得到gel/cs溶液;
20.(9)将步骤(7)得到的decm溶液与步骤(8)中的gel/cs溶液混合,低温搅拌,并用10mol/l的naoh溶液调节溶液的ph至5.0左右。所述的低温搅拌应为避免凝胶和产生气泡为宜,温度低于10℃,搅拌速度50~500rpm。
21.(10)将由步骤(9)得到的decm/gel/cs混合溶液缓慢倒入24孔板,在
‑
20℃冰箱冷冻6h后,冷冻干燥12~60h,再用交联剂交联12~60h。所述的交联剂为1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二亚胺盐酸盐(edc)、n
‑
羟基琥珀酰亚胺(nhs)、乙磺酸(mes)和乙醇的混合溶液。其中mes作为交联剂的缓冲液,edc、nhs和mes的浓度均为50mmol/l,乙醇溶液的体积分数为10~80%。
22.(11)交联后的脱细胞基质衍生支架用na2hpo4中和多余的酸,再分别用pbs缓冲液和蒸馏水清洗2~3次,每间隔30min换液。最后,将清洗后的支架在
‑
20℃冰箱冷冻6h,冷冻干燥器冻干12~60h得到decm/gel/cs脱细胞基质衍生支架。
23.采用上述方法制备得到的脱细胞基质衍生支架包含的三种材料decm、gel和cs均为可降解的生物材料,具有很高的生物相容性、无免疫原性和无毒性等。其中,decm是细胞赖以生存的脱细胞细胞外基质成分,最大限度地保留细胞外基质生物活性物质,gel含有丰富的rgd序列,有利于细胞的黏附、生长和繁殖。同时,该支架具有丰富的三维多孔结构,孔径主要分布于40
‑
150μm(大孔直径约150μm,小孔直径约40μm);孔隙率90.36~95.47%;3s的接触角为52.0~68.9
°
;溶胀率501.43~944.95%;蛋白吸收率57.09~77.47%;压缩模量4.82~7.19mpa;在15d的溶菌酶降解率为80.04~91.05%。
24.上述方案中脱细胞基质/明胶/壳聚糖(decm/gel/cs)复合支架的制备方法,所制备的decm/gel/cs复合支架,对成纤维细胞表现出良好的生物学性能,适用于皮肤组织工程领域。
25.本发明相对于现有技术,具有如下的优点和有益效果:
26.(1)本发明选用猪皮源脱细胞基质作为基体材料,复合明胶和壳聚糖制备复合多孔支架,实现材料功能的优势互补。猪皮来源广泛且成本较低,同时细胞外基质是细胞在生长过程中合成和分泌的一种物质,因此选用猪皮源脱细胞基质作为基体材料,最大限度提供了成纤维细胞的天然生长微环境;复合明胶以提高支架的机械强度的同时,增加支架的细胞黏附性;复合壳聚糖以提高支架机械强度和吸水性的同时,赋予支架广谱抗菌性能。
27.(2)本发明获得的复合支架具有大孔小孔相连和大孔包小孔的多孔结构,大孔直径在150μm左右,能为细胞提供充足的增殖空间;小孔直径在40μm左右,接近于天然的细胞外基质孔径大小(30μm左右),能增加支架的传质能力并为细胞提供丰富的附着位点。
28.(3)本发明制备的复合支架的孔隙率90.36~95.47%(对照组84.45
±
3.55%);3s的接触角为52.0~68.9
°
(对照组70
±
0.4
°
);4h的溶胀率501.43~944.95%(对照组299.58
±
11.30%);24h的蛋白吸收率57.09~77.47%(18.55
±
7.32%);在15d的溶菌酶降解率80.04~91.05%(对照组28.49
±
2.06%)等,各项检测结果都显示,该复合支架性能良好,能满足皮肤组织工程对细胞支架的需求。
29.(4)本发明制备的复合支架相对于天然的细胞外基质支架具有明显的抗菌性能,且抗菌性能稳定,这对于皮肤组织修复过程中抗感染的要求具有重要的意义。
附图说明
30.图1为脱细胞基质与未脱细胞组织的sem、h&e、masson三染、阿尔新蓝染色图;
31.图2为decm(对照1)、gel/cs(对照2)(质量比3:1)和decm/gel/cs(质量比1:3:1)支架的sem图;
32.图3为decm(对照1)、gel/cs(对照2)(质量比3:1)和decm/gel/cs(质量比1:3:2)支架的抗菌性能对比图;
33.图4为l929成纤维细胞在decm(对照1)、gel/cs(对照2)(质量比3:1)和decm/gel/cs(质量比1:3:1)支架上生长的sem对比图;
34.图5为l929成纤维细胞在decm(对照1)、gel/cs(对照2)(质量比3:1)和decm/gel/
cs(质量比1:3:1)支架上生长的激光共聚焦对比图。
具体实施方式
35.以下结合附图和具体实施例对本发明做进一步的说明,但本发明不以任何形式受限于实施例内容,在不脱离前后所述宗旨的范围内,所有基于本发明基本思想的修改和变动,都属于本发明请求技术保护的范围。
36.实施例1脱细胞细胞外基质支架的制备(作为对比例)及脱细胞效率的检测
37.(1)从市场购买新鲜的猪皮,将其洗净后剪成1.0cm2的小块,置于含有0.5wt%的胰蛋白酶和5mm乙二胺四乙酸(edta)的pbs溶液中,30℃水浴条件下搅拌8h进行脱细胞,其搅拌速度为300rpm;
38.(2)将由步骤(1)得到的基质置于含有5.0wt%triton
‑
x
‑
100和20mm edta的pbs溶液中,室温条件下搅拌48h进行脱细胞,其搅拌速度为300rpm;
39.(3)将由步骤(2)得到的基质置于含有20%的异丙醇水溶液中,常温条件下搅拌24h洗脱多余的脂肪,其搅拌速度为300rpm;
40.(4)将由步骤(3)得到的基质用pbs溶液在室温条件下清洗3次,每次间隔1h,用含有20mm mgcl2和50u/ml dnase的pbs溶液中,30℃水浴条件下搅拌24h进行完全脱细胞,其搅拌速度为300rpm;
41.(5)将由步骤(4)得到的基质分别用pbs溶液和蒸馏水在室温条件下清洗24h和1.0h,其搅拌速度为300rpm,再用含有1.0%过氧乙酸和10%乙醇的水溶液室温条件下搅拌3h进行灭菌,其搅拌速度为300rpm;
42.(6)将由步骤(5)得到的基质分别用pbs溶液和蒸馏水室温条件下搅拌3次,每间隔15min换液,其搅拌速度为300rpm。进而冷冻干燥24h得到脱细胞细胞外基质支架。
43.本发明对猪皮脱细胞基质的脱细胞效率进行了定性和定量两方面的检测。通过定性方面的检测,从图1中的sem可以看出,经脱细胞后的脱细胞基质是多孔多纤维结构,没有细胞或组织残留;从h&e染色中发现decm不含有深蓝色的细胞核;从masson染色图中发现decm保留了大量的胶原;从阿尔新蓝染色图发现decm保留了大部分的糖胺聚糖,初步判断decm脱细胞效果较好。经进一步的定量检测发现,decm后的胶原相比未脱细胞的含量有所提高,约113%;gags保留了96%,而dna的含量是未脱细胞的1.9%,因此,该脱细胞技术脱细胞效率较高。
44.实施例2明胶/壳聚糖(gel/cs)复合支架的制备(作为对比例)
45.(1)称取3g的明胶(gel)和1g的壳聚糖(cs)依次加入到100ml 0.5mol/l醋酸溶液中,在50℃加热条件下搅拌溶解。
46.(2)将步骤(1)中的gel/cs溶液缓慢倒入24孔板,在
‑
20℃冰箱冷冻12h后,用冷冻干燥器冻干24h得到多孔复合支架。
47.(3)步骤(2)中的复合支架用交联剂室温交联24h。所述的交联剂为1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二亚胺盐酸盐(edc)、n
‑
羟基琥珀酰亚胺(nhs)、乙磺酸(mes)和乙醇的混合溶液。其中mes作为交联剂的缓冲液,edc、nhs和mes的浓度均为50mmol/l,乙醇溶液的体积分数为60%。
48.(4)交联后的gel/cs支架用0.1mol/l的na2hpo4中和多余的酸,再分别用pbs缓冲液
和蒸馏水清洗3次,每间隔30min换液。最后,将清洗后的支架在
‑
20℃冰箱冷冻12h,通过冷冻干燥器冻干24h得到gel/cs复合支架。
49.实施例3脱细胞基质/明胶/壳聚糖(decm/gel/cs)复合支架的制备
50.(1)从市场购买新鲜的猪皮,将其洗净后剪成0.2cm2的小块,置于含有0.1wt%的胰蛋白酶和1mm乙二胺四乙酸(edta)的pbs溶液中,10℃水浴条件下搅拌2h进行脱细胞,其搅拌速度为100rpm;
51.(2)将由步骤(1)得到的基质置于含有0.5wt%triton
‑
x
‑
100和5mm edta的pbs溶液中,室温条件下搅拌12h进行脱细胞,其搅拌速度为100rpm;
52.(3)将由步骤(2)得到的基质置于含有5%的异丙醇水溶液中,常温条件下搅拌12h洗脱多余的脂肪,其搅拌速度为100rpm;
53.(4)将由步骤(3)得到的基质用pbs溶液在室温条件下清洗3~4次,每次间隔1h,用含有5mm mgcl2和10u/ml dnase的pbs溶液中,10℃水浴条件下搅拌12h进行完全脱细胞,其搅拌速度为100rpm;
54.(5)将由步骤(4)得到的基质分别用pbs溶液和蒸馏水在室温条件下清洗12h和0.1h,其搅拌速度为100rpm,再用含有0.1%过氧乙酸和2%乙醇的水溶液室温条件下搅拌1h进行灭菌,其搅拌速度为100rpm;
55.(6)将由步骤(5)得到的基质分别用pbs溶液和蒸馏水室温条件下搅拌2~3次,每间隔15min换液,其搅拌速度为100rpm。进而冷冻干燥12h得到脱细胞基质。
56.(7)将由步骤(6)得到的脱细胞基质,按5mg/100mg decm的比例称取胃蛋白酶,用0.5mol/l的醋酸溶液在4℃条件下搅拌溶解0.5wt%decm,其搅拌速度为100rpm;
57.(8)在40℃加热条件下,称取1g的明胶(gel)和壳聚糖(cs)依次溶于0.5mol/l醋酸溶液中,得到gel/cs溶液;
58.(9)将步骤(7)得到的decm溶液与步骤(8)中的gel/cs溶液混合,低温搅拌,并用10mol/l的naoh溶液调节溶液的ph至5.0左右。所述的低温搅拌应为避免凝胶和产生气泡为宜,温度低于10℃,搅拌速度100rpm。
59.(10)将由步骤(9)得到的decm/gel/cs混合溶液缓慢倒入24孔板,在
‑
20℃冰箱冷冻6h后,冷冻干燥12h,再用交联剂交联12h。所述的交联剂为1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二亚胺盐酸盐(edc)、n
‑
羟基琥珀酰亚胺(nhs)、乙磺酸(mes)和乙醇的混合溶液。其中mes作为交联剂的缓冲液,edc、nhs和mes的浓度均为50mmol/l,乙醇溶液的体积分数为10%。
60.(11)交联后的脱细胞基质衍生支架用0.1mol/l的na2hpo4中和多余的酸,再分别用pbs缓冲液和蒸馏水清洗2~3次,每间隔30min换液。最后,将清洗后的支架在
‑
20℃冰箱冷冻6h,通过冷冻干燥器冻干12h得到decm/gel/cs脱细胞基质衍生支架。
61.本发明对脱细胞基质衍生支架的各方面性能进行了检测。从图2可以看出,脱细胞基质衍生支架是大孔小孔相连和大孔包小孔的多孔结构,大孔直径约150μm,能为细胞提供充足的增殖空间;小孔直径约40μm,接近于天然的细胞外基质孔径大小(30μm左右),能增加支架的传质能力并为细胞提供丰富的附着位点。通过检测,其孔隙率90.36~95.47%,3s的接触角为52.0~68.9
°
,溶胀率501.43~944.95%,蛋白吸收率57.09~77.47%,压缩模量4.82~7.19mpa,在15d的溶菌酶降解率80.04~91.05%。对支架进行抗菌性能检测,从图3可以看出,添加壳聚糖的支架具有一定的抗菌性能,且随着壳聚糖的量增加,其抗菌性能增
加。在支架上接种l929成纤维细胞,检测支架的生物相容性,从图4中的sem和图5中的激光共聚焦图可以看出,相对于天然的脱细胞基质支架,脱细胞基质衍生支架具有更高的孔隙率,有利于细胞的生长;相对于gel/cs支架,添加decm的脱细胞基质衍生支架能为细胞提供更有利于其生长的微环境,因此细胞密度更高。
62.实施例4脱细胞基质/明胶/壳聚糖(decm/gel/cs)复合支架的制备
63.(1)从市场购买新鲜的猪皮,将其洗净后剪成0.5cm2的小块,置于含有0.2wt%的胰蛋白酶和2mm乙二胺四乙酸(edta)的pbs溶液中,20℃水浴条件下搅拌4h进行脱细胞,其搅拌速度为200rpm;
64.(2)将由步骤(1)得到的基质置于含有1.0wt%triton
‑
x
‑
100和10mm edta的pbs溶液中,室温条件下搅拌24h进行脱细胞,其搅拌速度为200rpm;
65.(3)将由步骤(2)得到的基质置于含有10%的异丙醇水溶液中,常温条件下搅拌24h洗脱多余的脂肪,其搅拌速度为200rpm;
66.(4)将由步骤(3)得到的基质用pbs溶液在室温条件下清洗3~4次,每次间隔1h,用含有10mm mgcl2和20u/ml dnase的pbs溶液中,20℃水浴条件下搅拌24h进行完全脱细胞,其搅拌速度为200rpm;
67.(5)将由步骤(4)得到的基质分别用pbs溶液和蒸馏水在室温条件下清洗24h和0.2h,其搅拌速度为200rpm,再用含有0.2%过氧乙酸和4%乙醇的水溶液室温条件下搅拌2h进行灭菌,其搅拌速度为200rpm;
68.(6)将由步骤(5)得到的基质分别用pbs溶液和蒸馏水室温条件下搅拌2~3次,每间隔15min换液,其搅拌速度为200rpm。进而冷冻干燥24h得到脱细胞基质。
69.(7)将由步骤(6)得到的脱细胞基质,按10mg/100mg decm的比例称取胃蛋白酶,用0.5mol/l的醋酸溶液在10℃条件下搅拌溶解1wt%decm,其搅拌速度为200rpm;
70.(8)在50℃加热条件下,称取2g的明胶(gel)和壳聚糖(cs)依次溶于0.5mol/l醋酸溶液中,得到gel/cs溶液;
71.(9)将步骤(7)得到的decm溶液与步骤(8)中的gel/cs溶液混合,低温搅拌,并用10mol/l的naoh溶液调节溶液的ph至5.0左右。所述的低温搅拌应为避免凝胶和产生气泡为宜,温度低于10℃,搅拌速度200rpm。
72.(10)将由步骤(9)得到的decm/gel/cs混合溶液缓慢倒入24孔板,在
‑
20℃冰箱冷冻6h后,冷冻干燥24h,再用交联剂交联24h。所述的交联剂为1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二亚胺盐酸盐(edc)、n
‑
羟基琥珀酰亚胺(nhs)、乙磺酸(mes)和乙醇的混合溶液。其中mes作为交联剂的缓冲液,edc、nhs和mes的浓度均为50mmol/l,乙醇溶液的体积分数为20%。
73.(11)交联后的脱细胞基质衍生支架用0.1mol/l的na2hpo4中和多余的酸,再分别用pbs缓冲液和蒸馏水清洗2~3次,每间隔30min换液。最后,将清洗后的支架在
‑
20℃冰箱冷冻6h,通过冷冻干燥器冻干24h得到decm/gel/cs脱细胞基质衍生支架。
74.实施例5脱细胞基质/明胶/壳聚糖(decm/gel/cs)复合支架的制备
75.(1)从市场购买新鲜的猪皮,将其洗净后剪成1cm2的小块,置于含有0.4wt%的胰蛋白酶和3mm乙二胺四乙酸(edta)的pbs溶液中,30℃水浴条件下搅拌6h进行脱细胞,其搅拌速度为300rpm;
76.(2)将由步骤(1)得到的基质置于含有2.0wt%triton
‑
x
‑
100和20mm edta的pbs溶
液中,室温条件下搅拌36h进行脱细胞,其搅拌速度为300rpm;
77.(3)将由步骤(2)得到的基质置于含有20%的异丙醇水溶液中,常温条件下搅拌36h洗脱多余的脂肪,其搅拌速度为300rpm;
78.(4)将由步骤(3)得到的基质用pbs溶液在室温条件下清洗3~4次,每次间隔1h,用含有20mm mgcl2和40u/ml dnase的pbs溶液中,30℃水浴条件下搅拌36h进行完全脱细胞,其搅拌速度为300rpm;
79.(5)将由步骤(4)得到的基质分别用pbs溶液和蒸馏水在室温条件下清洗36h和0.4h,其搅拌速度为300rpm,再用含有0.4%过氧乙酸和6%乙醇的水溶液室温条件下搅拌3h进行灭菌,其搅拌速度为300rpm;
80.(6)将由步骤(5)得到的基质分别用pbs溶液和蒸馏水室温条件下搅拌2~3次,每间隔15min换液,其搅拌速度为300rpm。进而冷冻干燥36h得到脱细胞基质。
81.(7)将由步骤(6)得到的脱细胞基质,按20mg/100mg decm的比例称取胃蛋白酶,用0.5mol/l的醋酸溶液在20℃条件下搅拌溶解2wt%decm,其搅拌速度为300rpm;
82.(8)在50℃加热条件下,称取3g的明胶(gel)和壳聚糖(cs)依次溶于0.5mol/l醋酸溶液中,得到gel/cs溶液;
83.(9)将步骤(7)得到的decm溶液与步骤(8)中的gel/cs溶液混合,低温搅拌,并用10mol/l的naoh溶液调节溶液的ph至5.0左右。所述的低温搅拌应为避免凝胶和产生气泡为宜,温度低于10℃,搅拌速度300rpm。
84.(10)将由步骤(9)得到的decm/gel/cs混合溶液缓慢倒入24孔板,在
‑
20℃冰箱冷冻6后,冷冻干燥36h,再用交联剂交联36h。所述的交联剂为1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二亚胺盐酸盐(edc)、n
‑
羟基琥珀酰亚胺(nhs)、乙磺酸(mes)和乙醇的混合溶液。其中mes作为交联剂的缓冲液,edc、nhs和mes的浓度均为50mmol/l,乙醇溶液的体积分数为40%。
85.(11)交联后的脱细胞基质衍生支架用0.1mol/l的na2hpo4中和多余的酸,再分别用pbs缓冲液和蒸馏水清洗2~3次,每间隔30min换液。最后,将清洗后的支架在
‑
20℃冰箱冷冻6h,通过冷冻干燥器冻干36h得到decm/gel/cs脱细胞基质衍生支架。
86.实施例6脱细胞基质/明胶/壳聚糖(decm/gel/cs)复合支架的制备
87.(1)从市场购买新鲜的猪皮,将其洗净后剪成1.5cm2的小块,置于含有0.8wt%的胰蛋白酶和4mm乙二胺四乙酸(edta)的pbs溶液中,40℃水浴条件下搅拌8h进行脱细胞,其搅拌速度为400rpm;
88.(2)将由步骤(1)得到的基质置于含有4.0wt%triton
‑
x
‑
100和40mm edta的pbs溶液中,室温条件下搅拌48h进行脱细胞,其搅拌速度为400rpm;
89.(3)将由步骤(2)得到的基质置于含有30%的异丙醇水溶液中,常温条件下搅拌48h洗脱多余的脂肪,其搅拌速度为400rpm;
90.(4)将由步骤(3)得到的基质用pbs溶液在室温条件下清洗3~4次,每次间隔1h,用含有30mm mgcl2和60u/ml dnase的pbs溶液中,40℃水浴条件下搅拌48h进行完全脱细胞,其搅拌速度为400rpm;
91.(5)将由步骤(4)得到的基质分别用pbs溶液和蒸馏水在室温条件下清洗48h和0.8h,其搅拌速度为400rpm,再用含有0.8%过氧乙酸和8%乙醇的水溶液室温条件下搅拌4h进行灭菌,其搅拌速度为400rpm;
92.(6)将由步骤(5)得到的基质分别用pbs溶液和蒸馏水室温条件下搅拌2~3次,每间隔15min换液,其搅拌速度为400rpm。进而冷冻干燥48h得到脱细胞基质。
93.(7)将由步骤(6)得到的脱细胞基质,按30mg/100mg decm的比例称取胃蛋白酶,用0.5mol/l的醋酸溶液在30℃条件下搅拌溶解3wt%decm,其搅拌速度为400rpm;
94.(8)在50℃加热条件下,称取4g的明胶(gel)和壳聚糖(cs)依次溶于0.5mol/l醋酸溶液中,得到gel/cs溶液;
95.(9)将步骤(7)得到的decm溶液与步骤(8)中的gel/cs溶液混合,低温搅拌,并用10mol/l的naoh溶液调节溶液的ph至5.0左右。所述的低温搅拌应为避免凝胶和产生气泡为宜,温度低于10℃,搅拌速度400rpm。
96.(10)将由步骤(9)得到的decm/gel/cs混合溶液缓慢倒入24孔板,在
‑
20℃冰箱冷冻6h后,冷冻干燥48h,再用交联剂交联48h。所述的交联剂为1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二亚胺盐酸盐(edc)、n
‑
羟基琥珀酰亚胺(nhs)、乙磺酸(mes)和乙醇的混合溶液。其中mes作为交联剂的缓冲液,edc、nhs和mes的浓度均为50mmol/l,乙醇溶液的体积分数为60%。
97.(11)交联后的脱细胞基质衍生支架用0.1mol/l的na2hpo4中和多余的酸,再分别用pbs缓冲液和蒸馏水清洗2~3次,每间隔30min换液。最后,将清洗后的支架在
‑
20℃冰箱冷冻6h,通过冷冻干燥器冻干48h得到decm/gel/cs脱细胞基质衍生支架。
98.实施例7脱细胞基质/明胶/壳聚糖(decm/gel/cs)复合支架的制备
99.(1)从市场购买新鲜的猪皮,将其洗净后剪成2.0cm2的小块,置于含有1.0wt%的胰蛋白酶和5mm乙二胺四乙酸(edta)的pbs溶液中,50℃水浴条件下搅拌10h进行脱细胞,其搅拌速度为500rpm;
100.(2)将由步骤(1)得到的基质置于含有5.0wt%triton
‑
x
‑
100和50mm edta的pbs溶液中,室温条件下搅拌60h进行脱细胞,其搅拌速度为500rpm;
101.(3)将由步骤(2)得到的基质置于含有40%的异丙醇水溶液中,常温条件下搅拌60h洗脱多余的脂肪,其搅拌速度为500rpm;
102.(4)将由步骤(3)得到的基质用pbs溶液在室温条件下清洗3~4次,每次间隔1h,用含有40mm mgcl2和80u/ml dnase的pbs溶液中,50℃水浴条件下搅拌60h进行完全脱细胞,其搅拌速度为500rpm;
103.(5)将由步骤(4)得到的基质分别用pbs溶液和蒸馏水在室温条件下清洗60h和1.0h,其搅拌速度为500rpm,再用含有1.0%过氧乙酸和10%乙醇的水溶液室温条件下搅拌5h进行灭菌,其搅拌速度为500rpm;
104.(6)将由步骤(5)得到的基质分别用pbs溶液和蒸馏水室温条件下搅拌2~3次,每间隔15min换液,其搅拌速度为500rpm。进而冷冻干燥60h得到脱细胞基质。
105.(7)将由步骤(6)得到的脱细胞基质,按40mg/100mg decm的比例称取胃蛋白酶,用0.5mol/l的醋酸溶液在40℃条件下搅拌溶解4wt%decm,其搅拌速度为500rpm;
106.(8)在50℃加热条件下,称取5g的明胶(gel)和壳聚糖(cs)依次溶于0.5mol/l醋酸溶液中,得到gel/cs溶液;
107.(9)将步骤(7)得到的decm溶液与步骤(8)中的gel/cs溶液混合,低温搅拌,并用10mol/l的naoh溶液调节溶液的ph至5.0左右。所述的低温搅拌应为避免凝胶和产生气泡为宜,温度低于10℃,搅拌速度500rpm。
108.(10)将由步骤(9)得到的decm/gel/cs混合溶液缓慢倒入24孔板,在
‑
20℃冰箱冷冻6后,冷冻干燥60h,再用交联剂交联60h。所述的交联剂为1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二亚胺盐酸盐(edc)、n
‑
羟基琥珀酰亚胺(nhs)、乙磺酸(mes)和乙醇的混合溶液。其中mes作为交联剂的缓冲液,edc、nhs和mes的浓度均为50mmol/l,乙醇溶液的体积分数为80%。
109.(11)交联后的脱细胞基质衍生支架用0.1mol/l的na2hpo4中和多余的酸,再分别用pbs缓冲液和蒸馏水清洗2~3次,每间隔30min换液。最后,将清洗后的支架在
‑
20℃冰箱冷冻6h,通过冷冻干燥器冻干60h得到decm/gel/cs脱细胞基质衍生支架。
110.以上所述实施例仅表达本发明的实施方式,但并不能因此而理解为对本发明专利范围的限制,对于本领域的技术人员来说,依据本发明的思想,在具体实施方式及应用范围上的改变之处,均属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1