一种用于皮肤修复的脐带血来源的富血小板血浆生物制剂及其制备方法和应用与流程
本发明创造属于血浆制剂领域,尤其是涉及一种用于皮肤修复的脐带血来源的富血小板血浆生物制剂及其制备方法和应用。
背景技术:
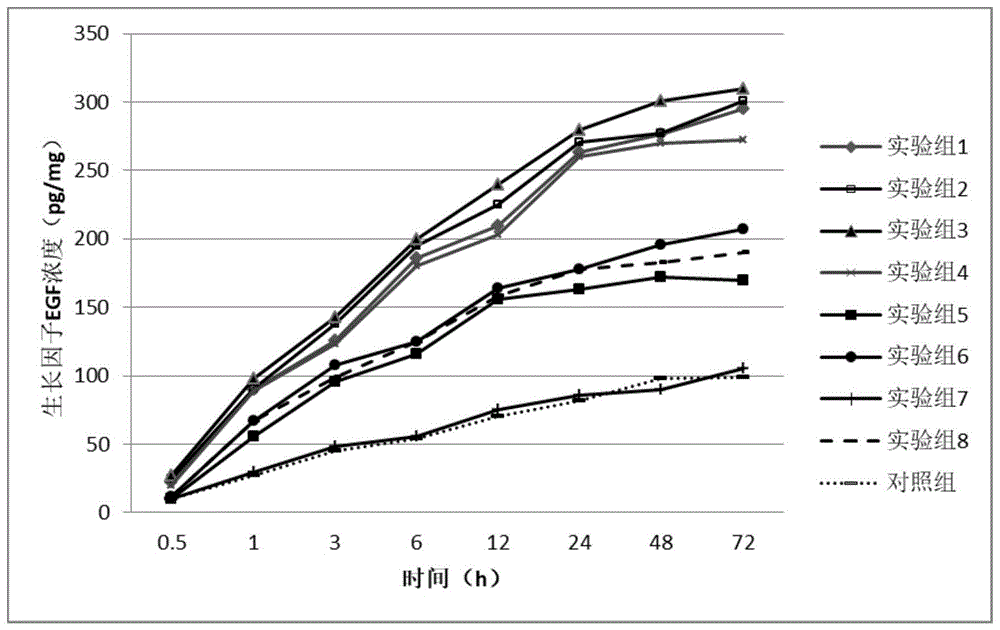
:沙棘(hippophaerhamnoideslinn)属于胡颓子科沙棘属植物,落叶灌木或小乔木,又名沙枣、酸柳。沙棘为药食同源植物。沙棘的根、茎、叶、花、果,特别是沙棘果实含有丰富的营养物质和生物活性物质,具有很高的药用价值,可以广泛应用于食品、医药等领域。近几年来对沙棘多糖功能的研究主要集中在抗病毒、抑菌作用、抗氧化和降血脂作用及保肝、护肝等方面。如沙棘果皮中的多糖能够显著抑制引发病毒性心肌炎的柯萨奇病毒b的扩增;沙棘果多糖具有明显的抗氧化活性,体外能够清除dpph自由基、羟自由基和超氧阴离子等自由基。沙棘多糖通过分离纯化可制备得到2个多糖级分:中性多糖hrwp-n和酸性多糖hrwp-a,hrwp-a是不含任何蛋白质的白色粉末,其总碳水化合物和糖醛酸含量分别测定为97.52%和96.54%。hrwp-a的分子量分布均一,是一种天然的高甲氧基hg型果胶(王海亮,沙棘多糖对神经系统相关疾病的药效学研究,吉林大学,博士论文,2019)。但酸性多糖hrwp-a对于皮肤修复是否具有作用鲜有研究和报道。魔芋葡甘露聚糖(konjacglucomannan,kgm)是一种水溶性杂多糖,由d-葡萄糖和d-甘露糖以β-1,4糖苷键连接而成,主链上带有少量乙酰基,由于其良好的胶溶、凝胶、成膜性能,被广泛的应用于食品,化工和医药领域,但是单一的魔芋葡甘露聚糖成膜后易溶于水,目前对其研究主要集中在魔芋葡甘露聚糖的疏水性修饰以及与壳聚糖、明胶、纤维素、羧甲基纤维素、pvp等混合成膜用于药物的控释以及生物支架。富血小板血浆(platelet-richplasma,prp),是自体全血经离心后得到的血小板浓缩物。prp中含有大量生长因子及蛋白质。在富血小板血浆活化后,可将这些生长因子释放,这些生长因子主要包括血小板源性生长因子、血管内皮细胞生长因子、转化生长因子、成纤维细胞生长因子、胰岛素样生长因子以及表皮细胞生长因子和血小板因-4等。有研究表明,prp主要通过其释放的多种生长因子和细胞因子来发挥组织再生及促进愈合的作用。技术实现要素:有鉴于此,本发明创造旨在克服现有技术中的缺陷,提出一种用于皮肤修复的脐带血来源的富血小板血浆生物制剂及其应用。为达到上述目的,本发明创造的技术方案是这样实现的:一种用于皮肤修复的脐带血来源的富血小板血浆生物制剂,所述生物制剂为负载有葡甘露聚糖和酸性沙棘多糖的脐带血来源的富血小板血浆,其中,所述富血小板血浆中血小板浓度为1×108-1×109个/ml;每ml富血小板血浆中含有葡甘露聚糖的质量为0.05-0.12μg,酸性沙棘多糖的质量为0.1-0.3μg。优选的,每ml富血小板血浆中含有葡甘露聚糖的质量为0.1μg,酸性沙棘多糖的质量为0.3μg。优选的,所述葡甘露聚糖的重均分子量为5000-10000da。本发明还提供一种上述富血小板血浆生物制剂的制备方法,该方法包括如下步骤:将经过活化处理的脐带血来源的富血小板血浆与葡甘露聚糖、酸性沙棘多糖混合均匀后倒入容器中,-20℃放置10-12h,-70℃放置5-8h,真空冻干机冻干,得到生物制剂,密封后钴60照射灭菌,避光保存备用。本发明还提供一种上述富血小板血浆生物制剂在制备创面修复和/或皮肤修复药物或材料上的应用。本发明还提供一种外用液体辅料,其中的活性成分为上述的生物制剂,所述活性成分的质量百分比为1%-3%,还包括外用辅料。优选的,所述外用辅料包括质量百分比为1-5%的壳聚糖、1-8%的聚乙烯醇和0.2-1%抗坏血酸,余量为纯化水。优选的,所述壳聚糖的平均分子量为20-300kda,脱乙酰度大于90%。相对于现有技术,本发明创造具有以下优势:本发明创造的发明人在研究富血小板血浆在促进皮肤创伤和术后愈合的过程中发现葡甘露聚糖、酸性沙棘多糖复配后能够加快富血小板血浆中生长因子的释放速率,激发富血小板血浆中生物活性因子的修复功能,加快伤口愈合,相较于单独的葡甘露聚糖或酸性沙棘多糖,复配后的生物制剂在模拟体液中的释放量增大;在小鼠创面修复试验中,使用本发明的液体敷料小鼠创面的愈合速度明显加快。附图说明图1-3为三种不同的生长因子egf、vegf和bfgf在sbf中的释放情况。具体实施方式除有定义外,以下实施例中所用的技术术语具有与本发明创造所属领域技术人员普遍理解的相同含义。以下实施例中所用的试验试剂,如无特殊说明,均为常规生化试剂;所述实验方法,如无特殊说明,均为常规方法。下面结合实施例来详细说明本发明创造。实施例1制备脐带血来源的富血小板血浆选用足月健康剖宫产新生儿出生后获得脐带血,其中捐献者必须经过严格体检,包括各项病毒检测、传染病检测,签署知情同意书和捐赠协议。将经过枸橼酸钠抗凝处理后脐带血放置在高速低温台式离心机进行两次离心,第一次离心条件为460×g,离心10min,全血分为2层,吸取上层的血浆层;第二次离心条件为1500×g,20min离心后,弃掉上层的血浆,得到血小板白色沉淀,用第一次离心的血浆重悬白色沉淀,得到富血小板血浆(prp)。prp中的血小板计数采用全自动血细胞计数仪(nexcelom,美国),保证prp中血小板浓度为1×108-1×109个/ml。实施例2制备酸性沙棘多糖(1)将沙棘果实风干研磨粉碎后加入95%的乙醇60℃回流12h除杂,将提取后的果渣过滤后干燥,再用90℃的热水浸提3次得到水提液,将水提液离心(5000rpm,30min)后,收集上清液,合并、浓缩比为10:1,95%的乙醇加入上清液中至用乙醇的浓度至80%,离心收集沉淀,真空干燥得到沙棘粗多糖。将沙棘粗多糖溶于水(5%w/v),离心(10000rpm,30min)除去不溶物,将上清液上样到deae-纤维素柱(购自amershampharmaciabiotech)上,然后用0.5mnacl洗脱。收集洗脱液,浓缩至原体积的1/10,透析除盐,冷冻干燥,得到沙棘总多糖hrwp。(2)将沙棘总多糖hrwp溶于蒸馏水,配成5%w/v的多糖水溶液,上样到deae-纤维素柱,依次用5倍柱体积的蒸馏水和0.5mnacl洗脱,分别收集洗脱液。0.5mnacl洗脱部分,透析除盐,冷冻干燥,得到酸性多糖级分。酸性多糖级分,依次通过sephadexg-75凝胶过滤柱层析和deae-sepharosefastflow离子交换柱层析进一步纯化,得到酸性多糖hrwp-a。实施例3葡甘露聚糖的制备取魔芋精粉溶胀,加0.03%的纤维素酶在50℃的水浴中进行酶解45min,100℃灭酶10min后加入枸橼酸钠搅拌5h,离心(10000rpm,30min)后取上清液进行超滤分级得到魔芋葡甘露聚糖粗品,将粗品经过脱糖、脱脂、sevag法脱蛋白、透析、浓缩后再分别经过40%、60%和80%乙醇分步进行沉淀,最后冷冻干燥后得到魔芋葡甘露聚糖,采用高效液相凝胶色谱法(hpgpc)测量得到的魔芋葡甘露聚糖的重均分子量为8.8kda。实施例4生物制剂的制备将脐带血来源的富血小板血浆prp与10%cacl2按照9:1的比例迅速混合,于室温下静置1h,然后放于4℃冰箱过夜。与葡甘露聚糖kgm-ⅰ、中性沙棘多糖hrwp-n混合均匀后倒入容器中,具体配比见表1,-20℃放置10-12h,-70℃放置5-8h,真空冻干机冻干,得到生物制剂prp/kgm-ⅰ/hrwp-n,密封后钴60照射灭菌,避光保存备用。试验例1生长因子释放速率实验按照表1的配比配置生物制剂prp/kgm-ⅰ/hrwp-n,分别测试不同配比的prp/kgm-ⅰ/hrwp-n在模拟体液(sbf,购自北京雷根生物技术有限公司)中的三种生长因子egf、vegf和bfgf释放速率。表1生物制剂的配比分组prp中血小板浓度(×108个)kgm-ⅰ(μg)hrwp-n(μg)实验组150.050.1实验组250.070.2实验组350.100.3实验组450.120.3实验组550.200.3实验组650.100.05实验组750.10/实验组85/0.3对照组5//将0.05g生物制剂浸泡在装有sbf的玻璃杯中,玻璃杯用保鲜膜密封以防止水分的流失,取特定时间下的浸泡液,用生长因子试剂盒(厦门慧嘉生物科技有限公司生产)测试其中生长因子的含量。具体结果见图1-3。由图1-3可以看出,采用不同配比的prp/kgm-ⅰ/hrwp-n对生长因子的释放量影响不同,采用每毫升富血小板血浆中含有葡甘露聚糖的质量范围为0.05-0.12μg同时酸性沙棘多糖的质量范围为0.1-0.3μg时,三种生长因子的释放量均有大幅度提高,在含有葡甘露聚糖的质量为0.1μg同时酸性沙棘多糖的质量为0.3μg时,三种生长因子的释放量均达到了最大值,表皮生长因子(egf)、血管内皮生长因子(vegf)、类胰岛素生长因子(bfgf),可以起到促进细胞增殖分化、促进皮肤组织修复作用,由此可以推测,本发明的生物制剂可以促进皮肤伤口愈合。制剂实施例将实验组1-4制得生物制剂的制备成为液体敷料,方法如下:1)将生物制剂按照不同的配比溶于水后加入聚乙烯醇和抗坏血酸溶解,再加入羟丙基甲基纤维素充分溶解后,得到预混液;2)将壳聚糖溶解于1%(w/v)的冰醋酸溶液中配置成浓度为1%(w/v)的壳聚糖溶液,将预混液缓慢加入壳聚糖溶液中,搅拌均匀,以1%的naoh溶液调节ph至5.8-6.8,补足余量的水,即得液体敷料。制得的液体敷料中生物制剂及其他配料的配比见表2。表2制剂实施例的配方创面修复试验100只balb/c小鼠,均为雄性,8-10周龄,随机分为5组,每组20只,分别为制剂组1-制剂组4以及对照组,制剂组1-4分别对应制剂实施例1-4,对照组对应制剂对比例。抓取小鼠,通过腹膜内注射1%戊巴比妥钠(50mg/kg)麻醉小鼠,使用脱毛膏脱除小鼠背部发毛,俯卧位固定,75%酒精消毒背部皮肤。在小鼠背中部用打孔器创建一处直径为10mm的全厚皮肤创口,然后将制剂实施例1-4及制剂对比例的液体敷料涂覆在皮肤创口上。各组小鼠每48小时换一次药。分别在术后第3、7、12天观察小鼠伤口愈合情况。用计算机图像分析软件photoshopcs4计算创面面积,测定各组的创面愈合率,计算公式如下:创面愈合率=[(s0-sd)/s0]×100%其中,s0表示原始创面面积,sd表示未愈合的创面面积。试验结果见表3。表3各组小鼠创面愈合率由表3的结果可以看出,本发明的液体敷料对小鼠创面具有很好的愈合作用,相较于不添加生物制剂的液体敷料,添加了生物制剂的液体敷料在使用12天后的愈合率达到了94%以上,最高可达到98%以上,故本发明的液体敷料具有很高的应用价值和推广价值。上所述仅为本发明创造的较佳实施例而已,并不用以限制本发明创造,凡在本发明创造的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明创造的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1