赤霉素及其衍生物在制备预防和/或治疗中枢神经系统疾病的用途
本发明实施例涉及生物医药领域,特别涉及赤霉素及其衍生物在制备预防和/或治疗中枢神经系统疾病药物的用途。
背景技术:
中枢神经系统疾病大致分为两类,第一类是由脑损伤引起的脑部疾病,例如帕金森病、老年痴呆症和脑肿瘤等;第二类是由脊髓损伤引起的运动、感觉功能障碍等。发明人在研究中发现,小胶质细胞在中枢神经系统疾病的进程中发挥重要作用,几乎所有的中枢神经系统疾病都与小胶质细胞异常活化相关。因此,基于小胶质细胞活化抑制机理的药物将有望应用于预防和治疗中枢神经系统疾病。
赤霉素(ga)作为一种重要的广谱性植物生长调节剂,在植物体广泛存在,它是促进植物生长发育的重要激素之一。现有技术中,赤霉素主要应用于促进植物种子萌发、加速生长以及增加果实产量,在医学领域,赤霉素曾被应用于治疗人类肺癌和糖尿病。然而,现有技术中暂未发现关于赤霉素及其衍生物作为预防和治疗中枢神经系统疾病药物的记载。
技术实现要素:
本发明实施方式的目的在于提供赤霉素及其衍生物在制备预防和/或治疗中枢神经系统疾病药物的用途。
如本文所用,术语“赤霉素及其衍生物”中“其衍生物”指的是式(ⅰ)所示化合物在药学上可接受的盐、酯及糖苷。
如本文所用,术语“小胶质细胞m1型活化”和“小胶质细胞m1型极化”可互换使用,其指的是相对于在正常生理状态下的静息状态,小胶质细胞处于激活状态并极化为促炎表型,并分泌促炎细胞因子。
如本文所用,术语“神经退行性疾病(neurodegene-rativedisease)”指的是以神经元或髓鞘变性或丢失导致的脑功能障碍,例如阿尔茨海默病(alzheimer’sdisease,ad)、帕金森病(parkinson’sdisease,pd)、多发性硬化(multiplesclerosis,ms)、亨廷顿病(huntingtondisease,hd)、肌萎缩侧索硬化症(amyotrophiclateralsclerosis,als)。
如本文所用,术语“精神病(psychosis)”指的是严重的精神障碍,患者出现认知、情感、意志、动作行为等精神活动均可持久的明显异常、如各种幻觉、妄想、思维逻辑障碍、情感淡漠、不协调兴奋等,例如抑郁症(depressivedisorder)、自闭症(infantileautism)和躁狂症(manicdisorder)。
如本文所用,术语“神经系统感染性疾病(infectiousdiseasesofnervoussystem)”指的是神经系统被包括病毒、细菌、真菌、立克次体、螺旋体和寄生虫等病原体感染引起的疾病,例如脑炎(encephalitis)、膜炎(meningitis)和脑脓肿等神经系统疾病。
如文本所用,术语“脑血管疾病”指的是发生在脑部血管、因颅内血液循环障碍而造成的脑组织损害及脑功能障碍的一组疾病。
如本文所用,术语“神经病理性疼痛(neuropathicpain,npp)”为由神经系统原发性损害和功能障碍所激发或引起的疼痛,包括痛觉过敏、自发性痛及异常痛。
为解决上述技术问题,本发明的实施方式提供了一种赤霉素及其衍生物在制备预防和/或治疗中枢神经系统疾病药物的用途,其特征在于,所述赤霉素具有式(ⅰ)所示的结构;
其中,r1为氢、羧基、c1~6烷基、或-or11,其中,r11为氢或者和r6键合成内酯;
r2为氢或羟基,或者与r3键合成双键;
r3为氢或羟基,或者与r2或r4键合成双键;
r4为氢或羟基,或者与r3键合成双键;
r5为氢或c1~6烷基;
r6为羟基、或-or61,其中r61为未取代或被c1~6烷基取代的c1~20烷基;或者r6和r11键合成内酯;
虚线表示一根键,虚线存在或不存在,虚线和r71不同时存在;当虚线存在,r71不存在时,r7为亚甲基;当虚线不存在,r71存在时,r7为羟基,r71为c1~6烷基;当虚线不存在,r71不存在时,r7为氢、羟基或c1~6烷基;
r8为氢、羟基或c1~6烷基。
在一些优选的方案中,所述式(ⅰ)中,r1为-or11,其中,r11和r6键合成内酯;
r2为氢或者与r3键合成双键;
r3为氢或者与r2或r4键合成双键;
r4为氢或者与r3键合成双键;
r5为c1~6烷基;
r6为羟基、或者r6和r11键合成内酯;
虚线表示一根键,虚线存在,且r71不存在,r7为亚甲基;
r8为氢或羟基。
在一些优选的方案中,所述赤霉素具有通式(ⅱ)所示的结构;
其中,r2为氢或者与r3键合成双键;
r3为氢或者与r2键合成双键;
r8为氢或羟基。
在一些优选的方案中,所述赤霉素为下述任一种结构,或任两种或两种以上结构的组合,
在一些优选的方案中,所述赤霉素为下述结构,
在一些优选的方案中,所述预防和/或治疗中枢神经系统疾病药物为小胶质细胞m1型活化抑制剂。
在一些优选的方案中,所述预防和/或治疗中枢神经系统疾病药物为psd-95基因表达促进剂。
在一些优选的方案中,所述中枢神经系统疾病包括:神经退行性疾病、神经系统感染性疾病、脑血管疾病、精神病、轻度认知损伤、术后认知功能障碍或神经病理性疼痛。
在一些优选的方案中,所述神经退行性疾病包括:阿尔茨海默病、帕金森病、多发性硬化、亨廷顿病或肌萎缩侧索硬化症。
在一些优选的方案中,所述脑血管疾病包括:缺血性脑血管病和出血性脑血管病。
在一些优选的方案中,所述缺血性脑血管病包括:短暂性脑缺血发作、急性缺血性脑卒中、脑动脉盗血综合征或慢性脑出血。
在一些优选的方案中,所述出血性脑血管病包括:蛛网膜下腔出血、高血压脑出血、脑血管畸形、动脉瘤、淀粉样脑出血或瘤卒中。
在一些优选的方案中,所述精神病包括:抑郁症、自闭症或躁狂症。
在一些优选的方案中,所述神经系统感染性疾病包括:脓毒症(sepsis)、脓毒性脑病(septicencephalopathy)、膜炎或脑炎。
在一些优选的方案中,所述中枢神经系统疾病包括:阿尔茨海默病、帕金森病、多发性硬化、急性缺血性脑卒中、术后认知功能障碍、亨廷顿病、萎缩侧索硬化症、脓毒性脑病、膜炎、脑炎、轻度认知损伤或神经病理性疼痛。
在一些优选的方案中,所述中枢神经系统疾病由小胶质细胞异常活化引起。
在一些优选的方案中,所述中枢神经系统疾病由小胶质细胞m1型活化引起。
本发明的实施方式还提供了一种预防和/或治疗中枢神经系统疾病的药物组合物,所述药物组合物包括:赤霉素或其衍生物;和
赤霉素或其衍生物在药学上可接受的载体或赋形剂。
本发明的实施方式还提供了一种预防和/或治疗中枢神经系统疾病的方法,所述方法包括步骤:向所述中枢神经系统疾病的患者施用上述赤霉素或其衍生物,或者上述药物组合物。
在不违背本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
本发明所用试剂和原料均市售可得。
本发明实施方式相对于现有技术而言,至少具有下述优点:
(1)本发明提供的用途,拓宽了赤霉素的应用范围,为赤霉素及其衍生物的药用提供了新思路。
(2)本发明提供的用途,为预防或治疗中枢神经系统疾病提供了一种低成本且有效的方法。
附图说明
一个或多个实施例通过与之对应的附图中的图片进行示例性说明,这些示例性说明并不构成对实施例的限定。
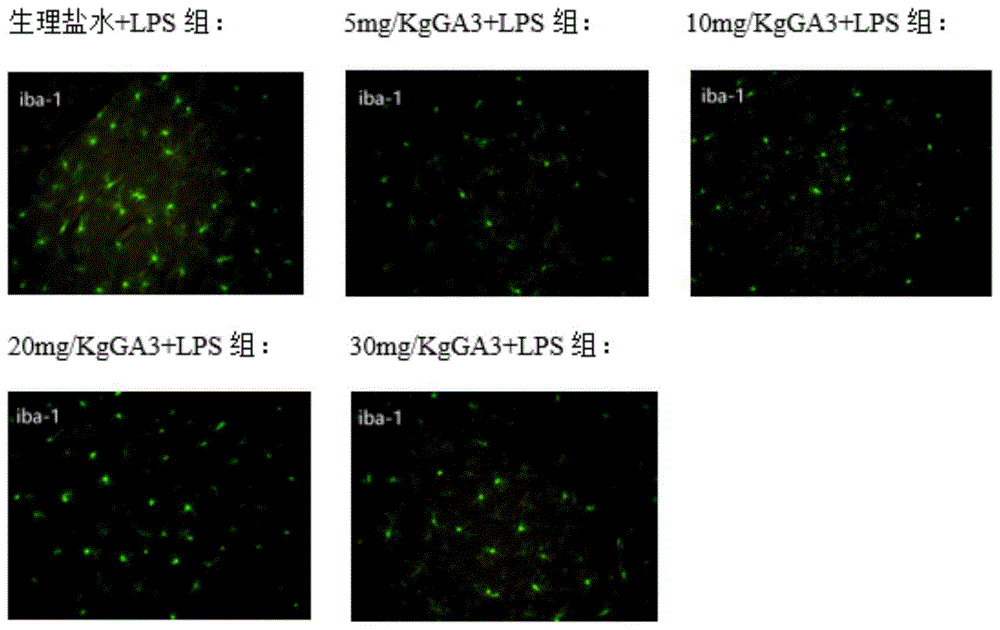
图1是根据本发明实施例五中免疫荧光检测脓毒症模型小鼠海马中iba-1蛋白表达显微照;
图2是根据本发明实施例五中脓毒症模型小鼠海马中iba-1蛋白阳性率示意图;
图3是根据本发明实施例六中脓毒症模型小鼠海马中psd-95基因的表达示意图;
图4是根据本发明实施例七中定向航行实验结果示意图;
图5是根据本发明实施例七中空间探索实验结果示意图;
图6是根据本发明实施例七中空间探索实验结果小鼠平均穿越平台次数统计图;
图7是根据本发明实施例八中mtt实验检测赤霉素对细胞活性影响示意图;
图8是根据本发明实施例八中ldh实验检测赤霉素对细胞毒性影响示意图;
图9是根据本发明实施例九中免疫荧光检测阿兹海默症模型小鼠海马中iba-1蛋白表达显微照;
图10是根据本发明实施例九中阿兹海默症模型小鼠海马中iba-1蛋白阳性率示意图;
图11是根据本发明实施例十中阿兹海默症模型小鼠海马中psd-95基因的表达示意图;
图12是根据本发明实施例十一中坐骨神经分支保留性损伤模型小鼠或脊髓背角中psd-95基因的表达示意图。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合实施例对本发明的各实施方式进行详细的阐述。然而,本领域的普通技术人员可以理解,在本发明各实施方式中,为了使读者更好地理解本申请而提出了许多技术细节。但是,即使没有这些技术细节和基于以下各实施方式的种种变化和修改,也可以实现本申请所要求保护的技术方案。
本发明人经过详尽的实验研究和论证,发现赤霉素及其衍生物具有较好的抑制小胶质细胞异常活化的功能,并且可改善基于小胶质细胞异常活化导致的各种中枢神经系统疾病,包括但不限于:阿尔茨海默病、帕金森病、多发性硬化、急性缺血性脑卒中、术后认知功能障碍、亨廷顿病、萎缩侧索硬化症、脓毒性脑病、膜炎、脑炎、轻度认知损伤或神经病理性疼痛等。
实施例一、赤霉素拮抗lps诱导小胶质细胞活化
从geo公共数据库下载6个lps诱导小胶质细胞活化模型的芯片表达谱,将其放入基因表达谱数据库(cmapconnectivitymap,cmap)进行分析比对,共找到53个p值小于0.05的小分子药物。其中50个小分子呈正相关,具有与lps相似的效应,赤霉素干预细胞后得到的基因表达谱与lps处理细胞后得到的基因表达谱呈显著负相关,表明赤霉素可能具有拮抗lps诱导小胶质细胞活化的作用。
实施例二、脓毒症模型的构建
对8-12周龄的c57bl/6j小鼠,分别以生理盐水(n=6)、5mg/kgga3(n=6)、10mg/kgga3(n=6)、20mg/kgga3(n=6)、30mg/kgga3(n=6)进行灌胃预处理;1小时后,以10mg/kglps行腹腔注射构建脓毒症模型;4小时后,小鼠出现厌食、寒颤、抱团、体毛竖立、眼周分泌物增多等状况时,说明模型构建成功。
实施例三、阿尔兹海默症模型的建立
本实验所用ad小鼠为spf级c57bl/6j品系ap-pswe/ps1de9(app/ps1)转基因ad模型鼠,购自南京大学实验动物中心,均为8~10周龄性成熟小鼠,采取剪鼠尾的方法,通过提取dna的方法鉴定阳性的app/ps1双转基因小鼠。鉴定之后随机分为sham组(野生型小鼠n=6)和ad组(n=6)、5mg/kgga3+ad组(n=6),其中5mg/kgga3+ad组以5mg/kgga3连续灌胃3天,其他两组使用生理盐水连续灌胃3天处理,随后进行后续实验。
实施例四、坐骨神经分支保留性损伤(sparednerveinjury,sni)模型的建立
将大鼠随机分为sham组、sni组和5mg/kgga3+sni组。sham组大鼠使用生理盐水灌胃预处理,只暴露神经,不做结扎切断。sni组大鼠使用生理盐水灌胃预处理,腹腔注射2%戊巴比妥钠45mg/kg麻醉后,将其置于恒温手术台上,常规备皮、皮肤消毒、铺洞巾,在右下肢股骨下方做水平切口1cm,分离肌肉后暴露坐骨神经的分支,保留其中的腓肠神经,6-0丝线分别结扎胫神经和腓总神经的两端,将结扎区域之间的神经剪断并截取1~2mm,防止其功能恢复。完成后用4-0丝线分层缝合肌肉和皮肤。大鼠在手术后恢复两周进行后续实验。5mg/kgga3+sni组在术前1小时进行5mg/kgga3灌胃预处理,腹腔注射2%戊巴比妥钠45mg/kg麻醉后,将其置于恒温手术台上,常规备皮、皮肤消毒、铺洞巾,在右下肢股骨下方做水平切口1cm,分离肌肉后暴露坐骨神经的分支,保留其中的腓肠神经,6-0丝线分别结扎胫神经和腓总神经的两端,将结扎区域之间的神经剪断并截取1~2mm,防止其功能恢复。完成后用4-0丝线分层缝合肌肉和皮肤。大鼠在手术后恢复两周进行后续实验。
实施例五、免疫荧光检测脓毒症模型小鼠海马中iba-1蛋白表达情况
取实施例二中所得脓毒症模型小鼠进行灌流取脑,4%多聚甲醛固定24小时后,30%蔗糖溶液进行沉糖脱水处理,使用冰冻包埋剂对全脑进行包埋,使用冰冻切片机将脑组织切成20um的薄片,并贴于载玻片上,待贴片干燥后,置于pbs液中清洗3次,每次10分钟。使用封闭液室温封闭一小时,后与iba-1一抗结合(以脑组织样品和iba-1一抗质量比为1:100的比例混合),室温孵育1小时或者4℃过夜。pbs漂洗3次,每次冲洗5分钟。二抗结合(以与iba-1一抗结合后的脑组织样品和二抗质量比为1:1000的比例混合),室温避光孵育1小时。pbs漂洗3次,每次冲洗10分钟后,再用蒸馏水漂洗一次。使用荧光显微观察小鼠海马中iba-1蛋白表达情况,光谱选择570nm长的激发光波(570nm长的激发光波显示绿色光),实验结果见图1和图2。
取实施例二所得的经ga3处理的脓毒症模型小鼠用相同的方式处理,荧光显微镜观察小鼠海马中iba-1蛋白表达情况,光谱选择570nm长的激发光波,实验结果见图1和图2。
如图1和图2所示,与生理盐水+lps组相比,ga3+lps组小鼠海马组织内的iba-1蛋白表达明显较少(表现为荧光显色细胞数减少)。实验结果证明ga3可以有效降低患脓毒症小鼠体内iba-1蛋白表达,从而抑制患脓毒症小鼠体内m1型小胶质细胞的活化。
实施例六、rt-pcr检测脓毒症模型小鼠海马中psd-95基因的表达情况
由于psd-95不仅参与调节、维持突触的结构形态与功能,还能结合n-甲基-d-天冬氨酸受体突触信号、谷氨酸受体与其相关的蛋白分子发生相互作用,组成受体-信号分子-调节分子-靶分子信号复合体,在学习记忆中发挥极其重要作用。因此,通过测定psd-95基因的表达情况可推测大脑认知功能是否正常。
取实施例二中所得脓毒症模型小鼠海马,加入1mltrizol震荡30秒,加入0.2ml氯仿,剧烈摇动30秒,室温3分钟。12000g,4℃离心15分钟,轻轻吸取上层无色水相,移入另一ep管中(约0.5ml)加等体积异丙醇,室温放置10分钟,4℃下以12000g的转速离心10分钟,在管底部可见微量rna沉淀,加入75%乙醇1ml,振荡,4℃下以7500g的转速离心离心5分钟弃上清,小心吸取残留乙醇,开盖干燥5分钟,用depc水20μl溶解rna,检测rna浓度。利用反转录试剂盒将rna逆转录为cdna,sybrgreenreal-timepcr法进行psd-95基因的表达检测,检测结果见图3。psd-95基因引物序列为:上游5’-gacaaccaagaaataccgct-3’,下游5’-gcttctagggtgtccgtgtt-3’。
如图3所示,与生理盐水+lps组相比,ga3+lps组小鼠海马组织内的psd-95表达明显增加,实验结果表明ga3可以有效增加患脓毒症小鼠体内psd-95表达,从而改善神经突触的可塑性,改善脑认知功能。
实施例七、morris水迷宫测试评估脓毒症后小鼠的学习记忆能力
根据实施例六免疫荧光和rt-pcr的结果,以5mg/kgga3浓度预处理小鼠后以10mg/kglps行腹腔注射构建脓毒症模型。模型构建5天后,行morris水迷宫测试。morris水迷宫直径为100cm,高为50cm。水池的内部不得有任何标记,水中加入适量的新鲜牛奶或奶粉,使水池成为不透明的乳白色。分为四个象限作为四个不同的入水点。于第三象限距桶壁20cm处放置逃生平台,逃生平台为一高约28cm的圆盘状小台,直径为6cm。水池内注入高约30cm(即逃生平台所处平面低于池内水液面2cm)的温水,水池自带的恒温装置将水温维持在(20±2)℃,水池周围用暗色布料环绕一圈以阻挡光线。在实验过程中,实验室内保持恒定的光源强度,水箱周围四个象限的桶壁上分别悬挂不同形状的图形(具体为圆形、三角形、正方形、星形)为小鼠创造远端视觉线索,当小鼠在水池中游动时提供大鼠确定并区分它的方向,从而认清其所处的空间位置以便找寻逃生平台所在的确切位置。所有的游泳测试、动物跟踪过程都用放置在天花板上的摄像机记录下来,并使用smart动物行为学视频分析系统进行分析。在正式开始实验之前,测试小鼠游泳运动能力,排除游泳运动能力存在缺陷的小鼠,整个实验过程持续5天以训练寻找水下平台。具体实验步骤为:
①定向航行实验:小鼠从不同象限以头部朝向圆桶水池的姿势放入水池中,每天进行4次试验,持续4天。允许小鼠游泳的最长时间是60秒。实验追踪在小鼠爬上平台之后停止,否则在指定的60秒结束之时停止。如果动物未能在指定的时间(即60秒)内找到平台,则轻轻将其引导至逃生平台,并允许其在逃生平台上停留15秒。最后一次定向航行实验后24小时进行空间探索实验。
②空间探索实验:逃生平台在最后一天被撤去,记录动物的逃避潜伏期和总行走距离。从第一象限入水点将小鼠面向池壁放入水中,记录60秒内大鼠穿越原逃生平台所处位置范围的次数以及逃避潜伏期。通过安装在水迷宫上方的摄像机监测全过程,传入电脑并记录和储存,再运用行为轨迹跟踪系统软件进行分析和数据处理。
定向航行实验结果见图4,空间探索的实验结果见图5和图6。
如图4所示,与sham组(生理盐水处理与脓毒症模型小鼠同批次小鼠)相比,lps处理后小鼠穿越平台所需的行程轨迹大幅增加,表明lps处理后小鼠的学习记忆能力发生了下降;而与lps处理组相比,经ga3+lps处理后小鼠穿越平台所需的行程轨迹减少,表明ga3可改善小鼠的学习记忆能力。
如图5和图6所示,与sham组(生理盐水处理与脓毒症模型小鼠同批次小鼠)相比,lps处理组穿越平台次数减少,表明经lps处理后小鼠学习记忆能力发生了下降;而与lps处理组相比,ga3+lps处理后小鼠穿越平台次数增加,表明ga3+lps处理后小鼠处理后学习记忆能力受损程度较仅lps处理组更小,进一步证明了ga3有助于改善脓毒症引起的脑损伤和认知功能下降。
实施例八、mtt和ldh实验检测不同浓度的赤霉素对细胞活性和毒性的影响
将状态良好的小胶质细胞株接种到24孔板,使细胞浓度为1×105/ml细胞,接种细胞密度介于50%至70%之间。分别使用0.03μm、0.3μm、3μm、30μm、300μm和600μm的赤霉酸预处理原代小胶质细胞,再使用100ng/ml的lps处理小胶质细胞24小时,构建小胶质细胞m1型活化模型。
将上述所得的m1型活化的小胶质细胞接种至96孔培养板,待细胞生长至融合状态后,分别加入10ulmtt孵育2小时,采用酶标仪测定450nm吸光度。所有实验均重复3次,实验结果见图7。
将上述所得的m1型活化的小胶质细胞接种至96孔培养板,待细胞生长至融合状态后,分别加入10ulldh孵育2小时,采用酶标仪测定450nm吸光度。所有实验均重复3次,实验结果见图8。
如图7所示,与control组相比,lps组的小胶质细胞活性发生下降。与lps组相比,lps+0.03μmga3、lps+0.3μmga3、lps+30μmga3、lps+300μmga3和lps+600μmga3组小胶质细胞活性均有提高,表明ga3可以改善经lps处理后的小胶质细胞活性。
如图8所示,与control组相比,lps组ldh含量大幅上升,说明经lps处理后小胶质细胞大量死亡。与lps组相比,lps+0.03μmga3、lps+0.3μmga3、lps+30μmga3、lps+300μmga3和lps+600μmga3组ldh含量均有下降,且随着ga3浓度增加而下降幅度增加,表明ga3可以有效降低经lps处理后的小胶质细胞的死亡率。
实施例九、免疫荧光检测阿兹海默症模型小鼠海马中iba-1蛋白表达情况
取实施例三所得阿兹海默症模型小鼠,按照与实施例五相同的方式检测其海马中iba-1蛋白表达情况,检测结果见图9和图10。
如图9和图10所示,与sham组(用生理盐水处理与阿兹海默症模型小鼠同批次小鼠)相比,ad组小鼠海马中iba-1蛋白表达变多(表现为荧光显色细胞数变多),表明m1型小胶质细胞的活化增多;与ad组相比,ga3+ad组小鼠海马中iba-1蛋白表达明显减少(表现为荧光显色细胞数变少),表明m1型小胶质细胞的活化减少。实验结果证明ga3可以有效降低患阿兹海默症小鼠体内iba-1蛋白表达,从而抑制患阿兹海默症小鼠体内m1型小胶质细胞的活化。
实施例十、rt-pcr检测阿兹海默症模型小鼠海马中psd-95基因的表达情况
取实施例三所得阿兹海默症模型小鼠,按照与实施例六相同的方式检测其海马中psd-95基因的表达情况,检测结果见图11。
如图11所示,与sham组(用生理盐水处理与阿兹海默症模型小鼠同批次小鼠)相比,ad组小鼠海马中psd-95基因的表达明显降低,表明ad组小鼠神经突触功能受到损伤;与ad组相比,ga3+ad组小鼠海马中psd-95基因的表达有所增加,表明ga3可以有效增加患阿兹海默症小鼠体内psd-95表达,从而改善神经突触的可塑性,改善脑认知功能。
实施例十一、rt-pcr检测坐骨神经分支保留性损伤模型小鼠海马中psd-95基因的表达情况
由于突触可塑性还是神经病理性疼痛形成和维持的主要机制之一,脊髓psd95在神经病理性疼痛的发展过程中起重要作用。因此通过检测psd-95基因的表达情况可间接推测神经病理性疼痛是否得到改善。
取实施例四所得坐骨神经分支保留性损伤模型小鼠,按照与实施例六相同的方式检测其或脊髓背角中psd-95基因的表达情况,检测结果见图12。
如图12所示,与sham组(用生理盐水处理与坐骨神经分支保留性损伤模型小鼠同批次小鼠)相比,sni组小鼠或脊髓背角中psd-95基因的表达明显降低,表明sni组小鼠神经突触功能受到损伤;与sni组相比,ga3+sni组小鼠或脊髓背角中psd-95基因的表达有所增加,表明ga3可以有效增加患坐骨神经分支保留性损伤小鼠体内psd-95表达,从而改善神经突触的可塑性,减轻神经病理性疼痛。
本领域的普通技术人员可以理解,上述各实施方式是实现本发明的具体实施例,而在实际应用中,可以在形式上和细节上对其作各种改变,而不偏离本发明的精神和范围。
- 还没有人留言评论。精彩留言会获得点赞!