包含羟尼酮与右美沙芬的药物组合物及其治疗肺纤维化的应用的制作方法
1.本发明属于药物领域,具体涉及一种包含羟尼酮与右美沙芬的药物组合物及其联合用于制备治疗肺纤维化的药物的用途。
背景技术:
2.肺纤维化是以成纤维细胞增殖及大量细胞外基质聚集并伴炎症损伤、组织结构破坏为特征的一大类肺疾病的终末期改变,也就是正常的肺泡组织被损坏后经过异常修复导致结构异常(疤痕形成)。绝大部分肺纤维化病人病因不明(特发性),这组疾病称为特发性间质性肺炎(iip),是间质性肺病中一大类。而特发性间质性肺炎(iip)中最常见的以肺纤维化病变为主要表现形式的疾病类型为特发性肺纤维化(ipf),是一种能导致肺功能进行性丧失的严重的间质性肺疾病。肺纤维化严重影响人体呼吸功能,表现为干咳、进行性呼吸困难(自觉气不够用),且随着病情和肺部损伤的加重,患者呼吸功能不断恶化。特发性肺纤维化发病率和死亡率逐年增加,诊断后的平均生存期短,死亡率高于大多数肿瘤,被称为一种“类肿瘤疾病”。因此,期望开发出肺纤维化的新型治疗药物。
技术实现要素:
3.为了改善上述技术问题,本发明提供一种药物组合物,其包含式(i)所示化合物(即羟尼酮)与右美沙芬,
[0004][0005]
式(i)。
[0006]
本发明还提供一种药物试剂盒,其包含分开放置的羟尼酮和右美沙芬。
[0007]
根据本发明的实施方案,所述药物组合物或药物试剂盒,其中,羟尼酮与右美沙芬的质量比可以为(1-10000):(1-5000),例如为(10-8000):(1-3000),(10-6000):(1-2000),(10-5000):(1-1000),(50-4000):(10-500),(100-2000):(50-300),(200-1000):(100-200),(300-800):(100-200),(300-500):(120-180),(1000-5000):(1-800),(2000-5000):(1-600),(2000-5000):(1-500),(2000-5000):(1-100),(2000-5000):(1-50),(3000-5000):(1-30),(10-5000):(100-5000),(20-4000):(500-4000),(30-3000):(1000-3000),(50-2000):(1000-3000),(60-1000):(1000-3000)或者(80-800):(1000-3000)。
[0008]
本领域技术人员可以理解,羟尼酮与右美沙芬的质量比可以为前述范围内的任意亚范围或者具体点值。
[0009]
根据本发明的实施方案,所述药物组合物或药物试剂盒,其还可以包含至少一种药学上可接受的辅料。例如,所述药学上可接受的辅料为制药领域中已知的各种药物辅料,
包括但不限于:稀释剂、粘合剂、抗氧化剂、ph调节剂、防腐剂、润滑剂、崩解剂等。
[0010]
例如,所述稀释剂选自乳糖、淀粉、纤维素衍生物、无机钙盐、山梨醇等。
[0011]
例如,所述粘合剂选自淀粉、明胶、羧甲基纤维素钠、聚乙烯吡咯烷酮等。
[0012]
例如,所述抗氧化剂选自维生素e、亚硫酸氢钠、亚硫酸钠、丁羟基茴香醚等。
[0013]
例如,所述ph调节剂选自盐酸、氢氧化钠、柠檬酸、酒石酸、tris、乙酸、磷酸二氢钠、磷酸氢二钠等。
[0014]
例如,所述防腐剂选自对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、间甲酚、苯扎氯铵等。
[0015]
例如,所述润滑剂选自硬脂酸镁、微粉硅胶、滑石粉等。
[0016]
例如,所述崩解剂选自淀粉、甲基纤维素、黄原胶、交联羧甲基纤维素钠等。
[0017]
根据本发明的实施方案,所述药物组合物或者分开放置的右美沙芬或羟尼酮药物试剂盒的剂型可以是口服制剂,例如片剂、胶囊、丸剂、粉剂、颗粒剂、悬浮剂、糖浆剂等;也可以是肠胃外给药(例如,注射给药)的剂型,例如可以为注射液、粉针剂等,可以通过静脉内、腹膜内、皮下或肌肉内的途径。
[0018]
例如,所述药物组合物或药物试剂盒中,所述右美沙芬和羟尼酮的给药方式可以相同或不同;例如二者可以同为注射给药或口服给药的剂型,或者二者之一为注射剂型而另一种为口服给药的剂型,例如,右美沙芬可以为注射给药的剂型而羟尼酮为口服给药的剂型,反之亦可。
[0019]
本发明提供所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒在制备治疗或缓解肺纤维化或者改善肺纤维化症状的药物中的应用。
[0020]
根据本发明的实施方案,所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒可以修复肺功能、抑制肺纤维化炎症和/或改善纤维化状况。
[0021]
根据本发明的实施方案,所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒能够降低肺纤维化对象的脾脏系数,抑制脾肿胀。
[0022]
根据本发明的实施方案,所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒能够缓解肺系数上升,改善肺部炎症和纤维化状况。
[0023]
根据本发明的实施方案,所述治疗或缓解肺纤维化或者改善肺纤维症状的药物能够改善肺纤维化对象的肺换气功能和/或酸碱平衡状态。具体地,羟尼酮与右美沙芬联合应用能够改善肺纤维化对象的血液酸碱度、氧分压、组织间液剩余碱、实际碳酸氢根、二氧化碳总量、氧饱和度和/或乳酸水平。
[0024]
根据本发明的实施方案,所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒能够降低肺纤维化对象的肺泡灌洗液中的白细胞绝对值、淋巴细胞绝对值和/或单核细胞绝对值,达到肺部抗炎的作用。
[0025]
根据本发明的实施方案,所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒能够降低肺纤维化对象的肺泡灌洗液中的nf-kb,tnf-a、il-2.il-6,il-1p和/或tgf-b水平。
[0026]
根据本发明的实施方案,所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒能够提高肺纤维化对象的肺泡灌洗液中的ifn-y水平。
[0027]
根据本发明的实施方案,所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒
能够改善糖皮质类激素对脾脏免疫细胞的抑制作用,将脾脏免疫细胞水平恢复至正常水平。
[0028]
例如,所述脾脏免疫细胞为cd8+t细胞、cd4+t细胞、b细胞。
[0029]
根据本发明的实施方案,所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒能够控制肺组织结构病变,例如降低肺纤维化对象的羟脯氨酸含量。
[0030]
根据本发明的实施方案,在肺纤维化初期和/或肺纤维化成形阶段,所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒能够减少肺组织结构变化和炎性细胞浸润,改善肺纤维化状况。
[0031]
根据本发明的实施方案,所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒能够抗ecm沉积。
[0032]
例如,所述包含羟尼酮与右美沙芬的药物组合物或药物试剂盒能够减少支气管粘膜下、肺间质胶原纤维沉积。
[0033]
本发明还提供一种治疗或缓解肺纤维化或者改善纤维化症状的方法,包括将上述药物组合物或者药物试剂盒给予有此需要的个体。
[0034]
本发明还提供上述药物组合物或药物试剂盒,其用作治疗或缓解肺纤维化或者改善纤维化症状的药物。
[0035]
本发明还提供上述药物组合物或药物试剂盒,其用于治疗或缓解肺纤维化或者改善纤维化症状的方法中。
[0036]
在本发明中,所述肺纤维化可以是特发性肺纤维化(ipf)。
[0037]
本发明的有益效果:
[0038]
实验表明,羟尼酮与右美沙芬联合在肺功能修复、肺纤维化炎症抑制和改善肺纤维化状况方面具有优异的效果。具体地,在博来霉素(blm)气管滴注诱导的小鼠特发性肺纤维化(ipf)模型中,羟尼酮(f351)与右美沙芬(dm)联合给药组的肺湿重和肺系数显著下降,羟脯氨酸含量降低,肺纤维化评分下降。因此,本发明的包含右美沙芬和羟尼酮的药物组合物或药物试剂盒可用作治疗或缓解肺纤维化或者改善肺纤维化症状的药物。
附图说明
[0039]
图1示出了实验过程中动物体重变化曲线。
[0040]
图2示出了实验过程中动物存活率结果。
[0041]
图3示出了体重、肺脏湿重和肺系数的结果。
[0042]
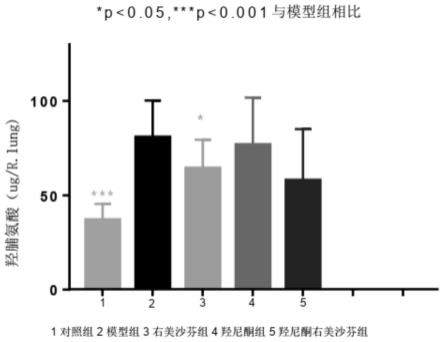
图4示出了右肺羟脯氨酸含量的结果。
[0043]
图5示出了24h造模各组小鼠肺组织的he结果(图中标尺均为放大200倍)。
[0044]
图6示出了24h造模各组小鼠肺组织的sr结果(图中标尺均为放大200倍)。
具体实施方式
[0045]
下文将结合具体实施例对本发明的技术方案做更进一步的详细说明。应当理解,下列实施例仅为示例性地说明和解释本发明,而不应被解释为对本发明保护范围的限制。凡基于本发明上述内容所实现的技术均涵盖在本发明旨在保护的范围内。
[0046]
除非另有说明,以下实施例中使用的原料和试剂均为市售商品,或者可以通过已
知方法制备。
[0047]
实施例1
[0048]
1.实验材料
[0049]
1.1受试物
[0050][0051]
1.2溶媒
[0052][0053]
1.3造模剂
[0054][0055]
1.4试剂
[0056]
羧甲基纤维素钠:sigma,lot no:slbj9393v
[0057]
戊巴比妥钠:中国医药集团上海化学试剂公司,lot no:f20021216
[0058]
pbs:赛默飞世尔生物化学制品(北京)有限公司,hyclone,sh30028.01.b
[0059]
95%乙醇:上海试剂公司,货号:80186961
[0060]
10%福尔马林中性固定液:西陇科学股份有限公司,lot no:1901232
[0061]
羟脯氨酸试剂盒:南京建成生物工程研究所,货号:a030-2-1,生产批号:20210317,有效期:20210916。
[0062]
1.5仪器设备
[0063]
普通光学显微镜:奥林帕斯型号:bx53
[0064]
2.动物及饲养条件
[0065]
2.1动物
[0066][0067]
2.2动物接收、健康评估及适应期
[0068]
动物到达公司后,动物房人员将动物从运输包装中转移至鼠笼并对每只动物进行检查。检查范围包括外观、四肢和孔腔等,以及动物姿势或运动时是否有异常表现。
[0069]
2.3环境
[0070]
实验用小鼠被安置于动物房的小鼠笼(260mm
╳
160mm
╳
120mm)中。整个实验期间安置动物的房间号被记录在实验记录里。小鼠垫料为经过高温处理过的玉米芯,每周更换两次垫料。安置实验用小鼠的房间位于准spf动物房内,该区域的过滤通风换气次数为每小时15-25次。温度保持在20-25℃(68-77
°
f)之间,相对湿度为40-70%。照明条件为每天12小时(08:00-20:00)日光灯照射和12小时黑暗。
[0071]
2.4食物和饮水
[0072]
实验用小鼠无限量获取啮齿动物专用饲料(已经辐照灭菌)。接收的每一批动物饲料均附有供应商提供的对应批次的分析证书。
[0073]
整个实验期间,实验用小鼠无限量获取经高温灭菌的市政自来水。实验开始前的适应期为30天。
[0074]
在可预见范围内,动物食物和饮用水中的已知污染物含量将不会对本实验的目的或实施造成影响。
[0075]
2.5笼具和动物标识
[0076]
每只动物均分配有一个唯一编号。采用剪脚趾法对动物进行编号识别,编号规则为:后面左脚开始1号剪左、2号剪左2、3号剪左3,依次剪到第5个脚趾为5号。在对动物进行分组之前,鼠笼的标签上标注动物种属/品系、性别、笼号、实验项目、给药、实验开始日期等信息。
[0077]
动物分组后,鼠笼用标签标注组别信息及上述信息。分组情况记录在随机分组文件中。用笼架将鼠笼分层以减轻环境因素对实验的影响。
[0078]
3.实验方法和过程
[0079]
3.1动物分组
[0080]
将小鼠按体重随机分为5组,分组及治疗情况见表1。
[0081]
表1动物分组治疗方案
[0082][0083][0084]
备注:dm(sc,tid),f351(p.o,qd),it:气管内注射。
[0085]
3.2造模
[0086]
戊巴比妥钠以剂量65mg/kg麻醉小鼠。在led冷光灯辅助下经气管滴注缓慢注入76μlblm(组别相应的浓度)溶液或相应体积的生理盐水。立即将小鼠直立并左右旋转,使药液在肺内均匀分布。
[0087]
3.3给药
[0088]
f351、0.5%cmc均为灌胃给药,每天一次,上午8:30点左右;dm皮下给药,一天三次,分别为上午8:30,中午12:00,下午16:00。
[0089]
3.4组织取材
[0090]
给药结束后24h,称取存活动物体重。将动物腹腔注射戊巴比妥钠过量麻醉后自腹腔主动脉放血处死动物。剪取肺脏称得湿重。小鼠左肺直接置于10%中性福尔马林溶液中固定24h以上后进行后续处理;右肺立即-80℃冷冻,待检测羟脯氨酸。
[0091]
3.5观察指标
[0092]
3.5.1动物一般状况,体重和死亡率
[0093]
自第一天给药起,每天对每只小鼠进行外观、行为活动及粪便性状等的观察。所有非正常的外观形态和行为活动都记录在临床观察表内。每周称体重2次,如体重变化剧烈,可视情况加测体重。
[0094]
3.5.2肺脏系数
[0095]
肺系数是反映肺脏质量与体质量比例关系的一个指标,肺湿重和体重分别通过电子天平称量,肺系数计算方法为(肺湿重mg/体重g)。
[0096]
3.5.3羟脯氨酸含量测定
[0097]
组织中胶原含量可以用羟脯氨酸的含量来反映。称取小鼠右肺湿组织,按试剂盒说明书进行测定肺组织羟脯氨酸含量。
[0098]
一、测定原理:
[0099]
羟脯氨酸在氧化剂的作用下所产生的氧化产物与二甲氨基苯甲醛作用呈现紫红色,根据其呈色的深浅可推算出其含量。
[0100]
二、试剂盒组成与配制:(50t/48样)
[0101]
试剂一:粉剂
×
1瓶,甲液10ml
×
1瓶,乙液20ml
×
1瓶,临用时将粉剂先加甲液10ml充分溶解(从瓶口向内看,完全溶解完),然后再加乙液20ml充分混匀。配好后的试剂4℃~8℃冰箱保存3个月有效。
[0102]
试剂二:液体30ml
×
1瓶,4℃冰箱避光保存3个月有效。
[0103]
试剂三:粉剂
×
1瓶,溶剂30ml
×
1瓶,临用时将粉剂一支加到30ml溶剂中充分溶解,配好后4℃冰箱避光保存1个月有效。
[0104]
试剂四:标准品5mg
×
3支,4℃冰箱保存6个月。
[0105]
100μg/ml标准贮备液的配制:测试前将一支标准品用双蒸水溶解后定容至50ml,4℃冰箱保存2周。
[0106]
5μg/ml标准应用液的配制:取100μg/ml标准贮备液1ml加双蒸水定容至20ml,现用现配。
[0107]
三、羟脯氨酸的测定:
[0108]
(一)样本前处理试剂(4℃保存):(50t)
[0109]
1、水解液60ml
×
1瓶:2、指示剂5ml
×
1瓶:3、调整ph甲液60ml
×
1瓶;
[0110]
4、ph调整乙液30ml
×
1瓶:5、活性炭
×
1袋。
[0111]
(二)样本前处理:
[0112]
1、样本水解:
[0113]
①
血清(浆):取0.5ml血清(浆)准确加水解液1ml,混匀。放试管中加盖后,95℃或者沸水浴水解20分钟。
[0114]
②
尿液(培养液):取1.0ml尿液(培养液)進确加水解液1ml,混匀。放试管中加盖后,95℃或者沸水浴水解20分钟。
[0115]
③
组织:精确称取组织湿重30~100mg放入试管中,准确加水解液1ml,混匀。加盖后95℃或者沸水浴水解20分钟(水解10分钟时混匀一次,目的是使水解更充分)。
[0116]
2、调ph值至6.0~6.8左右。
[0117]
①
将各试管流水冷却后各管加指示剂10μl,摇匀;
[0118]
②
各管准确加入调ph甲液1.0ml,混匀(此时溶液应为红色);
[0119]
③
用200μl的加样器吸取调ph的乙液向各管内逐滴小心加入调ph的乙液,每滴加入后均要混匀*,直至液体中指示剂的颜色变成黄绿色**(亦即红色消失时)。
[0120]
此时ph值在6.0-6.8左右(约加入调ph乙液100μl~500μl左右);(*加调ph乙液时,每加一滴均要混匀,为防止液体外溢,如果没有带盖的玻璃磨口试管,可用普通玻璃试管代
替,每次混匀时可用塑料薄膜或冰箱保鲜膜压住试管口,充分旋涡混匀即可。)
[0121]
④
然后加双蒸水至10ml,混匀;
[0122]
⑤
取3-4ml稀释的水解液加适量活性炭(约20~30mg左右,以上清液离心后澄清无色为准),混匀,3500转/分离心10分钟,小心取上清1ml作检测。
[0123]
(三)操作表
[0124] 空白管标准管测定管双蒸水1.0
ꢀꢀ
5μg/ml标准应用液 1.0 检测液(ml)
ꢀꢀ
1.0试剂一(ml)0.50.50.5
[0125]
混匀,静置10分钟
[0126]
试剂二(ml)0.50.50.5
[0127]
混匀,静置10分钟
[0128]
试剂三(ml)0.50.50.5
[0129]
混匀,60℃水浴15分钟,冷却后,3500转/分离心10分钟,取上清于波长550nm,1cm光径,双蒸水调零,测定各管吸光度值。
[0130]
四、计算公式(一)血清(浆)计算公式:
[0131]
1、计算公式:
[0132][0133]
(二)尿液的计算公式:
[0134]
1、计算公式:
[0135][0136]
(三)组织的计算公式:
[0137]
1、计算公式:
[0138][0139]
3.5.4肺脏组织病理学检查(he染色,光镜分析肺脏结构)。
[0140]
h&e染色:石蜡切片常规脱蜡至水,苏木素染液中浸染10min,自来水冲洗,1%盐酸酒精分化10s,自来水冲洗,2%碳酸氢钠溶液返蓝10s,自来水冲洗,1%伊红溶液浸染2min,自来水冲洗,95%酒精上行脱水,二甲苯透明,中性树脂封片后在光镜下观察。
[0141]
4.统计分析
[0142]
死亡率采用卡方检验;计量资料结果表示方式为平均数
±
标准差,组间的两两比较采用dunnett’s multi-comparison方法;组间等级资料采用mann-whitney非参数检验。p《0.05将被认为有统计学显著性差异。
[0143]
5.实验结果
[0144]
5.1动物一般状况,体重和死亡率
[0145]
实验开始时各组动物毛色光亮,活动正常,状态良好。如图1所示,整个实验过程对
照组体重正常,活动与状态良好。与对照组相比,模型组(blm/0.5%cmc(n=15))和各给药组均出现体重下降。与模型组相比,dm+f351组(blm/dm-10npk+f351-100mpk(n=15))体重有下降趋势,其他各给药组体重变化与模型组无显著性差异。
[0146]
如图2所示,除对照组和dm-10ng/kg组(右美沙芬组)未出现死亡外,其他各给药组动物均出现动物死亡现象,与模型组相比无显著性差异。
[0147]
5.2肺湿重
[0148]
如图3所示,与对照组相比,模型组肺湿重与肺系数显著增加。与模型组相比,dm+f351组肺湿重与肺系数显著下降,其他各给药组无显著性差异。
[0149]
5.3羟脯氨酸含量
[0150]
如图4所示,与对照组相比,模型组羟脯氨酸含量显著性增加。与模型组相比,各给药均组有下降趋势,其中相较于dm-10ng/kg组(右美沙芬组)和f351-100mg/kg(羟尼酮组)单独使用,dm+f351组(羟尼酮右美沙芬合用组)有下降趋势。
[0151]
5.4组织病理学检查
[0152]
图5为24h造模各组小鼠肺组织he结果。从图中可以看出,对照组肺组织结构清晰,支气管、血管周围无明显炎性细胞浸润,管壁无明显增厚。肺泡结构完整,肺泡间隔无明显增厚。模型组小鼠的肺组织结构发生明显变化严重,肺组织结构被破坏,肺泡间隔增厚,大量炎性细胞浸润,部分肺泡腔消失,代之以单核炎性细胞和纤维组织,其间见灶性成纤维细胞。dm-10ng/kg组(右美沙芬组)肺组织结构有破坏,肺泡间隔增厚,大量炎细胞浸润,部分肺泡腔消失,代之以单核炎性细胞和纤维组织,其间见灶性成纤维细胞。f351-100mg/kg组(羟尼酮组)整体比模型组的肺部结构稍好,部分肺泡间隔增厚,纤维灶形成,伴有炎细胞浸润,肺泡壁结构破坏,部分肺泡消失。dm+f351组(羟尼酮右美沙芬合用组)肺泡间隔增厚,炎细胞浸润,可见纤维沉积,呈灶状分布,肺泡壁结构破坏,部分肺泡消失。
[0153]
图6为24h造模各组小鼠肺组织sr结果。从图中可以看出,对照组的肺组织结构清晰,肺泡间隔小范围较轻增厚,存在稍多的红色胶原纤维。模型组小鼠的肺组织结构发生明显变化严重,肺泡结构破坏,出现纤维灶,肺泡间隔存在较多的sr染色为红色的胶原纤维。dm-10ng/kg组(右美沙芬组)肺泡间隔增厚,结构被破坏,出现纤维灶,存在较多的红色胶原纤维。f351-100mg/kg组(羟尼酮组)肺泡结构完整,肺泡间隔存在较多的sr染色为红色的胶原纤维。dm+f351组(羟尼酮右美沙芬合用组)肺泡间隔增厚,结构被破坏,出现纤维灶,存在少量的红色胶原纤维。
[0154]
肺纤维化评分:肺纤维化评分(0-8)参考肺间隔、肺泡和整体纤维程度变化来评定,具体结果见表1。
[0155]
表1肺部纤维化评分
[0156][0157]
组织病理学检查发现,与对照组相比,模型组肺脏病变程度显著加重。与模型组相比,dm+f647组纤维化评分有下降趋势,其余各给药组纤维化评分无显著性差异。具体结果见表2。
[0158]
表2肺部纤维化病变等级
[0159][0160]
6.实验结论
[0161]
(1)对比对照组,模型组与各给药组动物体重显著性下降。
[0162]
(2)对比对照组,模型组死亡率显著增加。除dm-10ng/kg组无动物出现死亡外,其他各给药组动物均出现动物死亡现象,与模型组相比无显著性差异。
[0163]
(3)对比对照组,模型组肺湿重与肺系数显著增加,而dm+f351组肺湿重与肺系数显著下降。
[0164]
(4)对比对照组,模型组与各给药组右肺羟脯氨酸含量显著升高。相较于dm-10ng/kg组和f351-100mg/kg单独使用,dm+f351组有下降趋势。
[0165]
(5)对比对照组,模型组肺部纤维化评分显著性增加。与模型组相比,dm+f351组纤
维化评分有下降趋势。
[0166]
以上,对本发明的实施方式进行了说明。但是,本发明不限定于上述实施方式。凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1